一种协同治疗结肠癌的自组装纳米片及其制备方法
1.本发明属于医药领域纳米片的制备领域,具体涉及一种能够调节结肠癌微环境中硫化氢浓度并引发协同治疗的自组装纳米片及其制备技术。
背景技术:
2.高浓度硫化氢(h2s)是结肠癌微环境主要特征之一,是治疗多种疾病的独特病理生物学障碍,在促进肿瘤增殖、营造免疫抑制微环境、保护肿瘤细胞免受氧化损伤等方面发挥着至关重要的作用。因此,调节结肠癌高浓度h2s微环境,破坏保护性屏障,能够增加肿瘤对药物的敏感性。
3.砒霜又名白砒,有效成分为三氧化二砷(ato),其注射液已被批准为急性早幼粒细胞白血病的一线化疗(ct)药物,抗肿瘤机制主要包括抑制细胞增殖、抑制侵袭转移和促进细胞凋亡。然而ato的非特异性使其容易对正常组织造成毒副作用,严重影响患者生存质量。此外,ato往往受限于肿瘤耐药性,导致治疗效果不佳。有研究表明,ato的毒性和疗效强弱主要与其所含的砷元素价态有关,三价砷(as
3+
)的毒性和疗效都显著高于五价砷(as
5+
)。原位激活药物体系,能够降低药物分布特异性差引起的毒副作用,h2s作为一种强还原性气体,能够将as
5+
还原成as
3+
,实现结肠癌部位as
5+
到as
3+
的转变,从而降低ato对正常组织的毒副作用;同时还原过程还伴随着h2s含量的下降,具有一定的h2s清除效果。
4.铜离子(cu
2+
)具有强大的阴离子结合能力,其能和h2s反应,消耗h2s的同时生成稳定产物硫化铜。硫化铜作为一种光热材料,不仅具有高效的光热转化效率,还能将过氧化氢(h2o2)转化为高度氧化的羟基自由基(
·
oh),产生ros诱导细胞凋亡,发挥化学动力学疗法(cdt)的作用。
5.消耗h2s作为调节结肠癌微环境的策略之一,仅能够在一定时间内降低h2s浓度,解决这一问题关键在于产生h2s的源头。氨基氧乙酸(aoaa)是一种应用广泛的h2s生成抑制剂,能够通过抑制胱硫醚-β-合成酶(cbs)的活性从而抑制h2s的生成。但aoaa的亲水特性使其疗效受限;目前常修饰甲酯或乙酯等基团改善药物的物理化学性质,使其能够更好地被细胞摄取,但是这种方法仍存在非靶部位起效、毒副作用等问题亟待解决。
6.因此,我们提出“两耗一抑”调节结肠癌微环境策略,利用cu
2+
和as
5+
双重消耗h2s,aoaa抑制h2s的生成,降低结肠癌微环境中h2s的浓度,增加结肠癌对药物的敏感性。随后,as
5+
被h2s原位还原成as
3+
,降低对正常组织的毒副作用,但是单独使用ato存在耐药性问题,导致治疗效果不佳。cu
2+
和h2s反应产物硫化铜能产生ros诱导细胞凋亡,然而,这一能力受到肿瘤微环境中h2o2含量的限制;硫化铜的高效光热转换能力,通过高温杀死肿瘤,不需要借助ros就可达到杀伤肿瘤的目的;三种不同作用机制的疗法相互协同,最大程度消融肿瘤。有研究表明,硫化铜具有良好的催化h2o2产生ros能力,为在更大程度上增加疗效,寻找药物联用进一步增强ros的生成能力成为有效的途径。as
3+
能够发挥化学疗法(ct)通过产生活性氧(ros)促进肿瘤细胞凋亡,两种疗法的联用进一步增加ros生成,能更好地杀伤肿瘤。光热治疗(ptt)是利用具有较高光热转换效率的材料,将其注射入人体内部后,在外部光源
的照射下将光能转化为热能来杀死癌细胞的一种治疗方法。ptt不需要借助ros就可达到杀伤肿瘤的目的,因此,可以用来消除具有ros抗性的残留肿瘤;此外,由于其微创治疗方式,具有良好的生物安全性。众所周知,硫化铜不仅能够产生ros杀伤肿瘤,还是一种良好的光热转换材料,在近红外激光的照射下,能发挥ptt效果。
7.自组装是将材料的单个单元关联成有序结构的过程。它通过非共价相互作用为无机和有机结构赋予独特的性质。目前,自组装纳米材料由于其简单性、自发性、可扩展性、多功能性和低成本等特点,在纳米技术、成像技术、生物传感器、生物医学科学等领域得到了广泛的应用。
技术实现要素:
8.针对现有技术的缺陷,本专利提出了一种新型的调节结肠癌微环境硫化氢浓度并引发协同治疗的自组装纳米片的制备技术,该自组装纳米片依靠非共价相互作用力将cu
2+
、as
5+
和aoaa相结合,形成h2s响应的自组装纳米片,通过改变结肠癌微环境并引发协同疗法,达到最大程度治疗结肠癌的目的。
9.本专利包括如下内容:
10.一种协同治疗结肠癌的自组装纳米片,所述的治疗结肠癌的自组装纳米片系通过非共价相互作用力将cu
2+
、as
5+
和氨基氧乙酸aoaa相结合,采用水热法制备的粒径均一的cu-as-aoaa自组装纳米片。
11.优选地,所述的治疗结肠癌的自组装纳米片的制备方法,包括以下步骤:
12.(1)将氯化铜(cucl2·
2h2o)、砷酸氢二钠(na2haso4·
7h2o)和氨基氧乙酸(aoaa)分别溶解于超纯水中,得到三份溶液;
13.(2)在冰水浴搅拌下,依次加入cucl2、na2haso4和aoaa溶液,反应结束后得到混合液;
14.(3)将混合液置于高压水热釜中,反应一定时间后固液分离,得到cu-as-aoaa自组装纳米片。
15.优选地,所述的治疗结肠癌的自组装纳米片的制备方法中所述cucl2·
2h2o、na2haso4·
7h2o和aoaa的质量比为0~20:10~30:1,优选0~0:10~20:1。
16.优选地,所述的治疗结肠癌的自组装纳米片的制备方法中cucl2溶液质量分数为0.4~0.8%(优选0.5~0.7%)、na2haso4溶液质量分数为0.8~2%(优选1~1.8%)和aoaa溶液质量分数为0.01~0.1%(优选0.03~0.08%)。
17.优选地,所述的治疗结肠癌的自组装纳米片的制备方法的步骤(2)中,所述冰水浴温度为0~8℃,优选2~6℃。
18.优选地,所述的治疗结肠癌的自组装纳米片的制备方法的步骤(2)中,所述反应时间为10~50min,优选20~40min。
19.优选地,所述的治疗结肠癌的自组装纳米片的制备方法的步骤(3)中,所述反应时间为15~45min,优选25~35min。
20.优选地,所述的治疗结肠癌的自组装纳米片的制备方法的步骤(3)中,所述反应温度为160~200℃,优选170~190℃。
21.优选地,所述的治疗结肠癌的自组装纳米片的制备方法的步骤(3)中,所述固液分
离方式可采用离心或过滤方式。
22.优选地,所述的治疗结肠癌的自组装纳米片的制备方法,步骤(1)中,所述cucl2·
2h2o、na2haso4·
7h2o和aoaa的质量比为为0~10:10~20:1;所述cucl2溶液质量分数为0.5~0.7%、na2haso4溶液质量分数为1~1.8%和aoaa溶液质量分数为0.03~0.08%;
23.步骤(2)中,所述冰水浴温度为2~6℃;所述反应时间为20~40min;
24.步骤(3)中,所述反应时间为25~35min;所述反应温度为170~190℃。
25.本发明制得的产物可利用透射电子显微镜(tem)、原子力显微镜(afm)、紫外可见近红外吸收光谱仪、热成像仪和电感耦合等离子光谱发生仪进行表征。
26.本发明提供的自组装纳米片能够调节结肠癌微环境硫化氢浓度并引发协同治疗,用于制备抗肿瘤药物。利用非共价相互作用力将cu
2+
、as
5+
和aoaa相结合,水热法制备了粒径均一的cu-as-aoaa自组装纳米片,通过静脉注射后,被动靶向至肿瘤组织,在h2s作用下激活,以期达到改善结肠癌微环境和协同治疗结肠癌的目的。本发明制备的cu-as-aoaa自组装纳米片形状均一;体外具有良好的h2s响应特性,反应产物具有光热转化效果和
·
oh生成能力。cu-as-aoaa自组装纳米片能够降低结肠癌微环境中h2s浓度,说明cu-as-aoaa自组装纳米片具有改善结肠癌微环境的潜力;适宜浓度的cu-as-aoaa自组装纳米片溶液与1064nm激光照射的结合治疗能够杀死90%以上的结肠癌肿瘤细胞,说明cu-as-aoaa自组装纳米片具有优异的体外协同抗肿瘤效果。
27.本专利的技术效果,解决结肠癌高浓度h2s微环境所引起的疗效受限问题;解决结肠癌单一疗法临床效果不佳、毒副作用明显等问题;解决砒霜有效成分三氧化二砷正常组织分布高,导致毒副作用的问题。
28.本专利的创新点:
29.1.本发明针对结肠癌高浓度硫化氢微环境所引起的疗效受限问题,提出两耗一抑概念,即双重消耗联合特异性抑制硫化氢,从而达到调节结肠癌高浓度硫化氢微环境的目的,改善结肠癌治疗效果;
30.2.本发明针对三氧化二砷治疗窗窄的问题,利用其砷离子价态不同毒性不同的特性,借助结肠癌微环境中高浓度硫化氢的强还原性,原位生成高毒性三价砷,解决三氧化二砷治疗窗窄的问题;
31.3.本发明提出cu-as-aoaa自组装纳米片制备技术,高浓度硫化氢的作用下响应性激活化学疗法、光热疗法和化学动力学疗法,改善结肠癌单一疗法治疗效果不佳等问题。
附图说明
32.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
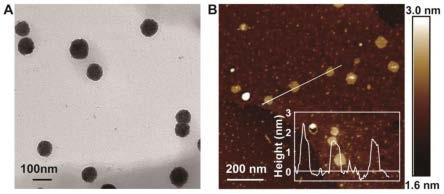
33.图1为本专利方法制备的cu-as-aoaa自组装纳米片的透射电镜(a)和原子力显微镜(b)图。
34.图2为本专利方法制备的cu-as-aoaa自组装纳米片与硫氢化钠(nahs)反应一定时间后的透射电镜图。
35.图3为本专利方法制备的cu-as-aoaa自组装纳米片与不同浓度nahs反应一定时间后800-1200nm区间吸收变化。
36.图4为本专利方法制备的cu-as-aoaa自组装纳米片与不同浓度nahs反应一定时间后的温度变化(1064nm,1w/cm2)。
37.图5为本专利方法制备的cu-as-aoaa自组装纳米片与不同浓度nahs反应一定时间后的热成像图(1064nm,1w/cm2)。
38.图6为本专利方法制备的cu-as-aoaa自组装纳米片与nahs反应后一定时间后
·
oh生成能力(1.cu-as-aoaa+0mm h2o2;2.0.5mm h2o2;3.cu-as-aoaa+0.05mm h2o2;4.cu-as-aoaa+0.1mm h2o2;5.cu-as-aoaa+0.2mm h2o2and 6.cu-as-aoaa+0.5mm h2o2)。
39.图7为本专利方法制备的cu-as-aoaa自组装纳米片与不同浓度nahs反应后砷释放曲线。
40.图8为与本专利方法制备的cu-as-aoaa自组装纳米片作用不同时间后结肠癌细胞内h2s浓度变化的激光共聚焦图。
41.图9为光照处理前后不同浓度cu-as-aoaa自组装纳米片与结肠癌细胞共培养后的细胞存活率。
具体实施方式
42.下面结合实施例对本发明做进一步的详细说明,以下实施例是对本发明的解释而本发明并不局限于以下实施例。
43.实施例
44.一、材料
45.二水合氯化铜(cucl2·
2h2o)和砷酸氢二钠(na2haso4·
7h2o)(美国,sigma aldrich公司);氨基氧乙酸(aoaa,中国,北京奇松生物公司);硫氢化钠(nahs,68-72%,中国,北京沃凯生物科技有限公司)。
46.二、方法
47.1.制备
48.将300mg na2haso4·
7h2o、170mg cucl2·
2h2o和18mg aoaa分别溶解在25ml超纯水中。将这3种溶液置于圆底烧瓶中冰水浴剧烈搅拌30min,随后将混合溶液转移至高压水热釜中,180℃反应30min。反应结束后离心3-4次,加纯水分散即得到cu-as-aoaa自组装纳米片。
49.2.表征
50.2.1与nahs反应前后形貌观察
51.移液枪量取50μl cu-as-aoaa溶液滴在硅片上,自然晾干,用afm观察其厚度。移液枪分别量取50μl cu-as-aoaa和反应后溶液滴在铜网上,常温放置干燥后上样,用tem观察其形态,结果见图1和2所示。
52.2.2紫外可见近红外吸收变化检测
53.将一定量的cu-as-aoaa溶液与不同浓度nahs(0、0.5、1、2、3mm)溶液反应,紫外可见近红外光谱仪测定800-1200nm波长范围内的吸收强度变化,结果见图3所示。
54.2.3光热效应实验
55.将一定量的cu-as-aoaa溶液与不同浓度nahs(0、0.5、1、2、3mm)溶液反应,用1064nm激光以1w/cm2照射5min,每隔30s用热成像仪记录反应后的溶液温度变化情况,结果见图4和5所示。
56.2.4羟基自由基产生能力测定
57.采用3,3',5,5'-四甲基联苯胺显色法考查cu-as-aoaa与nahs反应后产物产生羟基自由基的能力。将cu-as-aoaa溶液与h2o2溶液反应一定时间后加入3,3',5,5'-四甲基联苯胺溶液,用酶标仪检测吸收变化情况,结果见图6所示。
58.2.5体外释放实验
59.将cu-as-aoaa溶液置于透析袋中,透析袋浸入nahs(0、1、2、3mmol/l)的pbs释放介质中,于特定时间点吸取一定透析袋外面的液体,并补加释放介质,采用电感耦合等离子光谱检测砷离子的浓度,结果见图7所示。
60.3.体外细胞学评价
61.3.1结肠癌细胞内h2s含量变化
62.用7-叠氮基-4-甲基香豆素标记细胞内h2s,激光共聚焦显微镜(clsm)观察荧光变化,考察了cu-as-aoaa自组装纳米片h2s消耗能力,结果见图8所示。
63.3.2细胞毒性
64.采用cck-8法考察不同浓度cu-as-aoaa自组装纳米片对结肠癌细胞的杀伤作用,考察纳米粒的生物安全性和体外抗肿瘤作用,结果见图9所示。
65.结果表明:制备的cu-as-aoaa自组装纳米片形状均一;体外具有良好的h2s响应特性,反应产物具有光热转化效果和
·
oh生成能力。cu-as-aoaa自组装纳米片能够降低结肠癌微环境中h2s浓度,说明cu-as-aoaa自组装纳米片具有改善结肠癌微环境的潜力;适宜浓度的cu-as-aoaa自组装纳米片溶液与1064nm激光照射能的结合治疗够杀死90%以上的结肠癌肿瘤细胞,说明cu-as-aoaa自组装纳米片具有优异的体外协同抗肿瘤效果。
66.此外,需要说明的是,本说明书中所描述的具体实施例,其各原料以及工艺所取名称等可以不同。凡依本发明专利构思所述的原理所做的等效或简单变化,均包括于本发明专利的保护范围内。本发明所属技术领域的技术人员可以对所描述的具体实施例做各种各样的修改或补充或采用类似的方式替代,只要不偏离本发明的结构或者超越本权利要求书所定义的范围,均应属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1