富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液及其制备方法和用途
1.本发明属于干细胞新用途技术领域,涉及一种富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液及其制备方法和用途。
背景技术:
2.人脂肪间充质干细胞(human adipose mesenchymal stem cells,hasc)是一类具有自我更新和多向分化潜能的多能干细胞。研究发现,人脂肪间充质干细胞可以用于治疗多种疾病,其在治疗方面的作用通常归因于它们的细胞因子分泌和免疫调节作用,而不是它们定向分化成目的细胞的能力。
3.人脂肪间充质干细胞条件培养基上清液中包含多种生长因子、细胞因子、趋化因子、血管生成因子和外泌体等,这些物质在促进细胞的增殖、迁移,分化中有显著效果,相比于直接应用干细胞,上清液具有易工业化制造、冷冻干燥、储存,包装和运输的特点。此外,上清液因不含细胞,故不存在免疫排斥问题,使用相对安全。
4.创面愈合是一个复杂的生物学过程,包括急性创面愈合和慢性创面愈合。研究显示,在急性创面中,生长因子在促进肉芽组织形成的同时,还可促进创面再上皮化,加快愈合速度。对于慢性难愈性创面的治疗,使用重组人血小板生长因子、成纤维细胞生长因子能显著促进创面的肉芽组织形成及再上皮化,对临床难愈性的糖尿病足溃疡,褥疮以及其他创面,局部应用已显示出明显的治疗效果。然而,应用高剂量单一因子治疗难愈性创面虽然能在一定程度上发挥治疗效果,但因调控机制单一,提纯工艺冗杂,且价格昂贵等导致临床应用受限。
5.针对生长因子治疗创面的传统实施方法是将其配成溶液喷洒于创面,其优势是生长因子能与修复组织快速而均匀地结合发挥作用,但由于溶液易流失和蒸发,在一定程度上限制了生长因子发挥作用的时效性和稳定性。
6.因此,开发一种富含人脂肪间充质干细胞培养基上清液来源的干细胞因子复合物,并采用更为优胜的赋形剂承载,为创面制造一个湿润的环境,使生长因子能够持续稳定的作用于创面组织,具有广阔的临床应用前景。
技术实现要素:
7.有鉴于此,本发明为了解决上述现有技术对于急慢性创面的修复手段不良反应多,操作繁琐,应用受限的问题,提供一种富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液及其制备方法和用途。
8.为达到上述目的,本发明提供如下技术方案:
9.富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液的制备方法,包括以下步骤:
10.s1、纯化脂肪细胞
11.收集人体脂肪样本,使用生理盐水对其进行清洗,然后加入等体积的胶原酶消化,消化后多次过滤离心,去上清液,得到纯化的脂肪细胞;
12.s2、培养脂肪间充质干细胞(hascs)
13.在无血清无酚红的高辅酶培养基中添加5%血小板裂解物,重悬纯化的脂肪细胞后,将其转入细胞培养瓶进行培育,细胞接种密度为6万个/ml;在低氧条件下培养,促进细胞因子的分泌,将脂肪间充质干细胞培养至90
±
5%,收集p3代到p5代之间的培养上清液;
14.s3、收集传代前上清液
15.将传代前的上清液通过离心机进行高速离心,浓缩后制成细胞培养液,经直径0.22μm滤膜过滤除菌,最终获得干细胞复合因子浓缩液;
16.s4、制备复合型生物医用胶体液
17.将羧甲基纤维素钠、果胶按80~90:1的摩尔比混合,得到1ml水胶体凝胶,再将水胶体凝胶用生理盐水稀释至5~10倍体积,再加干细胞复合因子浓缩液(浓度为10~20ug/l),得到复合物多糖生物医用胶体液。
18.进一步,步骤s1中胶原酶为i型胶原酶、ⅱ型胶原酶混合物,消化的时间为30~60min,胶原酶的浓度为0.1%~0.5%,将消化后的脂肪细胞用直径为70μm的滤膜过滤,再在2000rpm/min的条件下离心5~10min,去除上清液,然后将细胞沉淀物以pbs分散,同样的条件,再次过滤离心得到纯化的脂肪细胞。
19.进一步,步骤s2中无血清无酚红的高辅酶培养基是每1l添加有辅酶a 10mg~28mg、辅羧酶5mg~15mg、黄素腺嘌呤二核苷酸4mg~12mg、尿苷酸磷酸0.5mg~2.5mg的间充质干细胞培养基;低氧培养条件为:24h内细胞的氧浓度为21%,24h~26h氧浓度由21%均匀降到18%,第27h的氧浓度为18%,第28~36h氧浓度由18%均匀降到8%,第37h的氧浓度为8%,第38h~44h氧浓度由8%均匀降到2%,后持续于2%的氧浓度下培养,二氧化碳浓度均为5%,其余为氮气。
20.进一步,步骤s2中收集提取脂肪间充质干细胞过程中培养获得的分泌物至少包括血管内皮生长因子(vegf)、角质细胞生长因子(kgf)、肝细胞生长因子(hgh)、转化生长因子β(tgf-β)、胰岛素样生长因子(igf)和血小板源性生长因子(pdgf)。
21.人脂肪间充质干细胞分泌的血管内皮生长因子(vegf)、角质细胞生长因子(kgf)、肝细胞生长因子(hgh)、转化生长因子β(tgf-β)、胰岛素样生长因子(igf)和血小板源性生长因子(pdgf),这些细胞因子主要的生物学活性是抗炎、抗凋亡、发挥免疫调节作用,强烈促进有丝分裂,参与干细胞诱导分化,组织细胞的生长、再生和重建,改善创伤部位组织功能,促进创面愈合。
22.血管内皮生长因子(vegf)介于728.56
±
124.23pg/ml、角质细胞生长因子(kgf)介于623.46
±
136.78pg/ml、肝细胞生长因子(hgh)介于2501.11
±
18.36pg/ml、转化生长因子β(tgf-β)介于4223.23
±
220.36pg/ml、胰岛素样生长因子(igf)介于1653.56
±
56.23pg/ml和血小板源性生长因子(pdgf)介于102.56
±
23.53pg/ml。
23.进一步,步骤s4中羧甲基纤维素钠为低粘度羧甲基纤维素钠、中粘度羧甲基纤维素钠和高粘度羧甲基纤维素钠按照1:1:1的摩尔比混合。
24.一种通过富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液制备方法制备的富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液,其融合了人脂肪间充
质干细胞因子复合物和多糖生物医用胶体液。
25.一种富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液在治疗急、慢性创面中的应用。
26.本发明的有益效果在于:
27.1、本发明所公开的富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液,干细胞复合因子浓缩液作为治疗创伤的核心内容,能够有效迅速修复急、慢性创面,并且修复过程副作用低、见效快,填补了市面上直接促进急、慢性创面修复的外用药的空缺。且干细胞因子复合物浓缩液与羧甲基纤维素钠、果胶复合,形成创面湿性环境,用于细胞修复在创面形成保护膜,阻断细菌感染创面,抑制细菌在创面的吸附,增殖等过程,同时该生物医用胶体液流动性和延展性良好,适合患者身体各个部位的贴敷。
28.2、本发明所公开的富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液,干细胞复合因子浓缩液促进烫伤创面修复效果明显,使用7d后,创面表皮完整且厚,皮下胶原排列有序;毛囊、血管再生规律且较多。
29.3、本发明所公开的富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液,浓缩脂肪间充质干细胞培养上清液制剂来源于人,无种属问题;并且成品中不含活细胞成分,不存在伦理学或免疫安全问题,无需现用现配,应用方便。
30.本发明的其他优点、目标和特征在某种程度上将在随后的说明书中进行阐述,并且在某种程度上,基于对下文的考察研究对本领域技术人员而言将是显而易见的,或者可以从本发明的实践中得到教导。本发明的目标和其他优点可以通过下面的说明书来实现和获得。
附图说明
31.为了使本发明的目的、技术方案和优点更加清楚,下面将结合附图对本发明作优选的详细描述,其中:
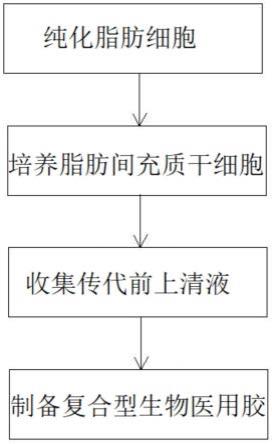
32.图1为本发明富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液的制备方法的流程图。
具体实施方式
33.实施例1
34.如图1所示的富含人脂肪间充质干细胞因子复合物的多糖生物医用胶体液的制备方法,包括以下步骤:
35.s1、纯化脂肪细胞;
36.收集人体脂肪样本,使用生理盐水对其进行清洗,然后加入等体积的胶原酶消化,消化后多次过滤离心,去上清液,得到纯化的脂肪细胞;胶原酶为i型胶原酶、ⅱ型胶原酶混合物,消化的时间为30~60min,胶原酶的浓度为0.1%~0.5%,将消化后的脂肪细胞用直径为70μm的滤膜过滤,再在2000rpm/min的条件下离心5~10min,去除上清液,然后将细胞沉淀物以pbs分散,同样的条件,再次过滤离心得到纯化的脂肪细胞。
37.s2、培养人脂肪间充质干细胞(hascs)
38.在无血清无酚红的高辅酶培养基中添加5%血小板裂解物,重悬纯化的脂肪细胞
后,将其转入细胞培养瓶进行培育,细胞接种密度为6万个/ml;无血清无酚红的高辅酶培养基是每1l添加有辅酶a 10mg~28mg、辅羧酶5mg~15mg、黄素腺嘌呤二核苷酸4mg~12mg、尿苷酸磷酸0.5mg~2.5mg的间充质干细胞培养基;在低氧条件下培养,促进细胞因子的分泌,,将脂肪间充质干细胞培养至90
±
5%,收集p3代的培养上清液;低氧培养条件为:24h内细胞的氧浓度为21%,24h~26h氧浓度由21%均匀降到18%,第27h的氧浓度为18%,第28~36h氧浓度由18%均匀降到8%,第37h的氧浓度为8%,第38h~44h氧浓度由8%均匀降到2%,后持续于2%的氧浓度下培养,二氧化碳浓度均为5%,其余为氮气。
39.分泌物至少包括血管内皮生长因子(vegf)、角质细胞生长因子(kgf)、肝细胞生长因子(hgh)、转化生长因子β(tgf-β)、胰岛素样生长因子(igf)和血小板源性生长因子(pdgf)。
40.人脂肪间充质干细胞分泌的血管内皮生长因子(vegf)、角质细胞生长因子(kgf)、肝细胞生长因子(hgh)、转化生长因子β(tgf-β)、胰岛素样生长因子(igf)和血小板源性生长因子(pdgf),这些细胞因子主要的生物学活性是抗炎、抗凋亡、发挥免疫调节作用,显著促进有丝分裂,参与干细胞诱导分化,组织细胞的生长、再生和重建,改善创伤部位组织功能,促进创面愈合血管内皮生长因子(vegf)介于728.56
±
124.23pg/ml、角质细胞生长因子(kgf)介于623.46
±
136.78pg/ml、肝细胞生长因子(hgh)介于2501.11
±
18.36pg/ml、转化生长因子β(tgf-β)介于4223.23
±
220.36pg/ml、胰岛素样生长因子(igf)介于1653.56
±
56.23pg/ml和血小板源性生长因子(pdgf)介于102.56
±
23.53pg/ml。
41.s3、收集传代前上清液
42.将传代前的上清液通过离心机进行高速离心,浓缩后制成细胞培养液,经直径0.22μm滤膜过滤除菌,最终获得干细胞复合因子浓缩液;
43.s4、制备复合型生物医用胶体液
44.将羧甲基纤维素钠、果胶按80~90:1的摩尔比混合,得到1ml水胶体凝胶,再将水胶体凝胶用生理盐水稀释至5~10倍体积,添加10ug/l干细胞复合因子浓缩液,得到复合物多糖生物医用胶体液。
45.实施例2
46.实施例2与实施例1的区别在于,步骤s4中羧甲基纤维素钠为低粘度羧甲基纤维素钠、中粘度羧甲基纤维素钠和高粘度羧甲基纤维素钠按照1:1:1的摩尔比混合。
47.实施例3
48.实施例3与实施例2的区别在于,步骤s2中,收集的上清液为p4代的上清。
49.实施例4
50.实施例4与实施例2的区别在于,步骤s2中,收集的上清液为p5代的上清。
51.实施例5
52.实施例5与实施例2的区别在于,步骤s4中,干细胞复合因子浓缩液浓度为15ug/l。
53.实施例6
54.实施例6与实施例2的区别在于,步骤s4中,干细胞复合因子浓缩液浓度为20ug/l。
55.对比例
56.多糖生物医用胶体液按重量百分比包括:低粘度羧甲基纤维素钠0.3%,中粘度羧甲基纤维素钠1.2%,高粘度羧甲基纤维素钠0.4%,氯化钠0.9%,其余为注射用水。将氯化
钠溶于注射用水,然后向水中加低、中、高粘度羧甲基纤维素钠开启恒温箱,在温度65℃下机械搅拌,直至低、中、高粘度羧甲基纤维素钠完全溶解,获得多糖生物医用胶体液。
57.采用上述实施例1~6所制得的成品对大鼠进行试验,试验方式如下:
58.1、建立大鼠急性创伤模型:取至少18只成年sd大鼠,分6个治疗组,每组3只。造模前12h褪去大鼠背部毛发,禁食,自由饮水。造模前进行腹腔注射水合氯醛溶液麻醉,常规消毒大鼠背部褪毛区,于每只大鼠背部脊柱两侧各标记1个直径1.2cm的圆形区域(圆形标记间距≥1cm),用无菌手术刀沿圆形标记切除全层皮肤,创口深至深筋膜。
59.2、治疗方法:大鼠背部左、右的伤口分别设置为治疗组、对照组。将1~6所制得的成品贴敷于相应组别大鼠皮肤创面上,创面形成后每隔2d用无菌生理盐水清洁创面,安尔碘消毒创面后更换新敷料。治疗过程观察创面组织修复情况,以及大鼠饮食行动等其它反应。
60.3、治疗效果检测
61.治疗结束后处死大鼠,取创面处皮肤全层及附带部分皮下组织送病理切片,每一份标本进行苏木精-伊红染色;
62.检测结果如下:
63.实施例1-6-大鼠表皮完整且厚,胶原排列有序;有毛囊,血管规律生长且较多;皮下胶原生成且排列整齐,效果较对比例好。
64.实施例1-6和对比例修复情况表,修复情况如表1所示,表1中的+代表修复程度,+越多,修复效果越好,-代表未有修复。
65.表1
[0066] 表皮胶原炎性浸润血管毛囊实施例1++++++-++++实施例2++++++++-++++实施例3+++++++-++++实施例4++++++-+++实施例5++++++-++++实施例6++++++++-+++++对比例+++++
[0067]
注:“+”的多少代表治疗后组织修复的程度。
[0068]
采用上述实施例1~6所制得的成品对大鼠进行试验,试验方式如下:
[0069]
1、建立大鼠慢性难愈合创面模型
[0070]
取至少21只成年sd大鼠,分为7组,对照组1组、慢性创面组6组,每组3只,造模前进行腹腔注射水合氯醛溶液麻醉。背部脱毛,用3.0cm
×
3.0cm的卡片在脱毛区用缝合线固定四周标记造模面积,准备一次性无菌切开包及其他物品,待麻醉生效后,用碘伏消毒3遍大鼠背部皮肤备皮处,沿标记线剪去皮下组织至肌筋膜,止血,形成大鼠全层皮肤缺损开放。
[0071]
2、治疗方法:
[0072]
造模后,即刻肌肉注射氢化可的松(80mg/kg),连续注射7d,2ml实施例1~6所制得的成品敷于创面。自实验前1d起,肌注青霉素钾盐(4 000单位/只),连续4d,以预防感染。创面隔日换药,常规冲洗及包扎。治疗过程观察创面组织修复情况,以及大鼠饮食行动等其它
反应。
[0073]
3、治疗效果检测
[0074]
用透明膜描记和照像法记录创面大小,部分动物创面采用计算机图象分析系统进行处理、校定,以计算创面愈合速度与质量。另外,治疗结束后处死大鼠,取创面处皮肤全层及附带部分皮下组织送病理切片,每一份标本进行苏木精-伊红染色
[0075]
检测结果如下:
[0076]
实施例1-6大鼠创面红润,分泌物少,创缘形状不规则,收缩明显。
[0077]
实施例1-6和对比例修复情况表,修复情况如表1所示,表1中的+代表修复程度,+越多,修复效果越好,-代表未有修复
[0078] 表皮胶原炎性浸润血管毛囊实施例1++++++-++++实施例2++++++-++++实施例3+++++++-++++实施例4++++++-+++实施例5++++++-++++实施例6+++++++-++++对比例+++++
[0079]
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1