一种微环境响应释药的多肽载药微针贴片、制备及应用
1.本发明属于药物递送技术领域,更具体地,涉及一种微环境响应释药的多肽载药微针贴片、制备及应用。
背景技术:
2.生理微环境主要指ph、氧化还原(谷胱甘肽、活性氧)、酶(基质金属蛋白酶、透明质酸酶、磷脂酶等)、葡萄糖、生理刺激(温度、压力)、其他(adenosine triphosphate三磷酸腺苷,atp)等,正常生理微环境与疾病组织的病理微环境存在明显的不同,例如,癌症、自身免疫疾病、感染、皮肤病和心血管疾病等。这使得利用这些病理微环境与正常组织生理环境的不同,设计具有对特定病理微环境响应的药物递送平台成为人们的研究热点。
3.皮肤是人体最大的器官,直接与外界环境接触,在内环境与外界环境之间形成保护性屏障。皮肤结构主要分为表皮层、真皮层及皮下组织。表皮层厚度为150-200μm,由无血管网的活细胞组成,起着严密的屏障作用,能够阻碍多数亲水性药物和大分子药物的渗透。真皮层是弹性纤维结构,具有丰富的毛细血管和神经网络。因此,药物注射会使真皮层内神经末梢受到损伤从而引起疼痛感。
4.微针作为近些年来发展较为迅猛的一种透皮药物传递系统,其特征尺寸为微米量级,可以刺穿皮肤角质层到达真皮层,且不损伤真皮层内神经末梢引发痛觉,并能将药物的皮肤渗透性提高几个数量级,药物经毛细血管吸收后进入全身血液系统发挥药效或局部治疗,可以避免口服给药引起的肝脏首过效应、胃肠对药物的降解。微针类型主要包括实心微针、包衣微针、可溶性微针、水凝胶微针及空心微针。其中,可溶解微针通常采用安全且具有水溶性的大分子材料,可以杜绝针头二次污染。负载的药物伴随着微针的溶解而释放。多数可溶解微针需要在皮肤上保留至少5分钟等待其完全溶解,而一些可生物降解的高分子聚合物微针在刺入皮肤后必须保持至少数日,它本身的控释性质才能完全被利用。并且目前缺乏按需响应病理微环境的相关刺激,并精准调控负载药物释放速率的微针药物传递系统。
技术实现要素:
5.针对现有技术的以上缺陷或改进需求,本发明提供了一种微环境响应释药的多肽载药微针贴片、制备及应用,其目的在于多重响应病理微环境的相关刺激释放药物,能在一定程度上对病理微环境进行重塑,并可实现对负载药物释放速率的有效控制。
6.为实现上述目的,按照本发明的一个方面,提供了一种微环境响应释药的多肽载药微针贴片,包括基底和针体,所述针体包括响应性多肽、生物活性高分子和药物,所述响应性多肽与生物活性高分子发生交联反应形成网络结构,所述药物通过物理包裹作用、配位作用或偶联共价作用负载于响应性多肽上;所述响应性多肽在环境触发下发生氨基酸之间的键断裂释放药物。
7.优选地,所述响应性多肽经过双键修饰,所述生物活性高分子含有不饱和基团,通
过双键与不饱和基团发生交联反应形成网络结构。
8.优选地,所述环境触发为ph响应触发、酶响应触发、葡萄糖响应触发、温度响应触发、氧化还原响应触发、atp响应触发。
9.优选地,通过控制所述响应性多肽与生物活性高分子发生交联反应的交联程度,控制所述多肽载药微针贴片的释药速率。
10.优选地,所述药物包括双甾体类有机化合物、黄酮类有机化合物、蒽醌类有机化合物、三萜类有机化合物、苷类有机化合物、生物碱类有机化合物、糖类有机化合物中的一种或几种;优选地,所述药物包括阿霉素、紫杉醇、喜树碱、姜黄素、5-氟尿嘧啶、曲美替尼、雷帕霉素、索拉非尼、氟维司群、恩杂鲁胺、甲氨蝶呤、维a酸、曲安奈德、博来霉素、阿法替尼、普萘洛尔、布洛芬、对乙酰氨基酚、阿司匹林中的一种或几种。
11.需要说明的是,在本发明的制备方法中,当药物中不含有反应活性位点时,可以通过预处理的方式使其修饰上反应活性基团,例如5-氟尿嘧啶,可以先进行预处理,得到羧基修饰的5-氟尿嘧啶,而当药物中含有反应活性基团时,即可直接与多肽通过化合键连接,例如维a酸。再例如,一些其他的药物可以通过物理包裹而包裹于响应性多肽中,例如亲疏水相互作用、静电相互作用等,示例性地,对于甲氨蝶呤而言,可以通过静电相互作用包裹于响应性多肽中;对于喜树碱而言,可以通过亲疏水相互作用包裹于响应性多肽中。再例如,一些其他的药物可以通过配位作用负载于响应性多肽上,示例性地,对于姜黄素而言,可以通过配位作用负载于响应性多肽上。
12.优选地,所述生物活性高分子包括甲基丙烯酰胺化明胶、甲基丙烯酰胺化丝素蛋白、甲基丙烯酰胺化透明质酸、甲基丙烯酰胺化硫酸软骨素、甲基丙烯酰胺化海藻酸钠、甲基丙烯酰胺化壳聚糖、甲基丙烯酰胺化葡聚糖、甲基丙烯酰胺化肝素、聚醚f127二丙烯酸酯、聚乙二醇二丙烯酸酯、四臂聚乙二醇丙烯酸酯、甲基丙烯酰胺化聚乙烯醇中的至少一种;所述基底材料为所述生物活性高分子或脱胶蚕丝、水溶性丝素蛋白、明胶、透明质酸钠、甲壳素、壳聚糖、壳聚糖季铵盐、海藻酸钠、葡聚糖、羧甲基葡聚糖、硫酸软骨素、肝素、聚乙二醇、聚乙烯醇、聚乙二醇-聚丙二醇-聚乙二醇中的至少一种。优选地,所述生物活性高分子在环境触发下降解。例如,在明胶酶响应触发条件下,甲基丙烯酰胺化明胶会发生水解。
13.按照本发明的另一个方面,提供了多肽载药微针贴片的制备方法,包括以下步骤:
14.(1)将聚硅氧烷类化合物和固化剂混合均匀后倾倒在微针模板上,除去气泡、干燥固化成型,分离微针模板得到微针阵列模具;
15.(2)将响应性多肽、生物活性高分子、药物和光固化剂溶解在去离子水或缓冲液中得到微针针体预聚液,将微针针体预聚液倒入微针阵列模具中后,除去气泡、光固化成型后获得含有成型针体的微针阵列模具;
16.(3)将基底材料溶解在去离子水或缓冲液中得到基底溶液,将基底溶液倒在含有成型针体的微针阵列模具上,除去气泡、室温避光干燥,固化成型后分离微针阵列模具得到多肽载药微针贴片。
17.优选地,所述步骤(2)之前还包括:根据环境触发条件,选择响应性多肽,使得响应性多肽在环境触发下发生氨基酸之间的键断裂释放药物;
18.或者根据环境触发条件,选择响应性多肽和生物活性高分子,使得响应性多肽在环境触发下发生氨基酸之间的键断裂释放药物,同时,生物活性高分子在环境触发下发生
降解。
19.优选地,所述缓冲液为醋酸缓冲液、磷酸盐缓冲液、柠檬酸盐缓冲液、硼酸盐缓冲液、三羟甲基氨基甲烷缓冲液中的一种,所述缓冲液的ph为5.5~8.5,缓冲液浓度为10~100mm,所述微针针体预聚液中响应性多肽的浓度为1-1000mm,所述微针针体预聚液中生物活性高分子的质量分数为5%-50%,所述微针针体预聚液中光固化剂的质量分数为0.5%-5%,基底溶液中基底材料的质量分数为5%-50%;所述光固化剂为2-羟基-2-甲基-1-[4-(2-羟基乙氧基)苯基]-1-丙酮、苯基-2,4,6-三甲基苯甲酰基亚磷酸锂、曙红y及其共引发剂中的一种,所述共引发剂为三乙醇胺或五甲基二乙烯三胺;所述光固化成型的固化光源波长为200-800nm,光固化时间小于或等于5分钟;所述响应性多肽通过固相合成法进行双键修饰。
[0020]
优选地,所述方法包括下列步骤:
[0021]
s1)聚二甲基硅氧烷(pdms)微针阵列阴模的制备:将聚二甲基硅氧烷和固化剂(sylgard
184
)按10:1混合均匀,随后将混合的预聚液倾倒至金字塔型微针阵列阳模表面,室温下使用真空除泡装置脱气处理适当时间,然后加热固化一定时间后,脱模即可得到聚二甲基硅氧烷微针阵列阴模。其中,脱气时间可以是0.5-2小时,脱气负压可以是0.06-0.09mpa。热固化温度可以是60-80℃,热固化时间可以是3-6小时。
[0022]
s2)多肽载药微针贴片针体的制备:称取一定量的响应性载药多肽、微针针体的形成材料(生物活性高分子)、光固化剂溶解在去离子水或缓冲液中,充分溶解得微针针体预聚液。将微针针体预聚液倾倒至步骤s1)所得的聚二甲基硅氧烷微针阵列阴模,随后辅助预聚液紧密填充微针阵列阴模。去除多余预聚液后使用光源照射被预聚液紧密填充微针阵列阴模,即可得到多肽载药微针阵列。微针针体的形成材料(生物活性高分子)可以是前文所述中的至少一种,取代度为10%-90%。辅助预聚液紧密填充微针阵列阴模的方式可以是真空脱气法、超声波脱气法、离心法中的一种。
[0023]
s3)多肽载药微针贴片基底的制备:称取一定量的微针基底的形成材料溶解在去离子水或缓冲液中,充分溶解得微针基底溶液。将微针基底溶液倾倒至步骤s2)所得的含有多肽载药微针阵列的聚二甲基硅氧烷微针阵列阴模,随后去除多余基底溶液,在室温下避光干燥。干燥时间可以是12-48小时。最后,将所述的聚二甲基硅氧烷微针阵列阴模剥离,即得到病理微环境响应释药多肽载药微针贴片。
[0024]
按照本发明的再一个方面,提供了多肽载药微针贴片的应用,用于制备通过经皮给药的药物。例如,制备用于治疗增生性瘢痕的药物、制备用于治疗银屑病的药物、制备用于治疗血管瘤的药物、制备用于治疗黑色素瘤的药物、制备用于治疗糖尿病的药物、制备用于治疗感染性囊肿的药物、制备用于治疗脱发的药物、制备用于治疗镇痛的药物。
[0025]
总体而言,通过本发明所构思的以上技术方案与现有技术相比,至少能够取得下列有益效果。
[0026]
(1)本发明提供的多肽载药微针贴片可响应病理微环境的相关刺激释放药物,能在一定程度上对病理微环境进行重塑。本发明将多肽作为药物载体,能够增加不溶性药物的水溶性,并且多肽无毒。本发明中经药物通过物理包裹作用、配位作用或偶联共价作用负载于响应性多肽上,响应性多肽在环境触发下发生氨基酸之间的键断裂释放药物,该方法为药物释放提供了第一重响应性能,并且响应性多肽与生物活性高分子发生交联反应形成
网络结构,能将药物固定在生物活性高分子上,使得对药物释放速率进行调控成为可能。
[0027]
(2)本发明中所使用响应性多肽与微针针体的形成材料(即生物活性高分子)可以根据不同的病理微环境进行选择、组合使用,适用范围较广。例如,响应性多肽可以通过氧化还原响应触发自身断裂释放药物,而生物活性高分子可以通过酶响应触发而自身降解,并且响应性能在一定程度上对病理微环境进行重塑,与药物形成协同作用,对疾病治疗起到积极作用。本发明提供的多肽载药微针贴片能在一定程度上对病理微环境进行重塑,例如改变病灶组织中不利于组织修复的酶、活性氧、ph值等因素。
[0028]
(3)本发明中轻微旋转微针贴片基底实现针体与基底分离,这是由于本发明中微针针体交联而微针基底背衬不交联或是采用另一种材料,两部分交界处材料机械强度较弱,沿径向用力后可将两部分分离。
[0029]
(4)本发明中响应性多肽的序列可以有多种组合,例如将具有靶向性的序列与具备环境响应性的序列进行组合等,既可以实现其环境响应性,又能实现其靶向性。并且,本发明中所采用的响应性功能多肽均由天然氨基酸固相合成得到,合成简单、成本低廉、易于修饰。并且多肽生物活性高、响应性能好、系统副作用小、体内易降解代谢。
[0030]
(5)本发明中所使用负载药物可以广泛选择,满足不同使用者的需求。
[0031]
(6)本发明中可以通过调控制备步骤条件参数(例如预交联溶液浓度、交联强度等),实现负载药物释放速率的精准控制。
[0032]
(7)本发明微针贴片采用分步筑造法,针体和基底可以分离,针体滞留在病灶部位程序性缓释药物,作用安全、高效,使用方便,具有工业转化潜力。
附图说明
[0033]
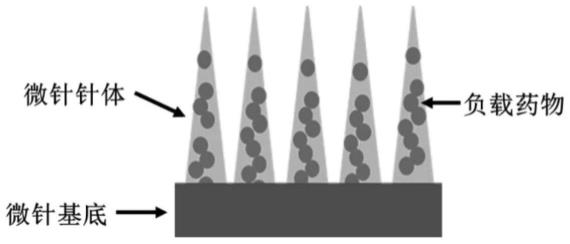
图1为本发明中微环境响应释药的多肽载药微针贴片的结构剖视图;
[0034]
图2为本发明中微环境响应释药的多肽载药微针贴片的光学照片;
[0035]
图3为本发明中微环境响应释药的多肽载药微针贴片透皮后的兔耳光学照片;
[0036]
图4为本发明中微环境响应性载药多肽的响应性能图;
[0037]
图5为本发明中微环境响应性微针针体材料的响应性能图;
[0038]
图6为本发明中微环境响应性微针针体材料响应性能的可控制性图;
[0039]
图7为本发明中微环境响应释药的多肽载药微针贴片的药物释放可控性能图;
[0040]
图8为本发明中微环境响应释药的多肽载药微针贴片对于增生性瘢痕疾病模型的治疗效果图。
具体实施方式
[0041]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。此外,下面所描述的本发明各个实施方式中所涉及到的技术特征只要彼此之间未构成冲突就可以相互组合。
[0042]
实施例1
[0043]
本实施例提供一种微环境响应释药的多肽载药微针贴片,该微针贴片包括基底、针体,其剖面结构如图1所示。
[0044]
本实施例中响应性多肽利用标准固相合成(spps)法合成,根据增生性瘢痕病理微环境中活性氧(ros)过表达的特点选择-pro-pro-pro-序列作为活性氧(ros)响应序列。负载药物选择增生性瘢痕的常规治疗药物5-氟尿嘧啶,并对其结构进行了羧基功能化修饰。微针针体的形成材料与微针基底的形成材料则根据增生性瘢痕病理微环境中基质金属蛋白酶-9(mmp-9)过表达的特点选择甲基丙烯酰胺化明胶与明胶。
[0045]
步骤1:增生性瘢痕病理微环境响应性载药多肽的制备,包括下列子步骤:
[0046]
1)称取1.0克,rink amide-mbha树脂至多肽合成装置,加入分析纯n,n-二甲基甲酰胺溶胀树脂2小时,随后用氩气增压排除溶剂。然后用10毫升含有20%哌啶的n,n-二甲基甲酰胺溶液进行树脂脱保护,反应2次,每次反应20分钟,反应结束后用n,n-二甲基甲酰胺洗涤树脂3次。随后,取少量树脂至于茚三酮与苯酚的乙醇溶液中,加热至沸腾,观察树脂颜色由白色变为紫色则说明树脂脱保护成功,可以进行氨基酸偶联反应。反之,则需要继续脱保护反应。
[0047]
2)称取0.8914克fmoc-lys(alloc)-oh,1.0252克六氟磷酸苯并三唑-1-基-氧基三吡咯烷基磷(pybop),溶解在10毫升n,n-二甲基甲酰胺中,然后将其转移至步骤1)含有处理过树脂的多肽合成装置中,再向体系内加入690微升二异丙基乙胺(dipea),室温下反应4小时。随后用10毫升n,n-二甲基甲酰胺洗涤树脂2次,再次按照同样的比例投料再次反应4小时,使其充分偶联在树脂上。最后使用10毫升n,n-二甲基甲酰胺洗涤树脂3次,取少量树脂至于茚三酮与苯酚的乙醇溶液中,加热至沸腾,观察树脂不变色则说明第一个氨基酸与树脂成功偶联。反之,则需要继续偶联反应。
[0048]
3)用10毫升含有20%哌啶的n,n-二甲基甲酰胺溶液对第一个氨基酸脱保护,反应2次,每次反应20分钟,反应结束后用n,n-二甲基甲酰胺洗涤树脂3次。随后,取少量树脂至于茚三酮与苯酚的乙醇溶液中,加热至沸腾,观察树脂颜色由白色变为紫色则说明第一个氨基酸脱保护成功,可以进行后续氨基酸偶联反应。反之,则需要继续脱保护反应。
[0049]
4)参照步骤2)和步骤3),依次缩合fmoc-pro-oh,fmoc-pro-oh,fmoc-pro-oh,羧基功能化5-氟尿嘧啶(5-fua),得到的氨基酸序列为5-fua-pro-pro-pro-lys。
[0050]
5)称取0.0758克四(三苯基膦)钯,用10毫升二氯甲烷溶解,然后将溶液转移至步骤4)含有处理过树脂的多肽合成装置中,再向体系中加入1943微升苯硅烷,脱除赖氨酸侧链保护基团,反应2次,每次20分钟,反应结束后用n,n-二甲基甲酰胺洗涤树脂3次。随后,取少量树脂至于茚三酮与苯酚的乙醇溶液中,加热至沸腾,观察树脂颜色由白色变为紫色则说明赖氨酸侧链脱保护成功,可以进行后续氨基酸偶联反应。反之,则需要继续脱保护反应。
[0051]
6)称取170微升甲基丙烯酸,1.0252克六氟磷酸苯并三唑-1-基-氧基三吡咯烷基磷(pybop),溶解在10毫升n,n-二甲基甲酰胺中,然后将其转移至步骤5)含有处理过树脂的多肽合成装置中,再向体系内加入690微升二异丙基乙胺(dipea),室温下反应4小时。随后用10毫升n,n-二甲基甲酰胺洗涤树脂2次,再次按照同样的比例投料再次反应4小时,使其充分偶联在树脂上。最后使用10毫升n,n-二甲基甲酰胺洗涤树脂3次,取少量树脂至于茚三酮与苯酚的乙醇溶液中,加热至沸腾,观察树脂不变色则说明氨基酸与赖氨酸侧链成功偶联。反之,则需要继续偶联反应。
[0052]
7)依次使用10毫升二氯甲烷、甲醇、二氯甲烷洗涤树脂各3次,随后使用真空油泵
对树脂进行1小时干燥处理。
[0053]
8)向多肽反应装置中加入9.5毫升三氟乙酸、0.25毫升三异丙基硅烷、0.25毫升去离子水,室温下反应3小时,将多肽与树脂切割分离。将切割液缓慢滴加在冰乙醚中,随即出现白色沉淀。然后再3000rpm转速下离心10分钟分离粗产物,弃去上清液,沉淀用适量甲醇溶解,通过中压纯化色谱系统纯化产物,最后冷冻干燥,收集白色粉末,即得到序列为5-fua-pppk(methacrylic acid),可以响应活性氧(ros)断键释放负载药物的增生性瘢痕病理微环境响应性载药多肽。
[0054]
步骤2:增生性瘢痕病理微环境响应释药多肽载药微针贴片的制备,包括下列子步骤:
[0055]
1)将聚二甲基硅氧烷(pdms)和固化剂(sylgard
184
)按10:1混合均匀,随后将混合的预聚液倾倒至金字塔型微针阵列阳模表面,室温下在-0.08mpa真空度下使用真空除泡装置脱气处理1小时,然后在80℃加热固化5小时,降至室温,脱模即可得到针长650μm,针距500μm,针体数量为10
×
10根/贴片的聚二甲基硅氧烷微针阵列阴模。
[0056]
2)称取135毫克实施例1所得到的响应性多肽、400毫克取代度为60%的甲基丙烯酰胺化明胶、10毫克的2-羟基-2-甲基-1-[4-(2-羟基乙氧基)苯基]-1-丙酮(irgacure 2959)溶解在2毫升去离子水中,充分溶解得微针针体预聚液,溶解后响应性载药多肽的浓度为100mm,微针针体的形成材料的质量分数为20%,光固化剂的质量分数为0.5%。将微针针体预聚液倾倒至步骤1)所得的聚二甲基硅氧烷微针阵列阴模,随后使用超声波脱气法辅助预聚液紧密填充微针阵列阴模。去除多余预聚液后使用波长为365nm,光功率为200mw/cm2的紫外光源照射被预聚液紧密填充微针阵列阴模,照射45秒,即可得到多肽载药微针阵列。
[0057]
3)称取400毫克明胶溶解在2毫升去离子水中,充分溶解得质量分数为20%的微针基底溶液。将微针基底溶液倾倒至步骤2)所得的含有多肽载药微针阵列的聚二甲基硅氧烷微针阵列阴模,随后去除多余基底溶液,在室温下避光干燥24小时。最后,将所述的聚二甲基硅氧烷微针阵列阴模剥离,即得到增生性瘢痕病理微环境响应释药多肽载药微针贴片。
[0058]
将得到的病理微环境响应释药多肽载药微针贴片置于皮肤镜下进行观察,如图2所示,微针针体为排列规整、形状均一、尖端锋利的四棱锥形。
[0059]
结果与表征:
[0060]
(1)微环境响应释药的多肽载药微针贴片的透皮与针体皮下滞留能力。
[0061]
将本实施例制备得到的微环境响应释药的多肽载药微针贴片垂直刺入兔耳皮肤,施力按压2分钟,随后轻微旋转微针贴片基底实现针体与基底分离。观察透皮与针体皮下滞留时间,如图3所示,可以观察到兔耳皮肤表面出现排列规则的点状矩阵,结果说明微针具有良好的机械强度,可有效刺穿兔耳表皮层,提升药物透皮给药速率。并且图3也说明了微针贴片的针体可以与基底分离,能够滞留在皮肤内释放药物,达到长效治疗的目的。
[0062]
(2)病理微环境响应释药多肽载药微针贴片的响应性能评价。分别对响应性多肽与响应性生物活性针体的响应性能进行评价。
[0063]
一方面,实施例1所得到的响应性载药多肽具有-pro-pro-pro-序列作为活性氧(ros)响应序列。称取300毫克载药多肽溶解于1毫升浓度为1
×
(即0.01m,1
×
即为1倍浓度)的磷酸盐缓冲液中,向体系内加入一定量的过氧化氢,最终过氧化氢的浓度分别为0μm、1μ
m、10μm、100μm、1000μm。37℃恒温震荡24小时后,使用高效液相色谱(hplc)法分析载药多肽的降解程度,评价其活性氧(ros)响应性能。结果如图4所示,载药多肽经活性氧(ros)作用后具有降解断键行为,其响应程度与活性氧(ros)含量呈正相关,过程具有可控性。
[0064]
另一方面,实施例1所使用的生物活性微针针体形成材料为具有基质金属蛋白酶-9(mmp-9)响应能力的甲基丙烯酰胺化明胶。移取100微升实施例1中所得的微针针体预聚液,在波长为365nm,光功率为200mw/cm2的紫外光源照射45秒,在室温下避光干燥24小时,即可得到微针针体材料。将上述材料分别至于基质金属蛋白酶-9酶活力为0u/ml、3u/ml、30u/ml、150u/ml、300u/ml的浓度为1
×
的磷酸盐缓冲液中。37℃恒温震荡,定时取出材料,使用称重法计算微针针体材料的降解程度,评价其酶响应性能。结果如图5所示,微针针体材料经基质金属蛋白酶-9作用后具有降解行为,其响应程度与酶活力呈正相关,过程具有可控性。
[0065]
(3)微环境响应释药多肽载药微针贴片药物释放速率可控性能评价。
[0066]
移取100微升实施例1中所得的微针针体预聚液,在波长为365nm,光功率为200mw/cm2的紫外光源分别照射10秒、30秒、45秒、60秒,在室温下避光干燥24小时,即可得到交联程度不同的微针针体材料。将上述材料至于基质金属蛋白酶-9酶活力为30u/ml的浓度为1
×
的磷酸盐缓冲液中。37℃恒温震荡,定时取出材料,使用称重法计算微针针体材料的降解程度,比较其酶响应速率。结果如图6所示,通过改变交联时间控制微针针体材料的交联程度,可以有效调控微针针体的降解速率,为药物释放速率可控性提供了保障。
[0067]
随后,将上述所得到的10秒与45秒交联后的微针针体材料至于过氧化氢浓度为100μm、基质金属蛋白酶-9酶活力为150u/ml的浓度为1
×
的磷酸盐缓冲液中。37℃恒温震荡,定时使用高效液相色谱(hplc)法分析材料的药物释放情况。结果如图7所示,通过改变微针贴片制备过程中的重要步骤参数可以起到药物释放速率可控效果。
[0068]
(4)病理微环境响应释药多肽载药微针贴片对于增生性瘢痕疾病模型的治疗效果评价
[0069]
将实施例1所得的载60微克/贴片的45秒交联的增生性瘢痕病理微环境响应释药多肽载药微针贴片按照结果与表征第(1)条中的方法按压于兔耳腹侧面增生性瘢痕病变皮损处,移除基底,将针体留在皮肤内,在活性氧(ros)与基质金属蛋白酶-9(mmp-9)的作用下,缓慢降解释放药物。从实验开始,每周治疗一次,连续三周,观察记录治疗效果。同时设立不给药组、不载药微针组、5-氟尿嘧啶注射组比较差异。治疗效果如图8所示,病理微环境响应释药多肽载药微针贴片对于增生性瘢痕疾病模型的治疗效果优于其他分组,可见瘢痕明显缩小,具有较好的治疗效果。并且在给药过程中动物没有相较于注射组产生明显的疼痛感,说明本发明是一种安全、有效、具有人文关怀的药物递送技术。本发明可在病灶处响应性释放药物,降低了药物给药频率与药物毒副作用,提高了药物的生物利用度,达到了长效治疗的目的,具有广阔的临床转化前景。
[0070]
实施例2
[0071]
本实施例与实施例1的不同之处在于响应性多肽及药物不同。具体地,根据恶性黑色素瘤环境中基质金属蛋白酶-2(mmp-2)过表达的特点选择asn-pro-asp序列作为mmp-2响应序列。负载药物选择adriamycin,通过标准固相合成(spps)法得到序列为adriamycin-npdk(methacrylic acid),可以响应mmp-2断键释放负载药物的恶性黑色素瘤病理微环境
响应性载药多肽。
[0072]
实施例3
[0073]
本实施例与实施例1的不同之处在于响应性多肽及药物不同。具体地,根据银屑病环境中基质金属蛋白酶-2(mmp-2)过表达的特点选择pro-leu-gly-val-arg序列作为mmp-2响应序列。负载药物选择tretinoin,通过标准固相合成(spps)法得到序列为tretinoin-plgvrk(methacrylicacid),可以响应mmp-2断键释放负载药物的银屑病病理微环境响应性载药多肽。
[0074]
实施例4
[0075]
本实施例与实施例1的不同之处在于响应性多肽及药物不同。具体地,根据增生性瘢痕环境中基质金属蛋白酶-9(mmp-9)过表达的特点选择leu-gly-arg-met-gly-leu-pro-gly序列作为mmp-9响应序列。负载药物选择5-fua,通过标准固相合成(spps)法得到序列为5-fua-lgrmglpgk(methacrylic acid),可以响应mmp-2断键释放负载药物的增生性瘢痕病理微环境响应性载药多肽。
[0076]
本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1