一种玫瑰精油醇传递体乳膏剂及其制备方法与应用
1.本发明属于生物医药技术领域,涉及一种玫瑰精油醇传递体乳膏剂及其制备方法与应用。
背景技术:
2.公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
3.皮肤光老化是皮肤长期暴露于紫外线下,变得干燥、粗糙、松弛,出现皱纹及色斑,发生皮革样病变,严重时甚至会发生皮肤癌。光老化发生的主要原因是紫外线驱动的氧化应激作用,导致机体内的自由基产生过多,造成皮肤的氧化损伤。玫瑰精油(rose essential oil,reo)中含有大量萜类、酚酸类及类黄酮类等化合物,可以清除自由基,具有很好的抗氧化作用。但是reo水溶性较差,直接使用影响皮肤水合作用;多种有效成分易挥发性,稳定性较差,致使其作用时间短、利用率低。
技术实现要素:
4.为了解决现有技术的不足,本发明的目的是提供一种玫瑰精油醇传递体乳膏剂及其制备方法与应用,本发明提供的玫瑰精油醇传递体乳膏剂能够促进reo透过角质层,并提高其抗光老化能力,具有缓释作用且使用安全。
5.为了实现上述目的,本发明的技术方案为:
6.一方面,一种玫瑰精油醇传递体,处方由蛋黄卵磷脂、表面活性剂、玫瑰精油、醇和水构成,玫瑰精油、蛋黄卵磷脂、表面活性剂、醇和水的添加比例为40:160~240:40~60:0.5~2.0:3.0~5.0,mg:mg:mg:ml:ml。
7.另一方面,一种上述玫瑰精油醇传递体的制备方法,将蛋黄卵磷脂、表面活性剂、玫瑰精油加入至醇中,搅拌溶解获得有机相,将有机相加入至水中,搅拌获得。
8.本发明采用醇注入法制备的玫瑰精油醇传递体具有更好的稳定性。
9.第三方面,一种玫瑰精油醇传递体乳膏剂,处方由主药、水相和油相构成,所述主药为上述玫瑰精油醇传递体,主药的重量和水相与油相总质量的比为1:0.1~10.0;水相的组成成分包括水、保湿剂和第一防腐剂,油相的组成成分包括液体油相、固体油相、乳化剂、辅助乳化剂、柔顺剂和第二防腐剂。
10.第四方面,一种上述玫瑰精油醇传递体乳膏剂的制备方法,将保湿剂和第一防腐剂加入至水中溶解制成水相;
11.将液体油相、固体油相、乳化剂、辅助乳化剂、柔顺剂和第二防腐剂加热熔融,混合均匀获得油相;
12.将油相加入至水中,高速匀质剪切获得乳膏基质;
13.向乳膏基质中加入主药搅拌均匀即得。
14.第五方面,一种上述玫瑰精油醇传递体和/或玫瑰精油醇传递体乳膏剂在制备抗皮肤光老化的产品中的应用。
15.本发明的有益效果为:
16.1.本发明采用蛋黄卵磷脂、表面活性剂、玫瑰精油、醇和水制备的玫瑰精油醇传递体可促进药物穿过角质层;醇和表面活性剂的加入,使其具有高度的变形性,能增加药物的经皮渗透作用。
17.2.经过体外释放研究表明,本发明制备的玫瑰精油醇传递体能够缓释玫瑰精油,避免有效成分挥发,增加其稳定性、延长作用时间,提高利用率。
18.3.经过抗氧化研究表明,本发明制备的玫瑰精油醇传递体不仅能够避免形成醇传递体带来的抗氧化能力的降低,反而提升了玫瑰精油的抗氧化能力。
19.4.本发明进一步将玫瑰精油醇传递体制成乳膏剂,利用乳膏剂的生物粘附性增加玫瑰精油在皮肤局部的滞留时间,促进其经皮渗透,更好的实现reo的缓释作用,从而达到更好的抗氧化作用,治疗和预防皮肤发生光老化。
20.5.本发明制备的玫瑰精油醇传递体制成乳膏剂无皮肤刺激性和皮肤致敏性,无急性毒性,可用于皮肤,使用安全。
附图说明
21.构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
22.图1为本发明实施例中昆明小鼠体重增加曲线图;
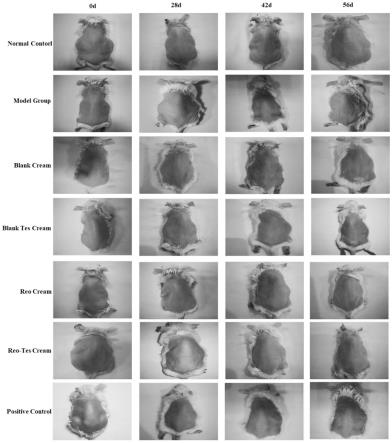
23.图2为本发明实施例中小鼠皮肤外观状态变化图;
24.图3为本发明实施例中皮内反应注射点的排列图;
25.图4为本发明实施例中皮肤刺激实验后外观观察图;
26.图5为本发明实施例中皮肤过敏反应外观观察图。
具体实施方式
27.应该指出,以下详细说明都是示例性的,旨在对本发明提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本发明所属技术领域的普通技术人员通常理解的相同含义。
28.需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本发明的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。
29.本发明所述的醇传递体由磷脂、醇、水以及表面活性剂形成的脂质体。
30.正如背景技术所介绍的,玫瑰精油水溶性差,影响皮肤水合作用,有效成分易挥发导致的稳定性差、作用时间短、利用率低等问题,为了解决如上的技术问题,本发明提出了一种玫瑰精油醇传递体乳膏剂及其制备方法与应用。
31.本发明的一种典型实施方式,提供了一种玫瑰精油醇传递体,处方由蛋黄卵磷脂、表面活性剂、玫瑰精油、醇和水构成,玫瑰精油、蛋黄卵磷脂、表面活性剂、醇和水的添加比
例为40:160~240:40~60:0.5~2.0:3.0~5.0,mg:mg:mg:ml:ml。
32.本发明利用蛋黄卵磷脂、表面活性剂、玫瑰精油、醇和水制成玫瑰精油醇传递体,不仅能够增加玫瑰精油的经皮渗透作用,而且具有缓释玫瑰精油的作用,从而解决直接使用影响皮肤水合作用以及作用时间短、利用率低等问题。
33.在一些实施例中,玫瑰精油与蛋黄卵磷脂的质量比(药脂比)为1:3~9。例如1:3、1:4、1:6、1:9等。研究表明,药脂比影响玫瑰精油的包封率和载药率,当玫瑰精油与蛋黄卵磷脂的质量比1:3~5时,获得的玫瑰精油醇传递体具有较高的包封率和更高的载药率。包封率越高,药物损失越少,载药率越高,玫瑰精油醇传递体的用量越少。因而当玫瑰精油与蛋黄卵磷脂的质量比1:3.8~4.2时,具有包封率和载药率更为适宜。
34.在一些实施例中,表面活性剂包括但不限于吐温20、吐温80、脱氧胆酸钠、油酸。表面活性剂能够增加玫瑰精油的溶解性,从而增加玫瑰精油的包封率。研究表明,表面活性剂的种类不仅影响玫瑰精油的包封率,而且影响玫瑰精油的载药率。当表面活性剂为吐温20时,制备的玫瑰精油醇传递体具有更高的包封率和载药率。
35.在一些实施例中,表面活性剂与蛋黄卵磷脂的质量比为1:4~6。例如1:4、1:4.5、1:5、1:5.5、1:6等。研究表明表面活性剂与蛋黄卵磷脂的质量比影响玫瑰精油醇传递体的包封率和载药率。当表面活性剂与蛋黄卵磷脂的质量比为1:4.6~5.4时,其包封率和载药率更高。
36.在一些实施例中,醇和水的体积比为1:2~8。例如1:2、1:2.5、1:3、1:3.5、1:4、1:4.5、1:5、1:5.5、1:6、1:6.5、1:7、1:7.5、1:8、1:8.5、1:9等。研究表明,包封率随着醇的浓度增加而增加,而当醇和水的体积比增加至1:1.5时,放置2h后出现分层,不稳定。因而在一种或多种实施例中,醇和水的体积比选为1:2~3,优选为1:2~2.5。
37.在一些实施例中,醇为乙醇或乙醇与丙二醇的混合物。研究表明,丙二醇与乙醇合用制备醇质体,既可起到协同促进渗透的作用,也可增加药物的溶解度。其中,丙二醇与乙醇可以任意比例混合,例如1:0.5~2。当乙醇与丙二醇的体积比为1:1.8~2.2时,包封率和载药率更高。
38.本发明的另一种实施方式,提供了一种上述玫瑰精油醇传递体的制备方法,将蛋黄卵磷脂、表面活性剂、玫瑰精油加入至醇中,搅拌溶解获得有机相,将有机相加入至水中,搅拌获得。
39.在一些实施例中,搅拌溶解获得有机相的过程中,进行加热搅拌。加热温度至30~40℃。加热搅拌时间为20~40min。研究表明加热搅拌的时间影响包封率和载药率,当加热搅拌的时间为25~35min时,包封率和载药率更高。
40.在一些实施例中,有机相加入至水中并搅拌的过程中的温度为30~40℃。
41.在一些实施例中,有机相加入至水后搅拌的时间为20~50min。研究表明有机相加入至水后搅拌的时间影响包封率和载药率,当有机相加入至水后搅拌的时间为35~45min时,包封率和载药率更高。
42.在一些实施例中,有机相加入至水后搅拌的速率为300~800rpm。当转速增加至1000rpm后,体系不稳,易损失。研究表明有机相加入至水后搅拌的速率影响包封率和载药率,当有机相加入至水后搅拌的速率为750~800min时,包封率和载药率更高。
43.本发明的第三种实施方式,提供了一种玫瑰精油醇传递体乳膏剂,处方由主药、水
相和油相构成,所述主药为上述玫瑰精油醇传递体,主药的重量和水相与油相总质量的比为1:0.1~10.0;水相的组成成分包括水、保湿剂和第一防腐剂,油相的组成成分包括液体油相、固体油相、乳化剂、辅助乳化剂、柔顺剂和第二防腐剂。
44.本发明利用乳膏剂的生物粘附性增加玫瑰精油在皮肤局部的滞留时间,促进其经皮渗透,更好的实现reo的缓释作用,从而达到更好的抗氧化作用,治疗和预防皮肤发生光老化。
45.在一些实施例中,乳化剂包括但不限于吐温80、卵磷脂、泊洛沙姆188。乳化剂的使用量为1~3%。当1.8~2.2%卵磷脂作为乳化剂时,玫瑰精油醇传递体乳膏剂的外观性状、涂展性及离心稳定性更好。
46.在一些实施例中,油相和水相的质量比为1:1~4。例如1:1、1:1.5、1:2、1:2.3、1:3、1:4等。当油相和水相的质量比为1:2.8~3.2时,玫瑰精油醇传递体乳膏剂的外观性状、涂展性、离心稳定性及肤感更好。
47.在一些实施例中,固体油相为单硬脂酸甘油酯、鲸蜡醇、六聚甘油硬脂酸酯中的一种或多种。研究表明,固体油相为六聚甘油硬脂酸酯和鲸蜡醇时,玫瑰精油醇传递体乳膏剂的外观性状、涂展性、离心稳定性及肤感更好。固体油相的添加量为5~15%。
48.在一些实施例中,柔顺剂为二甲基硅油(聚二甲基硅氧烷)。柔顺剂的添加量为0.1~2%。当不使用柔顺剂时,涂展性极差。当采用柔顺剂的添加量为1.7~2%时,涂展性更好。
49.在一些实施例中,保湿剂包括但不限于甘油、丙二醇和丁二醇。保湿剂用量为5~20%。研究表明保湿剂为甘油,且用量为14~16%时,效果更好。
50.在一些实施例中,辅助乳化剂如司盘60。用量为5~15%。
51.第一防腐剂可添加也可以不添加,第二防腐剂可添加也可以不添加,但是必须添加一种防腐剂,在一些实施例中,第一防腐剂为苯氧乙醇,第二防腐剂为羟苯甲酯。研究表明苯氧乙醇与羟苯甲酯联合应用,不仅可以降低使用剂量,而且能够协同增强抑菌能力。第一防腐剂的添加量为0~2%。第二防腐剂的添加量为0~2%。
52.本发明的第四种实施方式,提供了一种上述玫瑰精油醇传递体乳膏剂的制备方法,将保湿剂和第一防腐剂加入至水中溶解制成水相;
53.将液体油相、固体油相、乳化剂、辅助乳化剂、柔顺剂和第二防腐剂加热熔融,混合均匀获得油相;
54.将油相加入至水中,高速匀质剪切获得乳膏基质;
55.向乳膏基质中加入主药搅拌均匀即得。
56.在一些实施例中,水相的制备在70~90℃条件下进行。
57.在一些实施例中,油相的制备在70~90℃条件下进行。
58.在一些实施例中,将油相加入至水的过程中,温度为70~90℃。能够更好的保证油相流动,分散更均匀。
59.在一些实施例中,将油相加入至水的过程中,搅拌速率为200~400rpm。
60.本发明所述的高速匀质剪切中的速率不低于2000rpm。在一些实施例中,高速匀质剪切的转速为5000~10000rpm。当高速匀质剪切的转速为8000~10000rpm,外观更均匀细腻。
61.在一些实施例中,高速匀质剪切的时间为5~30min,当高速匀质剪切的时间为10~15min时,玫瑰精油醇传递体乳膏剂的涂展性更好。
62.本发明的第五种实施方式,提供了一种上述玫瑰精油醇传递体和/或玫瑰精油醇传递体乳膏剂在制备抗皮肤光老化的产品中的应用。
63.本发明所述的产品包括但不限于药品、医疗器械和化妆品。
64.为了使本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例详细说明本发明的技术方案。以下实施例中的原料除特殊说明外均为市售获得。
65.实施例1
66.精密称取180mg蛋黄卵磷脂,38mg吐温-20,25mg reo,1.0ml无水乙醇于具塞茄形瓶中,置于磁力搅拌器上,加热到30℃,搅拌溶解作为有机相,然后将有机相缓慢加入至3.5ml水中,温度保持在30℃不变,持续搅拌一段时间,制得reo醇传递体混悬液。
67.实施例2
68.本实施例与实施例1相同,不同在于:药脂比(w/w)为1:3,即180mg蛋黄卵磷脂、60mg reo。
69.实施例3
70.本实施例与实施例1相同,不同在于:药脂比(w/w)为1:4,即180mg蛋黄卵磷脂、45mg reo。
71.实施例4
72.本实施例与实施例1相同,不同在于:药脂比(w/w)为1:6,即180mg蛋黄卵磷脂、30mg reo。
73.实施例5
74.本实施例与实施例1相同,不同在于:药脂比(w/w)为1:9,即180mg蛋黄卵磷脂、20mg reo。
75.实施例6
76.本实施例与实施例1相同,不同在于:表面活性剂由吐温20改为吐温80。
77.实施例7
78.本实施例与实施例1相同,不同在于:表面活性剂由吐温20改为油酸。
79.实施例8
80.本实施例与实施例1相同,不同在于:表面活性剂由吐温20改为脱氧胆酸钠。
81.实施例9
82.本实施例与实施例1相同,不同在于:表面活性剂与磷脂比例(w/w)为1:4,即180mg蛋黄卵磷脂、40mg吐温20。
83.实施例10
84.本实施例与实施例1相同,不同在于:表面活性剂与磷脂比例(w/w)为1:5,即180mg蛋黄卵磷脂、36mg吐温20。
85.实施例11
86.本实施例与实施例1相同,不同在于:表面活性剂与磷脂比例(w/w)为1:6,即180mg蛋黄卵磷脂、30mg吐温20。
87.实施例12
88.本实施例与实施例1相同,不同在于:相体积比(乙醇/水)为1:9,即0.5ml无水乙醇,4.5ml水。
89.实施例13
90.本实施例与实施例1相同,不同在于:相体积比(乙醇/水)为1:4,即1.0ml无水乙醇,4.0ml水。
91.实施例14
92.本实施例与实施例1相同,不同在于:相体积比(乙醇/水)为3:7,即1.5ml无水乙醇,3.5ml水。
93.实施例15
94.本实施例与实施例1相同,不同在于:相体积比(乙醇/水)为2:3,即2.0ml无水乙醇,3.0ml水。
95.实施例16
96.本实施例与实施例1相同,不同在于:无水乙醇改为丙二醇与乙醇体积比为1:2的混合液。
97.实施例17
98.本实施例与实施例1相同,不同在于:无水乙醇改为丙二醇与乙醇体积比为1:1的混合液。
99.实施例18
100.本实施例与实施例1相同,不同在于:无水乙醇改为丙二醇与乙醇体积比为2:1的混合液。
101.实施例19
102.本实施例与实施例1相同,不同在于:有机相制备过程中,加热搅拌的时间为20min。
103.实施例20
104.本实施例与实施例1相同,不同在于:有机相制备过程中,加热搅拌的时间为30min。
105.实施例21
106.本实施例与实施例1相同,不同在于:有机相制备过程中,加热搅拌的时间为40min。
107.实施例22
108.本实施例与实施例1相同,不同在于:有机相与水相的混合时间为20min。
109.实施例23
110.本实施例与实施例1相同,不同在于:有机相与水相的混合时间为30min。
111.实施例24
112.本实施例与实施例1相同,不同在于:有机相与水相的混合时间为40min。
113.实施例25
114.本实施例与实施例1相同,不同在于:有机相与水相的混合时间为50min。
115.实施例26
116.本实施例与实施例1相同,不同在于:有机相制备过程中,加热搅拌的转速为
300rpm。
117.实施例27
118.本实施例与实施例1相同,不同在于:有机相制备过程中,加热搅拌的转速为500rpm。
119.实施例28
120.本实施例与实施例1相同,不同在于:有机相制备过程中,加热搅拌的转速为800rpm。
121.实施例29
122.精密称取179mg蛋黄卵磷脂,36mg吐温-20,45mg reo,1.5ml无水乙醇于具塞茄形瓶中,置于磁力搅拌器上,加热到30℃,800rpm搅拌30min,获得有机相,然后将有机相缓慢加入至3.5ml水中,温度保持在30℃不变,持续搅拌40min,制得reo醇传递体混悬液。
123.实施例30
124.(1)水相的制备:首先将水相的各成分按处方量称取放到25ml烧杯中,加热至80℃,搅拌使之溶解变成透明状态;
125.(2)油相的制备:另取25ml烧杯,将油相中各成分按处方量称取,然后加热至80℃左右,使其完全熔融,搅拌均匀;
126.(3)乳膏基质的制备:在80℃水浴中,将油相似流状加入到水相中,边加边搅拌(300rpm,15min)至乳化形成乳白色液体,离开水浴后,高速匀质剪切(5000rpm)10min,冷却至室温备用;
127.(4)reo-tes cream(玫瑰精油醇传递体乳膏剂)的制备:向上述乳膏基质中加入处方量的reo-tes(玫瑰精油醇传递体),用电动搅拌机搅拌均匀,即得reo-tes cream。
128.本实施例的处方见表1。
129.表1本实施例处方组成
[0130][0131][0132]
实施例31
[0133]
本实施例与实施例30相同,区别在于:乳化剂改为1%吐温80,即添加0.1g吐温80。
[0134]
实施例32
[0135]
本实施例与实施例30相同,区别在于:乳化剂改为2%吐温80,即添加0.2g吐温80,去离子水减为6.6g。
[0136]
实施例33
[0137]
本实施例与实施例30相同,区别在于:乳化剂改为3%吐温80,即添加0.3g吐温80,去离子水减为6.5g。
[0138]
实施例34
[0139]
本实施例与实施例30相同,区别在于:乳化剂改为1%卵磷脂,即添加0.1g卵磷脂。
[0140]
实施例35
[0141]
本实施例与实施例30相同,区别在于:乳化剂改为2%卵磷脂,即添加0.2g卵磷脂,去离子水减为6.6g。
[0142]
实施例36
[0143]
本实施例与实施例30相同,区别在于:乳化剂改为3%卵磷脂,即添加0.3g卵磷脂,去离子水减为6.5g。
[0144]
实施例37
[0145]
本实施例与实施例30相同,区别在于:乳化剂改为1%泊洛沙姆188,即添加0.1g泊洛沙姆188。
[0146]
实施例38
[0147]
本实施例与实施例30相同,区别在于:乳化剂改为3%泊洛沙姆188,即添加0.3g泊洛沙姆188,去离子水减为6.5g。
[0148]
实施例39
[0149]
本实施例与实施例30相同,区别在于:乳化剂改为5%泊洛沙姆188,即添加0.5g泊洛沙姆188,去离子水减为6.3g。
[0150]
实施例40
[0151]
本实施例与实施例30相同,区别在于:油相/水相(w/w)比例为2:8。
[0152]
实施例41
[0153]
本实施例与实施例30相同,区别在于:油相/水相(w/w)比例为3:7。
[0154]
实施例42
[0155]
本实施例与实施例30相同,区别在于:油相/水相(w/w)比例为4:6。
[0156]
实施例43
[0157]
本实施例与实施例30相同,区别在于:油相/水相(w/w)比例为5:5。
[0158]
实施例44
[0159]
本实施例与实施例30相同,区别在于:固体油相由单硬脂酸甘油酯和鲸蜡醇改为鲸蜡醇和六聚甘油硬脂酸酯。
[0160]
实施例45
[0161]
本实施例与实施例30相同,区别在于:固体油相由单硬脂酸甘油酯和鲸蜡醇改为单硬脂酸甘油酯和六聚甘油硬脂酸酯。
[0162]
实施例46
[0163]
本实施例与实施例30相同,区别在于:柔顺剂的添加量为0。
[0164]
实施例47
[0165]
本实施例与实施例30相同,区别在于:柔顺剂的添加量为1%,即柔顺剂0.1g,纯化水为6.8g。
[0166]
实施例48
[0167]
本实施例与实施例30相同,区别在于:保湿剂为15%甘油。
[0168]
实施例49
[0169]
本实施例与实施例30相同,区别在于:保湿剂为15%丙二醇。
[0170]
实施例50
[0171]
本实施例与实施例30相同,区别在于:保湿剂为15%丁二醇。
[0172]
实施例51
[0173]
本实施例与实施例30相同,区别在于:步骤(3)中,高速匀质剪切的速率为8000rpm。
[0174]
实施例52
[0175]
本实施例与实施例30相同,区别在于:步骤(3)中,高速匀质剪切的速率为10000rpm。
[0176]
实施例53
[0177]
本实施例与实施例30相同,区别在于:步骤(3)中,高速匀质剪切的时间为5min。
[0178]
实施例54
[0179]
本实施例与实施例30相同,区别在于:步骤(3)中,高速匀质剪切的时间为15min。
[0180]
实施例55
[0181]
本实施例与实施例30相同,区别在于:步骤(3)中,高速匀质剪切的时间为30min。
[0182]
实施例56
[0183]
(1)水相的制备:将水相成分按处方量称取放到25ml烧杯中,水浴加热(80℃)并搅拌10min使之溶解变成透明状态。
[0184]
(2)油相的制备:另取25ml烧杯,将油相各成分按处方量称取,然后水浴加热(80℃)10min,使其完全熔融,搅拌均匀;
[0185]
(3)乳膏基质的制备:在80℃水浴中,将油相似流状加入到水相中,边加边搅拌(300rpm),搅拌15min均匀后,离开水浴,移至高速匀质机下剪切10min(8000rpm),冷却备用;
[0186]
(4)reo-tes cream的制备:向上述乳膏基质中加入处方量的reo-tes,然后转移至电动搅拌机设备搅拌30min(300rpm),即得reo-tes cream。
[0187]
本实施例的处方见表2。
[0188]
表2本实施例处方组成
[0189][0190]
包封率(ee)和载药量(dl)的测定:
[0191]
采用超滤离心法测定reo-tes的ee和dl。精密移取100μl reo-tes混悬液至超滤离心管中,加入100μl纯化水混合均匀,离心(4000rpm,10min),再加入200μl纯化水离心(4000rpm,10min),取内层液体于5ml容量瓶内,用dmso涡旋破乳后,用dmso定容至刻度,在检测波长处测吸光度,计算包载药物量,记为wen。精密量取100μl reo-tes混悬液至5ml容量瓶内,用dmso涡旋使其破乳后,用dmso定容至刻度,在检测波长处测定吸光度,计算reo总量,记为wtotal。再根据下列公式,计算ee和dl。
[0192][0193][0194]
实施例2~27的ee和dl分别如表3~10所示。
[0195]
表3以药脂比为变量的ee和dl
[0196][0197]
表3表明,随着药脂比的增加,包封率呈现降低的趋势,载药量增加,当比例为1:4,ee和dl均较好,因此最佳的药脂比选择1:4。
[0198]
表4以表面活性剂为变量的ee和dl
[0199][0200]
由表4可知,采用吐温20作为表面活性剂时,包封率和载药量均较高。
[0201]
表5以吐温20/卵磷脂(w/w)为变量的ee和dl
[0202][0203]
由表5可知,随着吐温20与磷脂比例的增加,包封率和载药量呈现先增加后降低的趋势,可能是过多的表面活性剂使磷脂双分子层变得不稳定,从而导致包封率降低,因此,选择1:5为最佳比例。
[0204]
表6以相体积比为变量的ee和dl
[0205][0206]
由表6可知,包封率随着乙醇浓度增加而增加,但当有机相/水相增加至2:3后,醇传递体放置2h后出现分层,很不稳定,可能是大量乙醇导致了醇传递体溶解,因此未进行包封率的测定,因此,选择3:7为最佳比例。
[0207]
表7以有机相为变量的ee和dl
[0208][0209]
由表7可知,随着丙二醇/乙醇降低,包封率和载药量均降低,因此选择乙醇/丙二醇为1:2为最佳比例。
[0210]
表8以有机相加热时间为变量的ee和dl
[0211][0212]
表9以有机相与水的混合时间为变量的ee和dl
[0213][0214]
由表8和表9可知,随加热时间增加至30min后,混合时间增加至40min后包封率和载药量不再增加;因而选择加热时间为30min、混合时间为40min为更佳。
[0215]
表10以有机相与水的搅拌速度为变量的ee和dl
[0216][0217]
由表10可知,包封率和载药量随搅拌速度增加而增加,但是转速增至1000rpm后,体系不稳,溶液易飞溅到烧瓶壁上造成损失,所以选择转速为800rpm。
[0218]
根据实施例1~28的优化过程和表3~10的优化结果,可以确定一个效果更好的更佳处方和工艺,具体为实施例29。以下测试中reo-tes cream,均按实施例29的方法制备。
[0219]
按照实施例29的方法,制备三批reo-tes,外观呈淡黄色的混悬液,有明显的丁达尔现象;微观形态呈类球形,粒径均一,形状规则无粘连,其粒径、ζ-电位、包封率及载药量结果见表11。
[0220]
表11三批reo-tes的粒径、ζ-电位、包封率及载药量
[0221][0222]
由表11可知,粒径为(113.72
±
1.35)nm,ζ-电位为(-7.29
±
0.86)mv,ph为(4.93
±
0.05);ee为(92.13
±
0.79)%和dl为(15.80
±
0.44)%,实施例27的处方和工艺稳定可靠。
[0223]
三批reo-tes初步稳定性考察结果见表12。
[0224]
表12三批reo-tes初步稳定性考察结果
[0225][0226][0227]
表11表明,在一个月内,随着放置时间的延长reo-tes粒径逐渐变大,由最初的(113.72
±
1.35)nm增至(182.09
±
1.95)nm,ζ-电位由(-7.29
±
0.86)mv降低至(-11.96
±
0.24)mv,但粒径分布与ζ-电位分布仍比较均匀;ee有所降低,由最初(92.13
±
0.79)%降低至(64.24
±
1.47)%。说明reo-tes磷脂膜不稳定,发生渗漏而造成ee的降低,如果增加体系的黏性,有可能提高其稳定性。
[0228]
reo-tes体外释放实验:采用动态膜透析法考察reo-tes中reo的释放行为,并以reo-sol作为对照。
[0229]
分别精密吸取1ml reo-sol、blank tes和reo-tes装入透析袋,将透析袋置于装有25ml释放介质的离心管中,放置于恒温振荡仪(温度37℃,转速100rpm)。于1h、2h、4h、6h、8h、12h、24h、36h和48h取出4ml样品,并补充4ml释放介质,始终保持释放介质总体积为25ml。取出的样品采用uv法测定其吸光度,代入标准曲线方程,计算reo的浓度,累积释放百分率(q)计算见公式(3-1)。以q为纵坐标,以取样时间t为横坐标,绘制reo-sol和reo-tes体外释放曲线,并用数学模型对体外释药曲线进行拟合。
[0230][0231]
式中,ci为第i次取样时释放介质中reo的浓度,v为释放介质总体积,c1为第1次取样时释放介质中reo浓度,v1为第1次取样的体积,c
i-1
、v
i-1
依次类推,w为reo的总质量。
[0232]
reo-sol和reo-tes(实施例27)的体外累积释放百分率实验结果见表13。
[0233]
表13reo-sol和reo-tes的体外释放结果
[0234][0235]
由表13可知,reo-sol在24h累积释放百分率达到(79.18
±
3.13)%;reo-tes释放相对缓慢,24h仅释放(63.93
±
5.70)%,并且在24h之后reo-tes仍在释放药物,48h累积释放百分率达(77.47
±
5.03)%,说明reo-tes具有一定的缓释效果。
[0236]
超氧阴离子自由基(
·o2-)清除率实验
[0237]
以不加邻苯三酚的ph7.40tris-hcl缓冲液(50mmol/l)为空白对照,以抗氧化性较强的vc溶液(1ml)作为阳性对照组。reo-sol组中添加1ml reo-sol。reo-tes组中添加reo-tes醇传递体混悬液。当reo(vc)浓度为8mg/ml时,reo-tes组
·o2-清除率(73.17%)高于reo-sol组(49.94%),而同浓度vc的
·o2-清除率高达100%。
[0238]
以上结果表明将reo制备成reo-tes不仅增加了稳定性,而且具有缓释效果,还能够提高抗氧化能力。
[0239]
实施例31~55制备的玫瑰精油醇传递体乳膏剂的外观性状、涂展性及离心稳定性如表14~19所示。
[0240]
表14以乳化剂为变量的外观性状、涂展性及离心稳定性
[0241][0242]
由表14可知,泊洛沙姆188虽然安全性高可作为注射用乳剂的乳化剂,但是做为乳化剂制备的乳膏剂不均匀,有颗粒感;2%的吐温80乳化性很好,但是有特殊气味;卵磷脂(2%)使用安全,气味较小,制备的乳膏剂均匀,所以选择2%卵磷脂作为乳化剂更好。
[0243]
表15以油水相比例为变量的外观性状、涂展性及离心稳定性
[0244][0245]
油相/水相(w/w)不仅影响乳膏剂的黏稠度,也影响了乳膏剂的使用肤感(油腻感),本实验以油相/水相(w/w)为1:4、1:3、3:7、2:3制备乳膏剂,由表15可知,随着比例增加,乳膏剂的黏稠度和油腻感增加,当比例为1:3时,乳膏剂黏稠度适中,肤感最佳。
[0246]
表16以固体油相为变量的外观性状、涂展性及离心稳定性
[0247][0248]
由于烃类碳链长短不同,油相的种类对乳膏的外观和肤感有很大影响,选取致痘风险低、性质较好的单硬脂酸甘油酯、六聚甘油硬脂酸酯、鲸蜡醇中二者合用来改善乳膏剂的性质,表16结果显示,六聚甘油硬脂酸酯和鲸蜡醇合用,乳膏剂性质更好,可能因为六聚甘油硬脂酸酯是亲水性的乳化剂,适合o/w型乳剂,能够在乳液体系中形成层状液晶型胶体网络结构,同时降低乳膏剂黏度,而鲸蜡醇滋润不油腻,所以二者合用效果较好。
[0249]
表17以柔顺剂用量为变量的外观性状、涂展性及离心稳定性
[0250][0251]
常用的柔顺剂一般为二甲基硅油,又称硅油或硅酮,用量为0~2%较为安全,由表17可知,随着二甲基硅油用量增加,乳膏剂的涂展性越好,所以选择2%二甲基硅油为柔顺剂能够更好的增加乳膏剂的涂展性。
[0252]
表18以高速剪切速率为变量的外观性状、涂展性及离心稳定性
[0253][0254]
表19以高速剪切时间为变量的外观性状、涂展性及离心稳定性
[0255][0256][0257]
乳膏剂的黏度和外观均与颗粒大小有关,颗粒越小,分散度越高,乳膏剂的黏度也会变低。由表18和19可知,乳膏剂黏度随着高速剪切速度和时间的增加而降低,而外观颗粒感则减小,综合黏度和外观颗粒性两方面评价结果,选择高速剪切速率为8000rpm,时间为10min,效果更好。
[0258]
根据实施例31~55的优化过程和表14~19的优化结果,可以确定一个效果更好的更佳处方和工艺,具体为实施例56。以下测试中reo-tes cream,均按实施例56的方法制备。
[0259]
按照实施例56的方法,制备三批reo-tes cream,均为乳白色半固体,无异味,无肉眼可见异物,ph为(6.27
±
0.07),黏度为(25815
±
742)mpa
·
s,性质稳定。
[0260]
按照实施例56的方法制备的reo-tes cream的体外累积释放百分率实验结果见表20。
[0261]
表20体外累积释放百分率
[0262][0263]
本发明中,reo cream为按照实施例56的制备方法,将主要替换为reo-sol制得。
[0264]
表20可知,reo cream在12h累积释放百分率达到(69.50
±
4.49)%,12h以后几乎不在释放;reo-tes cream释放相对缓慢,12h仅释放(59.07
±
2.51)%,并且在12h之后reo-tes cream仍在释放药物,24h累积释放百分率达(66.63
±
2.18)%,36h累积释放百分率达(71.68
±
3.41)%,说明reo-tes cream具有一定的缓释效果,能够延长reo作用时间。
[0265]
reo cream和reo-tes cream在皮肤中单位面积累积透皮量和累积透皮百分率结果见表21。
[0266]
表21reo cream和reo-tes cream在皮肤中单位面积累积透皮量和累积透皮百分率
[0267][0268][0269]
由表21可知,各测定时间点reo-tes cream的累积透皮量均高于reo cream,24h时reo-tes cream累积透皮量为(0.6273
±
0.0092)mg/cm2,reo cream累积透皮量为(0.4587
±
0.0166)mg/cm2,reo-tes cream约是reo cream的1.37倍,说明将reo制备为tes可以增加其透皮量。
[0270]
reo-tes cream耐寒耐热试验结果见表22。
[0271]
表22reo-tes cream耐寒耐热试验结果
[0272][0273]
表22可知,经过耐热耐寒试验后未见油水分离,ph和黏度与实验前基本相同;同时经过离心分离后油水未分层。表明reo-tes cream的涂抹性和延展性良好。
[0274]
体内抗氧化试验:
[0275]
取昆明小鼠42只,随机分为7组,每组6只,在22~25℃、相对湿度为60%的环境下,实验小鼠自由饮水进食,适应性饲养1周。将小鼠提前禁食24h,用5%水合氯醛腹腔注射进行麻醉(剂量为0.1ml/10g),所有小鼠背部使用剃毛刀剃去鼠毛,然后使用薇婷脱毛膏除去表面绒毛,暴露大小约4cm
×
4cm的皮肤,间隔7d脱毛一次。将uva(15w)和uvb(15w)灯置于小鼠上方30cm垂直高处,照射前由紫外线感应卡测辐射强度范围为500~1000μw/cm2,第1~2周每次辐射剂量为最小红斑量,第3~4周每次辐射剂量为2倍最小红斑量,第5~6周每次辐射剂量为3倍最小红斑量,第7~8周每次辐射剂量为4倍最小红斑量,紫外辐照共持续8周。
[0276]
分组及给药:(1)正常组:不做任何处理;(2)模型组:只进行紫外照射不给予药物;(3)阳性对照组:每日于紫外照射前30min给予维生素e乳膏;(4)实验组:每日于紫外照射前30min分别给予blank cream、blank tes cream、reo cream和reo-tes cream。
[0277]
各组小鼠体重增加结果见图1。由图1可知,各组小鼠体重随着时间变化均有增加,其中到第八周时,正常组小鼠体重增加最多,大约增加10g;模型组体重增加最少,仅约2g,与正常组小鼠相比,体重增加明显变缓;blank cream组、blank tes cream组、reo cream组、reo-tes cream组和阳性对照组均有增加,分别为3.05g、1.77g、4.94g、7.55g和4.88g,均没有正常小鼠体重增加多,说明紫外线照射对小鼠的食欲有一定影响,而reo cream组、reo-tes cream组和阳性对照组均比模型组增加多,说明reo cream和reo-tes cream的治疗对小鼠皮肤光氧化有一定保护修复作用,同时从另一方面也说明两种乳膏剂无急性毒性。
[0278]
经紫外光照射后,小鼠的皮肤外观形态变化见图2。由图2可知,正常组小鼠背部皮肤光滑细腻,无明显毛细血管;模型组第28d时小鼠皮肤出现明显红斑,毛细血管扩张明显,第42d时出现较明显皱纹,第56d时皱纹加深,褶皱明显,皮肤粗糙,出现皮革样病变,根据评价标准为iii级光老化;blank cream组和blank tes cream组小鼠于第56d时皮肤皱纹非常明显,评价为iii级光老化,但与模型组各时间点相比,空白制剂组皮肤皱纹较细,褶皱较浅,说明空白制剂对皮肤光氧化有一定保护作用,这可能与空白乳膏剂中辅料,如甘油或者不饱和脂肪酸等成分具有一定保湿性和抗氧化性有关;阳性对照组第42d时皮肤较粗造,第56d时出现明显皱纹,光老化程度为i级;reo cream组28d时小鼠皮肤仍较光滑,第42d时出现细小皱纹,第56d时皱纹略有加深,且出现明显毛细血管,为ii级光老化,说明reo cream有明显的抗光氧化作用;reo-tes cream组42d时小鼠皮肤仍未见皱纹,至第56d时可观察到红斑及毛细血管,和细小皱纹,光老化程度为i级,说明reo-tes cream能够保护皮肤,大大降低紫外线造成的损伤。
[0279]
皮肤刺激性试验:以生理盐水和棉籽油为浸提介质,分别将1greo-tes乳膏剂置于
10ml的浸提介质中37℃浸提24h,生理盐水和棉籽油(不含试验物)作同样处理作为对照试剂。随机选取3只已适应性喂养一周的家兔,提前禁食24h,实验时用10%水合氯醛耳缘静脉注射进行麻醉(剂量为3ml/kg),除去家兔背部脊柱两侧足够面积的毛发(约20cm
×
15cm)作为试验和观察部位,按照图3进行皮内注射样品各0.2ml。注射后立即观察注射点的即时反应,并于注射后(24
±
2)h、(48
±
2)h和(72
±
2)h观察并记录注射点红斑、水肿的组织反应情况并评分。皮肤刺激反应评分标准见表23,皮肤刺激强度评价标准见表24。
[0280]
表23皮肤刺激反应评分标准
[0281][0282][0283]
表24皮肤刺激强度评价标准
[0284][0285]
皮内刺激试验后家兔皮肤外观观察见图4,皮肤刺激强度评分结果见表25。由图4可知,皮内注射试样后,生理盐水浸提物注射点处皮肤略有红肿,于72h时红肿消失,其余注射点处无明显变化。皮下注射试样后,各组皮肤he染色无明显区别,皮肤组织完整。对刺激强度进行评分,可得知皮下注射生理盐水浸提物有轻度刺激性。
[0286]
表25皮肤刺激强度评分表
[0287][0288]
皮肤过敏性试验:
[0289]
(1)诱导接触试验:选取15只适应性饲养一周的豚鼠,使用电动剃毛刀去除去豚鼠脊柱左侧实验部位(2.0cm
×
3.0cm)的毛发,皮肤应为无破损的健康状态。将豚鼠随机分为5组。第0、7天和14天,于a组豚鼠左侧脱毛区皮肤上涂抹1%的2,4-二硝基氯苯丙酮溶液0.5ml,b组涂抹blank cream 1g,c组涂抹blank tes cream 1g,d组涂抹reo cream 1g,e组涂抹reo-tes cream 1g,使用医用纱布包扎固定,6h后解除包扎,擦净皮肤。
[0290]
(2)激发接触试验:在最后一次诱导接触后14天,于a组豚鼠右侧脱毛区皮肤上涂抹1%的2,4-二硝基氯苯丙酮溶液0.5ml,b组涂抹blank cream 1g,c组涂抹blank tes cream 1g,d组涂抹reo cream 1g,e组涂抹reo-tes cream 1g,使用医用纱布包扎固定,6h后解除包扎,擦净皮肤,立即观察,并分别于(24
±
2)h、(48
±
2)h和(72
±
2)h再次观察皮肤状态。评分标准:无明显改变为0分,散发性或斑点状红斑为1分,中度融合性红斑为2分,重度红斑和/或水肿为3分,当试验样品组动物皮肤反应积分≥1时,应判为变态反应阳性,进行致敏强度分级(过敏反应发生率为0~8%时,致敏强度为弱;过敏反应发生率为9~28%时,致敏强度为轻;过敏反应发生率为29~64%时,致敏强度为中;过敏反应发生率为65~80%时,致敏强度为强;过敏反应发生率为81~100%时,致敏强度为极强),过敏反应发生率计算按如下公式进行。
[0291][0292]
各组豚鼠给药部位的皮肤外观观察结果见图5。由图5可知,各组豚鼠皮肤在给药前均处于健康状态。阳性对照组3只豚鼠在末次激发接触6h后,均出现重度红斑和水肿;24h后,水肿略有好转,但仍有紫红色红斑;48h后水肿消散,红斑稍有好转;72h后,红斑逐渐消退。blank cream组、blank tes cream组、reo cream组与reo-tes cream组均有1~2只豚鼠在末次激发接触6h后,出现一些散发性或斑点状红斑;但是在24h后,红斑均消退。对上述皮肤过敏反应进行评分,并计算致敏发生率得到表26,结果说明2,4-二硝基氯苯丙酮溶液有极强致敏性,其余4组无致敏性。
[0293]
表26皮肤过敏反应结果
[0294][0295]
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1