一种植物界面超组装食药同源材料及其制备方法和应用
1.本发明属于生物材料技术领域,具体涉及一种植物界面超组装食药同源材料及其制备方法和应用。
背景技术:
2.结肠炎(colitis)是指各种原因引起的结肠炎症性病变。可由细菌、真菌、病毒、寄生虫、原虫等生物引起,亦可由变态反应及理化因子引起,根据病因不同,可分为特异性炎性病变和非特异性炎性病变,前者指感染性结肠炎、缺血性结肠炎和伪膜性结肠炎等,后者包括溃疡性结肠炎及结肠crohn病。主要临床表现腹泻、腹痛、黏液便及脓血便、里急后重、甚则大便秘结、数日内不能通大便,常伴有消瘦乏力等,多反复发作。我国溃疡性结肠炎的发病率呈逐渐上升趋势,病程冗长,且有并发结肠癌的危险,因此受到人们越来越多的重视。
3.临床对于结肠炎主要应用柳氮磺胺吡啶、美沙拉嗪和奥沙拉嗪等氨基水杨酸类药物作为主要的治疗药物,对大部分轻、中度患者可收获较好的疗效,但对部分患者,特别是长期服药的患者存在易复发和副作用大等缺陷,且长期服药价格较高。因此,寻找廉价且副作用小的新疗法成为近年来医药学界的研究热点。目前结肠炎的一线治疗方法包括口服或直肠给予美莎拉嗪及前体药物柳氮磺吡啶和巴柳氮等,但具有严重的毒副作用,限制了它们的应用。
4.药食两用植物是指既可食用又能作为中药材防病治病的植物。我国幅员广大,民族众多,各个民族都有其独特的饮食文化和食疗经验。他们经常食用身边可随手拈来的野生或栽培的植物,以达到祛病强身之目的。但民间有很多食用植物,由于有关部门尚未对其进行科学、系统地研究,对其疗效和长期毒性尚未进行科学评价。近十几年来材料科技取得了突飞猛进的发展,功能材料的应用日益广泛,将功能材料在植物体内超组装合成,从而合成药食同源植物。
技术实现要素:
5.为解决现有技术的问题,本发明提供了一种植物界面超组装食药同源材料及其制备方法和应用。
6.本发明的具体技术方案如下:
7.本发明提供了一种植物界面超组装食药同源材料的制备方法,其特征在于,包括如下步骤:步骤s1,将二甲基咪唑、乙酸锌和目标药物溶于去离子水中,得到混合溶液;步骤s2,将新鲜的活体植物置于模拟日光下,在混合溶液中孵育,冻干即得植物界面超组装食药同源材料,其中植物界面超组装食药同源材料体内界面超组装的框架材料safs包裹了治疗或缓解结肠炎的目标药物。
8.本发明提供的植物界面超组装食药同源材料的制备方法,还具有这样的技术特征,其中,目标药物为美沙拉嗪(5-asa)。
9.本发明提供的植物界面超组装食药同源材料的制备方法,还具有这样的技术特征,其中,二甲基咪唑的浓度为1~300mmol/l,乙酸锌的浓度为1~300mmol/l,目标药物的浓度为1~2000μg/ml。
10.本发明提供的植物界面超组装食药同源材料的制备方法,还具有这样的技术特征,其中,在混合溶液中孵育的时间为5~40h。
11.本发明还提供了一种植物界面超组装食药同源材料,其特征在于,采用上述植物界面超组装食药同源材料的制备方法制备得到。
12.本发明还提供了一种上述植物界面超组装食药同源材料在制备用于治疗或缓解结肠炎的食品或药品中的应用。
13.发明的作用与效果
14.本发明首先将二甲基咪唑、乙酸锌和目标药物溶于去离子水中,得到混合溶液;然后将新鲜的活体植物置于模拟日光下,在混合溶液中孵育,冻干即得植物界面超组装食药同源材料,其中该植物界面超组装食药同源材料体内界面超组装的框架材料safs包裹了治疗或缓解结肠炎的目标药物。将该植物界面超组装食药同源材料应用在制备用于治疗或缓解结肠炎的食品或药品中。
15.本发明的植物界面超组装食药同源材料对结肠炎起到了有效的治疗或缓解,效果良好,且优于目标药物直接给药。
附图说明
16.图1是实施例1的葱体内界面超组装safs包裹5-asa的原理图。
17.图2是实施例1的葱体内界面超组装safs包裹5-asa的激光共聚焦图和未包裹5-asa的葱体内界面超组装safs的激光共聚焦图。图2中的a、b和c为孵育3h时葱体内界面超组装safs包裹5-asa的激光共聚焦图;图2中的d、e和f为孵育8h时葱体内界面超组装safs包裹5-asa的激光共聚焦图;图2中的g、h和i为孵育10h时葱体内界面超组装safs包裹5-asa的激光共聚焦图;图2中的j、k和l为孵育10h时未包裹5-asa的葱体内界面超组装safs的激光共聚焦图。图中白色和黑色线框内的物质为呈蓝光的5-asa。
18.图3是实施例1的植物界面超组装食药同源材料治疗小鼠结肠炎时小鼠体重变化图。
19.图4是实施例1的植物界面超组装食药同源材料治疗小鼠结肠炎后小鼠结肠的光学图像和长度数据图。图4中的a是结肠的光学图像;图4中的b是结肠的长度数据图。
20.图5是实施例1的植物界面超组装食药同源材料治疗小鼠结肠炎后疾病活动指数数据图。
21.图6是实施例1的植物界面超组装食药同源材料治疗小鼠结肠炎后结肠he染色图。
22.图7是实施例1的植物界面超组装食药同源材料治疗小鼠结肠炎后病理切片评分数据图。
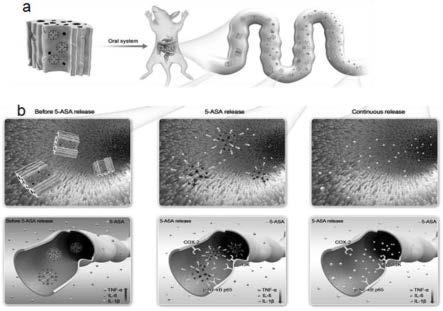
23.图8是实施例1的植物界面超组装食药同源材料在小鼠消化系统的原理图和在小鼠结肠内降低验证因子的原理图。图8中的a是植物界面超组装食药同源材料在小鼠消化系统的原理图;图8中的b是植物界面超组装食药同源材料在小鼠结肠内降低验证因子的原理图。
24.图9是实施例1的植物界面超组装食药同源材料在小鼠结肠内降低验证因子1l-1β、tnf-α和1l-6数据图。
25.图10是实施例1的植物界面超组装食药同源材料在小鼠结肠内药物释放时间曲线示意图。
26.图11是实施例2的植物界面超组装食药同源材料治疗小鼠结肠炎时小鼠体重变化图。
27.图12是实施例2的植物界面超组装食药同源材料治疗小鼠结肠炎后小鼠结肠的光学图像图和长度数据图。图12中的a是结肠的光学图像;图12中的b是结肠的长度数据图。
具体实施方式
28.在本发明中使用的术语,除非另有说明,一般具有本领域普通技术人员通常理解的含义。
29.在以下实施例中,未详细描述的各种过程和方法是本领域中公知的常规方法。
30.下述实施例中所采用的试剂为普通商业途径购得,未注明的实验操作及实验条件参考本领域的常规操作及常规条件。
31.下述实施例中所采用的活体葱购买于济南市历下区文化东路菜市场。绿豆芽由绿豆萌发4天得到。实验药品均采购于aladdin公司,二甲基咪唑cas号:654058-04-5,分子式:c7h
15
n2o4p,分子量:222.18;二水乙酸锌cas号:5970-45-6,分子式:zn(ch3coo)2·
2h2o,分子量:219.51;5-asa cas号:89-57-6,分子式:c7h7no3,分子量:153.14;硫酸葡聚糖钠盐(dss)cas号:9011-18-1。winsure品牌高功率阳光模拟器。balb/c(c)x小鼠由山东省科学院分析测试中心提供。
32.以下结合实施例和附图来说明本发明的具体实施方式。
33.《实施例1》
34.本实施例采用活体葱(so)界面超组装得到植物界面超组装食药同源材料,并将其应用于治疗小鼠结肠炎,植物界面超组装食药同源材料的制备包括如下步骤:
35.步骤s1,将二甲基咪唑、乙酸锌和目标药物溶于去离子水中,得到混合溶液,具体过程为:
36.将263mg二甲基咪唑、176mg二水乙酸锌和200μg 5-asa分别加入到20ml去离子水中,搅拌30min,然后分别取10ml二甲基咪唑溶液、15ml二水乙酸锌溶液和20ml 5-asa溶液混合,得到混合溶液;
37.步骤s2,将新鲜的活体植物置于模拟日光下,在混合溶液中孵育,冻干即得植物界面超组装食药同源材料,具体过程为:
38.将洗净的活体葱正置放入混合溶液中孵育,在高功率阳光模拟器(功率为300w)照射下孵育15h,用去离子水冲洗,冷冻干燥机冻干后即得植物界面超组装食药同源材料。
39.图1是实施例1的葱体内界面超组装safs包裹5-asa的原理图。
40.图2是实施例1的葱体内界面超组装safs包裹5-asa的激光共聚焦图和未包裹5-asa的葱体内界面超组装safs的激光共聚焦图。图2中的a、b和c为孵育3h时葱体内界面超组装safs包裹5-asa的激光共聚焦图;图2中的d、e和f为孵育8h时葱体内界面超组装safs包裹5-asa的激光共聚焦图;图2中的g、h和i为孵育10h时葱体内界面超组装safs包裹5-asa的激
光共聚焦图;
41.图2中的j、k和l为孵育10h时未包裹5-asa的葱体内界面超组装safs的激光共聚焦图。图中白色和黑色线框内的物质为呈蓝光的5-asa。
42.由图1和2可知,本实施例的植物界面超组装食药同源材料体内目标药物5-asa是被框架材料safs所包裹的。
43.将上述制得的植物界面超组装食药同源材料应用于治疗小鼠结肠炎,具体应用过程如下:
44.每3只balb/c(c)x小鼠分为1组,共6组:1.空白组;2.模型组;3.so组;4.safs/so组;5.5-asa组;6.safs/so+5-asa组。除空白组外,其余组每天喂食2%dss溶液诱导肠炎,一周后将2%dss溶液换成水,safs/so+5-asa组小鼠每天灌喂0.3ml的食药同源材料浆料(浓度为5~10g/ml),5-asa组小鼠每天灌喂0.3ml 5-asa药剂(4.4ug/ml)。每天称量体重,观察记录便血等情况,于14天后处死小鼠,取血,采用验证因子试剂盒测得验证因子,并截取结肠,he染色切片分析。
45.图3是实施例1的植物界面超组装食药同源材料治疗小鼠结肠炎时小鼠体重变化图。由图3可知,诱导肠炎的7天内小鼠体重明显下降,随着植物界面超组装食药同源材料和5-asa的给药天数增加,小鼠体重升高,并且safs/so+5-asa组小鼠体重增加比5-asa组小鼠明显。表明本实施例的植物界面超组装食药同源材料对小鼠结肠炎起到了有效的治疗效果,且治疗效果优于5-asa直接给药。
46.图4是实施例1的植物界面超组装食药同源材料治疗小鼠结肠炎后小鼠结肠的光学图像和长度数据图。图4中的a是结肠的光学图像;图4中的b是结肠的长度数据图。由图4可知,本实施例的植物界面超组装食药同源材料治疗小鼠结肠炎后,小鼠的结肠长度与无炎症小鼠的结肠相当。再次表明实施例的植物界面超组装食药同源材料治疗小鼠结肠炎的效果良好,且治疗效果优于5-asa直接给药。
47.图5是实施例1的植物界面超组装食药同源材料治疗小鼠结肠炎后疾病活动指数数据图。图6是实施例1的植物界面超组装食药同源材料治疗小鼠结肠炎后结肠he染色图。图7是实施例1的植物界面超组装食药同源材料治疗小鼠结肠炎后病理切片评分数据图。
48.由图5、6和7可知,safs/so+5-asa组小鼠疾病指数降低,结肠隐窝明显、细胞清晰,染色切片评分降低。该结果同样表明本实施例的植物界面超组装食药同源材料对小鼠结肠炎起到了有效的治疗效果,且治疗效果优于5-asa直接给药。
49.图8是实施例1的植物界面超组装食药同源材料在小鼠消化系统的原理图和在小鼠结肠内降低验证因子的原理图。图8中的a是植物界面超组装食药同源材料在小鼠消化系统的原理图;图8中的b是植物界面超组装食药同源材料在小鼠结肠内降低验证因子的原理图。由图8可知,在植物和safs的双重保护下可使更多的5-asa进入结肠,进入结肠前常用于检测炎症的三项炎症因子(tnf-α,il-6,il-1β)升高,食药同源材料包裹的5-asa进入结肠内释放后三项炎症因子降低。
50.图9是实施例1的植物界面超组装食药同源材料在小鼠结肠内降低验证因子1l-1β、tnf-α和1l-6数据图。由图9可知,safs/so+5-asa组小鼠结肠内验证因子1l-1β、tnf-α和1l-6均显著降低,且降低程度大于5-asa直接给药,表明本实施例的植物界面超组装食药同源材料对小鼠结肠炎起到了有效的治疗效果,且治疗效果优于5-asa直接给药。
51.图10是实施例1的植物界面超组装食药同源材料在小鼠结肠内药物释放时间曲线示意图。由图10可知,相同时间内safs/so+5-asa可携带更多的5-asa进入结肠内,更有效治疗结肠炎。
52.《实施例2》
53.本实施例采用活体绿豆芽(bs)界面超组装得到植物界面超组装食药同源材料,并将其应用于治疗小鼠结肠炎,植物界面超组装食药同源材料的制备包括如下步骤:
54.步骤s1,将二甲基咪唑、乙酸锌和目标药物溶于去离子水中,得到混合溶液,具体过程为:
55.将263mg二甲基咪唑、176mg二水乙酸锌和200μg 5-asa分别加入到20ml去离子水中,搅拌30min,然后分别取2ml二甲基咪唑溶液、2.5ml二水乙酸锌溶液和3ml 5-asa溶液混合,得到混合溶液;
56.步骤s2,将新鲜的活体植物置于模拟日光下,在混合溶液中孵育,冻干即得植物界面超组装食药同源材料,具体过程为:
57.将洗净的活体绿豆芽正置放入混合溶液中孵育,在高功率阳光模拟器(功率为300w)照射下孵育15h,用去离子水冲洗,冷冻干燥机冻干后即得植物界面超组装食药同源材料。
58.将上述制得的植物界面超组装食药同源材料应用于治疗小鼠结肠炎,具体应用过程如下:
59.每3只balb/c(c)x小鼠分为1组,共6组:1.空白组;2.模型组;3.bs组;4.safs/bs组;5.safs/bs+5-asa组;6.5-asa组。除空白组外,其余组每天喂食2%dss溶液诱导肠炎的同时,safs/so+5-asa组小鼠每天灌喂0.3ml的食药同源材料浆料(浓度为5~10g/ml),5-asa组小鼠每天灌喂0.3ml 5-asa药剂(4.4ug/ml)。每天称量体重,观察记录便血等情况,于8天后处死小鼠,截取结肠拍照。
60.图11是实施例2的植物界面超组装食药同源材料治疗小鼠结肠炎时小鼠体重变化图。图12是实施例2的植物界面超组装食药同源材料治疗小鼠结肠炎后小鼠结肠的光学图像图和长度数据图。图12中的a是结肠的光学图像;图12中的b是结肠的长度数据图。
61.由图11和12可知,边诱导肠炎边灌喂材料,safs/bs+5-asa组小鼠体重无明显降低,后期还有所升高;safs/bs+5-asa组小鼠结肠的光学图像和长度数据也显示该组小鼠结肠长度与无炎症小鼠结肠相当。表明本实施例的植物界面超组装食药同源材料对小鼠结肠炎起到了有效的治疗效果,且治疗效果优于5-asa直接给药。
62.以上是对实施例的详细描述,方便本领域的技术人员能正确理解和使用本发明。凡本领域的技术人员依据本发明在现有技术基础上,不经过创新性的劳动,仅通过分析、类推或有限列举等方法得到的改进或修改技术方案,都应该在由权利要求书所确定的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1