一种纳米脂质HPT滴眼液及其制备方法与流程
一种纳米脂质hpt滴眼液及其制备方法
技术领域
1.本发明涉及眼科生物药制剂技术领域,具体为一种纳米脂质hpt滴眼液及其制备方法。
背景技术:
2.随着人类生活节奏的加快,气候干燥、空气污染、人口老龄化等问题日益严重,高科技产品的普及和隐形眼镜的广泛应用,干眼症的发病率在眼科门诊的患病人群中逐年上升,并有逐渐年轻化的趋势,干眼症,也称为干燥性角膜结膜炎,是由多因素和复杂原因引起的泪液质或量或流体动力学异常,导致泪膜稳定性下降,并伴有眼部不适和/或眼表组织病变特征的多种疾病的总称,可导致严重的眼表免疫炎症和其它眼表疾病,包括角膜表面磨损、丝状角膜炎和角膜溃疡等并发症,最终导致角膜混浊和视力丧失。
3.目前临床上多采用人工泪液治疗干眼症,因其含有与正常人的泪液相同的离子、ph值、黏蛋白成分,同时渗透压以及黏度也很接近,可改善眼睛干涩、异物烧灼感、眼胀痛等症状,改善眼表润滑和湿度以及缓解炎症与营养的作用,同时可以增加泪液分泌量以及延长泪液破裂时间,虽然人工泪液可以改善干眼症症状,但并没有任何证据证明其可以解决与干眼症相关的炎症。
4.多核脱氧核糖核苷酸(hpt)是天然的dna分子,其来源主要是人类胎盘或者鳟鱼的生殖细胞,hpt结合水分子后形成3d凝胶并被酶切为核苷酸,自然的存在于ecm中被细胞用于新陈代谢,除了参与细胞生长,hpt还会促进血管内皮生长因子(vegf)和胶原蛋白的产生、多种细胞的迁移以及降低炎症反应,vegf生成的增加和炎症的减少都与促进组织愈合有关。
5.目前已知的hpt发挥作用的主要机制是其与腺苷酸受体,尤其是a2a受体的相互作用,但由于hpt分子量大且带有电荷,导致其不宜通过细胞膜被机体吸收,选择特定的分子量更适应于眼部疾病的治疗,同时可促进角膜和结膜病变的再生皮化(新细胞层的修复过程)。
技术实现要素:
6.本发明的目的在于提供一种纳米脂质hpt滴眼液及其方法,以解决上述背景技术中提出现有由于hpt分子量大且带有电荷,导致其不宜通过细胞膜被机体吸收的问题。
7.为实现上述目的,本发明提供如下技术方案:所述纳米脂质hpt滴眼液由以下重量份的物质组成:一种纳米脂质hpt滴眼液,包含以下重量比的物质:,按100份计,包含以下重量比的物质:hpt1~20份,稳定剂1~20份,抑菌剂 0.001~0.1份,ph调节剂0.01~1,渗透压调节:抗氧剂0~1,注射用水加至 100份。
8.作为本发明的一种优选,其中稳定剂为牛胆酸钠、蛋黄磷脂、胆固醇硫酸钠、胆固醇琥珀酸单酯、peg 2000-dspe、吐温80、泊洛沙姆188、聚乙烯醇(pva)、聚乙烯己内酰胺-聚乙酸乙烯酯-聚乙二醇接枝共聚物(soluplus)中的一种或多种;
9.作为本发明的进一步优选,稳定剂为蛋黄磷脂、胆固醇琥珀酸单酯、peg 2000
ꢀ‑
dspe。
10.作为本发明的一种优选,抑菌剂选自苯扎溴铵、苯扎氯胺、苯甲醇、硫柳汞、苯乙醇、三氯叔丁醇、对羟基苯甲酸甲酯/乙酯中的一种或多种;p h调节剂选自磷酸缓冲盐、枸橼酸盐缓冲液、醋酸盐缓冲液、硼酸盐缓冲液、盐酸、氢氧化钠中的一种或多种;所述的渗透压调节剂选自氯化钠、氯化钾、甘露醇、葡萄糖、木糖醇、磷酸盐、枸橼酸盐、醋酸盐中的一种或多种;所述的抗氧剂选自维生素a、dl-α-生育酚、抗坏血酸、亚硫酸钠、焦亚硫酸钠、硫代硫酸钠、茶多酚中的一种或多种。
11.作为本发明的一种优选,所述的纳米脂质hpt滴眼液,其特征在于所述的纳米脂质hpt滴眼液通过水化-高压均质法制备。
12.作为本发明的进一步优选,具体制备方法如下:
13.步骤一:步骤1:将ph调节剂中缓冲盐、渗透压调节剂分散于适量注射用水中,使其全部溶解,制得水相,保温,备用;
14.步骤二:将hpt、稳定剂、抗氧剂溶解在有机溶剂中后转移至圆底烧瓶中,旋转蒸发除掉有机溶剂,得到油状液体,将所得的油状物质在氮气流下继续干燥1h;将所得的油状物质用步骤一制得的水相在60℃水化,得hpt纳米脂质体粗分散体系,备用;
15.步骤三:将纳米脂质体粗分散体系转移至高压均质机中进行均质;
16.步骤四:将步骤三均质后的脂质体加入防腐剂,根据需要加入ph调节剂,备用;
17.步骤五:将步骤四调过ph值的脂质体制剂用配备100nm聚碳酸酯膜的脂质体挤出器循环挤出,装瓶,氮气灌封,即得纳米脂质hpt滴眼液。
18.上述纳米脂质滴眼液制备方法中,所述有机溶剂选自乙醇、甲醇、乙酸、丙酮、氯仿中一种或者其混合溶液。
19.所述的纳米脂质hpt滴眼液,所述索拉非尼纳米混悬滴眼液中药物粒子粒径为50~500nm;优选50~150nm。
20.所述的纳米脂质hpt滴眼液,其特征在于,渗透压为260~650m osmol/kg,优选260~400m osmol/kg。
21.所述的纳米脂质hpt滴眼液,其特征在于,ph为6.5~7.5。
22.所述的索拉非尼纳米混悬滴眼液,其特征在于:适用于滴眼途径给药,治疗包括但不限于干眼症。
23.与现有技术相比,本发明的有益效果是:
24.该纳米脂质hpt滴眼液及其制备方法,由于hpt包裹于脂质体磷脂膜上,这种“包封”起到了增强稳定性的作用,提高hpt的跨角膜能力,进而达到了提高生物利用度的目的。
具体实施方式
25.下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。
26.本发明提供的一种实施例:一种纳米脂质hpt滴眼液及其制备方法,该脂质体滴眼液具有以下性质:
①
长期储存稳定性好。
②
载药量高,符合临床需求。
③
通过滴入眼角膜表面,能更好释放药物到视网膜靶部位,提高靶组织药物生物利用度;
④
处方工艺简单,成本
低,适用于工业化生产;
⑤
根源上治疗干眼症,与市面上只是用来缓解症状的不同。
27.下面结合具体实施例对本技术做出详细说明,但本发明不局限于这些实施例。实施例中提及hpt分子量是100-500kd范围,其余试剂等均为市售商品。
28.实施例1配方1hpt含量1g:100ml
29.以100ml滴眼液计
30.hpt1g蛋黄卵磷脂pc-98t9g胆固醇琥珀酸单酯3gpeg2000-dspe0.2gdl-α-生育酚0.08g磷酸氢二钠0.25g磷酸二氢钠0.11g氯化钠0.9g苯扎氯铵0.005g氢氧化钠适量加注射用水至100ml
31.纳米脂质hpt滴眼液制备步骤如下:
32.步骤1:将磷酸氢二钠0.25g、磷酸二氢钠0.11g、氯化钠0.9g,分散于100m l注射用水中,使其全部溶解,制得水相,60℃保温,备用;
33.步骤2:将hpt1g、蛋黄卵磷脂pc-98t 9g、胆固醇琥珀酸单酯3g、peg2000
ꢀ‑
dspe 0.2g、dl-α-生育酚0.08g溶解在氯仿中后转移至圆底烧瓶中,旋转蒸发除掉氯仿,得到油状液体。将所得的油状物质在氮气流下继续干燥1h;将所得的油状物质用步骤1制得的水相在60℃水化30min,得hpt脂质体粗分散体系,备用;
34.步骤3:将脂质体粗分散体系转移至高压均质机中进行均质;
35.步骤4:将步骤3均质后的脂质体加入苯扎氯铵0.005g,用0.lmol/l氢氧化钠或盐酸溶液调节ph值至6.5-7.0,备用;
36.步骤5:将步骤4调过ph的脂质体制剂用配备100nm聚碳酸酯膜的脂质体挤出器循环挤出4次,装瓶,氮气灌封,即得纳米脂质hpt滴眼液;其中hpt 含量为1g。
37.其中,脂质体裸眼观察无油滴、无不溶性成分或块状团聚物,显微镜下观察无hpt析出,粒径35.6nm,zeta电位在-22.34mv,ph值为6.78,含量为 99.4%,包封率为97.5%,渗透压在270~300mosm/kg范围内。
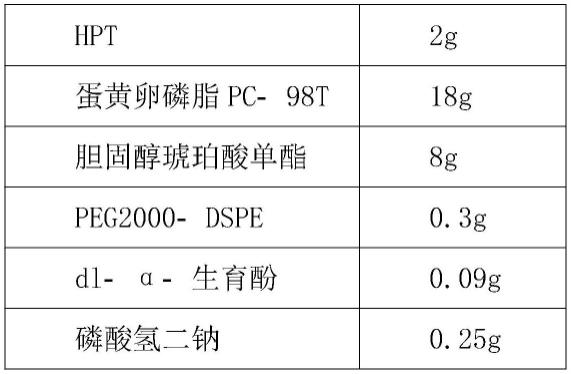
38.实施例2配方1hpt含量2g:100ml
39.以100ml滴眼液计
[0040][0041][0042]
步骤1:将磷酸氢二钠0.25g、磷酸二氢钠0.11g、氯化钠0.9g,分散于100m l注射用水中,使其全部溶解,制得水相,60℃保温,备用;
[0043]
步骤2:将hpt 2g、蛋黄卵磷脂pc-98t 18g、胆固醇琥珀酸单酯8g、peg2000
ꢀ‑
dspe 0.3g、dl-α-生育酚0.09g溶解在氯仿中后转移至圆底烧瓶中,旋转蒸发除掉氯仿,得到油状液体。将所得的油状物质在氮气流下继续干燥1h;将所得的油状物质用步骤1制得的水相在60℃水化30min,得hpt脂质体粗分散体系,备用;
[0044]
步骤3:将脂质体粗分散体系转移至高压均质机中进行均质;
[0045]
步骤4:将步骤3均质后的脂质体加入苯扎氯铵0.005g,用0.lmol/l氢氧化钠或盐酸溶液调节ph值至6.5-7.0,备用;
[0046]
步骤5:将步骤4调过ph的脂质体制剂用配备100nm聚碳酸酯膜的脂质体挤出器循环挤出4次,装瓶,氮气灌封,即得纳米脂质hpt滴眼液;其中hpt 含量为2g。
[0047]
其中,脂质体裸眼观察无油滴、无不溶性成分或块状团聚物,显微镜下观察无hpt析出,粒径为129.0nm,zeta电位在-29.36mv,ph值为6.87,含量为94.4%,包封率为93.7%,渗透压在270~300mosm/kg范围内。
[0048]
实施例3配方1hpt含量1g:100ml
[0049]
以100ml滴眼液计
[0050]
[0051][0052]
步骤1:将磷酸氢二钠0.5g、枸橼酸0.3g、氯化钠0.9g,分散于100ml 注射用水中,使其全部溶解,制得水相,60℃保温,备用;
[0053]
步骤2:将hpt 1g、蛋黄卵磷脂pc-98t 7g、胆固醇硫酸钠8g、peg2000
ꢀ‑
dspe 0.3g、抗坏血酸0.2g溶解在氯仿中后转移至圆底烧瓶中,旋转蒸发除掉氯仿,得到油状液体。将所得的油状物质在氮气流下继续干燥1h;将所得的油状物质用步骤1制得的水相在60℃水化30min,得hpt脂质体粗分散体系,备用;
[0054]
步骤3:将脂质体粗分散体系转移至高压均质机中进行均质;
[0055]
步骤4:将步骤3均质后的脂质体加入苯扎溴铵0.005g,用0.lmol/l氢氧化钠或盐酸溶液调节ph值至6.5-7.0,备用;
[0056]
步骤5:将步骤4调过ph的脂质体制剂用配备100nm聚碳酸酯膜的脂质体挤出器循环挤出4次,装瓶,氮气灌封,即得纳米脂质hpt滴眼液;其中hpt 含量为1g。
[0057]
其中,脂质体裸眼观察无油滴、无不溶性成分或块状团聚物,显微镜下观察无hpt析出,粒径为32.6nm,zeta电位在-25.73mv,ph值为6.88,含量为96.9%,包封率为97.2%,渗透压在270~300mosm/kg范围内。
[0058]
实施例4配方1hpt含量1g:100ml
[0059]
以100ml滴眼液计
[0060][0061]
步骤1:将磷酸氢二钠0.5g、枸橼酸0.3g、氯化钠0.9g,分散于100ml 注射用水中,使其全部溶解,制得水相,60℃保温,备用;
[0062]
步骤2:将hpt 1g、蛋黄卵磷脂lipoid s-10011g、胆固醇琥珀酸单酯5g、 peg2000-dspe 0.5g、抗坏血酸0.5g溶解在氯仿中后转移至圆底烧瓶中,旋转蒸发除掉氯仿,得到油状液体。将所得的油状物质在氮气流下继续干燥1h;将所得的油状物质用步骤1制得的水相在60℃水化30min,得hpt脂质体粗分散体系,备用;
[0063]
步骤3:将脂质体粗分散体系转移至高压均质机中进行均质;
[0064]
步骤4:将步骤3均质后的脂质体加入苯扎氯铵0.005g,用0.lmol/l氢氧化钠或盐酸溶液调节ph值至6.5-7.0,备用;
[0065]
步骤5:将步骤4调过ph的脂质体制剂用配备100nm聚碳酸酯膜的脂质体挤出器循环挤出4次,装瓶,氮气灌封,即得纳米脂质hpt滴眼液;其中hpt 含量为1g。
[0066]
其中,脂质体裸眼观察无油滴、无不溶性成分或块状团聚物,显微镜下观察无hpt析出,粒径为38.5nm,zeta电位在-30.22mv,ph值为6.98,含量为 98.9%,包封率为90.9%,渗透压在270~300mosm/kg范围内。
[0067]
实施例5配方1hpt含量1g:100ml
[0068]
以100ml滴眼液计
[0069][0070]
步骤1:将磷酸氢二钠0.25g、枸橼酸0.3g、氯化钠0.9g,分散于100ml 注射用水中,使其全部溶解,制得水相,60℃保温,备用;
[0071]
步骤2:将hpt 1g、蛋黄卵磷脂lipoid e-8015g、胆固醇琥珀酸单酯8g、 peg2000-dspe 0.8g、抗坏血酸0.9g溶解在氯仿中后转移至圆底烧瓶中,旋转蒸发除掉氯仿,得到油状液体。将所得的油状物质在氮气流下继续干燥1h;将所得的油状物质用步骤1制得的水相在60℃水化30min,得hpt脂质体粗分散体系,备用;
[0072]
步骤3:将脂质体粗分散体系转移至高压均质机中进行均质;
[0073]
步骤4:将步骤3均质后的脂质体加入苯扎氯铵0.01g,用0.lmol/l氢氧化钠或盐酸溶液调节ph值至6.5-7.0,备用;
[0074]
步骤5:将步骤4调过ph的脂质体制剂用配备100nm聚碳酸酯膜的脂质体挤出器循环挤出4次,装瓶,氮气灌封,即得纳米脂质hpt滴眼液;其中hpt 含量为1g。
[0075]
其中,脂质体裸眼观察无油滴、无不溶性成分或块状团聚物,显微镜下观察无hpt析出,粒径为36.6nm,zeta电位在-20.65mv,ph值为6.68,含量为99.6%,包封率为93.5%,渗透压在270~300mosm/kg范围内。
[0076]
实施例6配方1hpt含量1g:100ml
[0077]
以100ml滴眼液计
[0078]
hpt1g蛋黄卵磷脂pc-98t10g胆固醇琥珀酸单酯4g
peg2000-dspe0.5g亚硫酸钠0.5g醋酸0.5g醋酸钠0.9g氯化钠0.9g苯甲醇0.5g氢氧化钠适量加注射用水至100ml
[0079]
步骤1:将醋酸0.5g、醋酸钠0.9g、氯化钠0.9g,分散于100ml注射用水中,使其全部溶解,制得水相,60℃保温,备用;
[0080]
步骤2:将hpt 1g、蛋黄卵磷脂pc-98t 10g、胆固醇琥珀酸单酯4g、peg2000
ꢀ‑
dspe 0.5g、亚硫酸钠0.5g溶解在氯仿中后转移至圆底烧瓶中,旋转蒸发除掉氯仿,得到油状液体。将所得的油状物质在氮气流下继续干燥1h;将所得的油状物质用步骤1制得的水相在60℃水化30min,得hpt脂质体粗分散体系,备用;
[0081]
步骤3:将脂质体粗分散体系转移至高压均质机中进行均质;
[0082]
步骤4:将步骤3均质后的脂质体加入苯甲醇0.5g,用0.lmol/l氢氧化钠或盐酸溶液调节ph值至6.5-7.0,备用;
[0083]
步骤5:将步骤4调过ph的脂质体制剂用配备100nm聚碳酸酯膜的脂质体挤出器循环挤出4次,装瓶,氮气灌封,即得纳米脂质hpt滴眼液;其中hpt 含量为1g。
[0084]
其中,脂质体裸眼观察无油滴、无不溶性成分或块状团聚物,显微镜下观察无hpt析出,粒径为80.2nm,zeta电位在-18.65mv,ph值为6.73,含量为 99.2%,包封率为95.8%,渗透压在270~300mosm/kg范围内。
[0085]
实施例7配方1hpt含量1g:100ml
[0086]
以100ml滴眼液计
[0087]
[0088][0089]
步骤1:将磷酸氢二钠0.5g、磷酸二氢钠0.3g、氯化钾0.9g,分散于100m l注射用水中,使其全部溶解,制得水相,60℃保温,备用;
[0090]
步骤2:将hpt 1g、蛋黄卵磷脂pc-98t 12g、胆固醇琥珀酸单酯6g、peg2000
ꢀ‑
dspe 1g、dl-α-生育酚0.1g溶解在氯仿中后转移至圆底烧瓶中,旋转蒸发除掉氯仿,得到油状液体。将所得的油状物质在氮气流下继续干燥1h;将所得的油状物质用步骤1制得的水相在60℃水化30min,得hpt脂质体粗分散体系,备用;
[0091]
步骤3:将脂质体粗分散体系转移至高压均质机中进行均质;
[0092]
步骤4:将步骤3均质后的脂质体加入苯扎氯铵0.009g,用0.lmol/l氢氧化钠或盐酸溶液调节ph值至6.5-7.0,备用;
[0093]
步骤5:将步骤4调过ph的脂质体制剂用配备100nm聚碳酸酯膜的脂质体挤出器循环挤出4次,装瓶,氮气灌封,即得纳米脂质hpt滴眼液;其中hpt 含量为1g。
[0094]
其中,脂质体裸眼观察无油滴、无不溶性成分或块状团聚物,显微镜下观察无hpt析出,粒径为89.6nm,zeta电位在-25.79mv,ph值为6.88,含量为 99.8%,包封率为97.1%,渗透压在270~300mosm/kg范围内。
[0095]
对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1