一种基于FAPI的MR靶向成像造影剂及其制备方法
一种基于fapi的mr靶向成像造影剂及其制备方法
技术领域
1.本发明涉及造影剂技术领域,具体涉及一种基于fapi的mr靶向成像造影剂及其制备方法。
背景技术:
2.临床实践中,为了获得高质量的磁共振成像图像,磁共振成像需要经常注射造影剂,做增强磁共振成像,提高图像对比度。gd-dtpa等钆离子(gd
3+
)的螯合物是目前临床常用的磁共振成像造影剂,但由于其分子量小,存在弛豫率低、体内清除快、存留时间短等缺点,以致成像的时间窗口很短。
3.为了克服这些问题,现有一种组合性材料,如gd双分子膜质脂体纳米材料,具有比表面积大、生物相容性好、孔隙多、负载效果好等优点,且在纳米材料上包覆配体以及靶向剂,增大其分子量,达到存留时间长、窗口时间长的效果,在生物医学领域已经成为新兴的治疗药物和磁共振成像造影剂的纳米载体。
4.但是,在链接与配合的过程中,若仅采用浸泡的处理方式,很难将材料均匀的包覆在纳米微粒的表面,甚至由于纳米微粒的分散度较低,会导致载体以区块式分布在纳米微粒表面,导致微粒大量聚集在患者的某一个单一的患出,还需要加大造影剂的用量,成像时间减少,造影剂的用量增加。
技术实现要素:
5.本发明的目的在于提供一种基于fapi的mr靶向成像造影剂及其制备方法,以解决现有技术中载体在纳米微粒上分布不均匀,导致成像效果下降的技术问题。
6.为解决上述技术问题,本发明具体提供下述技术方案:
7.一种基于fapi的mr靶向成像造影剂,
8.其中,所述配体以及所述靶向剂固化设置在所述纳米微粒表面;
9.所述靶向剂具体为具有顺磁性效应的mr对比剂与靶向物质fapi的结合体。
10.进一步地,所述纳米微粒为经过造孔处理的gd双分子膜质脂体纳米微粒。
11.进一步地,所述纳米微粒和所述配体上均设置有多个微孔结构,且位于所述纳米微粒上的微孔结构粒径大于位于所述配体上微孔结构的粒径;
12.其中:
13.所述纳米微粒上的微孔结构用于容纳所述配体和所述靶向剂;
14.所述配体上的的微孔结构用于形成吸附体和用于承载药物。
15.进一步地,所述配体与所述gd双分子膜质脂体纳米微粒连接形成的粒子对肿瘤细胞具有强亲和性。
16.进一步地,所述微孔结构均具有多个层次的粗糙表面,且在每个粗糙表面上均形成有多个微孔孔隙,所述微孔孔隙之间通过大小不一的吼道连通在每个层次上形成网状的连通结构;
17.其中:
18.每个层次的粗糙表面之间通过长短不一的顶柱连接,且所述顶柱不与所述粗糙表面连通。
19.另外,本发明还提供了一种基于fapi的mr靶向成像造影剂的制备方法,包括如下步骤:
20.对纳米微粒进行造孔处理形成孔隙,并且按照次序分别通过瞬间凝固的方式在孔隙中形成顶柱,并且造孔之后对整个孔隙进行修饰形成多个层次的粗糙表面;
21.将配体浸泡在药物溶液中,并依次进行撞击震荡以及均质处理使得药物溶液进入配体的微孔结构中并均匀分布,分离多余的药物溶液,以制得初级产物;
22.在按照次序每次对纳米微粒进行瞬间凝固之前均将初级产物送入所述纳米微粒的微孔结构中,之后在每层纳米微粒和初级产物的结合体表面形成新的粗糙表面,直至完成指定层数的粗糙表面,并进行固化;
23.将固化后的结合体与靶向剂混合,充分浸泡,固化处理,以制得基于fapi的mr靶向成像造影剂。
24.进一步地,将固化后的结合体与靶向剂混合的具体步骤为:
25.将具有顺磁性效应的mr对比剂与靶向物质fapi混合,以制得靶向剂溶液;
26.将固化后的结合体与靶向剂溶液混合,依次进行撞击震荡以及均质处理,所述靶向剂进入结合体并在结合体上分布均匀,分离多余的靶向剂溶液,以制得基于fapi的mr靶向成像造影剂。
27.进一步地,撞击震荡的具体包括如下步骤:
28.将配体或结合体记为固相,将药物溶液或靶向剂记为液相;
29.将固相和液相均放置在同一个密闭容器中,并且使得固相和液相不接触;
30.对密闭容器进行抽真空处理使得固相和液相内的气体被抽离,在完成抽真空后将固定置入液相内,使得液相浸泡并进入固相的微孔结构中;
31.在充分浸泡后对悬浮在液相中的固相进行第一离心处理,液相在离心力的作用下进入固相的微孔结构以及吼道中,调整第一离心处理的转速使得转速发生波动,使得离心力发生变化;
32.在转动的过程中对液相进行扰动使得固相在溶液中上下浮动,并在浮动的过程中发生相互碰撞,所述溶液逐渐对所述微孔结构或吼道进行填充,以制得填充粒子。
33.进一步地,所述均质处理均包括如下步骤:
34.向密闭容器内充入气体至常压,并将充填粒子从液相中取出进行静置;
35.静置后进行第二离心处理,第二离心处理的转速大于第一离心处理的转速,多余的液相在离心力的作用下从固相的微孔结构和吼道中甩出;
36.其中:
37.第二离心处理时,对密闭容器反复进行抽真空和充气以调整密闭容器内的压强配合离心处理分离多余的液相。
38.进一步地,在将固化后的结合体与靶向剂混合时重复撞击震荡和均质处理不少于三次。
39.本发明与现有技术相比较具有如下有益效果:
40.1、本发明在脂质体纳米微粒上依次负载配体靶向剂,此靶向剂为将具有顺磁性效应的mr对比剂与靶向物质fapi结合,以达到靶向、富集、高效的肿瘤成像效果;
41.2、本发明通过撞击震荡处理,在包覆时将纳米微粒与溶液进行充分的碰撞与接触,克服“优势通道”的阻力,有效提高微粒的负载量以及单位质量,操作简单,效果好;
42.3、本发明通过均质处理,先后对配体以及靶向剂进行高度离心处理,多余的溶液在离子力的作用下离开微粒表面,使得多层载体均匀覆盖在纳米微粒上,有效防止药物提前释放,提高药品在体内的存留时间,延长成像时间。
附图说明
43.为了更清楚地说明本发明的实施方式或现有技术中的技术方案,下面将对实施方式或现有技术描述中所需要使用的附图作简单地介绍。显而易见地,下面描述中的附图仅仅是示例性的,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图引伸获得其它的实施附图。
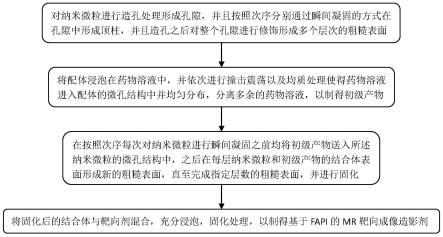
44.图1为本发明提供基于fapi的mr靶向成像造影剂的制备方法的流程示意图;
45.图2为本发明实施例1提供的均质离心机构的结构示意图。
46.图中的标号分别表示如下:
47.1-转盘;2-转动电机;3-支撑臂;4-转动位点;5-均质管;6-伸缩杆;7-油泵;8-转动环;9-磨砂轮;10-挡板。
具体实施方式
48.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
49.本发明提供了一种基于fapi的mr靶向成像造影剂,包括如下组分:
50.纳米微粒、配体以及靶向剂;
51.其中,所述配体以及所述靶向剂固化设置在所述纳米微粒表面;
52.所述靶向剂具体为具有顺磁性效应的mr对比剂与靶向物质fapi的结合体。
53.mri对比剂采用具有顺磁效应的顺磁性mri对比剂;
54.靶向物质fapi为成纤维细胞活化蛋白抑制剂,英文名称为fapi-2。
55.在本实施方式中,所述纳米微粒为经过造孔处理的gd双分子膜质脂体纳米微粒,所述配体与所述gd双分子膜质脂体纳米微粒连接形成的粒子对肿瘤细胞具有强亲和性。同时,为了使得纳米微粒具有更大的承载面,在纳米微粒和所述配体上均设置有多个微孔结构,而配体则直接吸附在纳米微粒的表面,因此,位于所述纳米微粒上的微孔结构粒径大于位于所述配体上微孔结构的粒径。
56.基于前述,对于位于纳米微粒和配体上的微孔结构来说,其分别为:
57.所述纳米微粒上的微孔结构用于容纳所述配体和所述靶向剂;
58.所述配体上的的微孔结构用于形成吸附体和用于承载药物。
59.基于前述,在纳米微粒上依次附着配体以及靶向剂,从而使得纳米粒子先通过包
裹在最外侧的靶向剂向患者的多个患处聚集,当聚集完成后,释放内部的配体与纳米微粒的结合体,此结合体对肿瘤细胞具有强亲和性,得药物在较低的浓度水平去对多个患处进行标记,而且还可以在患处存留较长的时间。
60.且使用具有顺磁性效应的mr对比剂与靶向物质fapi的结合体修饰后的纳米微粒,其具备主动聚集于肿瘤组织的能力,螯合顺磁性颗粒转化作用控制肿瘤局部温度,促进脂质体释放负载的亲和药物,以达到靶向、富集、高效的肿瘤成像效果。
61.在本实施例中,为了实现前述的负载,其主要是通过微孔结构以及多个层次的粗糙表面来实现,其具体的设置方式为:
62.所述微孔结构均具有多个层次的粗糙表面,且在每个粗糙表面上均形成有多个微孔孔隙,所述微孔孔隙之间通过大小不一的吼道连通在每个层次上形成网状的连通结构。
63.在前述中,通过形成多个层次的粗糙表面,即使得该纳米颗粒具有多层相同的结构,由于每层含有的药物量有限,从而使得药物可以维持在较低的浓度水平,而且通过多层的设置方式,从而使得药物可以以较低的浓度维持较长的时间,从而实现对病灶的靶向药物成像。
64.在本实施方式中,为了保证各层之间的层次性,在每个层次的粗糙表面之间通过长短不一的顶柱连接,且所述顶柱不与所述粗糙表面连通。从而使其形成具有稳定可靠不同的层次,使得每次在释放药物时只能释放一个层次上的药物,从而保障整个药物处于长时间的低浓度状态。
65.靶向剂设置在纳米微粒的表层,药物最开始的靶向导向作用,将整个载体以及药物均导向至病灶位置,从而提高药物的靶向移动速度,且完全包裹在亲和粒子的外围,防止大量的粒子直接与肿瘤细胞结合,使得浓度较低的造影剂在长时间内对多处患处进行标记,延长微粒在患者体内的存留时间。当所有患处均被标记完成后,带有靶向剂的微粒排出体外。
66.配体负载在纳米微粒的内层,具有较高的亲和性,随着纳米微粒的移动,药物可以跟随病灶的变化情况进行动态移动,可长期(病理内的长期)停留在病灶位置,为后续治疗提供更准确的靶向位,从而进一步提高药物的导向精准度。
67.如图1所示,本发明提供了一种基于fapi的mr靶向成像造影剂的制备方法,包括如下步骤:
68.对纳米微粒进行造孔处理形成孔隙,并且按照次序分别通过瞬间凝固的方式在孔隙中形成顶柱,并且造孔之后对整个孔隙进行修饰形成多个层次的粗糙表面;
69.将配体浸泡在药物溶液中,并依次进行撞击震荡以及均质处理使得药物溶液进入配体的微孔结构中并均匀分布,分离多余的药物溶液,以制得初级产物;
70.在按照次序每次对纳米微粒进行瞬间凝固之前均将初级产物送入所述纳米微粒的微孔结构中,之后在每层纳米微粒和初级产物的结合体表面形成新的粗糙表面,直至完成指定层数的粗糙表面,并进行固化;
71.将固化后的结合体与靶向剂混合,充分浸泡,固化处理,以制得基于fapi的mr靶向成像造影剂。
72.基于前述靶向剂的结构以及前述的制备过程可知,在本实施方式中,其重点在于两个方面:
73.第一、具有多层结构,从而使得药物在达到病灶位置后能够长时间维持在低浓度的状态;
74.第二、在制备的过程中,能够使得药物进入到微孔结构以及吼道中,并且还能够通过多种方式的处理来使得药物能够均匀分布在微孔或者吼道中。
75.将固化后的结合体与靶向剂混合的具体步骤为:
76.将具有顺磁性效应的mr对比剂与靶向物质fapi混合,以制得靶向剂溶液;
77.将固化后的结合体与靶向剂溶液混合,依次进行撞击震荡以及均质处理,所述靶向剂进入结合体并在结合体上分布均匀,分离多余的靶向剂溶液,以制得基于fapi的mr靶向成像造影剂。
78.如仅通过一般的震荡方式,由于毛细管力的作用导致其无法浸入,仅是能够将配体溶液悬浮在纳米微粒的表面,微粒克服“优势通道”的阻力实现溶液进入微孔结构或吼道中,本发明将离心处理与旋转结合,通过改变离心力的方向来实现纳米微粒在配体溶液中的震荡,增大纳米微粒在配体溶液当中的分散度,提高流体的动能,实现将溶液通入至微孔结构或吼道中。
79.由于在震荡时难以使得配体溶液在纳米微粒的表面分布均匀,因此通过离心作用来进行均匀化,此时纳米微粒在单一的离心力的作用下聚集在一起,从而将多余的溶液从微孔结构或吼道中甩出。
80.为了使用靶向剂将带有配体的纳米微粒完全包裹在内,故使用与s200中相同的撞击震荡以及均质处理,首先将上述以及制备完成的初级产物进行固化,固化完成后将初级产物与混合成的靶向剂溶液混合在一起,撞击震荡以及均质处理后,实现靶向剂对整体颗粒的包覆。
81.撞击震荡的具体包括如下步骤:
82.将配体或结合体记为固相,将药物溶液或靶向剂记为液相;
83.将固相和液相均放置在同一个密闭容器中,并且使得固相和液相不接触;
84.对密闭容器进行抽真空处理使得固相和液相内的气体被抽离,在完成抽真空后将固定置入液相内,使得液相浸泡并进入固相的微孔结构中;
85.在充分浸泡后对悬浮在液相中的固相进行第一离心处理,液相在离心力的作用下进入固相的微孔结构以及吼道中,调整第一离心处理的转速使得转速发生波动,使得离心力发生变化;
86.在转动的过程中对液相进行扰动使得固相在溶液中上下浮动,并在浮动的过程中发生相互碰撞,所述溶液逐渐对所述微孔结构或吼道进行填充,以制得填充粒子。
87.所述均质处理均包括如下步骤:
88.向密闭容器内充入气体至常压,并将充填粒子从液相中取出进行静置;
89.静置后进行第二离心处理,第二离心处理的转速大于第一离心处理的转速,多余的液相在离心力的作用下从固相的微孔结构和吼道中甩出;
90.其中:
91.第二离心处理时,对密闭容器反复进行抽真空和充气以调整密闭容器内的压强配合离心处理分离多余的液相。
92.在将固化后的结合体与靶向剂混合时重复撞击震荡和均质处理不少于三次。
93.在前述中,首先对悬浮在溶液中的产物微粒进行离心处理,产物微粒在离心作用下聚集在溶液下层,溶液中在离心力的作用下对产物微粒进行冲击,使得产物微粒中微孔结构或吼道内的液体或者是空气排出,使得少量溶液进入至产物微粒表面的微孔结构或吼道中。
94.保持离心的状态,将溶液与产物微粒自转,溶液与产物微粒持续自转的过程中,此时产物微粒受到方向不断变化的离心力。
95.产物微粒被扩散至溶液的内部并在受力的过程中在溶液中剧烈震动,在震动的过程中与溶液进行碰撞,更多的溶液克服通道优势进入至微孔结构或吼道中,微粒负载大量的溶液。
96.具体地,停止溶液与填充粒子的自转,进行第二离心处理,多余的溶液在离心力的作用下从所述填充粒子的微孔结构或吼道中甩出,以制得均质粒子。
97.由于填充粒子表面的微孔结构或吼道长短不一,故需要进行进一步的处理,使得溶液在填充粒子的表面分布均匀。在本实施例中,通过高速离心将填充粒子聚集在一起,在离心力的作用下,分布在微孔结构或吼道顶端的溶液在离心力的作用下被首先从微孔结构或吼道中排出,此时停止离心,以得到分布较为均匀的,且为下一步的负载提供通道。
98.另外,在本发明中,通过对密闭容器中的气压进行控制,从而使其在压力变化的过程中可以促进液相在微孔结构和吼道中充分分布,且能够均匀分布。
99.基于前述,以下具体实施方式中提供了一种具体的实施例,从而配合前述的离心作用,从而实现对于溶液与纳米微粒的撞击震荡以及均质处理。
100.如图2所示,在本实施例中,离心机构包括转盘1以及带动所述转盘1转动的转动电机2,所述转盘1上通过若干个支撑臂3转动设置有转动位点4,所述转动位点4套合设置在所述支撑臂3上,且所述转动位点4的底部周侧安装有磨砂轮9,所述转动位点4的上端卡合安装有均质管5。
101.在离心的过程中,混合的药品在均质管的带动下转动,当药品转动时,其中的纳米粒子与药液倾向于分层,但当均质管转动时,分层的药品在均质管内剧烈晃动,提高纳米微粒与溶液之间的接触面积,提高溶液对微孔结构或吼道的填充效果。
102.所述转盘1的中心位置穿过设置有伸缩杆6,所述伸缩杆6的底部穿过所述转盘1设置有油泵7,所述伸缩杆6的上端设置有转动环8,当所述转动环8上升至磨砂轮9位置时,所述转动环8的外壁与所述磨砂轮9贴合。
103.转动电机2通过齿轮与转盘1结合,使得转盘1高速转动,若干个支撑臂3固定安装在转盘1上,转动位点4仅转动安装在支撑臂3的端部,且无上下滑动的动作,当转盘1转动时,转动位点4以转盘1的转动中心为轴转动,即带动均质管5公转。
104.伸缩杆6穿过所述转盘1的中心位置,不影响转盘1的转动,且不跟随转盘1转动,其通过油泵7在转盘1上伸缩,当伸缩杆6将转动环8上升至磨砂轮9的高度时,磨砂轮9的表面与转动环8接触,当转动位点4转动时,磨砂轮9在受到摩擦后转动,实现转动位点4的自转。
105.在本实施例中,所述均质管5倾斜设置在所述转动位点4的端部,且所述均质管5从上至下与所述伸缩杆6的距离渐大,当均质管5转动时,药品在均质管5中受到时刻变化的离心力并剧烈晃动。
106.所述磨砂轮9与所述转动环8均水平设置。
107.优选的,为了防止均质管5被甩出,所述转动位点4上设置有挡板10,所述均质管5设置在所述挡板10与所述转动位点4之间。
108.基于该离心机构,在密闭容器内,撞击震荡与均质处理具体包括如下步骤:
109.(1)将溶液与产物微粒依次倒入至均质管中;
110.(2)将多个均质管依次放入转动位点上,转动环上升,转动环的外环与所述转动位点接触,启动转盘,转盘带动转动位点围绕伸缩杆公转;
111.(3)当转动位点转动时,转动环与转动位点通过磨砂轮接触并转动,多个均质管同时自转,溶液在均质管内晃动,以制得填充粒子;
112.(4)将转动环下降,转盘持续转动直至多余溶液与均质产物分层,以制得均质粒子。
113.通过本实施例的基于fapi的mr靶向成像造影剂及其制备方法,先后负载钆与靶向剂,将具有顺磁性效应的mr对比剂与靶向物质fapi结合,并将其负载在纳米微粒上,以达到靶向、富集、高效的肿瘤成像效果;且通过使用撞击震荡与均质化离心方法,将粒子与溶液进行充分的碰撞与接触,并使用高速离心以到达均质化包裹的目的,方法简单,效果好。
114.以上实施例仅为本技术的示例性实施例,不用于限制本技术,本技术的保护范围由权利要求书限定。本领域技术人员可以在本技术的实质和保护范围内,对本技术做出各种修改或等同替换,这种修改或等同替换也应视为落在本技术的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1