基于细胞载体的组合物和响应性超分子细胞载药体系
1.本发明涉及药物递送技术领域,具体而言,涉及一种基于细胞载体的组合物和响应性超分子细胞载药体系及其制备方法和应用。
背景技术:
2.炎症与人体各种疾病息息相关,其中也包括癌症、神经系统疾病等重大疾病。然而目前传统药物制剂对这些重大疾病的治疗效果均不明显且副作用广泛,可能与到达病变组织前的生理屏障作用以及在正常组织中的药物渗露等因素有关,这些影响因素都会影响药物的最终作用浓度和治疗效果。因此,针对这些与炎症相关的重大疾病,寻找新的递送策略,开发出新一代精准响应疾病微环境的药物制剂是研究和临床上亟待解决的问题。
3.鉴于此,特提出本发明。
技术实现要素:
4.本发明的目的在于提供一种一种基于细胞载体的组合物和响应性超分子细胞载药体系及其制备方法和应用,以改善上述技术问题。
5.本发明是这样实现的:
6.第一方面,本发明提供了一种基于细胞载体的组合物,其包括第一部分和第二部分;第一部分为作为超分子细胞载体的第一细胞,第一细胞的细胞膜上嵌有大环主体分子,第二部分为客体分子修饰的纳米粒子或客体分子修饰的第二细胞。或,第一细胞的细胞膜上嵌有客体分子,第二部分为大环主体分子修饰的纳米粒子或者大环主体分子修饰的第二细胞。大环主体分子与客体分子能够相互识别形成具有响应性断裂特征的主客体复合物。
7.需要说明的是上述组合物中,第一部分和第二部分为独立状态,即第一部分和第二部分未通过大环主体分子和客体分子复合在一起。例如,第一部分和第二部分组成的组合物以试剂盒的方式存在,需要使用时,将第一部分和第二部分混合在一起,使得第一部分和第二部分相应的大环主体分子和客体分子相互识别并结合形成复合物。
8.第二方面,本发明还提供了一种响应性超分子细胞载药体系,其包括上述组合物中的第一部分和第二部分,且第一部分和第二部分通过大环主体分子与客体分子相互识别并形成具有响应性断裂特征的主客体复合物。
9.第三方面,本发明还提供了上述响应性超分子细胞载药体系的制备方法,其包括:将第一部分和第二部分混合孵育,可选地,混合孵育时间为1.5~5min。
10.第四方面,本发明提供了上述基于细胞载体的组合物或上述响应性超分子细胞载药体系在制备用于治疗疾病的产品中的应用,可选地,疾病选自慢性炎症、急性炎症、糖尿病、脓毒症和癌症中的至少一种。
11.本发明具有以下有益效果:上述提供的基于细胞载体的组合物中的第一部分和第二部分可基于超分子主客体作用构建的新一代细胞制剂,进而实现基于细胞功能的靶向递送效果。由于主客体复合物的刺激响应性,将第一部分和第二部分充分混合后即得响应性
超分子细胞载药体系。其制备工艺简单、快速、条件温和、具有普适性和生物正交性,不需要对细胞表面进行共价键修饰,对修饰的细胞生理功能没有影响。并且,主客体分子复合物不同的响应性特征赋予了相应超分子细胞载药体系适应不同疾病微环境的能力,因此可根据疾病的病理特点选择合适类型的主客体复合物。
附图说明
12.为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
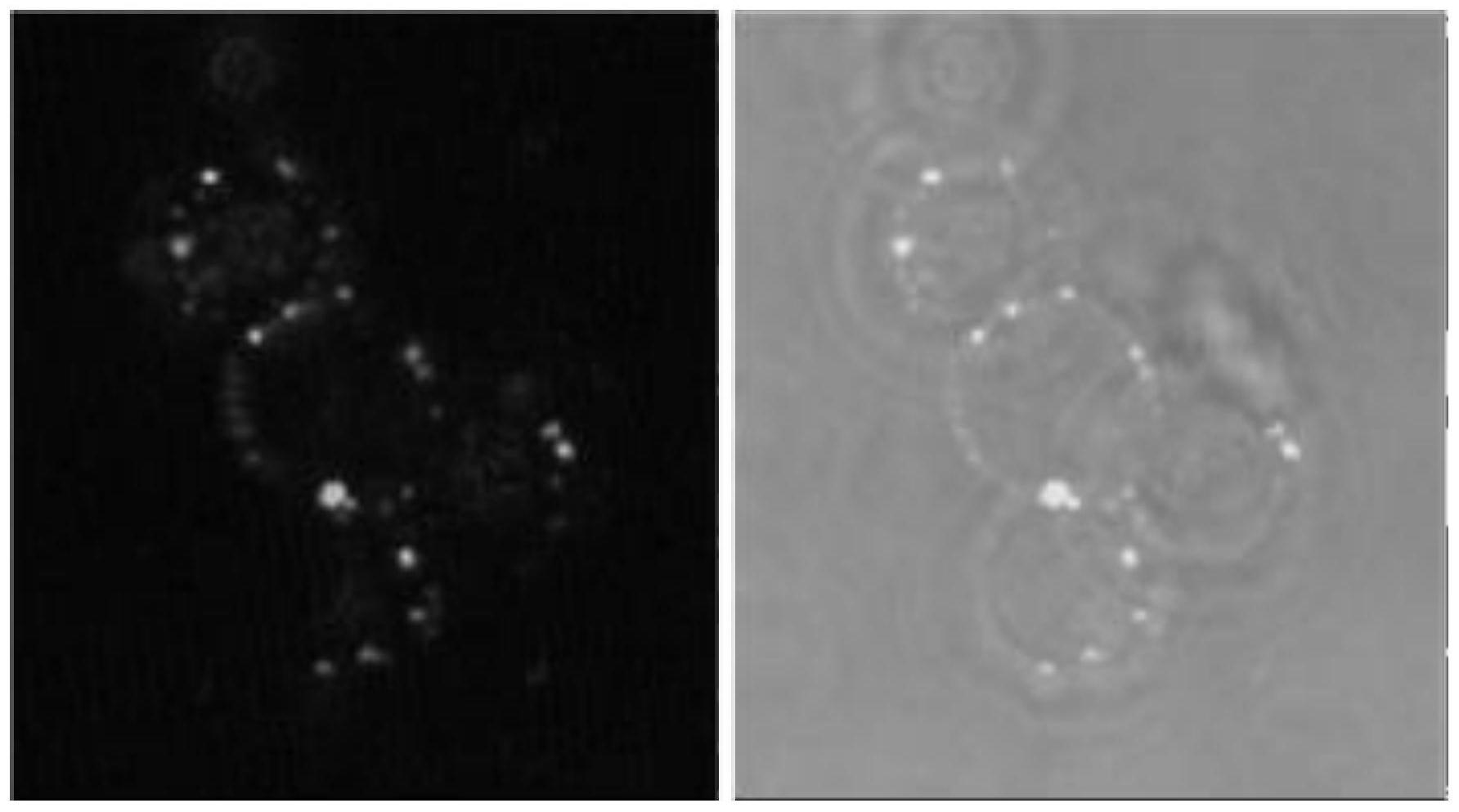
13.图1为本发明实施例1的超分子细胞载体与脂质体结合体的荧光成像图;
14.图2为本发明实施例1的超分子细胞载体与脂质体结合体的扫描电镜图;
15.图3为本发明实施例1的超分子细胞与脂质体结合体在正常环境下以及活性氧刺激下的荧光成像对比图;
16.图4为本发明实施例1的超分子细胞与脂质体结合体在急性肺炎小鼠的肺部定位图。
具体实施方式
17.为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
18.下面对本发明提供的一种基于细胞载体的组合物和响应性超分子细胞载药体系及其制备方法和应用进行具体说明。
19.发明人进行研究发现,现有的药物载体面临以下亟需解决的一些缺陷:通过细胞对药物载体的内吞作用来实现细胞对药物载体的负载,但被吞噬的药物载体可能在胞内环境中发生降解并引起细胞毒性;通过细胞表面与药物载体的共价结合或者特定的配体-受体结合来实现细胞对药物载体的负载,其中共价结合方式涉及到在细胞膜上进行复杂的多步化学反应,可能会影响细胞活性;通过特定配体-受体相互作用的结合方式仅限于表达相关受体的特定细胞,其应用范围局限性较大。基于此,发明人通过大量研究和实践创造性地提出了以下方案。
20.第一方面,本发明的一些实施方式提供了一种基于细胞载体的组合物,其包括第一部分和第二部分;第一部分为作为超分子细胞载体的第一细胞,第一细胞的细胞膜上嵌有大环主体分子,第二部分为客体分子修饰的纳米粒子或客体分子修饰的第二细胞;或,第一细胞的细胞膜上嵌有客体分子,第二部分为大环主体分子修饰的纳米粒子或者大环主体分子修饰的第二细胞;大环主体分子与客体分子能够相互识别形成具有响应性断裂特征的主客体复合物。
21.需要说明的是上述组合物中,第一部分和第二部分为独立状态,即第一部分和第二部分处于相对分离的状态,二者未相应的大环主体分子和客体分子复合在一起。例如,第
一部分和第二部分组成的组合物以试剂盒的方式存在,需要使用时,则将第一部分和第二部分混合在一起,使得第一部分和第二部分相应的大环主体分子和客体分子相互识别并结合形成复合物。
22.上述提供的基于细胞载体的组合物中的第一部分和第二部分可基于超分子主客体作用构建的新一代细胞制剂,进而实现基于细胞功能的靶向递送效果。二者结合在细胞表面不会进入胞内,避免了胞内降解引发毒性。并且通过主客体分子结合,其工艺简单、快速、条件温和、具有普适性和生物正交性,不需要对细胞表面进行共价键修饰,对修饰的细胞生理功能没有影响,同时,主客体分子复合物不同的响应性特征赋予了相应不同组合物形成的超分子细胞载药体系适应不同疾病微环境的能力,因此可根据疾病的病理特点选择合适类型的主客体复合物。例如,不同主客体分子复合物具有不同的刺激响应性,如氧化还原响应的环糊精/二茂铁复合物,光照响应的环糊精/偶氮苯复合物,ph响应的环糊精/苯并咪唑复合物,精胺响应的葫芦脲/奥沙利铂复合物。
23.具体地,一些实施方式中,大环主体分子或客体分子通过嵌膜材料嵌于第一细胞的细胞膜上,大环主体分子或客体分子位于第一细胞的外表面层,大环主体分子或客体分子与嵌膜材料偶联,利用嵌膜材料的疏水作用嵌入第一细胞的细胞膜与磷脂层自组装结合。以上结合方式避免了繁琐复杂的合成以及基因修饰的步骤,在能够有效维持受体细胞自身功能的情况下,简化了制备流程。
24.承上述,第二部分为客体分子或大环主体分子修饰的第二细胞时,客体分子或大环主体分子通过嵌膜材料嵌于第二细胞的细胞膜上。即通过同样地方式来实现客体分子或大环主体分子和细胞的结合。第二部分为客体分子或大环主体分子修饰的纳米粒子时,纳米粒子为客体分子或大环主体分子与嵌膜材料的偶联物,纳米粒子通过嵌膜材料嵌于第一细胞的细胞膜上,即当第一部分和第二部分结合时,除了主客体分子可以复合外,纳米粒子本身的嵌膜材料也可以和第一细胞的细胞膜结合,使得二者结构更为稳定。
25.需要说明的是,第一部分采用大环主体分子时,第二部分采用客体分子,第二部分采用客体分子时,第二部分采用大环主体分子,二者是相互对应的关系。
26.具体地,一些实施方式中,上述嵌膜材料包括但不限于dmpe-peg、dppe-peg、dspe-peg和chol-peg中的至少一种,peg-dmpe即peg-二肉豆蔻酰基磷脂酰乙醇胺,peg-dppe即peg-二棕榈酰基磷脂酰乙醇胺,peg-dspe即peg-二硬脂酰基磷脂酰乙醇胺,peg-chol即peg-胆固醇。
27.进一步地,一些实施方式中,大环主体分子包括但不限于环糊精(cd)、葫芦脲(cb)、杯芳烃、柱芳烃和冠醚中的至少一种,即大环主体分子可选择为环糊精、葫芦脲、杯芳烃、柱芳烃或冠醚,或者以上物质的两种或更多种的组合,组合比例不限。一些较佳地实施方式中,大环主体分子为环糊精。
28.一些实施方式中,客体分子包括但不限于二茂铁以及二茂铁的衍生物中的至少一种,或苯并咪唑以及苯并咪唑衍生物中的至少一种,或偶氮苯以及偶氮苯衍生物的至少一种,一些较佳地实施方式中,客体分子为二茂铁。
29.以上大环主体分子与客体分子能够相互识别形成主客体复合物且该主客体复合物具有响应相关刺激并断裂的特征。相关刺激为高活性氧水平,低p h水平,外界光照的至少一种。一些较佳地实施方式中,相关刺激为高活性氧水平。
30.一些实施方式中,大环主体分子和客体分子的摩尔比为1~10:1~10,具体可以为1:10、2:10;3:10、4:10、5:10、6:10、7:10、8:10、9:10、1:1、10:1、10:2、10:3、10:4、10:5、10:6、10:7、10:8、10:9中的任意一项或任意两项之间的范围。在该限定范围下,能够简单实现超分子人工受体细胞的制备。
31.一些较佳地实施方式中,大环主体分子和客体分子的摩尔比为1:1。
32.进一步地,一些实施方式中,第一细胞选自免疫细胞、祖细胞、干细胞、红细胞、血小板和脂肪细胞中的任意一种。
33.当第二部分为大环主体分子或客体分子修饰的第二细胞时,第二细胞为表面能够被peg-二硬脂酰基磷脂酰乙醇胺的细胞,示例性地,第二细胞选自肝细胞、干细胞、淋巴细胞、树突细胞、血小板和脂肪细胞和红细胞中的任意一种。
34.当第二部分为大环主体分子或客体分子修饰的纳米粒子时,该纳米粒子包括但不限于脂质体、胶束、纳米凝胶、无机纳米粒和纳米囊中的至少一种。
35.第二方面,本发明的一些实施方式还提供了一种响应性超分子细胞载药体系,其包括上述组合物中的第一部分和第二部分,且第一部分和第二部分通过大环主体分子与客体分子相互识别并形成具有响应性断裂特征的主客体复合物。即该响应性超分子细胞载药体系为上述组合物中的两个组分的结合状态。该主客体复合物在特定的体内微环境下响应相关刺激并断裂,从而可实现药物特异性释放以及在靶标部位积累,提高递药效率,减少药物渗漏对正常组织的副作用。
36.第三方面,本发明的一些实施方式还提供了上述响应性超分子细胞载药体系的制备方法,其包括:将上述第一部分和第二部分混合孵育,可选地,混合孵育时间为1.5~5min,示例性地,可选择混合2min。
37.该响应性超分子细胞载药体系的制备方法具有制备工艺简单、特异性和普适性的优势,为实现靶向递药和可控释放提供了新思路。
38.具体地,上述第一部分主要由以下步骤制备得到:先将大环主体分子或者客体分子偶联嵌膜材料,再将偶联后的嵌膜材料嵌入第一细胞的细胞膜中。可选地,偶联嵌膜材料的步骤为:将大环主体分子或客体分子与嵌膜材料于30~42℃下共孵育60~120min,一些实施方式中,偶联时,大环主体分子或客体分子的作用浓度为1μm~1mm,优选为10μm。
39.大环主体分子或客体分子和第一细胞的结合过程为:将偶联后的嵌膜材料与第一细胞在30-42℃共孵育60-120min;例如,孵育温度为37℃,孵育时间为90min。较佳地一些实施实施方式中,偶联有嵌膜材料的大环主体分子或者客体分子的浓度为1μm-1mm。
40.承上述,第二部分主要通过以下步骤得到:当第二部分为大环主体分子或客体分子修饰的第二细胞时,先将大环主体分子或者客体分子偶联嵌膜材料,再将偶联后的嵌膜材料嵌入第二细胞的细胞膜中;其中,偶联嵌膜材料的步骤为:将大环主体分子或客体分子与嵌膜材料于30~42℃下共孵育60~120min。一些较佳地实施方式中,偶联时,大环主体分子或客体分子的作用浓度为1μm~1mm,优选为10μm。
41.进一步地,大环主体分子或客体分子和第二细胞的结合过程为:将偶联后的嵌膜材料与第二细胞在30-42℃共孵育60-120分钟;优选地,偶联有嵌膜材料的大环主体分子或者客体分子的浓度为1μm-1mm。
42.当第二部分为大环主体分子或客体分子修饰的纳米粒子时,将大环主体分子或者
客体分子与纳米粒子偶联;一些较佳的实施方式中,将分子与嵌膜材料偶联,制备得到脂质体。
43.第四方面,本发明的一些实施方式还提供了上述基于细胞载体的组合物或上述响应性超分子细胞载药体系在制备用于治疗疾病的产品中的应用。一些实施方式中,疾病选自慢性炎症、急性炎症、糖尿病、脓毒症和癌症中的至少一种。
44.以下结合实施例对本发明的特征和性能作进一步的详细描述。
45.实施例1
46.本实施例提供了一种响应性超分子细胞载药体系及其制备方法,本实施例中,细胞载体选取红细胞,dspe-peg-β-cd购自西安瑞禧生物科技有限公司,dmem培养基购自赛默飞世尔科技(中国)有限公司,n,n-二甲基二茂铁甲胺和溴代十四烷购自上海阿拉丁生化科技股份有限公司。dii和dio均购自上海碧云天生物技术有限公司。
47.具体步骤为:
48.将n,n-二甲基二茂铁甲胺和溴代十四烷反应生成n,n-二甲基二茂铁甲基十四烷,与胆固醇,卵磷脂通过薄膜水化法制备出二茂铁修饰的脂质体。
49.将红细胞在含有10μm的dspe-peg-β-cd的空白dmem培养基中于37℃孵育2小时。
50.孵育后,洗去多余的dspe-peg-β-cd,再加入10μm的二茂铁修饰的负载dio的脂质体继续孵育2分钟。
51.洗去未结合的脂质体后,制得响应性超分子细胞载药体系即超分子细胞-脂质体结合体。
52.实施例2
53.本实施例提供了一种响应性超分子细胞载药体系及其制备方法,本实施例中,dspe-peg-β-cd和dmem培养基与实施例1购买来源相同。dspe-peg-ben(苯并咪唑)为实验室自制。本实施例中,细胞载体选取巨噬细胞,将巨噬细胞在含有50μm的dspe-peg-β-cd的空白dmem培养基中于37℃孵育1小时。
54.洗去多余的dspe-peg-β-cd后,加入50μm的dspe-peg-ben修饰的负载dox的脂质体继续孵育2分钟。最后洗去未结合的脂质体后,获得超分子细胞载药体系即超分子细胞-脂质体结合体。β-cd-ben复合物在较低ph下可以断裂,该超分子人工细胞载药体系可以响应肿瘤微环境低ph特性,实现药物在肿瘤部位的精准释放。
55.实施例3
56.本实施例提供了一种超分子细胞载药体系及其制备方法,dmpe-peg-β-cd和dmpe-peg-ben为实验室自制。本实施例中,将血小板在含有100μm的dmpe-peg-β-cd的空白dmem培养基中于37℃孵育2小时。
57.然后洗去多余的dmpe-peg-β-cd,加入100μm的dmpe-peg-ben修饰的负载脂质体继续孵育1分钟,洗去未结合的脂质体后,获得低ph响应的超分子细胞载药体系即超分子细胞-脂质体结合体。
58.实施例4
59.本实施例提供了一种超分子细胞载药体系及其制备方法,dppe-peg-β-cd和dppe-peg-ben为实验室自制。本实施例中,将造血干细胞在含有40μm的dppe-peg-β-cd的空白dmem培养基中于37℃孵育1.5小时。
60.然后洗去多余的dppe-peg-β-cd,加入80μm的dppe-peg-ben修饰的脂质体继续孵育5分钟,洗去未结合的脂质体后。获得低p h响应的超分子细胞载药体系即超分子细胞-脂质体结合体。
61.实施例5
62.本实施例提供了一种超分子细胞载药体系及其制备方法。dppe-peg-β-cd和dppe-peg-azo(偶氮苯)为实验室自制。本实施例中,将血小板在含有10μm的dspe-peg-β-cd的空白dmem培养基中于37℃孵育2小时,在洗去多余的dspe-peg-β-cd后加入10μm的dspe-peg-azo修饰的脂质体继续孵育2分钟,洗去未结合的脂质体,制得激光响应的超分子细胞载药体系即超分子细胞-脂质体结合体,β-cd-azo复合物在激光刺激下可以断裂。
63.实施例6
64.本实施例提供了一种超分子细胞载药体系及其制备方法,dmpe-peg-cb和dmpe-peg-ox(奥沙利铂)为实验室自制。本实施例中,将血小板在含有100μm的dmpe-peg-cb的空白dmem培养基中于37℃孵育2小时。
65.然后洗去多余的dmpe-peg-cb,加入100μm的dmpe-peg-ox修饰的负载脂质体继续孵育1分钟,洗去未结合的脂质体后,获得精胺响应的超分子细胞载药体系即超分子细胞-脂质体结合体。
66.实施例8
67.本实施例提供了一种超分子细胞载药体系及其制备方法,dmpe-peg-β-cd为实验室自制。本实施例中,将中性粒细胞在含有60μm的dmpe-peg-β-cd的空白dmem培养基中于37℃孵育2小时。孵育后,洗去多余的dmpe-peg-β-cd,然后加入30μm的dspe-peg-fc(fc为二茂铁)修饰的红细胞继续孵育2分钟,洗去未结合的细胞后,获得活性氧响应的超分子细胞载药体系即细胞-细胞结合体。
68.实施例9
69.本实施例提供了一种超分子细胞载药体系及其制备方法,dmpe-peg-fc(fc为二茂铁)与dmpe-peg-β-cd为实验室自制。本实施例中,将中性粒细胞在含有60μm的dmpe-peg-fc的空白dmem培养基中于37℃孵育2小时。孵育后,洗去多余的dmpe-peg-fc,然后加入30μm的dspe-peg-β-cd修饰的脂质体继续孵育2分钟,洗去未结合的脂质体后,获得活性氧响应的细胞-脂质体结合体。
70.试验例
71.一、将实施例1制得的超分子细胞-脂质体结合体进行荧光成像和扫描电镜成像。超分子细胞与脂质体结合体的荧光成像图参照图1所示,超分子细胞与脂质体结合体的扫描电镜图参照图2所示。
72.二、验证所述超分子细胞载药体系的活性氧响应性。
73.将实施例1制得的超分子细胞-脂质体结合体分别在正常条件下以及过氧化氢处理条件下孵育,通过荧光成像观察超分子人工细胞载体与纳米粒子之间的连接情况。对比正常条件下处理的体系,超分子人工细胞载药体系响应过氧化氢并释放纳米粒子,其荧光成像对比图参照图3所示。
74.三、验证所述超分子细胞载药体系的在肺炎中的响应性。
75.实施例1的超分子细胞-脂质体结合体在炎症性肺组织中的定位图参照图4所示,
该体系能够响应炎症微环境中的活性氧,释放负载的纳米粒子并增加药物的肺部累积。细胞载体用dii标记(左边的一个箭头指示),纳米粒子用dio标记(右边的四个箭头指示)。
76.综上所述,本发明实施例的响应性超分子细胞载药体系是通过响应性主客体作用相互连接形成的,是基于超分子主客体作用构建的新一代细胞制剂,可实现基于细胞功能的靶向递送效果;该超分子细胞载体的制备方法是将大环主体分子或者客体分子偶联嵌膜材料并嵌入第一细胞的细胞膜中;将相应的客体分子或者大环主体分子修饰在纳米粒子表面或者第二细胞的细胞膜上;由于主客体复合物的刺激响应性,充分混合后即得响应性超分子细胞载药体系。制备工艺简单、快速、条件温和、具有普适性和生物正交性,不需要对细胞表面进行共价键修饰,对修饰的细胞生理功能没有影响。
77.以上仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1