一种胎盘粉及其制备方法与流程
1.本发明属于生物医药技术领域,尤其涉及一种胎盘粉及其制备方法。
背景技术:
2.胎盘作为维持胎儿在母体内生长发育的临时性器官,因其特殊的屏障功能与内分泌功能,自古以来就为人们所重视。中医将经过简单的加工炮制后的人胎盘称为“紫河车”,《本草纲目》称其具有“安神养血、补气、益精、解毒、补血”的作用,对“疲劳、消瘦、衰弱者”有奇效,“久服者,耳聪目明,须发黑,延年益寿,有夺造化之功”。此后的中医古籍中均将其作为入药上品,并沿用至今。
3.目前制作紫河车、胎盘片或者胎盘胶囊的常用方法是收集新鲜胎盘,漂洗、剔除筋膜、挑破血管、挤出血液、反复漂洗数次至洁净为止,然后放入锅中煮至胎盘浮起,再置煤火上烘至起泡,待质酥松后磨成粉,此法由于经过多次漂洗、高温煮沸、高温烘焙的操作,容易在制作过程中大量流失胎盘内有效的活性成分,及各类有益激素、免疫球蛋白、微量元素等,使其药用效果大打折扣。
4.右旋糖酐(dextran)是一种链式葡聚糖,由葡萄糖单元以α-1,6-糖苷键连接而成,同时含有少量α-1,3-糖苷键组成的支链结构。右旋糖酐及其衍生物因具有安全、无毒等多种优点已被广泛应用于医药、工业、食品等多个领域,市场需求十分巨大(全球每年的需求近几百亿美金)。不同分子量的右旋糖酐具有不同的药用价值与生物学功能,重均分子量为20-70kda的中分子右旋糖酐是临床上使用较多的药用级右旋糖酐,主要用作血浆代用品,治疗出血性休克、创伤性休克及烧伤性休克等;重均分子量为6-8kda的低分子右旋糖酐是制备右旋糖酐铁的优良材料;重均分子量为3-5kda的小分子右旋糖酐可进行硫酸化,得到的衍生化产品在医疗中可以用于抗血栓。
5.现有技术公开了改进胎盘粉制备方法,将胎盘洗净血液后,放入一半量75%乙醇中浸泡片刻取出,装入干净无毒的塑料袋中密封,于冰箱冷冻室(-10
±
1℃)冻透(约12h),取出切薄片(约1~2mm厚薄),将此薄片置于预先铺有甘草细粉或炒山药细粉的干燥盘中,放入烘箱50℃烘干,粉碎、装入玻璃瓶或硬胶囊中,密封备用。此过程虽然降低了制备过程中的温度,但是制备过程中温度也达到了50℃,对活性物质也会造成部分损失。而且制备过程中加入乙醇,会导致蛋白质变性,活性物质失活。现有专利公开了一种胎盘胶囊制备步骤为:(1)取经过检验检疫的胎盘,24h内进行漂洗,剔除筋膜,挑破血管,挤出血液,反复漂洗数次至洁净为止;(2)剪碎胎盘组织,剪成每小块小于1cm3;(3)将步骤(2)中所得的胎盘组织放置于80目滤网上,直至滤网底部无明显液体渗出;(4)将步骤(3)所得胎盘平摊在烘箱托盘上,烘箱温度设置为40~80℃放入烘箱烘3~5h;(5)将步骤(4)得到的干燥物放入组织捣碎机,转速设置为5000~20000r/min,时间设置为1~10min,将其捣碎至粉末状;(6)过80目筛网,未通过的胎盘碎末继续搅拌,直至过筛;(7)将胎盘粉末灌装入空淀粉胶囊中。上述制备过程繁琐,有益成分流失。制备过程中温度达到40~80℃,该高温条件下破坏了胎盘中的活性成分。现有专利还公开了一种人胎盘冻干粉制剂的制备方法:取胎盘,清洗除去筋膜
与血管,置于质量浓度为10%的nacl溶液中,浸泡5h,将胎盘切碎,进行低温组织匀浆处理,得胎盘浆;与纯水混匀,低渗法获取组织和细胞内活性因子,搅拌提取,得组织液;添加0.8~2%的酵母粉发酵,去除产品中的腥味;用30~70μm的滤膜过滤,得胎盘提取液;冷冻干燥,得胎盘冻干粉;用胶囊囊壳(hpmcas或cap)包装,即得人胎盘冻干粉制剂。该方法采用先经低渗匀浆处理,然后酵母发酵去腥,再冷冻干燥,获得胎盘活性物质冻干粉,并形成胶囊制品,虽然制备过程中采用了低温制备,并形成了胶囊制品,避免了活性物质被高温破环和胃部强酸环境对活性物质的损坏,但是在制备过程中采用纯水的方法溶解活性物质,导致胎盘中脂溶性等活性物质的丢失,营养物质不能保全。
技术实现要素:
6.本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明第一个方面提出一种胎盘粉,能够最大化保全胎盘粉中的活性物质,保证其有效性和安全性。
7.本发明的第二个方面提出了一种胎盘粉的制备方法。
8.本发明的第三个方面提出了一种胎盘粉的应用。
9.根据本发明的第一个方面,提出了一种胎盘粉,所述胎盘粉中含有胎盘的冻干粉,且所述胎盘粉中还添加有葡糖氧化酶和右旋糖酐40,所述葡糖氧化酶和右旋糖酐40的质量之和占胎盘粉总质量的0.01%~0.03%。
10.在本发明的一些优选的实施方式中,所述葡糖氧化酶和右旋糖酐40的质量之和占胎盘粉总质量的0.015%~0.025%。
11.在本发明的一些更优选的实施方式中,所述葡糖氧化酶和右旋糖酐40的质量之和占胎盘粉总质量的0.018%~0.02%。
12.在本发明的一些更优选的实施方式中,所述葡糖氧化酶和右旋糖酐40的质量比为1:1。
13.根据本发明的第二个方面,提出了一种第一方面所述的胎盘粉的制备方法,包括如下步骤:
14.取新鲜胎盘清洗,剪碎,冷冻干燥,磨粉,得到胎盘粉,按第一方面所述的比例加葡糖氧化酶和右旋糖酐40,搅拌,辐照灭菌,制得所述胎盘粉。
15.在本发明的一些实施方式中,所述清洗具体为:用生理盐水快速清洗,去除胎盘污渍,保留血液和胎盘组织。
16.在本发明的一些实施方式中,所述剪碎具体为:将清洗后的胎盘剪成≤0.5cm3的小块。
17.在本发明的一些实施方式中,所述冷冻干燥之前包括预冷冻,所述预冷冻的温度为-40℃~-70℃。
18.在本发明的一些优选的实施方式中,所述冷冻干燥的温度为-40℃~-70℃,压力为1pa~20pa。
19.在本发明的一些优选的实施方式中,所述冷冻干燥的时间为24h~48h。
20.在本发明的一些优选的实施方式中,所述磨粉具体为:使用磨粉机对冷冻干燥后的胎盘进行研磨,转速为1800r/min~3000r/min,时间为1min~5min。
21.在本发明的一些优选的实施方式中,所述葡糖氧化酶和右旋糖酐40混合物的加入
量为胎盘粉质量的0.01%~0.02%。
22.在本发明的一些更优选的实施方式中,所述辐照灭菌的辐照剂量为8kgy~10kgy,时间为10min~20min,所述辐照灭菌的温度为4℃~20℃。
23.根据本发明的第三个方面,提出了第一方面所述的胎盘粉在制备食品、药品中的应用。
24.本发明的有益效果为:
25.本发明通过优化胎盘粉的制备方法,从而让胎盘粉的活性物质得到最大化的保全,同时使胎盘粉的有效性和安全性达到一个均衡。本发明在胎盘粉的制备过程中添加了右旋糖酐40,该成分可以起到抗氧化的作用,同时添加了葡糖氧化酶,葡糖氧化酶也有抗氧化的功效,葡糖氧化酶和右旋糖苷联合应用,起到的效果要优于两者单独效果的总和,并且优于两种成分分别和其他抗氧化功效物质联用的效果,具有良好的协同作用。本发明的胎盘粉很好的保存了其中多种有效成分的活性,具有较长的保质期,2~8℃保存21天生物活性物质含量仍然维持较高水平。
具体实施方式
26.以下将结合实施例对本发明的构思及产生的技术效果进行清楚、完整地描述,以充分地理解本发明的目的、特征和效果。显然,所描述的实施例只是本发明的一部分实施例,而不是全部实施例,基于本发明的实施例,本领域的技术人员在不付出创造性劳动的前提下所获得的其他实施例,均属于本发明保护的范围。
27.实施例1
28.本实施例制备了一种胎盘粉,具体过程为:
29.胎盘采集盒中装入200ml含有体积分数为5%体积分数的双抗(青霉素、链霉素)的生理盐水,另加入200μl肝素钠,充分混匀,将采集到的胎盘经过简单处理后第一时间内装入到胎盘采集盒内,注意胎儿面(即连接脐带的一面)朝下放置,运输温度保持在4℃~25℃。
30.用生理盐水快速清洗胎盘,去除胎盘污渍,保留血液和胎盘组织。将清洗后的胎盘用剪刀剪成0.5cm3的小块,放入到消毒干净的冷冻干燥机托盘中,用保鲜膜将铁盘密封住,放入-40℃冰箱中冷冻预冷,所检测母血细菌病毒要求均为阴性。
31.打开冷冻干燥机电源,等待三分钟,按桌面上的制冷键,冻干机开始制冷,当显示屏显示温度下降到-40℃时,放入预冷的胎盘,盖上玻璃罩,注意玻璃罩要盖正,以确保冷冻干燥机的密封性良好,按真空键。冷冻干燥机开始进入降温和抽真空的过程,当温度降低到-47℃左右,内部气压保持在1pa,此时证明冷冻干燥机运转正常,维持48h后冻干过程完成。打开放气阀,放气结束后关闭真空键,打开玻璃罩,拿出冻干的胎盘。
32.取出冻干的胎盘倒入到磨粉机中,固定好磨粉机上盖,接通电源,1800r/min磨粉1min后,收集粉末,同时按照0.2mg/g比例添加右旋糖酐40(南京网化化工科技有限公司,货号:9004-54-0)和葡糖氧化酶的混合物(货号:g130084-0.1mu,品牌:阿拉丁),右旋糖酐40和葡糖氧化酶的质量比为1:1。
33.将胎盘粉灌入胶囊中,并在4℃低温条件下辐照灭菌处理,辐照剂量9kgy,辐照时间10min,制备成安全性符合食品、药品安全性标准要求的胎盘粉。
34.实施例2
35.本实施例制备了一种胎盘粉,具体过程为:
36.胎盘采集盒中装入200ml含有5%双抗(青霉素、链霉素)的生理盐水,另加入200μl肝素钠,充分混匀,将采集到的胎盘经过简单处理后第一时间内装入到胎盘采集盒内,注意胎儿面(即连接脐带的一面)朝下放置,运输温度保持在4℃~25℃。
37.用生理盐水快速清洗胎盘,去除胎盘污渍,保留血液和胎盘组织。将清洗后的胎盘用剪刀剪成0.5cm3的小块,放入到消毒干净的冷冻干燥机托盘中,用保鲜膜将铁盘密封住,放入-70℃冰箱中冷冻预冷,所检测母血细菌病毒要求均为阴性。
38.打开冷冻干燥机电源,等待三分钟,按桌面上的制冷键,冻干机开始制冷,当显示屏显示温度下降到-70℃时,放入预冷的胎盘,盖上玻璃罩,注意玻璃罩要盖正,以确保冷冻干燥机的密封性良好,按真空键。冷冻干燥机开始进入降温和抽真空的过程,当温度降低到-75℃左右,内部气压保持在1pa,此时证明冷冻干燥机运转正常,维持30h后冻干过程完成。打开放气阀,放气结束后关闭真空键,打开玻璃罩,拿出冻干的胎盘。
39.取出冻干的胎盘倒入到磨粉机中,固定好磨粉机上盖,接通电源,2500r/min磨粉1min后,收集粉末,同时按照0.25mg/g比例添加右旋糖酐40(南京网化化工科技有限公司,货号:9004-54-0)和葡糖氧化酶的混合物(货号:g130084-0.1mu,品牌:阿拉丁),右旋糖酐40和葡糖氧化酶的质量比为1:1。
40.将胎盘粉灌入胶囊中,并在10℃低温条件下辐照灭菌处理,辐照剂量9kgy,辐照时间12min,制备成安全性符合食品、药品安全性标准要求的胎盘粉。
41.实施例3
42.本实施例制备了一种胎盘粉,具体过程为:
43.胎盘采集盒中装入200ml含有5%双抗(青霉素、链霉素)的生理盐水,另加入200μl肝素钠,充分混匀,将采集到的胎盘经过简单处理后第一时间内装入到胎盘采集盒内,注意胎儿面(即连接脐带的一面)朝下放置,运输温度保持在4℃~25℃。
44.用生理盐水快速清洗胎盘,去除胎盘污渍,保留血液和胎盘组织。将清洗后的胎盘用剪刀剪成0.5cm3的小块,放入到消毒干净的冷冻干燥机托盘中,用保鲜膜将铁盘密封住,放入-60℃冰箱中冷冻预冷,所检测母血细菌病毒要求均为阴性。
45.打开冷冻干燥机电源,等待三分钟,按桌面上的制冷键,冻干机开始制冷,当显示屏显示温度下降到-60℃时,放入预冷的胎盘,盖上玻璃罩,注意玻璃罩要盖正,以确保冷冻干燥机的密封性良好,按真空键。冷冻干燥机开始进入降温和抽真空的过程,当温度降低到-65℃左右,内部气压保持在1pa,此时证明冷冻干燥机运转正常,维持40h后冻干过程完成。打开放气阀,放气结束后关闭真空键,打开玻璃罩,拿出冻干的胎盘。
46.取出冻干的胎盘倒入到磨粉机中,固定好磨粉机上盖,接通电源,2500r/min磨粉1min后,收集粉末,同时按照0.15mg/g比例添加右旋糖酐40(南京网化化工科技有限公司,货号:9004-54-0)和葡糖氧化酶的混合物(货号:g130084-0.1mu,品牌:阿拉丁),右旋糖酐40和葡糖氧化酶的质量比为1:1。
47.将胎盘粉灌入胶囊中,并在15℃低温条件下辐照灭菌处理,辐照剂量10kgy,辐照时间15min,制备成安全性符合食品、药品安全性标准要求的胎盘粉。
48.对比例1
49.本对比例制备了一种胎盘粉,与实施例1的区别在于不加右旋糖酐40和葡糖氧化酶,其余步骤参考实施例1。
50.对比例2
51.本对比例制备了一种胎盘粉,与实施例1的区别在于只加0.2mg/g右旋糖酐40而不加葡糖氧化酶,其余步骤参考实施例1。
52.对比例3
53.本对比例制备了一种胎盘粉,与实施例1的区别在于只加0.2mg/g葡糖氧化酶而不加右旋糖酐40,其余步骤参考实施例1。
54.对比例4
55.本对比例制备了一种胎盘粉,与实施例1的区别在于加0.2mg/g右旋糖酐40和茶多酚的混合物,二者质量比为1:1,其余步骤参考实施例1。
56.对比例5
57.本对比例制备了一种胎盘粉,与实施例1的区别在于加0.2mg/g葡糖氧化酶和茶多酚的混合物,二者质量比为1:1,其与步骤参考实施例1。
58.对比例6
59.本对比例制备了一种胎盘粉,与实施例1的区别在于加0.2mg/g右旋糖酐40和抗坏血酸(货号:a103533-100g,阿拉丁)的混合物,二者质量比为1:1,其余步骤参考实施例1。
60.对比例7
61.本对比例制备了一种胎盘粉,与实施例1的区别在于加0.2mg/g葡糖氧化酶和抗坏血酸的混合物,二者质量比为1:1,其余步骤参考实施例1。
62.对比例8
63.本对比例制备了一种胎盘粉,与实施例1的区别在于加0.2mg/g葡糖氧化酶和右旋糖酐40的混合物,二者质量比为1:2,其余步骤参考实施例1。
64.试验例
65.对实施例1制备的胎盘粉进行安全性和有效性的验证:
66.一、胎盘粉的安全性验证
67.1.红细胞微核实验
68.前处理:将实施例1制备的胎盘粉样品用研钵磨碎后过200目筛网,取过筛后细粉末作为受试物,试验前用纯水配制至浓度为4mg/ml:
69.根据人体推荐量为50mg/天/人(人体重以60kg计),以人的可能摄入量的100倍作为高剂量,故以0.0833g/kg体重为最高剂量,下设0.0417g/kg体重(50倍)、0.0208g/kg体重(25倍),共3个剂量,同时设阴性对照组和阳性对照组。
70.阳性对照物:以环磷酰胺(cp)作为实验的阳性对照物,购自上海源叶生物科技有限公司,批号:sj0121ra140。
71.取检疫合格的雌、雄spf级km小鼠各25只,按体重随机分为5组,每组5只。用经口灌胃方式给予各组动物相应的受试物,灌胃体积为10ml/kg体重,共染毒2次,间隔24h。于末次染毒后6h采集标本。阳性对照组选用剂量为40mg/kg体重的环磷酰胺,临用前用纯水配制成浓度为4.0mg/ml;阴性对照组选用受试物的溶剂(纯水),操作程序同试验组。
72.颈椎脱臼处死动物,取出胸骨,去除肌肉等组织。横向剪开胸骨,暴露骨髓腔,然后
用止血钳挤出骨髓液,将骨髓液滴在载玻片一端的小牛血清液滴里,仔细混匀,常规涂片。自然晾干,放入甲醇液中固定5min,giemsa染色15min。立即用1/15mol/l磷酸盐缓冲液冲洗,晾干。观察每个动物骨髓的红细胞,计数嗜多染红细胞在总红细胞中比例。每个动物观察2000个嗜多染红细胞以计数含有微核的嗜多染红细胞频率,以千分率表示。一个嗜多染红细胞中含有多个微核存在时,只按一个细胞计。用spss软件建立数据库,按动物性别分别统计各组含微核细胞率的均数和标准差,用u检验分别比较受试物各剂量组雌、雄性动物与阴性(溶剂)对照组相应性别的微核细胞率。结果评价:试验组与对照组相比,试验结果含微核细胞率有明显的剂量-反应关系并有统计学意义时,即可确认为阳性结果。结果见下表1。
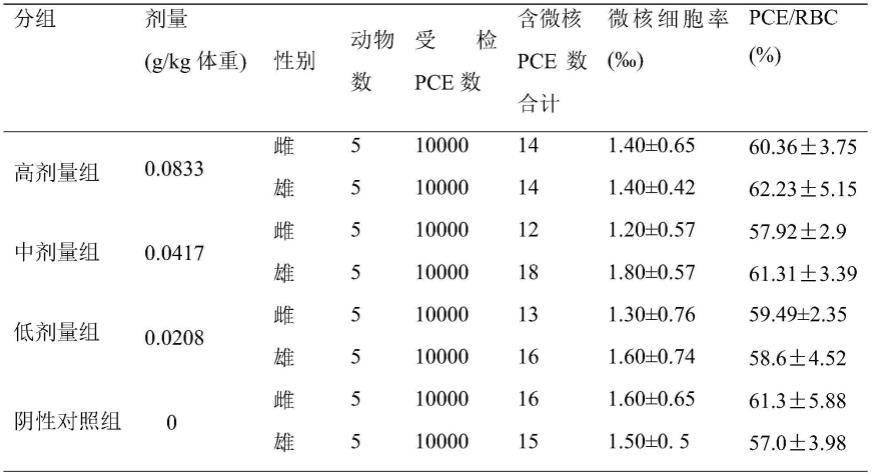
73.表1哺乳动物红细胞微核试验结果
[0074][0075][0076]
注:**表示与阴性对照组比较p《0.01;含微核细胞率(
‰
)和pce/rbc(%)均以小鼠为单位统计,表示为均值
±
标准差。
[0077]
由表1可见,受试物各剂量嗜多染红细胞(pce)与红细胞百分比未少于溶剂对照组的20%,表明受试物在实验剂量下无明显细胞毒性;受试物各剂量组的微核发生率与溶剂对照组相比,均无统计学差异(p>0.05);提示该受试物对小鼠骨髓细胞无致微核作用。
[0078]
2.哺乳动物染色体畸变实验
[0079]
细胞株:仓鼠肺细胞(chl细胞),购自中国科学院上海生命科学研究院细胞资源中心。
[0080]
代谢物活化系统:经β-萘黄酮和苯巴比妥钠诱导的大鼠肝匀浆上清液(s9),购自江苏齐氏生物科技有限公司(批号:21fs107c)。s9组分和辅助因子按1:9组成10%的s9混合液,无菌现用现配,用作本试验体外代谢物活化系统。
[0081]
阳性物:环磷酰胺(cp)购自上海源叶生物科技股份有限公司(批号:x13j11y115691),用mem培养液(不含血清)配制成使用浓度为7.5μg/ml。丝裂霉素c(mmc)购自美国mce公司(批号:31756),用mem培养液(不含血清)配制成使用浓度为0.6μg/ml。
[0082]
阴性对照:取等同于样品体积的无血清培养基作为阴性对照。
[0083]
受试物及剂量设计:将实施例1制备的胎盘粉样品用研钵磨碎后过200目筛网,取过筛后细粉末作为受试物。受试物用无血清mem培养基稀释,所得的棕褐色混悬液经121℃、20min高压灭菌处理,作为染毒液备用。染毒液用无血清mem培养基稀释,现配现用。
[0084]
细胞毒性实验:将chl细胞接种于细胞培养用的6孔培养板中,接种密度为1*106个/孔,置37℃、5%co2培养箱培养24h后,吸去培养板中的培养液,加入不同浓度(5000μg/ml、2500μg/ml、1250μg/ml)的受试物0.3ml,需代谢活化组同时加入s9混合液0.3ml,加不含血清的培养液至总体积为3.0ml,放培养箱中作用4h后,弃去含受试物的培养液,用pbs液洗细胞3次,加入含10%胎牛血清的mem培养液,继续培养24h。根据受试物不同浓度下细胞的相对有丝分裂指数,确定受试物的最高剂量。
[0085]
按照细胞毒性试验相同的处理方法,在加和不加s9混合液的条件下,受试物与试验系统的接触时间为4h。收获细胞前4h加入秋水仙素,终浓度为1.0μg/ml,按常规方法消化,低渗,固定,制片,giemsa染色。选取有丝分裂指数大于50%的剂量组进行染色体畸变分析。
[0086]
阅片分析:每一处理组选100个分散良好的中期分裂相(染色体数为2n
±
2)进行染色体畸变分析,记录染色体结构畸变的细胞数和畸变的类型,并计算染色体畸变细胞率,畸变细胞数/100(%),用χ2检验进行统计学分析。
[0087]
在加和不加s9混合液的条件下,阳性对照组的染色体畸变率与各自对照组比较,差异有统计学意义(p《0.01),试验系统成立;在加s9混合液的条件下,该受试物在加入浓度为5000μg/ml及以下剂量时,染色体畸变率与阴性对照组比较,差异无统计学意义(p》0.05);在不加s9混合液的条件下,该受试物在加入浓度为5000μg/ml及以下剂量时,染色体畸变率与阴性对照组比较,差异无统计学意义(p》0.05)。各处理组和对照组染色体畸变率及统计结果见下表2。
[0088]
表2体外哺乳类细胞染色体畸变实验结果
[0089][0090]
由表2可知,在试验条件下,该受试物(胎盘粉)在加与不加代谢活化系统的情况下染毒4h,均未引起chl细胞染色体畸变。因此证明本发明制备的胎盘粉是安全的。
[0091]
二、胎盘粉的保存期验证
[0092]
1.产品中有效成分检测分析
[0093]
对实施例1和对比例1制备的胎盘粉中各成分的分析参考以下方法:
[0094]
采用比色法对sod含量进行测定、采用化学发光法对胶原蛋白和透明质酸含量进
行测定,严格按照各试剂盒说明书操作;
[0095]
n-乙酰神经氨酸含量检测方法:利用0.1mol/l的甲酸水解释放出胎盘粉中的的n-乙酰神经氨酸,用邻苯二胺盐(opd)作为衍生化试剂,80℃避光衍生100min,采用高效液相色谱荧光检测。色谱条件为:用thermo hypersil gold柱(250mm
×
4.6mm,5μm)分离;流动相选择超纯水-乙腈作为梯度洗脱,具体见表3,柱温为30℃,流速为1.0ml/min;进样体积为10μl;荧光检测器激发波长为337nm,发射波长为448nm,结果见下表4:
[0096]
表3流动相洗脱程序
[0097]
时间(min)a(水)/%b(乙腈)/%09010780209109012109012.19010179010
[0098]
不同保存方式处理后胎盘粉保存21天生物活性物质含量(2~8℃)见下表5:
[0099]
表4不同工艺处理后初始样品中生物活性物质的含量
[0100][0101]
注:tpft:右旋糖酐+葡糖氧化酶组(实施例1),胎盘粉中添加了右旋糖酐+葡糖氧化酶。
[0102]
tpf:单纯胎盘粉组(对比例1)
[0103]
检测结果如表4所示,胎盘中含有丰富的胶原蛋白和透明质酸等活性物质,经过冻干处理后胶原蛋白的含量会有一定程度损失,但不多。另外,大量体内外和临床医学研究证实,n-乙酰神经氨酸具有显著的清除自由基、抗衰老、抗肿瘤、解毒等药理和保健功效。
[0104]
表5实施例1和对比例1~5制备的胎盘粉保存21天生物活性物质含量(2~8℃)
[0105][0106]
结果分析:对比例1未添加任何抗氧化剂,经过21天保存后,胶原蛋白、超氧化物歧化酶、透明质酸、n-乙酰神经氨酸的成分含量由103.51、34.44、125.42、13.89降低至80.8、25.55、99.33、8.6,与其他对比例相比,降低幅度最大。对比例2和3单独添加右旋糖酐或葡糖氧化酶,经过21天保存后,四种有效成分含量降低,但仍高于对比例1中的数据。对比例4和5,胎盘粉中添加右旋糖酐40和茶多酚的混合物或者是葡糖氧化酶和茶多酚的混合物,经过21天保存后,四种有效成分含量降低,但与对比例2和3相比,有效成分的含量并未显著升高。通过对比例1、2、3、4、5、6、7的结果可以得出,在添加抗氧化剂剂量相同的情况下,21天保存后活性成分剩余量会有一定的提高,但并未发现联合应用组中的活性成分含量要高于单一成分应用组。另外将茶多酚由抗坏血酸替代,分别与右旋糖酐或者葡糖氧化酶联合应用,也未发现联合应用组要优于单一成分组。但是实施例1中右旋糖酐和葡糖氧化酶联合应用,经过21天保存后,四种活性成分的含量与对比例相比显著提高。说明右旋糖酐+葡糖氧化酶联合应用有增效作用。原因可能是右旋糖酐40促进葡糖氧化酶的催化作用,提高其催化效率,从而提高抗氧化的效果。对比例8将右旋糖酐和葡糖氧化酶按照比例1:2进行配比,结果与实施例1相比活性成分含量降低,可见右旋糖酐和葡糖氧化酶和合适配比也是尤为重要的因素。
[0107]
上面对本发明实施例作了详细说明,但是本发明不限于上述实施例,在所属技术领域普通技术人员所具备的知识范围内,还可以在不脱离本发明宗旨的前提下作出各种变化。此外,在不冲突的情况下,本发明的实施例及实施例中的特征可以相互组合。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1