一种钆布醇注射液及其制备方法与流程
1.本发明属于造影剂技术领域,具体涉及一种钆布醇注射液及其制备方法。
背景技术:
2.钆布醇注射液(1.0mol/l)是由德国拜耳研发的一种以钆布醇为活性成分的钆螯合物注射液,通常作为造影剂用于磁共振成像(mri)。钆布醇具有高螯合稳定性的环状结构,释放风险较低,欧洲泌尿生殖放射学会(esur)在nsf(nephrogenic systemic fibrosis)风险分类中,将其定位为低nsf风险的钆造影剂。
3.中国专利cn106620726b提出一种钆布醇注射液的制备方法,具体是将磷酸盐与部分水混合均匀,得到混合液a;将考布曲钙钠、钆布醇与所述混合液a混合均匀,得到混合液b;用剩余部分的水稀释所述混合液b,即得钆布醇注射液。同时该专利公开了所述钆布醇注射液的ph值为6.7~8.0,若稀释后混合液的ph值高于上述范围,可以在稀释后进一步采用酸调节ph值。但是采用该专利方法制备的钆布醇注射液中游离钆离子的含量≥0.008mg/ml,游离钆离子含量较高。
技术实现要素:
4.本发明的目的在于提供一种钆布醇注射液及其制备方法,克服了现有技术制备的钆布醇注射液中游离钆离子的含量较高的技术缺陷。
5.为了实现本发明的目的,本发明提供了以下技术方案:
6.一种钆布醇注射液的制备方法,包括以下步骤:
7.(1)将ph调节剂与部分水混合,得到第一溶液;
8.(2)将所述第一溶液与氨丁三醇、考布曲钙、钆布醇及剩余水混合,得到钆布醇注射液;
9.所述步骤(1)~(2)中混合的温度≤50℃。
10.优选地,以钆布醇注射液的体积为单位体积计,所述钆布醇的浓度为0.59~0.66g/ml,所述考布曲钙的浓度为0.46~0.52mg/ml,所述氨丁三醇的浓度为1.15~1.28mg/ml,所述ph调节剂的体积分数为0.6%。
11.优选地,所述ph调节剂为盐酸,所述ph调节剂的浓度为1.0mol/l。
12.优选地,所述步骤(1)~(2)中混合的独立温度为20~50℃。
13.优选地,所述步骤(2)中混合包括:将氨丁三醇与所述第一溶液混合,得到第二溶液;将考布曲钙与所述第二溶液混合,得到第三溶液;将钆布醇与所述第三溶液及剩余水混合,得到钆布醇注射液。
14.优选地,所述部分水和剩余水的用量比为2~3:3~2。
15.优选地,所述步骤(2)中混合后还包括依次进行的过滤和灭菌。
16.优选地,所述灭菌为湿热灭菌,所述灭菌的的温度为121℃,灭菌时间为15min。
17.本发明还提供了由上述技术方案所述制备方法制备得到的钆布醇注射液,所述钆
布醇注射液中游离钆离子的含量<0.0002mg/ml。
18.优选地,所述钆布醇注射液中除游离钆离子以外的重金属离子的含量≤19ppm。
19.本发明提供了一种钆布醇注射液的制备方法,包括以下步骤:(1)将ph调节剂与部分水混合,得到第一溶液;(2)将所述第一溶液与氨丁三醇、考布曲钙、钆布醇及剩余水混合,得到钆布醇注射液;所述步骤(1)~(2)中混合的温度≤50℃。本发明通过先将ph调节剂与部分水混合均匀,改变了传统方法中ph调节顺序,避免了最后调节使钆布醇注射液局部过酸,从而导致钆游离的情况,大大降低了钆布醇注射液中游离钆离子的含量;同时氨丁三醇作为ph缓冲剂,其ph值调控有效范围通常在7.0~9.2之间,相比于磷酸盐的缓冲能力更强,在钆布醇注射液制备过程中可以更优的控制ph值的调节范围,使钆布醇注射液具有较好稳定性,有利于降低钆布醇注射液中游离钆离子的含量,此外能够避免采用磷酸盐易使重金属离子(如钆离子以及生产过程中生产组件和原料带入的其它重金属离子)形成沉淀的问题;配合使用考布曲钙作为金属离子络合剂,相比于考布曲钙钠对游离钆离子的络合能力更强,从而能够降低钆布醇注射液中游离钆离子的含量。实施例结果表明,采用本发明制备方法制备得到的钆布醇注射液中游离钆离子含量<0.0002mg/ml。进一步地,本发明提供的钆布醇注射液的制备方法工艺简单,原料易得,成本低廉。
具体实施方式
20.本发明提供了一种钆布醇注射液的制备方法,包括以下步骤:
21.(1)将ph调节剂与部分水混合,得到第一溶液;
22.(2)将所述第一溶液与氨丁三醇、考布曲钙、钆布醇及剩余水混合,得到钆布醇注射液;
23.所述步骤(1)~(2)中混合的温度≤50℃。
24.在本发明中,若无特殊说明,所用各制备原料均是本领域技术人员熟知的市售商品。
25.首先对本发明所述钆布醇注射液的制备原料进行说明。本发明所述钆布醇注射液的制备原料包括ph调节剂、氨丁三醇、钆布醇和水。
26.在本发明中,所述ph调节剂优选为盐酸,所述ph调节剂的浓度优选为1.0mol/l;以钆布醇注射液的体积为单位体积计,所述ph调节剂的体积分数优选为0.6%。
27.在本发明中,以钆布醇注射液的体积为单位体积计,所述氨丁三醇的浓度优选为1.15~1.28mg/ml,更优选为1.18~1.25mg/ml,进一步优选为1.21~1.22mg/ml。本发明使用氨丁三醇作为ph缓冲剂,氨丁三醇调控ph值的有效范围通常在7.0~9.2之间,相比于磷酸盐的缓冲能力更强,在钆布醇注射液制备过程中可以更优的控制ph值的调节范围;此外,使用氨丁三醇作为ph缓冲剂能够避免采用磷酸盐易使重金属离子(如钆离子以及生产过程中生产组件和原料带入的其它重金属离子)形成沉淀的问题。
28.在本发明中,以钆布醇注射液的体积为单位体积计,所述考布曲钙的浓度优选为0.46~0.52mg/ml,更优选为0.48~0.51mg/ml,进一步优选为0.49~0.50mg/ml。本发明中使用考布曲钙作为金属离子络合剂,相比于考布曲钙钠对游离钆离子的络合能力更强,从而有利于降低钆布醇注射液中游离钆离子的含量。
29.在本发明中,所述钆布醇优选为钆布醇水合物,更优选为钆布醇一水合物;在本发
明中,以钆布醇注射液的体积为单位体积计,所述钆布醇的浓度优选为0.59~0.66g/ml,更优选为0.61~0.64g/ml,进一步优选为0.62~0.63g/ml。
30.在本发明中,所述水优选为注射用水;在本发明的实施例中,具体采用新鲜注射用水,所述新鲜注射用水具体为新拆封的注射用水。本发明将所述水分两部分使用,即首先将部分水与ph调节剂混合,避免了最后调节使钆布醇注射液局部过酸,从而导致钆游离的情况,大大降低了钆布醇注射液中游离钆离子的含量,最后再采用剩余水补足至所需体积。在本发明中,所述部分水和剩余水的用量比优选为2~3:3~2,进一步优选为1:1。
31.下面对本发明所述钆布醇注射液的制备方法进行说明。
32.本发明将ph调节剂与部分水混合,得到第一溶液。在本发明中,所述混合的温度≤50℃,优选为20~50℃,具体可以为20~30℃、30~40℃或40~50℃。在本发明中,所述混合的方式优选为搅拌混合,本发明对所述搅拌混合的搅拌条件没有特殊限定,能达到混合均匀目的即可。
33.得到第一溶液后,本发明将所述第一溶液与氨丁三醇、考布曲钙、钆布醇及剩余水混合,得到钆布醇注射液。在本发明中,所述混合优选包括:将氨丁三醇与所述第一溶液混合,得到第二溶液;将考布曲钙与所述第二溶液混合,得到第三溶液;将钆布醇与所述第三溶液及剩余水混合,得到钆布醇注射液。在本发明中,所述氨丁三醇与第一溶液混合的温度≤50℃,优选为20~50℃,具体可以为20~30℃、30~40℃或40~50℃;所述混合的方式优选为搅拌混合。在本发明中,通过控制混合温度在上述范围内,可以在使原料易于溶解的基础上,避免原料在高温条件下不稳定、易分解的情况。本发明在得到第一混合溶液后加料氨丁三醇,氨丁三醇可以中和盐酸带来的酸性,避免了钆布醇遇酸会游离出钆离子的情况,有利于进一步降低钆布醇注射液中游离钆离子的含量。
34.得到第二溶液后,本发明优选将考布曲钙与所述第二溶液混合,得到第三溶液。在本发明中,所述考布曲钙与所述第二溶液混合的温度≤50℃,优选为20~50℃,具体可以为20~30℃、30~40℃或40~50℃;所述混合的方式优选为搅拌混合。在本发明中,通过控制混合温度在上述范围内,可以在使原料易于溶解的基础上,避免原料在高温条件下不稳定、易分解的情况。本发明在得到第二混合溶液后加料考布曲钙,考布曲钙作为络合剂,可以在第一时间络合后续加入的钆布醇所附带的钆离子,有利于进一步降低钆布醇注射液中游离钆离子的含量。
35.得到第三溶液后,本发明优选将钆布醇与所述第三溶液及剩余水混合,得到钆布醇注射液。在本发明中,所述钆布醇与所述第三溶液及剩余水混合的温度≤50℃,优选为20~50℃,具体可以为20~30℃、30~40℃或40~50℃;所述混合的方式优选为搅拌混合。在本发明中,通过控制混合温度在上述范围内,可以在使原料易于溶解的基础上,避免原料在高温条件下不稳定、易分解的情况。
36.在本发明中,所述将钆布醇与第三溶液及剩余水混合后优选还包括依次进行过滤和灭菌。本发明中,所述过滤使用的滤膜优选为聚醚砜(pes)滤膜,所述滤膜的孔径优选为0.22μm;本发明对所述过滤的具体操作方式并无特殊限定,采用本领域常规过滤方式即可。本发明中,所述灭菌优选为湿热灭菌,所述湿热灭菌的温度优选为121℃,所述湿热灭菌的时间优选为15min。
37.本发明还提供了上述技术方案所述制备方法制备得到的钆布醇注射液,所述钆布
醇注射液中游离钆离子的含量<0.0002mg/ml,更优选为0.00002~0.00012mg/ml。
38.在本发明中,所述钆布醇注射液的ph值优选为7.0~8.0,更优选为7.3~7.5。
39.在本发明中,所述钆布醇注射液中除游离钆离子以外的重金属离子的含量优选≤19ppm,具体可以为15~19ppm。
40.在本发明中,所述钆布醇注射液中钆布醇的含量优选为96.34~103.21%。
41.在本发明中,所述钆布醇注射液中考布曲钙的含量优选为0.35~0.62mg/ml。
42.在本发明中,所述钆布醇注射液中布醇(记为杂质b)的含量≤0.04%,具体为0.01~0.04%;所述钆布醇注射液中未检出4,10-二(2,3-二羟基-1-羟甲基丙基)-1,4,7,10-四氮杂环十二烷-1,7-二乙酸(di-tobo,记为杂质a)以及1,4,7,10-四氮杂环十二烷-1,4,7-三乙酸与钆的络合物(gd-d03a,记为杂质c)。
43.在本发明中,所述钆布醇注射液的规格优选为7.5ml,此时制备原料优选包括钆布醇一水合物4.45~4.90g,考布曲钙3.50~3.86mg,氨丁三醇8.65~9.55mg,盐酸(1mol/l)45μl,水以使所述钆布醇注射液的体积为7.5ml为基准。
44.为了进一步说明本发明,下面结合实施例对本发明提供的一种钆布醇注射液及其制备方法进行详细地描述,但不能将它们理解为对本发明保护范围的限定。显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
45.实施例1
46.(1)在配制设备中加入300ml的新鲜注射用水,加入浓度为1.0mol/l的盐酸4500μl,控制温度20~30℃,混合均匀,得到第一溶液;
47.(2)在第一溶液中加入865mg氨丁三醇,控制温度20~30℃,混合均匀,得到第二溶液;
48.(3)在第二溶液中加入350mg考布曲钙,控制温度20~30℃,混合均匀,得到第三溶液;
49.(4)在第三溶液中加入445g钆布醇一水合物,控制温度20~30℃,混合均匀,得到混合溶液;使用剩余注射用水将上述混合溶液定容至750ml,使用0.22μm的pes滤膜过滤,在121℃条件下湿热灭菌15min,得到钆布醇注射液。
50.实施例2
51.(1)在配制设备中加入450ml的新鲜注射用水,加入浓度为1.0mol/l的盐酸4500μl,控制温度40~50℃,混合均匀,得到第一溶液;
52.(2)在第一溶液中加入955mg氨丁三醇,控制温度40~50℃,混合均匀,得到第二溶液;
53.(3)在第二溶液中加入386mg考布曲钙,控制温度40~50℃,混合均匀,得到第三溶液;
54.(4)在第三溶液中加入490g钆布醇一水合物,控制温度40~50℃,混合均匀,得到混合溶液;使用剩余注射用水将上述混合溶液定容至750ml,使用0.22μm的pes滤膜过滤,在121℃条件下湿热灭菌15min,得到钆布醇注射液。
55.实施例3
56.(1)在配制设备中加入375ml的新鲜注射用水,加入浓度为1.0mol/l的盐酸4500μl,控制温度30~40℃,混合均匀,得到第一溶液;
57.(2)在第一溶液中加入910mg氨丁三醇,控制温度30~40℃,混合均匀,得到第二溶液;
58.(3)在第二溶液中加入368mg考布曲钙,控制温度30~40℃,混合均匀,得到第三溶液;
59.(4)在第三溶液中加入467.5g钆布醇一水合物,控制温度30~40℃,混合均匀,得到混合溶液;使用剩余注射用水将上述混合溶液定容至750ml,使用0.22μm的pes滤膜过滤,在121℃条件下湿热灭菌15min,得到钆布醇注射液。
60.对比例1
61.(1)在配制设备中加入375ml的新鲜注射用水,加入浓度为1.0mol/l的盐酸4500μl,控制温度70~80℃,混合均匀,得到第一溶液;
62.(2)在第一溶液中加入910mg氨丁三醇,控制温度70~80℃,混合均匀,得到第二溶液;
63.(3)在第二溶液中加入385mg考布曲钙,控制温度70~80℃,混合均匀,得到第三溶液;
64.(4)在第三溶液中加入467.5g钆布醇一水合物,控制温度70~80℃,混合均匀,得到混合溶液;使用剩余注射用水将上述混合溶液定容至750ml,使用0.22μm的pes滤膜过滤,在121℃条件下湿热灭菌15min,得到钆布醇注射液。
65.对比例2
66.(1)在配制设备中加入375ml的新鲜注射用水,再加入910mg氨丁三醇,控制温度30~40℃,混合均匀,得到第一溶液;
67.(2)在第一溶液中加入385mg考布曲钙,控制温度30~40℃,混合均匀,得到第二溶液;
68.(3)在第二溶液中加入467.5g钆布醇一水合物,控制温度30~40℃,混合均匀,得到第三溶液;
69.(4)在第三溶液中加入4500μl浓度为1.0mol/l的盐酸,使用剩余注射用水定容至750ml,使用0.22μm的pes滤膜过滤,在121℃条件下湿热灭菌15min,得到钆布醇注射液。
70.对比例3
71.(1)在配制设备中加入375ml的新鲜注射用水,加入浓度为1.0mol/l的盐酸4500μl,控制温度40~50℃,混合均匀,得到第一溶液;
72.(2)在第一溶液中加入910mg氨丁三醇,控制温度40~50℃,混合均匀,得到第二溶液;
73.(3)在第二溶液中加入402mg考布曲钙钠,控制温度40~50℃,混合均匀,得到第三溶液;
74.(4)在第三溶液中加入490g钆布醇一水合物,控制温度40~50℃,混合均匀,得到混合溶液;使用剩余注射用水将上述混合溶液定容至750ml,使用0.22μm的pes滤膜过滤,在121℃条件下湿热灭菌15min,得到钆布醇注射液。
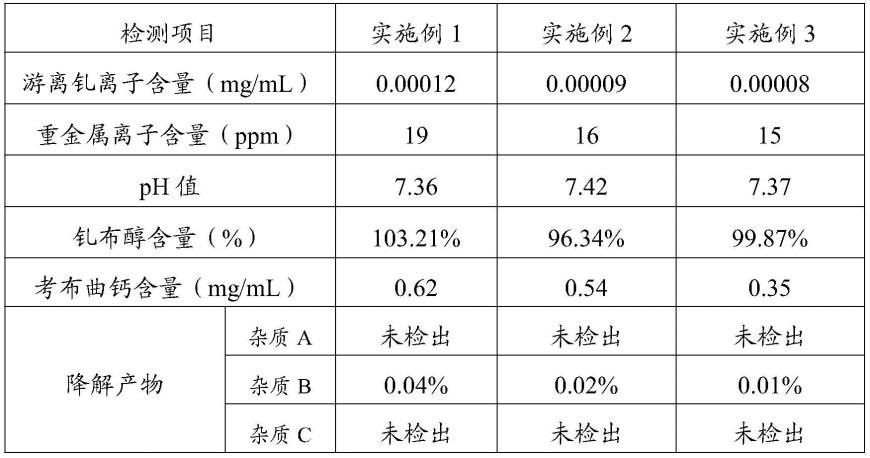
75.对实施例1~3制备得到的钆布醇注射液进行检测,测试结果如下表1所示。
76.表1实施例1~3钆布醇注射液测试结果
[0077][0078]
注:表1中所述重金属离子含量为除游离钆离子外的其余重金属离子的含量,为生产过程中由生产组件和原来带入的其它金属离子。
[0079]
表1中杂质a为杂质zk00158723:di-tobo(4,10-二(2,3-二羟基-1-羟甲基丙基)-1,4,7,10-四氮杂环十二烷-1,7-二乙酸);表1中杂质b为布醇;表1中杂质c为杂质zk00132534:gd-d03a(1,4,7,10-四氮杂环十二烷-1,4,7-三乙酸与钆的络合物)。
[0080]
由表1可知,本发明制备的钆布醇注射液中游离钆离子的含量为0.00008~0.00012mg/ml,游离钆离子的含量较低;重金属离子的含量为15~19ppm,杂质b的含量为0.01~0.04%,杂质a以及杂质c均未检出,制备的钆布醇注射液质量合格。
[0081]
对实施例1~3制备的钆布醇注射液进行稳定性测试,具体是在60℃条件下放置10天(其它条件不额外控制),取第10天样品进行检测。结果如表2所示。
[0082]
表2高温条件下钆布醇注射液稳定性测试结果
[0083][0084]
由表2可知,本发明制备的钆布醇注射液在高温条件下,试验10天后,ph值和游离钆离子含量无明显差别,具有良好的稳定性。
[0085]
对实施例1~3制备的钆布醇注射液进行稳定性测试,具体是在强光照条件下放置10天(其它条件不额外控制),所述强光照条件为:照度为4500lx
±
500lx,光源总照度不低于1.2
×
106lux
·
hr,近紫外灯能量不低于200w
·
hr/m2;取第10天样品进行检测。结果如表3所示。
[0086]
表3强光照条件下钆布醇注射液稳定性测试结果
[0087][0088][0089]
由表3可知,本发明制备方制备的钆布醇注射液在强光照条件下,试验10天后,ph值和游离钆含量无明显差别,具有良好的稳定性。
[0090]
将对比例1~3制备的钆布醇注射液进行检测,测试结果如下表4所示。
[0091]
表4对比例1~3钆布醇注射液测试结果
[0092][0093]
比较实施例3和对比例1可知,对比例1使用了较高的混合温度70~80℃,其制备的钆布醇注射液中游离钆离子的含量为0.003mg/ml,杂质b的含量为0.12%,其游离钆离子和杂质b的含量均比较高。本发明采用的混合温度为30~40℃,有利于降低钆布醇注射液中游离钆离子和杂质的含量。
[0094]
比较实施例3和对比例2可知,对比例2采用了最后使用盐酸调节ph值,其制备的钆
布醇注射液中游离钆离子的含量为0.00022mg/ml,游离钆离子的含量较高。本发明ph调节顺序不同于对比例2,先将ph调节剂与部分水混合均匀,避免了最后调节使局部过酸,从而导致钆游离的情况,由上述试验结果可知,采用先调节ph值的制备方式,能够大大降低了钆布醇注射液中游离钆离子的含量。
[0095]
比较实施例2和对比例3可知,对比例3采用了考布曲钙钠作为金属离子络合剂,其制备的钆布醇注射液中游离钆离子含量为0.0036mg/ml,游离钆离子的含量较高。本发明中实施例2采用考布曲钙作为金属离子络合剂,制备的钆布醇注射液中游离钆离子的含量明显降低,由上述试验结果可知,采用考布曲钙作为金属离子络合剂能够大大降低钆布醇注射液中游离钆离子的含量。
[0096]
尽管上述实施例对本发明做出了详尽的描述,但它仅仅是本发明一部分实施例,而不是全部实施例,人们还可以根据本实施例在不经创造性前提下获得其他实施例,这些实施例都属于本发明保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1