一种无创肝纤维化评估装置
1.本发明涉及医疗技术领域,具体涉及一种无创肝纤维化评估装置。
背景技术:
2.肝纤维化是慢性肝病预后的主要决定因素,尽早识别进展期纤维化和肝硬化并实施干预是肝细胞癌防治的关键,也是慢性肝病疾病管理的重要方面,能够作为辅助信息帮助医生进行慢性肝病疾病的相关诊断。
3.肝纤维化的无创评估具有无侵袭性、可重复性、价格低、患者耐受性好等优势,然而现有技术中,肝纤维化4因子指数(the fibrosis index based on four factors,fib-4)和天门冬氨酸氨基转移酶(ast)和血小板(plt)比率指数(aspartateaminotransferase-to-plateletratioindex,apri)作为应用最广泛的血清评估模型,它们的评估效能在不同研究中的表现参差不齐;肝脏硬度测量(liver stiffness measurement,lsm)是目前效能最佳的肝纤维化无创评估手段,但不少研究发现lsm易受肝坏死炎症的影响,导致其在伴有肝脏炎症的患者中评估纤维化的效能下降,而在接受抗病毒治疗的慢性乙型病毒性肝炎患者中,尤其是抗病毒治疗后lsm值出现明显下降的这部分患者中,lsm的评估效能也明显下降。
4.因此,准确率更高、评估效果更好的无创肝纤维化评估方案能够作为辅助信息帮助医生进行诊断,也是目前业界亟待解决的技术问题。
技术实现要素:
5.有鉴于此,本发明实施例提供了一种无创肝纤维化评估装置,以解决现有的肝纤维化的无创评估评估效能较差的问题。
6.根据第一方面,本发明实施例提供了一种无创肝纤维化评估装置,所述装置包括:信息获取模块,用于确定待评估者的评估信息以及肝相关信息,并从所述评估信息以及所述肝相关信息中确定肝指标信息;评分预测模块,用于基于所述肝指标信息,将所述肝指标信息输入至对应的无创肝纤维化评估模型中,得到所述无创肝纤维化评估模型输出的预测评分;所述无创肝纤维化评估模型包括第一无创肝纤维化评估模型和第二无创肝纤维化评估模型,所述第一无创肝纤维化评估模型是基于血清评估模型和肝评估参数序贯应用得到的,所述第二无创肝纤维化评估模型是基于血清评估模型和肝评估参数进行逻辑回归得到的,所述血清评估模型采用风险预测模型;当肝指标信息表征待评估者为肝治疗前评估者时,所述肝指标信息输入至所述第一无创肝纤维化评估模型,当肝指标信息表征待评估者为肝治疗后评估者时,所述肝指标信息输入至所述第二无创肝纤维化评估模型;患者评估模块,用于根据所述预测评分,确定待评估者对应的肝纤维化发生程度。
7.结合第一方面,在第一方面第一实施方式中,所述肝指标信息包括待评估者的性别、年龄、肝治疗信息、谷丙转氨酶、谷草转氨酶、白蛋白、总胆红素、血小板计数以及肝评估
参数;所述评分预测模块中的所述血清评估模型是基于样本肝指标信息训练得到的。
8.结合第一方面第一实施方式,在第一方面第二实施方式中,所述第一无创肝纤维化评估模型通过以下模块训练得到:第一训练模块,用于确定样本评估者对应的所述样本肝指标信息;第三训练模块,用于将所述样本肝指标信息输入至所述血清评估模型中,得到所述血清评估模型输出的第一样本评分;第四训练模块,用于确定所述第一样本评分对应的第一特征曲线下面积值,并基于灵敏度、特异性以及第一特征曲线下面积值,确定所述血清评估模型对应的第一界值以及第二界值;第五训练模块,用于确定所述肝评估参数对应的第二特征曲线下面积值,并基于灵敏度、特异性以及第二特征曲线下面积值,确定所述肝评估参数对应的第三界值以及第四界值;第六训练模块,用于基于所述血清评估模型以及对应的所述第一界值、第二界值、所述肝评估参数以及对应的所述第三界值、第四界值构建所述第一无创肝纤维化评估模型。
9.结合第一方面第二实施方式,在第一方面第三实施方式中,所述第一无创肝纤维化评估模型还通过以下模块训练得到:第二训练模块,用于基于所述样本肝指标信息对所述样本评估者进行分组。
10.结合第一方面第二实施方式,在第一方面第四实施方式中,第三训练模块具体包括:基于所述血清评估模型对应的第一评估因子和所述样本肝指标信息中的样本白蛋白、样本总胆红素以及样本血小板计数,得到所述血清评估模型输出的第一样本评分。
11.结合第一方面第二实施方式,在第一方面第五实施方式中,所述第二无创肝纤维化评估模型通过以下模块训练得到:第七训练模块,用于确定样本评估者对应的所述样本肝指标信息;第八训练模块,用于将治疗后的进展期纤维化以及肝硬化作为因变量,年龄、性别、样本评估者治疗前及治疗后的第一样本评分、肝指标信息作为自变量,采用单因逻辑回归分析对所述自变量进行分析,确定所述自变量中的预测因子;第九训练模块,用于采用多因素逻辑回归分析对所述预测因子进行分析,确定所述预测因子中的独立预测因子;第十训练模块,用于确定所述独立预测因子对应的回归系数以及回归常数,并基于所述独立预测因子、所述回归系数以及所述回归常数构建回归模型;第十一训练模块,用于将所述样本肝指标信息输入至所述回归模型中,得到所述回归模型输出的第二样本评分;第十二训练模块,用于确定所述第二样本评分对应的第三特征曲线下面积值,并基于灵敏度、特异性以及第三特征曲线下面积值,确定所述回归模型对应的第五界值以及第六界值;第十三训练模块,用于基于所述回归模型以及对应的所述第五界值、第六界值构
建所述第二无创肝纤维化评估模型。
12.本发明提供的无创肝纤维化评估装置,通过将已确定的肝指标信息输入至已训练好的无创肝纤维化评估模型,并基于无创肝纤维化评估模型输出的预测评分确定待评估者对应的肝纤维化发生程度,以此进行待评估者无创以及非侵入性肝纤维化的评估,其中第一无创肝纤维化评估模型通过序贯应用amap评分和lsm,在不增加额外经济负担的情况下,提高肝纤维化的评估效能,并且进一步减少肝活检需求,基于逻辑回归构建的第二无创肝纤维化评估模型针对接受治疗的慢乙肝患者尤其是治疗后lsm值出现明显下降的这部分患者,可以很好的弥补lsm在此类患者中评估效能不佳的缺陷,基于第一、第二无创肝纤维化评估模型确定的肝纤维化发生程度更加准确,作为辅助信息能够帮助医生进行更加准确的肝纤维化诊断。
附图说明
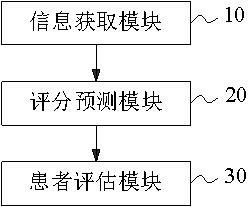
13.通过参考附图会更加清楚的理解本发明的特征和优点,附图是示意性的而不应理解为对本发明进行任何限制,在附图中:图1示出了本发明提供的无创肝纤维化评估装置的结构示意图;图2示出了本发明提供的无创肝纤维化评估装置利用第一无创肝纤维化评估模型进行评估时的示意图;图3示出了本发明提供的无创肝纤维化评估装置中第一无创肝纤维化评估模型训练过程的结构示意图之一;图4示出了本发明提供的无创肝纤维化评估装置中第一无创肝纤维化评估模型训练过程的结构示意图之二;图5示出了本发明提供的无创肝纤维化评估装置中第二无创肝纤维化评估模型训练过程的结构示意图。
具体实施方式
14.为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
15.慢性乙型肝炎病毒感染(chronic hepatitis b,chb)、非酒精性脂肪肝(non-alcoholic fatty liver disease , nafld)、酒精性脂肪肝、丙型病毒性肝炎等是当前慢性肝病的主要原因。其中,肝纤维化是慢性肝病预后的主要决定因素,其与危及生命的并发症和肝细胞癌相关,尽早识别进展期纤维化和肝硬化并实施干预是肝细胞癌防治的主要手段,也是慢性肝病疾病管理的重要方面。
16.由于肝纤维化的无创评估具有无侵袭性、可重复性、价格低、患者耐受性好等优势,在一些情况下可以成为肝活检的替代手段,例如肝纤维化的无创评估中利用患者临床特征、实验室检查结果构建的血清评估模型,以及lsm等无创手段的肝纤维化评估效能,目前已经被推荐用于评估慢性肝病患者的进展期纤维化或肝硬化,能够作为辅助信息帮助医生进行慢性肝病疾病的相关诊断。
17.然而现有技术中,肝纤维化4因子指数(the fibrosis index based on four factors,fib-4)和天门冬氨酸氨基转移酶(ast)和血小板(plt)比率指数(aspartateaminotransferase-to-plateletratioindex,apri)作为应用最广泛的血清评估模型,它们的评估效能在不同研究中的表现参差不齐;尽管lsm是目前效能最佳的肝纤维化无创评估手段,但不少研究发现lsm易受肝坏死炎症的影响,导致其在伴有肝脏炎症的患者中评估纤维化的效能下降,而在接受抗病毒治疗的慢性乙型病毒性肝炎患者中,尤其是抗病毒治疗后lsm值出现明显下降的这部分患者中,lsm的评估效能也明显下降。
18.为了解决上述问题,如图1和图2所示,在本实施例中提供了一种无创肝纤维化评估装置,该评估装置旨在提供一种非侵入性的、准确性更高的肝纤维化的评估装置,本发明实施例的无创肝纤维化评估装置可用于电子设备中,图1是根据本发明实施例的无创肝纤维化评估装置的结构示意图,如图1所示,该评估装置包括:信息获取模块10,用于确定待评估者的评估信息以及肝相关信息,并从评估信息以及肝相关信息中确定(提取出)肝指标信息。可以理解的是,待评估者即为待评估的患者。
19.在本发明实施例中,待评估者的评估信息包括性别、年龄、病史以及肝治疗信息(特别是肝病采用抗病毒治疗后的相关治疗信息)等等,肝相关信息则可以通过相关的医疗体检来获取。最终,确定得到的肝指标信息包括待评估者的性别、年龄、肝病的肝治疗信息、谷丙转氨酶(alt)、谷草转氨酶(ast)、白蛋白(alb)、总胆红素(tbil)、血小板计数(plt)、肝评估参数。其中,肝评估参数为lsm值。
20.需要说明的是,在本发明实施例一些可能的实施例中,lsm值还可以使用fibroscan等仪器进行测算。
21.评分预测模块20,用于将信息获取模块10中确定得到的肝指标信息输入至训练好的无创肝纤维化评估模型中,得到无创肝纤维化评估模型输出的预测评分。
22.在该评估装置中,训练好的无创肝纤维化评估模型包括第一无创肝纤维化评估模型和第二无创肝纤维化评估模型,第一无创肝纤维化评估模型是基于血清评估模型和lsm值序贯应用得到的,第二无创肝纤维化评估模型是基于血清评估模型和lsm值进行逻辑回归得到的,具体的,血清评估模型和lsm值序贯应用指的是所有待评估者先利用血清评估模型进行进展期纤维化或肝硬化的相关评估,位于血清模型不确定区域的患者则利用lsm值进行进一步进行评估,由此形成第一无创肝纤维化评估模型。下文将会具体阐述上述的不确定区域。
23.其中,血清评估模型优选的选取风险预测模型(amap评分模型),血清评估模型是基于样本肝指标信息训练得到的,可以理解的是,样本肝指标信息包括样本评估者的样本性别、样本年龄、肝病的样本肝治疗信息、样本谷丙转氨酶、样本谷草转氨酶、样本白蛋白、样本总胆红素、样本血小板计数以及样本lsm值。更具体的,amap模型是基于样本肝指标信息中的样本性别、样本年龄、样本白蛋白、样本总胆红素以及样本血小板计数计算得到对应的第一样本评分。
24.也就是说,除年龄、性别以外,amap评分模型中仅包含三种常见的临床检验指标,即白蛋白(alb)、总胆红素(tbil)、血小板计数(plt),使得amap评分模型以及基于amap评分模型的无创肝纤维化评估模型能够在基层医院也能很好的推广,由于不涉及肝脏炎症指标,amap评分在处于肝脏炎症活动期的患者中也能获取较好的评估性能。
25.患者评估模块30,用于根据评分预测模块20中得到的预测评分,确定待评估者对应的肝纤维化发生程度。
26.在该评估装置中,不同的无创肝纤维化评估模型会输出不同的预测评分,第一无创肝纤维化评估模型输出的是第一预测评分,第二无创肝纤维化评估模型输出的是第二预测评分。
27.进一步的,当第一预测评分不超过第一分值以及预测评分位于第一分值与第二分值之间且肝评估参数不超过第三分值时,肝纤维化发生程度为未发生肝纤维化,也就是该待评估者可以排除进展期纤维化或肝硬化;当第一预测评分不低于第二分值以及预测评分位于第一分值与第二分值之间且肝评估参数不低于第四分值时,肝纤维化发生程度为已发生肝纤维化,也就是该待评估者已经为进展期纤维化或肝硬化;当第一预测评分位于第一分值与第二分值之间且肝评估参数位于第三分值与第四分值之间时,肝纤维化发生程度为需要进行肝活检以此明确其肝纤维化具体的发生程度。
28.其中,第二分值的数值超过第一分值的数值,第四分值的数值超过第三分值的数值。
29.当第二预测评分不超过第五分值时,肝纤维化发生程度为未发生肝纤维化;当第二预测评分不低于第六分值时,肝纤维化发生程度为已发生肝纤维化;当第二预测评分位于第五分值与第六分值时,肝纤维化发生程度为需要进行肝活检以此明确其肝纤维化具体的发生程度。
30.其中,第六分值的数值超过第五分值的数值。
31.本发明的无创肝纤维化评估装置,通过将已确定的肝指标信息输入至已训练好的无创肝纤维化评估模型,并基于无创肝纤维化评估模型输出的预测评分确定待评估者对应的肝纤维化发生程度,以此进行待评估者无创以及非侵入性肝纤维化的评估,其中第一无创肝纤维化评估模型通过序贯应用amap评分和lsm,在不增加额外经济负担的情况下,提高肝纤维化的评估效能,并且进一步减少肝活检需求,基于逻辑回归构建的第二无创肝纤维化评估模型针对接受抗病毒治疗的慢乙肝患者,尤其是抗病毒治疗后lsm值出现明显下降的这部分患者,可以很好的弥补lsm在此类患者中评估效能不佳的缺陷,基于第一、第二无创肝纤维化评估模型确定的肝纤维化发生程度更加准确,作为辅助信息能够帮助医生进行更加准确的肝纤维化诊断。
32.如图3所示,在本实施例中提供了一种无创肝纤维化评估装置,本发明实施例的无创肝纤维化评估可用于电子设备中,图3是根据本发明实施例的无创肝纤维化评估装置的结构示意图,如图3所示,上述的第一无创肝纤维化评估模型通过以下模块训练得到:第一训练模块100、确定样本评估者对应的样本肝指标信息。本发明实施例共选取了2999例样本评估者,包括2053例慢乙肝患者(chb组)和946例非酒精性脂肪肝患者(nafld组),所有患者均接受了肝活检检查。chb患者中有889例在基线行肝活检后接受了为期72或104周的抗乙肝病毒治疗(chb纵向研究组),并在相应的治疗时间点接受了第二次肝活检。需要说明的是,选取的样本评估者需要排除以下情况的患者:未成年、肝癌或其他恶性肿瘤、失代偿肝硬化、其他肝炎病毒或人类免疫缺陷病毒感染、其他肝病(酒精相关性肝病、自身免疫性肝病、药物性肝病等)。
33.第三训练模块300,用于将样本肝指标信息输入至血清评估模型中,得到血清评估
模型输出的第一样本评分,具体的,第一样本评分的计算方式为:amap= ({0.06
ꢀ×
样本年龄 + 0.89
ꢀ×
样本性别 (男性: 1;女性: 0) + 0.48
ꢀ×ꢀ
[(log
10
样本tbil
ꢀ×ꢀ
0.66) + (样本alb
ꢀ×ꢀ‑
0.085)]
ꢀ‑ꢀ
0.01
ꢀ×
样本plt)} + 7.4)/14.77
ꢀ×ꢀ
100即,基于血清评估模型对应的第一评估因子和样本肝指标信息中的样本白蛋白、样本总胆红素以及样本血小板计数,得到血清评估模型输出的第一样本评分。
[0034]
可以理解的是,上式中0.06、0.89、0.48、0.66、-0.085、0.01、7.4、14.77以及100都是amap评分模型相应的第一评估因子。
[0035]
第四训练模块400,用于确定第一样本评分对应的第一特征曲线下面积(area under the receiver operating characteristic curve,auroc)值,并基于灵敏度、特异性以及第一特征曲线下面积值,确定血清评估模型对应的第一界值以及第二界值,在本发明实施例中,第一界值对应第一分值,第二界值对应第二分值。
[0036]
第五训练模块500,用于确定肝评估参数对应的第二特征曲线下面积值,并基于灵敏度、特异性以及第二特征曲线下面积值,确定肝评估参数对应的第三界值以及第四界值,在本发明实施例中,第三界值对应第三分值,第四界值对应第四分值。
[0037]
第四训练模块400和第五训练模块500中会利用auroc分析amap评分模型以及lsm在进展期纤维化和肝硬化评估方面的总体性能,通过delong测试对auroc进行比较,优选的该步骤中统计显著性水平设为p《0.05。auroc分析是利用amap评分模型的预测值或者lsm具体数值与肝活检病理评估进行分析,以此计算得到对应的auroc值。在auroc上,以灵敏度、特异性对应的取值作为amap评分模型和lsm的双重评估界值,amap评分模型对应的双重评估界值即为第一界值以及第二界值,其中第一界值对应第一分值,第二界值对应第二分值,lsm值对应的双重评估界值即为第三界值以及第四界值,其中第三界值对应第三分值,第四界值对应第四分值。
[0038]
现有技术中的无创评估模型多使用单个界值用于评估肝纤维化,以至于评估准确性不高,容易出现漏诊或误诊。本发明实施例中所提供的评估装置均选取双重界值,尽管有小部分患者不能明确评估,但双重界值的评估准确性更高,极少数患者被漏诊,从而避免了漏诊导致的严重后果。
[0039]
在本发明实施例的另一些可能实施方式中,lsm值的的双重评估界值的具体取值还将参考既往文献研究中提供的界值。
[0040]
第六训练模块600,用于基于血清评估模型以及对应的第一界值、第二界值、肝评估参数以及对应的第三界值、第四界值构建第一无创肝纤维化评估模型。
[0041]
第一无创肝纤维化评估模型具体为所有待评估者先利用血清评估模型进行进展期纤维化或肝硬化的相关评估,血清评估模型输出第一预测评分(与计算第一样本评分的方式和过程均一致),位于血清评估模型不确定区域(第一分值至第二分值之间)的患者则利用lsm值进行进一步进行评估,由此形成第一无创肝纤维化评估模型,也即,当第一预测评分不超过第一分值以及预测评分位于第一分值与第二分值之间且肝评估参数不超过第三分值时,肝纤维化发生程度为未发生肝纤维化,也就是该待评估者可以排除进展期纤维化或肝硬化;当第一预测评分不低于第二分值以及预测评分位于第一分值与第二分值之间且肝评估参数不低于第四分值时,肝纤维化发生程度为已发生肝纤维化,也就是该待评估
者已经为进展期纤维化或肝硬化;当第一预测评分位于第一分值与第二分值之间且肝评估参数位于第三分值与第四分值之间时,肝纤维化发生程度为需要进行肝活检以此明确其肝纤维化具体的发生程度。
[0042]
在本发明实施例的一些可能实施方式中,amap评分是在一定程度上能够反映肝细胞癌发展潜在风险的指标,amap评分是在考虑到大多数肝细胞癌是在肝硬化基础上研究并发展起来的,并且amap评分中涉及的几个参数与肝纤维化相关,在本发明实施例中,血清评估模型除了选取风险预测模型(amap评分模型)外,还会对照地选取fib-4模型以及apri模型,通过比较分析这三种血清评估模型在进展期纤维化和肝硬化评估方面的总体性能,以此验证并确定amap评分模型的评估效果以及准确性。在上述实施例中,fib-4模型以及apri模型同样是基于样本肝指标信息训练得到的,区别在于fib-4模型对应的第三样本评分、第七界值和第八界值(fib-4模型对应的双重评估界值)、apri模型对应的第四样本评分、第二评估因子、第九界值和第十界值(apri模型对应的双重评估界值)与amap评分模型有所差异。
[0043]
具体的,第三样本评分的计算方式为:fib-4= 样本年龄
×
样本ast/样本plt
ꢀ×
样本alt
1/2
第四样本评分的计算方式为:apri= (样本ast/ast上限值)
×ꢀ
100/样本plt可以理解的是,上式中100是apri模型相应的第二评估因子。
[0044]
因此,在本发明实施例中利用auroc分析比较amap、fib-4、apri和lsm在进展期纤维化和肝硬化评估方面的总体性能,通过delong测试对auroc进行比较,计算得出对应模型以及lsm值的auroc值。
[0045]
优选的,上述的灵敏度、特异性可以选取90%或者95%。
[0046]
最终选取的每个血清评估模型和lsm的评估界值具体为:对于慢性乙型肝炎病毒感染待评估者组(chb组),amap在进展期纤维化评估方面的下界值为40.50,amap在进展期纤维化评估方面的上界值为58.50,amap在肝硬化评估方面的下界值为42.50,amap在肝硬化评估方面的上界值为59.00,fib-4在进展期纤维化评估方面的下界值为0.6,fib-4在进展期纤维化评估方面的上界值为2.90,fib-4在肝硬化评估方面的下界值为0.65,fib-4在肝硬化评估方面的上界值为3.30,apri在进展期纤维化评估方面的下界值为0.26,apri在进展期纤维化评估方面的上界值为2.50,apri在肝硬化评估方面的下界值为0.30,apri在肝硬化评估方面的上界值为2.80,lsm在进展期纤维化评估方面的下界值为6.00,lsm在进展期纤维化评估方面的上界值为16.00,lsm在肝硬化评估方面的下界值为8.50,lsm在肝硬化评估方面的上界值为19.50,amap-lsm在进展期纤维化评估方面的下界值为26.50,amap-lsm在进展期纤维化评估方面的上界值为64.10,amap-lsm在肝硬化评估方面的下界值为20.70,amap-lsm在肝硬化评估方面的上界值为52.00;对于非酒精性脂肪肝患待评估者(nafld组),amap在进展期纤维化评估方面的下界值为41.00,amap在进展期纤维化评估方面的上界值为57.50,amap在肝硬化评估方面的下界值为47.50,amap在肝硬化评估方面的上界值为58.50,fib-4在进展期纤维化评估方面的下界值为0.62,fib-4在进展期纤维化评估方面的上界值为2.30,fib-4在肝硬化评估方面的下界值为0.95,fib-4在肝硬化评估方面的上界值为2.70,apri在进展期纤维化评估方面的下界值为0.28,apri在进展期纤维化
评估方面的上界值为1.28,apri在肝硬化评估方面的下界值为0.29,apri在肝硬化评估方面的上界值为1.30,lsm在进展期纤维化评估方面的下界值为8.00,lsm在进展期纤维化评估方面的上界值为14.50,lsm在肝硬化评估方面的下界值为11.60,apri在肝硬化评估方面的上界值为17.00。
[0047]
其中,下界值表示双重评估界值中的较小值,上界值则表示双重评估界值中的较大值。
[0048]
更进一步的,若通过血清评估模型计算得到的评分不超过下界值则排除进展期纤维化或肝硬化,不低于上界值则评估为进展期纤维化或肝硬化,介于双重界值之间的患者将纳入不确定区域,说明后续需要进行肝活检明确肝纤维化程度。上述实施例中还会计算并比较三种血清评估模型的不确定区域大小(不确定区域患者人数
÷
总人数
×
100%)以及评估的准确性((≥上界值中对比肝活检结果评估正确的患者人数+≤下界值中对比肝活检结果评估正确的人数)
÷
(总人数-不确定区域人数))。
[0049]
为尽可能地减小不确定区域,本发明实施例中会将血清评估模型与lsm序贯应用,即,所有患者先利用血清模型进行进展期纤维化或肝硬化评估,位于血清评估模型不确定区域的患者将利用lsm进一步进行评估,由此形成amap-lsm、fib-4-lsm、apri-lsm三种序贯装置,计算并比较三种序贯装置的最终不确定区域大小以及评估的准确性。
[0050]
进行相关分析后得出的结论为:amap评分适用于评估慢性肝病患者的进展期纤维化和肝硬化,在总体评估效能方面,amap评分的auroc与fib-4的auroc是相当的,二者之间的差异没有统计学意义,且amap评分auroc明显优于apri的auroc。
[0051]
需要说明的是,在本发明实施例中,在同样的取值标准下,amap评分的双重界值(对应amap评分的第一界值和第二界值)适用于评估或排除进展期纤维化、肝硬化的效能优于fib-4和apri,amap评分具有更小的不确定区域,可以确保更多的患者免于肝活检,并且评估准确性较高。当血清模型与lsm序贯应用时,amap-lsm序贯装置的评估效能同样优于fib-4-lsm和apri-lsm这两种序贯装置,其不确定区域更小,评估准确性更高。
[0052]
如图4所示,在本实施例中提供了一种无创肝纤维化评估装置,本发明实施例的无创肝纤维化评估可用于电子设备中,图4是根据本发明实施例的无创肝纤维化评估装置的流程示意图,如图4所示,上述的无创肝纤维化评估模型还通过以下模块训练得到:第一训练模块100,用于确定样本评估者对应的样本肝指标信息。
[0053]
第二训练模块200,用于基于样本肝指标信息对所述样本评估者进行分组,例如,以alt《40,40-100,》100,ast《40,40-100,》100为标准,分别将chb组和nafld组患者进行分组,共产生12个亚组。
[0054]
第三训练模块300,用于将分组后的样本肝指标信息输入至血清评估模型中,得到血清评估模型输出的第一样本评分。
[0055]
第四训练模块400,用于确定第一样本评分对应的第一特征曲线下面积值,并基于灵敏度、特异性以及第一特征曲线下面积值,确定血清评估模型对应的第一界值以及第二界值,在本发明实施例中,第一界值对应第一分值,第二界值对应第二分值。
[0056]
第五训练模块500,用于确定肝评估参数对应的第二特征曲线下面积值,并基于灵敏度、特异性以及第二特征曲线下面积值,确定肝评估参数对应的第三界值以及第四界值,在本发明实施例中,第三界值对应第三分值,第四界值对应第四分值。
[0057]
第六训练模块600,用于基于血清评估模型以及对应的第一界值、第二界值、肝评估参数以及对应的第三界值、第四界值构建第一无创肝纤维化评估模型。
[0058]
通过相关的实验数据表明,在本发明实施例中,其中,对于不同alt或ast水平的亚组,在alt》100和ast》100的患者中,amap评分模型和amap-lsm序贯装置比fiib-4、apri及其与lsm的序贯装置的不确定区域更小,评估准确性更高,因此,amap评分相比fib-4和apri更适合肝脏炎症活动的患者的纤维化评估。
[0059]
如图5所示,在本实施例中提供了一种无创肝纤维化评估装置,本发明实施例的无创肝纤维化评估可用于电子设备中,图5是根据本发明实施例的无创肝纤维化评估装置的流程示意图,如图5所示,上述的第二无创肝纤维化评估模型通过以下模块训练得到:第七训练模块700,用于确定样本评估者对应的样本肝指标信息。
[0060]
第七训练模块700详细请参见如图3所示实施例的第一训练模块100,在此不作过多赘述。
[0061]
第八训练模块800,用于将抗病毒治疗后的进展期纤维化以及肝硬化作为因变量,年龄、性别、样本评估者治疗前及治疗后的第一样本评分、肝指标信息作为自变量,采用单因逻辑回归分析对自变量进行分析,确定自变量中的预测因子。具体的,可以将p《0.05的自变量可作为进展期纤维化或肝硬化的预测因子,并参与多因素二元逻辑回归分析。
[0062]
在本发明实施例的一些可能实施例中,血清评估模型除了选取风险预测模型(amap评分模型)外,还会对照地选取fib-4模型以及apri模型时,自变量还需要包括对应的第三样本评分、第四样本评分。
[0063]
第八训练模块800的目的是选取效果更佳的可作为进展期纤维化或肝硬化的预测因子,并参与多因素(二元)逻辑回归分析。
[0064]
以血清评估模型选用了amap评分模型并且对照地选取fib-4模型以及apri模型为例进行说明,最终确定得到的预测因子有:年龄、amap
治疗前
、amap
治疗后
、fib-4
治疗前
、fib-4
治疗后
、apri
治疗前
、apri
治疗后
、lsm
治疗前
、lsm
治疗后
、alt
治疗前
、alt
治疗后
、ast
治疗后
、alb
治疗前
、alb
治疗后
、tbil
治疗后
、plt
治疗前
、alt
治疗后
。
[0065]
第九训练模块900,用于采用多因素逻辑回归分析对预测因子进行分析,确定预测因子中的独立预测因子。
[0066]
利用多因素二元逻辑回归分析对上述预测因子进行分析,以获取独立预测因子,以及独立预测因子的回归系数和本次回归分析的常数项。需要说明的是,由于amap评分、fib-4、apri三种血清评估模型中部分指标相同,因此三者不同时参与回归分析过程,且已包含在三种血清评估模型中的血清指标也不参与血清评估模型的回归分析。
[0067]
第九训练模块900的目的是选取效果更佳的可作为进展期纤维化或肝硬化的独立预测因子,并参与之后的构建无创肝纤维化评估模型。
[0068]
第十训练模块1000,用于确定独立预测因子对应的回归系数以及回归常数,并基于独立预测因子、回归系数以及回归常数构建回归模型。
[0069]
第十一训练模块1100,用于将样本肝指标信息输入至回归模型中,得到回归模型输出的第二样本评分。
[0070]
第十二训练模块1200,用于确定第二样本评分对应的第三特征曲线下面积值,并基于灵敏度、特异性以及第三特征曲线下面积值,确定回归模型对应的第五界值以及第六
界值。
[0071]
第十三训练模块1300,用于基于回归模型以及对应的第五界值、第六界值构建第二无创肝纤维化评估模型。
[0072]
最终得到amap-lsm、fib-4-lsm、apri-lsm三种回归模型,计算上述模型的auroc并与lsm做比较,其中,amap-lsm回归模型也就是第二无创肝纤维化评估模型其对应的auroc值最高,amap-lsm回归模型其评估治疗后进展期纤维化或肝硬化的计算方式为:amap-lsm
肝硬化
= (0.085
ꢀ×
amap
治疗前 +0.049
ꢀ×
amap
治疗后 +0.214
ꢀ×
lsm
治疗后
ꢀ‑
9.023)
ꢀ×
100amap-lsm
进展期纤维化
= (0.079
ꢀ×
amap
治疗前 +0.057
ꢀ×
amap
治疗后
+0.289
ꢀ×
lsm
治疗后
ꢀ‑
8.831)
ꢀ×
100用amap评分和lsm构建的amap-lsm回归模型,在抗病毒治疗后的慢乙肝患者,尤其是lsm显著下降的慢乙肝患者中,评估进展期纤维化和肝硬化方面的auroc较高,且明显高于lsm的单独应用,同时该amap-lsm回归模型的双重界值(对应该amap-lsm回归模型的第五界值和第六界值)在评估肝纤维化方面同样表现出色,也就是说,该amap-lsm回归模型可以有效弥补lsm在此类患者中评估效能降低的缺陷。
[0073]
在本发明实施例的另一些可能实施方式中,得到amap-lsm、fib-4-lsm、apri-lsm三种回归模型后,还会确定amap-lsm回归模型的双重界值,计算amap-lsm回归模型的不确定区域大小以及评估的准确性。
[0074]
具体的是通过比较chb纵向研究组中患者治疗前和治疗后的lsm值,根据是否出现明显变化将患者分为三个亚组:lsm明显下降组、lsm无明显变化组、lsm明显上升组。lsm明显变化的定义是治疗后lsm值较治疗前的改变值超过治疗前lsm值的30%。在三个亚组中分别计算并比较amap-lsm回归模型和lsm的auroc、不确定区域和评估准确性。
[0075]
以上所描述的装置实施例仅仅是示意性的,其中所述作为分离部件说明的单元可以是或者也可以不是物理上分开的,作为单元显示的部件可以是或者也可以不是物理单元,即可以位于一个地方,或者也可以分布到多个网络单元上。可以根据实际的需要选择其中的部分或者全部模块来实现本实施例方案的目的。本领域普通技术人员在不付出创造性的劳动的情况下,即可以理解并实施。
[0076]
最后应说明的是:以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1