聚糖治疗剂和治疗方法与流程
背景技术:
1、维持或恢复人体健康面临着大量的难题,很多难题都是由缺乏有效的治疗选项而导致的。持续需要新颖的疗法和治疗方案。
技术实现思路
1、本文提供聚糖治疗剂制剂和其药物组合物、医疗食品以及膳食补充剂,以及发现可有效治疗多种疾病、病症或病理病况的相关方法。
2、在第一方面中,本发明涉及治疗人类受试者的免疫失衡的方法。本文提供了一种治疗人类受试者的免疫失衡的方法,包含:给予受试者包含有效量的聚糖治疗剂制剂的药物组合物、医疗食品或膳食补充剂来治疗受试者。本文提供了一种治疗人类受试者的免疫失衡的方法,包含:给予受试者包含聚糖治疗剂制剂的第一药剂,任选地与第二药剂或疗法组合。在一个实施例中,第一药剂是药物组合物。在一个实施例中,第一药剂是医疗食品。在一个实施例中,第一药剂是膳食补充剂。在一个实施例中,第二药剂是免疫调节剂。在一个实施例中,第二药剂或疗法治疗受试者的第二疾病、病症或病理病况。在一个实施例中,第一药剂和第二药剂按用于治疗免疫失衡的有效量给予。在一个实施例中,第一药剂按用于治疗受试者的免疫失衡的有效量给予,第二药剂按用于治疗受试者的第二疾病、病症或病理病况的有效量给予。在一个实施例中,第二药剂是膳食纤维。在一个实施例中,第二药剂是益生菌。在一个实施例中,将组合给予已治疗过免疫失衡的受试者。在一个实施例中,将组合给予尚未治疗过免疫失衡的受试者。在一个实施例中,将第一药剂给予已用第二药剂治疗过的受试者。在一个实施例中,将第二药剂给予已用第一药剂治疗过的受试者。在一个实施例中,将第一药剂和第二药剂同时给予受试者。
3、本文提供一种用于减少有免疫失衡的受试者的感染和/或炎症的方法,所述方法包给予受试者有效量的聚糖治疗剂制剂来减少感染和/或炎症。
4、本文提供一种调节有免疫失衡的受试者的肠道细菌群落的组成和/或代谢活动的方法,包含给予受试者可有效调节受试者的免疫系统的量的聚糖治疗剂组合物和任选地抗炎剂或促炎剂。在一个实施例中,方法进一步包含给予益生微生物。在一个实施例中,调节短链脂肪酸(short-chain fatty acid,scfa)。在一个实施例中,scfa是乙酸盐、丙酸盐、丁酸盐、异戊酸盐、戊酸盐、己酸盐、庚酸盐以及辛酸盐中的一个或多个。在一个实施例中,减少一种或多种scfa。在一些实施例中,增加一种或多种scfa。在一个实施例中,给予组合物来调节(例如刺激)肠有益菌的生长或活性,肠有益菌例如双歧杆菌属(bifidobacteria)。在一个实施例中,给予聚糖治疗剂制剂来调节一个或多个细菌分类群的生长或功能,这一个或多个细菌分类群包括双歧杆菌属、双歧杆菌目(bifidobacteriales)、拟杆菌目(bacteroidales)、梭菌目(clostridiales)、副拟杆菌属(parabacteroides)以及阿克曼氏菌属(akkermansia)。在一个实施例中,给予聚糖治疗剂制剂来调节一个或多个细菌分类群的生长或功能,这一个或多个细菌分类群包括布劳特氏菌属(blautia)、双歧杆菌属(bifidobacterium)、罗斯氏菌属(roseburia)、粪球菌属(coprococcus)、毛螺菌科(lachnospiraceae)、粪栖杆菌属(faecalibacterium)、副拟杆菌属以及瘤胃球菌科(ruminococcaceae)。在一个实施例中,调节一个或多个宿主通路,包括炎症反应、补体、凋亡、抗原呈递、氧化应激、细胞粘附、细胞骨架重塑、notch信号传导、wnt信号传导和/或表19中所列的代谢通路中的一个或多个(超级通路或子通路或代谢物水平)。在一个实施例中,调节一种或多种胆汁酸。在一个实施例中,胆汁酸是初级胆汁酸。在一个实施例中,胆汁酸是次级胆汁酸。在一个实施例中,胆汁酸是甘氨脱氧胆酸、甘氨石胆酸、α-鼠胆酸、β-鼠胆酸、牛磺胆酸以及牛磺鹅脱氧胆酸(taurochenodeoxycholic acid)中的一个或多个。在一个实施例中,胆汁酸是脱氧胆酸(deoxycholic acid,dca)和/或石胆酸(lithocholicacid,lca)。在一个实施例中,增加胆汁酸。在一个实施例中,减少胆汁酸。在一个实施例中,组合物的给予引起了对一种或多种生物标志物的调节,这一种或多种生物标志物包括白细胞介素10、白细胞介素4、白细胞介素13以及白细胞介素35。在一个实施例中,组合物的给予引起了对一种或多种生物标志物的调节,这一种或多种生物标志物包括c-反应蛋白、白细胞介素-6、白细胞介素-8、白细胞介素-18、胰岛素、血糖、瘦素、血清淀粉样蛋白a、血清淀粉样蛋白p以及肿瘤坏死因子-α。在一个实施例中,调节选自以下的一个或多个细胞因子:tnf-α、il-8、单核细胞趋化蛋白1(monocyte chemoattracting protein 1,mcp-1)、tgf-β、il-12、ifn-γ、il-4以及il-10。在一个实施例中,组合物的给予引起了i)免疫反应减弱或ii)免疫反应增强。在一个实施例中,减少促炎性细胞因子的产生或释放。在一个实施例中,增加促炎性细胞因子的产生或释放。在一个实施例中,增加抗炎性细胞因子的产生或释放。在一个实施例中,减少抗炎性细胞因子的产生或释放。
5、本文提供一种调节有免疫失衡的受试者的通路的功能和/或活性的方法,包含给予受试者聚糖治疗剂组合物和任选地第二药剂。在一个实施例中,调节短链脂肪酸(scfa)。在一个实施例中,scfa是乙酸盐、丙酸盐、丁酸盐、异戊酸盐、戊酸盐、己酸盐、庚酸盐以及辛酸盐中的一个或多个。在一个实施例中,减少一种或多种scfa。在一些实施例中,增加一种或多种scfa。在一个实施例中,调节一个或多个通路,包括炎症反应、补体、凋亡、抗原呈递、氧化应激、细胞粘附、细胞骨架重塑、notch信号传导、wnt信号传导和/或表19中所列的代谢通路中的一个或多个(超级通路或子通路或代谢物水平)。在一个实施例中,调节一种或多种胆汁酸。在一个实施例中,胆汁酸是初级胆汁酸。在一个实施例中,胆汁酸是次级胆汁酸。在一个实施例中,胆汁酸是甘氨脱氧胆酸、甘氨石胆酸、α-鼠胆酸、β-鼠胆酸、牛磺胆酸以及牛磺鹅脱氧胆酸中的一个或多个。在一个实施例中,胆汁酸是脱氧胆酸(dca)和/或石胆酸(lca)。在一个实施例中,增加胆汁酸。在一个实施例中,减少胆汁酸。
6、本文提供一种治疗有免疫失衡的受试者的生态失调的方法,包含给予受试者包含有效量的聚糖治疗剂制剂的药物组合物来治疗生态失调。
7、对于以上方法中的任一种和所有方法来说,在一个实施例中,免疫失衡是受试者的免疫系统的抑制。在一个实施例中,受试者展现有缺陷的免疫监视。在一个实施例中,受试者有病原性感染。在一个实施例中,受试者有癌症。在一个实施例中,免疫失衡是受试者的免疫系统的异常活化。在一个实施例中,受试者有炎症性疾病,炎症性疾病提高了患癌症的风险。在一个实施例中,受试者有移植物抗宿主病。在一个实施例中,受试者有自身免疫疾病。在一个实施例中,受试者有炎症性胃肠道疾病。在一个实施例中,免疫失衡是急性的。在一个实施例中,免疫失衡是慢性的。在一个实施例中,免疫失衡是局部的。在一个实施例中,免疫失衡是全身性的。在一个实施例中,免疫失衡伴随着病原性细胞的异常生长。在一个实施例中,病原性细胞是胞内病原体、胞外病原体或癌细胞。
8、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)聚糖治疗剂制剂所具有的平均支化度(degree of branching,db)是至少0.01,iv)制剂中的聚糖的至少50%所具有的聚合度(degree of polymerization,dp)是至少3个并且小于30个聚糖单元,v)制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率大体上在约1:1到约5:1之间,或vi)i)、ii)、iii)、iv)以及v)中的一个、两个、三个、四个或五个的任何组合。
9、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)支化寡糖包含葡萄糖、半乳糖、阿拉伯糖、甘露糖、果糖、木糖、岩藻糖或鼠李糖聚糖单元,iv)聚糖治疗剂制剂中的支化聚糖的平均支化度(db)在0.01与0.3之间,v)聚糖治疗剂制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,vi)聚糖治疗剂制剂的平均dp在约dp6与约dp10之间,vii)聚糖治疗剂制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率在约1:1到约5:1之间,viii)聚糖治疗剂制剂在23℃下在水中所具有的最终溶解度极限是至少约60白利度(brix),或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
10、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含一个或多个聚糖单元,iii)支化聚糖包含至少1%的支化聚糖单元,iv)支化聚糖所具有的聚合度(dp)在2个与30个聚糖单元之间,v)支化聚糖具有1:1、1:2、1:3、1:4或1:5的β构型:α构型,vi)支化聚糖包含(1-2)、(1-3)、(1-4)、(1-6)、(2-3)以及(2-6)中的一个或多个的β键与α键的混合物,vii)聚糖治疗剂制剂包含支化聚糖与未支化聚糖的混合物,viii)聚糖治疗剂制剂包含易消化的聚糖与不易消化的聚糖的混合物,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
11、在第二方面中,本发明涉及治疗人类受试者的营养失衡的方法。本文提供了一种治疗人类受试者的营养失衡的方法,包含:给予受试者包含有效量的聚糖治疗剂制剂的药物组合物、医疗食品或膳食补充剂来治疗受试者。
12、本文提供一种治疗人类受试者的营养失衡的方法,包含:给予受试者包含聚糖治疗剂制剂的第一药剂,任选地与第二药剂或疗法组合。在一个实施例中,第一药剂是药物组合物。在一个实施例中,第一药剂是医疗食品。在一个实施例中,第一药剂是膳食补充剂。在一个实施例中,第二药剂是代谢调节剂。在一个实施例中,第二药剂或疗法治疗受试者的第二疾病、病症或病理病况。在一个实施例中,第一药剂和第二药剂按用于治疗营养失衡的有效量给予。在一个实施例中,第一药剂按用于治疗受试者的营养失衡的有效量给予,第二药剂按用于治疗受试者的第二疾病、病症或病理病况的有效量给予。在一个实施例中,第二药剂是膳食纤维。在一个实施例中,第二药剂是益生菌。在一个实施例中,将组合给予已治疗过营养失衡的受试者。在一个实施例中,将组合给予尚未治疗过营养失衡的受试者。在一个实施例中,将第一药剂给予已用第二药剂治疗过的受试者。在一个实施例中,将第二药剂给予已用第一药剂治疗过的受试者。在一个实施例中,将第一药剂和第二药剂同时给予受试者。
13、本文提供一种用于减少有营养失衡的受试者的炎症的方法,方法包含给予受试者有效量的聚糖治疗剂制剂来减少炎症。
14、本文提供一种调节有营养失衡的受试者的肠道细菌群落的组成和/或代谢活动的方法,包含给予受试者可有效调节受试者的免疫系统的量的聚糖治疗剂组合物和抗炎剂或促炎剂。在一个实施例中,方法进一步包含给予益生微生物。在一个实施例中,调节短链脂肪酸(scfa)。在一个实施例中,scfa是乙酸盐、丙酸盐、丁酸盐、异戊酸盐、戊酸盐、己酸盐、庚酸盐以及辛酸盐中的一个或多个。在一个实施例中,减少一种或多种scfa。在一些实施例中,增加一种或多种scfa。在一个实施例中,给予组合物来调节(例如刺激)肠有益菌的生长或活性,肠有益菌例如双歧杆菌属。在一个实施例中,给予聚糖治疗剂制剂来调节一个或多个细菌分类群的生长或功能,这一个或多个细菌分类群包括双歧杆菌属、双歧杆菌目、拟杆菌目、梭菌目、副拟杆菌属以及阿克曼氏菌属。在一个实施例中,给予聚糖治疗剂制剂来调节一个或多个细菌分类群的生长或功能,这一个或多个细菌分类群包括布劳特氏菌属、双歧杆菌属、罗斯氏菌属、粪球菌属、毛螺菌科、粪栖杆菌属、副拟杆菌属以及瘤胃球菌科。在一个实施例中,调节一个或多个宿主通路,包括炎症反应、补体、凋亡、抗原呈递、氧化应激、细胞粘附、细胞骨架重塑、notch信号传导、wnt信号传导和/或表19中所列的代谢通路中的一个或多个(超级通路或子通路或代谢物水平)。在一个实施例中,调节一种或多种胆汁酸。在一个实施例中,胆汁酸是初级胆汁酸。在一个实施例中,胆汁酸是次级胆汁酸。在一个实施例中,胆汁酸是甘氨脱氧胆酸、甘氨石胆酸、α-鼠胆酸、β-鼠胆酸、牛磺胆酸以及牛磺鹅脱氧胆酸中的一个或多个。在一个实施例中,胆汁酸是脱氧胆酸(dca)和/或石胆酸(lca)。在一个实施例中,增加胆汁酸。在一个实施例中,减少胆汁酸。在一个实施例中,组合物的给予引起了对一种或多种生物标志物的调节,这一种或多种生物标志物包括白细胞介素10、白细胞介素4、白细胞介素13以及白细胞介素35。在一个实施例中,组合物的给予引起了对一种或多种生物标志物的调节,这一种或多种生物标志物包括c-反应蛋白、白细胞介素-6、白细胞介素-8、白细胞介素-18、胰岛素、血糖、瘦素、血清淀粉样蛋白a、血清淀粉样蛋白p以及肿瘤坏死因子-α。在一个实施例中,调节选自tnf-α、il-8、单核细胞趋化蛋白1(mcp-1)、tgf-β、il-12、ifn-γ、il-4以及il-10的一个或多个细胞因子。在一个实施例中,组合物的给予引起了i)免疫反应减弱或ii)免疫反应增强。在一个实施例中,减少促炎性细胞因子的产生或释放。在一个实施例中,增加促炎性细胞因子的产生或释放。在一个实施例中,增加抗炎性细胞因子的产生或释放。在一个实施例中,减少抗炎性细胞因子的产生或释放。
15、本文提供一种调节有营养失衡的受试者的通路的功能和/或活性的方法,包含给予受试者聚糖治疗剂组合物和任选地第二药剂。在一个实施例中,调节短链脂肪酸(scfa)。在一个实施例中,scfa是乙酸盐、丙酸盐、丁酸盐、异戊酸盐、戊酸盐、己酸盐、庚酸盐以及辛酸盐中的一个或多个。在一个实施例中,减少一种或多种scfa。在一些实施例中,增加一种或多种scfa。在一个实施例中,调节一个或多个通路,包括炎症反应、补体、凋亡、抗原呈递、氧化应激、细胞粘附、细胞骨架重塑、notch信号传导、wnt信号传导和/或表19中所列的代谢通路中的一个或多个(超级通路或子通路或代谢物水平)。在一个实施例中,调节一种或多种胆汁酸。在一个实施例中,胆汁酸是初级胆汁酸。在一个实施例中,胆汁酸是次级胆汁酸。在一个实施例中,胆汁酸是甘氨脱氧胆酸、甘氨石胆酸、α-鼠胆酸、β-鼠胆酸、牛磺胆酸以及牛磺鹅脱氧胆酸中的一个或多个。在一个实施例中,胆汁酸是脱氧胆酸(dca)和/或石胆酸(lca)。在一个实施例中,增加胆汁酸。在一个实施例中,减少胆汁酸。
16、本文提供一种治疗有营养失衡的受试者的生态失调的方法,包含给予受试者包含有效量的聚糖治疗剂制剂的药物组合物来治疗生态失调。
17、对于以上方法中的任一种和所有方法来说,在一个实施例中,营养失衡是急性的。在一个实施例中,营养失衡是慢性的。在一个实施例中,受试者有代谢疾病或综合征。在一个实施例中,受试者有消耗性综合征。在一个实施例中,消耗性综合征是恶病质。在一个实施例中,受试者有癌症。在一个实施例中,癌症是胃肠癌。在一个实施例中,癌症是非胃肠癌。
18、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)聚糖治疗剂制剂所具有的平均支化度(db)是至少0.01,iv)制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,v)制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率大体上在约1:1到约5:1之间,或vi)i)、ii)、iii)、iv)以及v)中的一个、两个、三个、四个或五个的任何组合。
19、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)支化寡糖包含葡萄糖、半乳糖、阿拉伯糖、甘露糖、果糖、木糖、岩藻糖或鼠李糖聚糖单元,iv)聚糖治疗剂制剂中的支化聚糖的平均支化度(db)在0.01与0.3之间,v)聚糖治疗剂制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,vi)聚糖治疗剂制剂的平均dp在约dp6与约dp10之间,vii)聚糖治疗剂制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率在约1:1到约5:1之间,viii)聚糖治疗剂制剂在23℃下在水中所具有的最终溶解度极限是至少约60白利度,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
20、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含一个或多个聚糖单元,iii)支化聚糖包含至少1%的支化聚糖单元,iv)支化聚糖所具有的聚合度(dp)在2个与30个聚糖单元之间,v)支化聚糖具有1:1、1:2、1:3、1:4或1:5的β构型:α构型,vi)支化聚糖包含(1-2)、(1-3)、(1-4)、(1-6)、(2-3)以及(2-6)中的一个或多个的β键与α键的混合物,vii)聚糖治疗剂制剂包含支化聚糖与未支化聚糖的混合物,viii)聚糖治疗剂制剂包含易消化的聚糖与不易消化的聚糖的混合物,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
21、在第三方面中,本发明涉及治疗人类受试者的癌症的方法。本文提供了一种治疗人类受试者的癌症的方法,包含:给予受试者包含有效量的聚糖治疗剂制剂的药物组合物、医疗食品或膳食补充剂来治疗受试者。
22、本文提供一种治疗人类受试者的癌症的方法,包含:给予受试者包含聚糖治疗剂制剂的第一药剂,任选地与第二药剂或疗法组合。
23、在一个实施例中,第一药剂是药物组合物。在一个实施例中,第一药剂是医疗食品。在一个实施例中,第一药剂是膳食补充剂。在一个实施例中,第二药剂是检查点调节剂、癌症疫苗、抗癌生物制剂或化疗剂。在一个实施例中,免疫检查点抑制剂是抗体、融合蛋白或小分子。在一个实施例中,癌症疫苗是肿瘤细胞疫苗、抗原疫苗、树突状细胞疫苗、dna疫苗或基于载体的疫苗。在一个实施例中,抗癌生物制剂是细胞因子或抗体。在一个实施例中,化疗剂是烷化剂、抗代谢物、叶酸类似物、嘧啶类似物、嘌呤类似物、长春花属生物碱(vinca alkaloid)、表鬼臼毒素(epipodopyyllo toxin)、抗生素、l-天冬酰胺酶、拓扑异构酶(topoisomerase)抑制剂、干扰素、铂配位络合物、蒽二酮取代的脲、甲基肼衍生物、肾上腺皮质抑制剂、肾上腺皮质类固醇、孕激素、雌激素、抗雌激素、雄激素、抗雄激素或促性腺激素释放激素类似物。在一个实施例中,第二疗法是过继t细胞疗法、nk细胞疗法或非药物治疗。在一个实施例中,非药物治疗是放疗、冷冻疗法(cryotherapy)、热疗(hyperthermia)或手术切除肿瘤组织。在一个实施例中,过继t细胞疗法包含给予自体和/或同种异体t细胞。在一个实施例中,第二药剂是膳食纤维。在一个实施例中,第二药剂是益生菌。在一个实施例中,将组合给予已用抗癌疗法治疗过的受试者。在一个实施例中,将组合给予尚未用抗癌疗法治疗的受试者。在一个实施例中,将第一药剂给予已用第二药剂治疗过的受试者。在一个实施例中,将第二药剂给予已用第一药剂治疗过的受试者。在一个实施例中,将第一药剂和第二药剂同时给予受试者。
24、本文提供一种调节有癌症的受试者的肠道细菌群落的组成和/或代谢活动的方法,包含给予受试者可有效调节受试者的免疫系统的量的聚糖治疗剂组合物和抗炎剂或促炎剂。在一个实施例中,方法进一步包含给予抗癌剂。在一个实施例中,方法进一步包含给予益生微生物。在一个实施例中,调节短链脂肪酸(scfa)。在一个实施例中,scfa是乙酸盐、丙酸盐、丁酸盐、异戊酸盐、戊酸盐、己酸盐、庚酸盐以及辛酸盐中的一个或多个。在一个实施例中,减少一种或多种scfa。在一些实施例中,增加一种或多种scfa。在一个实施例中,给予组合物来诱导受试者中的癌细胞和癌前细胞的凋亡。在一个实施例中,给予组合物来调节(例如刺激)肠有益菌的生长或活性,肠有益菌例如双歧杆菌属。在一个实施例中,给予聚糖治疗剂制剂来调节一个或多个细菌分类群的生长或功能,这一个或多个细菌分类群包括双歧杆菌属、双歧杆菌目、拟杆菌目、梭菌目、副拟杆菌属以及阿克曼氏菌属。在一个实施例中,给予聚糖治疗剂制剂来调节一个或多个细菌分类群的生长或功能,这一个或多个细菌分类群包括布劳特氏菌属、双歧杆菌属、罗斯氏菌属、粪球菌属、毛螺菌科、粪栖杆菌属、副拟杆菌属以及瘤胃球菌科。在一个实施例中,调节一个或多个宿主通路,包括炎症反应、补体、凋亡、抗原呈递、氧化应激、细胞粘附、细胞骨架重塑、notch信号传导、wnt信号传导和/或表19中所列的代谢通路中的一个或多个(超级通路或子通路或代谢物水平)。在一个实施例中,调节一种或多种胆汁酸。在一个实施例中,胆汁酸是初级胆汁酸。在一个实施例中,胆汁酸是次级胆汁酸。在一个实施例中,胆汁酸是甘氨脱氧胆酸、甘氨石胆酸、α-鼠胆酸、β-鼠胆酸、牛磺胆酸以及牛磺鹅脱氧胆酸中的一个或多个。在一个实施例中,胆汁酸是脱氧胆酸(dca)和/或石胆酸(lca)。在一个实施例中,增加胆汁酸。在一个实施例中,减少胆汁酸。在一个实施例中,组合物的给予引起了对一种或多种生物标志物的调节,这一种或多种生物标志物包括白细胞介素10、白细胞介素4、白细胞介素13以及白细胞介素35。在一个实施例中,组合物的给予引起了对一种或多种生物标志物的调节,这一种或多种生物标志物包括c-反应蛋白、白细胞介素-6、白细胞介素-8、白细胞介素-18、胰岛素、血糖、瘦素、血清淀粉样蛋白a、血清淀粉样蛋白p以及肿瘤坏死因子-α。在一个实施例中,调节选自tnf-α、il-8、单核细胞趋化蛋白1(mcp-1)、tgf-β、il-12、ifn-γ、il-4以及il-10的一个或多个细胞因子。在一个实施例中,组合物的给予引起了i)肠癌减少,和/或ii)免疫反应增强。在一个实施例中,减少促炎性细胞因子的产生或释放。在一个实施例中,增加抗炎性细胞因子的产生或释放。
25、本文提供一种调节有免疫失衡的受试者的通路的功能和/或活性的方法,包含给予受试者聚糖治疗剂组合物和任选地第二药剂。在一个实施例中,调节短链脂肪酸(scfa)。在一个实施例中,scfa是乙酸盐、丙酸盐、丁酸盐、异戊酸盐、戊酸盐、己酸盐、庚酸盐以及辛酸盐中的一个或多个。在一个实施例中,减少一种或多种scfa。在一些实施例中,增加一种或多种scfa。在一个实施例中,调节一个或多个通路,包括炎症反应、补体、凋亡、抗原呈递、氧化应激、细胞粘附、细胞骨架重塑、notch信号传导、wnt信号传导和/或表19中所列的代谢通路中的一个或多个(超级通路或子通路或代谢物水平)。在一个实施例中,调节一种或多种胆汁酸。在一个实施例中,胆汁酸是初级胆汁酸。在一个实施例中,胆汁酸是次级胆汁酸。在一个实施例中,胆汁酸是甘氨脱氧胆酸、甘氨石胆酸、α-鼠胆酸、β-鼠胆酸、牛磺胆酸以及牛磺鹅脱氧胆酸中的一个或多个。在一个实施例中,胆汁酸是脱氧胆酸(dca)和/或石胆酸(lca)。在一个实施例中,增加胆汁酸。在一个实施例中,减少胆汁酸。
26、本文提供一种治疗有癌症的受试者的生态失调的方法,包含给予受试者包含有效量的聚糖治疗剂制剂的药物组合物来治疗生态失调。在一个实施例中,受试者经历了抗癌疗法。在一个实施例中,癌症疗法。在一个实施例中,癌症疗法是非药物疗法。在一个实施例中,受试者经历了针对癌症疼痛的疼痛管理疗法。在一个实施例中,疼痛管理疗法包含给予阿片类药物(opioids)。在一个实施例中,受试者出现便秘。在一个实施例中,便秘是急性的。在一个实施例中,便秘是慢性的。在一个实施例中,受试者出现腹泻。在一个实施例中,腹泻是急性的。在一个实施例中,腹泻是慢性的。
27、本文提供一种用于减少有癌症的受试者的感染和/或炎症的方法,方法包给予受试者有效量的聚糖治疗剂制剂来减少感染和/或炎症。
28、本文提供一种用于诱导有癌症的受试者中的癌细胞或癌前细胞的凋亡的方法,方法包含给予受试者有效量的聚糖治疗剂制剂来诱导癌细胞或癌前细胞的凋亡。
29、在一个实施例中,癌症是结肠癌或肝癌。在一个实施例中,聚糖治疗剂制剂与另一种药剂或疗法组合给予。在一个实施例中,另一种药剂或疗法选自放疗和化疗以及抗生素疗法。在一个实施例中,另一种药剂选自益生菌、益生元膳食纤维、抗菌剂、抗炎剂或抗癌剂。在一个实施例中,调节选自jun、myc、fos、adamts1、atf3、ddit4、egr1、sox9、il1a、gadd45b或gadd45g的一个或多个基因或基因产物。
30、本文提供一种降低受试者的癌症风险的方法,包含给予受试者有效量的聚糖治疗剂制剂来促进受试者中的健康微生物群,由此降低受试者的癌症风险。
31、在一个实施例中,癌症选自乳癌、卵巢癌、骨肉瘤、子宫颈癌、肺癌、膀胱癌、胰腺癌、前列腺癌或黑素瘤。在一个实施例中,聚糖治疗剂制剂与另一种药剂或疗法组合给予。在一个实施例中,另一种药剂或疗法选自放疗和化疗以及抗生素疗法。在一个实施例中,另一种药剂选自益生菌、益生元膳食纤维、抗菌剂、抗炎剂或抗癌剂。在一个实施例中,健康微生物群包含选自以下的微生物菌种:拟杆菌属(bacteroides)、布劳特氏菌属、梭菌属(clostridium)、梭杆菌属(fusobacterium)、真杆菌属(eubacterium)、瘤胃球菌属(ruminococcus)、消化球菌属(peptococcus)、消化链球菌属(peptostreptococcus)、阿克曼氏菌属、粪栖杆菌属、罗斯氏菌属、普雷沃氏菌属(prevotella)、双歧杆菌属、乳杆菌属(lactobacilli)、小克里斯滕森氏菌(christensenella minuta)或克里斯滕森菌科(christensenellaceae)物种、嗜热链球菌(streptococcus thermophilus)、肠球菌属(enterococcus)和芽孢杆菌属(bacillus)物种、大肠杆菌(e.coli)以及布拉氏酵母菌(sacharomyces boulardii)
32、本文提供一种调节有癌症的受试者的肠道细菌群落的组成的方法,包含给予受试者可有效刺激消化系统中的有益菌的生长的量的聚糖治疗剂制剂和抗癌剂。
33、本文提供一种调节有癌症的受试者的肠道细菌群落的代谢活动的方法,包含给予受试者可有效调节消化系统中的有益菌的代谢活动的量的聚糖治疗剂组合物和抗癌剂。在一个实施例中,代谢活动是表19中所列的代谢活动中的一个或多个(超级通路或子通路或代谢物水平)。在一个实施例中,方法进一步包含给予抗炎剂。在一个实施例中,方法进一步包含给予益生微生物。在一个实施例中,有益菌选自以下中的一个或多个:拟杆菌属、布劳特氏菌属、梭菌属、梭杆菌属、真杆菌属、瘤胃球菌属、消化球菌属、消化链球菌属、阿克曼氏菌属、粪栖杆菌属、罗斯氏菌属、普雷沃氏菌属、双歧杆菌属、乳杆菌属、小克里斯滕森氏菌以及克里斯滕森菌科。在一个实施例中,有益菌包括双歧杆菌属。在一个实施例中,肠有益菌微生物群紊乱。在一个实施例中,癌症是结肠癌或肝癌。
34、在一个实施例中,抑制致癌基因的表达。在一个实施例中,致癌基因是jun、myc和fos中的一个。在一个实施例中,将聚糖治疗剂组合物标记为医疗食品。在一个实施例中,方法进一步包含改变受试者的膳食。在一个实施例中,改变是以下中的一个或多个:i)增加膳食纤维摄入,ii)消除胃肠道刺激物,iii)餐前给予抗胆碱能药物。在一个实施例中,方法进一步包含以下中的一个或多个:i)采取减少焦虑的措施,ii)有规律的锻炼,iii)做焦虑或抑郁方面的咨询。在一个实施例中,方法进一步包含鉴别患gi相关疾病的风险因素,从而诊断gi相关疾病,评定所述疾病的预后或严重程度,评定治疗方案的成效或其任何组合,并且其中gi相关疾病是癌症。在一个实施例中,鉴别风险因素包含从受试者的组织获取受试者的组织样品或微生物培养物的代谢物概况。在一个实施例中,出于诊断、预后风险评估或治疗评估目的,代谢物包括短链脂肪酸、胆汁酸和乳酸盐以及表2中所列的那些。在一个实施例中,胆汁酸是初级胆汁酸。在一个实施例中,胆汁酸是次级胆汁酸。在一个实施例中,胆汁酸是甘氨脱氧胆酸、甘氨石胆酸、α-鼠胆酸、β-鼠胆酸、牛磺胆酸以及牛磺鹅脱氧胆酸中的一个或多个。在一个实施例中,胆汁酸是脱氧胆酸(dca)和/或石胆酸(lca)。在一个实施例中,增加胆汁酸。在一个实施例中,减少胆汁酸。
35、对于以上方法中的任一种和所有方法来说,在一个实施例中,癌症是原发性肿瘤或非转移性肿瘤。在一个实施例中,癌症是转移性肿瘤或转移的肿瘤。在一个实施例中,癌症是实体癌。在一个实施例中,癌症是液体癌(liquid cancer)。在一个实施例中,癌症是免疫原性癌症。在一个实施例中,免疫原性癌症包含以下特征中的一个或多个:(a)肿瘤浸润性淋巴细胞(tumor infiltrating lymphocyte,til),(b)体细胞突变,(c)新抗原(neoantigen),(d)三级淋巴结构,(e)高表达的炎症基因表达,或(f)展现免疫抑制表型的免疫细胞。在一个实施例中,癌症是胃肠癌。在一个实施例中,胃肠癌是结肠直肠癌、胰腺癌、胃癌、食道癌、肝细胞癌、胆管细胞癌、口腔癌或唇癌。在一个实施例中,癌症是非胃肠癌。在一个实施例中,非胃肠癌是泌尿生殖系统癌症、妇科癌症、肺癌、头颈癌、中枢神经系统(central nervous system,cns)癌症、恶性间皮瘤、乳癌、皮肤癌、甲状腺癌、骨与软组织肉瘤或血液学瘤形成。在一个实施例中,泌尿生殖系统癌症是激素敏感性前列腺癌、激素难治性前列腺癌、肾细胞癌、膀胱癌或阴茎癌。在一个实施例中,妇科癌症是卵巢癌、子宫颈癌、子宫内膜癌。在一个实施例中,肺癌是小细胞肺癌或非小细胞肺癌。在一个实施例中,头颈癌是鳞状细胞癌。在一个实施例中,cns癌症是恶性神经胶质瘤、星形细胞瘤、成视网膜细胞瘤或脑转移。在一个实施例中,乳癌是激素难治性转移性乳癌。在一个实施例中,皮肤癌是恶性黑素瘤、基底细胞和鳞状细胞皮肤癌、梅克尔细胞癌(merkel cell carcinoma)、皮肤淋巴瘤或卡波西肉瘤(kaposi sarcoma)。在一个实施例中,血液学瘤形成是多发性骨髓瘤、急性骨髓性白血病、慢性骨髓性白血病、骨髓发育不良综合征、急性成淋巴细胞性白血病或霍奇金氏淋巴瘤(hodgkin's lymphoma)。
36、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)聚糖治疗剂制剂所具有的平均支化度(db)是至少0.01,iv)制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,v)制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率大体上在约1:1到约5:1之间,或vi)i)、ii)、iii)、iv)以及v)中的一个、两个、三个、四个或五个的任何组合。
37、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)支化寡糖包含葡萄糖、半乳糖、阿拉伯糖、甘露糖、果糖、木糖、岩藻糖或鼠李糖聚糖单元,iv)聚糖治疗剂制剂中的支化聚糖的平均支化度(db)在0.01与0.3之间,v)聚糖治疗剂制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,vi)聚糖治疗剂制剂的平均dp在约dp6与约dp10之间,vii)聚糖治疗剂制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率在约1:1到约5:1之间,viii)聚糖治疗剂制剂在23℃下在水中所具有的最终溶解度极限是至少约60白利度,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
38、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含一个或多个聚糖单元,iii)支化聚糖包含至少1%的支化聚糖单元,iv)支化聚糖所具有的聚合度(dp)在2个与30个聚糖单元之间,v)支化聚糖具有1:1、1:2、1:3、1:4或1:5的β构型:α构型,vi)支化聚糖包含(1-2)、(1-3)、(1-4)、(1-6)、(2-3)以及(2-6)中的一个或多个的β键与α键的混合物,vii)聚糖治疗剂制剂包含支化聚糖与未支化聚糖的混合物,viii)聚糖治疗剂制剂包含易消化的聚糖与不易消化的聚糖的混合物,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
39、在第四方面中,本发明涉及用聚糖治疗剂制剂治疗也接受第二治疗或疗法的受试者的方法和选择治疗受试者的方法。本文提供一种治疗受试者的方法,包含:a)给予已用第二治疗或疗法治疗过的受试者包含聚糖治疗剂制剂的药物组合物,b)给予已用包含聚糖治疗剂制剂的药物组合物治疗过的受试者第二治疗或疗法,或c)给予受试者包含聚糖治疗剂制剂的药物组合物和给予第二治疗或疗法。
40、在一个实施例中,治疗或疗法是抗癌治疗或疗法。在一个实施例中,治疗或疗法是针对营养失衡的治疗。在一个实施例中,治疗或疗法是针对免疫失衡的治疗。
41、本文提供一种选择治疗受试者的方法,包含:(a)鉴别有疾病、病症或病理病况的受试者,和(b)选择所鉴别的受试者用聚糖治疗剂制剂进行治疗。
42、在一个实施例中,疾病、病症或病理病况是癌症。在一个实施例中,疾病、病症或病理病况是营养失衡。在一个实施例中,疾病、病症或病理病况是免疫失衡。在一个实施例中,在聚糖治疗剂制剂将提供受试者治疗益处的基础上实施选择步骤。在一个实施例中,在受试者将受益于或预计受益于聚糖治疗剂制剂的给予的基础上实施选择步骤。在一个实施例中,受试者未经过治疗。在一个实施例中,受试者已接受过抗癌治疗或疗法。在一个实施例中,受试者已接受过针对营养失衡的治疗。在一个实施例中,受试者已接受过针对免疫失衡的治疗。在一个实施例中,方法进一步包含评估受试者的胃肠道微生物群。在一个实施例中,在治疗之前、在治疗过程中和/或在治疗之后实施评估。在一个实施例中,用聚糖治疗剂制剂治疗可调节细菌分类群的丰度。在一个实施例中,聚糖治疗剂制剂按可有效引起受试者的胃肠道微生物群中的细菌分类群转变或调节的量和时间给予。在一个实施例中,分类群是双歧杆菌属、拟杆菌属和阿克曼氏菌属。在一个实施例中,分类群是双歧杆菌属、双歧杆菌目、拟杆菌目、梭菌目、副拟杆菌属以及阿克曼氏菌属中的一个或多个。在一个实施例中,分类群是布劳特氏菌属、双歧杆菌属、罗斯氏菌属、粪球菌属、毛螺菌科、粪栖杆菌属、副拟杆菌属以及瘤胃球菌科中的一个或多个。在一个实施例中,治疗引起受试者中的th17或th1细胞水平增加。在一个实施例中,方法进一步包含鉴别患癌症或第二疾病或病症的风险因素,从而诊断癌症或第二疾病或病症,评定癌症或第二疾病或病症的预后或严重程度,评定治疗方案的成效或其任何组合。在一个实施例中,鉴别风险因素包含从受试者的组织获取受试者的组织样品或微生物培养物的代谢物概况。在一个实施例中,出于诊断、预后风险评估或治疗评估目的,代谢物包括短链脂肪酸、胆汁酸和乳酸盐以及表2中所列的代谢物。在一个实施例中,胆汁酸是初级胆汁酸。在一个实施例中,胆汁酸是次级胆汁酸。在一个实施例中,胆汁酸是甘氨脱氧胆酸、甘氨石胆酸、α-鼠胆酸、β-鼠胆酸、牛磺胆酸以及牛磺鹅脱氧胆酸中的一个或多个。在一个实施例中,胆汁酸是脱氧胆酸(dca)和/或石胆酸(lca)。在一个实施例中,增加胆汁酸。在一个实施例中,减少胆汁酸。在一个实施例中,方法进一步包含改变受试者的膳食。在一个实施例中,改变是以下中的一个或多个:i)增加膳食纤维摄入,ii)消除胃肠道刺激物,iii)餐前给予抗胆碱能药物。在一个实施例中,方法进一步包含以下中的一个或多个:i)采取减少焦虑的措施,ii)有规律的锻炼,iii)做焦虑或抑郁方面的咨询。
43、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)聚糖治疗剂制剂所具有的平均支化度(db)是至少0.01,iv)制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,v)制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率大体上在约1:1到约5:1之间,或vi)i)、ii)、iii)、iv)以及v)中的一个、两个、三个、四个或五个的任何组合。
44、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)支化寡糖包含葡萄糖、半乳糖、阿拉伯糖、甘露糖、果糖、木糖、岩藻糖或鼠李糖聚糖单元,iv)聚糖治疗剂制剂中的支化聚糖的平均支化度(db)在0.01与0.3之间,v)聚糖治疗剂制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,vi)聚糖治疗剂制剂的平均dp在约dp6与约dp10之间,vii)聚糖治疗剂制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率在约1:1到约5:1之间,viii)聚糖治疗剂制剂在23℃下在水中所具有的最终溶解度极限是至少约60白利度,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
45、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含一个或多个聚糖单元,iii)支化聚糖包含至少1%的支化聚糖单元,iv)支化聚糖所具有的聚合度(dp)在2个与30个聚糖单元之间,v)支化聚糖具有1:1、1:2、1:3、1:4或1:5的β构型:α构型,vi)支化聚糖包含(1-2)、(1-3)、(1-4)、(1-6)、(2-3)以及(2-6)中的一个或多个的β键与α键的混合物,vii)聚糖治疗剂制剂包含支化聚糖与未支化聚糖的混合物,viii)聚糖治疗剂制剂包含易消化的聚糖与不易消化的聚糖的混合物,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
46、在第五方面中,本发明涉及治疗某种治疗或疗法在人类受试者中的症状的方法,所述症状例如毒性症状。本文提供一种减轻某种治疗或疗法在受试者中的症状的方法,包含a)给予已接受过所述治疗或疗法的受试者包含聚糖治疗剂制剂的药物组合物;b)给予已用包含聚糖治疗剂制剂的药物组合物治疗过的受试者所述治疗或疗法;或c)给予受试者包含聚糖治疗剂制剂的药物组合物并给予所述治疗或疗法,由此减轻所述治疗或疗法在受试者中的症状。
47、在一个实施例中,治疗或疗法是抗癌治疗或疗法。在一个实施例中,治疗或疗法是针对营养失衡的治疗。在一个实施例中,治疗或疗法是针对免疫失衡的治疗。在一个实施例中,症状是治疗或疗法的副作用。在一个实施例中,症状的发作是在给予聚糖治疗剂制剂之前。在一个实施例中,在症状发作之后给予聚糖治疗剂制剂。在一个实施例中,治疗或疗法的症状是不合需要的。在一个实施例中,症状是胃肠道症状。在一个实施例中,症状是消化异常。在一个实施例中,胃肠道症状是以下中的一个或多个:腹痛、痉挛、恶心、呕吐、胃部不适、胀气、腹胀、肠胃气胀、腹泻、便秘、胃灼热、粘膜炎以及体重增长、体重减轻。在一个实施例中,症状是非胃肠道症状。在一个实施例中,非胃肠道症状是焦虑、恐惧、抑郁、精神模糊、皮炎、胸痛、呼吸急促中的一个或多个。在一个实施例中,症状是抗癌治疗或疗法并发的或是抗癌治疗或疗法的结果。在一个实施例中,症状是针对营养失衡的治疗并发的或是针对营养失衡的治疗的结果。在一个实施例中,症状是针对免疫失衡的治疗并发的或是针对免疫失衡的治疗的结果。在一个实施例中,症状是以下中的一个或多个:放射损伤疼痛、外科手术疼痛、幻觉痛、急性疼痛、慢性疼痛或持续性疼痛、爆发性疼痛、周围神经病、口腔炎、粘膜炎、恶心、呕吐、腹泻、便秘、尿失禁、疲劳、贫血、淋巴水肿、感染、焦虑、恐惧、抑郁、生育缺陷以及增加的患第二癌症的风险。在一个实施例中,症状是营养不良或恶病质。在一个实施例中,症状是粘膜炎。在一个实施例中,粘膜炎是口腔粘膜炎。在一个实施例中,粘膜炎与化疗治疗或放疗相关。在一个实施例中,症状对于药物治疗或疗法来说是剂量限制性的,从而阻止了用药物的最大有效剂量来治疗受试者。
48、本文提供一种减小药物治疗在对其有需要的受试者中的毒性的方法,包含:a)给予已接受过药物治疗的受试者包含聚糖治疗剂制剂的药物组合物;b)给予已用包含聚糖治疗剂制剂的药物组合物治疗的受试者药物治疗;或c)按有效量给予受试者包含聚糖治疗剂制剂的药物组合物并给予药物治疗来治疗受试者。
49、在一个实施例中,药物治疗包含给予免疫调节药物。在一个实施例中,药物治疗包含给予代谢调节药物。在一个实施例中,药物治疗包含给予抗癌药物。在一个实施例中,抗癌药物是伊立替康(irinotecan)或5-氟尿嘧啶。在一个实施例中,毒性是剂量限制性毒性,从而阻止了用药物的最大有效剂量来治疗受试者。在一个实施例中,将受试者对药物治疗的耐受性提高到超过亚有效剂量(sub-efficacious dose)的剂量。在一个实施例中,将受试者对药物治疗的耐受性提高到等于或超过药物在受试者中的最大有效剂量的剂量。在一个实施例中,方法进一步包含给予已接受过第一治疗的受试者包含聚糖治疗剂制剂的药物组合物,并且任选地提供第二治疗,例如其中第二治疗包含按比之前的治疗更高的剂量、更频繁的时间间隔、更高的单独给药总数给予药物或疗法,得到更高的cmax,得到更高的谷值水平等。在一个实施例中,方法进一步包含为已接受过包含聚糖治疗剂制剂的药物组合物和已接受过第一治疗的受试者提供后续治疗,其中第二治疗包含按比之前的治疗更高的剂量、更频繁的时间间隔、更高的单独给药总数给予药物或疗法,得到更高的cmax,得到更高的谷值水平等。在一个实施例中,方法进一步包含评定以下中的一个或多个:聚糖治疗对受试者的适合性、受试者对聚糖治疗的反应性和/或聚糖治疗在受试者中的进展,包含:a)获取与聚糖治疗剂制剂所调节的生物标志物的水平相关的参数的值,和b)响应于所述值,对受试者进行分类,为受试者选择治疗,或给予受试者治疗,由此评定受试者。在一个实施例中,一个或多个生物标志物选自:i)胃肠道微生物群的改变,ii)胃环境的代谢物的改变,iii)有机酸的产生,iv)免疫系统的调节,v)炎症生物标志物的调节,vi)免疫球蛋白的调节,vii)结肠中矿物质的吸收增加,viii)脂质代谢的调节,ix)胆固醇减少,x)宿主稳态的调节。在一个实施例中,调节是表19中所列的代谢通路中的一个或多个(超级通路或子通路或代谢物水平)。
50、本文提供一种治疗与肠胃不适相关的症状的方法,包含给予正在进行抗癌疗法的受试者包含有效量的支化聚糖混合物的聚糖治疗剂组合物来治疗与肠胃不适相关的一个或多个症状。
51、在一个实施例中,方法进一步包含给予抗炎剂。在一个实施例中,方法进一步包含给予益生微生物。在一个实施例中,肠有益菌微生物群紊乱。在一个实施例中,抗癌疗法是放疗或化疗。在一个实施例中,症状是便秘或腹泻。在一个实施例中,症状是胀气、胃灼热、胃部不适、腹胀、肠胃气胀、腹泻、腹痛、痉挛、恶心或呕吐。在一个实施例中,组合物的给予引起了i)腹泻减少,ii)便秘减少,iii)有毒代谢产物减少。在一个实施例中,在病况治疗结束之后,症状的减轻或消除继续保持着。在一个实施例中,组合物的给予引起了肠道的规律性改善。在一个实施例中,在据报告胃肠道病症的一种或多种症状中的至少一种症状严重的受试者中,在治疗后胃肠道病症的一种或多种症状中的至少一种症状减轻了约10%、20%、30%、40%、50%、60%、70%、80%、90%、95%或100%。在一个实施例中,在治疗之后至少约一天、一周、一个月、3个月、6个月、9个月或一年,胃肠道病症的一种或多种症状中的至少一种症状的减轻继续保持着。
52、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)聚糖治疗剂制剂所具有的平均支化度(db)是至少0.01,iv)制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,v)制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率大体上在约1:1到约5:1之间,或vi)i)、ii)、iii)、iv)以及v)中的一个、两个、三个、四个或五个的任何组合。
53、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)支化寡糖包含葡萄糖、半乳糖、阿拉伯糖、甘露糖、果糖、木糖、岩藻糖或鼠李糖聚糖单元,iv)聚糖治疗剂制剂中的支化聚糖的平均支化度(db)在0.01与0.3之间,v)聚糖治疗剂制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,vi)聚糖治疗剂制剂的平均dp在约dp6与约dp10之间,vii)聚糖治疗剂制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率在约1:1到约5:1之间,viii)聚糖治疗剂制剂在23℃下在水中所具有的最终溶解度极限是至少约60白利度,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
54、对于以上方法中的任一种和所有方法来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含一个或多个聚糖单元,iii)支化聚糖包含至少1%的支化聚糖单元,iv)支化聚糖所具有的聚合度(dp)在2个与30个聚糖单元之间,v)支化聚糖具有1:1、1:2、1:3、1:4或1:5的β构型:α构型,vi)支化聚糖包含(1-2)、(1-3)、(1-4)、(1-6)、(2-3)以及(2-6)中的一个或多个的β键与α键的混合物,vii)聚糖治疗剂制剂包含支化聚糖与未支化聚糖的混合物,viii)聚糖治疗剂制剂包含易消化的聚糖与不易消化的聚糖的混合物,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
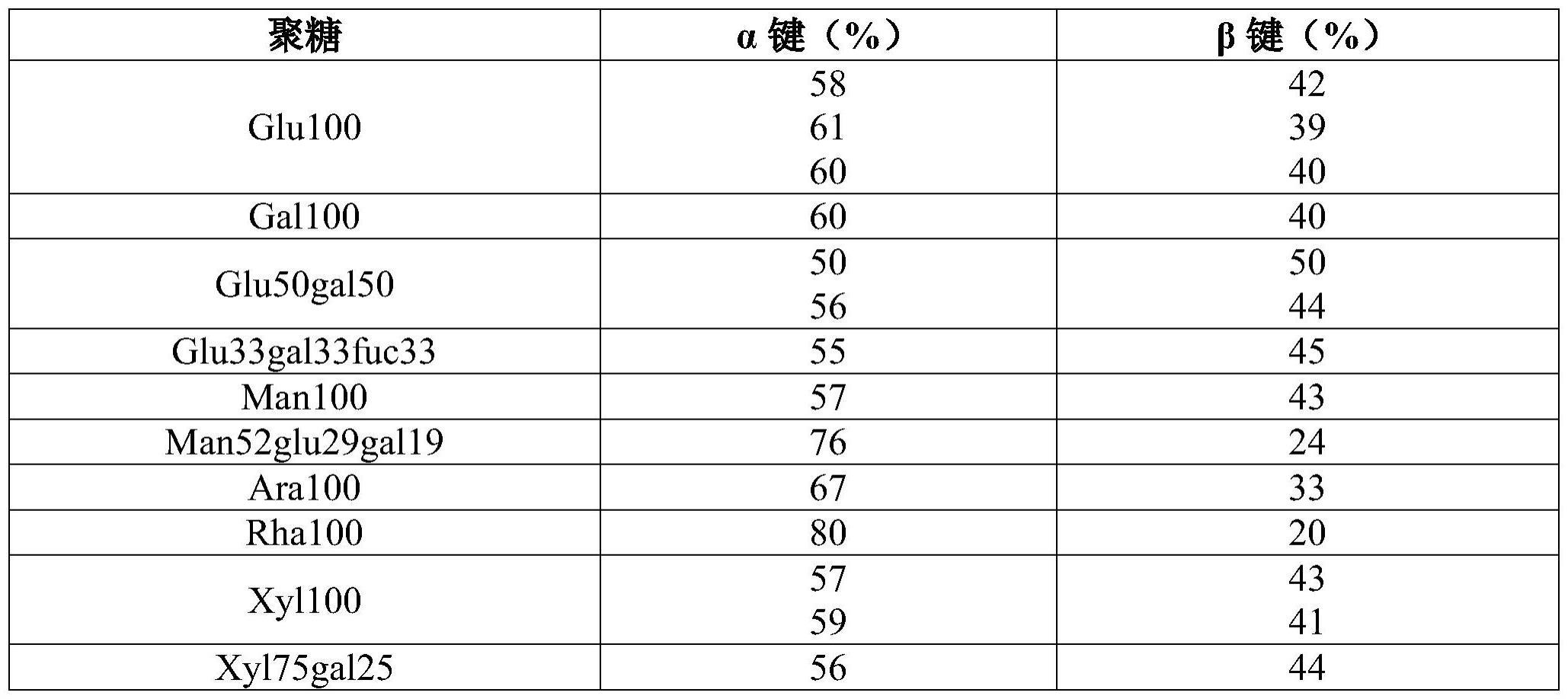
55、对于以上方面中的任一个和所有方面来说,并且对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含选自xyl100、rha100、ara100、gal100、glu100、fuc100、fru100以及man100的一个或多个同聚糖。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含选自ara50gal50、xyl75gal25、ara80xyl20、ara60xyl40、ara50xyl50、glu80man20、glu60man40、man60glu40、man80glu20、gal75xyl25、glu50gal50、man62glu38的一个或多个杂聚糖以及混合聚糖glu90sor10和glu90gly10。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含选自xyl75glu12gal12、xyl33glu33gal33、glu33gal33fuc33、man52glu29gal19以及glu33gal33neu33的一个或多个杂聚糖。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含选自xyl100、rha100、ara100、gal100、glu100、man100、fuc100、fru100、ara50gal50、xyl75gal25、ara80xyl20、ara60xyl40、ara50xyl50、glu80man20、glu60man40、man60glu40、man80glu20、gal75xyl25、glu50gal50、man62glu38的一个或多个同聚糖或杂聚糖,以及混合聚糖glu90sor10和glu90gly10、xyl75glu12gal12、xyl33glu33gal33、glu33gal33fuc33、man52glu29gal19以及glu33gal33neu33。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含选自以下的一个或多个同聚糖或杂聚糖:ara50gal50、glu33gal33fuc33、glu50gal50、gal100、glu100、xyl100、ara100、ara60xyl40、glu80man20、glu60man40、man52glu29gal19、man100。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含选自man100、xyl100或glu100的一个或多个同聚糖。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含man100。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含xyl100。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含glu100。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含选自glu50gal50、glu80man20、glu33gal33fuc33、man52glu29gal19的一个或多个杂聚糖。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含包含glu50gal50。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含glu80man20。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含glu33gal33fuc33。对于本文所述的任何包括给予聚糖治疗剂制剂的方法来说,聚糖治疗剂制剂可以包含man52glu29gal19。
56、对于以上方面中的任一个和所有方面来说,并且对于任何调节有益菌的方法来说,有益菌包括以下各个属的细菌:阿克曼氏菌属、厌氧细杆菌属(anaerofilum)、拟杆菌属、布劳特氏菌属、双歧杆菌属、丁酸弧菌属(butyrivibrio)、梭菌属、粪球菌属、小杆菌属(dialister)、多尔氏菌属(dorea)、梭杆菌属、真杆菌属、粪栖杆菌属、毛螺菌属(lachnospira)、乳杆菌属(lactobacillus)、考拉杆菌属(phascolarctobacterium)、消化球菌属、消化链球菌属、普雷沃氏菌属、罗斯氏菌属、瘤胃球菌属以及链球菌,和/或以下各个种中的一个或多个:嗜粘蛋白阿克曼氏菌(akkermansia municiphilia)、矮小菌(minuta)、球形梭菌(clostridium coccoides)、柔嫩梭菌(clostridium leptum)、闪烁梭菌(clostridium scindens)、隐蔽小杆菌(dialister invisus)、直肠真杆菌(eubacteriumrectal)、挑剔真杆菌(eubacterium eligens)、普氏栖粪杆菌(faecalibacteriumprausnitzii)、唾液链球菌(streptococcus salivarius)和嗜热链球菌(streptococcusthermophilus),以及表1、表3和表4中所列的分类群。
57、在第六方面中,本发明涉及用于治疗癌症的试剂盒。本文提供一种用于治疗人类受试者的癌症的试剂盒,包含包装,所述包装包含(i)包含聚糖治疗剂制剂的第一药物组合物,(ii)任选地第二抗肿瘤或抗癌药物组合物,以及(iii)使用第一和/或第二药物组合物治疗人类患者的癌症的说明书。
58、在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)聚糖治疗剂制剂所具有的平均支化度(db)是至少0.01,iv)制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,v)制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率大体上在约1:1到约5:1之间,或vi)i)、ii)、iii)、iv)以及v)中的一个、两个、三个、四个或五个的任何组合。
59、在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)支化寡糖包含葡萄糖、半乳糖、阿拉伯糖、甘露糖、果糖、木糖、岩藻糖或鼠李糖聚糖单元,iv)聚糖治疗剂制剂中的支化聚糖的平均支化度(db)在0.01与0.3之间,v)聚糖治疗剂制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,vi)聚糖治疗剂制剂的平均dp在约dp6与约dp10之间,vii)聚糖治疗剂制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率在约1:1到约5:1之间,viii)聚糖治疗剂制剂在23℃下在水中所具有的最终溶解度极限是至少约60白利度,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
60、在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含一个或多个聚糖单元,iii)支化聚糖包含至少1%的支化聚糖单元,iv)支化聚糖所具有的聚合度(dp)在2个与30个聚糖单元之间,v)支化聚糖具有1:1、1:2、1:3、1:4或1:5的β构型:α构型,vi)支化聚糖包含(1-2)、(1-3)、(1-4)、(1-6)、(2-3)以及(2-6)中的一个或多个的β键与α键的混合物,vii)聚糖治疗剂制剂包含支化聚糖与未支化聚糖的混合物,viii)聚糖治疗剂制剂包含易消化的聚糖与不易消化的聚糖的混合物,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
61、在第七方面中,本发明涉及用于治疗疾病、病症或病况的剂型。本文提供可有效治疗疾病、病症或病理状况的单位剂型,包含被配制成用于口服、肠内、经直肠、静脉内或瘤内给予的聚糖治疗剂制剂。
62、在一个实施例中,疾病、病症或病理病况是癌症。在一个实施例中,疾病、病症或病理病况是营养失衡。在一个实施例中,疾病、病症或病理病况是免疫失衡。在一个实施例中,将单位剂型配制为药物组合物。在一个实施例中,将单位剂型配制为医疗食品。在一个实施例中,将单位剂型配制为膳食补充剂。在一个实施例中,将剂型配制成由受试者口服。在一个实施例中,将剂型配制成溶解在水溶液中,作为饮料、糖浆、溶液或悬浮液口服。在一个实施例中,将剂型配制成用于肠内给药。在一个实施例中,经鼻胃、鼻空肠、口腔胃或口腔空肠给药。在一个实施例中,将剂型配制成用于经直肠给药。在一个实施例中,给药方式是灌肠剂、栓剂或结肠镜检查。在一个实施例中,将剂型配制为延迟释放或时间控制系统。在一个实施例中,将剂型配制成用于在胃肠(gastrointestinal,gi)道的特定区域中释放聚糖治疗剂制剂。在一个实施例中,胃肠道的特定区域包含胃、小肠、大肠或结肠。在一个实施例中,组合物调节胃肠道中所存在的细菌属的丰度。在一个实施例中,细菌分类群是双歧杆菌属、拟杆菌属、阿克曼氏菌属。在一个实施例中,细菌分类群是双歧杆菌属、双歧杆菌目、拟杆菌目、梭菌目、副拟杆菌属以及阿克曼氏菌属。在一个实施例中,细菌分类群是布劳特氏菌属、双歧杆菌属、罗斯氏菌属、粪球菌属、毛螺菌科、粪栖杆菌属、副拟杆菌属以及瘤胃球菌科。在一个实施例中,组合物调节小肠或大肠中的一个或两个中所存在的细菌属的丰度。在一个实施例中,组合物调节主要在小肠中的选自下组的细菌属的丰度:无色杆菌属(achromobacter)、土壤杆菌属(agrobacterium)、布劳特氏菌属、伯克氏菌属(burkholderia)、粪球菌属、克拉菌属(cryocola)、肠球菌属、真杆菌属、霍尔德曼氏菌属(holdemania)、乳球菌属(lactococcus)、分枝杆菌属(mycobacterium)、假支杆菌属(pseudoramibacter)、罗尔斯通氏菌属(ralstonia)、鞘氨醇单胞菌属(sphingomonas)、链球菌属(streptococcus)以及图利杆菌属(turicibacter)。在一个实施例中,组合物调节主要在大肠中的选自下组的细菌属的丰度:厌氧棍状菌属(anaerotruncus)、阿克曼氏菌属、拟杆菌属、嗜胆菌属(bilophila)、丁酸菌属(butyricimonas)、臭杆菌属(odoribacter)、副拟杆菌属、考拉杆菌属、普雷沃氏菌属以及瘤胃球菌属。
63、在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)聚糖治疗剂制剂所具有的平均支化度(db)是至少0.01,iv)制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,v)制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率大体上在约1:1到约5:1之间,或vi)i)、ii)、iii)、iv)以及v)中的一个、两个、三个、四个或五个的任何组合。
64、在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)支化寡糖包含葡萄糖、半乳糖、阿拉伯糖、甘露糖、果糖、木糖、岩藻糖或鼠李糖聚糖单元,iv)聚糖治疗剂制剂中的支化聚糖的平均支化度(db)在0.01与0.3之间,v)聚糖治疗剂制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,vi)聚糖治疗剂制剂的平均dp在约dp6与约dp10之间,vii)聚糖治疗剂制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率在约1:1到约5:1之间,viii)聚糖治疗剂制剂在23℃下在水中所具有的最终溶解度极限是至少约60白利度,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
65、在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含一个或多个聚糖单元,iii)支化聚糖包含至少1%的支化聚糖单元,iv)支化聚糖所具有的聚合度(dp)在2个与30个聚糖单元之间,v)支化聚糖具有1:1、1:2、1:3、1:4或1:5的β构型:α构型,vi)支化聚糖包含(1-2)、(1-3)、(1-4)、(1-6)、(2-3)以及(2-6)中的一个或多个的β键与α键的混合物,vii)聚糖治疗剂制剂包含支化聚糖与未支化聚糖的混合物,viii)聚糖治疗剂制剂包含易消化的聚糖与不易消化的聚糖的混合物,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
66、在第八方面中,本发明涉及一种包含聚糖治疗剂制剂的组合物。本文提供一种组合物,所述组合物包含:a)易消化的聚糖治疗剂制剂和基本上不易消化的糖类或膳食纤维,b)基本上不易消化的聚糖治疗剂制剂和易消化的糖类或膳食纤维,c)基本上不易消化的聚糖治疗剂制剂和基本上不易消化的糖类或膳食纤维,或d)易消化的聚糖治疗剂制剂和易消化的糖类或膳食纤维,以及(a)、(b)、(c)、(d)中的任一个,任选地包含益生菌。
67、在一个实施例中,将组合物配制为药物组合物。在一个实施例中,组合物进一步包含药学上可接受的赋形剂或载体。在一个实施例中,将组合物配制为医疗食品。在一个实施例中,将组合物标记为医疗食品。在一个实施例中,将组合物配制为膳食补充剂。在一个实施例中,将组合物标记为膳食补充剂。在一个实施例中,组合物进一步包含必需营养素。在一个实施例中,组合物可有效治疗免疫失衡。在一个实施例中,组合物可有效治疗营养失衡。在一个实施例中,组合物可有效治疗癌症。在一个实施例中,肠道微生物群组分选择性消化聚糖治疗剂制剂。在一个实施例中,选择性消化引起了对肠道微生物群的组成和/或活性的调节。在一个实施例中,选择性刺激以下中的一个或多个的生长:拟杆菌属、布劳特氏菌属、梭菌属、梭杆菌属、真杆菌属、瘤胃球菌属、消化球菌属、消化链球菌属、阿克曼氏菌属、粪栖杆菌属、罗斯氏菌属、普雷沃氏菌属、双歧杆菌属、乳杆菌属、小克里斯滕森氏菌以及克里斯滕森菌科。在一个实施例中,在肠中没有特定细菌的情况下,聚糖治疗剂制剂基本上不易被人类消化,其中特定细菌能够利用聚糖治疗剂作为碳源。在一个实施例中,聚糖治疗剂可抵抗胃的酸度。在一个实施例中,聚糖治疗剂可抵抗被哺乳动物酶水解。在一个实施例中,哺乳动物酶是人淀粉酶。在一个实施例中,聚糖治疗剂可抵抗胃肠吸收。
68、本文提供一种用于本文所述的方法中的任一个中的组合物。
69、本文提供一种包含所述组合物的剂型。
70、对于以上任一个和所有来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)聚糖治疗剂制剂所具有的平均支化度(db)是至少0.01,iv)制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,v)制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率大体上在约1:1到约5:1之间,或vi)i)、ii)、iii)、iv)以及v)中的一个、两个、三个、四个或五个的任何组合。
71、对于以上任一个和所有来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含支化寡糖,iii)支化寡糖包含葡萄糖、半乳糖、阿拉伯糖、甘露糖、果糖、木糖、岩藻糖或鼠李糖聚糖单元,iv)聚糖治疗剂制剂中的支化聚糖的平均支化度(db)在0.01与0.3之间,v)聚糖治疗剂制剂中的聚糖的至少50%所具有的聚合度(dp)是至少3个并且小于30个聚糖单元,vi)聚糖治疗剂制剂的平均dp在约dp6与约dp10之间,vii)聚糖治疗剂制剂的聚糖中所存在的α-糖苷键与β-糖苷键的比率在约1:1到约5:1之间,viii)聚糖治疗剂制剂在23℃下在水中所具有的最终溶解度极限是至少约60白利度,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
72、对于以上任一个和所有来说,在一个实施例中,聚糖治疗剂制剂:i)包含支化聚糖,ii)支化聚糖包含一个或多个聚糖单元,iii)支化聚糖包含至少1%的支化聚糖单元,iv)支化聚糖所具有的聚合度(dp)在2个与30个聚糖单元之间,v)支化聚糖具有1:1、1:2、1:3、1:4或1:5的β构型:α构型,vi)支化聚糖包含(1-2)、(1-3)、(1-4)、(1-6)、(2-3)以及(2-6)中的一个或多个的β键与α键的混合物,vii)聚糖治疗剂制剂包含支化聚糖与未支化聚糖的混合物,viii)聚糖治疗剂制剂包含易消化的聚糖与不易消化的聚糖的混合物,或ix)i)、ii)、iii)、iv)、v)、vi)、vii)以及viii)中的一个、两个、三个或四个、五个、六个、七个或八个的任何组合。
73、对于以上方面中的任一个和所有方面来说,并且对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含选自xyl100、rha100、ara100、gal100、glu100、fuc100、fru100以及man100的一个或多个同聚糖。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含选自ara50gal50、xyl75gal25、ara80xyl20、ara60xyl40、ara50xyl50、glu80man20、glu60man40、man60glu40、man80glu20、gal75xyl25、glu50gal50、man62glu38的一个或多个杂聚糖,以及混合聚糖glu90sor10和glu90gly10。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含选自xyl75glu12gal12、xyl33glu33gal33、glu33gal33fuc33、man52glu29gal19以及glu33gal33neu33的一个或多个杂聚糖。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含选自以下的一个或多个同聚糖或杂聚糖:xyl100、rha100、ara100、gal100、glu100、man100、fuc100、fru100、ara50gal50、xyl75gal25、ara80xyl20、ara60xyl40、ara50xyl50、glu80man20、glu60man40、man60glu40、man80glu20、gal75xyl25、glu50gal50、man62glu38;以及混合聚糖glu90sor10和glu90gly10、xyl75glu12gal12、xyl33glu33gal33、glu33gal33fuc33、man52glu29gal19以及glu33gal33neu33。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含选自以下的一个或多个同聚糖或杂聚糖:ara50gal50、glu33gal33fuc33、glu50gal50、gal100、glu100、xyl100、ara100、ara60xyl40、glu80man20、glu60man40、man52glu29gal19、man100。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含选自man100、xyl100或glu100的一个或多个同聚糖。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含man100。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含xyl100。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含glu100。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含选自glu50gal50、glu80man20、glu33gal33fuc33、man52glu29gal19的一个或多个杂聚糖。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含glu50gal50。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含glu80man20。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含glu33gal33fuc33。对于包含本文所述的聚糖治疗剂制剂的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒来说,聚糖治疗剂制剂可以包含man52glu29gal19。
74、对于以上方面中的任一个和所有方面来说,并且对于包含益生菌的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒以及任何包括给予益生菌的方法来说,益生菌可以包含以下各个属的细菌:阿克曼氏菌属、厌氧细杆菌属、拟杆菌属、布劳特氏菌属、双歧杆菌属、丁酸弧菌属、梭菌属、粪球菌属、小杆菌属、多尔氏菌属、梭杆菌属、真杆菌属、粪栖杆菌属、毛螺菌属、乳杆菌属、考拉杆菌属、消化球菌属、消化链球菌属、普雷沃氏菌属、罗斯氏菌属、瘤胃球菌属以及链球菌属,和/或以下各个种中的一个或多个:嗜粘蛋白阿克曼氏菌、矮小菌、球形梭菌、柔嫩梭菌、闪烁梭菌、隐蔽小杆菌、直肠真杆菌、挑剔真杆菌、普氏栖粪杆菌、唾液链球菌和嗜热链球菌,以及表1、表3和表4中所列的分类群。
75、对于以上方面中的任一个和所有方面来说,并且对于包含抗癌剂或抗癌药物的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒以及任何包括给予癌症药剂的方法来说,癌症药剂可以包含例如检查点抑制剂(例如抗pd-1、抗pd-l1、抗ctla4、抗tim-3、抗lag-3);疫苗(例如自体癌症疫苗、同种异体癌症疫苗、新抗原癌症疫苗、共用抗原癌症疫苗(例如ny-eso-1));靶向激酶抑制剂(例如甲磺酸伊马替尼(imatinib mesylate)、依鲁替尼(ibrutinib)、来那替尼(neratinib)、帕布昔利布(palpociclib)、埃罗替尼(erlotinib)、拉帕替尼(lapatinib));抗体(例如贝伐单抗(bevacizumab)、曲妥珠单抗(trastuzumab)、利妥昔单抗(rituximab)、西妥昔单抗(cetuximab));化疗药物(例如伊立替康、5-氟尿嘧啶、来那度胺(lenalidomide)、卡培他滨(capecitabine)、多西他赛(docetaxel));抗体-药物结合物(例如阿多-曲妥珠单抗恩他新(ado-trastuzumab emtansine));以及本文其它地方所提到的任何其它抗癌药物。在一个实施例中,抗癌剂是pd-l1。在一个实施例中,抗癌剂是5-fu和/或伊立替康。
76、对于以上方面中的任一个和所有方面来说,并且对于包含免疫调节剂或药物(例如促炎性或抗炎性)的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒以及任何包括给予免疫调节剂(例如促炎性或抗炎性)的方法来说,免疫调节剂可以包含例如促炎剂(例如促炎性细胞因子)、抗炎剂(例如抗炎性细胞因子、非类固醇抗炎药(non-steroidanti-inflammatory drug,nsaid)、抗过敏剂)、类固醇、激素、白细胞介素、疫苗/抗原、抗微生物剂(例如抗病毒剂)以及抗肿瘤剂。
77、对于以上方面中的任一个和所有方面来说,并且对于包含代谢调节剂或药物的任何药物组合物、医疗食品、膳食补充剂、剂型或试剂盒以及任何包括给予代谢调节剂的方法来说,代谢调节剂可以包含例如胰岛素、二甲双胍(metformin)、氯卡色林(lorcaserin)、索马托品(somatropin)、米格列醇(miglitol)、西他列汀(sitagliptin)、辛伐他汀(simvastatin)、助孕素(progestagen)、皮质类固醇(corticosteroids)、激素以及白细胞介素。
78、在以上方面中的任一个和所有方面中,在一些实施例中,本发明的特征在于用于以下用途的化合物和组合物(例如药物组合物、医疗食品或膳食补充剂):例如治疗受试者的免疫失衡;减少有免疫失衡的受试者的感染和/或炎症;调节有免疫失衡的受试者的肠道细菌群落的组成和/或代谢活动;治疗有免疫失衡的受试者的生态失调;治疗受试者的营养失衡;调节有营养失衡的受试者的肠道细菌群落的组成和/或代谢活动;治疗有营养失衡的受试者的生态失调;治疗受试者的癌症;调节有癌症的受试者的肠道细菌群落的组成和/或代谢活动;治疗有癌症的受试者的生态失调;减少有癌症的受试者的感染和/或炎症;诱导有癌症的受试者的癌细胞或癌前细胞凋亡;降低受试者的癌症风险;调节有癌症的受试者的肠道细菌群落的组成;调节有癌症的受试者的肠道细菌群落的代谢活动;减轻治疗或疗法在受试者中的症状;减小药物治疗或疗法在受试者中的毒性;治疗与肠胃不适相关的症状;调节有免疫失衡的受试者的通路的功能和/或活性;调节有营养失衡的受试者的通路的功能和/或活性;和/或调节有癌症的受试者的通路的功能和/或活性。
- 还没有人留言评论。精彩留言会获得点赞!