胰腺神经内分泌肿瘤细胞转移能力预测方法及相关设备
本技术涉及胰腺神经内分泌肿瘤细胞领域,尤其涉及一种胰腺神经内分泌肿瘤细胞转移能力预测方法及相关设备。
背景技术:
1、胰腺神经内分泌肿瘤(pannen)是一种高度异质性肿瘤,每年发病率不到10万分之一。对于手术切除的非转移性肿瘤患者,其10年生存率略高于50%。但是大约60%的pannen患者有转移,最常见的是转移到肝脏。更重要的是,pannen转移患者术后中位生存时间明显缩短。pannen分级方案由欧洲神经内分泌肿瘤学会(enets)制定,并于2010年被世界卫生组织采纳。这种最常见的分类系统把胰腺神经内分泌肿瘤分为三个等级,即gl、g2和g3,分别对应高分化肿瘤(gl和g2)和低分化肿瘤(g3)。世界卫生组织2017年更新的nen分类在形态学上区分了来源于胰腺的高分化神经内分泌肿瘤(net)(即pannet)与低分化神经内分泌癌(pannec)。
2、pannet的病理分类主要依据核分裂象计数和ki-67指数。ki-67广泛用于pannet的分期、预后评估和治疗决策。然而,ki-67仅仅是肿瘤增殖特征的反映,近35%的g1(ki-67指数<2%)和g2(2≤ki-67指数<20%)pannet患者在诊断时已经发生转移。另外,g分级也用于指导pannet患者根治性切除手术后的后续治疗。根治性切除术后是否需要化疗或其他治疗在临床上是一个争议的焦点。术后早期发生复发和转移会严重影响患者预后,而ki-67不能预测pannen转移的潜能。因此,ki-67不能作为指导临床治疗的检测指标。
3、一些研究试图找到预测pannet转移能力的指标,如moore md等发现uchl1联合ki-67可提高pannet转移的预测精度,gill等人表明mirna-3653是pannet转移风险增加的潜在标志,但这些转移标志物存在敏感性和特异性不高、指导治疗效果差等缺点。另外,这些研究都没有充分考虑到pannet的肿瘤异质性,一篇发表在gut上的文章揭示了pannet的肿瘤间基因表达异质性,比如zhou y等人通过单细胞测序描述了pannet细胞亚群在不同肿瘤间异质性。基于pannet的异质性特点,识别具有高转移潜力的特异性亚群并确定精确的转移标记物对指导临床工作具有重要意义。
4、目前,临床中应用的诊断标志物大多是蛋白质,蛋白质组学分析旨在大规模地描述蛋白质的特征,有助于阐明疾病发生的机制,并发现新的诊断标志物和治疗靶点。因此,蛋白质组学在筛选新的诊断标志物方面具有独特的优势。
5、因此可以考虑利用蛋白质组学对当前的胰腺神经内分泌肿瘤细胞转移能力预测进行改进。
技术实现思路
1、为了解决上述技术问题或者至少部分地解决上述技术问题,本技术提供了一种胰腺神经内分泌肿瘤细胞转移能力预测方法及相关设备。
2、第一方面,本技术提供了一种胰腺神经内分泌肿瘤细胞转移能力预测方法,所述方法包括步骤:
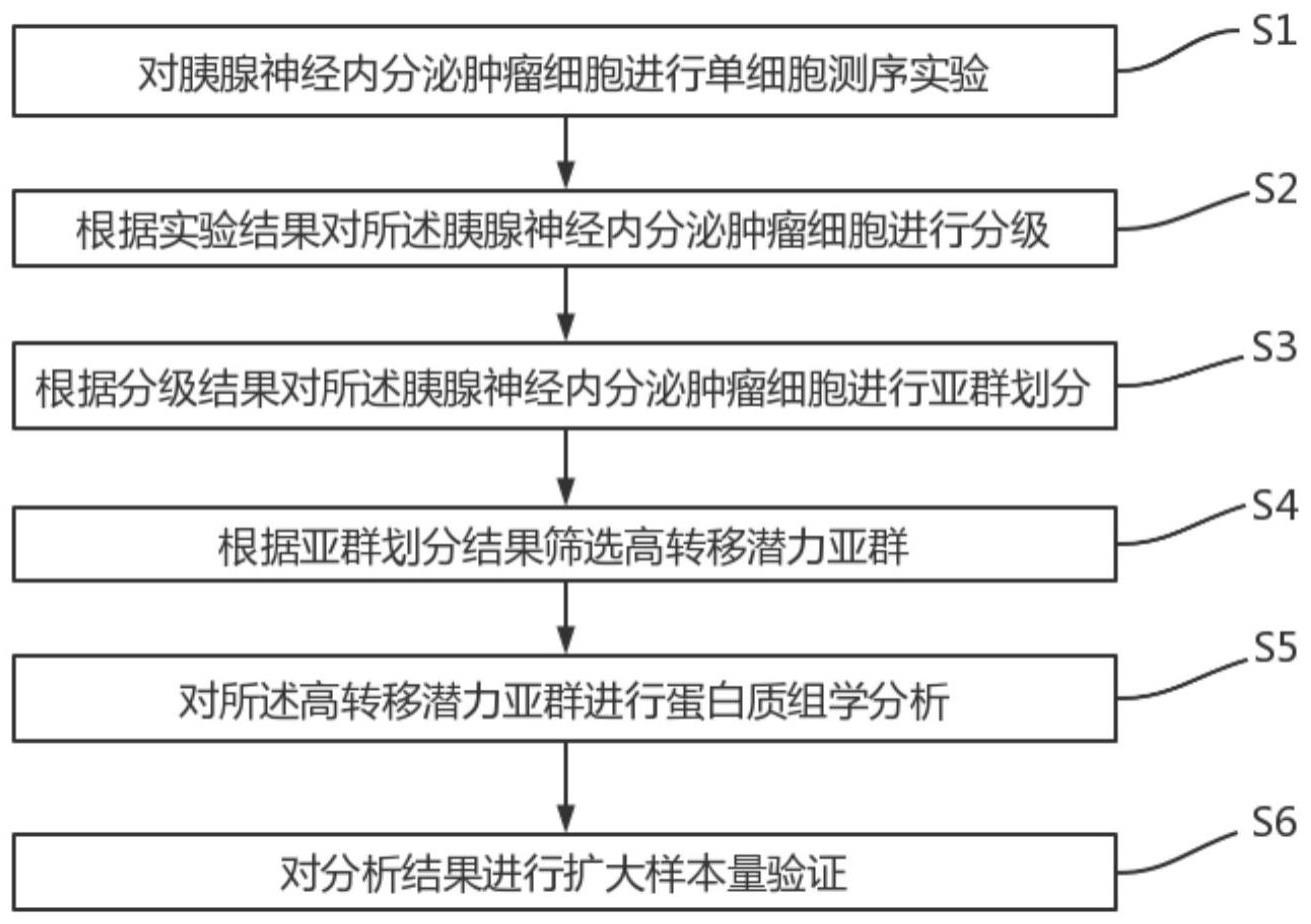
3、对胰腺神经内分泌肿瘤细胞进行单细胞测序实验;
4、根据实验结果对所述胰腺神经内分泌肿瘤细胞进行分级;
5、根据分级结果对所述胰腺神经内分泌肿瘤细胞进行亚群划分;
6、根据亚群划分结果筛选高转移潜力亚群;
7、对所述高转移潜力亚群进行蛋白质组学分析;
8、对分析结果进行扩大样本量验证。
9、优选地,所述对胰腺神经内分泌肿瘤细胞进行单细胞测序实验包括步骤:
10、配置单细胞测序实验设备;
11、选取胰腺神经内分泌肿瘤细胞;
12、将所述胰腺神经内分泌肿瘤细胞置入所述单细胞测序实验设备中;
13、配置所述单细胞测序实验设备的实验参数;
14、使用所述单细胞测序实验设备对所述胰腺神经内分泌肿瘤细胞进行实验。
15、优选地,所述根据实验结果对所述胰腺神经内分泌肿瘤细胞进行分级包括步骤:
16、获取胰腺神经内分泌肿瘤细胞分级系统;
17、获取所述胰腺神经内分泌肿瘤细胞的参数信息;
18、将所述参数信息输入所述胰腺神经内分泌肿瘤细胞分级系统;
19、获取所述胰腺神经内分泌肿瘤细胞分级系统的第一输出结果;
20、将所述第一输出结果作为分级结果。
21、优选地,所述根据分级结果对所述胰腺神经内分泌肿瘤细胞进行亚群划分包括步骤:
22、获取胰腺神经内分泌肿瘤细胞亚群划分系统;
23、获取所述胰腺神经内分泌肿瘤细胞的分级结果;
24、将所述分级结果输入所述胰腺神经内分泌肿瘤细胞亚群划分系统;
25、获取所述胰腺神经内分泌肿瘤细胞亚群划分系统的第二输出结果;
26、将所述第二输出结果作为亚群划分结果。
27、优选地,所述根据亚群划分结果筛选高转移潜力亚群包括步骤:
28、获取胰腺神经内分泌肿瘤细胞高转移潜力亚群划分系统;
29、获取所述胰腺神经内分泌肿瘤细胞的亚群划分结果;
30、将所述亚群划分结果输入所述胰腺神经内分泌肿瘤细胞高转移潜力亚群划分系统;
31、获取所述胰腺神经内分泌肿瘤细胞高转移潜力亚群划分系统的第三输出结果;
32、将所述第三输出结果作为高转移潜力亚群划分结果。
33、优选地,所述对所述高转移潜力亚群进行蛋白质组学分析包括步骤:
34、配置蛋白质组学分析设备;
35、选取胰腺神经内分泌肿瘤细胞高转移潜力亚群;
36、将所述胰腺神经内分泌肿瘤细胞高转移潜力亚群置入所述蛋白质组学分析设备中;
37、配置所述蛋白质组学分析设备的实验参数;
38、使用所述蛋白质组学分析设备对所述胰腺神经内分泌肿瘤细胞高转移潜力亚群进行实验。优选地,所述对分析结果进行扩大样本量验证包括步骤:
39、配置扩大样本量验证设备;
40、选取胰腺神经内分泌肿瘤细胞高转移潜力亚群;
41、将所述胰腺神经内分泌肿瘤细胞高转移潜力亚群置入所述扩大样本量验证设备中;
42、配置所述扩大样本量验证设备的实验参数;
43、使用所述扩大样本量验证设备对所述胰腺神经内分泌肿瘤细胞高转移潜力亚群进行实验。第二方面,本技术提供了一种胰腺神经内分泌肿瘤细胞转移能力预测装置,包括:单细胞测序实验模块,用于对胰腺神经内分泌肿瘤细胞进行单细胞测序实验;
44、分级模块,用于根据实验结果对所述胰腺神经内分泌肿瘤细胞进行分级;
45、亚群划分模块,用于根据分级结果对所述胰腺神经内分泌肿瘤细胞进行亚群划分;
46、高转移潜力亚群筛选模块,用于根据亚群划分结果筛选高转移潜力亚群;
47、蛋白质组学分析模块,用于对所述高转移潜力亚群进行蛋白质组学分析;
48、扩大样本量验证模块,用于对分析结果进行扩大样本量验证。
49、第三方面,提供了一种电子设备,所述电子设备包括:
50、至少一个处理器;以及,
51、与所述至少一个处理器通信连接的存储器;其中,
52、所述存储器存储有可被所述至少一个处理器执行的指令,所述指令被所述至少一个处理器执行,以使所述至少一个处理器能够执行前述任一权利要求1-7所述胰腺神经内分泌肿瘤细胞转移能力预测方法。
53、第四方面,提供了一种非暂态计算机可读存储介质,该非暂态计算机可读存储介质存储计算机指令,该计算机指令用于使该计算机执行前述任一权利要求1-7所述胰腺神经内分泌肿瘤细胞转移能力预测方法。
54、本技术实施例提供的上述技术方案与现有技术相比具有如下优点:
55、本技术提供的一种胰腺神经内分泌肿瘤细胞转移能力预测方法及相关设备通过单细胞测序和蛋白质组学分析找出了一个能够提供准确评估pannet细胞转移潜力的指标,该指标联合ki-67就可以更准确地预测胰腺神经内分泌肿瘤细胞转移能力,并可识别存在不同生存风险的亚组。
- 还没有人留言评论。精彩留言会获得点赞!