一种血小板膜伪装鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅纳米体系及其制备方法
本发明属于纳米技术与生物医药领域,特别涉及一种血小板膜伪装鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅纳米体系及其制备方法。
背景技术:
1、目前,临床上针对三阴性乳腺癌(tnbc)的标准治疗方案仍然是手术治疗和化疗,但tnbc相较于其他亚型乳腺癌更易发生远处转移,而且临床上有相当一部分患者对化疗耐药。另外,tnbc是一类具有高度异质性的混合型肿瘤,临床上在对tnbc的治疗上缺乏明确靶点及靶向治疗。因此,寻找tnbc更加有效的治疗方式是临床亟待解决的难点和重点。同时,tnbc患者病情发展迅速。若在治疗过程中,能通过增强肿瘤部位成像实现对肿瘤发展的实时监测,将更利于肿瘤的治疗与监测。
2、随着对肿瘤微环境(tumor microenvironment,tem)的深入研究,研究者们发现tnbc由于缺氧和糖酵解肿瘤代谢特点,通常表现为酸性和高乳酸的肿瘤微环境。然而,这些肿瘤微环境特点影响肿瘤相关巨噬细胞(tumor-associated macrophages,tams)向m2型巨噬细胞极化,也增加了血管内皮因子(evgf)的表达,抑制了tnbc的肿瘤免疫,促进其增殖及转移。
3、乳酸氧化酶作为一种天然蛋白质酶,被视为黄素蛋白家族中的一员。乳酸氧化酶生成的efmnh2-pyruvate复合体不稳定,丙酮酸很快从复合体上分离下来,还原型中间体efmnh2被氧化,同时形成过氧化氢,由于反应过程中不需要外源辅酶作为电子受体,而具有较好的应用前景。然而,乳酸氧化酶作为一种非人源蛋白,自身具有免疫原性可能引起抗体反应等。另一方面,其被细胞内吞后受到细胞溶酶体蛋白酶的水解从而失活。
4、因此,通过合理设计一种仿生纳米平台成功递送乳酸氧化酶至肿瘤部位,通过消耗肿瘤细胞内外的乳酸起到调整肿瘤微环境,从而实现tnbc的铁死亡、免疫治疗效应和诊断,是至关重要的。
技术实现思路
1、为解决上述现有技术存在的缺陷,本发明的目的是提供一种血小板膜伪装鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅纳米体系及其制备方法。
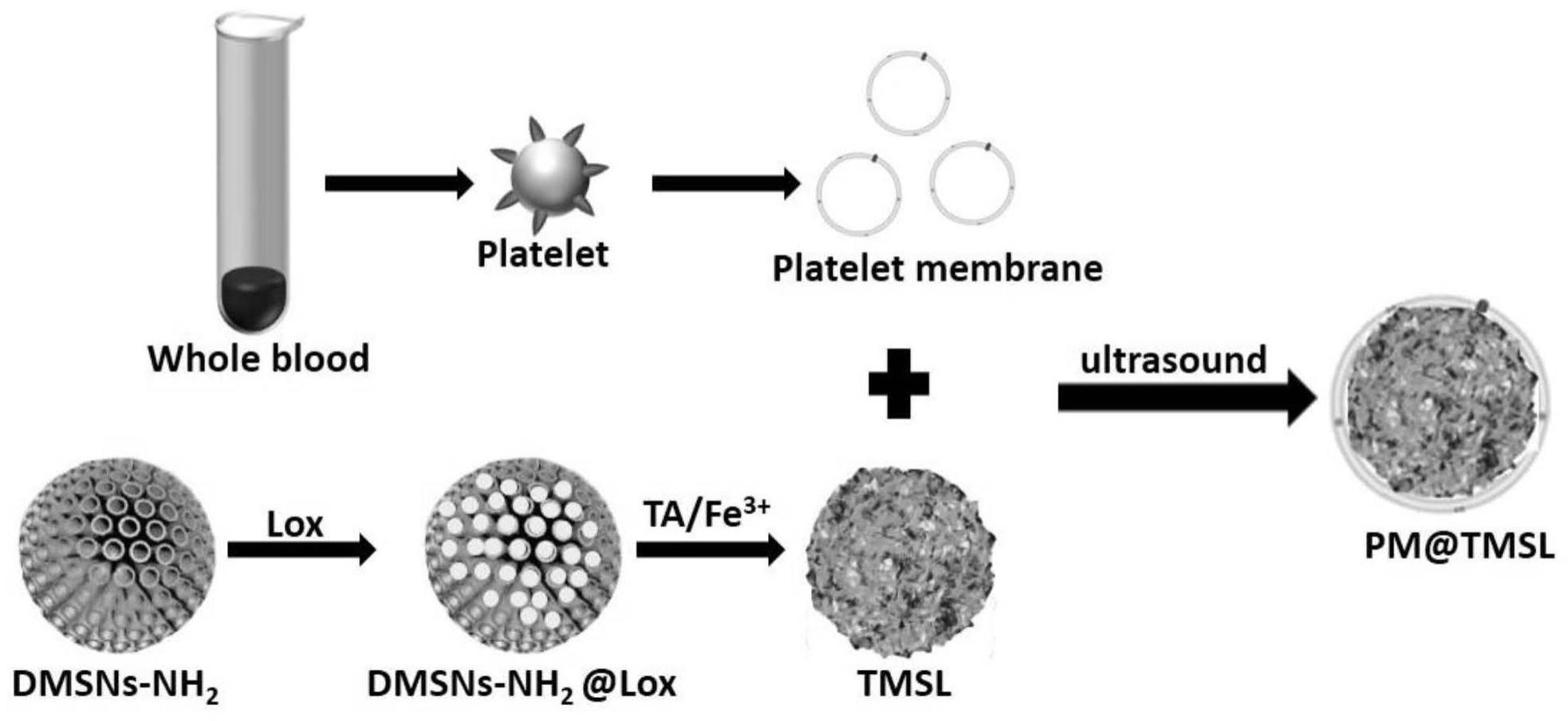
2、本发明提供的这种血小板膜伪装鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅纳米体系的制备方法,包括如下步骤:
3、1)制备纳米级血小板膜(pm);
4、2)制备鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅,包括如下步骤:
5、2-a.氨基化介孔二氧化硅(dmsns-nh2)的制备:将三乙醇胺溶解于去离子水中,在适宜温度下再加入十六烷基三甲基溴化铵和水杨酸钠,混合均匀,得到混合液,接着向混合液中加入正硅酸乙酯,加热搅拌反应,反应结束后,离心、洗涤、干燥,得到初级产物,再将初级产物加入由乙醇和浓盐酸组成的混合溶剂中继续水浴搅拌,结束后,离心、洗涤、干燥,得到介孔二氧化硅;将介孔二氧化硅溶解于甲苯中,再加入3-氨基丙基三乙氧基硅烷,加热回流,待反应结束后,离心、洗涤、干燥,得到氨基化介孔二氧化硅;
6、2-b.鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅(tmsl)的制备:在室温下,将乳酸氧化酶与氨基化介孔二氧化硅按配比混合,得到混合液,接着将鞣酸溶液和fecl3·6h2o溶液逐滴加入混合液中,超声分散,再加入3-(n-吗啉)丙磺酸缓冲液,搅拌,离心,得到鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅;
7、3)制备血小板膜伪装鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅纳米体系(pm@tmsl):将鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅与纳米级血小板膜超声融合后,过滤、离心,得到血小板膜伪装鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅纳米体系。
8、所述步骤1)中,制备纳米级血小板膜的步骤具体为:收集小鼠全血标本,置于含有肝素抗凝剂的试管中,通过离心和洗涤从全血中分离出血小板,再通过反复冻融提取出血小板膜,将血小板膜悬置于磷酸盐缓冲溶液中,超声处理,得到纳米级血小板膜。
9、所述步骤2-a中,所述三乙醇胺(tea)、十六烷基三甲基溴化铵(ctab)、水杨酸钠、正硅酸乙酯(teos)的质量体积比为(0.3~0.5)g:(0.1~0.6)g:(0.05~0.2)g:(1~6)ml;所述初级产物与混合溶剂的质量体积比为(0.15~0.5)g:(20~120)ml;所述混合溶剂中,乙醇与浓盐酸的体积比为(20~90)ml:(0.2~1.2)ml;所述介孔二氧化硅与3-氨基丙基三乙氧基硅烷的质量体积比为(0.1~0.5)g:(0.1~2)ml。
10、所述步骤2-a中,适宜温度为60~100℃;加热搅拌反应的温度为60~100℃,时间为1~4h;继续搅拌的温度为60~90℃,继续搅拌的时间为4~10h;加热回流的温度为60~100℃,加热回流的时间为2~8h。
11、所述步骤2-b中,乳酸氧化酶与氨基化介孔二氧化硅的质量比为(100~400)μg:(100~400)μg;所述鞣酸溶液的浓度为20~40mm,fecl3·6h2o溶液的浓度为20~50mm,3-(n-吗啉)丙磺酸缓冲液的浓度为10~40mm,ph为7.4;所述氨基化介孔二氧化硅、鞣酸溶液、fecl3·6h2o溶液与3-(n-吗啉)丙磺酸缓冲液的质量体积比为(100~400)μg:(1~10)μl:(1~10)μl:(200~2000)μl。
12、所述步骤3)中,鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅的质量与纳米级血小板膜的个数之比为(100~200)μg:(106~108)个。
13、根据上述制备方法制得的血小板膜伪装鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅纳米体系。
14、所述血小板膜伪装鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅纳米体系,所述乳酸氧化酶负载于氨基化介孔二氧化硅的孔洞中,鞣酸铁涂层位于氨基化介孔二氧化硅的表面,血小板膜包裹鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅。
15、所述血小板膜伪装鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅纳米体系中,乳酸氧化酶的封装率为94%~97%。
16、所述血小板膜伪装鞣酸铁涂层负载乳酸氧化酶的氨基化介孔二氧化硅纳米体系在制备靶向治疗三阴性乳腺癌药物中的应用。
17、本发明的原理:
18、本发明的血小板膜伪装鞣酸铁(feiiita)涂层负载乳酸氧化酶(lox)的氨基化介孔二氧化硅(dmsns-nh2)纳米体系(pm@tmsl),首先通过血小板膜表达的p-选择素对tnbc细胞表面高表达的cd44受体的主动靶向及epr效应的被动聚集作用进而靶向tnbc部位。随后,pm@tmsl被内吞入肿瘤细胞内并形成酸性内涵体,体系表面涂层的feiiita在酸性内涵体或溶酶体环境中因羟基基团被质子化导致交联剂的快速破坏和薄膜解聚,产生“质子海绵效应”进而实现溶酶体逃逸,成功将乳酸氧化酶(lox)靶向递送至肿瘤细胞,lox通过消耗肿瘤细胞内外的乳酸,一方面减少tams向m2巨噬细胞极化甚至m2巨噬细胞反极化成m1巨噬细胞,解除肿瘤的免疫抑制作用。另一方面,乳酸氧化酶可氧化乳酸产生h2o2,而且鞣酸(ta)可将释放的fe3+还原成fe2+,通过工业化的芬顿效应将h2o2转化为羟基自由基(ho·),过多的活性氧可损伤肿瘤细胞线粒体,从而导致肿瘤细胞发生凋亡。铁死亡作为一种铁依赖的新型细胞程序死亡方式,铁死亡过程中的脂质过氧化(lpo)水平与细胞氧化环境(如h2o2)有着紧密联系,因此本发明纳米体系能够诱导细胞铁死亡。同时,ta作为一种邻苯二酚衍生物,与fe3+形成配位络合物并涂层于氨基化介孔二氧化硅,可增强材料磁性用于三阴性乳腺癌磁共振成像诊断。
19、本发明的有益效果:
20、1)本发明纳米体系是一种集诊疗于一体化的多模式仿生靶向纳米药物系统,利用tnbc的固有特性高表达cd44受体、高乳酸肿瘤微环境、富含铁及脂质,能够实现诊疗一体化。
21、2)本发明纳米体系通过feiiita涂层氨基化树枝状介孔二氧化硅,具有生物相容性好,磁共振成像多功能及溶酶体逃逸的优点,实现乳酸氧化酶蛋白质的有效运输,通过消耗肿瘤细胞内外乳酸实现tnbc免疫治疗及凋亡。同时,ta实现fe3+与fe2+的循环供给,利用芬顿反应诱导tnbc铁死亡,实现了集诱发tnbc凋亡、免疫治疗与铁死亡的多模式组合疗法。
22、3)本发明纳米体系通过天然血小板膜伪装负载乳酸氧化酶(lox)的氨基化介孔二氧化硅(dmsns-nh2),既降低了网状内皮系统对纳米体系的吞噬清除作用,又增强了纳米体系的靶向能力。
- 还没有人留言评论。精彩留言会获得点赞!