一种智能化伤口治疗装置及其治疗方法
本发明属于医疗器械,具体地,涉及一种提高冷等离子体治疗效率,缩短冷等离子体治疗周期的伤口智能化治疗装置及其治疗方法。
背景技术:
1、皮肤伤口的愈合是长久以来的研究热点,其大致可分为急性伤口和慢性伤口。伤口愈合过程主要分为止血、炎症、增殖、重塑四个阶段,但愈合过程中会被病原体、糖尿病等各种因素影响,使得伤口反复经历炎症和增殖阶段而转化为慢性伤口,导致伤口愈合周期长、恢复困难,严重者甚至会导致截肢以及生命危险。
2、相较于裸露伤口,矫形治疗、整形治疗、负压治疗等特殊情况下的伤口护理则更为困难。此时,皮肤表面会被绷带、石膏、负压罩、模具等覆盖,护理人员无法通过视觉检查即时获得伤口信息,造成伤口感染发现不及时等问题;并且在此情景下,治疗需拆卸皮肤表面的覆盖物,过程痛苦,操作复杂,存在二次感染的隐患。因此,在此类特殊情况下,实时获得伤口信息并快速、无痛进行针对治疗尤为重要。
3、冷等离子体技术是近年新兴的医疗手段,其是电子、正负离子、紫外线、基态或激发态原子或分子等多种粒子的混合体系,是物质存在的第四态。作为一种物理治疗手段,冷等离子体因具有的高效、广谱杀菌能力,并因其低温、无痛、无毒、无过敏性等优点而并被认为是具有前景的伤口疗法。
4、冷等离子体在伤口治疗方面关键活性成分大致可分为活性氧(ros)和活性氮(rns)。前者包括氧原子(o)、超氧阴离子单线态氧(1o2)、羟基自由基(·oh)、臭氧(o3)等,后者包括氮原子(n)、一氧化氮(no)等。其中,·oh、1o2、o3等ros因于其优良的病原体灭活效果被认为在伤口愈合的止血、炎症阶段起到关键作用;而no等rns因于其促进血管重塑和生成、促进组织重塑等效果而在增殖重塑阶段起到关键作用。
5、空气冷等离子体中,输入较低密度的能量时即可形成大量ros。但由于n2分子强键断裂所需能量高达10ev,空气冷等离子体中通过n2分子和o2分子直接合成no的途径受限。为提高以no等rns的生成量,可适当提高输入能量,在相对高温下通过式(1)和式(2)生成no,其中式(2)途径起主导作用。同时,在空气非平衡放电中,电子和中性粒子相互碰撞可形成高度振动激发态的n2分子,进而可通过式(3)等途径形成游离态n原子,促进式(2)反应的发生。
6、
7、此外,作为一种臭氧猝灭剂,no形成量的增加能有效降低以o3为代表的ros的浓度。综上可知,可通过技术手段实现冷等离子体中活性成分的智能化调控,得到以活性氧或活性氮为主导成分的冷等离子体。
8、沿面介质阻挡放电(sdbd)作为冷等离子体的一种形成方式,具有空气放电、处理面积大、放电功率低、制作成本低等优点。当sdbd组件选用柔性材料时,可形成柔性等离子体,弯曲贴附于物体/人体表面,不受表面形态的限制,更适用于皮肤表面伤口治疗,特别是大面积的创面治疗。
9、在伤口监测方面,目前主要手段通过相应传感器件,监测伤口ph值、温度、血氧饱和度、拉伸情况、液体渗出情况、光谱信息等。例如,ph是伤口状态地一项重要判定指标,弱酸性环境利于成纤维细胞增殖、血管生成等,而弱碱性环境则利于细菌增生。因此,若传感器件测得伤口ph呈上升趋势,则存在炎症风险。前述各类传感器的原理及工作方式均为广谱已知信息,因此此处不进行详细阐明。
10、在伤口监测及治疗方面,现有技术已提出使用单一或多种传感器监测伤口信息,并通过信号反馈进行等离子体治疗。如专利号为cn 110268807 a的专利文件公开的平面柔性覆盖组件,可在不将该覆盖组件从身体区域取下的情况下,通过至少一个集成的传感器得到身体区域的至少一个参数,实现关于等离子体处理和必要时的伤口愈合过程说明。
11、类似于专利号为cn 110268807 a的专利文件公开的平面柔性覆盖组件,存在治疗方式单一、无法实现不同伤口愈合阶段的针对性治疗等问题。未经调控的接近室温的柔性冷等离子体是一个以ros为主要成分的氧化性体系,目前主要应用于感染性伤口的治疗,主要通过灭活感染性病原体实现。但在伤口愈合的不同阶段具有关键作用的冷等离子体成分实则不同,例如具有强氧化性的ros可快速消杀病原体,在伤口感染期间具有显著作用;而伤口增殖和重塑期的关键促进因素则是rns。现有技术未对柔性等离子体中活性成分进行调控,因此无法实现不同愈合阶段的针对性治疗,导致治疗效率低、周期长。
技术实现思路
1、由于现有技术存在的上述问题,本发明提出一种智能化伤口治疗装置,通过该装置实现的治疗方法是一种提高了冷等离子体治疗效率,缩短冷等离子体治疗周期的智能化伤口方法。
2、本发明可通过以下技术方案实现:
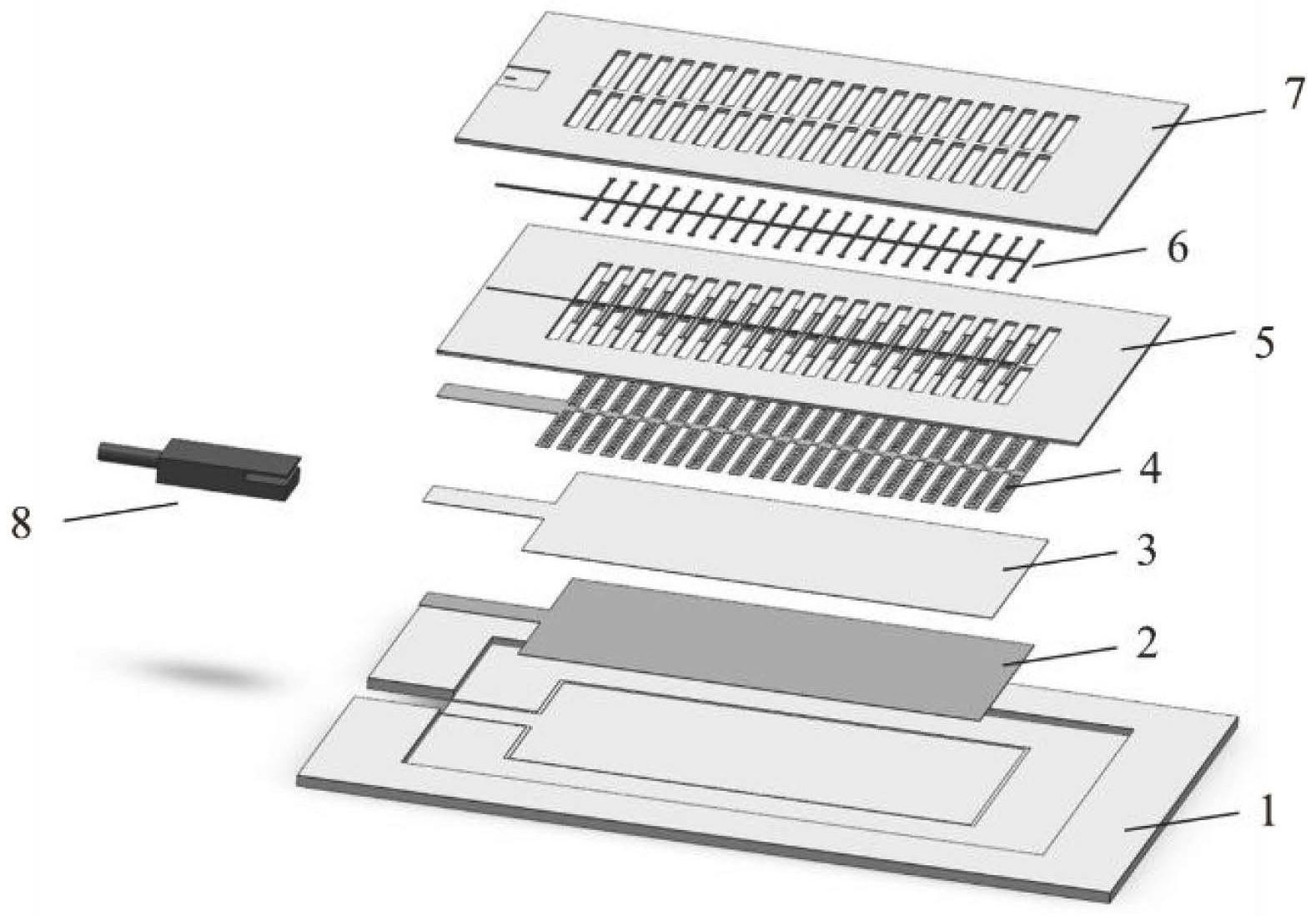
3、一种智能化伤口治疗装置,从下至上依次包括柔性外壳、第一柔性等离子体电极、柔性介质层、第二柔性等离子体电极、柔性基底层、伤口监测传感单元、柔性封装层,所述第一柔性等离子体电极、第二柔性等离子体电极通过接线端口与外接电源连接;所述柔性外壳设有一面开放的凹槽,一面开放的凹台和接触面,其中,所述凹槽用于内嵌第一柔性等离子体电极、柔性介质层、第二柔性等离子体电极组成的柔性等离子体发生单元;所述凹台用于内嵌所述伤口监测传感单元、柔性基底层及柔性封装层;所述接触面设有医用压敏胶;所述柔性基底层含两面开放的开槽和一面开放的凹槽,其中所述开槽与第二柔性等离子体电极位置对应,为柔性电极提供放电气隙,同时为冷等离子体提供流通通道,所述凹槽设于远离所述柔性外壳的一面,内嵌所述伤口监测传感单元;所述柔性封装层为用于封装所述柔性基底层及内嵌于柔性基底层中的伤口监测传感单元。
4、进一步地,所述柔性外壳为聚氨酯、硅橡胶、橡胶、硅胶、聚氯乙烯、聚乙烯、聚对二甲苯中单一/混合的柔性材质,厚度为1~5mm。
5、进一步地,所述第一柔性等离子体电极和第二柔性等离子体电极为石墨烯、纳米银、纳米金、镍石墨中单一/混合材质的柔性导电涂层及相应非导电基底,或为导电箔、导电丝、导电纳米管、导电膜、导电纤维、导电布材质的柔性导电电极,厚度为几微米~几十微米。
6、进一步地,所述第一柔性等离子体电极的结构为与第二柔性等离子体电极尺寸规格对应的平板、条状、网状结构。
7、进一步地,所述柔性介质层为聚酰亚胺、硅橡胶、氟橡胶、聚对苯二甲酸乙二酯、聚二甲基硅氧烷、纳米二氧化硅中单一/混合的绝缘材质;所述柔性介质层尺寸规格不小于所述第一、第二柔性等离子体电极,厚度可为几十微米~几百微米。
8、进一步地,所述第二柔性等离子体电极电极结构为蛇形、马鞍形的易拉伸结构,或为蜂窝、正方形、长方形、圆形、正三角形规则排布的结构。
9、进一步地,所述第一柔性等离子体电极、第二柔性等离子体电极由高压驱动,工作模式分为“活性氧模式”及“活性氮模式”;所述“活性氧模式”通过幅值为0.15~2.6kv,频率为5~40khz的正弦输入、脉冲直流输入的激发形式实现;所述“活性氮模式”通过幅值为3.0~10kv,频率为5~40khz的正弦输入,调制部分采用脉冲重复率为200~1000hz,占空比为1~30%激发实现。
10、进一步地,所述柔性基底层为聚二甲基硅氧烷、硅橡胶、凝胶中单一/混合的非导电耐热材质,厚度为1~2.5mm。
11、进一步地,所述伤口监测传感单元含传感器和导线,厚度为0.5~2.0mm;所述伤口监测传感单元设有至少一个传感器;所述传感器为ph传感器、温度传感器、光学传感器、应变传感器、导电率传感器中一种或多种监测传感器,所述传感器为居中式或阵列式分布;所述导线为直线型或蛇形排布,外部由聚酰亚胺绝缘性材料封装,所述导线一端延伸至接线端口并通过电路与外接电源相连;所述伤口监测传感单元与柔性等离子体发生单元之间由延伸至接线端口的柔性基底层隔开。
12、进一步地,所述柔性封装层为聚二甲基硅氧烷、硅橡胶、凝胶中单一/混合的非导电耐热材质,厚度为0.01~0.5mm;所述柔性封装层设有两面开放、与第二柔性等离子体电极以及所述柔性外壳上的开槽位置对应的开槽、接线端口卡槽;所述柔性封装层上的开槽为柔性电极提供放电气隙,同时为冷等离子体提供流通通道,使其直达皮肤表面,并具有热量缓冲的功能,使得任何模式下达到皮肤表面的等离子体温度均接近于室温;所述接线端口卡槽与接线端口相连。
13、本发明提出的通过以上一种智能化伤口治疗装置实现的伤口治疗方法,包括以下步骤:
14、1)采用伤口监测传感单元进行伤口监测,实时反馈伤口状态;
15、2)采用沿面介质阻挡放电(sdbd)结构的柔性等离子体发生单元,在此基础上使用调控电参数的手段,通过相对低压的激发条件得到以活性氧为主要成分的具有灭活病原体效果的“活性氧模式”等离子体;通过相对高压的激发条件得到以活性氮为主要成分的促进伤口增殖重塑的“活性氮模式”等离子体,二者均放电稳定,接触温度均接近于室温,无烫伤风险;
16、3)根据步骤1)得到的伤口状态,对处于止血、炎症阶段的伤口进行步骤2)所述的“活性氧模式”治疗;对处于增殖、重塑阶段的伤口进行步骤2)所述的“活性氮模式”治疗。
17、与现有技术相比,本发明具有以下有益效果:
18、1)本发明不仅可利用至少一种、至少一个伤口监测传感器实时监测伤口愈合状态,同时本发明支持利用多种、多个伤口监测传感器分区域实时监测伤口状态,由此实现对小面积、大面积伤口状态的准确分析;
19、2)本发明利用调控技术形成以活性氧或活性氮为主要成分的冷等离子体,可针对性的促进伤口度过伤口感染期或增殖重塑期,因此具有提高冷等离子体治疗效率,缩短冷等离子体治疗周期的效果;
20、3)本发明利用设有冷等离子体通道的柔性隔热层,提高放电稳定性的同时避免局部过热风险,确保不同模式下装置与皮肤接触温度均接近于室温;
21、4)根据伤口监测传感器设置情况,对应的,柔性等离子体发生单元可为一组或多组,由此可对小面积伤口进行针对性治疗,或可对大面积伤口进行分区域针对性治疗,进一步提高冷等离子体治疗效率,因而具有广阔的应用前景。
- 还没有人留言评论。精彩留言会获得点赞!