具有低峰-谷比的的制作方法
具有低峰-谷比的pth化合物
1.本技术是中国申请号为
2017800601397、发明名称为“具有低峰-谷比的pth化合物”且申请日为
2017年9月
28日的中国专利申请的分案申请。
2.本发明涉及包含pth化合物的药物组合物,其中在皮下施用后,pth化合物的药代动力学特性在一次注射间隔内表现出小于4的峰-谷比。
3.甲状旁腺功能减退症是罕见的钙和磷酸盐代谢的内分泌紊乱,其通常由于甲状旁腺在甲状腺手术过程中的损伤或去除而引起。
甲状旁腺功能减退症在内分泌失调中是不寻常的,因为它直到最近还没有用缺失的激素,甲状旁腺激素或pth替代治疗。
甲状旁腺功能减退症的常规疗法包括大剂量的维生素d和口服补钙,虽然通常是有效的,但与血ca2+
明显波动相关,导致高钙血症和低钙血症、尿钙排泄过多和肾钙质沉着症。
4.钙是人体中最丰富的矿物质,其严密的调节是许多关键生物功能所必需的,例如骨矿化、肌肉收缩、神经传导、激素释放和血液凝固。
特别重要的是保持钙浓度尽可能稳定,因为各种细胞系统或器官、包括中枢神经系统、肌肉和外/内分泌腺对ca2+
的微小变化具有高度敏感性。pth是钙稳态的主要调节剂。
5.与血清ca2+
浓度相关的不适当低的pth水平(甲状旁腺功能减退症的特征)导致肾小管对ca2+
的重吸收减少,同时导致肾小管对磷酸盐的重吸收增加。
因此,甲状旁腺功能减退症的主要生化异常是低钙血症和高磷酸盐血症。
该疾病的临床特征包括低钙血症的症状,例如口周麻木、感觉异常和腕骨/脚蹬肌肉痉挛。
喉痉挛、手足抽搐和发作是严重的且可能危及生命的并发症。
高磷酸盐血症和升高的钙x磷酸盐产物促进软组织、包括脉管系统、脑、肾和其他器官中不溶性钙磷酸盐复合物的异位沉积。
6.甲状旁腺功能减退症的标准疗法是口服钙和维生素d补充剂。
治疗的目标是a)改善低钙血症的症状;b)将空腹血清钙维持在或略低于低-正常范围;c)将空腹血清磷保持在高正常范围内或仅略微升高;d)避免或最大限度地减少高钙尿症;e)维持钙-磷酸盐产品的水平远低于正常上限和f)避免肾脏(结石和肾钙质沉着症)和其他软组织的异位钙化。
7.长期大剂量使用钙和活性维生素d会产生一些问题,特别是在高钙尿症、肾结石、肾钙质沉着和异位软组织钙化方面。
此外,用钙和活性维生素d的常规疗法无法缓解生活质量诉怨,也不能逆转疾病的骨重塑特征的异常。
简言之,对甲状旁腺功能减退症的改进疗法的需求很高。
8.在
2015年,natpara,pth(1-84)被批准用于每日一次皮下注射,作为甲状旁腺功能减退症患者的维生素d和钙的辅助。natpara,pth(1-84)被批准控制低钙血症,是基于一项关键性试验,证明了
42%的pth(1-84)治疗参与者在减少剂量的钙补充剂和活性形式的维生素d下达到了正常的血钙水平,相比之下安慰剂治疗参与者为3%。
在注射后监测血清钙的时间过程中,
71%的用pth(1-84)治疗的患者在
24小时期间的一次或多次测量中发生高钙血症。pth(1-84)在注射后
2-8小时减少尿钙排泄,但在
24小时内,尿钙排泄没有变化。
类似地,尿磷酸盐排泄仅在注射pth(1-84)后的前8小时期间增加。
9.虽然这代表了疾病治疗的重要进展,但相对于在治疗患者中的常规疗法,natpara尚未证明能够降低高钙血症(升高的血清钙水平)、低钙血症(低血清钙)或高钙尿症(升高
的尿钙)的发生率。
10.因此,非常需要改进的基于pth的用于甲状旁腺功能减退症的疗法。
11.pth(1-34)或特立帕肽于
2002年被fda批准用于治疗骨质疏松症。
尽管未被批准用于该适应症,但pth(1-34)历来用于治疗甲状旁腺功能减退症,患者每天接受两次或三次注射。
为了促进更多的生理学pth水平,已经进行了临床研究,其中与每日两次注射相比,pth(1-34)通过泵递送施用。
超过6个月,泵输送产生正常、稳态钙水平,波动最小,并避免了血清和尿钙水平升高,这在注射pth后很快就会明显。
当通过泵施用pth(1-34)时尿钙排泄的显著减少可表明pth必须连续暴露于肾小管以实现肾钙保存效果。pth(1-34)的泵输送实现了骨转换、血清钙和尿钙排泄标记物的同时标准化。
与每日两次pth(1-34)注射方案相比,通过每日较低剂量的pth(1-34)和镁补充需求减少实现了这些结果。
12.然而,连续泵疗法对患者来说是不方便和具有挑战性的,并且本发明的目的是提供更便利的、提供连续暴露于pth的治疗选择。
13.pth的长期推注施用与骨代谢增加引起的进行性骨皮质丢失有关。
在用pth(1-84)治疗的患者的6年随访中(rubin,jcem 2016),骨转换标志物仍然大于治疗前的值,在pth(1-84)开始后的早期年间达到峰值并且此后下降,但是截止到第6年仍然显著高于基线值。
通过双重x-射线吸收测定法(dxa)测得的骨矿物质密度(bmd)与pth的已知部位特异性影响一致,即在腰椎中增加和在远端
1/3半径处下降(i/3半径)。
在远端i/3半径处观察到的减少与间歇性pth增加皮质孔隙度和骨内膜再吸收的已知效果一致。
14.本发明的一个目的是提供间歇施用pth的方法,其比目前应用的pth疗法具有更低的骨转换标记物的升高。
优选地,间歇是指每日间隔,或者可选地或更优选地每周间隔。
15.在forteo,pth(1-34)和natpara,pth(1-84)的临床前期开发计划中,在每日注射pth化合物治疗的大鼠中观察到骨肉瘤发生率的剂量依赖性增加。
在natpara研究中,由于该组中主要来自转移性骨肉瘤的过度死亡,因此,对大鼠停止给予高剂量。
16.因此,本发明的一个目的是提供间歇性pth替代疗法,其以较低的施用剂量提供症状控制。
优选地,间歇是指每日间隔,或者可选地或更优选地每周间隔。
17.总之,对于更便利且更安全的、副作用减少的甲状旁腺功能减退症的治疗方法存在需求。
18.因此,本发明的目的是至少部分地克服上述缺陷。
19.该目的通过包含pth化合物的药物组合物实现,其中在施用后、优选皮下施用后,pth化合物的药代动力学特性在一次注射间隔内表现出小于4的峰-谷比。
20.令人惊讶地发现,这种pth化合物能够实现pth的稳定血浆曲线,其确保生理血清和尿钙水平乃至与健康受试者中测量的相差无几的降低的尿钙水平。
21.在本发明中,使用的术语具有如下含义。
22.如本文所用,术语“注射间隔”是指两次连续施用本发明药物组合物之间的时间。
23.如本文所用,术语“稳态”是指在连续两次施用之间以恒定的时间间隔向患者施用多次恒定剂量如经过
3、4、5、6、7或以上次恒定剂量后实现的状态,该状态的特征在于pth化合物的血浆水平(如果pth化合物不释放pth即是稳定的pth化合物),或释放pth(如果pth化合物是控释pth化合物)的血浆水平,在间隔的开始和结束时变化不超过
10%,优选不超过
7.5%,甚至更优选不超过5%,甚至更优选不超过4%,且最优选不超过3%。
术语“间隔开
始”是指施用剂量的时间点,而术语“间隔结束”是指施用下一剂量的时间点。
24.如本文所用,术语“峰-谷比”是指稳态下pth化合物的最高血浆浓度与最低血浆浓度之间的比,如果pth化合物不释放pth即是稳定的pth化合物,或如果pth化合物是控释pth化合物时的释放的pth的比,在两次连续给非人灵长类动物、优选为食蟹猴(cynomolgus monkey)施用之间的时间期限内。
然而,由于游离pth与总pth之间存在良好的相关性(即仍然包含在pth化合物和释放的pth中的pth的总和),因此总pth提供了足够好的近似性。
两次连续施用之间的时间期限也称为“注射间隔”,“施用间隔”或“间隔”。
25.如本文所用,术语“控释pth化合物”是指包含至少一种pth分子或pth部分的任意的化合物、缀合物、晶体或混合物,并且至少一种pth分子或pth部分从其中释放,其中释放半衰期为至少
12小时。
26.如本文所用,术语“释放半衰期”和“半衰期”是指在生理条件下(即水性缓冲液
,ph 7.4,37℃)直至被包含在控释pth化合物中的所有pth或pth部分的一半从所述控释pth化合物中释放所需的时间。
27.如本文所用,术语“稳定的pth化合物”是指至少一个pth部分与另一个部分的任意共价缀合物,其中至少一个pth部分通过稳定的连接键连接至所述另一个部分。
28.如本文所用,术语“pth”是指所有的pth多肽,优选地来自哺乳动物物种,更优选地来自人和哺乳动物物种,更优选地来自人和鼠物种,及其变体、类似物、直向同源物、同系物和其衍生物和片段,其特征在于升高的血清钙和肾磷排泄和减少的血清磷和肾钙排泄。
术语“pth”还指所有的pth-相关多肽(pthrp),例如seq id no:121的多肽,其结合至并且活化共有的pth/pthrp1受体。
优选地,术语“pth”是指seq id no:51的pth多肽及其基本上表现出相同生物活性的变体、同系物和衍生物,即升高血清钙和肾磷排泄和减少血清磷和肾钙排泄。
29.优选地,术语“pth”是指如下多肽序列:
30.seq id no:
1(pth 1-84)[0031][0032]seq id no:
2(pth 1-83)[0033][0034]seq id no:
3(pth 1-82)[0035][0036]seq id no:
4(pth 1-81)[0037][0038]seq id no:
5(pth 1-80)[0039][0040]seq id no:
6(pth 1-79)[0041][0042]seq id no:
7(pth 1-78)[0043][0044]seq id no:
8(pth 1-77)[0045][0046]seq id no:
9(pth 1-76)[0047][0048]seq id no:
10(pth 1-75)[0049][0050]seq id no:
11(pth 1-74)[0051][0052]seq id no:
12(pth 1-73)[0053][0054]seq id no:
13(pth 1-72)[0055][0056]seq id no:
14(pth 1-71)[0057][0058]seq id no:
15(pth 1-70)[0059][0060]seq id no:
16(pth 1-69)[0061][0062]seq id no:
17(pth 1-68)[0063][0064]seq id no:
18(pth 1-67)[0065][0066]seq id no:
19(pth 1-66)[0067][0068]seq id no:
20(pth 1-65)[0069][0070]seq id no:
211(pth 1-64)[0071][0072]seq id no:
22(pth 1-63)[0073][0074]seq id no:
23(pth 1-62)[0075][0076]seq id no:
24(pth 1-61)[0077][0078]seq id no:
25(pth 1-60)[0079][0080]seq id no:
26(pth 1-59)[0081][0082]seq id no:
27(pth 1-58)[0083][0084]seq id no:
28(pth 1-57)[0085][0086]seq id no:
29(pth 1-56)[0087][0088]seq id no:
30(pth 1-55)[0089][0090]seq id no:
31(pth 1-54)[0091][0092]seq id no:
32(pth 1-53)[0093][0094]seq id no:
33(pth 1-52)[0095][0096]seq id no:
34(pth 1-51)[0097][0098]seq id no:
35(pth 1-50)[0099][0100]seq id no:
36(pth 1-49)[0101][0102]seq id no:
37(pth 1-48)[0103][0104]seq id no:
38(pth 1-47)[0105][0106]seq id no:
39(pth 1-46)[0107][0108]seq id no:
40(pth 1-45)[0109][0110]seq id no:
41(pth 1-44)[0111][0112]seq id no:
42(pth 1-43)[0113][0114]seq id no:
433(pth 1-42)[0115][0116]seq id no:
444(pth 1-41)[0117][0118]seq id no:
455(pth 1-40)[0119][0120]seq id no:
46(pth 1-39)[0121][0122]seq id no:
47(pth 1-38)[0123][0124]seq id no:
488(pth 1-37)[0125][0126]seq id no:
49(pth 1-36)[0127][0128]seq id no:
50(pth 1-35)[0129][0130]seq id no:
51(pth 1-34)[0131][0132]seq id no:
52(pth 1-33)[0133][0134]seq id no:
53(pth 1-32)[0135][0136]seq id no:
54(pth 1-31)[0137][0138]seq id no:
55(pth 1-30)[0139][0140]seq id no:
56(pth 1-29)[0141][0142]seq id no:
57(pth 1-28)[0143][0144]seq id no:
58(pth 1-27)[0145][0146]seq id no:
59(pth 1-26)[0147][0148]seq id no:
60(pth 1-25)[0149][0150]seq id no:
61(酰胺化pth 1-84)[0151]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkadvnvltkaksq;其中c-末端酰胺化seq id no:
62(酰胺化pth 1-83)[0152]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkadvnvltkaks;其中c-末端酰胺化seq id no:
63(酰胺化pth 1-82)[0153]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkadvnvltkak;其中c-末端酰胺化
[0154]seq id no:64(酰胺化pth 1-81)[0155]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkadvnvltka;其中c-末端酰胺化
[0156]seq id no:65(酰胺化pth 1-80)[0157]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkadvnvltk;其中c-末端酰胺化
[0158]seq id no:66(酰胺化pth 1-79)[0159]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkadvnvlt;其中c-末端酰胺化
[0160]seq id no:67(酰胺化pth 1-78)[0161]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkadvnvl
;其中c-末端酰胺化
[0162]seq id no:68(酰胺化pth 1-77)[0163]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkadvnv;其中c-末端酰胺化
[0164]seq id no:69(酰胺化pth 1-76)[0165]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkadvn;其中c-末端酰胺化
[0166]seq id no:70(酰胺化pth 1-75)[0167]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkadv;其中c-末端酰胺化
[0168]seq id no:71(酰胺化pth 1-74)[0169]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadkad;其中c-末端酰胺化
[0170]seq id no:72(酰胺化pth 1-73)[0171]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadka;其中c-末端酰胺化
[0172]seq id no:73(酰胺化pth 1-72)[0173]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgeadk;其中c-末端酰胺化
[0174]seq id no:74(酰胺化pth 1-71)[0175]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgead;其中c-末端酰胺化
[0176]seq id no:75(酰胺化pth 1-70)[0177]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslgea;其中c-末端酰胺化
[0178]seq id no:76(酰胺化pth 1-69)[0179]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslge;其中c-末端酰胺化
[0180]seq id no:77(酰胺化pth 1-68)[0181]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshekslg;其中c-末端酰胺化
[0182]seq id no:78(酰胺化pth 1-67)[0183]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlvesheksl
;其中c-末端酰胺化
[0184]seq id no:79(酰胺化pth 1-66)[0185]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlvesheks;其中c-末端酰胺化
[0186]seq id no:80(酰胺化pth 1-65)[0187]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshek;其中c-末端酰胺化
[0188]seq id no:81(酰胺化pth 1-64)[0189]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlveshe;其中c-末端酰胺化
[0190]seq id no:82(酰胺化pth 1-63)[0191]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlvesh;其中c-末端酰胺化
[0192]seq id no:83(酰胺化pth 1-62)[0193]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlves;其中c-末端酰胺化
[0194]seq id no:84(酰胺化pth 1-61)[0195]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlve;其中c-末端酰胺化
[0196]seq id no:85(酰胺化pth 1-60)[0197]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvlv;其中c-末端酰胺化
[0198]seq id no:86(酰胺化pth 1-59)[0199]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednvl
;其中c-末端酰胺化
[0200]seq id no:87(酰胺化pth 1-58)[0201]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkednv;其中c-末端酰胺化
[0202]seq id no:88(酰胺化pth 1-57)[0203]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkkedn;其中c-末端酰胺化
[0204]seq id no:89(酰胺化pth 1-56)[0205]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkked;其中c-末端酰胺化
[0206]seq id no:90(酰胺化pth 1-55)[0207]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkke;其中c-末端酰胺化
[0208]seq id no:91(酰胺化pth 1-54)[0209]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprkk;其中c-末端酰胺化
[0210]seq id no:92(酰胺化pth 1-53)[0211]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrprk;其中c-末端酰胺化
[0212]seq id no:93(酰胺化pth 1-52)[0213]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdagsqrpr;其中c-末端酰胺化
[0214]seq id no:94(酰胺化pth 1-51)[0215]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdags qrp;其中c-末端酰胺化
[0216]seq id no:95(酰胺化pth 1-50)[0217]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdags qr;其中c-末端酰胺化
[0218]seq id no:96(酰胺化pth 1-49)[0219]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdags q;其中c-末端酰胺化
[0220]seq id no:97(酰胺化pth 1-48)[0221]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdags;其中c-末端酰胺化
[0222]seq id no:98(酰胺化pth 1-47)[0223]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprdag;其中c-末端酰胺化
[0224]seq id no:99(酰胺化pth 1-46)[0225]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprda;其中c-末端酰胺化
[0226]seq id no:100(酰胺化pth 1-45)[0227]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplaprd;其中c-末端酰胺化
[0228]seq id no:101(酰胺化pth 1-44)[0229]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplapr;其中c-末端酰胺化
[0230]seq id no:102(酰胺化pth 1-43)[0231]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgaplap;其中c-末端酰胺化
[0232]seq id no:103(酰胺化pth 1-42)[0233]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgapla;其中c-末端酰胺化
[0234]seq id no:104(酰胺化pth 1-41)[0235]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgapl
;其中c-末端酰胺化
[0236]seq id no:105(酰胺化pth 1-40)[0237]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalgap;其中c-末端酰胺化
[0238]seq id no:106(酰胺化pth 1-39)[0239]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalga;其中c-末端酰胺化
[0240]seq id no:107(酰胺化pth 1-38)[0241]svseiqlmhnlgkhlnsmervewlrkklqdvhnfvalg;其中c-末端酰胺化
[0242]seq id no:108(酰胺化pth 1-37)[0243]svseiqlmhnlgkhlnsmervewlrkklqdvhnfval
;其中c-末端酰胺化
[0244]seq id no:109(酰胺化pth 1-36)[0245]svseiqlmhnlgkhlnsmervewlrkklqdvhnfva;其中c-末端酰胺化
[0246]seq id no:110(酰胺化pth 1-35)[0247]svseiqlmhnlgkhlnsmervewlrkklqdvhnfv;其中c-末端酰胺化seq id no:111(酰胺化pth 1-34)[0248]svseiqlmhnlgkhlnsmervewlrkklqdvhnf;其中c-末端酰胺化seq id no:112(酰胺化pth 1-33)[0249]svseiqlmhnlgkhlnsmervewlrkklqdvhn;其中c-末端酰胺化seq id no:113(酰胺化pth 1-32)[0250]svseiqlmhnlgkhlnsmervewlrkklqdvh;其中c-末端酰胺化
[0251]seq id no:114(酰胺化pth 1-31)[0252]svseiqlmhnlgkhlnsmervewlrkklqdv;其中c-末端酰胺化
[0253]seq id no:115(酰胺化pth 1-30)[0254]svseiqlmhnlgkhlnsmervewlrkklqd;其中c-末端酰胺化
[0255]seq id no:116(酰胺化pth 1-29)[0256]svseiqlmhnlgkhlnsmervewlrkklq;其中c-末端酰胺化
[0257]seq id no:117(酰胺化pth 1-28)[0258]svseiqlmhnlgkhlnsmervewlrkkl
;其中c-末端酰胺化
[0259]seq id no:118(酰胺化pth 1-27)[0260]svseiqlmhnlgkhlnsmervewlrkk;其中c-末端酰胺化
[0261]seq id no:119(酰胺化pth 1-26)[0262]svseiqlmhnlgkhlnsmervewlrk;其中c-末端酰胺化
[0263]seq id no:120(酰胺化pth 1-25)[0264]svseiqlmhnlgkhlnsmervewlr;其中c-末端酰胺化
[0265]seq id no:121(pthrp)[0266][0267]更优选地,术语“pth”是指seq id:nos 47、48、49、50、51、52、53、54、55、107、108、109、110、111、112、113、114和
115的序列。
甚至更优选地,术语“pth”是指seq id:nos 50、51、52、110、111和
112的序列。
在特别优选的实施方案中,术语“pth”是指seq id:no 51的序列。
[0268]如本文所用,术语“pth多肽变体”是指来自相同物种的多肽,其不同于参比pth或pthrp多肽。
优选地,这种参比物是pth多肽序列并具有seq id no:
51的序列。
通常,差异是有限的,使得参比物和变体的氨基酸序列总体上非常相似,并且在许多区域中是相同的。
优选地,pth多肽变体与参比pth或pthrp多肽、优选与seq id no:
51的pth多肽具有至少
70
%、80
%、90
%或
95%的同一性。
所谓氨基酸序列至少、例如
95%“等同于”查询氨基酸序列的多肽,预期为主题多肽的氨基酸序列与查询序列相同,但主题多肽序列可以包括查询氨基酸序列每
100
个氨基酸最多五个氨基酸改变。
参比序列的这些改变可以发生在参比氨基酸序列的氨基(n-末端)或羧基末端(c-末端)位置或这些末端位置之间的任何位置,分别散布在
参比序列的残基中或在参比序列内一个或更多的连续组中。
查询序列可以是参比序列的完整氨基酸序列或如本文所述指定的任何片段。
优选地,查询序列是seq id no:
51的序列。
[0269]此类pth多肽变体可以是天然存在的变体,例如由占据染色体或生物体上的给定基因座的pth或pthrp的几种替代形式之一编码的天然存在的等位基因变体,或由天然存在的来源于单一初级转录物的剪接变体编码的同种型。
或者,pth多肽变体可以是未知天然存在且可以通过本领域已知的诱变技术制备的变体。
[0270]本领域已知可以从生物活性多肽的n-末端或c-末端缺失一个或多个氨基酸而基本上不丧失生物学功能。
这种n-和/或c-末端缺失也包括在术语pth多肽变体中。
[0271]本领域普通技术人员还认识到,可以改变pth或pthrp多肽的一些氨基酸序列,而不会显著影响多肽的结构或功能。
这些突变体包括根据本领域已知的一般规则选择的缺失、插入、倒位、重复和取代,以便对活性几乎没有影响。
例如,bowie等人(1990),science 247:
1306-1310提供了关于如何进行表型沉默氨基酸取代的指导,其全部内容通过引用并入本文,其中作者指出有两种主要方法用于研究氨基酸序列的改变耐受性。
[0272]术语pth多肽还包括由pth和pthrp类似物、直向同源物(orthologs)和/或物种同系物编码的所有pth和pthrp多肽。
本领域普通技术人员还认识到pthrp和pthrp类似物结合以激活常见的pth/pthrp1受体,因此术语pth多肽也包括所有pthrp类似物。
如本文所用,术语“pth类似物”是指不同和不相关生物的pth和pthrp,其在每个生物体中执行相同的功能但不是源自生物体祖先共有的祖先结构。
相反,类似的pth和pthrp分别产生,然后演变为执行相同或类似的功能。
换句话说,类似的pth和pthrp多肽是具有非常不同的氨基酸序列但执行相同生物活性的多肽,即提高血清钙和肾磷排泄,以及降低血清磷和肾钙排泄。
[0273]如本文所用,术语“pth直向同源物”是指两种不同物种内的pth和pthrp,这些序列通过祖先物种中的共同同源pth或pthrp彼此相关,但它们已经进化成彼此不同。
[0274]如本文所用,术语“pth同系物”是指不同生物体的pth和pthrp,其在每个生物体中发挥相同的功能并且源自生物体祖先共有的祖先结构。
换句话说,同系pth多肽是具有非常相似的氨基酸序列的多肽,其执行相同的生物活性,即提高血清钙和肾磷排泄,并降低血清磷和肾钙排泄。
优选地,pth多肽同系物可以定义为与参比pth或pthrp多肽、优选seq id no:
51的pth多肽表现出至少
40
%、50
%、60
%、70
%、80
%、90
%或
95%同一性的多肽。
[0275]因此,本发明的pth多肽可以是例如:(i)其中至少一个氨基酸残基被保守或非保守氨基酸残基、优选保守氨基酸残基取代,且这种取代的氨基酸残基可能是也可能不是遗传密码编码的;和/或(ii)其中氨基酸残基的至少一个包含取代基;和/或(iii)其中pth多肽与另一种化合物融合,例如增加多肽半衰期的化合物(例如聚乙二醇);和/或(iv)其中额外的氨基酸融合至pth多肽,例如igg fc融合区多肽或前导序列或分泌序列(secretory sequence)或用于纯化上述形式的多肽的序列或前蛋白质(pre-protein)序列。
[0276]如本文所用,术语“pth多肽片段”是指包含pth或pthrp多肽、优选seq id no:
51的多肽的部分氨基酸序列的毗连区的任何多肽。
[0277]更具体地,pth多肽片段包含pth或pthrp多肽、更优选seq id no:
51的多肽的至少6个、例如至少8个、至少
10个或至少
17个连续氨基酸。pth多肽片段可另外描述为包含至少6个氨基酸的pth或pthrp多肽的亚属,其中“至少
6”定义为6和表示pth或pthrp多肽、优选seq id no:
51的多肽的c-末端氨基酸的整数之间的任何整数。
进一步包括长度为至少6个氨基
酸的pth或pthrp多肽片段的种类,如上所述,其进一步根据其n-末端和c-末端位置进行说明。
作为单个物种的术语“pth多肽片段”还包括所有pth或pthrp多肽片段,其长度至少为6个氨基酸,如上所述,其可特别由n-末端和c-末端位置指定。
也就是说,在pth或pthrp多肽、优选地seq id:no51的pth多肽的任何给定氨基酸序列上,长度至少6个连续氨基酸残基的片段可占据的n末端和c末端位置的每个组合均包括在本发明中。
[0278]术语“pth”还包括具有如上所述序列的聚(氨基酸)缀合物,但具有包含酰胺和非酰胺连接键的骨架,例如酯连接键,例如缩酚酸肽(depsipeptide)。
缩酚酸肽是氨基酸残基的链,其中骨架包含酰胺(肽)和酯键。
因此,如本文所用,术语“侧链”是指与氨基酸部分的
α-碳连接的部分,如果氨基酸部分通过胺键连接如在多肽中,或指连接到聚(氨基酸)缀合物骨架上的任何含碳原子的部分,例如在缩酚酸肽的情况下。
优选地,术语“pth”是指具有通过酰胺(肽)键形成的骨架的多肽。
[0279]由于术语pth包括pth和pthrp的上述变体、类似物、直向同源物、同系物、衍生物和片段,所有对参比序列内特定位置的引用还包括pth或pthrp部分的变体、类似物、直向同源物、同系物、衍生物和片段中的等同位置,即使没有特别提及。
[0280]如本文所用,术语“胶束”是指分散在液体胶体中的两亲分子的聚集体。
在水溶液中,典型的胶束形成聚集体,其中表面活性剂分子的亲水部分面向周围溶剂,表面活性剂分子的疏水部分面向内部,也称为“正相胶束”。“反向胶束”具有面向内部的亲水部分和面向周围溶剂的疏水部分。
[0281]如本文所用,术语“脂质体”是指具有至少一个脂质双层的囊泡、优选球形囊泡。
优选地,脂质体包含磷脂,甚至更优选磷脂酰胆碱。
术语“脂质体”是指各种结构和大小,例如具有多于一个同心脂双层、平均直径为
100
至
1000nm的多层脂质体囊泡(mlv)、具有一个脂双层和平均直径为
25至
100nm的小单层脂质体囊泡(suv)、具有一个脂双层且平均直径约为
1000
μm的大单层脂质体囊泡(luv)和具有一个脂双层且平均直径为
1-100
μm的巨单层囊泡(guv)。
术语“脂质体”还包括弹性囊泡,例如转移体(transferosome)和醇质体(ethosomes)。
[0282]如本文所用,术语“超声水凝胶(aquasome)”是指直径为
60-300nm的球形纳米粒,其包含至少三层自组装结构,即涂有寡聚化膜的固相纳米晶体核,药物分子在有或没有药物改性的情况下被吸附到该寡聚化膜上。
[0283]如本文所用,术语“醇质体”是指脂质囊泡包含磷脂和相对高浓度的乙醇和/或异丙醇以及水,其具有的尺寸范围在数十纳米至微米。
[0284]如本文所用,术语“leciplex”是指带正电荷基于磷脂的囊泡系统,其包含大豆pc、阳离子试剂和生物相容性溶剂如peg 300、peg 400、二乙二醇单乙醚、四氢糠醇聚乙二醇醚或
2-吡咯烷酮或n-甲基-2-吡咯烷酮。
[0285]如本文所用,术语“类脂质体(niosome)”是指包含非离子表面活性剂的单层或多层囊泡。
[0286]如本文所用,术语“药质体(pharmacosome)”是指来自与生物活性部分共价结合的脂质的超细囊泡、胶束或六边形聚集体。
[0287]如本文所用,术语“前类脂质体(proniosome)”是指表面活性剂涂覆的载体的干制剂,其经再水化和适度搅拌得到类脂质体。
[0288]如本文所用,术语“聚合物囊泡(polymersome)”是指一种人造球形囊泡,其包含由两亲性合成嵌段共聚物形成的膜,并且可任选地在其核心中包含水溶液。
聚合物囊泡具有的直径范围在
50nm至5μm或更大。
该术语还包括合成体(syntosome),其是被改造成包含允许某些化学物质通过膜进入或离开囊泡的通道的聚合物囊泡。
[0289]如本文所用,术语“sphingosome”是指同心的双层囊泡,其中水性体积完全被主要由天然或合成鞘脂组成的膜脂双层包围。
[0290]如本文所用,术语“转移体”是指包含水性核心的超柔性脂质囊泡,由共同的极性和适合的边缘活化的脂质的混合物形成,其促进高度弯曲的双层的形成,这使得转移体高度可变形。
[0291]如本文所用,术语“ufasome”是指包含不饱和脂肪酸的囊泡。
[0292]如本文所用,术语“多肽”是指包含至多且包括
50
个氨基酸单体的肽。
[0293]如本文所用,术语“蛋白质”是指超过
50
个氨基酸残基的肽。
优选地,蛋白质包含至多
20000
个氨基酸残基,例如至多
15000
个氨基酸残基,例如至多
10000
个氨基酸残基,例如至多
5000
个氨基酸残基,例如至多
4000
个氨基酸残基,例如至多
3000
个氨基酸残基,例如至多
2000
个氨基酸残基,例如至多
1000
个氨基酸残基。
[0294]如本文所用,术语“生理条件”是指在ph 7.4,37℃
的水性缓冲剂。
[0295]如本文所用,术语“药物组合物”是指组合物,其含有一种或多种活性成分,例如至少一种控释pth化合物,和一种或多种赋形剂,以及任何产品,其直接或间接地来自组合物成分的任何两种或更多种的组合、络合或聚集,或来自成分的一种或多种的解离,或来自成分的一种或多种的其它类型的反应或相互作用。
因此,本发明的药物组合物包括通过混合一种或多种控释pth化合物和药学上可接受的赋形剂制备的任何组合物。
[0296]如本文所用,术语“液体组合物”是指包含水溶性pth化合物、优选水溶性控释pth化合物和一种或多种溶剂如水的混合物。
[0297]术语“悬浮液组合物”涉及包含水不溶性pth化合物、优选水不溶性控释pth化合物和一种或多种溶剂如水的混合物。
[0298]如本文所用,术语“干组合物”是指以干形式提供的药物组合物。
适合的干燥方法是喷雾干燥和冻干,即冷冻干燥。
根据karlfischer测定,这类干前药组合物具有最大
10%、优选小于5%、更优选小于2%的残余水含量。
优选地,通过冻干干燥来干燥本发明的药物组合物。
[0299]如本文所用的术语“药物”是指用于治疗、治愈、预防或诊断疾病或用于以其它方式增强身体或精神健康的物质,例如pth。
如果药物与另一部分缀合,则源自该药物的所得产物部分称为“生物活性部分”。
[0300]如本文所用,术语“前药”是指缀合物,其中生物活性部分通过可逆连接基部分、也称作“可逆前药连接基部分”可逆地和共价地连接至特化的保护基团,其包含与生物活性部分的可逆连接,并且其中所述专门的保护基团改变或消除母体分子中的不希望的性质。
这还包括增强药物中所需的性质和抑制不希望的性质。
专门的无毒保护基称为“载体”。
前药以其相应药物的形式释放可逆和共价结合的生物活性部分。
换句话说,前药是包含生物活性部分的缀合物,所述生物活性部分通过可逆的前药连接基部分与载体部分共价和可逆地缀合,所述载体与可逆的前药连接基部分的共价和可逆缀合是直接的或通过间隔基。
这类
缀合物以游离药物的形式释放先前缀合的生物活性部分。
[0301]如本文所用,术语“可逆的前药连接基部分”是间隔基部分,其将生物活性部分如pth部分与载体部分直接或通过另外的间隔基部分连接,并且其中可逆的前药连接基部分与生物活性部分之间的连接键是可逆的。
优选地,载体部分和可逆的前药连接基部分之间的连接键是稳定的。
[0302]“可生物降解的连接键”或“可逆连接键”是在不存在酶、在生理条件下(ph7.4,37℃
的水性缓冲液)下可水解降解,即可裂解的连接键,半衰期为1小时至3个月,优选1小时至2个月,甚至更优选1小时至1个月,甚至更优选1小时至3周,最优选1小时至2周。
因此,“稳定的连接键”是在生理条件(ph7.4、37℃
的水性缓冲液)下具有超过三个月半衰期的连接键。
[0303]如本文所用,术语“无痕迹前药连接基”是指可逆的前药连接基,即可逆和共价连接生物活性部分与载体的连接基部分。
其在裂解时以其游离形式释放药物。
如本文所用,术语药物的“游离形式”是指处于其未修饰的药理学活性形式的药物。
[0304]如本文所用,术语“赋形剂”是指与治疗剂如药物或前药一起施用的稀释剂、佐剂或载体。
这种药物赋形剂可以是无菌液体,例如水和油,包括石油、动物、植物或合成来源的那些,包括但不限于花生油、大豆油、矿物油、芝麻油等。
当药物组合物口服给药时,水是优选的赋形剂。
当静脉内施用药物组合物时,盐水和右旋糖水溶液是优选的赋形剂。
盐水溶液和右旋糖水溶液和甘油溶液优选用作可注射溶液的液体赋形剂。
合适的药物赋形剂包括淀粉、葡萄糖、乳糖、蔗糖、甘露醇、海藻糖、明胶、麦芽、稻米、面粉、白垩、硅胶、硬脂酸钠、甘油单硬脂酸酯、滑石粉、氯化钠、脱脂奶粉、甘油、丙二醇、水、乙醇等。
如果需要,药物组合物还可含有少量的润湿剂或乳化剂、ph缓冲剂,例如乙酸盐、琥珀酸盐、三羟甲基氨基甲酸盐、碳酸盐、磷酸盐、hepes(4-(2-羟乙基)-1-哌嗪乙磺酸)、mes(2-(n-吗啉代)乙磺酸),或可含有洗涤剂,如吐温、泊洛沙姆、poloxamines、chaps、igepal
或氨基酸,如甘氨酸、赖氨酸或组氨酸。
这些药物组合物可以采取溶液、悬浮液、乳液、片剂、丸剂、胶囊、粉末、缓释制剂等形式。
药物组合物可以配制成栓剂,具有传统的粘合剂和赋形剂如甘油三酯。
口服制剂可包括标准赋形剂,例如药物级甘露糖醇、乳糖、淀粉、硬脂酸镁、糖精钠、纤维素、碳酸镁等。
这些组合物含有治疗有效量的药物或生物活性部分,以及适合量的赋形剂,以提供给患者适当施用的形式。
该制剂应适合施用方式。
[0305]如本文所用,术语“试剂”是指包含至少一个用于与另一种化合物或药物的官能团反应的官能团的化合物。
应理解,包含官能团(例如伯胺或仲胺或羟基官能团)的药物也是试剂。
[0306]如本文所用,术语“部分”是指分子的一部分,其与相应的试剂相比缺少一个或多个原子。
例如,如果式“h-x-h”的试剂与另一种试剂反应并成为反应产物的一部分,则反应产物的相应部分具有结构“h-x‑”
或
“‑x‑”,而每个
“‑”
表示与另一部分的连接。
因此,生物活性部分作为药物从前药中释放。
[0307]应理解,如果提供一组原子的序列或化学结构,该组原子连接到两个部分或中断一个部分,则所述序列或化学结构可以以任一方向连接到两个部分,另有明确的除外。
例如,
“‑c(o)n(r1)‑”
部分可以连接到两个部分或作为
“‑c(o)n(r1)‑”
或
“‑n(r1)c(o)‑”
打断一个部分。
类似地,部分
10%,即范围从
180
到
220
并且包括
180
和
220
;优选
200+/-8%,即范围从
184至
216并且包括
184和
216;甚至更优选地,范围从并且包括
200+/-5%,即范围从
190
到
210并且包括
190
和
210;并且最优选地
200+/-2%,即范围从
196到
204并且包括
196和
204。
应当理解,给出为“约
20
%”的百分比并不意味着“20
%
+/-10%”,即范围从
10%至
30
%并包括
10%和
30
%,而是“约
20
%”意指范围
18%至
22%且包括
18%和
22%,即加减数值即
20
的
10%。
[0315]如本文所用,术语“聚合物”是指包含重复结构单元即单体的分子,其通过化学键以线性、环状、支化、交联或树枝状方式或其组合连接,其可以是合成或生物来源的,或两者兼而有之。
应理解,聚合物还可包含一种或多种其它化学基团和/或部分,例如一种或多种官能团。
优选地,可溶性聚合物的分子量至少为
0.5kda,例如分子量至少为
1kda,分子量至少为
2kda,分子量至少为
3kda或分子量至少为
5kda。
如果聚合物是可溶的,则其优选具有至多
1000kda的分子量,例如至多
750kda,例如至多
500kda,例如至多
300kda,例如至多
200kda,例如至多
100kda。
应理解,对于不溶性聚合物,例如水凝胶,不能提供有意义的分子量范围。
应当理解,蛋白质也是其中氨基酸是重复结构单元的聚合物,即使每个氨基酸的侧链可以是不同的。
[0316]如本文所用,术语“聚合的”是指包含一种或多种聚合物或聚合物部分的试剂或部分。
聚合物试剂或部分还可任选地包含一个或多个其它部分/部分,其优选选自:
[0317]·c1-50
烷基、c2-50
烯基、c2-50
炔基、c3-10环烷基、3-至
10-元杂环基、8-至
11-元杂双环基、苯基、萘基、茚基、茚满基和四氢萘基;和
[0318]·
选自如下的连接基
[0319][0320]其中
[0321]虚线表示连接至部分或试剂的其余部分,且
[0322]-r和-ra彼此独立地选自-h、甲基、乙基、丙基、丁基、戊基和己基。
[0323]本领域技术人员理解,由聚合反应得到的聚合产物并非都具有相同的分子量,而是具有分子量分布。
因此,本文所用的聚合物中分子量范围、分子量、单体的数量范围和聚合物中单体的数量,是指数均分子量和单体的平均数量,即聚合物或聚合物部分的分子量的算术平均值以及聚合物或聚合部分的单体数的算术平均值。
[0324]因此,在包含“x”单体单元的聚合物部分中,对于“x”给出的任何整数因此对应于单体的算术平均数。
对于“x”给出的任何整数范围提供的是其中单体的算术平均数的整数范围。
给定为“约x”的“x”的整数表示单体的算术平均数在x+/-10%的整数范围内,优选x+/-8%,更优选x+/-5%且最优选x+/-2%。
[0325]如本文所用,术语“数均分子量”是指各聚合物的分子量的常规算术平均值。
[0326]如本文所用,术语关于载体的“水溶性”是指当这种载体是本发明的pth化合物、优选控释pth化合物的一部分时,包含这种水溶性载体的至少
1g pth化合物、优选控释pth化合物,可以在
20℃
溶解在1升水中以形成均匀溶液。
相应地,关于载体的术语“水不溶性”是指当这种载体是本发明的pth化合物、优选控释pth化合物的一部分时,包含这种水不溶性载体的少于
1g pth化合物、优选控释pth化合物可以在
20℃
溶解在1升水中以形成均匀溶液。
[0327]如本文所用,术语关于pth化合物的“水溶性”是指至少
1g pth化合物可以在
20℃
溶解在1升水中以形成均匀溶液。
相应地,关于pth化合物的术语“水不溶性”是指少于
1g的pth化合物在
20℃
可溶于1升水中以形成均匀溶液。
[0328]如本文所用,术语“水凝胶”是指由均聚物或共聚物组成的亲水或两亲性聚合网状结构,其由于存在共价化学交联而不溶。
交联提供网状结构和物理完整性。
[0329]如本文所用,术语“热凝胶化”(thermogelling)是指化合物在低温下为液体或低粘度溶液,其在约
0.1/
秒的剪切速率下具有小于
500cps(25℃)的粘度,其低温范围在约
0℃
至约
10℃,但是在较高温度下为高粘度化合物,在剪切速率为约
0.1/
秒时小于
10000cps(25℃),所述较高温度范围在约
30℃
至约
40℃,例如约
37℃。
[0330]如本文所用,与部分或试剂有关的术语“基于peg的”是指所述部分或试剂包含peg。
优选地,基于peg的部分或试剂包含至少
10%(w/w)peg,例如至少
20
%(w/w)peg,例如至少
30
%(w/w)peg,例如至少
40
%(w/w)peg,例如至少
50
%(w/w),例如至少
60(w/w)peg,例如至少
70
%(w/w)peg,例如至少
80
%(w/w)peg,例如至少
90
%(w/w)peg,例如至少
95%。
基于peg的部分或试剂的剩余重量百分比是优选选自以下部分和连接基的其它部分:
[0331]·c1-50
烷基、c2-50
烯基、c2-50
炔基、c3-10环烷基、3-至
10-元杂环基、8-至
11-元杂双环基、苯基、萘基、茚基、茚满基和四氢萘基;和
[0332]·
选自如下的连接基
[0333][0334]其中
[0335]虚线表示连接至部分或试剂的其余部分,且
[0336]-r和-ra彼此独立地选自-h、甲基、乙基、丙基、丁基、戊基和己基。
[0337]如本文所用,与部分或试剂相关的术语“基于peg的包含至少x%peg”是指所述部srx4、-n(rx4rx4a)、-no2、-oc(o)rx4、-n(rx4)c(o)rx4a、-n(rx4)s(o)2rx4a、-n(rx4)s(o)rx4a、-n(rx4)c(o)orx4a、-n(rx4)c(o)n(rx4arx4b)、-oc(o)n(rx4rx4a)和c1-6烷基;其中c1-6烷基任选地被一个或多个相同或不同的卤素取代;
[0359]每个-rx4、-rx4a、-rx4b独立地选自-h、卤素、c1-6烷基、c2-6烯基和c2-6炔基;
[0360]甚至更优选地,一个或多个另外任选的取代基彼此独立地选自卤素、-cn、-coorx1、-orx1、-c(o)rx1、-c(o)n(rx1rx1a)、-s(o)2n(rx1rx1a)、-s(o)n(rx1rx1a)、-s(o)2rx1、-s(o)rx1、-n(rx1)s(o)2n(rx1arx1b)、-srx1、-n(rx1rx1a)、-no2、-oc(o)rx1、-n(rx1)c(o)rx1a、-n(rx1)s(o)2rx1a、-n(rx1)s(o)rx1a、-n(rx1)c(o)orx1a、-n(rx1)c(o)n(rx1arx1b)、-oc(o)n(rx1rx1a)、-t0、c1-6烷基、c2-6烯基和c2-6炔基;其中-t0、c1-6烷基、c2-6烯基和c2-6炔基任选地被一个或多个相同或不同的-rx2取代,且其中c1-6烷基、c2-6烯基和c2-6炔基任选地被一个或多个基团打断,所述基团选自-t0-、-c(o)o-、-o-、-c(o)-、-c(o)n(rx3)-、-s(o)2n(rx3)-、-s(o)n(rx3)-、-s(o)2-、-s(o)-、-n(rx3)s(o)2n(rx3a)-、-s-、-n(rx3)-、-oc(orx3)(rx3a)-、-n(rx3)c(o)n(rx3a)-和-oc(o)n(rx3)-;
[0361]每个-rx1、-rx1a、-rx1b、-rx2、-rx3、-rx3a独立地选自-h、卤素、c1-6烷基、c2-6烯基和c2-6炔基;
[0362]每个t0独立地选自苯基、萘基、茚基、茚满基、四氢萘基、c3-10环烷基、3-至
10-元杂环基和
8-至
11-元杂双环基;其中每个t0独立地任选地被一个或多个相同或不同的-rx2取代。
[0363]优选地,任选取代的分子的最多6个-h原子独立地被取代基取代,例如5个-h原子独立地被取代基取代,4个-h原子独立地被取代基取代,3个-h原子独立地被取代基取代,2个-h原子独立地被取代基取代,或者1个-h原子被取代基取代。
[0364]术语“打断”是指将部分插入两个碳原子之间或-如果插入位于部分末端之一-碳或杂原子与氢原子之间,优选地碳与氢原子之间。
[0365]如本文所用,术语“c1-4烷基”单独或以组合方式表示具有
1-4个碳原子的直链或支链烷基部分。
如果存在于分子末端,直链或支链c1-4烷基的实例是甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基和叔丁基。
当分子的两个部分通过c1-4烷基连接时,这类c1-4烷基的实例是-ch2-、-ch2-ch2-、-ch(ch3)-、-ch2-ch2-ch2-、-ch(c2h5)-、-c(ch3)2-。c1-4烷基碳的每个氢可以任选地被如上述所定义的取代基替代。
任选地,c1-4烷基可以被一个或多个如下所定义的部分打断。
[0366]如本文所用,术语“c1-6烷基”单独或以组合方式表示具有
1-6个碳原子的直链或支链烷基部分。
如果存在于分子的末端,则直链或支链c1-6烷基的实例是甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、2-甲基丁基、2,2-二甲基丙基、正己基、2-甲基戊基、3-甲基戊基、2,2-二甲基丁基、2,3-二甲基丁基和
3,3-二甲基丙基。
当分子的两个部分通过c1-6烷基连接时,这类c1-6烷基的实例是-ch2-、-ch2-ch2-、-ch(ch3)-、-ch2-ch2-ch2-、-ch(c2h5)-和-c(ch3)2-。c1-6烷基碳的每个氢可以任选地被如上述所定义的取代基替代。
任选地,c1-6烷基可以被一个或多个如下所定义的部分打断。
[0367]因此,“c1-10烷基”、“c1-20
烷基”或“c1-50
烷基”是指分别具有
1-10、1-20
或
1-50
个碳原子的烷基链,其中c1-10、c1-20
或c1-50
碳的每个氢原子可以任选地被如上述所定义的取代基替代。
任选地,c1-10或c1-50
烷基可以被一个或多个如下所定义的部分打断。
[0368]如本文所用,术语“c2-6烯基”单独或以组合方式表示包含至少一个碳-碳双键并且具有
2-6个碳原子的直链或支链烃部分。
如果存在于分子的末端,则实例是-ch=ch2、-ch=ch-ch3、-ch2-ch=ch2、-ch=chch2-ch3和-ch=ch-ch=ch2。
当分子的两个部分通过c2-6烯基连接时,这类c2-6烯基的实例是-ch=ch-。c2-6烯基部分的每个氢可以任选地被如上述所定义的取代基替代。
任选地,c2-6烯基可以被一个或多个如下所定义的部分打断。
[0369]因此,术语“c2-10烯基”、“c2-20
烯基”或“c2-50
烯基”单独或以组合方式表示包含至少一个碳-碳双键、具有
2-10、2-20
或
2-50
个碳原子的直链或支链烃部分。c2-10烯基、c2-20
烯基或c2-50
烯基的每个氢原子可以任选地被如上述所定义的取代基替代。
任选地,c2-10烯基、c2-20
烯基或c2-50
烯基可以被一个或多个如下所定义的部分打断。
[0370]如本文所用,术语“c2-6炔基”单独或以组合方式表示包含至少一个碳-碳三键并且具有
2-6个碳原子的直链或支链烃部分。
如果存在于分子的末端,则实例是-c≡ch、-ch2-c≡ch、ch2-ch2-c≡ch和ch2-c≡c-ch3。
当分子的两个部分通过c2-6炔基连接时,实例是-c≡c-。c2-6炔基的每个氢原子可以任选地被如上述所定义的取代基替代。
任选地,一个或多个双键可以出现。
任选地,c2-6炔基可以被一个或多个如下所定义的部分打断。
[0371]因此,如本文所用,术语“c2-10炔基”、“c2-20
炔基”和“c2-50
炔基”单独或以组合方式分别表示包含至少一个碳-碳三键、具有
2-10、2-20
或
2-50
个碳原子的直链或支链烃部分。c2-10炔基、c2-20
炔基或c2-50
炔基的每个氢原子可以任选地被如上述所定义的取代基替代。
任选地,一个或多个双键可以出现。
任选地,c2-10炔基、c2-20
炔基或c2-50
炔基可以被一个或多个如下所定义的部分打断。
[0372]如上所述,c1-4烷基、c1-6烷基、c1-10烷基、c1-20
烷基、c1-50
烷基、c2-6烯基、c2-10烯基、c2-20
烯基、c2-50
烯基、c2-6炔基、c2-10炔基、c2-20
烯基或c2-50
炔基可以任选地被一个或多个部分打断,所述部分优选自
[0373][0374]其中
[0375]虚线表示连接至部分或试剂的其余部分;且
[0376]-r和-ra彼此独立地选自-h、甲基、乙基、丙基、丁基、戊基和己基。
[0377]如本文所用,术语“c3-10环烷基”是指具有
3-10个碳原子的环烷基,其可以是饱和的或不饱和的,例如环丙基、环丁基、环戊基、环己基、环己烯基、环庚基、环辛基、环壬基或环癸基。c3-10环烷基碳的每个氢原子可以被如上述所定义的取代基替代。
术语“c3-10环烷基”还包括桥连双环,如降崁烷或降冰片烯。
[0378]术语“8-至
30-元碳多环基”或“8-至
30-元碳多环”是指具有
8-30
个环原子的两个或多个环的环状部分,其中两个相邻环共享至少一个环原子并且可以包含达最大数量的双键(芳族或非芳族环,其为完全、部分或不饱和的)。
优选地,
8-至
30-元碳多环基是指
2、3、4或5个环、更优选
2、3或4个环的环状部分。
[0379]如本文所用,术语“3-至
10-元杂环基”或“3-至
10-元杂环”指具有
3、4、5、6、7、8、9或
10个环原子的环,其可包含达最多的双键数(芳环或非芳环,其为完全、部分或不饱和的),其中至少1个环原子、至多4个环原子被选自硫(包括-s(o)-、-s(o)2-)、氧和氮(包括=n(o)-)的杂原子替代,且其中环通过碳或氮原子与分子的其余部分连接。3-至
10-元杂环的实例包括但不限于氮丙啶、环氧乙烷、硫杂丙环(thiirane)、吖丙因(azirine)、环氧乙烯(oxirene)、硫杂丙烯(thiirene)、氮杂环丁烷、氧杂环丁烷、硫杂环丁烷、呋喃、噻吩、吡咯、吡咯啉、咪唑、咪唑啉、吡唑、吡唑啉、噁唑、噁唑啉、异噁唑、异噁唑啉、噻唑、噻唑啉、异噻唑、异噻唑啉、噻二唑、噻二唑啉、四氢呋喃、四氢噻吩、吡咯烷、咪唑烷、吡唑烷、噁唑烷、异噁唑烷、噻唑烷、异噻唑烷、噻二唑烷、环丁砜(sulfolane)、吡喃、二氢吡喃、四氢吡喃、咪唑烷、吡啶、哒嗪、吡嗪、嘧啶、哌嗪、哌啶、吗啉、四唑、三唑、三唑烷、四唑烷、二氮杂庚环、吖庚因和高哌嗪。3-至
10-元杂环基或
3-至
10-元杂环基团的每个氢原子可以被如下定义的取代基取代。
[0380]如本文所用,术语“8-至
11-元杂双环基”或“8-至
11-元杂双环”是指具有8至
11个环原子的两个环的杂环部分,其中至少一个环原子由两个环共享,并且可以包含最多数量的双键(芳香族或非芳香族环,其为完全、部分或不饱和的),其中至少1个环原子、至多6个环原子被选自硫(包括-s(o)-、-s(o)2-)、氧和氮(包括=n(o)-)的杂原子替代,其中环通过碳或氮原子与分子的其余部分连接。8至
11元杂双环的实例是吲哚、二氢吲哚、苯并呋喃、苯并噻吩、苯并噁唑、苯并异噁唑、苯并噻唑、苯并异噻唑、苯并咪唑、苯并咪唑啉、喹啉、喹唑啉、二氢喹唑啉、喹啉、二氢喹啉、四氢喹啉、十氢喹啉、异喹啉、十氢异喹啉、四氢异喹啉、二氢异喹啉、苯并氮杂嘌呤和蝶啶。
术语
8-至
11-元杂二环还包括两个环的螺结构,如
1,4-二氧杂-8-氮杂螺
[4.5]癸烷,或桥连的杂环如
8-氮杂-双环
[3.2.1]辛烷。8-至
11-元杂双环基或
8-至
11-元杂双环碳的每个氢原子可以被如下定义的取代基替代。
[0381]类似地,术语“8-至
30-元杂多环基”或“8-至
30-元杂多环”是指具有8至
30
个环原子的两个以上环的杂环部分,优选地三个、四个或五个环,其中两个相邻的环共享至少一个环原子并且可以包含最多数量的双键(芳环或非芳环,其为完全、部分或不饱和的),其中至少1个环原子、至多
10个环原子被杂原子替换,所述杂原子选自硫(包括硫-s(o)-、-s(o)2-)、氧和氮(包括=n(o)-),且其中环通过碳或氮原子与分子的其余部分连接。
[0382]应当理解,与如下结构部分相关的短语“rx/ry对与它们所连接的原子一起形成c3-10环烷基或
3-至
10-元杂环基”[0383][0384]是指rx和ry形成如下结构:
[0385][0386]其中r是c3-10环烷基或
3-至
10-元杂环基。
[0387]还应当理解,与如下结构部分相关的短语“rx/ry对与它们所连接的原子一起形成环a”[0388][0389]是指rx和ry形成如下结构:
[0390][0391]如本文所用,“卤素”是指氟、氯、溴或碘。
通常优选卤素是氟或氯。
[0392]通常,术语“包含”或“含有”也涵盖“由
…
组成”。
[0393]优选地,pth化合物包含pth分子或pth部分,其具有如下的序列:seq id no:47、seq id no:48、seq id no:49、seq id no:50、seq id no:51、seq id no:52、seq id no:53、seq id no:54、seq id no:55、seq id no:107、seq id no:108、seq id no:109、seq id no:110、seq id no:111、seq id no:112、seq id no:113、seq id no:114或seq id no:115。
更优选地,pth分子或pth部分具有如下的序列:seq id no:50、seq id no:51、seq id no:52、seq id no:110、seq id no:111或seq id no:112。
[0394]在一个实施方案中,pth分子或pth部分具有seq id no:50
的序列。
[0395]在另一个实施方案中,pth分子或pth部分具有seq id no:52的序列。
[0396]在另一个实施方案中,pth分子或pth部分具有seq id no:110的序列。
[0397]在另一个实施方案中,pth分子或pth部分具有seq id no:111的序列。
[0398]在另一个实施方案中,pth分子或pth部分具有seq id no:112的序列。
[0399]最优选地,pth分子或pth部分具有seq id no:51的序列。
[0400]pth化合物的施用优选通过皮下施用。
在另一个实施方案中,pth化合物的施用通过静脉内施用进行。
在另一个实施方案中,pth化合物的施用通过肌内施用进行。
[0401]两次连续施用之间的时间间隔,优选在两次连续皮下施用之间的时间间隔,即施用间隔,优选至少
24小时,例如
24小时、36小时、48小时、60
小时、72小时、每
84小时、96小时、108小时、120
小时、132小时、144小时、156小时、一周、两周、三周或四周。
[0402]在一个实施方案中,两次连续施用之间、优选两次连续皮下施用之间的时间间隔是
24小时。
[0403]在另一个实施方案中,两次连续施用之间、优选两次连续皮下施用之间的时间间隔是
48小时。
[0404]在另一个实施方案中,两次连续施用之间、优选两次连续皮下施用之间的时间间
隔是
72小时。
[0405]在另一个实施方案中,两次连续施用之间、优选两次连续皮下施用之间的时间间隔是
96小时。
[0406]在另一个实施方案中,两次连续施用之间、优选两次连续皮下施用之间的时间间隔是
120
小时。
[0407]在另一个实施方案中,两次连续施用之间、优选两次连续皮下施用之间的时间间隔是
144小时。
[0408]在另一个实施方案中,两次连续施用之间、优选两次连续皮下施用之间的时间间隔是1周。
[0409]在每个施用间隔中测量的峰-谷比小于4,优选小于
3.8,更优选小于
3.6,甚至更优选小于
3.4,甚至更优选小于
3.2,甚至更优选小于3,甚至更优选小于
2.8,甚至更优选小于
2.6,甚至更优选小于
2.4,甚至更优选小于
2.2,且最优选小于
2。
[0410]优选地,皮下施用通过皮下注射进行。
优选地,所述皮下注射使用笔型装置进行。
[0411]在一个实施方案中,pth化合物是稳定的pth化合物。
[0412]在一个实施方案中,pth化合物是稳定的pth化合物,其中至少一个pth部分通过稳定的连接键共价缀合至聚合物部分,以直接或通过间隔基部分的方式。
[0413]优选地,在这类稳定的pth化合物中,pth部分通过稳定的连接键共价缀合至水溶性聚合物部分,以直接或通过间隔基部分的方式。
[0414]优选地,这类聚合物部分选自:
2-甲基丙烯酰基-氧基乙基磷酰胆碱、聚(丙烯酸)、聚(丙烯酸酯)、聚(丙烯酰胺)、聚(烷氧基)聚合物、聚(酰胺)、聚(酰氨基胺)、聚(氨基酸)、聚(酸酐)、聚(天冬酰胺)、聚(丁酸)、聚(乙醇酸)、聚对苯二甲酸丁二醇酯、聚(己内酯)、聚(碳酸酯)、聚(氰基丙烯酸酯)、聚(二甲基丙烯酰胺)、聚(酯)、聚(乙烯)、聚(乙二醇)、聚(环氧乙烷)、聚(磷酸乙酯)、聚(乙基噁唑啉)、聚(乙醇酸)、聚(丙烯酸羟乙酯)、聚(羟乙基-噁唑啉)、聚(羟甲基丙烯酸酯)、聚(羟丙基甲基丙烯酰胺)、聚(甲基丙烯酸羟丙酯)、聚(羟丙基噁唑啉)、聚(亚氨基碳酸酯)(polyiminocarbonates)、聚(乳酸)、聚(乳酸-共-乙醇酸)、聚(甲基丙烯酰胺)、聚(甲基丙烯酸酯)、聚(甲基噁唑啉)、聚(有机磷腈)(poly(organophosphazenes))、聚(原酸酯)、聚(噁唑啉)、聚(丙二醇)、聚(硅氧烷)(poly(siloxanes))、聚(氨基甲酸酯)、聚(乙烯醇)、聚(乙烯胺)、聚(乙烯基甲基醚)、聚(乙烯基吡咯烷酮)、硅酮(silicones)、纤维素、羧甲基纤维素、羟丙基甲基纤维素、甲壳质、脱乙酰壳多糖、葡聚糖、糊精、明胶、透明质酸和衍生物、官能化透明质酸、甘露聚糖、果胶、鼠李糖半乳糖醛酸聚糖(rhamnogalacturonan)、淀粉、羟烷基淀粉、羟乙基淀粉和其它基于碳水化合物的聚合物、木聚糖及其共聚物。
[0415]甚至更优选地,所述聚合物部分是基于peg的部分。
[0416]在另一个实施方案中,所述至少一个pth部分通过稳定连接键与白蛋白结合部分共价缀合。
优选地,所述白蛋白结合部分是c8-24烷基部分或脂肪酸衍生物。
优选的脂肪酸衍生物是wo 2005/027978 a2和wo 2014/060512 a1中公开的那些,其通过引用并入本文。
[0417]在另一个实施方案中,稳定的pth化合物是融合蛋白,即pth部分通过肽键稳定地和共价地结合到另一个肽或蛋白质部分。
[0418]在优选的实施方案中,pth化合物是控释pth化合物。
[0419]在一个实施方案中,控释pth化合物是水不溶性的。
[0420]优选地,水不溶性控释pth化合物选自晶体、纳米粒、微粒、纳米球和微球。
[0421]在一个实施方案中,水不溶性控释pth化合物是包含至少一种pth分子或pth部分的晶体。
[0422]在另一个实施方案中,水不溶性控释pth化合物是包含至少一种pth分子或pth部分的纳米粒。
[0423]在另一个实施方案中,水不溶性控释pth化合物是包含至少一种pth分子或pth部分的微粒。
[0424]在另一个实施方案中,水不溶性控释pth化合物是包含至少一种pth分子或pth部分的纳米球。
[0425]在另一个实施方案中,水不溶性控释pth化合物是包含至少一种pth分子或pth部分的微球。
[0426]在一个实施方案中,水不溶性控释pth化合物是包含至少一种pth分子或pth部分的囊泡(vesicle)。
优选地,这类包含至少一种pth分子或pth部分的囊泡是胶束、脂质体或聚合物囊泡(polymersome)。
[0427]在一个实施方案中,水不溶性控释pth化合物是包含至少一种pth分子或pth部分的胶束。
[0428]在另一个实施方案中,水不溶性控释pth化合物是包含至少一种pth分子或pth部分的脂质体,优选地,这类脂质体选自超声水凝胶(aquasomes);非离子表面活性剂囊泡,例如类脂质体(niosomes)和前类脂质体(proniosomes);阳离子脂质体,例如
leciplex;转移体(transfersomes);醇质体(ethosomes);ufasomes;sphingosomes;和药质体(pharmacosomes)。
[0429]在另一个实施方案中,水不溶性控释pth化合物是包含至少一种pth分子或pth部分的聚合物囊泡。
[0430]在另一个实施方案中,水不溶性控释pth化合物包含至少一种pth分子,其非共价地被包埋在水不溶性聚合物中。
优选地,这类水不溶性聚合物包含选自如下的聚合物:
2-甲基丙烯酰基-氧基乙基磷酰胆碱、聚(丙烯酸)、聚(丙烯酸酯)、聚(丙烯酰胺)、聚(烷氧基)聚合物、聚(酰胺)、聚(酰氨基胺)、聚(氨基酸)、聚(酸酐)、聚(天冬酰胺)、聚(丁酸)、聚(乙醇酸)、聚对苯二甲酸丁二醇酯、聚(己内酯)、聚(碳酸酯)、聚(氰基丙烯酸酯)、聚(二甲基丙烯酰胺)、聚(酯)、聚(乙烯)、聚(乙二醇)、聚(环氧乙烷)、聚(磷酸乙酯)、聚(乙基噁唑啉)、聚(乙醇酸)、聚(丙烯酸羟乙酯)、聚(羟乙基-噁唑啉)、聚(羟甲基丙烯酸酯)、聚(羟丙基甲基丙烯酰胺)、聚(甲基丙烯酸羟丙酯)、聚(羟丙基噁唑啉)、聚(亚氨基碳酸酯)、聚(乳酸)、聚(乳酸-共-乙醇酸)、聚(甲基丙烯酰胺)、聚(甲基丙烯酸酯)、聚(甲基噁唑啉)、聚(有机磷腈)、聚(原酸酯)、聚(噁唑啉)、聚(丙二醇)、聚(硅氧烷)、聚(氨基甲酸酯)、聚(乙烯醇)、聚(乙烯胺)、聚(乙烯基甲基醚)、聚(乙烯基吡咯烷酮)、硅酮、纤维素、羧甲基纤维素、羟丙基甲基纤维素、甲壳质、脱乙酰壳多糖、葡聚糖、糊精、明胶、透明质酸和衍生物、官能化透明质酸、甘露聚糖、果胶、鼠李糖半乳糖醛酸聚糖、淀粉、羟烷基淀粉、羟乙基淀粉和其它基于碳水化合物的聚合物、木聚糖及其共聚物。
[0431]在一个优选的实施方案中,水不溶性控释pth化合物包含至少一种pth分子,其非
共价地被包埋在聚(乳酸-共-乙醇酸)(plga)中。
[0432]在另一个实施方案中,水不溶性控释pth化合物包含至少一种pth部分,其以共价和可逆的方式缀合至水不溶性聚合物。
优选地,这类水不溶性聚合物包含选自如下的聚合物:
2-甲基丙烯酰基-氧基乙基磷酰胆碱、聚(丙烯酸)、聚(丙烯酸酯)、聚(丙烯酰胺)、聚(烷氧基)聚合物、聚(酰胺)、聚(酰氨基胺)、聚(氨基酸)、聚(酸酐)、聚(天冬酰胺)、聚(丁酸)、聚(乙醇酸)、聚对苯二甲酸丁二醇酯、聚(己内酯)、聚(碳酸酯)、聚(氰基丙烯酸酯)、聚(二甲基丙烯酰胺)、聚(酯)、聚(乙烯)、聚(乙二醇)、聚(环氧乙烷)、聚(磷酸乙酯)、聚(乙基噁唑啉)、聚(乙醇酸)、聚(丙烯酸羟乙酯)、聚(羟乙基-噁唑啉)、聚(羟甲基丙烯酸酯)、聚(羟丙基甲基丙烯酰胺)、聚(甲基丙烯酸羟丙酯)、聚(羟丙基噁唑啉)、聚(亚氨基碳酸酯)、聚(乳酸)、聚(乳酸-共-乙醇酸)、聚(甲基丙烯酰胺)、聚(甲基丙烯酸酯)、聚(甲基噁唑啉)、聚(有机磷腈)、聚(原酸酯)、聚(噁唑啉)、聚(丙二醇)、聚(硅氧烷)、聚(氨基甲酸酯)、聚(乙烯醇)、聚(乙烯胺)、聚(乙烯基甲基醚)、聚(乙烯基吡咯烷酮)、硅酮、纤维素、羧甲基纤维素、羟丙基甲基纤维素、甲壳质、脱乙酰壳多糖、葡聚糖、糊精、明胶、透明质酸和衍生物、官能化透明质酸、甘露聚糖、果胶、鼠李糖半乳糖醛酸聚糖、淀粉、羟烷基淀粉、羟乙基淀粉和其它基于碳水化合物的聚合物、木聚糖及其共聚物。
[0433]在一个实施方案中,这类水不溶性控释pth化合物是包含缀合物d-l
的化合物,其中
[0434]-d是pth部分;且
[0435]-l
包含可逆前药连接基部分-l
1-,该部分-l
1-通过pth的官能团连接至pth部分-d;
[0436]其中-l
1-被-l
2-z’取代,且任选地进一步被取代;其中
[0437]-l
2-是单一化学键或间隔基部分;且
[0438]-z’是水不溶性载体部分。
[0439]应当理解,多个部分-l
2-l
1-d连接至水不溶性载体-z’,且这类控释pth化合物是pth前药,更具体地为载体连接的pth前药。
[0440]-d、-l
1-、-l
2-和-z'
的优选实施方案如下所述。
[0441]在一个优选的实施方案中,控释pth化合物是水溶性的。
[0442]在一个优选的实施方案中,这类水溶性控释pth化合物是式(ia)或(ib)的化合物或其药学上可接受的盐
[0443][0444][0445]其中
[0446]-d是pth部分;
[0447]-l
1-是通过pth官能团连接至pth部分-d的可逆前药连接基部分;
[0448]-l
2-是单一化学键或间隔基部分;
[0449]-z是水溶性载体部分;
[0450]x是选自
1、2、3、4、5、6、7、8、9、10、11、12、13、14、15或
16的整数;且
[0451]y是选自
1、2、3、4和5的整数。
[0452]应当理解,式(ia)和(ib)的化合物是pth前药,更具体地为水溶性pth前药。
[0453]优选地,-d具有如下的序列:seq id no:47、seq id no:48、seq id no:49、seq id no:50、seq id no:51、seq id no:52、seq id no:53、seq id no:54、seq id no:55、seq id no:107、seq id no:108、seq id no:109、seq id no:110、seq id no:111、seq id no:112、seq id no:113、seq id no:114或seq id no:115。
更优选地,-d具有如下的序列:seq id no:50、seq id no:51、seq id no:52、seq id no:110、seq id no:111或seq id no:112。
[0454]在一个实施方案中,-d具有seq id no:50
的序列。
[0455]在另一个实施方案中,-d具有seq id no:52的序列。
[0456]在另一个实施方案中,-d具有seq id no:110的序列。
[0457]在另一个实施方案中,-d具有seq id no:111的序列。
[0458]在另一个实施方案中,-d具有seq id no:112的序列。
[0459]最优选地,-d具有id no:51的序列seq。
[0460]部分-l
1-缀合至-d的氨基酸残基侧链的官能团、缀合至-d的n-末端胺官能团或c-末端羧基官能团,或缀合至-d的骨架多肽链中的氮原子。
与n-末端或c-末端的连接可以分别直接通过相应的胺或羧基官能团,或间接地进行,其中间隔基部分首先缀合至间隔基部分-l
1-所缀合的胺或羧基官能团。
[0461]优选地,与-l
1-缀合的pth的氨基酸残基包括选自如下的官能团:羧酸、伯胺和仲胺、马来酰亚胺、硫醇、磺酸、碳酸酯、氨基甲酸酯、羟基、醛、酮、肼、异氰酸酯、异硫氰酸酯、磷酸、膦酸、卤代乙酰基、烷基卤化物、丙烯酰基、芳基氟、羟胺、硫酸酯、二硫化物、乙烯基砜、乙烯基酮、重氮烷、环氧乙烷、胍和氮丙啶。
甚至更优选地,与-l
1-缀合的pth的氨基酸残基包括选自羟基、伯胺和仲胺以及胍的官能团。
甚至更优选地,与-l
1-缀合的pth的氨基酸残基包含伯或仲胺官能团。
最优选地,与-l
1-缀合的pth的氨基酸残基包含伯胺官能团。
[0462]如果部分-l
1-缀合至pth的氨基酸残基侧链的官能团,则所述氨基酸残基选自蛋白原(proteinogenic)氨基酸残基和非蛋白原氨基酸残基。
[0463]在一个实施方案中,-l
1-与pth的非蛋白原氨基酸残基的侧链的官能团缀合。
应当理解,在天然pth或其片段的序列中未发现这种非蛋白原氨基酸,并且它可能仅存在于pth的变体和衍生物中。
[0464]在另一个实施方案中,-l
1-与pth的蛋白原氨基酸残基的侧链的官能团缀合。
优选地,所述氨基酸选自组氨酸、赖氨酸、色氨酸、丝氨酸、苏氨酸、酪氨酸、天冬氨酸、谷氨酸和精氨酸。
甚至更优选地,所述氨基酸选自赖氨酸、天冬氨酸、精氨酸和丝氨酸。
甚至更优选地,所述氨基酸选自赖氨酸、精氨酸和丝氨酸。
[0465]在一个实施方案中,-l
1-缀合至pth的组氨酸的侧链的官能团。
[0466]在另一个实施方案中,-l
1-缀合至pth的赖氨酸的侧链的官能团。
[0467]在另一个实施方案中,-l
1-缀合至pth的色氨酸的侧链的官能团。
[0468]在另一个实施方案中,-l
1-缀合至pth的丝氨酸的侧链的官能团。
[0469]在另一个实施方案中,-l
1-缀合至pth的苏氨酸的侧链的官能团。
[0470]在另一个实施方案中,-l
1-缀合至pth的酪氨酸的侧链的官能团。
[0471]在另一个实施方案中,-l
1-缀合至pth的天冬氨酸的侧链的官能团。
[0472]在另一个实施方案中,-l
1-缀合至pth的谷氨酸的侧链的官能团。
[0473]在另一个实施方案中,-l
1-缀合至pth的精氨酸的侧链的官能团。
[0474]应当理解,并非每个pth部分均可以包含所有这些氨基酸残基。
[0475]在一个优选的实施方案中,-l
1-直接通过相应的胺官能团或间接地缀合至pth的n-末端胺官能团,其中间接方式中间隔基部分首先缀合至间隔基部分-l
1-所缀合的胺官能团。
甚至更优选地,-l
1-直接缀合至pth的n-末端胺官能团。
[0476]在一个等同优选的实施方案中,-l
1-直接通过相应羧基官能团或间接缀合至pth的c-末端官能团,其中间接方式中间隔基部分首先缀合至间隔基部分-l
1-所缀合的羧基官能团。
[0477]最优选地,l1-直接缀合至pth的n-末端胺官能团。
[0478]部分-l
1-可以通过任意类型的连接键连接至-d,条件是它是可逆的。
优选地,-l
1-通过连接键连接至-d,所述连接键选自酰胺、酯、氨基甲酸酯、乙缩醛、缩醛胺(aminal)、亚胺、肟、腙、二硫化物和酰基胍。
甚至更优选地,-l
1-通过连接键连接至-d,所述连接键选自酰胺、酯、氨基甲酸酯和酰基胍。
应当理解,这些连接键的一些本身是不可逆的,但在本发明中,包含在-l
1-中的相邻基团赋予这些连接键可逆性。
[0479]在一个实施方案中,-l
1-通过酯连接键连接至-d。
[0480]在另一个实施方案中,-l
1-通过氨基甲酸酯连接键连接至-d。
[0481]在另一个实施方案中,-l
1-通过酰基胍连接至-d。
[0482]在一个优选的实施方案中,-l
1-通过酰胺连接键连接至-d。
[0483]部分-l
1-是可逆前药连接基,药物即pth从其上以其游离形式释放,即它是无痕迹前药连接基。
适合的前药连接基是本领域已知的,例如公开在wo2005/099768a2、wo2006/136586a2、wo2011/089216a1和wo2013/024053a1中的可逆前药连接基部分,这些文献作为引用并入。
[0484]在另一个实施方案中,-l
1-是如wo2011/012722a1、wo2011/089214a1、wo2011/089215a1、wo2013/024052a1和wo2013/160340a1中所述的可逆前药连接基,这些文献作为引用并入。
[0485]特别优选的部分-l
1-公开在wo2009/095479a2中。
因此,在一个优选的实施方案中,部分-l
1-具有式(ii):
[0486][0487]其中虚线表示连接至为pth部分的-d的氮、羟基或硫羟基;
[0488]-x-选自-c(r4r4a)-;-n(r4)-;-o-;-c(r4r4a)-c(r5r5a)-;-c(r5r5a)-c(r4r4a)-;-c(r4r4a)-n(r6)-;-n(r6)-c(r4r4a)-;-c(r4r4a)-o-;-o-c(r4r4a)-;和-c(r7r7a)-;
[0489]x1选自c;和s(o);
[0490]-x2-选自-c(r8r8a)-;和-c(r8r8a)-c(r9r9a)-;
[0491]=x3选自=o;=s;和=n-cn;
[0492]-r1、-r1a、-r2、-r2a、-r4、-r4a、-r5、-r5a、-r6、-r8、-r8a、-r9和-r9a独立地选自-h;和c1-6烷基;
[0493]-r3和-r3a独立地选自-h;和c1-6烷基,条件是在-r3、-r3a之一或它们两者均不为-h的情况中,它们通过sp3-杂化碳原子连接至它们所连接的n;
[0494]-r7选自-n(r10r10a);和-nr10-(c=o)-r11;
[0495]-r7a、-r10、-r10a和-r11彼此独立地选自-h;和c1-6烷基;
[0496]任选地,-r1a/-r4a、-r1a/-r5a、-r1a/-r7a、-r4a/-r5a和-r8a/-r9a对的一个或多个形成化学键;
[0497]任选地,-r1/-r1a、-r2/-r2a、-r4/-r4a、-r5/-r5a、-r8/-r8a和-r9/-r9a对的一个或多个与它们所连接的原子一起形成c3-10环烷基;或
3-至
10-元杂环基;
[0498]任选地,-r1/-r4、-r1/-r5、-r1/-r6、-r1/-r7a、-r4/-r5、-r4/-r6、-r8/-r9和-r2/-r3对的一个或多个与它们所连接的原子其形成环a;
[0499]任选地,r3/r3a与它们所连接的氮原子一起形成
3-至
10-元杂环;
[0500]a选自苯基;萘基;茚基;茚满基;四氢萘基;c3-10环烷基;
3-至
10-元杂环基;和
8-至
11-元杂双环基;且
[0501]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代,条件是式(ii)中用星号标记的氢不被-l
2-z或-l
2-z’或取代基替代;
[0502]其中
[0503]-l
2-是单一化学键或间隔基;
[0504]-z是水溶性载体;且
[0505]-z’是水不溶性载体。
[0506]优选地,式(ii)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0507]在一个实施方案中,式(ii)的-l
1-不被进一步取代。
[0508]应当理解,如果式(ii)的-r3/-r3a与它们所连接的氮原子一起形成
3-至
10-元杂环,则可以形成仅这类
3-至
10-元杂环,其中直接连接至氮的原子是sp3-杂化碳原子。
换句话说,这类由-r3/-r3a与它们所连接的氮一起形成的
3-至
10-元杂环具有如下结构:
[0509][0510]其中
[0511]虚线表示连接至-l
1-的其余部分;
[0512]所述环包含
3-10个原子,包含至少一个氮;且
[0513]r#
和r##
表示sp3-杂化碳原子。
[0514]还应当理解,
3-至
10-元杂环可以进一步被取代。
[0515]由式(ii)的-r3/-r3a与它们所连接的氮一起形成的适合的
3-至
10-元杂环的示例性实施方案如下:
[0516][0517]其中
[0518]虚线表示连接至分子的其余部分;且
[0519]-r选自-h和c1-6烷基。
[0520]式(ii)的-l
1-可以任选地进一步被取代。
通常,可以使用任意的取代基,只要裂解原理不受影响,即式(ii)中用星号标记的氢不被替代,且式(ii)的部分
[0521]的氮保留为伯、仲或叔胺的部分,即-r3和-r3a彼此独立地为-h或通过sp3-杂化碳原子连接至-n《。
[0522]在一个实施方案中,式(ii)的-r1或-r1a被-l
2-z或-l
2-z’取代。
在另一个实施方案中,式(ii)的-r2或-r2a被-l
2-z或-l
2-z’取代。
在另一个实施方案中,式(ii)的-r3或-r3a被-l
2-z或-l
2-z’取代。
在另一个实施方案中,式(ii)的-r4被-l
2-z或-l
2-z’取代。
在另一个实施方案中,式(ii)的-r5或-r5a被-l
2-z或-l
2-z’取代。
在另一个实施方案中,式(ii)的-r6被-l
2-z或-l
2-z’取代。
在另一个实施方案中,式(ii)的-r7或-r7a被-l
2-z或-l
2-z’取代。
在另一个实施方案中,式(ii)的-r8或-r8a被-l
2-z或-l
2-z’取代。
在另一个实施方案中,式(ii)的-r9或-r9a被-l
2-z或-l
2-z’取代。
在另一个实施方案中,-r10被-l
2-z或-l
2-z’取代。
在另一个实施方案中,-r11被-l
2-z或-l
2-z’取代。
优选地,式(ii)的-r3被-l
2-z或-l
2-z’取代。
[0523]优选地,式(ii)的-x-选自-c(r4r4a)-、-n(r4)-和-c(r7r7a)-。
[0524]在一个实施方案中,式(ii)的-x-是-c(r4r4a)-。
[0525]在一个实施方案中,式(ii)的-x-是-c(r7r7a)-。
[0526]优选地,式(ii)的-r7是-nr10-(c=o)-r11。
[0527]优选地,式(ii)的-r7a选自-h、甲基和乙基。
最优选地,式(ii)的-r7a是-h。
[0528]优选地,-r10选自-h、甲基和乙基。
最优选地,-r10是甲基。
[0529]优选地,-r11选自-h、甲基和乙基。
最优选地,-r11是-h。
[0530]优选地,-r11被-l
2-z或-l
2-z’取代。
[0531]在另一个优选的实施方案中,式(ii)的-x-是-n(r4)-。
[0532]优选地,-r4选自-h、甲基和乙基。
优选地,-r4是-h。
[0533]优选地,式(ii)的x1是c。
[0534]优选地,式(ii)的=x3是=o。
[0535]优选地,式(ii)的-x2-是-c(r8r8a)-。
[0536]优选地,式(ii)的-r8和-r8a独立地选自-h、甲基和乙基。
更优选地,式(ii)的-r8和-r8a的至少一个是-h。
甚至更优选地,式(ii)的-r8和-r8a均为-h。
[0537]优选地,式(ii)的-r1和-r1a独立地选自-h、甲基和乙基。
[0538]在一个优选的实施方案中,式(ii)的-r1和-r1a的至少一个是-h,更优选地,式(ii)的-r1和-r1a均为-h。
[0539]在另一个优选的实施方案中,式(ii)的-r1和-r1a的至少一个是甲基,更优选地,式(ii)的-r1和-r1a均为甲基。
[0540]优选地,式(ii)的-r2和-r2a独立地选自-h、甲基和乙基。
更优选地,式(ii)的-r2和-r2a的至少一个是-h。
甚至更优选地,式(ii)的-r2和-r2a均为h。
[0541]优选地,-式(ii)的r3和-r3a独立地选自-h、甲基、乙基、丙基和丁基。
[0542]在一个优选的实施方案中,式(ii)的-r3和-r3a的至少一个是甲基,更优选地,式(ii)的-r3是甲基且式(ii)的-r3a是-h。
[0543]在另一个优选的实施方案中,式(ii)的-r3和-r3a均为-h。
[0544]优选地,-d通过形成酰胺键、通过n连接至-l
1-。
[0545]在一个优选的实施方案中,部分-l
1-具有式(iia-i):
[0546][0547]其中
[0548]虚线表示通过形成酰胺键连接至为pth部分的-d的氮;
[0549]-r1、-r1a、-r2、-r2a、-r3、-r3a、-r7、-r7a和-x2-如式(ii)中所定义的使用;且
[0550]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代,条件是式(iia-i)中用星号标记的氢不被-l
2-z或-l
2-z’或取代基替代。
[0551]应当理解,在式(iia-i)的-r3、-r3a之一或它们两者不为-h的情况中,它们通过sp3-杂化碳原子连接至它们所连接的n。
[0552]优选地,式(iia-i)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0553]优选地,式(iia-i)的部分-l
1-不被进一步取代。
[0554]优选地,式(iia-i)的-r1和-r1a独立地选自-h、甲基和乙基。
更优选地,式(iia-i)的-r1和-r1a的至少一个是-h。
甚至更优选地,式(iia-i)的-r1和-r1a均为-h。
[0555]优选地,式(iia-i)的-r7是-nr10-(c=o)-r11。
[0556]优选地,式(ii-i)的-r7a选自-h、甲基和乙基。
最优选地,式(ii-i)-的r7a是-h。
[0557]优选地,式(iia-i)的-r10选自-h、甲基和乙基。
最优选地,式(iia-i)-的r10是甲基。
[0558]优选地,式(iia-i)的-r11选自-h、甲基和乙基。
最优选地,式(iia-i)-的r11是-h。
[0559]优选地,式(iia-i)的-r11被-l
2-z或-l
2-z’取代。
[0560]优选地,式(iia-i)的-x2-是-c(r8r8a)-。
[0561]优选地,式(iia-i)的-r8和-r8a独立地选自-h、甲基和乙基。
更优选地,式(iia-i)的-r8和-r8a至少一个是-h。
甚至更优选地,式(iia-i)的-r8和-r8a均为-h。
[0562]优选地,式(iia-i)的-r2和-r2a独立地选自-h、甲基和乙基。
更优选地,式(iia-i)的-r2和-r2a的至少一个是-h。
甚至更优选地,式(iia-i)的-r2和-r2a均为h。
[0563]优选地,式(iia-i)的-r3和-r3a独立地选自-h、甲基、乙基、丙基和丁基。
甚至更优选地,式(iia-i)的-r3和-r3a的至少一个是甲基。
[0564]优选地,式(iia-i)的-r3是-h且式(iia-i)的-r3a是甲基。
[0565]更优选地,部分-l
1-具有式(iia-ii):
[0566][0567]其中虚线表示通过形成酰胺键连接至为pth部分的-d的氮;
[0568]-r2、-r2a、-r10、-r11和-x2-如式(ii)中所定义的使用;且
[0569]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代,条件是式(iia-ii)中用星号标记的氢不被-l
2-z或-l
2-z’或取代基替代。
[0570]应当理解,在式(iia-ii)的-r3、-r3a之一或它们两者不为-h的情况中,它们通过sp3-杂化碳原子连接至它们所连接的n。
[0571]优选地,式(iia-ii)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0572]优选地,式(iia-ii)的部分-l
1-不被进一步取代。
[0573]优选地,式(iia-ii)的-x2-是-c(r8r8a)-。
[0574]优选地,式(iia-ii)的-r8和-r8a独立地选自-h、甲基和乙基。
更优选地,式(iia-ii)的-r8和-r8a的至少一个是-h。
甚至更优选地,式(iia-ii)的-r8和-r8a均为-h。
[0575]优选地,式(iia-ii)的-r3和-r3a独立地选自-h、甲基、乙基、丙基和丁基。
甚至更优选地,式(iia-ii)的-r3和-r3a的至少一个是甲基。
[0576]优选地,式(iia-ii)的-r3是-h且式(iia-ii)的-r3a是甲基。
[0577]优选地,式(iia-ii)的-r10选自-h、甲基和乙基。
最优选地,式(iia-ii)的-r10是甲基。
[0578]优选地,式(iia-ii)的-r11选自-h、甲基和乙基。
最优选地,式(iia-ii)的-r11是-h。
[0579]优选地,式(iia-ii)的-r11被-l
2-z或-l
2-z’取代。
[0580]在一个甚至更优选的实施方案中,部分-l
1-具有式(iia-ii’):
[0581][0582]其中
[0583]其中虚线表示通过形成酰胺键连接至为pth部分的d的氮;
[0584]用星号标记的虚线表示连接至-l
2-;
[0585]-r3、-r3a、-r10和-x2-如式(ii)中所定义的使用;且
[0586]其中-l
1-任选地进一步被取代,条件是式(iia-ii’)中用星号标记的氢不被取代基替代。
[0587]应当理解,在式(iia-ii’)的-r3、-r3a之一或它们两者不为-h的情况中,它们通过sp3-杂化碳原子连接至它们所连接的n。
[0588]优选地,式(iia-ii’)的部分-l
1-不被进一步取代。
[0589]优选地,式(iia-ii’)的-x2-是-c(r8r8a)-。
[0590]优选地,式(iia-ii’)的-r8和-r8a独立地选自-h、甲基和乙基。
更优选地,式(iia-ii’)的-r8和-r8a的至少一个是-h。
甚至更优选地,式(iia-ii’)的-r8和-r8a均为-h。
[0591]优选地,式(iia-ii’)的-r3和-r3a独立地选自-h、甲基、乙基、丙基和丁基。
甚至更优选地,式(iia-ii’)的-r3和-r3a的至少一个是甲基。
[0592]优选地,式(iia-ii’)的-r3是-h且式(iia-ii’)的-r3a是甲基。
[0593]优选地,式(iia-ii’)的-r10选自-h、甲基和乙基。
最优选地,式(iia-ii’)的-r10是甲基。
[0594]甚至更优选地,部分-l
1-具有式(iia-iii):
[0595][0596]其中虚线表示通过形成酰胺键连接至为pth部分的d的氮;且
[0597]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代,条件是式(iia-iii)中用星号标记的氢不被-l
2-z或-l
2-z’或取代基替代。
[0598]应当理解,在式(iia-iii)的-r3、-r3a之一或它们两者不为-h的情况中,它们通过sp3-杂化碳原子连接至它们所连接的n。
[0599]优选地,式(iia-iii)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0600]优选地,式(iia-iii)的部分-l
1-不被进一步取代。
[0601]最优选地,部分-l
1-是式(iia-iii’):
[0602][0603]其中
[0604]其中虚线表示通过形成酰胺键连接至为pth部分的-d的氮;
[0605]用星号标记的虚线表示连接至-l
2-;
[0606]-r2、-r2a、-r3、-r3a和-x2-如式(ii)中所定义的使用;且
[0607]其中-l
1-任选地进一步被取代,条件是式(iib-iii’)中用星号标记的氢不被取代基替代。
[0608]应当理解,在式(iia-iii’)的-r3、-r3a之一或它们两者不为-h的情况中,它们通过sp3-杂化碳原子连接至它们所连接的n。
[0609]优选地,式(iia-iii’)的部分-l
1-不被进一步取代。
[0610]在另一个优选的实施方案中,部分-l
1-具有式(iib-i)[0611][0612]其中
[0613]虚线表示通过形成酰胺键连接至为pth部分的-d的氮;
[0614]-r1、-r1a、-r2、-r2a、-r3、-r3a、-r4和-x2-如式(ii)中所定义的使用;且
[0615]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代,条件是式(iib-i)中用星号标记的氢不被-l
2-z或-l
2-z’或取代基替代。
[0616]应当理解,在式(iib-i)的-r3、-r3a之一或它们两者不为-h的情况中,它们通过sp3-杂化碳原子连接至它们所连接的n。
[0617]优选地,式(iib-i)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0618]优选地,式(iib-i)的部分-l
1-不被进一步取代。
[0619]优选地,式(iib-i)的-r1和-r1a独立地选自-h、甲基和乙基。
更优选地,式(iib-i)的-r1和-r1a的至少一个是甲基。
甚至更优选地,式(iib-i)的-r1和-r1a均为甲基。
[0620]优选地,式(iib-i)的-r4选自-h、甲基和乙基。
更优选地,式(iib-i)的-r4是-h。
[0621]优选地,式(iib-i)的-x2-是-c(r8r8a)-。
[0622]优选地,式(iib-i)的-r8和-r8a独立地选自-h、甲基和乙基。
更优选地,式(iib-i)的-r8和-r8a的至少一个是-h。
甚至更优选地,式(iib-i)的-r8和-r8a均为-h。
[0623]优选地,式(iib-i)的-r2和-r2a独立地选自-h、甲基和乙基。
更优选地,式(iib-i)的-r2和-r2a的至少一个是-h。
甚至更优选地,式(iib-i)的-r2和-r2a均为h。
[0624]优选地,式(iib-i)的-r3和-r3a独立地选自-h,
甲基、乙基、丙基和丁基。
甚至更优选地,式(iib-i)的-r3和-r3a的至少一个-h。
甚至更优选地,式(iib-i)的-r3和-r3a均为-h。
[0625]更优选地,部分-l
1-具有式(iib-ii):
[0626][0627]其中虚线表示通过形成酰胺键连接至为pth部分的-d的氮;
[0628]-r2、-r2a、-r3、-r3a和-x2-如式(ii)中所定义的使用;且
[0629]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代,条件是式(iib-ii)中用星号标记的氢不被-l
2-z或-l
2-z’或取代基替代。
[0630]应当理解,在式(iib-ii)的-r3、-r3a之一或它们两者不为-h的情况中,它们通过sp3-杂化碳原子连接至它们所连接的n。
[0631]优选地,式(iib-ii)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0632]优选地,式(iib-ii)的部分-l
1-不被进一步取代。
[0633]优选地,式(iib-ii)的-x2-是-c(r8r8a)-。
[0634]优选地,式(iib-ii)的-r8和-r8a独立地选自-h、甲基和乙基。
更优选地,式(iib-ii)的-r8和-r8a的至少一个是-h。
甚至更优选地,式(iib-ii)的-r8和-r8a均为-h。
[0635]优选地,式(iib-ii)的-r2和-r2a独立地选自-h、甲基和乙基。
更优选地,式(iib-ii)的-r2和-r2a的至少一个是-h。
甚至更优选地,式(iib-ii)的-r2和-r2a均为h。
[0636]优选地,式(iib-ii)的-r3和-r3a独立地选自-h、甲基、乙基、丙基和丁基。
甚至更优选地,式(iib-ii)的-r3和-r3a的至少一个是-h。
甚至更优选地,式(iib-ii)的-r3和-r3a均为-h。
[0637]甚至更优选地,部分-l
1-具有式(iib-ii’):
[0638][0639]其中
[0640]虚线表示通过形成酰胺键连接至为pth部分的-d的氮;
[0641]-r2、-r2a、-r3a和-x2-如式(ii)中所定义的使用;且
[0642]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代,条件是式(iib-ii’)中用星号标记的氢不被-l
2-z或-l
2-z’或取代基替代。
[0643]应当理解,在式(iia-ii’)的-r3a不为-h的情况中,其通过sp3-杂化碳原子连接至它所连接的n。
[0644]优选地,式(iib-ii’)的部分-l
1-不被进一步取代。
[0645]优选地,式(iib-ii’)的-x2-是-c(r8r8a)-。
[0646]优选地,式(iib-ii’)的-r8和-r8a独立地选自-h、甲基和乙基。
更优选地,式(iib-ii’)的-r8和-r8a的至少一个是-h。
甚至更优选地,式(iib-ii’)的-r8和-r8a均为-h。
[0647]优选地,式(iib-ii’)的-r2和-r2a独立地选自-h、甲基和乙基。
更优选地,式(iib-ii’)的-r2和-r2a的至少一个是-h。
甚至更优选地,式(iib-ii’)的-r2和-r2a均为h。
[0648]优选地,式(iib-ii’)的-r3a选自-h、甲基、乙基、丙基和丁基。
在一个实施方案中,式(iib-ii’)的-r3a是-h。
[0649]甚至更优选地,部分-l
1-具有式(iib-iii):
[0650][0651]其中
[0652]虚线表示通过形成酰胺键连接至为pth部分的-d的氮;且
[0653]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代,条件是式(iib-iii)中用星号标记的氢不被-l
2-z或-l
2-z’或取代基替代。
[0654]应当理解,在式(iib-iii)的-r3、-r3a之一或它们两者不为-h的情况中,它们通过sp3-杂化碳原子连接至它们所连接的n。
[0655]优选地,式(iib-iii)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0656]优选地,式(iib-iii)的部分-l
1-不被进一步取代。
[0657]最优选地,部分-l
1-具有式(iib-iii’):
[0658][0659]其中
[0660]虚线表示通过形成酰胺键连接至为pth部分的-d的氮;
[0661]用星号标记的虚线表示连接至-l
2-z或-l
2-z’;且
[0662]其中-l
1-任选地进一步被取代,条件是式(iib-iii’)中用星号标记的氢不被取代基替代。
[0663]应当理解,式(iib-iii’)中与用星号标记的虚线相邻的氮通过sp3-杂化碳原子连接至-l
2-。
[0664]优选地,式(iib-iii’)的部分-l
1-未被进一步取代。
[0665]另一个优选的部分-l
1-公开在wo2016/020373a1中。
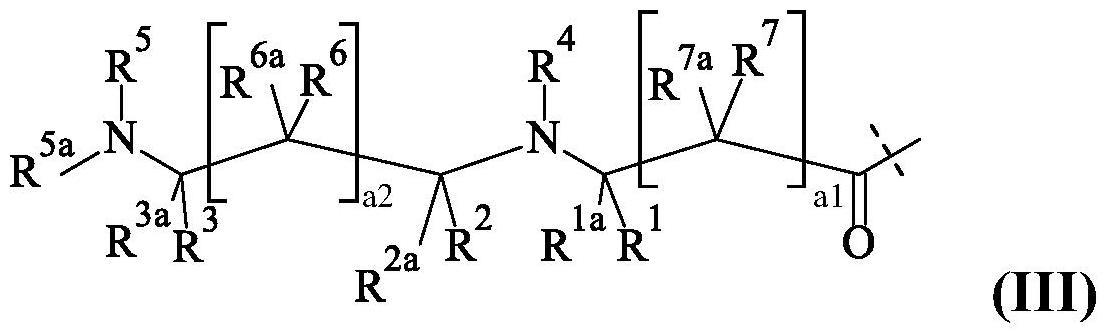
因此,在另一个优选的实施方案中,部分-l
1-具有式(iii):r6、-r5/-r7和-r6/-r7对的一个或多个与它们所连接的原子一起形成环a;
[0679]a选自苯基;萘基;茚基;茚满基;四氢萘基;c3-10环烷基;
3-至
10-元杂环基;和
8-至
11-元杂双环基;
[0680]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步取代;
[0681]其中
[0682]-l
2-是单一化学键或间隔基;
[0683]-z是水溶性载体;且
[0684]-z’是水不溶性载体。
[0685]式(iii)的-l
1-的任选另外的取代基优选地如上所述。
[0686]优选地,式(iii)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0687]在一个实施方案中,式(iii)的-l
1-未被进一步取代。
[0688]-l
1-的另外优选的实施方案公开在ep1536334b1、wo2009/009712a1、wo2008/034122a1、wo2009/143412a2、wo2011/082368a2和us8618124b2中,这些文献作为引用整体并入。
[0689]-l
1-的另外优选的实施方案公开在us8946405b2和us8754190b2中,这些文献作为引用整体并入。
因此,优选的部分-l
1-具有式(iv):
[0690][0691]其中
[0692]虚线表示连接至为pth部分的-d,且其中连接通过-d的官能团进行,所述-d的官能团选自-oh、-sh和-nh2;
[0693]m是0或1;
[0694]至少-r1和-r2之一或两者彼此独立地选自-cn、-no2、任选取代的芳基、任选取代的杂芳基、任选取代的烯基、任选取代的炔基、-c(o)r3、-s(o)r3、-s(o)2r3和-sr4;
[0695]-r1和-r2的一个且仅一个选自-h、任选取代的烷基、任选取代的芳基烷基和任选取代的杂芳基烷基;
[0696]-r3选自-h、任选取代的烷基、任选取代的芳基、任选取代的芳基烷基、任选取代的杂芳基、任选取代的杂芳基烷基、-or9和-n(r9)2;
[0697]-r4选自任选取代的烷基、任选取代的芳基、任选取代的芳基烷基、任选取代的杂芳基和任选取代的杂芳基烷基;
[0698]每个-r5独立地选自-h、任选取代的烷基、任选取代的烯基烷基、任选取代的炔基烷基、任选取代的芳基、任选取代的芳基烷基、任选取代的杂芳基和任选取代的杂芳基烷基;
[0699]-r9选自-h和任选取代的烷基;
[0700]-y-不存在且-x-是-o-或-s-;或
[0701]-y-是-n(q)ch2-且-x-是-o-;
[0702]q选自任选取代的烷基、任选取代的芳基、任选取代的芳基烷基、任选取代的杂芳
基和任选取代的杂芳基烷基;
[0703]任选地,-r1和-r2可以连接形成
3-8-元环;且
[0704]任选地,两个-r9与它们所连接的氮一起形成杂环;
[0705]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代;
[0706]其中
[0707]-l
2-是单一化学键或间隔基;
[0708]-z是水溶性载体;且
[0709]-z’是水不溶性载体。
[0710]仅在式(iv)的上下文中,所用术语具有如下含义:
[0711]如本文所用,术语“烷基”包括
1-8个碳或在一些实施方案中
1-6个或
1-4个碳原子的直链、支链或环状饱和烃基。
[0712]术语“烷氧基”包括键合至氧的烷基,包括甲氧基、乙氧基、异丙氧基、环丙氧基、环丁氧基等。
[0713]术语“烯基”包括具有碳-碳双键的非芳族不饱和烃。
[0714]术语“炔基”包括具有碳-碳三键的非芳族不饱和烃。
[0715]术语“芳基”包括
6-18个碳、优选
6-10个碳的芳香烃基团,包括基团,例如苯基、萘基和蒽基。
术语“杂芳基”包括芳族环,其包含
3-15个碳,包含至少一个n、o或s原子,优选地
3-7个碳,包含至少一个n、o或s原子,包括基团如吡咯基、吡啶基、嘧啶基、咪唑基、噁唑基、异噁唑基、噻唑基、异噻唑基、喹啉基、吲哚基、茚基等。
[0716]在一些情况中,烯基、炔基、芳基或杂芳基部分可以通过亚烷基键偶联至分子的其余部分。
那些情况中,取代基称作烯基烷基、炔基烷基、芳基烷基或杂芳基烷基,表示亚烷基部分位于烯基、炔基、芳基或杂芳基部分与烯基、炔基、芳基或杂芳基所偶联的分子之间。
[0717]术语“卤素”包括溴、氟、氯和碘。
[0718]术语“杂环”是指
4-8元芳族或非芳族环,其包含
3-7个碳原子和至少一个n、o或s原子。
实例为哌啶基、哌嗪基、四氢吡喃基、吡咯烷基和四氢呋喃基,以及为上述术语“杂芳基”提供的示例性基团。
[0719]当环系任选地被取代时,适合的取代基选自烷基、烯基、炔基或另外的环,它们各自任选地进一步被取代。
任意基团包括上述基团上的任选取代基包括卤素、硝基、氰基、-or、-sr、-nr2、-ocor、-nrcor、-coor、-conr2、-sor、-so2r、-sonr2、-so2nr2,其中每个r独立地为烷基、烯基、炔基、芳基或杂芳基,或两个r基团与它们所连接的原子一起形成环。
[0720]优选地,式(iv)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0721]-l
1-的另一个优选的实施方案公开在wo2013/036857a1中,其作为引用整体并入。
因此,优选的部分-l
1-具有式(v):
[0722][0723]其中
[0724]虚线表示连接至为pth部分的-d,且其中连接通过-d的胺官能团进行;
[0725]-r1选自任选取代的c1-c6直链、支链或环烷基;任选取代的芳基;任选取代的杂芳基;烷氧基;和-nr52;
[0726]-r2选自-h;任选取代的c1-c6烷基;任选取代的芳基;和任选取代的杂芳基;
[0727]-r3选自-h;任选取代的c1-c6烷基;任选取代的芳基;和任选取代的杂芳基;
[0728]-r4选自-h;任选取代的c1-c6烷基;任选取代的芳基;和任选取代的杂芳基;
[0729]每个-r5彼此独立地选自-h;任选取代的c1-c6烷基;任选取代的芳基;和任选取代的杂芳基;或彼此结合时两个-r5可以为环烷基或环杂烷基;
[0730]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代;
[0731]其中
[0732]-l
2-是单一化学键或间隔基;
[0733]-z是水溶性载体;且
[0734]-z’是水不溶性载体。
[0735]仅在式(v)的上下文中,所用术语具有如下含义:
[0736]“烷基”、“烯基”和“炔基”包括
1-8个碳或
1-6个碳或
1-4个碳的直链、支链或环状烃基,其中烷基是饱和烃,烯基包括一个或多个碳-碳双键,且炔基包括一个或多个碳-碳三键。
除非另有指定,否则它们包含
1-6个c。
[0737]“芳基”包括
6-18个碳、优选
6-10个碳的芳香烃,包括基团例如苯基、萘基和蒽。“杂芳基”包括包含
3-15个碳、包含至少一个n、o或s原子的芳族环,优选地
3-7个碳、包含至少一个n、o或s原子的芳族环,包括基团如吡咯基、吡啶基、嘧啶基、咪唑基、噁唑基、异噁唑基、噻唑基、异噻唑基、喹啉基、吲哚基、茚基等。
[0738]术语“取代的”是指烷基、烯基、炔基、芳基或杂芳基,其包含一个或多个取代基替代一个或多个氢原子。
取代基通常可以选自卤素,包括f、cl、br和i;低级烷基,包括直链、支链和环状的;低级卤代烷基,包括氟烷基、氯烷基、溴烷基和碘烷基;oh;低级烷氧基,包括直链、支链和环状的;sh;低级烷硫基,包括直链、支链和环状的;氨基、烷基氨基、二烷基氨基;甲硅烷基,包括烷基甲硅烷基、烷氧基甲硅烷基和芳基甲硅烷基;硝基;氰基;羰基;羧酸、羧酸酯、羧酰胺、氨基羰基;氨基酰基;氨基甲酸酯;脲;硫代氨基甲酸酯;硫脲;酮;砜;磺酰胺;芳基,包括苯基、萘基和蒽基;杂芳基,包括
5-元杂芳基,包括为吡咯、咪唑、呋喃、噻吩、噁唑、噻唑、异噁唑、异噻唑、噻二唑、三唑、噁二唑和四唑,
6-元芳基包括吡啶、嘧啶、吡嗪,和稠合杂芳基包括苯并呋喃、苯并噻吩、苯并噁唑、苯并咪唑、吲哚、苯并噻唑、苯并异噁唑和苯并异噻唑。
[0739]优选地,式(v)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0740]-l
1-的另一个优选的实施方案公开在us7585837b2中,其作为引用整体并入。
因此,优选的部分-l
1-具有式(vi):
[0741][0742]其中
[0743]虚线表示连接至为pth部分的-d,且其中连接通过-d的胺官能团进行;
[0744]r1和r2独立地选自氢、烷基、烷氧基、烷氧基烷基、芳基、烷芳基、芳烷基、卤素、硝基、-so3h、-so2nhr5、氨基、铵、羧基、po3h2和opo3h2;
[0745]r3、r4和r5独立地选自氢、烷基和芳基;
[0746]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代;
[0747]其中
[0748]-l
2-是单一化学键或间隔基;
[0749]-z是水溶性载体;且
[0750]-z’是水不溶性载体。
[0751]式(vi)的适合的取代基为烷基(例如c1-6烷基)、烯基(例如c2-6烯基)、炔基(例如c2-6炔基)、芳基(例如苯基)、杂烷基、杂烯基、杂炔基、杂芳基(例如芳族
4-7元杂环)或卤素部分。
[0752]仅中式(vi)的上下文中,所用术语具有如下含义:
[0753]术语“烷基”、“烷氧基”、“烷氧基烷基”、“芳基”、“烷芳基”和“芳烷基”是指
1-8个、优选地
1-4个碳原子的烷基基团,例如甲基、乙基、丙基、异丙基和丁基;以及
6-10个碳原子的芳基基团,例如苯基和萘基。
术语“卤素”包括溴、氟、氯和碘。
[0754]优选地,式(vi)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0755]-l
1-的另一个优选的实施方案公开在wo2002/089789a1中,其作为引用整体并入。
因此,优选的部分-l
1-具有式(vii):
[0756][0757]其中
[0758]虚线表示连接至为pth部分的-d,且其中连接通过-d的胺官能团进行;
[0759]l1是双官能连接基,
[0760]y1和y2独立地为o、s或nr7;
[0761]r2、r3、r4、r5、r6和r7独立地选自氢、c1-6烷基、c3-12支链烷基、c3-8环烷基、c1-6取代的烷基、c3-8取代的环烷基、芳基、取代的芳基、芳烷基、c1-6杂烷基、取代的c1-6杂烷基、c1-6烷氧基、苯氧基和c1-6杂烷氧基;
[0762]ar是这样的部分,当包括在式(vii)中时,其形成多取代的芳香烃或多取代的杂环基;
[0763]x是化学键或主动转运入靶细胞的部分、疏水性部分或其组合,
[0764]y是0或1;
[0765]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代;
[0766]其中
[0767]-l
2-是单一化学键或间隔基;
[0768]-z是水溶性载体;且
[0769]-z’是水不溶性载体。
[0770]仅在式(vii)的上下文中,所用术语具有如下含义:
[0771]术语“烷基”应当理解为包括例如直链、支链、取代的c1-12烷基,包括烷氧基、c3-8环烷基或取代的环烷基等。
[0772]术语“取代的”应当理解为包括用一个或多个不同原子添加或替代官能团或化合物内包含的一个或多个原子。
[0773]取代的烷基包括羧基烷基、氨基烷基、二烷基氨基、羟基烷基和巯基烷基;取代的环烷基包括部分例如
4-氯环己基;芳基包括部分例如萘基;取代的芳基包括部分例如
3-溴-苯基;芳烷基包括部分例如甲苯甲酰基;杂烷基包括部分例如乙基噻吩;取代的杂烷基包括部分例如
3-甲氧基噻吩;烷氧基包括部分例如甲氧基;并且苯氧基包括部分例如
3-硝基苯氧基。
卤代-应理解为包括氟、氯、碘和溴。
[0774]优选地,式(vii)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0775]在另一个优选的实施方案中,-l
1-包含式(viii)的亚结构
[0776][0777]其中
[0778]用星号标记的虚线表示通过形成酰胺键键连接至为pth部分的-d的氮;
[0779]未标记的虚线表示连接至-l
1-的其余部分;且
[0780]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代;
[0781]其中
[0782]-l
2-是单一化学键或间隔基;
[0783]-z是水溶性载体;且
[0784]-z’是水不溶性载体。
[0785]优选地,式(viii)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0786]在一个实施方案中,式(viii)的-l
1-不被进一步取代。
[0787]在另一个优选的实施方案中,-l
1-包含式(ix)的亚结构,
[0788][0789]其中
[0790]用星号标记的虚线表示通过形成氨基甲酸酯键连接至为pth部分的-d的氮;
[0791]未标记的虚线表示连接至-l
1-的其余部分;且
[0792]其中-l
1-被-l
2-z或-l
2-z’取代,且其中-l
1-任选地进一步被取代;
[0793]其中
[0794]-l
2-是单一化学键或间隔基;
[0795]-z是水溶性载体;且
[0796]-z’是水不溶性载体。
[0797]优选地,式(ix)的-l
1-被一个部分-l
2-z或-l
2-z’取代。
[0798]在一个实施方案中,式(ix)的-l
1-不被进一步取代。
[0799]在本发明的前药中,-l
2-是化学键或间隔基部分。
[0800]在一个实施方案中,-l
2-是化学键。
[0801]在另一个实施方案中,-l
2-是间隔基部分。
[0802]当-l
2-不是单一化学键时,-l
2-优选选自-t-、-c(o)o-、-o-、-c(o)-、-c(o)n(ry1)-、-s(o)2n(ry1)-、-s(o)n(ry1)-、-s(o)2-、-s(o)-、-n(ry1)s(o)2n(ry1a)-、-s-、-n(ry1)-、-oc(ory1)(ry1a)-、-n(ry1)c(o)n(ry1a)-、-oc(o)n(ry1)-、c1-50
烷基、c2-50
烯基和c2-50
炔基;其中-t-、c1-50
烷基、c2-50
烯基和c2-50
炔基任选地被一个或多个相同或不同的-ry2取代,且其中c1-50
烷基、c2-50
烯基和c2-50
炔基任选地被一个或多个基团打断,所述基团选自-t-、-c(o)o-、-o-、-c(o)-、-c(o)n(ry3)-、-s(o)2n(ry3)-、-s(o)n(ry3)-、-s(o)2-、-s(o)-、-n(ry3)s(o)2n(ry3a)-、-s-、-n(ry3)-、-oc(ory3)(ry3a)-、-n(ry3)c(o)n(ry3a)-和-oc(o)n(ry3)-;
[0803]-ry1和-ry1a彼此独立地选自-h、-t、c1-50
烷基、c2-50
烯基和c2-50
炔基;其中-t、c1-50
烷基、c2-50
烯基和c2-50
炔基任选地被一个或多个相同或不同的-ry2取代,且其中c1-50
烷基、c2-50
烯基和c2-50
炔基任选地被一个或多个基团打断,所述基团选自-t-、-c(o)o-、-o-、-c(o)-、-c(o)n(ry4)-、-s(o)2n(ry4)-、-s(o)n(ry4)-、-s(o)2-、-s(o)-、-n(ry4)s(o)2n(ry4a)-、-s-、-n(ry4)-、-oc(ory4)(ry4a)-、-n(ry4)c(o)n(ry4a)-和-oc(o)n(ry4)-;
[0804]每个t独立地选自苯基、萘基、茚基、茚满基、四氢萘基、c3-10环烷基、3-至
10-元杂环基、8-至
11-元杂双环基、8-至
30-元碳多环基和
8-至
30-元杂多环基;其中每个t独立地任选地被一个或多个相同或不同的-ry2取代;
[0805]每个-ry2独立地选自卤素、-cn、氧代(=o)、-coory5、-ory5、-c(o)ry5、-c(o)n(ry5ry5a)、-s(o)2n(ry5ry5a)、-s(o)n(ry5ry5a)、-s(o)2ry5、-s(o)ry5、-n(ry5)s(o)2n(ry5ary5b)、-sry5、-n(ry5ry5a)、-no2、-oc(o)ry5、-n(ry5)c(o)ry5a、-n(ry5)s(o)2ry5a、-n(ry5)s(o)ry5a、-n(ry5)c(o)ory5a、-n(ry5)c(o)n(ry5ary5b)、-oc(o)n(ry5ry5a)和c1-6烷基;其中c1-6烷基任选地被一个或多个相同或不同的卤素取代;且
[0806]每个-ry3、-ry3a、-ry4、-ry4a、-ry5、-ry5a和-ry5b独立地选自-h和c1-6烷基,其中c1-6烷基任选地被一个或多个相同或不同的卤素取代。
[0807]当-l
2-不是单一化学键时,-l
2-甚至更优选选自-t-、-c(o)o-、-o-、-c(o)-、-c(o)n(ry1)-、-s(o)2n(ry1)-、-s(o)n(ry1)-、-s(o)2-、-s(o)-、-n(ry1)s(o)2n(ry1a)-、-s-、-n(ry1)-、-oc(ory1)(ry1a)-、-n(ry1)c(o)n(ry1a)-、-oc(o)n(ry1)-、c1-50
烷基、c2-50
烯基和c2-50
炔基;其中-t-、c1-20
烷基、c2-20
烯基和c2-20
炔基任选地被一个或多个相同或不同的-ry2取代,且其中c1-20
烷基、c2-20
烯基和c2-20
炔基任选地被一个或多个基团打断,所述基团选自-t-、-c(o)o-、-o-、-c(o)-、-c(o)n(ry3)-、-s(o)2n(ry3)-、-s(o)n(ry3)-、-s(o)2-、-s(o)-、-n(ry3)s(o)2n(ry3a)-、-s-、-n(ry3)-、-oc(ory3)(ry3a)-、-n(ry3)c(o)n(ry3a)-和-oc(o)n(ry3)-;
[0808]-ry1和-ry1a彼此独立地选自-h、-t、c1-10烷基、c2-10烯基和c2-10炔基;其中-t、c1-10烷基、c2-10烯基和c2-10炔基任选地被一个或多个相同或不同的-ry2取代,且其中c1-10烷基、c2-10烯基和c2-10炔基任选地被一个或多个基团打断,所述基团选自-t-、-c(o)o-、-o-、-c(o)-、-c(o)n(ry4)-、-s(o)2n(ry4)-、-s(o)n(ry4)-、-s(o)2-、-s(o)-、-n(ry4)s(o)2n(ry4a)-、-s-、-n(ry4)-、-oc(ory4)(ry4a)-、-n(ry4)c(o)n(ry4a)-和-oc(o)n(ry4)-;
[0809]每个t独立地选自苯基、萘基、茚基、茚满基、四氢萘基、c3-10环烷基、3-至
10-元杂环基、8-至
11-元杂双环基、8-至
30-元碳多环基和
8-至
30-元杂多环基;其中每个t独立地任选地被一个或多个相同或不同的-ry2取代;
[0810]-ry2选自卤素、-cn、氧代(=o)、-coory5、-ory5、-c(o)ry5、-c(o)n(ry5ry5a)、-s(o)2n(ry5ry5a)、-s(o)n(ry5ry5a)、-s(o)2ry5、-s(o)ry5、-n(ry5)s(o)2n(ry5ary5b)、-sry5、-n(ry5ry5a)、-no2、-oc(o)ry5、-n(ry5)c(o)ry5a、-n(ry5)s(o)2ry5a、-n(ry5)s(o)ry5a、-n(ry5)c(o)ory5a、-n(ry5)c(o)n(ry5ary5b)、-oc(o)n(ry5ry5a)和c1-6烷基;其中c1-6烷基任选地被一个或多个相同或不同的卤素取代;且
[0811]每个-ry3、-ry3a、-ry4、-ry4a、-ry5、-ry5a和-ry5b彼此独立地选自-h和c1-6烷基;其中c1-6烷基任选地被一个或多个相同或不同的卤素取代。
[0812]当-l
2-不是单一化学键时,-l
2-甚至更优选选自-t-、-c(o)o-、-o-、-c(o)-、-c(o)n(ry1)-、-s(o)2n(ry1)-、-s(o)n(ry1)-、-s(o)2-、-s(o)-、-n(ry1)s(o)2n(ry1a)-、-s-、-n(ry1)-、-oc(ory1)(ry1a)-、-n(ry1)c(o)n(ry1a)-、-oc(o)n(ry1)-、c1-50
烷基、c2-50
烯基和c2-50
炔基;其中-t-、c1-50
烷基、c2-50
烯基和c2-50
炔基任选地被一个或多个相同或不同的-ry2取代,且其中c1-50
烷基、c2-50
烯基和c2-50
炔基任选地被一个或多个基团打断,所述基团选自-t-、-c(o)o-、-o-、-c(o)-、-c(o)n(ry3)-、-s(o)2n(ry3)-、-s(o)n(ry3)-、-s(o)2-、-s(o)-、-n(ry3)s(o)2n(ry3a)-、-s-、-n(ry3)-、-oc(ory3)(ry3a)-、-n(ry3)c(o)n(ry3a)-和-oc(o)n(ry3)-;
[0813]-ry1和-ry1a独立地选自-h、-t、c1-10烷基、c2-10烯基和c2-10炔基;
[0814]每个t独立地选自苯基、萘基、茚基、茚满基、四氢萘基、c3-10环烷基、3-至
10-元杂环基、8-至
11-元杂双环基、8-至
30-元碳多环基和
8-至
30-元杂多环基;
[0815]每个-ry2独立地各自选自卤素和c1-6烷基;且
[0816]每个-ry3、-ry3a、-ry4、-ry4a、-ry5、-ry5a和-ry5b彼此独立地选自-h和c1-6烷基;其中c1-6烷基任选地被一个或多个相同或不同的卤素取代。
[0817]甚至更优选地,-l
2-是c1-20
烷基链,其任选地被一个或多个基团打断,所述基团独立地选自-o-、-t-和-c(o)n(ry1)-;且该c1-20
烷基链任选地被一个或多个基团取代,所述基团独立地选自-oh、-t和-c(o)n(ry6ry6a);其中-ry1、-ry6、-ry6a独立地选自h和c1-4烷基,且其中t选自苯基、萘基、茚基、茚满基、四氢萘基、c3-10环烷基、3-至
10-元杂环基、8-至
11-元杂双环基、8-至
30-元碳多环基和
8-至
30-元杂多环基。
[0818]优选地,-l
2-具有
14g/mol-750g/mol
的分子量。
[0819]优选地,-l
2-包含选自如下的部分
[0820][0821][0822]其中
[0823]虚线表示分别连接至-l
2-、-l
1-、-z和/或-z'
的其余部分;且
[0824]-r和-ra彼此独立地选自-h、甲基、乙基、丙基、丁基、戊基和己基。
[0825]在一个优选的实施方案中,-l
2-具有
1-20
个原子的链长。
[0826]如本文所用,术语“链长”在部分-l
2-方面是指存在于-l
1-与-z之间最短连接中的-l
2-的原子数。
[0827]优选地,-l
2-具有式(i)[0828][0829]其中
[0830]用星号标记的虚线表示连接至-l
1-;
[0831]未标记的虚线表示连接至-z或-z'
;
[0832]n选自
0、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17和
18;且
[0833]其中式(i)的部分任选地进一步被取代。
[0834]优选地,式(i)的n选自
3、4、5、6、7、8和
9。
甚至更优选地,式(i)的n是
4、5、6或
7。
在一个实施方案中,式(i)的n是
4。
在另一个实施方案中,式(i)的n是
5。
在另一个实施方案中,式(i)的n是
6。
[0835]在一个优选的实施方案中,部分-l
1-l
2-选自
[0836][0837][0838]其中
[0839]未标记的虚线表示通过形成酰胺键连接至为pth部分的-d的氮;且
[0840]用星号标记的虚线表示连接至-z或-z’。
[0841]在另一个优选的实施方案中,部分-l
1-l
2-选自
[0842][0843]其中
[0844]未标记的虚线表示通过形成酰胺键连接至为pth部分的-d的氮;且
[0845]用星号标记的虚线表示连接至-z或-z’。
[0846]在一个优选的实施方案中,部分-l
1-l
2-具有式(iica-ii)。
[0847]在另一个优选的实施方案中,部分-l
1-l
2-具有式(iicb-iii)。
[0848]优选地,本发明的控释pth化合物具有式(ia),其中x=
1。
[0849]载体-z包含c8-24烷基或聚合物。
优选地,-z包含聚合物,优选地,聚合物选自:
2-甲基丙烯酰基-氧基乙基磷酰胆碱、聚(丙烯酸)、聚(丙烯酸酯)、聚(丙烯酰胺)、聚(烷氧基)聚合物、聚(酰胺)、聚(酰氨基胺)、聚(氨基酸)、聚(酸酐)、聚(天冬酰胺)、聚(丁酸)、聚(乙醇酸)、聚对苯二甲酸丁二醇酯、聚(己内酯)、聚(碳酸酯)、聚(氰基丙烯酸酯)、聚(二甲基丙烯酰胺)、聚(酯)、聚(乙烯)、聚(乙二醇)、聚(环氧乙烷)、聚(磷酸乙酯)、聚(乙基噁唑啉)、聚(乙醇酸)、聚(丙烯酸羟乙酯)、聚(羟乙基-噁唑啉)、聚(羟甲基丙烯酸酯)、聚(羟丙基甲基丙烯酰胺)、聚(甲基丙烯酸羟丙酯)、聚(羟丙基噁唑啉)、聚(亚氨基碳酸酯)、聚(乳酸)、聚(乳酸-共-乙醇酸)、聚(甲基丙烯酰胺)、聚(甲基丙烯酸酯)、聚(甲基噁唑啉)、聚(有机磷腈)、聚(原酸酯)、聚(噁唑啉)、聚(丙二醇)、聚(硅氧烷)、聚(氨基甲酸酯)、聚(乙烯醇)、聚(乙烯胺)、聚(乙烯基甲基醚)、聚(乙烯基吡咯烷酮)、硅酮、纤维素、羧甲基纤维素、羟丙基甲基纤维素、甲壳质、脱乙酰壳多糖、葡聚糖、糊精、明胶、透明质酸和衍生物、官能化透明质酸、甘露聚糖、果胶、鼠李糖半乳糖醛酸聚糖、淀粉、羟烷基淀粉、羟乙基淀粉和其它基于碳水化合物的聚合物、木聚糖及其共聚物。
[0850]优选地,-z具有
5-200kda的分子量。
甚至更优选地,-z具有
8-100kda的分子量,甚至更优选地
10-80kda,甚至更优选地
12-60,甚至更优选地
15-40
且最优选地-z具有约
20kda的分子量。
在另一个等同优选的实施方案中,-z具有约
40kda的分子量。
[0851]在一个实施方案中,这类水溶性载体-z包含蛋白质。
优选的蛋白质选自如us2012/0035101a1中所述的绒毛膜促性腺激素的羧基末端多肽,该文献作为引用并入;白蛋白;如wo2011123813a2中所述的xten序列,该文献作为引用并入;如wo2011/144756a1中所述的脯氨酸/丙氨酸无规卷曲序列,该文献作为引用并入;如wo2008/155134a1和wo2013/024049a1中所述的脯氨酸/丙氨酸/丝氨酸无规卷曲序列,该文献作为引用并入;和fc融合蛋白。
[0852]在一个实施方案中,-z是聚肌氨酸(polysarcosine)。
[0853]在另一个优选的实施方案中,-z包含聚(n-甲基甘氨酸)。
[0854]在一个特别优选的实施方案中,-z包含无规卷曲蛋白部分。
[0855]在一个优选的实施方案中,-z包含1个无规卷曲蛋白部分。
[0856]在另一个优选的实施方案中,-z包含2个无规卷曲蛋白部分。
[0857]在另一个优选的实施方案中,-z包含3个无规卷曲蛋白部分。
[0858]在另一个优选的实施方案中,-z包含4个无规卷曲蛋白部分。
[0859]在另一个优选的实施方案中,-z包含5个无规卷曲蛋白部分。
[0860]在另一个优选的实施方案中,-z包含6个无规卷曲蛋白部分。
[0861]在另一个优选的实施方案中,-z包含7个无规卷曲蛋白部分。
[0862]在另一个优选的实施方案中,-z包含8个无规卷曲蛋白部分。
[0863]优选地,这类无规卷曲蛋白部分包含至少
25个氨基酸残基和至多
2000
个氨基酸。
甚至更优选地,这类无规卷曲蛋白部分包含至少
30
个氨基酸残基和至多
1500
个氨基酸残基。
甚至更优选地,这类无规卷曲蛋白部分包含至少
50
个氨基酸残基和至多
500
个氨基酸残基。
[0864]在一个优选的实施方案中,-z包含无规卷曲蛋白部分,其中形成所述无规卷曲蛋白部分的氨基酸总数的至少
80
%、优选至少
85%、甚至更优选至少
90
%、甚至更优选至少
95%、甚至更优选至少
98%且最优选地至少
99%选自丙氨酸和脯氨酸。
甚至更优选地,至少
10%但少于
75%、优选少于
65%的这类无规卷曲蛋白部分的氨基酸残基总数是脯氨酸残基。
优选地,这类无规卷曲蛋白部分如wo 2011/144756a1中所述,其通过引用整体并入本文。
甚至更优选地,-z包含至少一个部分,选自seq id no:1、seq id no:2、seq id no:3、seq id no:4、seq id no:5、seq id no:6、seq id no:7、seq id no:8、seq id no:9、seq id no:10、seq id no:11、seq id no:12、seq id no:13、seq id no:14、seq id no:15、seq id no:16、seq id no:17、seq id no:51和seq id no:61,如wo2011/144756中所公开的,所述文献通过引用并入本文。
包含含有丙氨酸和脯氨酸的这类无规卷曲蛋白的部分称作“pa”或“pa部分”。
[0865]因此,-z包含pa部分。
[0866]在一个等同优选的实施方案中,-z包含无规卷曲蛋白部分,其中形成所述无规卷曲蛋白部分的氨基酸总数的至少
80
%、优选地至少
85%、甚至更优选地至少
90
%、甚至更优选地至少
95%、甚至更优选地至少
98%且最优选地至少
99%选自丙氨酸、丝氨酸和脯氨酸。
甚至更优选地,至少4%但少于
40
%的这类无规卷曲蛋白部分的氨基酸残基总数是脯氨酸残基。
优选地,这类无规卷曲蛋白部分如wo 2008/155134 a1中所述,其通过引用整体并入本文。
甚至更优选地,-z包含至少一种部分,其选自seq id no:2、seq id no:4、seq id no:6、seq id no:8、seq id no:10、seq id no:12、seq id no:14、seq id no:16、seq id no:18、seq id no:20、seq id no:22、seq id no:24、seq id no:26、seq id no:28、seq id no:30、seq id no:32、seq id no:34、seq id no:36、seq id no:40、seq id no:42、seq id no:44、seq id no:46、seq id no:50、seq id no:52、seq id no:54和seq id no:56,如wo 2008/155134a1中所公开的,所述文献通过引用并入本文。
包含含有丙氨酸、丝氨酸和脯氨no:216、seq id no:217、seq id no:218、seq id no:219、seq id no:220、seq id no:221、seq id no:759、seq id no:760、seq id no:761、seq id no:762、seq id no:763、seq id no:764、seq id no:765、seq id no:766、seq id no:767、seq id no:768、seq id no:769、seq id no:770、seq id no:771、seq id no:772、seq id no:773、seq id no:774、seq id no:775、seq id no:776、seq id no:777、seq id no:778、seq id no:779、seq id no:1715、seq id no:1716、seq id no:1718、seq id no:1719、seq id no:1720、seq id no:1721和seq id no:1722,如wo2010/091122a1中公开,其通过引用并入本文。
包含含有丙氨酸、甘氨酸、丝氨酸、苏氨酸、谷氨酸和脯氨酸的这类无规卷曲蛋白部分的部分称作“xten”或“xten部分”,与其在wo 2010/091122 a1中的命名一致。
[0888]因此,-z包含xten部分。
[0889]在另一个优选的实施方案中,-z包含脂肪酸衍生物。
优选的脂肪酸衍生物是wo 2005/027978 a2和wo 2014/060512 a1中公开的那些,其通过引用并入本文。
[0890]在另一个优选的实施方案中,-z是基于透明质酸的聚合物。
[0891]在一个实施方案中,-z是如wo 2012/02047a1中公开的载体,该文献通过引用并入本文。
[0892]在另一个实施方案中,-z是如wo 2013/024048 a1中公开的载体,该文献通过引用并入本文。
[0893]在另一个实施方案中,-z是基于peg的聚合物,例如基于peg的直链、支链或多臂聚合物。
[0894]在一个实施方案中,-z是基于peg的直链聚合物。
[0895]在另一个实施方案中,-z是基于peg的多臂聚合物。
优选地,-z是基于peg的多臂聚合物,其具有至少4个基于peg的臂。
[0896]优选地,这类基于peg的多臂聚合物-z连接至多个部分-l
2-l
1-d,其中每个部分-l
2-l
1-d优选地连接至臂的末端,优选地,连接至臂的末端。
优选地,这类基于peg的多臂聚合物-z连接至
2、3、4、5、6、7、8、9、10、11、12、13、14、15或
16个部分-l
2-l
1-d。
甚至更优选地,这类基于peg的多臂聚合物-z连接至
2、3、4、6或8个部分-l
2-l
1-d。
甚至更优选地,这类基于peg的多臂聚合物-z连接至
2、4或6个部分-l
2-l
1-d,甚至更优选地这类基于peg的多臂聚合物-z连接至4或6个部分-l
2-l
1-d,且最优选地,这类基于peg的多臂聚合物-z连接至4个部分-l
2-l
1-d。
[0897]优选地,这类基于peg的多臂聚合物-z是多臂peg衍生物,例如详细描述在jenkem technology,usa中的产品清单(2014年
12月
18日从http://www.jenkemusa.com/pages/pegproducts.aspx下载得到),例如
4-臂-peg衍生物,特别是包含季戊四醇核的
4-臂-peg、包含六甘油核的
8-臂-peg衍生物和包含三季戊四醇核的
8-臂-peg衍生物。
更优选地,水溶性peg基载体-z包含选自如下的部分:
[0898]包含季戊四醇核的
4-臂peg胺:
[0899][0900]其中n为
20-500
;
[0901]包含六甘油核的
8-臂peg胺:
[0902][0903]其中n为
20-500
;且
[0904]r=六甘油或三季戊四醇核结构;和
[0905]包含山梨醇或二季戊四醇核的
6-臂peg胺:
[0906][0907]其中n为
20-500
;且
[0908]r=包含山梨醇或二季戊四醇核;
[0909]且其中虚线表示连接至pth前药的其余部分。
[0910]在一个优选的实施方案中,-z是基于peg的支链聚合物。
在一个实施方案中,-z是基于peg的支链聚合物,其具有
1、2、3、4、5或6个支化点。
优选地,-z是基于peg的支链聚合物,其具有
1、2或3个支化点。
在一个实施方案中,-z是基于peg的支链聚合物,其具有1个支化点。
在另一个实施方案中,-z是基于peg的支链聚合物,其具有2个支化点。
在另一个实施方案中,-z是基于peg的支链聚合物,其具有3个支化点。
[0911]支化点优选选自-n《、-ch《
和
》c《。
[0912]优选地,这类基于peg的支链部分-z具有至少
10kda的分子量。
[0913]在一个实施方案中,这类支链部分-z具有从
10kda到
500kda且包括
10kda和
500kda的分子量,更优选地具有从
10kda到
250kda且包括
10kda和
250kda的分子量,甚至更优选地具有从
10kda到
150kda且包括
10kda和
150kda的分子量,甚至更优选地具有从
12kda到
100kda且包括
12kda和
100kda的分子量,且最优选地具有从
15kda到
80kda且包括
15kda和
80kda的分子量。
[0914]优选地,这类支链部分-z具有从
10kda到
80kda且包括
10kda和
80kda的分子量。
在一个实施方案中,分子量约为
10kda。
在另一个实施方案中,这类支链部分-z的分子量约为
20kda。
在另一个实施方案中,这类支链部分-z的分子量约为
30kda。
在另一个实施方案中,这类支链部分-z的分子量约为
40kda。
在另一个实施方案中,这类支链部分-z的分子量约为
50kda。
在另一个实施方案中,这类支链部分-z的分子量约为
60kda。
在另一个实施方案中,这类支链部分-z的分子量约为
70kda。
在另一个实施方案中,这类支链部分-z的分子量约为
80kda。
最优选地,这类支链部分-z具有约
40kda的分子量。
[0915]优选地,-z或-z'
包含部分
[0916][0917]在一个等同优选的实施方案中,-z包含酰胺键。
[0918]优选地,-z包含式(a)的部分
[0919][0920]其中
[0921]虚线表示连接至-l
2-或连接至-z的其余部分;
[0922]bpa是选自-n《、-cr《
和
》c《
的分支点;
[0923]-r选自-h和c1-6烷基;
[0924]如果bpa是-n《
或-cr《,则a是0,且如果bpa是
》c《,则n是1;
[0925]-sa-、-sa’-、-sa”‑
和-sa”’-彼此独立地为化学键或选自c1-50
烷基、c2-50
烯基和c2-50
炔基;其中c1-50
烷基、c2-50
烯基和c2-50
炔基任选地被一个或多个相同或不同的-r1取代,且其中c1-50
烷基、c2-50
烯基和c2-50
炔基任选地被一个或多个基团打断,所述基团选自-t-、-c(o)o-、-o-、-c(o)-、-c(o)n(r2)-、-s(o)2n(r2)-、-s(o)n(r2)-、-s(o)2-、-s(o)-、-n(r2)s(o)2n(r2a)-、-s-、-n(r2)-、-oc(or2)(r2a)-、-n(r2)c(o)n(r2a)-和-oc(o)n(r2)-;
[0926]每个-t-独立地选自苯基、萘基、茚基、茚满基、四氢萘基、c3-10环烷基、3-至
10-元杂环基、8-至
11-元杂双环基、8-至
30-元碳多环基和
8-至
30-元杂多环基;其中每个-t-独立地任选地被一个或多个相同或不同的-r1取代;
[0927]每个-r1独立地选自卤素、-cn、氧代(=o)、-coor3、-or3、-c(o)r3、-c(o)n(r3r3a)、-s(o)2n(r3r3a)、-s(o)n(r3r3a)、-s(o)2r3、-s(o)r3、-n(r3)s(o)2n(r3ar3b)、-sr3、-n(r3r3a)、-no2、-oc(o)r3、-n(r3)c(o)r3a、-n(r3)s(o)2r3a、-n(r3)s(o)r3a、-n(r3)c(o)or3a、-n(r3)c(o)n(r3ar3b)、-oc(o)n(r3r3a)和c1-6烷基;其中c1-6烷基任选地被一个或多个相同或不同的卤素取代;
[0928]每个-r2、-r2a、-r3、-r3a和-r3b独立地选自-h和c1-6烷基,其中c1-6烷基任选地被一个或多个相同或不同的卤素取代;且
[0929]-pa’、-pa”和-pa”’
独立地为聚合物部分。
[0930]在一个实施方案中,式(a)的bpa是-n《。
[0931]在另一个实施方案中,式(a)的bpa是
》c《。
[0932]在一个优选的实施方案中,式(a)的bpa是-cr《。
优选地,-r是-h。
因此,式(a)的a是
0。
[0933]在一个实施方案中,式(a)的-sa-是化学键。
[0934]在另一个实施方案中,式(a)的-sa-选自c1-10烷基、c2-10烯基和c2-10炔基,该c1-10烷基、c2-10烯基和c2-10炔基任选地被一个或多个化学基团打断,所述化学基团选自-t-、-c(o)o-、-o-、-c(o)-、-c(o)n(r4)-、-s(o)2n(r4)-、-s(o)n(r4)-、-s(o)2-、-s(o)-、-n(r4)s(o)2n(r4a)-、-s-、-n(r4)-、-oc(or4)(r4a)-、-n(r4)c(o)n(r4a)-和-oc(o)n(r4)-;其中-t-是
3-至
10-元杂环基;且-r4和-r4a独立地选自-h、甲基、乙基、丙基和丁基。
[0935]优选地,式(a)的-sa-选自c1-10烷基,其被一个或多个选自-t-、-c(o)n(r4)-和-o-的化学基团打断。
[0936]在一个实施方案中,式(a)的-sa’-是化学键。
[0937]在另一个实施方案中,式(a)的-sa’-选自c1-10烷基、c2-10烯基和c2-10炔基,该c1-10烷基、c2-10烯基和c2-10炔基任选地被一个或多个化学基团打断,所述化学基团选自-c(o)o-、-o-、-c(o)-、-c(o)n(r4)-、-s(o)2n(r4)-、-s(o)n(r4)-、-s(o)2-、-s(o)-、-n(r4)s(o)2n(r4a)-、-s-、-n(r4)-、-oc(or4)(r4a)-、-n(r4)c(o)n(r4a)-和-oc(o)n(r4)-;其中-r4和-r4a独立地选自-h、甲基、乙基、丙基和丁基。
优选地,式(a)的-sa’-选自甲基、乙基、丙基、丁基,其任选地被一个或多个选自-o-、-c(o)-和-c(o)n(r4)-的化学基团打断。
[0938]在一个实施方案中,式(a)的-sa”‑
是化学键。
[0939]在另一个实施方案中,式(a)的-sa”‑
选自c1-10烷基、c2-10烯基和c2-10炔基,该c1-10烷基、c2-10烯基和c2-10炔基任选地被一个或多个化学基团打断,所述化学基团选自-c(o)o-、-o-、-c(o)-、-c(o)n(r4)-、-s(o)2n(r4)-、-s(o)n(r4)-、-s(o)2-、-s(o)-、-n(r4)s(o)2n(r4a)-、-s-、-n(r4)-、-oc(or4)(r4a)-、-n(r4)c(o)n(r4a)-和-oc(o)n(r4)-;其中-r4和-r4a独立地选自-h、甲基、乙基、丙基和丁基。
优选地,式(a)的-sa”‑
选自甲基、乙基、丙基、丁基,其任选地被一个或多个选自-o-、-c(o)-和-c(o)n(r4)-的化学基团打断。
[0940]在一个实施方案中,式(a)的-sa”’-是化学键。
[0941]在另一个实施方案中,式(a)的-sa”’-选自c1-10烷基、c2-10烯基和c2-10炔基,该c1-10烷基、c2-10烯基和c2-10炔基任选地被一个或多个化学基团打断,所述化学基团选自-c(o)o-、-o-、-c(o)-、-c(o)n(r4)-、-s(o)2n(r4)-、-s(o)n(r4)-、-s(o)2-、-s(o)-、-n(r4)s(o)2n(r4a)-、-s-、-n(r4)-、-oc(or4)(r4a)-、-n(r4)c(o)n(r4a)-和-oc(o)n(r4)-;其中-r4和-r4a独立地选自-h、甲基、乙基、丙基和丁基。
优选地,式(a)的-sa”’-选自甲基、乙基、丙基、丁基,其任选地被一个或多个选自-o-、-c(o)-和-c(o)n(r4)-的化学基团打断。
[0942]优选地,式(a)的-pa’、-pa”和-pa”’
独立地包含聚合物,其选自
2-甲基丙烯酰基-氧基乙基磷酰胆碱、聚(丙烯酸)、聚(丙烯酸酯)、聚(丙烯酰胺)、聚(烷氧基)聚合物、聚(酰胺)、聚(酰氨基胺)、聚(氨基酸)、聚(酸酐)、聚(天冬酰胺)、聚(丁酸)、聚(乙醇酸)、聚对苯二甲酸丁二醇酯、聚(己内酯)、聚(碳酸酯)、聚(氰基丙烯酸酯)、聚(二甲基丙烯酰胺)、聚(酯)、聚(乙烯)、聚(乙二醇)、聚(环氧乙烷)、聚(磷酸乙酯)、聚(乙基噁唑啉)、聚(乙醇酸)、聚(丙烯酸羟乙酯)、聚(羟乙基-噁唑啉)、聚(羟甲基丙烯酸酯)、聚(羟丙基甲基丙烯酰胺)、聚(甲基丙烯酸羟丙酯)、聚(羟丙基噁唑啉)、聚(亚氨基碳酸酯)、聚(乳酸)、聚(乳酸-共-乙醇酸)、聚(甲基丙烯酰胺)、聚(甲基丙烯酸酯)、聚(甲基噁唑啉)、聚(有机磷腈)、聚(原酸酯)、聚(噁唑啉)、聚(丙二醇)、聚(硅氧烷)、聚(氨基甲酸酯)、聚(乙烯醇)、聚(乙烯胺)、聚(乙烯基甲基醚)、聚(乙烯基吡咯烷酮)、硅酮、纤维素、羧甲基纤维素、羟丙基甲基纤维素、甲壳质、脱乙酰壳多糖、葡聚糖、糊精、明胶、透明质酸和衍生物、官能化透明质酸、甘露聚糖、果胶、鼠李糖半乳糖醛酸聚糖、淀粉、羟烷基淀粉、羟乙基淀粉和其它基于碳水化合物的聚合物、木聚糖及其共聚物。
[0943]更优选地,式(a)的-pa’、-pa”和-pa”’
独立地包含基于peg的部分。
甚至更优选地,式(a)的-pa’、-pa”和-pa”’
独立地包含基于peg的部分,其包含至少
20
%peg、甚至更优选至少
30
%、甚至更优选至少
40
% peg、甚至更优选至少
50
%peg、甚至更优选至少
60
% peg、甚至
更优选至少
70
% peg、甚至更优选至少
80
% peg且最优选至少
90
% peg。
[0944]优选地,式(a)的-pa’、-pa”和-pa”’
独立地具有
5kda-50kda且包括
5kda和
50kda的分子量,更优选具有
5kda-40kda且包括
5kda和
40kda的分子量,甚至更优选
7.5kda-35kda且包括
7.5kda和
35kda的分子量,甚至更优选
7.5kda-30kda且包括
7.5kda和
30kda的分子量,甚至更优选
10kda-30kda且包括
10kda和
30kda的分子量。
[0945]在一个实施方案中,式(a)的-pa’、-pa”和-pa”’
具有约
5kda的分子量
[0946]在另一个实施方案中,式(a)的-pa’、-pa”和-pa”’
具有约
7.5kda的分子量。
[0947]在另一个实施方案中,式(a)的-pa’、-pa”和-pa”’
具有约
10kda的分子量。
[0948]在另一个实施方案中,式(a)的-pa’、-pa”和-pa”’
具有约
12.5kda的分子量。
[0949]在另一个实施方案中,式(a)的-pa’、-pa”和-pa”’
具有约
15kda的分子量。
[0950]在另一个实施方案中,式(a)的-pa’、-pa”和-pa”’
具有约
20kda的分子量。
[0951]在一个实施方案中,-z包含一个式(a)的部分。
[0952]在另一个实施方案中,-z包含两个式(a)的部分。
[0953]在另一个实施方案中,-z包含三个式(a)的部分。
[0954]优选地,-z是式(a)的部分。
[0955]更优选地,-z包含式(b)的部分
[0956][0957]其中
[0958]虚线表示连接至-l
2-或连接至-z的其余部分;且
[0959]m和p彼此独立地为
150-1000
且包括
150
和
1000
的整数;优选地,
150-500
且包括
150
和
500
的整数;更优选地,
200-500
且包括
200
和
500
的整数;且最优选地,
400-500
且包括
400
和
500
的整数。
[0960]优选地,式(b)的m和p是相同的整数。
[0961]最优选地,式(b)的m和p为约
450。
[0962]优选地,-z是式(b)的部分。
[0963]载体-z’是水不溶性聚合物,甚至更优选水凝胶。
优选地,这类水凝胶包含聚合物,其选自
2-甲基丙烯酰基-氧基乙基磷酰胆碱、聚(丙烯酸)、聚(丙烯酸酯)、聚(丙烯酰胺)、聚(烷氧基)聚合物、聚(酰胺)、聚(酰氨基胺)、聚(氨基酸)、聚(酸酐)、聚(天冬酰胺)、聚(丁酸)、聚(乙醇酸)、聚对苯二甲酸丁二醇酯、聚(己内酯)、聚(碳酸酯)、聚(氰基丙烯酸酯)、聚(二甲基丙烯酰胺)、聚(酯)、聚(乙烯)、聚(乙二醇)、聚(环氧乙烷)、聚(磷酸乙酯)、聚(乙基噁唑啉)、聚(乙醇酸)、聚(丙烯酸羟乙酯)、聚(羟乙基-噁唑啉)、聚(羟甲基丙烯酸酯)、聚(羟丙基甲基丙烯酰胺)、聚(甲基丙烯酸羟丙酯)、聚(羟丙基噁唑啉)、聚(亚氨基碳酸酯)、聚(乳酸)、聚(乳酸-共-乙醇酸)、聚(甲基丙烯酰胺)、聚(甲基丙烯酸酯)、聚(甲基噁唑啉)、聚(有机磷腈)、聚(原酸酯)、聚(噁唑啉)、聚(丙二醇)、聚(硅氧烷)、聚(氨基甲酸酯)、聚(乙烯醇)、聚(乙烯胺)、聚(乙烯基甲基醚)、聚(乙烯基吡咯烷酮)、硅酮、纤维素、羧甲基纤维
素、羟丙基甲基纤维素、甲壳质、脱乙酰壳多糖、葡聚糖、糊精、明胶、透明质酸和衍生物、官能化透明质酸、甘露聚糖、果胶、鼠李糖半乳糖醛酸聚糖、淀粉、羟烷基淀粉、羟乙基淀粉和其它基于碳水化合物的聚合物、木聚糖及其共聚物。
[0964]如果载体-z’是水凝胶,则它优选地为包含peg或透明质酸的水凝胶。
最优选地,这类水凝胶包含peg。
[0965]甚至更优选地,载体-z’是如wo 2006/003014 a2、wo 2011/012715 a1或wo 2014/056926a1中所述的水凝胶,这些文献作为引用整体并入本文。
[0966]在另一个实施方案中,-z'
是通过聚合物链的物理聚集形成的聚合物网状结构,所述物理聚集优选通过氢键、结晶、螺旋形成或配合导致。
在一个实施方案中,这类聚合物网状结构是热胶凝聚合物。
[0967]如果本发明的控释pth化合物是前药,则它的总质量优选地为至少
10kda,例如至少
12kda,例如至少
15kda,例如至少
20kda或例如至少
30kda。
如果控释pth化合物是水溶性前药,则它的总质量优选地为至多
250kda,例如至多
200kda、180kda、150kda或
100kda。
应当理解,在控释pth化合物是水不溶性的情况中,不能提供有意义的分子量上限。
[0968]在一个优选的实施方案中,控释pth化合物具有式(iie-i):
[0969][0970]其中
[0971]无标记的虚线表示通过形成酰胺键连接至为pth部分的-d的氮;且
[0972]用星号标记的虚线表示连接至部分
[0973][0974]其中m和p独立地是从
400
到
500
且包括
400
和
500
的整数。
[0975]优选地,-d通过pth部分的n-末端胺官能团连接至式(iie-i)的pth前药。
[0976]在另一个优选的实施方案中,本发明的pth前药具有式(iif-i):
[0977][0978]其中
[0979]无标记的虚线表示通过形成酰胺键连接至为pth部分的-d的氮;且
[0980]用星号标记的虚线表示连接至部分
[0981][0982]其中m和p独立地是从
400
到
500
且包括
400
和
500
的整数。
[0983]优选地,-d通过pth部分的n-末端胺官能团连接至式(iif-i)的pth前药。
[0984]在一个优选的实施方案中,pth前药形式的控释pth的残余活性低于
10%
,
更优选地,低于1%,甚至更优选地,低于
0.1%,甚至更优选地,低于
0.01%,甚至更优选地,低于
0.001%,且最优选地,低于
0.0001%。
[0985]如本文所用,术语“残余活性”是指本发明其中pth部分结合于载体的pth前药相对于相应的游离pth显示的活性。
在本文中,术语“活性”是指结合pth/pthrp1受体的活化结构域,导致腺苷酸环化酶活化以产生camp,磷脂酶c产生细胞内钙,或rankl
的成骨细胞表达(其与破骨细胞上rank(核因子kb受体活化剂)结合)。
可以理解,测定本发明的pth前药的残余活性需要一段时间,在此期间一定量的pth可能从本发明的pth前药释放,并且这种释放的pth将曲解对pth前药测定的结果。
因此,可以接受的做法是用缀合物测试前药的残余活性,其中药物部分,在这种情况下是pth,不可逆地即稳定地与载体结合,尽可能接近要测定残余活性的pth前药的结构。
[0986]优选地,本发明的药物组合物具有从ph 3到ph 8且包括ph 3和ph 8的ph。
更优选地,该药物组合物具有从ph 4到ph 6且包括ph 4和ph 6的ph。
最优选地,该药物组合物具有从ph 4到ph 5且包括ph 4和ph 5的ph。
[0987]在一个实施方案中,本发明的药物组合物是液体或混悬液制剂。
应当理解,如果本发明的控释pth化合物是水不溶性的,则该药物组合物是混悬液制剂。
[0988]在另一个实施方案中,本发明的药物组合物是在施用于患者前重构的干制剂。
[0989]这类液体、悬浮液、干或重构药物组合物包含至少一种赋形剂。
肠胃外制剂中使用的赋形剂可以分类为例如缓冲剂、等渗调节剂、防腐剂、稳定剂、抗吸附剂、氧化保护剂、增粘剂/粘度增强剂或其它助剂。
然而,在一些情况下,一种赋形剂可具有双重或三重功能。
优选地,包含在本发明药物组合物中的至少一种赋形剂选自:
[0990](i)缓冲剂:生理上耐受的缓冲液,以保持ph在所需范围内,例如磷酸钠、碳酸氢盐、琥珀酸盐、组氨酸、柠檬酸盐和乙酸盐、硫酸盐、硝酸盐、氯化物、丙酮酸盐;也可使用抗酸剂例如mg(oh)2或znco3;
[0991](ii)等渗调节剂:为了最小化因注射储库渗透压差引起的细胞损伤导致的疼痛;甘油和氯化钠是实例;有效浓度可以通过使用血清的推定渗透压
285-315mosmol/kg的渗透压测定法测定;
[0992](iii)防腐剂和/或抗微生物剂:多剂量胃肠外制剂需要添加足够浓度的防腐剂,以最小化患者注射后感染的风险,并已建立相应的法规要求;典型的防腐剂包括间甲酚、苯酚、对羟基苯甲酸甲酯、对羟基苯甲酸乙酯、对羟基苯甲酸丙酯、对羟基苯甲酸丁酯、三氯叔丁醇、苄醇、硝酸苯汞、硫柳汞、山梨酸、山梨酸钾、苯甲酸、氯甲酚和苯扎氯铵;
[0993](iv)稳定剂:通过增强蛋白质稳定力、通过变性状态的去稳定或通过赋形剂与蛋白质的直接结合来实现稳定化;稳定剂可以是氨基酸,例如丙氨酸、精氨酸、天冬氨酸、甘氨酸、组氨酸、赖氨酸、脯氨酸;糖,例如葡萄糖、蔗糖、海藻糖;多元醇,例如甘油、甘露糖醇、山梨醇;盐,例如磷酸钾、硫酸钠;螯合剂,例如edta、六磷酸盐;配体,例如二价金属离子(锌、钙等),其它盐类或有机分子,例如酚类衍生物;此外,可以使用寡聚体或聚合物,例如环糊精、葡聚糖、树枝状大分子(dendrimer)、peg或pvp或鱼精蛋白或hsa;
[0994](v)抗吸附剂:主要使用离子或非离子表面活性剂或其它蛋白质或可溶性聚合物来竞争性地涂覆或吸附到制剂容器的内表面;例如泊洛沙姆(pluronic f-68)、peg十二烷基醚(brij 35)、聚山梨醇酯
20
和
80、葡聚糖、聚乙二醇、peg-聚组氨酸、bsa和hsa和明胶;选择的赋形剂浓度和类型取决于要避免的效果,但典型地恰好在cmc值以上在界面处形成表面活性剂单层;
[0995](vi)氧化保护剂:抗氧化剂如抗坏血酸、ectoine、甲硫氨酸、谷胱甘肽、硫代甘油、桑色素(morin)、聚乙烯亚胺(pei)、没食子酸丙酯和维生素e;也可使用螯合剂如柠檬酸、edta、六磷酸盐和巯基乙酸(thioglycolic acid);
[0996](vii)增粘剂/粘度增强剂:在悬浮液的情况下,延迟颗粒在小瓶和注射器中的沉降并且用于促进颗粒的混合和再悬浮并使悬浮液更容易注射(即注射器柱塞上的力小);合适的增粘剂或粘度增强剂是例如卡波姆增粘剂如卡波姆
940、carbopol ultrez 10,纤维素衍生物如羟丙基甲酰基纤维素(羟丙甲纤维素,hpmc)或二乙基氨基乙基纤维素(deae或deae-c),胶体硅酸镁(veegum)或硅酸钠;羟基磷灰石凝胶、磷酸三钙凝胶、黄原胶、角叉菜胶如satia gum utc 30
;脂肪族聚(羟基酸),例如聚(d、l-或
l-乳酸)(pla)和聚(乙醇酸)(pga)和它们的共聚物(plga);d,l-丙交酯、乙交酯和己内酯的三元共聚物;泊洛沙姆;亲水性聚(氧乙烯)嵌段和疏水性聚(氧丙烯)嵌段构成聚(氧乙烯)-聚(氧丙烯)-聚(氧乙烯)的三嵌段(例如);聚醚酯共聚物,例如聚对苯二甲酸乙二醇酯/聚对苯二甲酸丁二醇酯共聚物、蔗糖乙酸异丁酸酯(sucrose acetate isobutyrate/saib)、葡聚糖或其衍生物、葡聚糖和peg的组合;聚二甲基硅氧烷;胶原;脱乙酰壳聚糖;聚乙烯醇(pva)和衍生物;聚烷基酰亚胺(polyalkylimides);聚(丙烯酰胺-共-二烯丙基二甲基铵(dadma));聚乙烯吡咯烷酮(pvp);葡糖氨基聚糖(gag),例如硫酸皮肤素、硫酸软骨素、硫酸角质素、肝素、硫酸乙酰肝素、透明质酸(hyaluronan);由疏水性a-嵌段如聚丙交酯(pla)或聚(丙交酯-共-乙交酯)(plga)和亲水性b-嵌段如聚乙二醇(peg)或聚乙烯吡咯烷酮组成的aba三嵌段或ab嵌段共聚物;此类嵌段共聚物以及上述泊洛沙姆可能表现出反向热凝胶化行为(室温的流体状态以促进施用,且注射后体温下高于溶胶-凝胶转变温度的凝胶状态);
[0997](viii)播散剂或扩散剂:通过间隙中胞外基质中的成分水解来改变结缔组织的通透性,例如但不限于透明质酸,一种在结缔组织的细胞间隙中发现的多糖;扩散剂例如但不限于透明质酸酶,暂时降低胞外基质的粘度并促进注射药物的扩散;和
[0998](ix)其它助剂:例如润湿剂、粘度调节剂、抗生素、透明质酸酶;酸和碱,例如盐酸和氢氧化钠是制备过程中ph调节所必需的助剂。
[0999]本发明的另一方面是在哺乳动物患者、优选人患者中治疗、控制、延迟或预防可用pth治疗、控制、延迟或预防的一种或多种病症的方法,包含下列步骤:施用包含至少一种控释pth化合物的药物组合物,每
24小时1次,其剂量为在
24小时期限内不超过
70
%的维持血xbridgetm beh300 prep c18 10μm,150x30mm,流速
40ml/min。
使用溶剂系统a(包含
0.1%tfav/v的水)和溶剂系统b(包含
0.1%tfav/v的乙腈)的线性梯度。
收集包含产物的hplc级分并冻干,另有描述除外。
[1014]快速色谱法:
[1015]使用来自biotage ab,sweden的isolera one系统,应用biotage kp-sil
硅胶柱和正庚烷和乙酸乙酯作为洗脱液,进行快速色谱纯化。
在
254nm检测产物。
离子交换色谱法:
[1016]使用配备macrocap sp阳离子交换柱的amersham bioscience aektabasic系统(amersham bioscience/ge healthcare)进行离子交换色谱(iex)。17mm乙酸ph4.5(溶剂a)和
17mm乙酸、1m nacl,ph4.5(溶剂b)用作流动相。
[1017]尺寸排阻色谱法:
[1018]使用配备hiprep 26/10脱盐柱的amersham bioscience aektabasic系统(amersham bioscience/ge healthcare)进行尺寸排阻色谱(sec)。0.1%(v/v)乙酸用作流动相。
[1019]分析方法
[1020]用waters acquity系统进行分析型超性能
lc(uplc)-ms,该系统配备waters beh300 c18柱(2.1x50mm,1.7μm粒径
,
流速:
0.25ml/min;溶剂a:包含
0.04%tfa(v/v)的水,溶剂b:包含
0.05%tfa(v/v)的乙腈),其偶联至来自thermo scientific的
ltq orbitrap discovery质谱仪或偶联至waters micromass zq。
[1021]血浆总pth(1-34)浓度的定量:
[1022]血浆总pth(1-34)浓度如下测定:通过在血浆蛋白沉淀后、继之以用内切蛋白酶
lys-c(来源:
lysobacter enzymogenes)和内切蛋白酶glu-c(来源:金黄色葡萄球菌(staphylococcus aureus)v8)连续消化上清液,来定量接近于n末端的标记肽(序列:iqlmhnlgk)和c末端标记肽(序列:
lqdvhnf)的标记肽。
随后,进行反相液相色谱进行分析并且通过质谱进行(rp-hplc-ms)检测。
[1023]制备空白肝素或edta血浆中pth(1-34)缀合物的校准标准品,浓度范围为1至
1000ng/ml pth(1-34)eq(用大鼠血浆稀释)和1至
1000ng/ml pth(1-34)eq(用猴血浆稀释)。
[1024]这些溶液用于产生校准曲线。
为了质量控制,相应地制备了三个独立于校准标准溶液的样品。
下端的浓度(相应
lloq的
3-5倍浓度)、中间范围(相应uloq浓度的
0.05-0.1倍)和上端(相应uloq的浓度为
0.5-0.8倍)。
[1025]根据样品制备后的目标信号响应的不同,可以改变样品制备体积。
本文描述了蛋白质沉淀的处理方法,用于分析源自大鼠物种的血浆样品。
首先通过向
50
μl血浆样品中添加
100
μl内标溶液(625ng/ml
氘代缀合物),然后添加
400
μl乙腈,来进行蛋白质沉淀。
将2次
150
μl上清液转移到新的孔板中并蒸发至干(在温和的氮气流中,在
50℃)。
使用
50
μl重构溶剂(50mm tris 0.5mm cacl2缓冲液,调节至ph 8.0)溶解残余物。
蛋白水解消化如下进行:
[1026]将
20
μg lys-c(序号
125-05061,wako chemicals gmbh,neuss,germany)溶解在
80
μ
l 10mm乙酸中。
将3μ
l lys-c溶液加入每个空腔中,并将样品在
37℃
温育
15小时。
然后将
10μg clu-c(序号v1651,promega gmbh,mannheim,germany)溶解在
25μl水中,并将
1.5μ
l glu-c溶液加入每个空腔中,在
37℃
继续温育
1.5小时。
温育后,将样品用2μl水/甲酸
4:6(v/v)酸化,并将
10μl注入uplc-ms系统。
[1027]在waters acquity beh300 c18分析柱(1.7μm粒径;柱尺寸
50
×
2.1mm)上进行色谱。
含有
0.1%甲酸(v/v)的水(uplc级)用作流动相a,含有
0.1%甲酸的乙腈(uplc级)作为流动相b。
[1028]以多次反应监测(mrm)模式用ab sciex 6500+qtrap进行质量分析,监测转换m/z 352.0
至
462.1(标记肽iqlmhnlgk),
355.4至
467.1(标记肽iqlmhnlgk,内标),
436.9至
631.4(标记肽
lqdvhnf)和
441.9至
631.4(标记肽
lqdvhnf,内标)。
[1029]血浆peg浓度的定量:
[1030]通过在血浆蛋白沉淀和酶消化上清液后定量pth(1-34)缀合物的聚合部分来测定血浆总peg浓度。
接下来通过尺寸排阻色谱法和质谱检测(sec-ms)进行分析。
[1031]空白肝素化猴血浆中pth(1-34)缀合物的校准标准品,浓度范围为
50
至
4500ng/ml peg当量。
[1032]这些溶液用于产生二次校准曲线。
校准曲线加权
1/x。
为了质量控制,相应地制备了三个独立于校准标准溶液的样品。
下端浓度(lloq浓度
2-4倍),中间浓度(uloq浓度
0.1-0.2倍)和上端浓度(uloq浓度
0.8倍)。
通过向
100
μl血浆样品中加入
200
μl预冷(5-10℃)甲醇进行蛋白质沉淀。
将
180
μl上清液转移到新的孔板中并蒸发至干(在温和的氮气流中,在
45℃)。
使用
50
μl重构溶剂(50mm tris 0.5mm cacl2缓冲液,调节至ph 8.0)溶解残余物。
蛋白水解消化如下进行:将
20
μg lys-c(序号
125-05061,wako chemicals gmbh,neuss,germany)溶解在
80
μ
l 10mm乙酸中。
将3μ
l lys-c溶液加入每个空腔中,并将样品在
37℃
温育
15小时。
然后将
10μg clu-c(序号v1651,promega gmbh,mannheim,germany)溶解在
25μl水中,并将
1.5μ
l glu-c溶液加入每个空腔中并在
37℃
继续温育
1.5小时。
温育后,将样品用2μl水/甲酸
4:6(v/v)酸化,并将5μl注入sec-ms系统。
[1033]通过使用经esi探头与agilent 6460triplequad质谱仪偶联的agilent 1290uplc进行sec-ms分析。
通过在ms界面上施加高压源内碎片化(200-300v)来获得聚合物的不同前体离子。
色谱法在tosoh tsk gel superaw3000
分析柱(4.0
μm粒径;柱尺寸
150
×
6.0mm)上以
0.50ml/min(t=
65℃)的流速进行。
含有
0.1%甲酸(v/v)的水(uplc级)用作流动相a和含
0.1%甲酸的乙腈(uplc级)作为流动相b。
样品分析的色谱设置包含
50
%的等度洗脱b,历时8分钟。
[1034]以单一反应监测(srm)模式进行质量分析,监测m/z 133.1至
45.1的跃迁。
血浆游离pth浓度的定量:
[1035]将酸化血浆中的游离pth浓度确定为血浆蛋白沉淀后肽pth(1-34)和肽pth(1-33)的总和,然后进行固相萃取。
随后,进行使用液相色谱分离和质谱检测(lc-ms)的分析。
[1036]制备空白酸化edta大鼠血浆中pth(1-34)和pth(1-33)的校准标准品,对于每种分析物,浓度范围为
5.00
至
500pg/ml
的酸化血浆。
对于纯净血浆中的两种分析物,相应的浓度范围为
7.00
至
700pg/ml,因为血浆以血浆
:0.5m柠檬酸盐缓冲液ph4=
1:0.4v/v的体积比被酸化。
[1037]标准溶液用于产生校准曲线。
为了质量控制,在酸化的血浆中以
15.0、150
和
400pg/ml
的浓度制备独立于校准标准溶液的三个样品。
[1038]蛋白沉淀如下进行:加入
50.0
μl冷的内标溶液后,向
150
μl血浆样品中加入
150
μl冷乙腈,然后离心。
将上清液滗析入新的聚丙烯管中,加入
900
μl冷水。
在另一个离心步骤之后,将管保持在冰水中直至加载到spe柱上。
[1039]固相萃取:将hlbμ
洗脱柱用
200
μl甲醇、然后用
200
μl水调节。
通过施加正压将柱加载
420
μl稀释样品3次。
用
200
μl甲醇
:
水
5:95v/v洗涤spe柱。
用
40.0
μ
l spe洗脱溶剂(乙腈
:
水
:
三氟乙酸
60:40:1v/v/v)洗脱样品,然后用
40.0
μl水洗脱。
将洗脱溶剂在柱上静置2分钟,然后施加非常温和的压力进行洗脱。
[1040]通过
lc-ms、使用xselect csh c18柱(2.1x100mm,
2.5μm)在
50℃
和使用
0.2%甲酸和
0.5%二甲基亚砜水溶液作为流动相a、0.5%二甲亚砜在乙腈
:
甲醇(75:25,v/v)中作为流动相b并以
0.500ml/min的流速梯度操作,进行代谢物与干扰内源性化合物之间的分离。
[1041]配备涡轮离子喷雾源的三重
6500
四极质谱仪用于正离子模式的检测。
对于pth(1-34)、pth(1-33)和pth(1-33)(leu-d10)3,通过计数5次相同srm跃迁进行定量。
[1042]定量基于m/z跃迁的多次反应监测(mrm):
[1043]687.3-787.3:pth(1-34)[1044]662.8-757.9:pth(1-33)[1045]692.3-793.3:pth(1-34)(leu-d10)3[1046]667.8-763.9:pth(1-33)(leu-d10)3[1047]两种分析物均使用具有
1/x2加权因子的线性校准曲线。
[1048]在酸化的血浆中测定游离pth的浓度,作为稳定分析物的方式。
通过将大鼠edta血浆稀释
1.4倍(在空白、零、校准和qc样品的情况下)或大鼠全血(在研究样品的情况下)稀释
1.2倍来制备酸化血浆。
推定大约
50
%(v/v)的全血是血浆,则净血浆浓度比酸化血浆中报告的浓度高约
1.4倍。
将游离pth浓度计算为pth(1-34)等价物中的游离pth(1-34)和游离pth(1-33)的总和。
[1049]由于-l
1-连接至-d的可逆性质,使用本发明pth前药的稳定类似物进行pth受体活性的测量,即它们使用与本发明pth前药类似的结构制备,但不像-z可逆连接至-d而具有稳定的连接。
[1050]这是必要的,因为本发明的pth前药在实验过程中会释放pth,并且所释放的pth会影响结果。
[1051]实施例1[1052]连接基试剂
1f的合成
[1053]连接基试剂
1f根据如下方案合成:
[1054][1055][1056]向n-甲基-n-boc-乙二胺(2g,11.48mmol)和nacnbh3(819mg,12.63mmol)在meoh(20ml)中的溶液中逐步加入
2,4,6-三甲氧基苯甲醛(2.08g,10.61mmol)。
将该混合物在rt搅拌
90min,用
3m hcl(4ml)酸化,再搅拌
15min。
将该反应混合物加入到饱和nahco3溶液(200ml)中,用dcm萃取
5x。
用na2so4干燥合并的有机相,真空蒸发溶剂。
高真空干燥得到的n-甲基-n-boc-n’‑tmob-乙二胺
1a,不经进一步纯化用于下一步反应。
[1057]收率:
3.76g(11.48mmol,89%纯度
,1a:
双tmob保护的产物=
8:1)[1058]ms:m/z 355.22=
[m+h]+
,(单同位素质量计算值=
354.21)[1059]向
1a(2g,5.65mmol)在dcm(24ml)中的溶液中加入comu(4.84g,11.3mmol)、n-fmoc-n-me-asp(obn)-oh(2.08g,4.52mmol)和
2,4,6-可力丁(2.65ml,20.34mmol)。
将该反应混合物在rt搅拌
3h,用dcm(250ml)稀释,用
0.1m h2so4(100ml)洗涤
3x,用盐水(100ml)洗涤
3x。
用dcm(100ml)再萃取水相。
用na2so4干燥合并的有机相,过滤,将残余物浓缩至
24ml
体积。
使用快速色谱法纯化
1b。
[1060]收率:
5.31g(148%
,6.66mmol)[1061]ms:m/z 796.38=
[m+h]+
,(单同位素质量计算值=
795.37)[1062]向
1b(5.31g,
最大
4.52mmol
参考n-fmoc-n-me-asp(obn)-oh)在thf(60ml)中的溶液中加入dbu(1.8ml,3%v/v)。
将该溶液在rt搅拌
12min,用dcm(400ml)稀释,用
0.1m h2so4(150ml)洗涤
3x,用盐水(150ml)洗涤
3x。
用dcm(100ml)再萃取水相。
用na2so4干燥合并的有机相,过滤。
蒸发溶剂后分离
1c,不经进一步纯化用于下一步反应。
[1063]ms:m/z 574.31=
[m+h]+
,(单同位素质量计算值=
573.30)[1064]将
1c(5.31g,4.52mmol,
粗)溶于乙腈(26ml),加入comu(3.87g,9.04mmol)、6-三苯甲基巯基己酸(2.12g,5.42mmol)和
2,4,6-可力丁(2.35ml,18.08mmol)。
将该反应混合物在rt搅拌
4h,用dcm(400ml)稀释,用
0.1mh2so4(100ml)洗涤
3x,用盐水(100ml)洗涤
3x。
用dcm(100ml)再萃取水相。
用na2so4干燥合并的有机相,过滤,蒸发溶剂后分离
1d。
使用快速色谱法纯化产物
1d。
[1065]收率:
2.63g(62%
,94%纯度)[1066]ms:m/z 856.41=
[m+h]+
,(单同位素质量计算值=
855.41)[1067]向
1d(2.63g,2.78mmol)在i-proh(33ml)和h2o(11ml)中的溶液中加入
lioh(267mg,11.12mmol),将该反应混合物在rt搅拌
70min。
用dcm(200ml)稀释该混合物,用
0.1m h2so4(50ml)洗涤
3x,用盐水(50ml)洗涤
3x。
用dcm(100ml)再萃取水相。
用na2so4干燥合并的有机相,过滤,蒸发溶剂后分离
1e。
使用快速色谱法纯化产物
1e。
[1068]收率:
2.1g(88%)[1069]ms:m/z 878.4=
[m+na]+
,(单同位素质量计算值=
837.40)[1070]向
1e(170mg,0.198mmol)在无水dcm(4ml)中的溶液中加入dcc(123mg,0.59mmol)和催化量的dmap。5min后,加入n-羟基-琥珀酰亚胺(114mg,0.99mmol),将该反应混合物在rt搅拌
1h。
过滤该反应混合物,真空除去溶剂,将残余物溶于
90
%乙腈
+0.1%tfa(3.4ml)。
通过rp-hplc纯化粗混合物。
用
0.5m ph7.4磷酸盐缓冲液中和产物级分,浓缩。
用dcm萃取剩余的水相,蒸发溶剂后分离
1f。
[1071]收率:
154mg(81%)[1072]ms:m/z 953.4=
[m+h]+
,(单同位素质量计算值=
952.43)[1073]实施例2[1074]连接基试剂
2g的合成
[1075][1076][1077]将
4-甲氧基三苯基甲基氯(3.00g,9.71mmol)溶于dcm(20ml),在搅拌下滴加到乙二胺
2a(6.5ml,97.3mmol)在dcm(20ml)中的溶液中。
将该反应混合物在rt搅拌
2h,此后,用乙醚(300ml)稀释,用盐水
/0.1m naoh 30/1(v/v)洗涤
3x,用盐水洗涤1次。
用na2so4干燥有机相,蒸发溶剂后分离
2b。
[1078]收率:
3.18g(98%)[1079]将mmt保护的中间体
2b(3.18g,9.56mmol)溶于dcm(30ml)。
加入
6-(三苯甲硫基)-己酸(4.48g,11.5mmol)、pybop(5.67g,10.9mmol)和dipea(5.0ml,28.6mmol),将该混合物在rt搅拌
30min。
用乙醚(250ml)稀释该溶液,用盐水
/0.1m naoh 30/1(v/v)洗涤
3x,用盐水洗涤1次。
用na2so4干燥有机相,真空除去溶剂。
使用快速色谱法纯化
2c。
[1080]收率:
5.69g(85%)[1081]ms:m/z 705.4=
[m+h]+
,(单同位素质量计算值=
704.34)[1082]将化合物
2c(3.19g,4.53mmol)溶于无水thf(50ml),加入
1mbh3·thf的thf溶液(8.5ml,8.5mmol),将该混合物在rt搅拌
16h。
再加入
1m bh3·thf的thf溶液(14ml,14.0mmol),将该混合物在rt再搅拌
16h,加入甲醇(8.5ml)和n,n′‑
二甲基-乙二胺(3.00ml,27.9mmol),将该混合物回流加热
3h。
将该混合物冷却,加入乙酸乙酯(300ml)。
用na2co3水溶
液洗涤该溶液
2x,用nahco3水溶液洗涤
2x。
用na2so4干燥有机相,真空除去溶剂,得到
2d。
[1083]收率:
3.22g(103%)[1084]ms:m/z 691.4=
[m+h]+
,(单同位素质量计算值=
690.36)[1085]将二碳酸二叔丁酯(2.32g,10.6mmol)和dipea(3.09ml,17.7mmol)溶于dcm(5ml),加入到
2d(2.45g,3.55mmol)在dcm(5ml)中的溶液中。
将该混合物在rt搅拌
30min。
真空浓缩该溶液,通过快速色谱法纯化,得到产物
2e。
[1086]收率:
2.09g(74%)[1087]ms:m/z 791.4=
[m+h]+
,(单同位素质量计算值=
790.42)[1088]将化合物
2e(5.01g,6.34mmol)溶于乙腈(80ml),加入
0.4m hcl
水溶液(80ml),然后加入乙腈(20ml),将该混合物在rt搅拌
1h。
通过添加
5m naoh水溶液将ph调整至ph5.5。
真空除去有机溶剂,用dcm将其余水溶液萃取
4x。
用na2so4干燥合并的有机相,真空除去溶剂,得到产物
2f。
[1089]收率:
4.77g(95%)[1090]ms:m/z 519.3=
[m+h]+
,(单同位素质量计算值=
518.30)[1091]将化合物
2f(5.27g,6.65mmol)溶于dcm(30ml),加入到氯甲酸对硝基苯酯(2.01g,9.98mmol)在dcm(25ml)中的溶液中。
加入
2,4,6-三甲基吡啶(4.38ml,33.3mmol),将该溶液在rt搅拌
45min。
真空浓缩该溶液,通过快速色谱法纯化,得到产物
2g。
[1092]收率:
4.04g(89%)[1093]ms:m/z 706.32=
[m+na]+
,(单同位素质量计算值=
683.30)[1094]实施例3[1095]永久性s1 pth(1-34)缀合物3的合成
[1096][1097]根据材料和方法中给定的方法,使具有fmoc保护的n-末端的tcp树脂上侧链保护的pth(1-34)进行fmoc脱保护。
将
6-三苯甲基巯基己酸(62.5mg,160
μmol)、pybop(80.1mg,154μmol)和dipea(53μ
l,306μmol)在dmf(2ml)中的溶液加入到
0.21g(51μmol)树脂中。
将该混悬液在rt搅拌
80min。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
通过添加
10ml
裂解合剂
100/3/3/2/1(v/w/v/v/v)tfa/dtt/tes/
水/茴香硫醚并且将该混悬液在rt搅拌
1h,从树脂上裂解肽并且除去保护基。
使粗产物3在预冷却的乙醚(-18℃)中沉淀。
将沉淀溶于acn/
水,通过rp-hplc纯化。
冷冻干燥产物级分。
[1098]收率:
36mg(14%),3*8tfa[1099]ms:m/z 1062.31=
[m+4h]4+
,(单同位素质量计算值
[m+4h]4+
=
1062.30)[1100]实施例4[1101]永久性k26 pth(1-34)缀合物4的合成
[1102][1103]根据材料和方法中给定的方法,使具有boc保护的n-末端和ivdde保护的
lys26侧链的tcp树脂上侧链保护的pth(1-34)进行ivdde脱保护。
将
6-三苯甲基巯基己酸(107mg,273μmol)、pybop(141mg,273μmol)和dipea(95μ
l,545μmol)在dmf(3ml)中的溶液加入到
0.80g(90.9μmol)树脂中。
将该混悬液在rt搅拌
1h。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
通过添加
6ml
裂解合剂
100/3/3/2/1(v/w/v/v/v)tfa/dtt/tes/
水/茴香硫醚并且将该混悬液在rt搅拌
1h,从树脂上裂解肽并且除去保护基。
使粗产物4在预冷却的乙醚(-18℃)中沉淀。
将沉淀溶于acn/
水,通过rp-hplc纯化。
冷冻干燥产物级分。
[1104]收率:
40mg(8%),4*8tfa[1105]ms:m/z 1062.30
=
[m+4h]4+
,(单同位素质量计算值
[m+4h]4+
=
1062.30)[1106]实施例5[1107]暂时性s1 pth(1-34)缀合物的合成
[1108][1109]根据材料和方法中给定的方法,使具有fmoc保护的n-末端的tcp树脂上侧链保护的pth(1-34)进行fmoc脱保护。
将fmoc-aib-oh(79mg,244μmol)、pybop(127mg,244μmol)和dipea(64μ
l,365μmol)在dmf(1.5ml)中的溶液加入到
0.60g(61μmol)树脂中。
将该混悬液在rt搅拌
16h。
用
10x dmf洗涤树脂,如上所述fmoc-脱保护。
将
2g(167mg,244μmol)和dipea(64μ
l,365μmol)在dmf(1.5ml)中的溶液加入到树脂中。
将该混悬液在rt搅拌
24h。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
通过添加
7ml
裂解合剂
100/3/3/2/1(v/w/v/v/v)tfa/dtt/tes/
水/茴香硫醚并且将该混悬液在rt搅拌
1h,从树脂上裂解肽并且除去保护基。
使粗产物5在预冷却的乙醚(-18℃)中沉淀。
将沉淀溶于acn/
水,通过rp-hplc纯化。
冷冻干燥产物级分。
[1110]收率:
78mg(24%),5*9tfa[1111]ms:m/z 1101.59=
[m+4h]4+
,(单同位素质量计算值
[m+4h]4+
=
1101.57)[1112]实施例6[1113]暂时性s1 pth(1-34)缀合物6的合成
[1114][1115]根据材料和方法中给定的方法,使具有fmoc保护的n-末端的tcp树脂上侧链保护的pth(1-34)进行fmoc脱保护。
将fmoc-ala-oh(32mg,102μmol)、pybop(53mg,102μmol)和dipea(27μ
l,152μmol)在dmf(3ml)中的溶液加入到
0.25g(25μmol)树脂中。
将该混悬液在rt振摇
1h。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
如上所述进行fmoc脱保护。
将
2g(69mg,102μmol)和dipea(27μ
l,152μmol)在dmf(3ml)中的溶液加入到树脂中。
将该混悬液在rt搅拌
1.5h。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
通过添加
3ml
裂解合剂
100/3/3/2/1(v/w/v/v/v)tfa/dtt/tes/
水/茴香硫醚并且将该混悬液在rt搅拌
1h从树脂上裂解肽并且除去保护基。
使粗产物6在预冷却的乙醚(-18℃)中沉淀。
将沉淀溶于acn/
水,通过rp-hplc纯化。
冷冻干燥产物级分。
[1116]收率:
25mg(18%),6*9tfa[1117]ms:m/z 1098.75=
[m+4h]4+
,(单同位素质量计算值
[m+4h]4+
=
1098.07)[1118]实施例7[1119]暂时性s1 pth(1-34)缀合物7的合成
[1120][1121]根据材料和方法中给定的方法,使具有fmoc保护的n-末端的tcp树脂上侧链保护的pth(1-34)进行fmoc脱保护。
将fmoc-ser(trt)-oh(117mg,205μmol)、pybop(108mg,207μmol)和dipea(53μ
l,305μmol)在dmf(2ml)中的溶液加入到
0.50g(51μmol)树脂中。
将该混悬液在rt搅拌
1h。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
如上所述进行fmoc脱保护。
将
2g(144mg,211μmol)和dipea(53μ
l,305μmol)在dmf(1.8ml)中的溶液加入到树脂中。
将该混悬液在rt振摇
7h。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
通过添加
6ml
裂解合剂
100/3/3/2/1(v/w/v/v/v)tfa/dtt/tes/
水/茴香硫醚并且将该混悬液在rt搅拌
1h,从树脂上裂解肽并且除去保护基。
使粗产物7在预冷却的乙醚(-18℃)中沉淀。
将沉淀溶于acn/
水,通过rp-hplc纯化。
冷冻干燥产物级分。
[1122]收率:
54mg(20
%),7*9tfa[1123]ms:m/z 1102.08=
[m+4h]4+
,(单同位素质量计算值
[m+4h]4+
=
1102.07)[1124]实施例8[1125]暂时性s1 pth(1-34)缀合物8的合成
[1126][1127]根据材料和方法中给定的方法,使具有fmoc保护的n-末端的tcp树脂上侧链保护的pth(1-34)进行fmoc脱保护。
将fmoc-leu-oh(36mg,102μmol)、pybop(53mg,102μmol)和dipea(27μ
l,152μmol)在dmf(3ml)中的溶液加入到
0.25g(25μmol)树脂中。
将该混悬液在rt搅拌
1h。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
如上所述进行fmoc脱保护。
将
2g(69mg,102μmol)和dipea(27μ
l,152μmol)在dmf(3ml)中的溶液加入到树脂中。
将该混悬液在rt搅
拌
1.5h。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
通过添加
3ml
裂解合剂
100/3/3/2/1(v/w/v/v/v)tfa/dtt/tes/
水/茴香硫醚并且将该混悬液在rt搅拌
1h,从树脂上裂解肽并且除去保护基。
使粗产物8在预冷却的乙醚(-18℃)中沉淀。
将沉淀溶于acn/
水,通过rp-hplc纯化。
冷冻干燥产物级分。
[1128]收率:
31mg(22%),8*9tfa[1129]ms:m/z 1109.32=
[m+4h]4+
,(单同位素质量计算值
[m+4h]4+
=
1108.58)[1130]实施例9[1131]暂时性s1 pth(1-34)缀合物9的合成
[1132][1133]根据材料和方法中给定的方法,使具有fmoc保护的n-末端的tcp树脂上侧链保护的pth(1-34)进行fmoc脱保护。
将
1e(182mg,213μmol)、pybop(111mg,213μmol)和dipea(93μ
l,532μmol)在dmf(5ml)中的溶液加入到
2.00g(107μmol)树脂中。
将该混悬液在rt振摇
16h。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
通过添加
20ml
裂解合剂
100/3/3/2/1(v/w/v/v/v)tfa/dtt/tes/
水/茴香硫醚并且将该混悬液在rt搅拌
1h,从树脂上裂解肽并且除去保护基。
使粗产物9在预冷却的乙醚(-18℃)中沉淀。
将沉淀溶于acn/
水,通过rp-hplc纯化。
冷冻干燥产物级分。
[1134]收率:
47mg(8%),9*9tfa[1135]ms:m/z 1108.58=
[m+4h]4+
,(单同位素质量计算值
[m+4h]4+
=
1108.57)[1136]实施例
10[1137]暂时性k26 pth(1-34)缀合物
10的合成
[1138][1139]根据材料和方法中给定的方法,使具有boc保护的n-末端和ivdde保护的
lys26侧链的tcp树脂上侧链保护的pth(1-34)进行ivdde脱保护。
将
1f(867mg,910μmol)和dipea(0.24ml,1.36mmol)在dmf(5ml)中的溶液加入到
1.91g(227μmol)树脂中。
将该混悬液在rt搅拌
1h。
用
10x dmf、10x dcm洗涤树脂,真空干燥。
通过添加
20ml
裂解合剂
100/3/3/2/1(v/w/v/v/v)tfa/dtt/tes/
水/茴香硫醚并且将该混悬液在rt搅拌
1h,从树脂上裂解肽并且除去保护基。
使粗产物
10在预冷却的乙醚(-18℃)中沉淀。
将沉淀溶于acn/
水,通过rp-hplc纯化。
冷冻干燥产物级分。
[1140]收率:
92mg(7%),10*9tfa[1141]ms:m/z 1108.58=
[m+4h]4+
,(单同位素质量计算值
[m+4h]4+
=
1108.57)[1142]实施例
11[1143]低分子量暂时性s1 peg缀合物
11b的合成
[1144][1145]将
0.15ml 0.5m nah2po4缓冲液(ph7.4)加入到
0.5ml 20mg/ml
硫醇
5(10mg,1.84μmol)在包含
0.1%tfa(v/v)的
1/1(v/v)乙腈/水中的溶液中。
将该溶液在rt温育
10min,此后,加入
238μ
l 10mg/ml
马来酰亚胺
11a(2.4mg,2.21μmol)在包含
0.1%tfa(v/v)的
1/1(v/v)乙腈/水中的溶液。
将该溶液在rt温育
20min。
加入
10μ
l tfa,通过rp-hplc纯化该混合物。
冷冻干燥产物级分,得到
11b。
收率:
3.1mg(26%),11b*9tfams:m/z 1097.00
=
[m+4h]4+
,(单
同位素质量计算值
[m+5h]5+
=
1096.99)[1146]实施例
12[1147]低分子量暂时性s1 peg缀合物
12的合成
[1148][1149]如对
11b所述,通过使用硫醇
6(10mg,1.85μmol)和马来酰亚胺
11a(2.4mg,2.21μmol)合成缀合物
12。
[1150]收率:
10mg(83%),12*9tfa[1151]ms:m/z 1094.20
=
[m+4h]4+
,(单同位素质量计算值
[m+4h]4+
=
1094.19)[1152]实施例
13[1153]低分子量暂时性s1 peg缀合物
13的合成
[1154][1155]如对
11b所述,通过使用硫醇
7(10mg,1.84μmol)和马来酰亚胺
11a(2.4mg,2.21μmol)合成缀合物
13。
[1156]收率:
8mg(67%),13*9tfa[1157]ms:m/z 1097.40
=
[m+5h]5+
,(单同位素质量计算值
[m+5h]5+
=
1097.39)[1158]实施例
14[1159]低分子量暂时性s1 peg缀合物
14的合成
[1160][1161]如对
11b所述,通过使用硫醇
8(10mg,1.83μmol)和马来酰亚胺
11a(2.4mg,2.21μmol)合成缀合物
14。
[1162]收率:
4mg(33%),14*9tfa[1163]ms:m/z 1378.01=
[m+4h]4+
,(单同位素质量计算值
[m+4h]4+
=
1378.00)[1164]实施例
15[1165]低分子量暂时性k26 peg缀合物
15的合成
[1166][1167]如对
11b所述,通过使用硫醇
10(5.2mg,0.95μmol)和马来酰亚胺
11a(1.23mg,1.14μmol)合成缀合物
15。
[1168]收率:
2.1mg(33%),15*9tfa[1169]ms:m/z 1102.60
=
[m+5h]5+
,(单同位素质量计算值
[m+5h]5+
=
1102.59)[1170]实施例
16[1171]永久性
2x20kda s1 peg缀合物
16的合成
[1172][1173]将
772μl在包含
0.1%tfa(v/v)的
1/1(v/v)乙腈/水中含有硫醇
3(19.4mg/ml,15mg,3.54μmol)和
2.5mg/ml boc-l-met的溶液加入到
1.87ml
溶液中,所述溶液在包含
0.1%tfa(v/v)的水中含有peg 2x20kda马来酰亚胺(sunbright gl2-400ma,187mg,4.32μmol)和
2.5mg/ml boc-l-met。
加入
0.5m nah2po4缓冲液(0.66ml,ph7.0)并将混合物在rt搅拌
30
分钟,加入
10μ
l 270mg/ml
的
2-巯基乙醇水溶液。
将混合物在rt搅拌5分钟并加入
0.33ml1m hcl。
通过iex、然后使用线性梯度的溶剂系统a(含有
0.1%acohv/v的水)和溶剂系统b(含有
0.1%acoh v/v的乙腈)的rp-hplc纯化缀合物
16。
将含有产物的级分冷冻干燥。
[1174]收率:
97mg(2.01μmol,57%)缀合物
16*8acoh[1175]实施例
17[1176]永久性
2x20kda k26 peg缀合物
17的合成
[1177][1178]如对
16所述,通过硫醇
4(15mg,3.53μmol)和peg 2x20kda马来酰亚胺(sunbright gl2-400ma,187mg,4.32μmol)反应,制备缀合物
17。
[1179]收率:
80mg(1.79μmol,51%)缀合物
17*8acoh[1180]实施例
18[1181]暂时性
2x20kda s1 peg缀合物
18的合成
[1182][1183]如对
16所述,通过硫醇
5(37mg,8.40
μmol)和peg 2x20kda马来酰亚胺(sunbright gl2-400ma,445mg,9.24μmol)反应,制备缀合物
18。
该反应通过添加
50
μ
l tfa淬灭,在先不添加
2-巯基乙醇。
通过iex、然后sec用于脱盐来纯化缀合物
18。
冷冻干燥包含产物的级分。
[1184]收率:
161mg(3.33μmol,40
%)缀合物
18*9acoh[1185]实施例
19[1186]暂时性
2x20kda s1 peg缀合物
19的合成
[1187][1188]如对
16所述,通过硫醇
7(27mg,6.14μmol)和peg 2x20kda马来酰亚胺(sunbright gl2-400ma,325mg,7.50
μmol)反应,制备缀合物
19。
[1189]收率:
249mg(5.16μmol,84%)缀合物
19*9acoh[1190]实施例
20
[1191]暂时性
2x20kda s1 peg缀合物
20
的合成
[1192][1193]如对
16所述,通过硫醇
9(38mg,8.59μmol)和peg 2x20kda马来酰亚胺(sunbright gl2-400ma,455mg,9.45μmol)反应,制备缀合物
20。
该反应通过添加
50
μ
l tfa淬灭,在先不添加
2-巯基乙醇。
通过iex、然后sec用于脱盐来纯化缀合物
20。
冷冻干燥包含产物的级分。
[1194]收率:
194mg(4.01μmol,47%)缀合物
20*9acoh[1195]实施例
21[1196]暂时性
2x20kda k26 peg缀合物
21的合成
[1197][1198]如对
16所述,通过硫醇
10(34mg,7.58μmol)和peg 2x20kda马来酰亚胺(sunbright gl2-400ma,401mg,9.26μmol)反应,制备缀合物
21。
[1199]收率:
256mg(5.30
μmol,70
%)缀合物
21*9acoh[1200]实施例
22[1201]暂时性低分子量peg缀合物的体外释放动力学
[1202]将缀合物
11b、12、13、14和
15溶于ph 7.4的磷酸盐缓冲液(60mm nah2po4,3mm edta,0.01% tween-20,
用naoh调整至ph 7.4),其中含有
0.05mg/ml
五氟苯酚作为内标,浓度约为
1mg缀合物
/ml。
将溶液无菌过滤并在
37℃
孵育。
在各时间点,取出等分试样并通过rp-hplc和esi-ms分析。
在特定时间点释放的pth的分数由释放的pth和peg缀合物的uv峰面积之比计算。
将释放的%pth对孵育时间作图。
应用曲线拟合软件计算相应的释放半衰期。
[1203]结果:
[1204]对于缀合物
11b,得到
3.2d的释放半衰期时间。
[1205]对于缀合物
12,得到
8.7d的释放半衰期时间。
[1206]对于缀合物
13,得到
10.8d的释放半衰期时间。
[1207]对于缀合物
14,得到
25.3d的释放半衰期时间。
[1208]对于缀合物
15,得到
6.9d的释放半衰期时间。
[1209]实施例
23[1210]暂时性
2x20kda peg缀合物的体外释放动力学
[1211]将缀合物
18、19、20
和
21溶解于ph 7.4的磷酸盐缓冲液(60mm nah2po4,3mm edta,0.01%tween-20,
用naoh调整至ph 7.4),其中含有
0.08mg/ml
五氟苯酚作为内标,浓度约为
5mg缀合物
/ml。
将溶液无菌过滤并在
37℃
孵育。
在各时间点,取出等分试样并通过rp-hplc分析。
在特定时间点释放的pth的分数由释放的pth和peg缀合物的uv峰面积之比计算。
将释放的%pth对孵育时间作图。
应用曲线拟合软件计算相应的释放半衰期。
[1212]结果:
[1213]对于缀合物
18,得到
2.8d的释放半衰期时间。
[1214]对于缀合物
19,得到
13.4d的释放半衰期时间。
[1215]对于缀合物
20,得到
1.3d的释放半衰期时间。
[1216]对于缀合物
21,得到
7.1d的释放半衰期时间。
[1217]实施例
24[1218]永久性
2x20kda peg缀合物
16和
17在基于细胞的试验中的pth受体活性
[1219]通过测量超表达pth/pthrp1受体的hek293细胞的camp产生,来量化永久性peg化的缀合物
16和
17的残余pth活性(hohenstein a,hebell m,zikry h,el ghazaly m,mueller f,rohde,j.development and validation of a novel cell-based assay for potency determination of human parathyroid hormone(pth),journal of pharmaceutical and biomedical analysis september 2014,98:345-350)。
来自nibsc(national institute for biological standards and control,uk)的pth(1-34)用作参比标准品。
[1220]结果:
[1221]对于缀合物
16,发现相对于pth(1-34)参比物的
0.12%的受体活性。
[1222]对于缀合物
17,发现相对于pth(1-34)参比物的
0.11%的受体活性。
[1223]结果表明:永久性
2x20kda peg缀合物
16和
17中受体活性的有效降低。
可以得出结论,具有暂时性ser1或
lys26连接的pth的类似缀合物(例如
18和
21)是适合的pth前药,提供低残留受体活性。
由于在测定条件下的连接基裂解,所以不可能在细胞测定中直接分析暂时性缀合物。
释放的pth会影响测定结果。
[1224]实施例
25[1225]永久性
2x20kda peg缀合物
16和
17在大鼠中的药代动力学研究
[1226]雄性wistar大鼠(6周,
230-260g)接受单次静脉内(2组,每组n=3只动物)或单次皮下(2组,每组n=3只动物)施用
16或
17,剂量分别为
29μg/
大鼠ptheq和
31μg/
大鼠ptheq。
在给药后直至
168小时收集血样,并产生血浆。
如材料和方法中所述,通过定量
lysc和gluc消化后的n-末端标记肽(序列:iqlmhnlgk)和c-末端标记肽(序列:
lqdvhnf)来确定血浆pth(1-34)浓度。
[1227]结果:剂量施用耐受良好,在施用期间和施用后没有明显的不适迹象。
在整个研究中的任何时间都没有观察到剂量部位反应。
在静脉内注射
16和
17后,在
15分钟(分析的最早时间点)观察到总pth(1-34)tmax,然后总pth(1-34)含量缓慢衰减,半衰期分别约为
13小时和
11小时。
在皮下注射后,对于
16和
17,总pth(1-34)浓度在
24小时tmax达到峰值,随后总pth(1-34)含量缓慢衰减,两种缀合物半衰期均约为
1.5天。
生物利用度分别约为
40
%和
60
%。
直到剂量后
168小时获得n-和c-末端标记肽的类似pk曲线,表明缀合物中存在完整的pth(1-34)。
[1228]有利的持久pk和缀合物中pth的稳定性表明,永久性2×
20kda peg模型化合物作为皮下注射后缓释pth前药的适合性。
可以得出结论,具有暂时性ser1(例如
18)或
lys26连接的pth的类似缀合物是适合的pth前药,其提供持久水平的释放的生物活性pth。
[1229]实施例
26[1230]暂时性
2x20kda s1 peg缀合物
19在食蟹猴中的药代动力学研究
[1231]雄性non-naive食蟹猴(2-4岁,
3.7-5.4kg)以
770
μg/kg ptheq的剂量接受
19的单次皮下(n=3只动物)施用。
在给药后至
504小时收集血样,并产生血浆。
如材料和方法中所述,通过定量
lysc和gluc消化后n-末端标记肽(序列:iqlmhnlgk)和c-末端标记肽(序列:
lqdvhnf)来确定总血浆pth(1-34)浓度。
使用材料和方法中描述的方法测定peg浓度。
[1232]结果:剂量施用耐受良好,施用期间没有明显的不适症状。
一只动物在给药后
72小时显示出可见不适症状,但在之后的几天恢复。
在整个研究中的任何时间都没有观察到剂量部位反应。
总pth(1-34)浓度在
24小时tmax达到峰值,随后总pth(1-34)含量缓慢衰减,对于n-末端标记肽半衰期为约
2.5d,对于c-末端标记肽为
0.9d。peg浓度在
24小时tmax达到峰值,然后peg浓度缓慢下降,半衰期为
3.5d。
[1233]可以得出结论,缀合物
19是用于持续递送pth的适合的前药。
[1234]实施例
27[1235]暂时性
2x20kda s1 peg缀合物
18在食蟹猴中的药代动力学研究
[1236]non naive食蟹猴(2-3岁,
2.5-4kg)以
0.2、0.5和1μg/kg ptheq的剂量水平接受
18的每日皮下(n=2只动物-1只雄性
/1只雌性)施用,持续
28天。
采集血样直至
28天(在第
1、13和
27天,于剂量前、剂量后
2h、4h、8h、12h和
24h收集样品),并产生血浆。
如材料和方法中所述,通过定量
lysc和gluc消化后n-末端标记肽(序列:iqlmhnlgk)和c-末端标记肽(序列:
lqdvhnf)来确定总血浆pth(1-34)浓度。
[1237]结果:所有剂量施用均无异常进行。
在整个研究中的任何时间都没有观察到剂量部位反应。
在三组中观察到剂量线性。
与第
13天和第
27天相比,从第1天开始观察剂量叠加(dose stacking)。
在稳态下(第
27天期间),通过n-末端标记肽(序列:iqlmhnlgk)定量总pth(1-34)浓度。
[1238]在食蟹猴的稳定状态下每日皮下施用后,观察到所有剂量组的总pth(1-34)的低于3的低峰-谷比。
由于稳态下的游离肽浓度与总pth(1-34)浓度相关,因此在食蟹猴中游离肽的峰-谷比低于
4。
[1239]实施例
28[1240]暂时性
2x20kda s1 peg缀合物
18在食蟹猴中的药代动力学研究
[1241]naive食蟹猴(2-3.5岁,
2-5kg)(3-5只雄性
/3-5只雌性)接受每天皮下施用
18,剂量水平为
0.2、0.5和
1.5μg pth/kg。
收集血样:第1天:剂量前、剂量后4小时、8小时、12小时、18小时和
24小时,第8天:剂量前;第
14天:剂量前,8小时和
12小时,在第
28天:3小时、6小时、8小时、12小时、18小时、24小时、72小时、168小时和
336小时)并且产生血浆。
如上述在材料和方法中所示,定量在
lysc和gluc消化后n-末端特征肽(序列:iqlmhnlgk),来确定总pth血浆浓度。
[1242]结果:表示为cmax和auc的全身暴露以近似剂量比例的方式增加。
从第1天至第
28天,表示为auc的总pth的全身暴露累积约3倍。
[1243]在第
28天在食蟹猴中每日皮下施用后,观察到所有剂量组的总pth的低平均峰-谷比
1.5(从第8天观察到稳态)。
这种总pth的低平均峰-谷比也可以被转化成游离pth。
[1244]实施例
29[1245]暂时性
2x20kdas1 peg缀合物
18在sprague-dawley大鼠中的药代动力学研究
[1246]sprague-dawley crl:cd(sd)大鼠(8周龄开始给药)接受每日皮下施用
18持续
28天,剂量水平
10、30
和
60
μg pth/kg。
每个剂量组含有9只雄性和9只雌性的tk组被分成3个亚组,每个亚组3只大鼠。
收集血样长达
28天,3只大鼠每个性别、每个采样时间点。
在第1天收集样品:剂量前,剂量后4小时、8小时、12小时、18小时和
24小时,以及第
28天:3小时、6小时、8小时、12小时、18小时、24小时和
336小时,并且产生血浆。
如上述材料和方法中所示,定量
lysc和gluc消化后n-末端特征肽(序列:iqlmhnlgk),来确定总pth血浆浓度。
[1247]如上述材料和方法中所呈现的,通过
lc-ms/ms定量游离pth血浆浓度,测定为pth(1-34)和pth(1-33)的总和。
[1248]结果:表示为平均cmax和auc的总pth和游离pth的全身暴露以近似剂量比例的方式增加。
表示为平均auc的总pth的全身暴露从第1天至第
28天累积
3-6倍,且表示为平均auc的游离pth从第1天到第
28天累积
2-3倍。
雌性大鼠中的总pth的全身暴露比雄性大鼠高约2倍。
游离pth的全身暴露在雄性中比在雌性中稍高。
[1249]在第
28天在sprague-dawley大鼠中每日皮下施用后,观察到所有剂量组的总pth的低平均峰-谷比
1.2(从第8天观察到稳态)。
在第
28天在sprague-dawley大鼠中每日皮下施用后,观察到
1.5-2.4范围的游离pth的低平均峰-谷比。
[1250]缩写:
[1251]acnꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
乙腈
[1252]acohꢀꢀꢀꢀꢀꢀꢀꢀꢀ
乙酸
[1253]aibꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
2-氨基异丁酸
[1254]bmdꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
骨矿物质密度
[1255]bnꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
苄基
[1256]bocꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
叔丁氧羰基
[1257]comuꢀꢀꢀꢀꢀꢀꢀꢀꢀ(1-氰基-2-乙氧基-2-氧代亚乙基氨基氧基)二甲基氨基-吗啉代-碳鎓六氟磷酸盐
[1258]campꢀꢀꢀꢀꢀꢀꢀꢀꢀ
环腺苷酸
[1259]dꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
天
[1260]dbuꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
1,3-二氮杂双环
[5.4.0]十一烯
[1261]dccꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀn,n’‑
二环己基碳二亚胺
[1262]dcmꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二氯甲烷
[1263]dipeaꢀꢀꢀꢀꢀꢀꢀꢀn,n-二异丙基乙胺
[1264]dmapꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二甲基氨基-吡啶
[1265]dmfꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀn,n-二甲基甲酰胺
[1266]dmsoꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二甲亚砜
[1267]dttꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
二硫苏糖醇
[1268]edtaꢀꢀꢀꢀꢀꢀꢀꢀꢀ
乙二胺四乙酸
[1269]eqꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
化学计算当量
[1270]esi-msꢀꢀꢀꢀꢀꢀꢀ
电喷雾电离质谱法
[1271]etꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
乙基
[1272]fmocꢀꢀꢀꢀꢀꢀꢀꢀꢀ
9-芴基甲氧羰基
[1273]glu-cꢀꢀꢀꢀꢀꢀꢀꢀ
内切蛋白酶(endoproteinase)glu-c[1274]hꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
小时
[1275]hatuꢀꢀꢀꢀꢀꢀꢀꢀꢀo-(7-氮杂苯并三唑-1-基)-n,n,n′
,n′‑
四甲基脲鎓六氟磷酸盐
[1276]hplcꢀꢀꢀꢀꢀꢀꢀꢀꢀ
高效液相色谱法
[1277]ivddeꢀꢀꢀꢀꢀꢀꢀꢀ
4,4-二甲基-2,6-二氧代环己-1-亚基)-3-甲基丁基
[1278]lcꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
液相色谱法
[1279]ltqꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
线性四极阱
[1280]lys-cꢀꢀꢀꢀꢀꢀꢀꢀ
内切蛋白酶
lys-c[1281]lloqꢀꢀꢀꢀꢀꢀꢀꢀꢀ
定量下限
[1282]mal
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
3-马来酰亚氨基丙基
[1283]meꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
甲基
[1284]meohꢀꢀꢀꢀꢀꢀꢀꢀꢀ
甲醇
[1285]minꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
分钟
[1286]mmtꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
单甲氧基三苯甲基
[1287]msꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
质谱/质谱法
[1288]m/zꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
质荷比
[1289]otbuꢀꢀꢀꢀꢀꢀꢀꢀꢀ
叔丁氧基
[1290]pegꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
聚(乙二醇)[1291]phꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀph值
[1292]pkꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
药代动力学
[1293]prꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
丙基
[1294]pthꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
甲状旁腺激素
[1295]pybopꢀꢀꢀꢀꢀꢀꢀꢀ
苯并三唑-1-基-氧基三吡咯烷子基磷鎓六氟磷酸盐
[1296]q-tofꢀꢀꢀꢀꢀꢀꢀꢀ
四极飞行时间
[1297]rp-hplcꢀꢀꢀꢀꢀꢀ
反相高效液相色谱法
[1298]rtꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
室温
[1299]simꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
单离子监测
[1300]secꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
尺寸排阻色谱法
[1301]scꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
皮下
[1302]t1/2ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
半衰期
[1303]tcpꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
氯化三苯甲基聚苯乙烯
[1304]tesꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三乙基硅烷
[1305]tfaꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三氟乙酸
[1306]thfꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
四氢呋喃
[1307]tmobꢀꢀꢀꢀꢀꢀꢀꢀꢀ
2,4,6-三甲氧基苄基
[1308]trtꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
三苯基甲基,三苯甲基
[1309]uloqꢀꢀꢀꢀꢀꢀꢀꢀꢀ
定量上限
[1310]uplcꢀꢀꢀꢀꢀꢀꢀꢀꢀ
超性能液相色谱法
[1311]uvꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
紫外线
[1312]zqꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
单四极杆
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1