CDKs抑制剂的药物组合物及制备方法与流程
本发明属于医药,具体涉及一类cdks激酶抑制剂的组合物,组合物的制备方法以及该组合物在制备用于治疗癌症的药物中的用途。
背景技术:
1、肿瘤的发生与多种癌基因和抑癌基因的失衡有关。几乎所有癌基因、抑癌基因的功能效应,最终都会汇聚到细胞周期上来。因此,可以说肿瘤是一类细胞周期性疾病(cellcycle disease,ccd),调节或阻断细胞周期是治疗肿瘤的途径之一。目前,已发现的与细胞周期调控有关的分子很多,其中细胞周期蛋白依赖性激酶(cyclin-dependent-kinases,cdks)是细胞周期调控网络的核心分子。cdks为催化亚单位,是一类丝氨酸(ser)/苏氨酸(thr)激酶,作为细胞内重要的信号传导分子,参与细胞周期的不同时期。研究表明,以cdks为中心的细胞周期调控网络,任何环节的异常都将引起细胞周期异常,最终导致肿瘤的发生。cdks家族目前有21个亚型,通过与其调节性亚单元cyclins(细胞周期蛋白)结合发挥作用。cdks各种亚型的功能,除了作用于细胞周期之外,还包括对转录、dna修复、分化和细胞程序性死亡的调节。基于cdks在调控肿瘤细胞的增殖和死亡中所起的关键作用,cdks激酶家族为抗肿瘤药物的发现与研制提供了机会和新的领域。
2、在参与细胞周期的cdks亚型中,cdk4/6发挥着不可替代的作用。与癌症有关的细胞周期突变主要存在于g1期和g1/s期转化过程中,cdk4/6与cyclind形成的复合物,通过抑癌基因rb产物prb磷酸化,释放结合的转录因子e2f,启动与s期有关的基因转录,促使细胞通过检验点,并从g1期向s期转移。大约80%的人类肿瘤中有cyclin d-cdk4/6-ink4-rb通路的异常。这条通路的改变,加速了g1期进程,使得肿瘤细胞增殖加快而获得生存优势。因此,对该通路的干预成为一种治疗策略,cdk4/6成为一种极具潜力的抗肿瘤靶点。
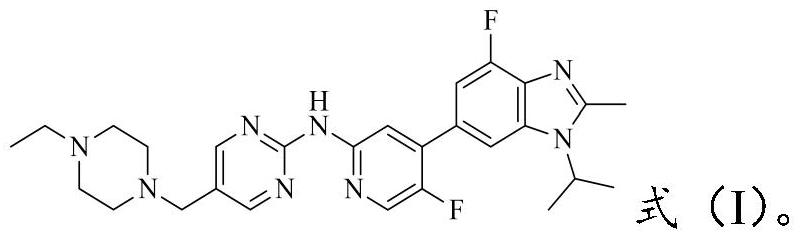
3、pct/cn2014/095615公开了如下化合物式(i)。研究表明,该化合物具有优异的cdk4/6激酶抑制活性,显示出良好的血脑屏障通过性,为cdks抑制剂作为肿瘤的治疗提供了可能性,且具有良好的安全性,
4、
技术实现思路
1、本发明提供了一种式(i)化合物的药物组合物及制备方法。解决的技术问题是提供一种适合于式(i)化合物的理化性质,并具有较好的崩解、溶出、释放、稳定性等药剂性质的药物组合物。具体地,本发明提供了一种药物组合物,其包括式(i)化合物、填充剂、黏合剂和崩解剂,任选地,还包括润滑剂和/或助流剂,
2、
3、在某些实施方案中,所述的药物组合物,其包括式(i)化合物、填充剂、黏合剂和崩解剂,任选地,还包括润滑剂和/或助流剂,
4、
5、其中,所述的填充剂选自微晶纤维素/一水乳糖或微晶纤维素/预胶化淀粉。
6、在某些实施方案中,所述的药物组合物,其包括式(i)化合物、填充剂、黏合剂和崩解剂,任选地,还包括润滑剂和/或助流剂,
7、
8、其中,所述填充剂选自微晶纤维素、一水乳糖、预胶化淀粉、甘露醇、无水磷酸氢钙、淀粉、糊精中的一种或多种;
9、所述黏合剂选自共聚维酮va64、羟丙基纤维素、聚维酮k30、羧甲基纤维素钠、甲基纤维素或羟丙甲纤维素中的一种或多种;
10、所述崩解剂选自交联羧甲基纤维素钠、羧甲淀粉钠、低取代羟丙基纤维素或交联聚维酮中的一种或多种;
11、所述润滑剂选自硬脂酸镁、硬脂酸、硬脂富马酸钠、山嵛酸甘油酯中的一种或多种;
12、所述助流剂选自二氧化硅或滑石粉。
13、在某些实施方案中,所述的药物组合物,其包括式(i)化合物、填充剂、黏合剂和崩解剂,
14、
15、其中,所述填充剂选自微晶纤维素、一水乳糖、预胶化淀粉、无水磷酸氢钙、淀粉、糊精中的一种或多种;
16、所述黏合剂选自羟丙基纤维素、聚维酮k30或羟丙甲纤维素中的一种或多种;
17、所述崩解剂选自交联羧甲基纤维素钠、羧甲淀粉钠或交联聚维酮中的一种或多种。
18、在某些实施方案中,所述的药物组合物,其包括式(i)化合物、填充剂、黏合剂和崩解剂,任选地,还包括润滑剂和/或助流剂,
19、
20、其中,所述填充剂选自微晶纤维素、一水乳糖、预胶化淀粉、无水磷酸氢钙、淀粉、糊精中的一种或多种;
21、所述黏合剂选自羟丙基纤维素、聚维酮k30或羟丙甲纤维素中的一种或多种;
22、所述崩解剂选自交联羧甲基纤维素钠、羧甲淀粉钠或交联聚维酮中的一种或多种;
23、所述润滑剂选自硬脂酸镁、硬脂酸、山嵛酸甘油酯中的一种或多种;
24、所述助流剂选自二氧化硅或滑石粉。
25、在某些实施方案中,所述的药物组合物,其包括式(i)化合物、填充剂、黏合剂和崩解剂,任选地,还包括润滑剂和/或助流剂,
26、所述的填充剂选自微晶纤维素、一水乳糖、预胶化淀粉中的一种或两种;
27、所述的黏合剂选自羟丙基纤维素或聚维酮k30;
28、所述的崩解剂选自交联羧甲基纤维素钠或交联聚维酮;
29、所述的润滑剂为硬脂酸镁;所述的助流剂为二氧化硅。
30、在某些实施方案中,所述的药物组合物,其包括式(i)化合物、填充剂、黏合剂和崩解剂,任选地,还包括润滑剂和/或助流剂,
31、所述的填充剂选自微晶纤维素/一水乳糖或微晶纤维素/预胶化淀粉;
32、所述的黏合剂为聚维酮k30或羟丙基纤维素;
33、所述的崩解剂为交联羧甲基纤维素钠;
34、所述的润滑剂为硬脂酸镁;所述的助流剂为二氧化硅。
35、在某些实施方案中,所述的药物组合物,其包括式(i)化合物、填充剂、黏合剂和崩解剂,
36、所述的填充剂选自微晶纤维素/一水乳糖或微晶纤维素/预胶化淀粉;
37、所述的黏合剂为聚维酮k30;
38、所述的崩解剂为交联羧甲基纤维素钠。
39、在某些实施方案中,所述的药物组合物,其包括式(i)化合物、填充剂、黏合剂和崩解剂,任选地,还包括润滑剂和/或助流剂,
40、所述的填充剂选自微晶纤维素ph101/一水乳糖或微晶纤维素ph101/预胶化淀粉;
41、所述的黏合剂为聚维酮k30;
42、所述的崩解剂为交联羧甲基纤维素钠;
43、所述的润滑剂为硬脂酸镁;所述的助流剂为二氧化硅。在某些实施方案中,所述的药物组合物,其包括式(i)化合物、填充剂、黏合剂和崩解剂,任选地,还包括润滑剂和/或助流剂,
44、
45、且按重量百分数计,各组分重量比如下:
46、
47、在某些实施方案中,所述填充剂选自微晶纤维素、一水乳糖、预胶化淀粉、甘露醇、无水磷酸氢钙、淀粉、糊精中的一种或多种。
48、在某些实施方案中,所述填充剂选自微晶纤维素、一水乳糖、预胶化淀粉、无水磷酸氢钙中的一种或多种。
49、在某些实施方案中,所述填充剂选自微晶纤维素、一水乳糖、预胶化淀粉中的一种或多种。
50、在某些实施方案中,所述填充剂选自微晶纤维素ph101、一水乳糖、预胶化淀粉、无水磷酸氢钙中的一种或多种。
51、在某些实施方案中,所述填充剂选自微晶纤维素ph101、一水乳糖、预胶化淀粉中的一种或两种。
52、在某些实施方案中,所述填充剂的重量百分比选自30%-70%。
53、在某些实施方案中,所述填充剂的重量百分比选自40%-70%。
54、在某些实施方案中,所述填充剂的重量百分比选自50%-65%。
55、在某些实施方案中,所述黏合剂选自共聚维酮va64、羟丙基纤维素、聚维酮k30、羧甲基纤维素钠或羟丙甲纤维素中的一种或多种。
56、在某些实施方案中,所述黏合剂选自羟丙基纤维素、聚维酮k30或羟丙甲纤维素中的一种或多种。
57、在某些实施方案中,所述黏合剂选自共聚维酮va64、羟丙基纤维素、聚维酮k30中的一种或多种。
58、在某些实施方案中,所述黏合剂选自共聚维酮va64、羟丙基纤维素或聚维酮k30。
59、在某些实施方案中,所述黏合剂选自羟丙基纤维素或聚维酮k30。
60、在某些实施方案中,所述黏合剂为聚维酮k30。
61、在某些实施方案中,所述黏合剂的重量百分比选自1%-5%。
62、在某些实施方案中,所述黏合剂的重量百分比选自2%-5%。
63、在某些实施方案中,所述黏合剂的重量百分比选自2%-4%。
64、在某些实施方案中,所述黏合剂的重量百分比选自3%-5%。
65、在某些实施方案中,所述崩解剂选自交联羧甲基纤维素钠、羧甲淀粉钠、低取代羟丙基纤维素或交联聚维酮中的一种或多种。
66、在某些实施方案中,所述崩解剂选自交联羧甲基纤维素钠、羧甲淀粉钠或交联聚维酮中的一种或多种。
67、在某些实施方案中,所述崩解剂选自交联羧甲基纤维素钠、羧甲淀粉钠或交联聚维酮。
68、在某些实施方案中,所述崩解剂选自交联羧甲基纤维素钠或羧甲淀粉钠。
69、在某些实施方案中,所述崩解剂选自交联羧甲基纤维素钠或交联聚维酮。
70、在某些实施方案中,所述崩解剂为交联羧甲基纤维素钠。
71、在某些实施方案中,所述崩解剂的重量百分比选自2%-8%。
72、在某些实施方案中,所述崩解剂的重量百分比选自2%-6%。
73、在某些实施方案中,所述崩解剂的重量百分比选自4%-6%。
74、在某些实施方案中,所述崩解剂可以一次性加入或分内外两次加入。
75、在某些实施方案中,所述崩解剂分内外两次加入,且内外两次添加量的重量比为5:1-1:3,例如5:1,4:1,3:1,2:1,1:1,1:2,1:3。
76、在某些实施方案中,所述崩解剂分内外两次加入,且内外两次添加量的重量比为2:1-1:2,例如2:1,1:1,1:2。
77、在某些实施方案中,所述润滑剂选自硬脂酸镁、硬脂酸、硬脂富马酸钠、山嵛酸甘油酯中的一种或多种。
78、在某些实施方案中,所述润滑剂选自硬脂酸镁、硬脂酸、山嵛酸甘油酯中的一种或多种。
79、在某些实施方案中,所述润滑剂选自硬脂酸镁、硬脂酸、硬脂富马酸钠中的一种或多种。
80、在某些实施方案中,所述润滑剂选自硬脂酸镁或硬脂酸。
81、在某些实施方案中,所述润滑剂为硬脂酸镁。
82、在某些实施方案中,所述润滑剂的重量百分比选自0-3%。
83、在某些实施方案中,所述润滑剂的重量百分比选自0.01%-3%。
84、在某些实施方案中,所述润滑剂的重量百分比选自0.5%-3%。
85、在某些实施方案中,所述润滑剂的重量百分比选自1%-3%。
86、在某些实施方案中,所述润滑剂的重量百分比选自1%-2%。
87、在某些实施方案中,所述助流剂选自二氧化硅或滑石粉。
88、在某些实施方案中,所述助流剂为二氧化硅。
89、在某些实施方案中,所述助流剂的重量百分比选自0-4%。
90、在某些实施方案中,所述助流剂的重量百分比选自0.01%-4%。
91、在某些实施方案中,所述助流剂的重量百分比选自0.5-4%。
92、在某些实施方案中,所述助流剂的重量百分比选自0-3%。
93、在某些实施方案中,所述助流剂的重量百分比选自0.5-3%。
94、在某些实施方案中,所述助流剂的重量百分比选自0-2%。
95、在某些实施方案中,所述助流剂的重量百分比选自0.5-2%。
96、在某些实施方案中,所述助流剂的重量百分比选自0-1%。
97、在某些实施方案中,所述助流剂的重量百分比选自0.01-1%。
98、在某些实施方案中,所述助流剂的重量百分比选自0.5-1%。
99、在某些实施方案中,所述的药物组合物,按重量百分数计,其包含20%-50%的式(i)化合物、50%-65%的填充剂、1%-5%的黏合剂、2%-8%的崩解剂、1%-3%的润滑剂、0.01-1%助流剂。
100、在某些实施方案中,所述的药物组合物,按重量百分数计,其包含20%-50%的式(i)化合物、50%-65%的填充剂、1%-5%的黏合剂、2%-8%的崩解剂、1%-3%的润滑剂、0.01-1%助流剂;
101、所述的填充剂选自微晶纤维素、一水乳糖、预胶化淀粉、无水磷酸氢钙中的一种或两种;
102、所述的黏合剂选自羟丙基纤维素或聚维酮k30;
103、所述的崩解剂选自交联羧甲基纤维素钠或交联聚维酮;
104、所述的润滑剂为硬脂酸镁;所述的助流剂为二氧化硅。
105、在某些实施方案中,所述的药物组合物,按重量百分数计,其包含20%-50%的式(i)化合物、40%-60%的填充剂、3%-5%的黏合剂、4%-6%的崩解剂、1%-3%的润滑剂、0.01-1%助流剂;
106、所述的填充剂选自微晶纤维素、一水乳糖、预胶化淀粉、无水磷酸氢钙中的一种或两种;
107、所述的黏合剂为聚维酮k30;
108、所述的崩解剂为交联羧甲基纤维素钠;
109、所述的润滑剂为硬脂酸镁;所述的助流剂为二氧化硅。
110、在某些实施方案中,所述的药物组合物,按重量百分数计,其包含20%-50%的式(i)化合物、50%-65%的填充剂、3%-5%的黏合剂、4%-6%的崩解剂、1%-3%的润滑剂、0.01-1%助流剂;
111、所述的填充剂选自微晶纤维素/一水乳糖、微晶纤维素/预胶化淀粉或微晶纤维素/无水磷酸氢钙;
112、所述的黏合剂为聚维酮k30;
113、所述的崩解剂为交联羧甲基纤维素钠;
114、所述的润滑剂为硬脂酸镁;所述的助流剂为二氧化硅。
115、在某些实施方案中,所述的药物组合物,按重量百分数计,其包含20%-50%的式(i)化合物、50%-65%的填充剂、3%-5%的黏合剂、4%-6%的崩解剂、1%-3%的润滑剂、0.01-1%助流剂;
116、所述的填充剂选自微晶纤维素ph101/一水乳糖、微晶纤维素ph101/预胶化淀粉或微晶纤维素ph101/无水磷酸氢钙;
117、所述的黏合剂为聚维酮k30;
118、所述的崩解剂为交联羧甲基纤维素钠;
119、所述的润滑剂为硬脂酸镁;所述的助流剂为二氧化硅。
120、在某些实施方案中,所述的药物组合物,按重量百分数计,其包含20%-40%的式(i)化合物、50%-60%的填充剂、3%-5%的黏合剂、4%-6%的崩解剂、1%-3%的润滑剂、0.01-1%助流剂。
121、在某些实施方案中,所述的药物组合物,按重量百分数计,其包含30%-40%的式(i)化合物、50%-60%的填充剂、3%-4%的黏合剂、4%-6%的崩解剂、1%-3%的润滑剂、0.01-1%助流剂。
122、在某些实施方案中,所述的药物组合物,按重量百分数计,其包含30%-40%的式(i)化合物、50%-60%的填充剂、3%-3.5%的黏合剂、4%-6%的崩解剂、1%-3%的润滑剂、0.01-1%助流剂。
123、在某些实施方案中,所述的药物组合物,按重量百分数计,其包含30%-40%的式(i)化合物、50%-60%的填充剂、3%-3.5%的黏合剂、4%-6%的崩解剂、1%-2%的润滑剂、0.01-1%助流剂。
124、在某些实施方案中,所述的填充剂选自微晶纤维素、一水乳糖、预胶化淀粉中的一种或两种。在某些实施方案中,所述的填充剂选自微晶纤维素/一水乳糖、微晶纤维素/预胶化淀粉、或微晶纤维素/无水磷酸氢钙。
125、在某些实施方案中,所述的填充剂选自微晶纤维素/一水乳糖、或微晶纤维素/预胶化淀粉。
126、在某些实施方案中,微晶纤维素/一水乳糖的重量比选自7:1-1:2,例如7:1,6:1,5:1,4:1,3:1,2:1,1:1,1:2。
127、在某些实施方案中,微晶纤维素/预胶化淀粉的重量比选自7:1-1:2,例如7:1,6:1,5:1,4:1,3:1,2:1,1:1,1:2。
128、在某些实施方案中,微晶纤维素/无水磷酸氢钙的重量比选自7:1-1:2,例如7:1,6:1,5:1,4:1,3:1,2:1,1:1,1:2。
129、在某些实施方案中,所述的填充剂选自微晶纤维素ph101/一水乳糖、微晶纤维素ph101/预胶化淀粉、或微晶纤维素ph101/无水磷酸氢钙。
130、在某些实施方案中,所述的填充剂选自微晶纤维素ph101/一水乳糖、或微晶纤维素ph101/预胶化淀粉。
131、在某些实施方案中,微晶纤维素ph101/一水乳糖的重量比选自7:1-1:2,例如7:1,6:1,5:1,4:1,3:1,2:1,1:1,1:2。
132、在某些实施方案中,微晶纤维素ph101/预胶化淀粉的重量比选自7:1-1:2,例如7:1,6:1,5:1,4:1,3:1,2:1,1:1,1:2。
133、在某些实施方案中,微晶纤维素ph101/无水磷酸氢钙的重量比选自7:1-1:2,例如7:1,6:1,5:1,4:1,3:1,2:1,1:1,1:2。
134、在某些实施方案中,微晶纤维素ph101/一水乳糖的重量比选自5:1-1:1。
135、在某些实施方案中,微晶纤维素ph101/预胶化淀粉的重量比选自5:1-1:1。
136、在某些实施方案中,微晶纤维素ph101/无水磷酸氢钙的重量比选自5:1-1:1。
137、在某些实施方案中,微晶纤维素ph101/一水乳糖的重量比选自4:1-1:1。
138、在某些实施方案中,微晶纤维素ph101/预胶化淀粉的重量比选自5:1-2:1。
139、在某些实施方案中,微晶纤维素ph101/无水磷酸氢钙的重量比选自4:1-1:1。
140、在某些实施方案中,所述的崩解剂为交联羧甲基纤维素钠。
141、在某些实施方案中,所述崩解剂可以一次性加入或分内外两次加入。
142、在某些实施方案中,所述崩解剂分内外两次加入,且内外两次添加量的重量比为5:1-1:3,例如5:1,4:1,3:1,2:1,1:1,1:2,1:3。
143、在某些实施方案中,所述崩解剂分内外两次加入,且内外两次添加量的重量比为2:1-1:2,例如2:1,1:1,1:2。
144、在某些实施方案中,所述崩解剂分内外两次加入,且内外两次添加量的重量比为1:1。
145、在某些实施方案中,所述润滑剂的重量百分比为1%。
146、在某些实施方案中,所述助流剂的重量百分比为0.5%。
147、在某些实施方案中,所述组合物任选包含适量的润湿剂,所述润湿剂选自无水乙醇或水。
148、在某些实施方案中,所述组合物任选包含适量的润湿剂,所述润湿剂为水。
149、在某些实施方案中,所述药物组合物可制备成片剂或胶囊剂。
150、另一方面,本发明还提供了一种制备如上所述的药物组合物的片剂的制备方法,包含以下步骤:
151、(1)将式(i)化合物与填充剂、内加崩解剂混合,获得预混合物;
152、(2)配制黏合剂溶液;
153、(3)将步骤(2)得到的所述黏合剂溶液与步骤(1)的所述预混合物进行混合,制粒;
154、(4)干燥步骤(3)得到的颗粒,并进行干整粒;
155、(5)将步骤(4)干整粒后得到的颗粒与外加崩解剂、任选的润滑剂、任选的助流剂一起进行总混,得到最终混合物;
156、(6)对步骤(5)所得的最终混合物进行压制,制得片芯;
157、(7)对步骤(6)获得的所述片芯包衣。
158、在某些实施方案中,在配制黏合剂溶液时,以无水乙醇或水作为润湿剂。
159、在某些实施方案中,在配制黏合剂溶液时,以水作为润湿剂。
160、在某些实施方案中,所述包衣过程所采用的包衣粉选自胃溶型薄膜包衣预混剂,包衣增重2%-8%,优选的,包衣增重2%-6%。
161、在某些实施方案中,所述包衣过程所采用的包衣分散剂选自无水乙醇或水。
162、在某些实施方案中,所述包衣过程所采用的包衣分散剂为水。
163、在另一方面,本发明还涉及前述药物组合物在制备用于预防和/或治疗受试者中由cdk4/6激酶介导的癌症相关疾病的药物中的用途。
164、本发明还提供一种在有需要的哺乳动物中治疗和/或预防由cdk4/6激酶介导的癌症相关疾病的方法,该方法包括给有需要的哺乳动物施用治疗和/或预防有效量的本发明所述的药物组合物。
165、在某些实施方案中,所述cdk4/6激酶介导的癌症相关疾病选自:脑瘤、肺癌、鳞状上皮细胞癌、膀胱癌、胃癌、卵巢癌、腹膜癌、胰腺癌、乳腺癌、头颈癌、子宫颈癌、子宫内膜癌、直肠癌、肝癌、肾癌、食管腺癌、食管鳞状细胞癌、前列腺癌、雌性生殖道癌、原位癌、淋巴瘤、神经纤维瘤、甲状腺癌、骨癌、皮肤癌、脑癌、结肠癌、睾丸癌、胃肠道间质瘤、前列腺肿瘤、肥大细胞肿瘤、多发性骨髓瘤、黑色素瘤、胶质瘤、肉瘤。
166、在另一方面,本发明还提供了一种试剂盒,包含:
167、(a)前述药物组合物,
168、和(b)有效量的一种或多种抗癌剂。
169、术语解释
170、在本发明中,除非另有说明,否则本文中使用的科学和技术名词具有本领域技术人员通常理解的含义,然而为了更好地理解本发明,下面提供了部分术语的定义。当本发明所提供的术语的定义和解释与本领域技术人员所通常理解的含义不符的时候,以本发明所提供的术语的定义和解释为准。
171、本发明所述的填充剂包括但不限于微晶纤维素、一水乳糖、预胶化淀粉、甘露醇、无水磷酸氢钙、淀粉、糊精。
172、本发明所述的黏合剂包括但不限于共聚维酮va64、羟丙基纤维素、羟丙甲纤维素、羧甲基纤维素钠、聚维酮k30、共聚维酮、麦芽糊精、麦芽糖。
173、本发明所述的润湿剂是指用来配制黏合剂溶液的溶剂,在制备药物组合物的过程中会逐渐被清除。其包括但不限于90%以上的乙醇和水,具体实例包括但不限于90%乙醇、95%乙醇、无水乙醇、水等。
174、本发明所述的“适量的润湿剂”中的“适量”是指根据黏合剂的用量来调整润湿剂的用量,主要根据黏合剂用量百分比(处方中)和黏合剂质量分数确定,黏合剂常用质量分数(与润湿剂的质量比)选自2%-10%(w/w),包括但不限于2%、3%、4%、5%、6%、7%、8%、9%和10%。
175、本发明所述的崩解剂包括但不限于交联羧甲基纤维素钠、羟甲基纤维素、羟甲基纤维素钙、低取代羟丙甲基纤维素、交联聚维酮、羟甲基淀粉钠、羟丙基淀粉。
176、本发明所述的润滑剂包括但不限于硬脂酸镁、硬脂酸钙、硬脂酸、硬脂富马酸钠、山嵛酸甘油酯、氢化植物油、聚乙二醇、月桂醇硫酸镁。
177、本发明所述的助流剂包括但不限于滑石粉、微粉硅胶、二氧化硅。
178、本发明所述的分散剂是指用来溶解包衣粉的溶剂,在片芯包衣过程中会逐渐被清除。所述分散剂包括但不限于无水乙醇和水。
179、本发明的药物组合物可以包装在不影响药物制剂稳定性的任何包装内。例如内包装可以为pvc铝塑泡罩包装、双铝包装、pvdc铝塑泡罩包装等,外包装为复合膜袋。
180、本发明所述的“有效量”是指能够预防、减轻、延缓、抑制或治愈受试者病症的药物剂量。给药剂量的大小与药物给药方式、药剂的药代动力学、疾病的严重程度、受试者的个性体征(性别、体重、身高、年龄)等相关。
181、本发明所述的“微晶纤维素/一水乳糖”是指,微晶纤维素和一水乳糖以任何可能的比例混合,比例包括但不限于,100:1-1:100,10:1-1:10,7:1-1:2,7:1,6:1,5:1,4:1,3:1,2:1,1:1,1:2,1:3,1:4,微晶纤维素和一水乳糖均包括其工业用途的各种产品型号。本发明所述的“微晶纤维素/预胶化淀粉”、“微晶纤维素/无水磷酸氢钙”定义同上。
182、本发明所述的药物组合物中,其各个组分的重量百分比之和小于或等于100%。
183、发明的有益效果
184、1、本发明药物组合物具有良好的崩解和溶出性能。
185、2、本发明药物组合物性质稳定,可提供较长的保质期。
186、3、本发明药物组合物工艺稳定,成本可控,可重复性强,能够满足工业化生产的要求。
- 还没有人留言评论。精彩留言会获得点赞!