一种刺激响应型脂肽递送系统及其制备方法和应用
本发明属于医药,具体涉及一种刺激响应型脂肽递送系统及其制备方法和应用。
背景技术:
1、恶性肿瘤的发病率和死亡率仅次于心血管疾病,严重威胁人类生命健康,给社会及家庭带来沉重的经济与精神负担。全球癌症统计数据显示,2021年全球癌症新发病例超2000万例,死亡病例超1000万例。据预测,截至2040年,全球的新发癌症患者总数将达到2800万,并将有约1620万患者因癌症而失去生命。
2、小分子化疗药物是目前临床上应用最普遍的肿瘤治疗手段之一。然而,化疗药物往往会引起肿瘤的多药耐药。此外,化疗药物所引起的全身毒性和不良反应也严重影响了治疗的有效性。为解决上述难题,临床上广泛采用联合用药策略。与单一药物相比,联合用药可通过相同或不同的机制靶向多个位点,协同增强抗肿瘤作用,并可以通过多种机制克服耐药问题;联合用药可通过较低剂量的药物取得相同或更佳的效果,同时,可以缓解或中和单药治疗引起的不良反应。
3、核酸类药物通过调控基因的转录和表达过程而发挥作用,主要包括rna和dna,目前应用较多的为反义寡核苷酸、mrna、mirna、sirna、sarna等。与小分子药物、蛋白药物等传统药物疗法比较,核酸类药物具有设计简单、研发周期短、成功率高、特异性强、疗效持久、能够在根本上调控致病基因等优势,在癌症、病毒感染等疾病治疗中具有很大的潜力。基因治疗是肿瘤辅助治疗的强有力手段,联合应用多种基因或多种疗法比单一基因或疗法能更有效地杀伤肿瘤细胞,达到想要的治疗效果。
4、由于小分子药物与核酸药物的理化性质差异较大,因此,在构建共递送系统时不仅要考虑二者作用机制之间的协同治疗效果,还应充分考虑二者分子结构特性及其与递送载体之间的相互作用力,从而实现小分子药物和核酸药物的时空共递送,最大化二者的协同治疗效果。脂肽递送系统是基于功能化的两亲性脂肽分子构建的纳米药物递送系统,凭借其灵活设计性,在多药共载领域展现出巨大优势。两亲性脂肽载体的亲脂嵌段可以通过疏水相互作用包载脂溶性小分子药物,亲水嵌段可通过静电作用和/或氢键作用包载核酸类药物。此外,还可在脂肽载体中引入功能化嵌段,例如还原敏感、ph敏感、酶敏感触发断裂化学键;溶酶体逃逸嵌段;响应触发释放嵌段等等,从而实现药物的快速释放和时空共递送。
5、因此,如何构建一种刺激响应型纳米递送系统,将疏水性药物与核酸药物高效共递送至肿瘤部位,并且在细胞内解离释放以及内涵体逃逸是亟待解决的难题。
技术实现思路
1、为了克服现有技术的不足,本发明的目的在于提供共同递送小分子药物和核酸的脂肽复合物及其制备方法和应用。利用两亲性脂肽分子共同递送包载质粒dna、反义寡核苷酸、小干扰rna、信使rna等核酸类药物和小分子疏水性药物制备双药递送系统。所制备的双药递送系统具有ph响应性,包载能力好,具有抵御阴离子置换的能力,能够提高核酸类药物在血清中稳定性,有效延长其体内的半衰期,有效降低核酸类药物的解离和释放,有效地介导核酸类药物的内涵体逃逸。
2、为了实现上述目的,本发明采用以下技术方案:
3、本发明提供一种用于共同递送小分子药物和核酸的刺激响应型脂肽递送系统。所述刺激响应型脂肽递送系统由两亲性脂肽分载体材料、小分子疏水性药物、核酸类药物以及透明质酸组成。
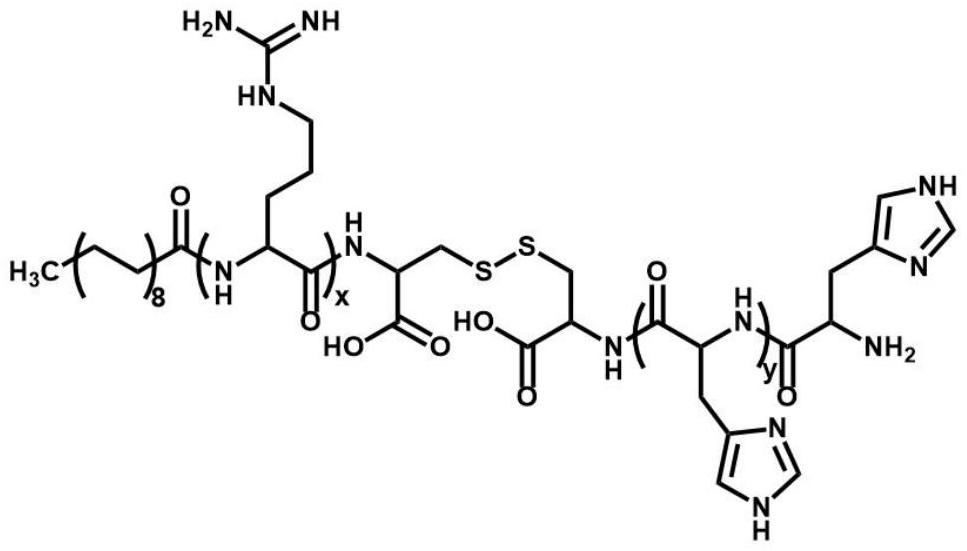
4、进一步的,两亲性脂肽分子由硬脂酸、寡聚精氨酸、二硫键、寡聚组氨酸片段(硬脂酸-寡聚精氨酸x-ss-寡聚组氨酸y,sa-pargx-ss-phisy)组成。其结构式如下:
5、
6、x取自1-30中的任意自然数,y取自1-30中的任意自然数。
7、进一步的,小分子疏水性药物为阿托伐他汀、紫草素、姜黄素、白藜芦醇、雷公藤红素、多西他赛、10-羟基喜树碱、替尼泊苷和6-巯基嘌呤或紫杉醇。
8、进一步的,核酸药物选自质粒dna、反义寡核苷酸、小干扰rna、微小rna和信使rna。
9、进一步的,所述的透明质酸(ha)的分子量为100da~100000da,优选的为1000da~10000da。
10、本发明还提供了刺激响应型脂肽递送系统的制备方法,所述制备方法包括以下步骤:
11、(1)将两亲性脂肽分子和小分子疏水性药物溶于有机溶剂中,超声溶解,于旋转蒸发仪上真空干燥得到均匀透明薄膜。
12、(2)按照相应的氮磷比向步骤(1)得到的均匀透明薄膜中加入核酸药物溶液,水化,得共载核酸药物和小分子疏水性药物的脂肽复合物
13、(3)向步骤(2)得到的共载核酸药物和小分子疏水性药物的脂肽复合物中加入透明质酸,孵育后,得到刺激响应型脂肽递送系统。
14、进一步的,以摩尔量计,透明质酸与脂肽分子的比例为(1:1)~(1:10),优选的为(1:3)~(1:5)。
15、进一步的,以质量百分比计,所述疏水性药物的载药量为1%~10%;优选的为3%~8%。
16、进一步的,以氮磷比(n/p比,表示载体中氨基氮与sirna分子中磷酸基团的摩尔比),所述核酸药物的n/p比(1:1)~(40:1),优选的为(15:1)~(35:1)。
17、进一步的,步骤(1)中有机溶剂为石油醚、环己烷、二氯甲烷、三氯甲烷、乙酸乙酯、甲醇、乙醇、丙酮或异丙醇中的一种或几种;优选的为二氯甲烷、乙酸乙酯或甲醇中的一种或几种。
18、进一步的,步骤(1)中超声时间为0~1h,优选的为5~20min;超声频率为28khz或40khz。
19、进一步的,步骤(2)的水化温度为30~60℃,优选为35~50℃;水化时间为0~4h,优选为0.25~2h。
20、进一步的,步骤(3)中孵育温度为37℃;孵育时间为0~4h,优选为0.25~2h。
21、本发明提供刺激响应型脂肽递送系统或其药学上可接受的盐在制备治疗肿瘤药物中的应用;所述肿瘤为黑色素瘤,肺癌,乳腺癌或结直肠癌。
22、本发明提供一种药物组合物,包括刺激响应型脂肽递送系统或其药学上可接受的盐以及药学上可接受的辅料。
23、本发明提供上述药物组合物在制备治疗肿瘤药物中的应用;所述肿瘤为黑色素瘤,肺癌,乳腺癌或结直肠癌。
24、本发明提供的刺激响应型脂肽递送系统共同包载小分子和核酸药物的分子机制是:两亲性脂肽分子的硬脂酸通过疏水作用力包载小分子药物形成内核,寡组氨酸和寡精氨酸片段分别通过氢键和静电相互作用包载核酸药物形成中间层,最外层通过静电相互作用修饰具有肿瘤靶向能力的透明质酸ha。
25、本发明的有益效果:
26、本发明所构建的脂肽复合物对小分子和核酸药物均具有较高的载药量,可在血液循环中保持稳定,并借助透明质酸与肿瘤细胞表面过度表达的cd44受体之间的相互作用,主动靶向递送至肿瘤细胞。在内涵体/溶酶体酸性和还原性环境触发下,脂肽分子中寡聚组氨酸嵌段发生质子化,二硫键断裂,导致复合物结构的破坏,引发小分子和核酸药物的快速同步释放。sa-pargx嵌段的膜通透作用与phisy的“质子海绵”效应共同介导高效的内涵体/溶酶体逃过程,实现疏水性小分子和核酸药物的有效胞浆共递送,从而发挥协同抗肿瘤的功效。
- 还没有人留言评论。精彩留言会获得点赞!