背载血小板激活抑制剂纳米粒的工程化血小板及其制备方法及应用
本发明涉及药物,涉及一种背载血小板激活抑制剂纳米粒的工程化血小板及其制备方法及应用。
背景技术:
1、癌症是目前导致死亡的主要原因之一。传统的治疗方式比如免疫治疗、化疗、放疗等仍然不尽人意。最近的证据表明,血小板与肿瘤的发展息息相关。由于肿瘤生长速度较快,肿瘤血管完整性较差,纳米药物通过渗漏的脉管系统进入肿瘤组织中。然而破损的内皮会吸引静息状态的血小板并启动凝血反应以保护肿瘤血管的完整性,削弱增强渗透性和保留(epr)效应,减少了纳米药物在肿瘤部位的积累,抑制了其治疗效果。
2、此外,据报道,静息的血小板可以与肿瘤细胞相互接触,并将肿瘤细胞的pd-l1储存至α颗粒中。当血小板激活时,储存的pd-l1会从α颗粒中释放出来并转移至血小板表面。含有肿瘤源性pd-l1的血小板会与t细胞相互作用,从而显著抑制cd8阳性t细胞的增殖、活化和细胞毒性,抑制全身抗肿瘤免疫,并促进免疫逃逸。因此,血小板数量和活性的增加与预后不良和总体生存率降低有关抑制血小板的数量和功能成为一种有前景的治疗策略,可减轻肿瘤免疫抑制、破坏肿瘤血管完整性并增强靶向递送化疗纳米药物。然而,血小板的全身性消耗可能会引起了凝血功能障碍和全身毒性的增加。
3、血小板具有天然的特异组织靶向性,近年来,被广泛应用于递药系统。在肿瘤部位,由于炎症微环境的影响,血小板会激活,而后通过级联反应会招募更多的血小板到达肿瘤部位。因此基于血小板的递送系统应运而生,以减少药物的脱靶效应,降低副作用。此外,激活的血小板可以分泌基质金属蛋白酶,而明胶可以特异性且快速的被基质金属蛋白酶降解,释放出包载的药物。
技术实现思路
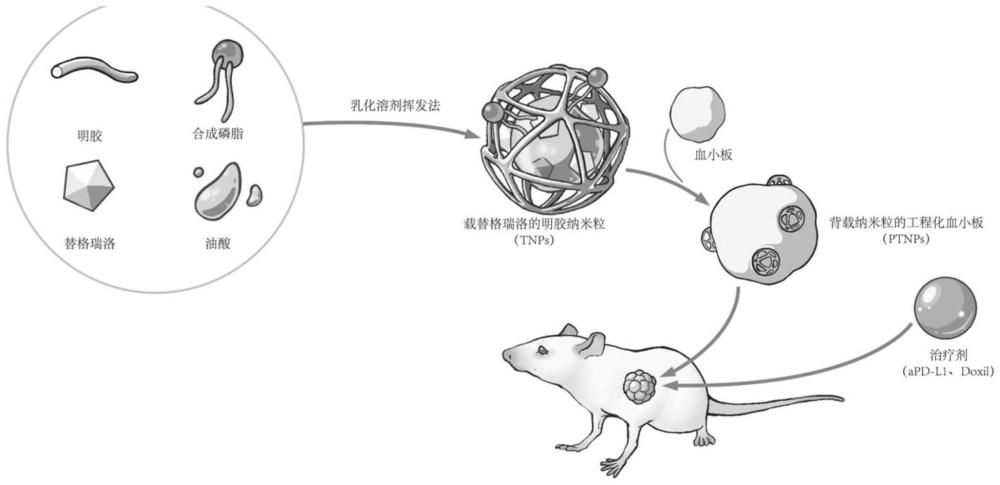
1、本发明所解决的技术问题是为了克服现有的技术缺陷,考虑到血小板的肿瘤靶向能力以及明胶颗粒快速响应基质金属蛋白酶(mmps)的能力,开发了一种新的血小板活化抑制剂递送系统,该系统旨在最大限度地减少抗血小板药物的全身毒性并增强其临床应用。具体来说,我们设计了负载替格瑞洛的明胶纳米粒子(tnps)并将其缀合到静息血小板的表面,形成背载血小板激活抑制剂纳米粒的工程化血小板(ptnps),这些工程化血小板可以靶向激活的肿瘤相关血小板,并通过其分泌的基质金属蛋白酶降解明胶纳米粒,随后释放包载的血小板激活抑制剂,替格瑞洛。这一过程维持了新招募的血小板的静息状态,以抑制肿瘤血管屏障的修复,并减轻了血小板介导的肿瘤免疫抑制。该工程化血小板可以与化疗纳米药物以及免疫检查点抑制剂协同使用,增强抗肿瘤治疗的长期疗效并减少副作用。
2、具体地,本发明的第一个目的是,针对传统抗肿瘤纳米制剂以及免疫检查点抑制剂疗效不佳的痛点,克服了传统抗血小板药物非靶向分布多,副作用大的缺点,提供一种靶向肿瘤相关血小板的新剂型,即背载血小板激活抑制剂纳米粒的工程化血小板(ptnps)。
3、本发明的第二个目的是,提供所述背载血小板激活抑制剂纳米粒的工程化血小板的制备方法。
4、本发明的第三个目的是,提供所述背载血小板激活抑制剂纳米粒的工程化血小板的应用。
5、为实现上述第一个目的,本发明采取的技术方案是:提供背载血小板激活抑制剂纳米粒的工程化血小板,所述的工程化血小板外部通过4-(n-马来酰亚胺甲基)环己烷-1-羧酸磺酸基琥珀酰亚胺酯钠盐(sulfosuccinimidyl 4-(n-maleimidomethyl)cyclohexane-1-carboxylate,sulfo-smcc)偶联了含血小板激活抑制剂的纳米粒。载血小板激活抑制剂的纳米粒可以由乳化溶剂挥发法、二次去溶剂法、纳米沉淀法、反相微乳法等方法制备。
6、具体地,所述的背载血小板激活抑制剂纳米粒的工程化血小板包含替格瑞洛、明胶、油酸、合成磷脂、sulfo-smcc、以及血小板,其中,替格瑞洛、明胶、油酸、合成磷脂共同构成纳米粒,1个血小板装载1-14个纳米粒。优选1个血小板装载10个纳米粒,含有15皮克替格瑞洛。
7、本发明所述的替格瑞洛还可以为其他血小板激活抑制剂,如阿司匹林、氯吡格雷、替罗非班、西洛他唑或其衍生物中的一种或几种抑制血小板激活的药物。
8、所述的明胶还可以为其他基质金属蛋白酶敏感的有机载体,如胶原、基质金属蛋白酶敏感肽或其衍生物中的一种或几种,能够特异性的被基质金属蛋白酶降解。
9、所述的油酸、合成磷脂还可以为其他乳化剂、稳定剂。所述合成磷脂优选1,2-二油酰-sn-甘油-3-磷酸胆碱(dopc)。
10、所述的sulfo-smcc还可以为其他交联剂,如nhs-ss-nhs等蛋白质连接键修饰,并耦合在血小板表面。
11、所述的载血小板激活抑制剂纳米粒为球状,粒径为70-110nm。所述纳米粒以明胶为主体,油酸、合成磷脂起到乳化剂和稳定剂作用,血小板激活抑制剂为包载药物。其中各成分的重量百分比组成是:血小板激活抑制剂占3%-5%,合成磷脂占1%-3%,油酸占30%-40%,余量为明胶。
12、所述的血小板为鼠源性,由鼠新鲜血浆提取而来。
13、为了实现上述第二个目的,本发明采取的技术方案是将载有血小板激活抑制剂的纳米粒装载于血小板外部,所述的制备方法包括以下步骤:
14、(1)制备包载血小板激活抑制剂的纳米粒;
15、(2)提取血小板;
16、(3)将纳米粒耦合在血小板表面。
17、其中,步骤(1)所述的纳米粒通过乳化溶剂挥发法制备。具体地,将替格瑞洛、油酸、合成磷脂溶解于二氯甲烷中制得有机相,然后将有机相转移至明胶水溶液中,水相有机相体积比为1:2-1:4,在冰浴下进行超声制备纳米颗粒,所制备的纳米粒为球状,粒径为70-110nm。而后通过悬蒸法挥发有机溶剂,备用。
18、步骤(2)中,通过枸橼酸钠抗凝后的新鲜血液通过离心获得富血小板血浆,将富血小板血浆与血液保存液acd等体积混合,800g离心10分钟,获得纯净的血小板,置于含有前列环素的任氏液中备用。
19、步骤(3)中,先将步骤(1)中制备的纳米粒与过量的sulfo-smcc在pbs中混合,并在室温-37℃下搅拌反应0.5小时。使用超滤管纯化纳米粒,并在pbs中洗涤三次,以除去过量的sulfo-smcc;而后将sulfo-smcc耦合的纳米粒与步骤(2)中提取的血小板在任氏液中孵育0.5-1小时。800g离心10分钟,并在任氏液中洗涤三次,除去未偶联的纳米凝胶。
20、背载血小板激活抑制剂纳米粒的工程化血小板成功制备。
21、为实现上述第三个目的,本发明采取的技术方案是:制备一种背载血小板激活抑制剂纳米粒的工程化血小板,并考察其辅助纳米药物或免疫检查点抑制剂抗肿瘤的应用。
22、所述的背载血小板激活抑制剂纳米粒的工程化血小板在制备药物传递系统中的应用。
23、所述的背载血小板激活抑制剂纳米粒的工程化血小板在制备与抗pd-l1、抗pd-1、抗ctla-4免疫检查点抑制剂联合使用的药物中的应用。
24、所述的背载血小板激活抑制剂纳米粒的工程化血小板在制备与阿霉素脂质体、紫杉醇白蛋白纳米粒纳米化疗药联合使用的药物中的应用。
25、具体地,本发明制备了背载血小板激活抑制剂纳米粒的工程化血小板(ptnps),并对其性质进行了考察,同时制备了背载空白纳米粒的工程化血小板(pnps),载血小板激活抑制剂的纳米粒(tnps)以及血小板激活抑制剂溶液剂(ticagrelor)。详细考察内容如下:
26、1)对制备的背载血小板激活抑制剂纳米粒的工程化血小板的理化性质进行了表征,如:纳米粒的粒径,功能化血小板的形态,粘附效率,蛋白表达情况,药物释放情况等。
27、2)考察了背载血小板激活抑制剂纳米粒的工程化血小板在荷黑色素瘤小鼠的靶向性。
28、3)考察了背载血小板激活抑制剂纳米粒的工程化血小板提高抗肿瘤免疫治疗疗效的能力。
29、4)考察了背载血小板激活抑制剂纳米粒的工程化血小板增强纳米药物抗肿瘤疗效等能力。
30、结果表明,本发明所制备的背载血小板激活抑制剂纳米粒的工程化血小板能够靶向肿瘤相关血小板,并抑制其余血小板的激活,破坏肿瘤血管内皮屏障,缓解免疫抑制性微环境,促进纳米药物以及免疫检查点抑制剂的抗肿瘤效果。
31、本发明的有益效果:
32、本发明提供的背载血小板激活抑制剂纳米粒的工程化血小板能够靶向肿瘤部位相关的血小板,通过激活血小板释放的基质金属蛋白酶特异性的降解背载的纳米粒,释放血小板激活抑制剂,抑制血小板激活。减少血小板表面pd-l1的表达,以缓解肿瘤免疫抑制性微环境,维持肿瘤血管不完整性,增强纳米药物渗透效率,促进免疫检查点抑制剂以及纳米化疗制剂的抗肿瘤效果。
- 还没有人留言评论。精彩留言会获得点赞!