手术操作训练用的人工器官模型、该人工器官模型的制造方法以及使用该人工器官模型的手术操作训练方法与流程
1.本发明涉及一种手术操作训练用的人工器官模型、该人工器官模型的制造方法以及使用该人工器官模型的手术操作训练方法。
背景技术:
2.关于对手术执刀技术具有高要求的手术,例如以心脏手术为例,在日本每年会进行约5万例的手术。然而,现状是,这些手术会被分摊给大量的医院(约500家医院)和大量的心脏外科医生,因此实际上每名外科医生的执刀数是有限的。
3.而且,随着患者的高龄化、再次手术的增长、非体外循环冠状动脉旁路移植术(off
‑
pump coronary artery bypass grafting)手术的普遍化,支架插入后限定吻合部位的病例等病例的难易程度逐年上升,据说年轻心脏外科医生可执刀的机会逐渐减少。
4.为了弥补减少的执刀经验,以往使用猪等动物的内部器官或人工器官进行操作训练。
5.其中,作为人工器官模型,以往提出了利用有机硅(silicone)、聚氨酯弹性体、苯乙烯弹性体、聚乙烯醇(pva)等制造的模型。
6.其中,对于将血管等模拟器官封入由聚乙烯醇(pva)生成的凝胶状而制成的模型,它虽然是人造的,但与实际的人体组织具有相似的切开感,因此比较合适。
技术实现要素:
7.然而,在上述以往的人工器官模型中,依然存在缺乏实际器官的再现性之处,因而需要开发更加适于手术操作训练的人工组织。
8.本发明是鉴于这样的事由而完成的,目的在于提供一种与以往的人工组织相比能够更良好地用于手术操作训练的人工组织模型以及其制造方法。
9.发明人们为了提高在手术操作训练中与切开实际的人体器官相比时的再现性,在反复试验后,得到了关于器官的膜剥离再现性较高的人工器官模型的见解,在实际制造试验品并潜心开发后,完成了本发明。
10.即,根据本发明的主要观点能够得到:(1)一种手术操作训练用的人工器官模型,其特征在于,上述手术操作训练用的人工器官模型具有纤维材料结构体,上述纤维材料结构体由2层以上的纤维材料层以手术操作训练实施者可剥离的强度相互粘合并层叠而成,上述纤维材料结构体是通过在使上述2层以上的纤维材料层以上述强度相互粘合后,以导电性的液体、液状溶胶(sol)或液状凝胶(gel)将其整体地浸润而形成的。
11.根据这样的结构,通过层叠并相互粘合纤维材料层,能够再现人体的膜结构体,然后,通过以导电液/凝胶赋予润湿性以及导电性,能够实现使用电手术刀等进行的剥离操作
的模拟。即,通过施加在外科上合适的对抗牵引 (countertraction)、牵引力,能够实现利用电手术刀进行的剥离、切断、烧灼、凝固等处理。此外,可在各层间适当配置输尿管、血管、肠道、神经等作为手术训练操作对象的器官以及结构体。在此,上述导电性的液体、液状溶胶或凝胶优选为具有1cp以上的粘度的电解质水溶液、具有流动性的水凝胶、水溶胶、乳液、蛋清、蛋清以及电解质水溶液的混合溶液等。
12.此外,根据该第1观点的人工器官模型,优选以以下的方式实施。
13.(2)在上述(1)的手术操作训练用的人工器官模型中,其特征在于,在上述2层以上的纤维材料层中,相邻的2个纤维材料层形成为具有彼此不同的材料、材质或不同的颜色,以使得上述手术操作训练实施者可识别出上述2个纤维材料层为不同的膜。
14.(3)在上述(1)的手术操作训练用的人工器官模型中,其特征在于,在上述2层以上的纤维材料层中的被选择的2个纤维材料层之间配置有手术操作训练用的模拟器官。
15.(4)在上述(3)的手术操作训练用的人工器官模型中,其特征在于,上述模拟器官为由人工材料形成的人工模拟器官。
16.(5)在上述(3)的手术操作训练用的人工器官模型中,其特征在于,上述模拟器官获取自动物。
17.(6)在上述(3)的手术操作训练用的人工器官模型中,其特征在于,上述模拟器官为输尿管、血管、肠道、神经中的一种或两种以上。
18.(7)在上述(1)的手术操作训练用的人工器官模型中,其特征在于,使用热塑性树脂来进行上述纤维材料层之间的粘合。
19.(8)在上述(1)的手术操作训练用的人工器官模型中,其特征在于,通过由多孔质材料形成的粘合层来进行上述纤维材料层之间的粘合。
20.(9)在上述(8)的手术操作训练用的人工器官模型中,其特征在于,上述粘合层为粘合衬(adhesive interlining)。
21.(10)在上述(9)的手术操作训练用的人工器官模型中,其特征在于,根据需要的剥离强度,使用2个以上的上述粘合衬。
22.(11)在上述(1)的手术操作训练用的人工器官模型中,其特征在于,该人工器官模型粘合于指定的模拟器官的表面。
23.(12)在上述(1)的手术操作训练用的人工器官模型中,其特征在于,上述导电性的液体或凝胶的粘度为50000cp以下。
24.(13)在上述(12)的手术操作训练用的人工器官模型中,其特征在于,上述导电性的液体或凝胶的粘度为140cp~20000cp。
25.(14)在上述(12)的手术操作训练用的人工器官模型中,其特征在于,上述导电性的液体或凝胶的粘度为900cp~5000cp。
26.(15)在上述(1)的手术操作训练用的人工器官模型中,其特征在于,上述导电性的液体或凝胶为无色透明。
27.(16)在上述(1)的手术操作训练用的人工器官模型中,其特征在于,上述纤维材料结构体在被导电性的液体或凝胶整体地浸润后,被封装。
28.(17)一种手术操作训练用的人工器官模型的制造方法,其特征在于,上述制造方法具有:准备2层以上的纤维材料层的工序;使上述2层以上的纤维材料层层叠并相互粘合的工序;和向上述相互粘合的2层以上的纤维材料层供给导电性的液体或凝胶,以浸润上述相互粘合的2层以上的纤维材料层的工序。
29.(18)在上述(17)的制造方法中,其特征在于,在上述粘合工序中,以通过手术操作训练实施者的手术操作可剥离的强度将上述2层以上的纤维材料层彼此粘合。
30.(19)在上述(17)的制造方法中,其特征在于,上述制造方法还具有对上述2层以上的纤维材料层中相邻的2个纤维材料层作如下准备的工序:使上述2层以上的纤维材料层中相邻的2个纤维材料层具有彼此不同的材料、材质或不同的颜色,以使得上述手术操作训练实施者可识别出上述2个纤维材料层为不同的膜。
31.(20)在上述(17)的制造方法中,其特征在于,使上述2层以上的纤维材料层层叠并相互粘合的工序具有:在层叠上述2层以上的纤维材料层时,使片状的粘合层位于上述纤维层之间的工序;和加热上述层叠后的2层以上的纤维材料层而使上述纤维材料层彼此粘合的工序。
32.(21)在上述(17)制造方法中,其特征在于,上述制造方法还具有:在上述2层以上的纤维材料层中的被选择的2个纤维材料层之间配置手术操作训练用的模拟器官的工序。
33.(22)在上述(21)的制造方法中,其特征在于,上述模拟器官为由人工材料形成的人工模拟器官。
34.(23)在上述(21)的制造方法中,其特征在于,上述模拟器官获取自动物。
35.(24)在上述(21)的制造方法中,其特征在于,上述模拟器官为输尿管、血管、肠道、神经中的一种或两种以上。
36.(25)在上述(17)的制造方法中,其特征在于,使用热塑性树脂来进行上述纤维材料层之间的粘合。
37.(26)在上述(17)的制造方法中,其特征在于,通过层叠使用所选择的1片或多片浸渗有或涂布有上述热塑性树脂或粘合剂的薄膜片来进行上述纤维材料层之间的粘合。
38.(27)在上述(17)的制造方法中,其特征在于,上述制造方法还具有:将上述人工器官模型粘合于指定的模拟器官的表面的工序。
39.(28)在上述(17)的制造方法中,其特征在于,上述制造方法还具有:
对被上述导电性的液体或凝胶湿润的纤维材料层进行封装的工序。
40.(29)在一种使用人工器官模型的手术操作训练方法中,其特征在于,上述人工器官模型具有纤维材料结构体,上述纤维材料结构体由2层以上的纤维材料层以手术操作训练实施者可剥离的强度相互粘合并层叠而成,上述纤维材料结构体是通过在使上述2层以上的纤维材料层以上述强度相互粘合后,以导电性的液体或液状凝胶将其整体地浸润而形成的,该手术操作训练方法具有:用钳子将上述2层以上的纤维材料层中的表层提起而施加牵引力(对抗牵引) 的工序;和通过电手术刀或超声手术刀切开上述提起的纤维材料层,使其与下层的纤维材料层分离而进行剥离的工序。
41.(30)在上述(28)所述的训练方法中,其特征在于,在上述人工器官模型的2层以上的纤维材料层中的被选择的2个纤维材料层之间,配置有手术操作训练用的模拟器官,该训练方法还进一步具有获取上述模拟器官的工序。
42.应予说明,上述以外的本发明的特征示于以下的用于实施发明的方式的项目以及附图中。
附图说明
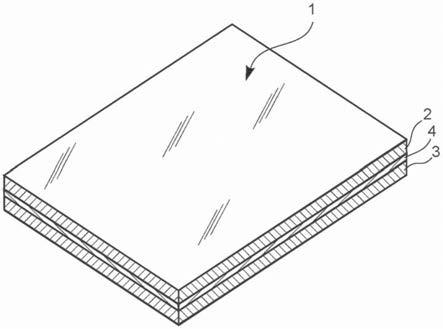
43.图1为表示本发明的第一实施方式的人工器官模型的概略结构图。
44.图2为表示同一实施方式的制造工序的概略图。
45.图3为表示使用同一实施方式的人工器官模型的手术操作训练的照片。
46.图4为表示使用同一实施方式的人工器官模型的手术操作训练的模式图。
47.图5为表示使用同一实施方式的人工器官模型的手术操作训练的模式图。
48.图6为表示第二实施方式的人工器官模型的概略结构图。
49.图7为同一实施方式的图6的a
‑
a视图以及俯视图。
50.图8为同一实施方式的与图7对应的照片。
51.图9为表示第三实施方式的人工器官模型的概略结构图。
52.图10为表示同一实施方式的外观的照片。
53.图11为同一实施方式的与图10对应的概略结构图。
54.图12为表示同一实施方式的手术操作训练的照片。
55.图13为表示第四实施方式的人工器官模型的照片。
56.图14为同一实施方式的与图13对应的概略结构图。
57.图15为同一实施方式的图14的a
‑
a视图。
58.图16为同一实施方式的图14的b
‑
b视图。
59.图17为表示同一实施方式的剥离强度测定结果的表。
60.图18为对同一实施方式的试片(test piece)间的剥离强度进行比较的图。
61.图19为表示同一实施方式的导电性粘液的最佳粘度的分布的图。
62.图20为表示同一实施方式的第四实施例的人工器官模型的制造工序的图。
63.图21为表示安装了同一实施方式的人工器官模型的状态的立体图。
64.图22为表示组装同一实施方式的人工器官模型的多层次结构的模式图。
65.图23为表示同一实施方式的人工器官模型的固定框的照片。
66.图24为表示同一实施方式的人工器官模型的固定框的照片。
67.图25为表示同一实施方式的人工器官模型的完成状态的照片。
68.图26为表示同一实施方式的人工器官模型的使用形态的照片。
具体实施方式
69.下面,参照附图对本发明的一个实施方式进行说明。
70.(第一实施方式)(结构)图1为表示具有本发明的最基础的形态的人工器官模型1(基础模型)的立体图,图2为表示其制造工序的模式图。
71.人工器官模型1为具有第1、第2纤维材料层2、3的2层结构,在第 1、第2纤维材料层2、3之间设有粘合层4,第1、第2纤维材料2、3通过该粘合层4以可剥离的方式粘合。
72.各纤维材料层2、3为天然或化学纤维的纺织品或非织造物 (nonwovens),构成为使纤维材料的长度方向大致沿着各层的面方向延长。而且,各纤维材料层2、3各自模拟不同的器官(皮肤层、脂肪层、血管等),彼此被染成不同的颜色、或者由不同的材质或材料的纤维构成,从而使用户能够容易地识别纤维材料层2、3的分界线。
73.上述粘合层4为由纤维材料形成的薄膜片状的材料,其含有或浸渗有指定的粘合剂,或在一面或两面涂布有指定的粘合剂而形成。该粘合层由多孔质材料构成,以使之后浸渗于该人工器官模型的导电性凝胶可在其厚度方向上流通,其优选为粘合衬。此外,根据上述第1、第2纤维材料层间所需要的剥离强度,该粘合层4可使用一片或重叠多片来使用。
74.而且,在本实施方式中,如上述图2所示,在将上述粘合层4夹于上述第1、第2纤维材料层2、3之间并沿厚度方向层叠后(步骤s1~s3),使用熨斗 (iron)等进行加压并加热,然后,进行冷却,从而使上述第1、第2纤维材料层2、 3相互粘合(步骤s4)。接着,利用导电性粘液使其整体地湿润,从而完成该人工器官模型1的制造(步骤s4)。
75.应予说明,在此,在ebm公司的实施品中,会对纤维结构体进行染色,以清楚显示纤维材料层的视觉识别性、层的边界。因此,导电性粘液(或单纯的液体)仅仅是具有流动性的液体状,且必须为无色或透明(透光性),以不妨碍纤维材料层的识别。(本发明中的粘合层的功能)在本发明中,通过使用粘合层4(具体而言,使用粘合衬),将上述第1、第2 纤维材料层2、3彼此粘合来构筑本模型1的基本结构体。这是与如以往的使用 pva的模型般由pva自身构成基本结构体的模型大为不同的一点。
76.在此,通过将粘合衬4用于纤维材料层2、3之间的边界层,赋予任意的剥离强度。由此,在由多层纤维材料形成的纤维结构体中,可设计针对剥离操作训练的剥离强度,并且能够实现有目的的再现。
77.在此,发明人们为了验证本发明的粘合层所实现的剥离强度的意义,在利用导电
性粘液对上述纤维材料层进行湿润之前的干燥状态、自然状态下,利用粘合衬将宽度10mm、长度15cm、厚度约3mm的单层纤维材料粘合为2 层的长条形的2层纤维材料结构体,以此作为试片(样品)a、b,使用定额为10n 的负载传感器,实施对剥离强度的测量。
78.制作试片a:有粘合衬且未经导电性粘液浸润、试片b:有粘合衬且经导电性粘液浸润、试片c:单层的纤维材料层(无边界层)作为上述试片,并在图17中展示其试验以及测量的结果。应予说明,将试片的一端50mm的部分作为试片a、b、c中均未使用粘合衬的非粘合区域,并作为拉伸试验机的夹具的把持用区域(夹紧(chuck)区域)。
79.作为试验方法,参考通常实施的胶带(tape)的剥离强度的测量系统来设计测量系统。将初始状态下的上述夹具的间隔设为20mm。夹紧区域为宽度 10mm、长度10mm,并设为与试片一致的形状。设想外科手术中的剥离操作,将拉伸速度设定为300mm/min。对夹紧区域施加从初始状态开始位移200mm的变位,采用最大载荷作为剥离强度。由于剥离强度与试片的宽度成比例地增加,因此采用最大载荷除以宽度而得到的值(n/cm)作为剥离强度。
80.将这样测量得到的剥离强度的试验结果示于图17以及图18中。
81.即,试片a为仅利用粘合衬的粘合而未被提供粘液浸润的所谓的干燥状态的试片。根据该结构,a的剥离强度为0.911n,标准偏差为0.146。
82.试片b为对使用粘合衬进行粘合的纤维结构体浸润了导电性粘液的试片。剥离强度为o.559n,标准偏差为0.158n,与试片a相比,该值明显较低,但其显示出稳定的剥离强度。关于剥离强度的一定程度的下降,认为是由于粘液的水分对粘合衬产生了作用。
83.试片c为未使用粘合衬的纤维层单层的试验结果。c的剥离强度为 3.217n,标准偏差为0.290,与使用了粘合衬的a、b相比,其明显具有稳定的高剥离强度。该试片c的结果显示,在本发明中,通过使用粘合衬,能够有目的地再现脆弱的剥离边界面。
84.即,在本发明中,通过使用粘合衬,能够在构成纤维结构体的纤维层单层的剥离强度以下的区域(范围)中,再现任意的剥离强度。此外,导电性粘液作为不具有在构成器官模型后的结构性强度、而仅具有流动性的液体,专用于对本器官模型赋予导电性。而且,如上述试验的情况般,在当使用粘液时剥离强度下降的情况下,最好能考虑到该情况来调整上述粘合衬的粘合强度。
85.(导电性粘液的功能)在本发明中,经过纤维材料结构体的制造工序,最后使导电性粘液浸渗于该纤维结构体,从而使结构体的内部充满粘液,由此,完成本发明,其中,该纤维材料结构体具备多层结构,该多层结构具有上述粘合层4。
86.在本发明中,重要的是,上述导电性粘液并不是用于使上述纤维材料层2、3彼此粘合,而是专用于赋予人工器官模型以润湿性和导电性。而且,在手术操作训练中,需要将该润湿性和导电性保持一定时间以上(例如5分钟~60 分钟),因此上述导电性粘液需要具有一定的粘性。
87.即,与使水凝胶硬化而使其流动性消失,从而将其用作结构主体来模拟对象器官自身的以往的模型不同,本发明的导电性粘液不用于模拟对象器官本身。不如说,本实施方式中的导电性粘液虽是粘液,但如果具有一定程度以上的粘性(粘度),则会黏在手术刀上而妨碍手术操作的训练,因此其优选为具有流动性,例如粘性为10000cp以下。即,由于本实
施方式中的粘液必须具有流动性,因此应当表达为溶胶。
88.本发明中的导电性粘液是指:通过使液体中包含电解质、导电粒子而具有导电性的液体。而且,即使在使用本模型的训练中,本发明中的导电性粘液也必须具有指定的流动性(粘性)。
89.下面,示出为了调查适合作为本发明中使用的导电性粘液的粘度范围而进行的试验例。
90.关于凝胶、溶胶等包含高分子的粘液,其大多为非牛顿流体,具有根据测定条件不同而测得的粘度的值不同的特征。因此,本发明的发明人们为了展示对于器官模型的优选范围,对于粘度测定,采用国际上通常使用的作为单圆筒旋转粘度计的布氏粘度计,根据jis z 8803:2011规定的粘度测定方法(使用 brookfield制旋转b型粘度计,并使用spindle lv
‑
3,在转速为12rpm的条件下进行测量),在室温(摄氏17度~20度)、最大测定值设为500000cp的条件下,进行粘度的测定。
91.作为导电性粘液,以作为吸水性聚合物材料的聚丙烯酸钠为溶质,以蒸馏水为溶剂。
92.图19示出了导电性粘液的重量浓度和粘度之间的关系。
93.可以明显看出,对导电性粘液的粘度进行了指数性近似。最小值为溶液浓度0%,即为作为蒸馏水单体的粘度1cp,作为器官模型,可使用的范围的最大值为50000cp。即,可以说50000cp以下为具有足够的流动性的粘度。50000cp 以下的范围有足够的流动性,在凝胶和溶胶的连续的状态变化中,其属于溶胶领域。
94.其中,内窥镜外科的熟练专科医生所进行的器官模型评价试验的结果明显显示出,在良好的剥离操作训练中可使用的范围为140cp至20000cp的范围。此时的溶液的重量浓度为0.5%至3.0%的范围。
95.进一步进行深入评价实验的结果显示,从浸润性、膜组织的视觉识别性、触觉视觉再现性等观点出发,作为剥离操作训练的器官模型而特别优选的范围为900cp~5000cp,此时的重量浓度为0.9%至2.0%的范围。
96.导电性粘液的必要构成为具有粘液固有的流动性、和导电性。关于流动性,是指能够浸润纤维结构体,且在实施剥离操作的时间内粘液残存于纤维结构体的范围的粘度。
97.关于导电性,是指在用于手术训练的剥离操作的单极、多极电手术刀的任一种中,电极间不绝缘,即为可导通的比较低的电阻值。
98.由此,作为特别适合的粘液,有水溶胶、水凝胶、以电解质单体为溶质的溶液、乳液(emulsion)、作为天然来源的材料的蛋清、蛋清以及盐类水溶液(例如食盐水)的混合液等。
99.在本发明中,导电性粘液最好未被进一步染色,为无色且尽可能透明。这是由于,通过对纤维材料结构体(纤维材料层2、3)浸润粘液以赋予纤维结构体润湿感,能够使外科医生在视觉、触觉上将该纤维结构体识别为人体的膜组织,从而将大幅提高作为剥离操作的对象物的再现性。
100.(使用方法)接着,参照图3~图5,以用于内窥镜剥离操作训练的情况为例,对上述人工器官模型1的使用方法进行说明。
101.在这种情况下,首先,助手(第1使用者)用镊子5(钳子)夹持第1纤维材料层2并向
上方提起。由此,对上述第1纤维材料层2施加牵引力(对抗牵引)。由此,在层叠方向上排列的上部的多条纤维材料被成束提起。该纤维材料的长度方向的拉伸强度比层叠方向上的结合力更强,即剪切力具有各向异性,因此,其以在纤维材料间的空隙扩大的同时如帐篷般形成棱线的形状(图3、图4中符号6所示的三角形状)被提起。
102.即,在以往的pva制的人工器官模型中,由于弹性模量在所有方向上均等,即使被钳子5夹持并向上提起,也仅会发生局部变形,而在本发明的结构中,一根一根的纤维材料在长度方向上的弹性不足,大致不会伸长,因此,向上拉起一处时,将会以底部(foot)大幅扩展的状态(图4中符号6所示的形状) 被拉起,从而变形为三角形状。
103.接着,对于上述被提起为三角形状的部分6的高度方向的中央部分,外科医生(第2使用者)使用电手术刀7(或超声手术刀)切开第1纤维材料层2(图4 中符号8所示的线),开始剥离操作。此时,注意不要损伤第2纤维材料层3。在此,如果浸渗的凝胶的导电性不足,则无法导电,需要提高输出而施加高电压,由此会导致纤维材料焦糊。因此,需要用于确保足够的导电性的导电性凝胶。
104.作为一个技巧,外科医生可通过一次剥离操作动作,例如切开相当于底边的一半左右长度的长度(图4中符号8所示),实现高效的剥离动作。
105.在此,外科医生应当掌握的技巧有牵引力、剥离部位、剥离长度等。如果这些不适当,会导致第1、第2纤维材料层2、3损伤,因此这样的操作是不当的。
106.(第二实施方式)接着,作为具体的手术操作训练的最优例子,参照图6~8,对在作为上述第一实施方式的剥离基础模型1中配置放入模拟器官的例1’进行说明。在这个例子中,示出了配置有模拟人工血管模型10的内窥镜下静脉获取手术(evh)训练用的人工器官模型1’。
107.作为使用了该人工器官模型1’的训练对象操作的内窥镜下血管获取手术(endoscopic vessel harvest,evh),其为cabg(coronary artery bypass grafting,冠状动脉旁路移植术)中的移植物(graft)获取法,由于它的微创性,以欧美为中心,它的适用范围逐渐扩大。然而,对于该操作,在掌握适当的技能前需要具有相当的经验,另一方面,已知不适当的静脉获取操作会增大对静脉的损伤,使静脉移植物的通畅性(patency)降低,进而影响患者的长期预后,因此该操作是极其需要使用非人体模型进行训练的领域。
108.图6为表示该人工器官模型1’的各层的模式图,图7(a)为图6的a
‑
a 视图,图7(b)为其俯视图。应予说明,对于与上述基础人工器官模型1相同的结构要素,标记相同符号并省略其详细说明。图8为与该人工器官模型1’的图7 相对应的照片。
109.在该人工器官模型1’中,如图6所示,在第1、第2纤维材料层2、3 之间配置有人工血管模型10,其与配置于其上下方的粘合层4一起在厚度方向上被加压、加热而相互粘合后,利用液状凝胶湿润并固化。根据该人工器官模型1’,可使用内窥镜(endoscope scope),实现对血管模型10和纤维结构体2、3 进行剥离的操作训练。
110.此外,作为上述人工器官模型1’,也可替换上述的人工血管10,不配置人工器官,而配置天然的动物来源的器官。例如,可以考虑配置猪血管而用作心脏外科领域的冠状动脉旁路手术中的胸廓内动脉(ita,internal thoracicartery)剥离模型的例子。
111.在此,胸廓内动脉剥离为使用电手术刀、超声手术刀,用于获取移植血管的手术操作。胸廓内动脉附带分支,对其进行结扎、切断处理,以剥离、获取主管部分。
112.根据该人工器官模型1’,能够实现对应于冠状动脉旁路手术(cabg, opcab(off
‑
pump coronary artery bypass grafting))、内窥镜下冠状动脉旁路手术 (mics cab(minimally invasive coronary artery bypass grafting,微创冠状动脉旁路移植术))、机器人辅助冠状动脉旁路手术(robotic coronary artery bypass grafting) 等技术的训练。
113.(第三实施方式)如图9所示,为了呈现手术操作训练的临场感,本实施方式为在实际的动物器官12的表面上粘合上述第二实施方式的人工器官模型1’而构成的例11。作为制造方法,优选在按图9所示的顺序在动物器官12的表面层叠各层2~4、10 后,进行加压、加热,然后,使用液状凝胶使其整体湿润,但也可仅将上述第二实施方式中完成的人工器官模型1’粘合于动物器官12上。图10、11为此人工器官模型11的外观图。
114.图12为心脏外科医生将该人工器官模型11视为胸廓内动脉(ita)而使用电手术刀进行剥离的情况。虽然在该图中难以识别,但通过根据染色识别不同层、根据纤维结构进行牵引,由此实现有效的训练。
115.(第四实施方式)本实施方式的人工器官模型1”如图13、图14所示,它是在上述第一~第三实施方式的人工器官模型1、1’的基础上发展出的、内窥镜下乙状结肠模型。
116.图15以及图16分别是从图14的a
‑
a线以及b
‑
b线处切断该人工器官模型1”的剖视图。在此例子中,具有5个纤维材料层14~18,各层14~18被染成相邻层彼此颜色不同,并经由未图示的粘合层而层叠。
117.而且,在各纤维材料层14~18之间适当配置有s形肠道19、输尿管 20、血管21、神经22等手术训练中的目标器官。这些目标模拟器官为不能损伤、应当摘除、不能触摸等的对象,与各纤维材料14~18层适度地粘合。此外,图中23所示为脂肪层。
118.应予说明,在本发明中,如本第四实施方式所示,多个纤维材料层也可为彼此大小、厚度不同。此外,关于粘合范围,未必一定要将纤维材料层彼此整体粘合,也可部分地粘合。在这种情况下,优选根据上述粘合层应当覆盖的范围,切割成适宜的形状使用。
119.(第四实施方式的制造工序)接着,对用于具体制造上述第四实施方式所涉及的器官模型的工序进行说明。
120.图20为表示本实施方式的具体制造工序的流程图。
121.应予说明,表示各工序的四方框内所示的数字为表示工序的编号,与下文中适当参照的工序编号一致。
122.(1)工序1.对纤维(纤维材料)进行染色的工序在工序1中,根据各纤维材料14~18所代表的层,将作为上述纤维材料层 14~18的纤维聚集体染成所期望的颜色。具体而言,通过如下般将纤维在染料中浸渍指定时间来进行。
123.1)在容器中蓄积7l的60℃的温水,在其中溶解用于染色的染料。
124.2)投入上述纤维聚集体,使其整体吸收染料。
125.3)经过15分钟左右后,翻转,再放置15分钟。
126.4)最后水洗除去多余的染料,使各纤维聚集体完全干燥。
127.(2)工序2.将纤维以及粘合衬切割成所期望的形状的工序在工序1中,根据各纤维材料层所代表的层,将作为纤维材料层14~18的纤维聚集体切割成形为所期望的形状。具体而言,通过如下般用激光将纤维切断来进行。
128.1)用激光对在上述染色工序中被染成黄色的“纤维1”、在同工序中被染成桃红色的“纤维2”以及“粘合衬”进行切割,制成组装部分。
129.2)测量未进行染色的“纤维3”、“纤维4”以及“粘合衬”的尺寸,使用辊式切割机(roll cutter)进行切割,制成组装部分。
130.在此,由于纤维与粘合衬一对一对应,因此将粘合衬切割成与纤维相同的形状。
131.(3)工序3.目标器官的制作工序在工序3中,用有机硅制成上述s形肠道、输尿管、血管、神经(对应于上述符号19~22)等手术训练中的目标器官。
132.1)准备各器官专用的金属模具,在其中倒入有机硅,制作血管 (ima(inferior mesenteric artery,肠系膜下动脉)、imv(inferior mesenteric vein,肠系膜下静脉)、性腺动静脉)、腹下神经(hypogastric nerve)、输尿管。
133.2)接着,将无纺布以螺旋状缠绕于上述制成的各器官,进行提高其与纤维材料层的粘合性的处理。
134.(4)工序4.器官模型的组装工序在工序4中,将在上文中制成的纤维材料层14~18与目标器官19~22相互粘合,如图21、图22所示,组装器官模型。具体实施以下工序。
135.1)将“肠道”用的相同形状的部分重叠,通过粘合衬固定。
136.2)通过缝纫机将“肠道周围脂肪”部分缝合于“肠道”。
137.3)通过缝纫机将“肠道”缝合为筒状。
138.4)通过粘合衬将“肠道下弹性脂肪_proximal”“肠道下弹性脂肪_distal”固定于“肠道”。
139.5)通过手缝将“血管模型(ima)”的末梢多点缝于“肠道下弹性脂肪 _distal”,并固定位置。
140.6)通过粘合衬将“肠道周围脂肪”固定于“肠道下弹性脂肪”。
141.7)通过粘合衬将“直肠固有筋膜_肠系膜后叶侧”固定于“肠道周围脂肪”。
142.8)通过粘合衬将“肠系膜后叶侧的脂肪”固定于“直肠固有筋膜_肠系膜后侧”。
143.9)在“肠系膜后叶侧的脂肪”与“直肠固有筋膜_肠系膜后侧”上形成供“血管模型(ima)”的中枢侧贯穿的孔,使“血管模型(ima)”的中枢侧穿过该孔。
144.10)将“血管模型(ima)”、“血管模型(imv)”夹于“肠系膜前叶侧的脂肪”、“肠系膜后叶侧的脂肪”之间,并通过粘合衬固定。
145.11)使“直肠固有筋膜_肠系膜前叶侧”覆盖“肠系膜头叶侧的脂肪”、“肠道周围的脂肪”,并通过粘合衬固定。由此,完成肠道单元的制造。
146.12)通过手缝分别将“血管模型(性腺动静脉)”、“输尿管”、“腹下神经”多点缝于“后腹膜”,并固定位置。
147.13)通过“后腹膜”和“腹下神经前筋膜”夹住12)的结构物,并利用粘合衬进行固定。
148.14)在“后腹膜”和“腹下神经前筋膜”上形成供“血管模型(ima)”的中枢侧贯穿的孔。
149.15)通过粘合衬将在上述11)中完成的肠道单元固定于“腹下神经前筋膜”。此时,使“血管模型(ima)”的中枢侧穿过在14)中开口的孔。
150.16)通过手缝将“血管模型(ima)”、“腹下神经”缝于“后腹膜”并进行固定。(或用订书机进行固定)17)通过粘合衬将“肠系膜外侧脂肪_外侧”、“肠系膜外侧脂肪_内侧”固定于肠道单元上。
151.18)通过粘合衬将相同形状的纤维固定于“后腹膜”下。
152.19)通过手缝将“肠道”的末梢部缝合固定于“后腹膜”。
153.20)切掉从模型中露出的结构物(血管模型、输尿管、腹下神经)。
154.由此,能够得到如下的图21所示的层结构体(器官模型的基本结构体)。
155.(5)工序5.模型固定框的制作工序在工序5中,准备用于使在工序4中得到的层结构物立体成形的固定框(图 23、24)。
156.1)首先,将不锈钢平纹金属网切割成30cm
×
40cm。
157.2)出于安全考虑,在切口贴上胶带(图24)。
158.3)将其按压于石膏制的骨盆模型内腔模具来制作形状(图23)。
159.(6)工序6.模型的固定工序在工序6中,将在工序4中组装成的器官模型固定于在工序5中准备的模型固定框。
160.1)首先,将器官模型与金属网合在一起,确定固定位置。
161.2)隔着金属网,用魔术笔标记固定处。
162.3)暂时从金属网上取下模型,在标记处系线。
163.4)利用系于上述模型的线,将模型固定于金属网。
164.5)切掉多余的线。
165.(7)工序7.增加器官的工序在工序7中,在直肠的z轴方向上部增加具有膀胱功能的结构体。
166.1)将纤维2切割成15cm
×
20cm左右的大小。
167.2)通过手缝将上述纤维缝于直肠附近的不锈钢平纹金属网。
168.(8)工序8.通过导电性粘液进行浸润的工序在工序8中,进行作为最终工序的利用导电性粘液进行的湿润。可根据用途选择导电性粘液的种类。在此,将通常使用的粘液按照种类区分为工序a、工序b。工序8
‑
1a粘液混合、配合子工序a(水溶胶)
169.1a)首先,称量“胶凝剂(聚丙烯酸钠)”和“甘油”,将它们混合(溶液a)。2a)将“碳酸氢钠”、“杀菌剂”与“自来水”混合(溶液b)。3a)在溶液b中倒入溶液a,立即搅拌混合。
170.4a)通过离心搅拌消泡器进行搅拌消泡。工序8
‑
1b粘液混合、配合子工序b(天然来源的蛋清食盐水混合液)1b)称量蛋清。
2b)称量并制备10wt%的食盐水。3b)相对于10份蛋清,混合5份10wt%的食盐水。4b)通过离心搅拌消泡器进行搅拌脱泡。工序8
‑
2向乙状结肠模型倒入、刷涂的工序
171.5)将上述工序8
‑
1a或b中得到的导电性粘液倒入乙状结肠模型,并用手或刷子刷涂于纤维层。
172.6)优选将模型在上述粘液中放置一晚左右。放置后的状态中的优选粘液粘度为1210cp。应予说明,该粘度的设定可通过调整聚丙烯酸钠、甘油、碳酸氢钠、水的配合比例来进行,本发明中的粘度的优选的下限以及上限为上述值。
173.由此,完成第四实施方式所涉及的乙状结肠模型。
174.应予说明,在本实施方式中,导电性粘液必须为具有流动性的溶胶,不能是相反地失去了流动性的固体凝胶。在上述工序8
‑
1a、工序8
‑
1b中,导电性粘液均被定义为水溶胶,这可通过滤纸的透过实验来证明。例如,将作为对象的导电性粘液倒入如咖啡滤纸般的滤纸,静置。可确认到本实施方式中使用的粘液在数分钟左右内透过滤纸。这与对作为模型的主要结构体的纤维结构体进行浸润的浸润性能同义。另一方面,确认了水凝胶、有机凝胶、醇凝胶等不透过滤纸的凝胶作为本实施方式中使用的导电性粘液并不优选这一点。(9)工序9.对完成的器官模型进行捆包的工序在工序9中,如图25所示,用包装膜(wrap)将通过工序8的导电性粘液的湿润而完成的人工器官模型封装,使粘液不干燥且不固化。
175.1)用包装膜包裹浸润了凝胶的模型。或者,也可用真空包装袋进行包装。
176.2)将用包装膜(真空包装袋)包裹的模型放入塑料袋并封口。
177.3)出于防止导电性粘液泄漏、防止金属网变形的考虑,放入收纳盒 (container box),并盖上盖子。由此,能够有效地防止干燥或固化。
178.由此,能够防止导电性粘液的流出、蒸发、干燥,维持所期望的湿润状态。
179.图26表示这样制造出来的人工器官模型的使用形态。
180.在使用上述人工器官模型时,从收纳盒中取出该人工器官模型,去掉塑料袋以及包装膜以解除封装状态。最好在即将开始进行手术操作的训练前,解除该封装状态。由此,上述导电性粘液带来的润湿性和导电性在手术操作训练中可保持一定时间以上(例如5分钟~60分钟)。
181.应予说明,本发明不限定于上述一个实施方式,自不必说,在不改变发明的主旨的范围内可进行各种变形。
182.例如,上述一个实施方式的粘合层为粘合衬,但不限于此。只要是多孔质材料,也可由其他的材料成形而成。此外,只要是不妨碍导电性粘液的流通性的结构,也可通过粘合剂直接将纤维材料层彼此粘合。符号说明
183.1...人工器官模型2...第1纤维材料层
3...第2纤维材料层4...粘合层5...镊子(钳子)6...三角形部分7...电手术刀10...模拟人工血管模型11...第三实施方式的人工器官模型12...动物器官14~18...纤维材料层19...s形肠道20...输尿管21...血管22...神经
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1