以香兰素为还原剂制备液态纳米银的方法与流程
本发明涉及金属粉末的化学制造技术领域,具体涉及以香兰素为还原剂制备液态纳米银的方法。
背景技术:
目前,植物组织培养技术自用于科学研究和生产实践以来取得了显著的经济效益和社会效益。但是植物组织培养技术产业化过程中,微生物污染问题频发,造成人力、物力和财力的巨大浪费。导致植物组培污染的主要原因是霉菌、细菌和酵母菌抑制失败或者效果太差。传统植物组培抑菌剂主要有氯化汞、次氯酸钠、漂白粉、酒精等[1]。但是氯化汞容易给环境造成污染;漂白粉容易吸潮;酒精不能达到彻底的灭菌,必须结合其它药剂才可以灭菌。
纳米银具有强效杀菌、无耐药性、广谱抗菌等特点。现有研究发现,纳米银微粒可杀死细菌、真菌以及支原体、衣原体等致病微生物,尤其对杆菌、球菌、丝菌的杀灭效果远远超过传统的银离子杀菌剂[2-3]。纳米银的制备主要包括物理法、化学法以及生物法。
化学法制备纳米银一般需要三个组成因素:金属银的前驱体、还原剂和稳定剂(保护剂)。银的前驱体提供银离子,为氧化剂。在多种的金属银前驱体中,硝酸银因其化学形式稳定,价格低廉而使用广泛。不同还原剂的还原能力不仅会影响纳米银的合成效率,还会影响纳米银终产物的稳定性、形貌和尺度,进而影响所得材料的应用活性。其中,硼氢化钠、柠檬酸三钠、次磷酸钠为常用的还原剂,十二烷基硫酸钠、十六烷基三甲基溴化铵、聚乙烯吡啰烷酮为常用的稳定剂[4]。例如,郑蕾[5]以硼氢化钠为还原剂制备出了液态纳米银溶液,并将溶液应用到植物组培污染防治中。然而,这种方法存在纳米银杂质含量较高、粒径分布宽、易团聚等问题。
技术实现要素:
发明人考虑到现有技术的上述情况而作出了本发明,本发明通过新颖、安全的化学过程,经过对实验条件的优化,合成尺寸较小、粒度均匀、可在体系中稳定存在的液态纳米银。
本发明以食品添加剂香兰素为还原剂,选择ctab或pvp为稳定剂,通过对实验条件的优化,能够制备出性能优异的液态纳米银产品。此外,本实验所选用的食品添加剂香兰素通常用于奶茶咖啡的增香,作为化学原料参与反应,尤其是液态纳米银合成尚属首例,开创了香兰素在化学合成领域应用的先河。
根据本发明的实施例,提供了一种以香兰素为还原剂制备液态纳米银的方法,其特征在于包括以下步骤:步骤1、在硝酸银溶液中加入稳定剂;步骤2、在磁力搅拌器的作用下搅拌并升温至40℃至60℃之间;步骤3、继续加入含香兰素的氢氧化钠溶液,使硝酸银和香兰素的摩尔比控制在1:15至1:25;步骤4、继续搅拌,得到液态纳米银产物。
本发明具有的优点和有益效果包括:
1、制备所得液态纳米银抗菌效果优异,尤其对枯草芽孢杆菌的抑菌率达到了81.2%,对黑曲霉的抑菌率也达到了100%,有效抑菌时长可达30天;
2、作为还原剂的香兰素,通常只是用于食品增香,作为化学原料参与反应,尤其是液态纳米银合成尚属首例,开创了香兰素在此领域应用的先河,为香兰素在更多领域的应用探索提供了参考;
3、制备方法简单易行,符合绿色化学理念。
附图说明
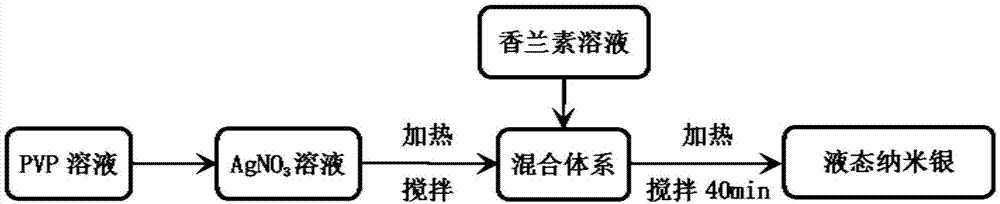
图1为根据本发明的实施例的以香兰素为还原剂制备液态纳米银的方法的实验流程示意图。
具体实施方式
下面,结合附图对技术方案的实施作进一步的详细描述。
本领域的技术人员能够理解,尽管以下的说明涉及到有关本发明的实施例的很多技术细节,但这仅为用来说明本发明的原理的示例、而不意味着任何限制。本发明能够适用于不同于以下例举的技术细节之外的场合,只要它们不背离本发明的原理和精神即可。
另外,为了避免使本说明书的描述限于冗繁,在本说明书中的描述中,可能对可在现有技术资料中获得的部分技术细节进行了省略、简化、变通等处理,这对于本领域的技术人员来说是可以理解的,并且这不会影响本说明书的公开充分性。
下面结合附图对具体实施方案进行详细描述。
根据本发明的实施例,以抗坏血酸为还原剂制备液态纳米银的方法主要包括溶液配制和制备实验两个阶段。
其中,溶液配制阶段包括:
1)配制硝酸银溶液,其浓度可为0.00025~0.00075mol/l;
具体地,先配置硝酸银母液,称取0.10g硝酸银溶于盛有120ml去离子水的棕色试剂瓶中,贴签,避光保存,
如需浓度为0.0005mol/l,则向盛有27ml去离子水的烧杯中加入3ml硝酸银母液,作为硝酸银使用液;
2)配置氢氧化钠溶液,其浓度可为0.08至0.12mol/l:
如需浓度为0.1mol/l,则称取氢氧化钠0.40g,加去离子水溶解后,转移到带橡胶塞试剂瓶,加水使总量为100ml,贴签备用;
3)配制稳定剂(pvp溶液),其浓度可为5~10mg/ml;
如需浓度为7.5mg/ml,则称取聚乙烯吡啰烷酮0.15g,溶于盛有20ml去离子的烧杯中;
4)配制香兰素溶液,其浓度可为1.5~2.5mg/ml;
作为示例,可称取香兰素0.3g,用0.1mol/l的氢氧化钠溶液溶解后,转移至带橡胶塞的试剂瓶,加水至总量为200ml,得到0.01mol/l的香兰素溶液,贴签备用。
图1为根据本发明的实施例的以抗坏血酸为还原剂制备液态纳米银的方法的实验流程示意图。
如图1所示,制备实验阶段包括:
在盛有30ml硝酸银使用液(0.0005mol/l,含硝酸银0.000015mol)的烧杯中加入2ml的pvp溶液(含聚乙烯吡啰烷酮0.015g),在磁力搅拌器的作用下搅拌并升温至50℃,逐滴向体系中加入30ml香兰素(0.01mol/l,含香兰素0.0003mol)的naoh溶液,搅拌反应40min,得到液态纳米银产物。
其中,上述流程中的各个实验条件仅为示例,并非限定选择范围。各个实验条件的范围可如下选定,以便获得最优效果。
1)物料比(硝酸银/香兰素):保持体系其他试剂用量及实验条件不变,仅改变还原剂香兰素的用量,利用紫外分光光度计对其进行表征测试;
随着香兰素用量的增大,有明显的波峰产生,说明已经制备出了纳米银溶液。在硝酸银与香兰素的物料比为1:20时,有尖锐的波峰产生,即纳米银粒子尺寸小,粒径分布较窄。随之硝酸银和香兰素物料比逐渐增大,吸收峰红移,粒径逐渐增大,纳米粒子的密度增大。故制备粒径最小纳米银粒子的硝酸银与香兰素的优选物料比为1:15~25,此时得到的纳米银粒子粒径小,产率高。
2)搅拌时间:保持体系其他试剂用量及实验条件不变,仅改变搅拌时间,利用紫外分光光度计对其进行表征测试;
当搅拌时间为30min时,有波峰产生,标志着已有纳米银溶液生成,30min的搅拌时间为此法制备纳米银溶液的最低搅拌时间。随着搅拌时间的增加,吸收强度先增大后降低,当搅拌时间达到40min时,达到吸收强度的最大值,所以用香兰素还原制备纳米银所需的搅拌时间优选为35~45min。
3)pvp用量:当pvp的用量从0.1g增加至0.15g时,纳米银的吸收峰变得越来越强。这说明增加pvp的用量使得反应易于进行。其原因是:在此反应过程中,pvp不仅充当了保护剂,同时也是还原剂。因此在加大其用量时,使得ag+更加易于还原成ag。因此吸收峰强度逐渐增强。而当pvp的用量从0.15g增加至0.175g甚至0.2g的时候,吸收峰强度逐渐减弱,其原因是当pvp的用量过大的时候,pvp大量附着在已经生成的银晶核上,使得[ag(nh3)2]+络合离子无法将还原后的ag附着在晶核上,使其继续长大,同时其它已经形成的银颗粒在长大到一定尺寸后,不再增长,对纳米银的产生和粒径都起着抑制的作用。故制备纳米银粒子的优选pvp用量为0.12~0.18g(2ml)。
4)合成温度:保持体系各组配比不变,搅拌时间一定,在室温20.4℃下制备纳米银,当搅拌时间达到40min时,体系并没有任何颜色变化,但放置12小时后,体系变成了黄色溶液,并对其用紫外可见分光光度计进行检测,发现其在430nm处有明显的吸收峰,峰形尖锐,说明粒径分布均匀,所制备的纳米银溶液稳定。12小时的反应时间过于长久,不适合生产应用,每升高10℃,反应速率生高2-4倍。
在30℃、40℃、50℃、60℃的范围内,随着温度的上升,明显的吸收峰在逐渐生成,当温度升到50℃时,有最强的吸收峰,此温度为制备纳米银的最适温度。这是由于温度较低时,还原剂对于银离子的还原速率相对较低,纳米银颗粒成核的数量较少,颗粒间相互作用的时间延长,这种情况下升高温度,用于银晶粒生长的银离子会形成大量晶核,在晶核上生长的银离子浓度随之减小,从而形成大量粒径较小的纳米银晶粒,而稳定剂pvp的存在又能从一定程度上缓解颗粒之间的团聚效应。因此,在一定范围内升高温度有利于形成粒径较小的纳米银粒子。但是,如果温度继续升高,溶液中粒子的布朗运动加速,生成的纳米银粒子间不断发生碰撞,会产生纳米银颗粒团聚的现象。因此,故制备纳米银粒子的优选温度为40至60℃。
当将纳米银用于抑菌时,其菌种主要包括大肠杆菌、金黄色葡萄球菌和黑曲霉,而所用培养基通常采用lb培养基和pda培养基。在本发明的研发过程中,通过将液态纳米银在传统的lb、pda培养基中进行枯草芽孢杆菌和黑曲霉抑制实验,然后优化纳米银合成,最终将纳米银应用于组培专用的ms培养基,并验证了纳米银对枯草芽孢杆菌以及黑曲霉菌的抑制效果。
经过实验验证,上述香兰素法制备的纳米银对枯草芽孢杆菌的抑菌率达到了81.2%,对黑曲霉的抑菌率也达到了100%。
最后,本领域的技术人员能够理解,对本发明的上述实施例能够做出各种修改、变型、以及替换,其均落入如所附权利要求限定的本发明的保护范围。
参考文献列表
[1]周俊辉,李宏彬,杨耀强等.植物组织培养中污染的鉴定与防止初步研究[j].微生物学杂志,2002(02)
[2]周梦琼,张丽敏,陈铭德.纳米银颗粒抗菌性能的实验探究活动[j].生物学教学,2011,36(7):10一19
[3]刘芳.纳米银抗菌材料的制备及其抗菌性能研究[j].中国消毒学杂志,2012,29(12):1089-1090.
[4]刘敏,胡嘉想,秦光和等.纳米银抗菌凝胶剂的毒理学评价[j].中国消毒学杂志,2010,27(3):260-261.
[5]郑蕾,纳米银在植物组培污染防治中的应用[d],安徽农业大学,103624。
- 还没有人留言评论。精彩留言会获得点赞!