一种电池正极片浸出液中同步回收镍钴锰的方法与流程
1.本发明属于有色金属湿法冶金、资源回收领域,涉及一种电池正极片浸出液中同步回收镍钴锰的方法。
背景技术:
2.近年来,随着信息化自动化、5g等电子技术的不断发展,人工智能、智能制造、新能源汽车等产业已经成为我国经济增长的新引擎,也是实现经济高质量发展的重要驱动力。而驱动其发展的核心就是电池系统,随着电池的需求不断扩大,相关原材料必然愈发紧缺,此外如何做到对报废电池中的有价金属进行绿色高效回收也成为世界发展进程中需要解决的难题。
3.利用湿法冶金技术对废旧锂离子电池中的有价金属进行回收是目前最行之有效的办法,但是受限于湿法冶金技术及原料的原因,其回收流程基本沿用传统冶矿方面的技术,该套技术对于电池回收来说流程长、污染大,并不是最好的回收工艺。
4.cn105483382a公开了一种含镍钴锰的废电池材料浸出液的分离回收方法,其使用三烷基羟肟酸作为第一萃取剂将含镍钴锰锂的电池浸出液中的镍和钴萃取至有机相中,达到与锰和锂分离的目的;使用硫酸或盐酸对有机相进行反萃得到镍钴溶液,再使用第二萃取剂对含镍钴的溶液进行萃取,将钴萃取至有机相中,使镍钴分离;再使用第三萃取剂对含锰锂的溶液进行萃取,将锰萃取至有机相中,达到锰与锂分离的目的。通过三次萃取分别使镍钴与锰锂分离、镍与钴分离、锰与锂分离。其流程复杂,采用多次萃取操作,使用多种不同的萃取剂会造成萃取剂相互溶解影响萃取性能。
5.cn107653378a公开了一种废旧镍钴锰锂离子电池中有价金属的回收方法,其将废旧锂离子电池拆解后置于酸溶液中浸泡,得到含镍钴锰锂等有价金属和铜铝的浸出液,再使用铁置换除铜,水解除铁铝后得到镍钴锰锂的溶液,再按照前驱体要求的比例配入所缺的元素使溶液总金属浓度70~100g/l左右,再王其中加入碱和氨水合成镍钴锰前驱体。其采用沉淀法将铁、铜等杂质去除,再通过按照配比添加镍钴锰使溶液中镍钴锰的含量符合前驱体要求,再使用碱沉淀得到镍钴锰前驱体。使用沉淀法回收会导致有价离子回收率偏低,部分杂质去除不干净,得到的前驱体纯度不够等情况,而且该流程产生的各种滤渣后处理麻烦,不符合绿色化学特征。
6.cn109207727a公开了一种从废旧镍钴铜三元锂离子电池回收制备金属材料的方法,其先对废旧锂离子电池进行拆解、浸出得到含铜、锂、镍、钴的浸出液,浸出液经过除杂后得到除杂液,使用没有萃取体系进行分馏萃取得到有机相和富镍萃余液,用盐酸对有机相进行反萃,得到含钴反萃液,并在钴和锂的反萃液中加入碱性物质,分离钴和锂,再用硫酸对反萃钴后的有机相进行反萃,得到含铜反萃液,将富镍萃余液进行萃镍处理得到富镍有机相,在对富镍有机相进行反萃,回收镍。其流程经过除杂、萃钴锂、两步反萃得到钴和铜,再萃取富集镍最终将镍钴锂铜回收。其工艺路线流程长且复杂,经济效益低。
7.上述方案存在有工艺流程复杂、回收率偏低或得到的前驱体纯度低等问题,因此,
开发一种工艺流程简单、成本低且回收率高的在电池正极片浸出液中同步回收镍钴锰的方法是十分必要的。
技术实现要素:
8.本发明的目的在于提供一种电池正极片浸出液中同步回收镍钴锰的方法,本发明通过在第二步萃取中采用bc194萃取剂能将镍钴锰同步萃取,并且萃取率高,与杂质离子分离效果好;水溶性低,对环境友好,实际使用过程中损耗少,浓度组分变化不大;反萃率高,可达到镍钴锰的高效回收;反萃后的有机相可循环使用,运营成本低,经济效益高。
9.为达到此发明目的,本发明采用以下技术方案:
10.本发明提供了一种电池正极片浸出液中同步回收镍钴锰的方法,所述方法包括以下步骤:
11.(1)使用萃取剂a对正极片浸出液进行第一步萃取,得到负载有机相1和萃余水相1;
12.(2)使用羧酸类萃取剂b对步骤(1)得到的萃余水相1进行第二步萃取,得到负载有机相2和萃余水相2;
13.(3)对步骤(2)得到的负载有机相2进行洗涤和反萃,得到富镍、钴、锰溶液;
14.其中,步骤(2)所述羧酸类萃取剂b为bc194萃取剂,所述bc194萃取剂的结构式如下:
[0015][0016]
通过本发明提供的方法,将含镍钴锰正极片浸出液中的镍钴锰实现同步回收,且不受钙、镁等杂质金属离子的影响,操作简单,工艺运行稳定,降低了分别回收镍、钴、锰的分离成本及萃取除杂的净化成本。同时,本发明在步骤(2)中通过采用特定的羧酸类萃取剂,其实现了除杂率及对ni、co、mn提取率均达99.0%以上,硫酸反萃率大于99.5%。
[0017]
本发明所述浸出液中li的浓度为1~20g/l,例如:1g/l、5g/l、8g/l、9g/l、10g/l、11g/l、12g/l、15g/l、18g/l、19g/l或20g/l等。
[0018]
本发明所述浸出液中ni的浓度为1~60g/l,例如:1g/l、10g/l、20g/l、30g/l、40g/l、41g/l、42g/l、43g/l、44g/l、45g/l、46g/l、50g/l、55g/l或60g/l等。
[0019]
本发明所述浸出液中co的浓度为1~25g/l,例如:1g/l、5g/l、15g/l、16g/l、17g/l、18g/l、19g/l、20g/l、21g/l、22g/l、23g/l、24g/l或25g/l等。
[0020]
本发明所述浸出液中mn的浓度为1~20g/l,例如:1g/l、5g/l、10g/l或20g/l等,但不限于所列举的数值,该范围内其他未列举的数值同样适用。
[0021]
本发明所述浸出液中fe浓度≤5g/l,例如:0.1g/l、0.5g/l、1g/l、3g/l、4g/l或5g/l等。
[0022]
本发明所述浸出液中al浓度≤1g/l,例如:0.2g/l、0.4g/l、0.6g/l、0.8g/l或1g/l等。
[0023]
本发明所述浸出液中cu浓度≤10g/l,例如:1g/l、3g/l、5g/l、6g/l、7g/l、8g/l、9g/l或10g/l等。
[0024]
本发明所述浸出液中zn浓度≤5g/l,例如:0.1g/l、0.5g/l、1g/l、3g/l、4g/l或5g/l等。
[0025]
本发明所述浸出液中ca浓度为0.1~0.5g/l,例如:0.1g/l、0.2g/l、0.3g/l、0.4g/l或0.5g/l等。
[0026]
本发明所述浸出液中mg浓度为0.1~50g/l,例如:0.1g/l、10g/l、20g/l、30g/l、40g/l或50g/l等。
[0027]
优选地,步骤(1)所述第一步萃取的萃取剂a包括膦类萃取剂、肟类萃取剂或羧酸类萃取剂中的任意一种或至少两种的组合,优选为羧酸类萃取剂。
[0028]
优选地,所述羧酸类萃取剂的结构通式如下:
[0029][0030]
其中,10≤m+n≤22。
[0031]
优选地,所述c
nh2n+1
为碳原子数为1~21,(例如:1、3、5、7、9、14、16、18或21等)的直链或支链的烷基。
[0032]
优选地,所述c
mh2m+1
为碳原子数为1~21(例如:1、3、5、7、9、14、16、18或21等)的直链或支链的烷基。
[0033]
本发明所述膦类萃取剂包括p204、p507或c272中的任意一种或至少两种的组合。
[0034]
本发明中,若浸出液中含有铜离子,则第一萃取中优先选用肟类萃取剂来除去浸出液中的铜。
[0035]
本发明所述肟类萃取剂包括mextral 984h、lix984n、lix63或cp50中的任意一种或至少两种的组合。
[0036]
优选地,所述萃取剂a与所述的浸出液的体积比为(0.1~10):1,例如:0.1:1、0.5:1、1:1、2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1或10:1等。
[0037]
优选地,步骤(1)所述萃取剂a还包括稀释剂。
[0038]
优选地,所述稀释剂包括磺化煤油、十二烷、煤油、escaid110、己烷或庚烷中的任意一种或至少两种的组合。
[0039]
优选地,步骤(1)所述萃取剂a在萃取前还需要进行皂化处理。
[0040]
优选地,所述皂化处理的皂化剂为碱性溶液。
[0041]
优选地,所述碱性溶液包括氢氧化钠、氢氧化钾或氨水中的任意一种或至少两种的组合。
[0042]
优选地,所述碱性溶液的浓度为6~14mol/l,例如:6mol/l、7mol/l、8mol/l、9mol/l、10mol/l、11mol/l、12mol/l、13mol/l或14mol/l等。
[0043]
优选地,步骤(1)所述的第一步萃取的方法包括单级萃取和/或多级逆流萃取,优选为多级逆流萃取。
[0044]
优选地,所述第一步萃取中的搅拌转速为100~300r/min,例如:100r/min、120r/min、140r/min、160r/min、180r/min、200r/min、210r/min、230r/min、250r/min、270r/min或300r/min等。
[0045]
优选地,所述第一步萃取中混合的时间为3~30min,例如:3min、6min、9min、10min、15min、18min、20min、22min、26min、27min或30min等。
[0046]
优选地,所述第一步萃取中静置分相的时间为5~60min,例如:5min、10min、15min、20min、30min、40min、50min或60min等。
[0047]
优选地,所述多级逆流萃取的萃取级数为2~30级,例如:2级、5级、10级、15级、20级、25级或30级等。
[0048]
优选地,步骤(1)所述第一步萃取后得到的负载有机相1需经过洗涤处理和反萃处理后得到含铁、铝、铜、锌离子溶液和空白有机相1。
[0049]
优选地,所述洗涤处理的级数为2~20级,例如:2级、4级、6级、10级、15级、18级或20级等。
[0050]
优选地,所述洗涤处理使用的洗涤剂为酸溶液。
[0051]
优选地,所述酸溶液包括稀硫酸和/或盐酸溶液。
[0052]
优选地,所述酸溶液的ph值为0.1~4,例如:0.1、0.5、1、2、3或4等。
[0053]
优选地,所述反萃处理的级数为1~6级,例如:1级、2级、3级、4级、5级或6级。
[0054]
优选地,所述反萃处理使用的反萃剂为酸溶液。
[0055]
优选地,所述酸溶液包括稀硫酸和/或盐酸溶液。
[0056]
优选地,所述酸溶液的h
+
浓度为4~8m,例如:4m、5m、6m、7m或8m等。
[0057]
优选地,所述空白有机相1作为萃取剂重复使用。
[0058]
本发明中,第一萃取的ph值的作业ph值由于萃取剂不同会有不同的ph值作业区间,本发明中不做具体限定,可参照现有技术中第一萃取中所去除的杂质离子进行选择,如采用p204时,第一萃取的ph值为2.5~3.5,采用肟类萃取剂时,第一萃取的ph值为2~2.5。
[0059]
优选地,步骤(2)所述bc194萃取剂在萃取有机相中的体积分数为5~30%,例如:5%、8%、10%、15%、20%、25%或30%等。
[0060]
优选地,所述bc194萃取剂还包括稀释剂。
[0061]
优选地,所述稀释剂包括磺化煤油、煤油、十二烷、己烷、庚烷或escaid110中的任意一种或至少两种的组合。
[0062]
优选地,所述bc194萃取剂使用前应进行皂化处理。
[0063]
优选地,所述皂化处理的皂化剂为碱性溶液。
[0064]
优选地,所述碱性溶液包括氢氧化钠、氢氧化钾或氨水中的任意一种或至少两种的组合。
[0065]
优选地,所述碱性溶液的浓度为6~14mol/l,例如:6mol/l、8mol/l、10mol/l、11mol/l、12mol/l、13mol/l或14mol/l等。
[0066]
优选地,步骤(2)所述的第二步萃取的方法包括单级萃取和/或多级逆流萃取,优选为多级逆流萃取。
[0067]
本发明中,所述逆流萃取是萃取分离操作法之一,含有被萃取物的水相及有机相分别从萃取器的两端流入,以相反方向流动,进行连续多级搅拌接触分层而达到分离的目的。
[0068]
优选地,所述第二步萃取中的搅拌转速为100~300r/min,例如:100r/min、120r/min、140r/min、160r/min、180r/min、200r/min、210r/min、230r/min、250r/min、270r/min或
300r/min等。
[0069]
优选地,所述第二步萃取中混合的时间为3~30min,例如:3min、6min、9min、10min、15min、18min、20min、22min、26min、27min或30min等。
[0070]
优选地,所述第二步萃取中静置分相的时间为5~60min,例如:5min、10min、15min、20min、30min、40min、50min或60min等。
[0071]
优选地,所述多级逆流萃取的萃取级数为2~30级,例如:2级、5级、10级、15级、20级、25级或30级等。
[0072]
优选地,所述洗涤处理使用的洗涤剂为酸溶液。
[0073]
优选地,所述酸溶液包括稀硫酸和/或盐酸溶液。
[0074]
优选地,所述酸溶液的ph值为0.1~4,例如:0.1、0.5、1、2、3或4等。
[0075]
优选地,所述反萃处理的级数为1~6级,例如:1级、2级、3级、4级、5级或6级。
[0076]
优选地,所述反萃处理使用的反萃剂为酸溶液。
[0077]
优选地,所述酸溶液包括稀硫酸和/或盐酸溶液。
[0078]
优选地,所述酸溶液的h
+
浓度为4~8m,例如:4m、5m、6m、7m或8m等。
[0079]
本发明中,相关工序的反应方程式如下:
[0080]
羧酸类萃取剂皂化:ha
(org)
+naoh
→
naa
(org)
+h2o
[0081]
羧酸类萃取剂萃取:2naa
(org)
+mso4→
ma
2(org)
+na2so4[0082]
硫酸反萃:ma
2(org)
+h2so4→
2ha
(org)
+mso4[0083]
其中:m为fe
3+
、cu
2+
、al
3+
、zn
2+
、ni
2+
、co
2+
、mn
2+
中的任意一种或至少两种的组合。
[0084]
作为本发明的优选方案,所述方法包括以下步骤:
[0085]
(1)使用稀释剂对萃取剂a进行稀释处理,再使用6~14mol/l的皂化剂进行皂化处理;
[0086]
(2)使用步骤(1)所述皂化后的萃取剂a对正极片浸出液以100~300r/min混合3~30min,静置5~60min后得到负载有机相1和萃余水相1;
[0087]
(3)使用ph值为0.1~4酸性洗涤剂洗涤步骤(2)得到的负载有机相1,再使用h
+
浓度为4~8m的酸性反萃剂进行反萃,得到含铁、铝、铜、锌离子溶液和空白有机相1;
[0088]
(4)配制萃取有机相,其中萃取剂bc194所占萃取有机相中的体积分数为5~30%的,再使用6~14mol/l的皂化剂进行皂化处理;
[0089]
(5)用步骤(4)所述皂化后的bc194对步骤(2)得到的萃余水相1以100~300r/min混合3~30min,静置5~60min后得到负载有机相2和萃余水相2;
[0090]
(6)使用ph值为0.1~4酸性洗涤剂洗涤步骤(5)得到的负载有机相2,再使用h
+
浓度为4~8m的酸性反萃剂进行反萃,得到富镍、钴、锰溶液。
[0091]
相对于现有技术,本发明具有以下有益效果:
[0092]
(1)本发明提供的方法,对金属离子分离效果好,通过利用萃取剂及萃取ph值间的耦合作用,将含镍钴锰电池浸出液中的镍钴锰实现同步萃取回收,且不受钙、镁等杂质金属离子的影响,操作简单,降低了分别回收镍、钴、锰的分离成本及杂质金属离子的提取净化成本,此外,所采用羧酸类萃取剂水溶性小,可循环利用。
[0093]
(2)本发明提供的回收方法中除杂率≥99%,镍钴锰提取率≥99%,硫酸反萃率≥99.5%。
附图说明
[0094]
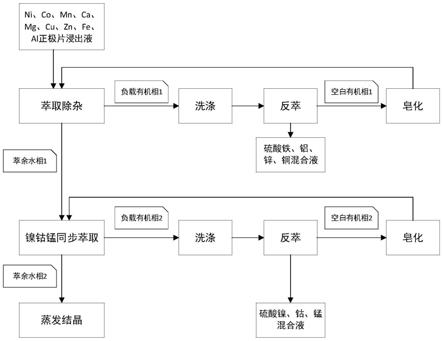
图1是本发明实施例1中回收流程的示意图。
[0095]
图2是本发明所使用到的羧酸类萃取剂bc194的e-ph曲线图。
具体实施方式
[0096]
下面通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
[0097]
本发明实施例中使用的bc194萃取剂均通过以下方法制备:
[0098][0099]
在500ml圆底烧瓶中加入吡啶二羧酸20g(0.12mol),室温搅拌下,缓慢滴加200ml二氯亚砜,温度上升说明反应发生,滴加完毕后回流反应30分钟,蒸馏除去多余的二氯亚砜。随后在烧瓶中加入二氯甲烷200ml,三乙胺25g(0.25mol),滴加对辛基苯胺24.6g(0.12mol),室温反应1小时后,停止反应。用ph=1的盐酸洗涤两次后,然后用水洗涤1次,硫酸钠干燥后旋干溶剂,得到目标产物32.1g,产率约75%。
[0100]
表征数据:
13
c nmr(101mhz,cdcl3)δ168.1(s),142.3(s),139.2(s),135.1(s),127.7(s),125.6(s),128.3(m),121.6(m),51.6(m),32.5
–
31.1(m),29.7(m),27.4(m),24.7(m),14.3(d,j=5.9hz);1h nmr(400mhz,cdcl3)δ9.86(1h),8.81(1h),8.75(1h),8.52(1h),7.58(2h),7.15(1h),2.52(2h),1.56(2h),1.27(10h),0.86(3h);ms:354.2。
[0101]
制得的萃取剂bc194的e-ph曲线图如图2所示,由图2可以看出,bc194萃取剂对ni、co、mn的萃取选择性好,在萃取平衡ph=6,ni、co、mn的萃取率可达到90%以上,同时ca、mg的萃取率小于15%,具有应用于正极片浸出液同步提取镍钴锰的优势。
[0102]
实施例1
[0103]
本实施例提供一种含镍钴锰的电池正极片浸出液中镍钴锰的回收方法,如图1所示。
[0104]
本实施例中的浸出液为含镍钴锰的电池正极片浸出液,浸出液的ph值为4.82,成分如表1所示:
[0105]
表1
[0106]
元素fealzncunicomncamgli含量(g/l)0.0010.0010.520.75118200.40.510
[0107]
本实施例中在第一步萃取之前先采用皂化后mextral984h萃取剂(体积分数为20%,稀释剂为磺化煤油,皂化剂为10.2mol/l的naoh溶液)对浸出液中的铜进行萃取,萃取级数1级,有机相与浸出液的体积比为0.5:1,混合时间为15min,搅拌速度为150r/min,静置20min,温度为室温25℃,控制水相ph为2.7,分相后分别获得负载铜有机相和除铜后浸出液,采用ph为0.8的稀硫酸对负载铜有机相进行1级逆流洗涤后,再采用3.5mol/l硫酸进行反萃1次,有机相1与洗涤液或反萃液的体积比均为10:1,获得硫酸铜溶液。
[0108]
本实施例中第一步萃取采用p204作为萃取剂,体积分数为25%,稀释剂为
escaid110,并用10.2mol/l的naoh溶液进行皂化。
[0109]
采用皂化后的p204对除铜后浸出液进行多级逆流萃取,萃取级数4级,有机相与除铜后浸出液的体积比为0.5:1,混合时间为15min,搅拌速度为150r/min,静置时间为20min,温度为室温25℃,分相后分别获得负载有机相1和ph值为3.2的萃余水相1,采用ph为0.8的稀硫酸对负载有机相1进行5级逆流洗涤后,再采用3.5mol/l硫酸进行反萃2次,负载有机相1与洗涤液或反萃液的体积比均为10:1,得到硫酸锌溶液,空白有机相1返回皂化工序循环使用。
[0110]
采用皂化后的bc194(体积分数为25%,稀释剂为escaid110,皂化剂10.2mol/l的naoh溶液)对萃余水相1进行多级逆流萃取,萃取级数15级,有机相与水相1的体积比为4:1,混合时间为15min,搅拌速度为150r/min,静置20min,温度为室温25℃,分别获得负载有机相2和ph值为6.3的萃余水相2,采用ph为0.8的稀硫酸对负载有机相2进行8级逆流洗涤后,再采用3.5mol/l硫酸进行反萃3次,负载有机相2与洗涤液或反萃液的体积比均为8:1,得到富镍、钴、锰溶液。
[0111]
本实施例中的除杂率为99.5%,ni、co及mn的提取率分别为99.9%、99.5%及99.2%,反萃率分别为99.5%、99.6%及99.6%。
[0112]
实施例2
[0113]
本实施例提供一种含镍钴锰的浸出液中镍钴锰的回收方法,本实施例中的浸出液为含镍钴锰的电池浸出液,浸出液的ph值为2.35,成分如表2所示:
[0114]
表2
[0115]
元素fealzncunicomncamgli含量(g/l)0.50.010.20.34820180.50.510
[0116]
本实施例中第一步萃取采用c272作为萃取剂,体积分数为25%,稀释剂为磺化煤油,并用13mol/l的naoh溶液进行皂化。
[0117]
采用皂化后的c272对浸出液进行多级逆流萃取,萃取级数4级,有机相与浸出液的体积比为0.4:1,混合时间为8min,搅拌速度为200r/min,实验温度为室温25℃,静置时间为10min,分相后分别获得负载有机相1和ph值为3.3的萃余水相1,采用ph为1的稀硫酸对负载有机相1进行5级逆流洗涤后,再采用2mol/l硫酸进行反萃3次,负载有机相1与洗涤液或反萃液的体积为15:1,得到得到硫酸铁、硫酸铜、硫酸锌、硫酸铝等混合溶液。
[0118]
采用皂化后的bc194(体积分数为25%,稀释剂为escaid110,皂化剂10.2mol/l的naoh溶液)对萃余水相1进行多级逆流萃取,萃取级数11级,有机相与萃余水相1的体积比为4:1,混合时间为5min,搅拌速度为200r/min,静置10min,实验温度为室温25℃,分别获得负载有机相2和ph值为6.1的萃余水相2,采用ph为1的稀硫酸对负载有机相2进行8级逆流洗涤后,再采用2mol/l的硫酸进行反萃5次,负载有机相2与洗涤液或反萃液的体积比为10:1,得到富镍、钴、锰溶液。
[0119]
本实施例中的除杂率为99.4%,ni、co及mn的提取率分别为99.8%、99.6%及99.5%,反萃率分别为99.7%、99.7%及99.6%。
[0120]
实施例3
[0121]
本实施例提供一种含镍钴锰的浸出液中镍钴锰的回收方法,本实施例中的浸出液为含镍钴锰的电池浸出液,浸出液的ph值为4.3,成分如表3所示:
[0122]
表3
[0123][0124][0125]
本实施例中在第一萃取之前先采用皂化后lix984n萃取剂(体积分数为25%,稀释剂为磺化煤油,皂化剂为11mol/l的naoh溶液)对浸出液中的铜进行萃取,萃取级数1级,相比为0.5:1,混合时间为3min,搅拌速度为200r/min,静置10min,实验温度为25℃,控制水相ph为2.6,分相后分别获得负载铜有机相和除铜后浸出液,采用ph为1的稀硫酸对负载铜有机相进行1级逆流洗涤后,再采用2mol/l硫酸进行反萃2次,有机相1与洗涤液或反萃液的体积为10:1,获得硫酸铜溶液。
[0126]
本实施例中第一萃取采用p507作为萃取剂,体积分数为20%,稀释剂为磺化煤油,并采用11mol/l的naoh溶液进行皂化。
[0127]
采用皂化后的p507对含镍钴锰的除铜后浸出液进行7级逆流萃取,萃取剂与除铜后浸出液的体积比为0.5:1,混合时间为3min,搅拌速度为300r/min,实验温度为25℃,分相后分别获得负载有机相1和ph值为2.5的萃余水相1,采用ph为1的盐酸对负载有机相1进行6级逆流洗涤后,再采用4mol/l的盐酸进行反萃2次,负载有机相1与洗涤液或反萃液的体积为15:1,得到氯化钙和氯化锌等混合溶液有机相返回皂化工序循环使用。
[0128]
采用皂化后的bc194(体积分数为30%,稀释剂为escaid 110,皂化剂11mol/l的naoh溶液)对萃余水相1进行第二次萃取,萃取级数12级的多级逆流萃取,bc194萃取剂与萃余水相1的体积比为3:1,混合时间为3min,搅拌速度为300r/min,实验温度为室温25℃,分别获得负载有机相2和ph值为7.1的萃余水相2,采用ph为1的硫酸对负载有机相2进行10级逆流洗涤后,再采用2mol/l的硫酸进行反萃6次,负载有机相2与洗涤液或反萃液的体积为9:1得到富镍、钴、锰溶液。
[0129]
本实施例中的除杂率为99.3%,ni、co及mn的提取率分别为99.8%、99.7%及99.6%,反萃率分别为99.7%、99.6%及99.5%。
[0130]
实施例4
[0131]
本实施例与实施例1的区别仅在于控制萃余水相2的ph为5.5,本实施例中的除杂率为99.3%,ni、co及mn的提取率分别为99.2%、99.0%及99.2%,反萃率分别为99.7%、99.6%及99.6%,洗涤工序降低,洗涤成本减少。
[0132]
对比例1
[0133]
本对比例与实施例1的区别仅在于第二步萃取中的萃取剂bc194替换为等量的p507,镍钴锰无法同步萃取。
[0134]
对比例2
[0135]
本对比例与实施例1的区别仅在于第二步萃取中的萃取剂bc194替换为等量的p204,镍钴锰无法同步萃取。
[0136]
对比例3
[0137]
本对比例与实施例1的区别仅在于将第二步萃取中的萃取剂bc194替换为羧酸类
萃取剂versatic 10,ni、co及mn的提取率分别为98.6%、98.4%及97.8%,水溶性高,易造成工艺不稳定,废水处理成本高。
[0138]
通过实施例1-4和对比例1-3的结果可知,本发明提供的方法,通过利用萃取剂及萃取ph值间的耦合作用,将废锂离子电池正极片浸出液中的镍钴锰实现同步萃取回收,且不受钙、镁等杂质金属离子的影响,操作简单,降低了分别回收镍、钴、锰的分离成本及杂质金属离子的提取净化成本。同时,羧酸类萃取剂除杂率≥99.0%,硫酸反萃率≥99.5%。
[0139]
申请人声明,以上所述仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,所属技术领域的技术人员应该明了,任何属于本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,均落在本发明的保护范围和公开范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1