一种选择性结合G-四链体的金纳米簇及其制备方法和应用
本发明属于金纳米簇合成与应用,具体涉及一种选择性结合g-四链体的金纳米簇及其制备方法和应用。
背景技术:
1、g-四链体是由富含鸟嘌呤的核酸分子通过分子内或分子间hoogsteen氢键连接形成的具有四股核苷酸链的dna二级结构,通常需要特定的阳离子(如钾离子)位于结构中心来进一步稳定该结构。相关研究表明,g-四链体形成基序广泛存在于动植物、细菌、病毒等的基因组中,这些基序并非随机分布于基因组上,而是存在染色体上的一些重要功能区,如端粒末端、基因启动子区域、内含子区域。这些基序折叠形成的g-四链体结构参与一系列重要生命过程,包括端粒结构维持、dna复制、基因转录/翻译、基因组稳定性维持等。此外,g-四链体还存在于rna的非编码区(包括5′端非翻译区以及3′端非翻译区)来调控一些基因的表达。最新研究表明,相较于正常细胞,肿瘤细胞具有更高的g-四链体形成水平,乳腺癌、头颈癌、胃癌、肝癌等实体肿瘤中g-四链体的含量也较正常组织高。鉴于g-四链体在肿瘤细胞/组织内高水平存在且参与肿瘤发生发展的一些重要过程(如端粒稳态维持、作为基因表达调控原件调节原癌基因表达),g-四链体是近些年发展起来的十分有潜力的抗肿瘤靶标,用于新型抗肿瘤药物的开发。
2、迄今为止,已有数量众多的化学小分子、多肽、抗体(含纳米抗体)被开发出来,用于g-四链体基序的鉴定、g-四链体结构的原位检测、细胞内g-四链体的动力学监测以及g-四链体生物学功能调节,但截至目前仅有两个小分子开展了临床实验,用于神经内分泌/类癌肿瘤、乳腺/卵巢癌的治疗。这两个小分子因为生物利用度低而被迫终止实验,这极大低估了g-四链体作为一种新型抗肿瘤靶点用于肿瘤治疗的潜能。在与g-四链体结合的分子中,化学小分子通常具有平面芳香大共轭体系,水溶性差,体内作用效果有限;多肽和纳米抗体不仅易丧失生物学活性,而且难以跨过细胞膜进入细胞内与g-四链体相结合。因此,迫切需要开发更多类型能与g-四链体相结合的分子或材料。
技术实现思路
1、本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出一种金纳米簇的制备方法。
2、本发明还提出一种上述制备方法制备得到的金纳米簇。
3、本发明还提出一种上述金纳米簇的应用。
4、本发明还提出一种含有上述金纳米簇的抗肿瘤药物。
5、根据本发明的一个方面,提出了一种金纳米簇的制备方法,所述方法包括以下步骤:将还原性谷胱甘肽、n,n,n-三甲基-(11-巯基十一烷基)氯化铵和氯金酸通过水热反应,合成得到金纳米簇。
6、在本发明的一些实施方式中,所述还原性谷胱甘肽与所述n,n,n-三甲基-(11-巯基十一烷基)氯化铵的添加摩尔比为1:(0.5~2)。
7、在本发明的一些实施方式中,所述还原性谷胱甘肽与所述n,n,n-三甲基-(11-巯基十一烷基)氯化铵的添加摩尔比为1:1。
8、在本发明的一些实施方式中,所述还原性谷胱甘肽与所述氯金酸的添加摩尔比为(1~4):(1~2)。
9、在本发明的一些实施方式中,所述还原性谷胱甘肽与所述氯金酸的添加摩尔比为2:1。
10、在本发明的一些实施方式中,所述n,n,n-三甲基-(11-巯基十一烷基)氯化铵与所述氯金酸的添加摩尔比为(1~4):(1~2)。
11、在本发明的一些实施方式中,所述n,n,n-三甲基-(11-巯基十一烷基)氯化铵与所述氯金酸的添加摩尔比为2:1。
12、在本发明的一些实施方式中,所述水热反应温度为65℃~75℃。
13、在本发明的一些实施方式中,所述水热反应时间为10-24小时。
14、在本发明的一些实施方式中,所述水热反应采用油浴或水浴。
15、在本发明的一些实施方式中,所述制备方法还包括将得到的金纳米簇置于大小为3000-3500道尔顿的透析袋中透析2-5次的步骤。
16、在本发明的一些实施方式中,所述单次透析时间不少于4小时;用于充分去除未反应的配体和氯金酸。
17、在本发明的一些实施方式中,所述制备方法还包括将透析得到的金纳米簇进行浓缩的步骤。
18、在本发明的一些实施方式中,所述浓缩方式采用离心法,所述浓缩条件为将透析后的金纳米簇溶液转移至截留分子量为3000~10000道尔顿的超滤管中,使用6000~8000转每分的转速在室温离心30至60分钟。
19、根据本发明的第二方面,提出了上述方法制备得到的金纳米簇。
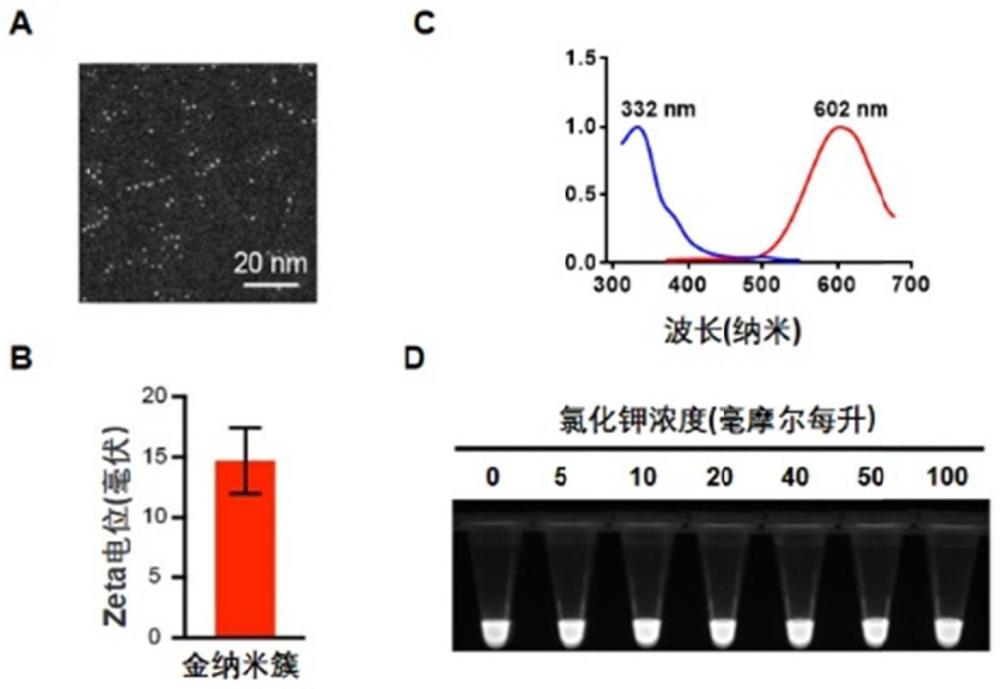
20、在本发明的一些实施方式中,所述金纳米簇的最大激发波长位于330~335纳米区间,最大发射波长位于590~605纳米区间。
21、在本发明的一些实施方式中,所述金纳米簇粒径范围为0.9~1.3纳米。
22、在本发明的一些实施方式中,所述金纳米簇平均粒径为1.1纳米。
23、在本发明的一些实施方式中,所述金纳米簇为水溶性金纳米簇。
24、在本发明的一些实施方式中,所述金纳米簇为耐受钾离子的金纳米簇。
25、在本发明的一些实施方式中,所述金纳米簇可选择性结合g-四链体dna和/或g-四链体rna。
26、在本发明的一些实施方式中,所述g-四链体dna的序列如seq idno:1、seq id no:2或seq id no:3所示。
27、在本发明的一些实施方式中,所述g-四链体rna的序列如seq idno:4所示。
28、根据本发明的第三方面,提出了上述金纳米簇的应用,所述应用为在制备抗肿瘤药物中的应用。
29、在本发明的一些实施方式中,所述肿瘤包括乳腺癌、前列腺癌、肝癌、非小细胞肺癌、脑癌、卵巢癌、子宫癌、胃癌、皮肤癌、白血病、头颈癌、结肠癌、膀胱癌、直肠癌中的至少一种。
30、在本发明的一些实施方式中,所述抗肿瘤药物还可以包括化疗药物、光敏剂或光热剂。
31、在本发明的一些实施方式中,所述化疗药物包括环磷酰胺、顺铂、鬼臼毒素、喜树碱、紫杉醇、多柔比星、表柔比星和5-氟尿嘧啶中的至少一种。
32、在本发明的一些实施方式中,所述应用为在制备c-myc基因表达抑制剂中的应用。
33、在本发明的一些实施方式中,所述应用为g-四链体结构检测中的应用。
34、根据本发明的第三方面,提出了一种抗肿瘤药物,所述抗肿瘤药物包含上述金纳米簇。
35、在本发明的一些实施方式中,所述抗肿瘤药物还可以包括化疗药物、光敏剂或光热剂。
36、在本发明的一些实施方式中,所述化疗药物包括环磷酰胺、顺铂、鬼臼毒素、喜树碱、紫杉醇、多柔比星、表柔比星和5-氟尿嘧啶中的至少一种。
37、在本发明的一些实施方式中,所述抗肿瘤药物还包括药学上可接受的辅料。
38、根据本发明的一些实施方式,至少具有以下有益效果:本发明通过以还原性谷胱甘肽作为还原剂,以n,n,n-三甲基-(11-巯基十一烷基)氯化铵作为功能配体,与氯金酸通过水热反应一步合成金纳米簇,制备方法简单,制备得到的金纳米簇为水溶性且可选择性结合g-四链体dna以及g-四链体rna,金纳米簇还可以容易进入到细胞核内与g-四链体结合,展现出抗肿瘤效果。
- 还没有人留言评论。精彩留言会获得点赞!