球形氮化铝粉末的制备方法与流程
相关申请的交叉引用本申请要求于2017年8月11日在韩国知识产权局提交的韩国专利申请no.10-2017-0102525的权益,该申请的公开内容通过引用全部并入本说明书中。本发明涉及一种球形氮化铝粉末的制备方法。
背景技术:
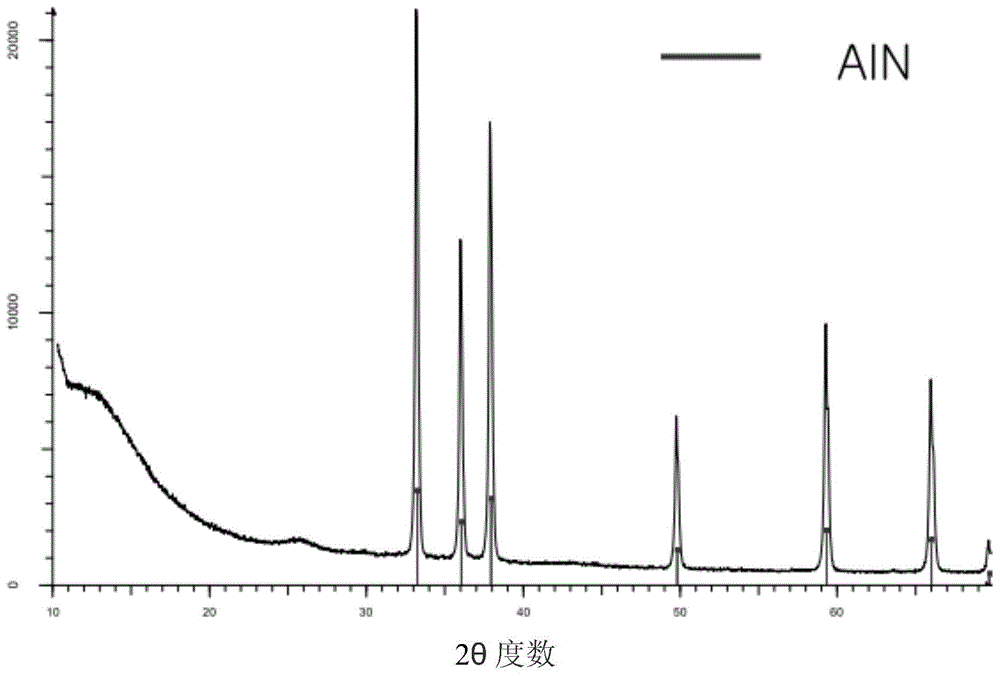
:氮化铝具有高热导率和优异的电绝缘性能,并且已经用作高导热基板、散热元件、隔热/散热填料等。近来,在以笔记本电脑机、信息终端等为代表的高性能电子设备上安装的诸如ic和cpu的电子半导体元件正在小型化和高度集成化,使得散热元件的小型化变得必需。散热元件的实例包括:高导热填料填充在诸如树脂和橡胶的基质中的散热片和膜状隔离片;高导热填料混合在硅油中以具有流动性的散热油脂;以及高导热填料混合在环氧树脂中的散热粘合剂。此处,作为高导热填料,使用氮化铝、氮化硼、氧化铝、氧化镁、二氧化硅、石墨、各种金属粉末等。然而,为了提高散热材料的热导率,重要的是致密地填充具有高导热性能的填料。为此,要求氮化铝粉末具有数微米至数十微米的尺寸的球形氮化铝粒子。通常,作为氮化铝粉末的制备方法,已知的有在氮气气氛中烧制氧化铝和碳的还原氮化方法、使金属铝与氮直接反应的直接氮化方法、以及使烷基铝与氨反应然后加热的气相方法。然而,通过还原氮化方法和气相方法难以形成具有球形形状的氮化铝粉末,并且它们的粒子尺寸为约亚微米尺寸。同时,直接氮化方法可以相对容易地控制粒子尺寸,从而得到数微米至数十微米的氮化铝粒子。然而,在该方法中粉碎步骤是必须的。因此,得到的氮化铝粉末的粒子具有角或无定形形状,这引起流动性降低,并且难以在树脂中非常致密地填充作为填料的氮化铝粉末。鉴于上述情况,已经进行各种研究以得到具有球形形状和所需要的平均粒子尺寸的氮化铝粉末。例如,专利文献1(日本未审查专利申请公开no.h3-23206)公开了一种通过在惰性气氛中烧制氧化铝粉末和碳粉的混合物来形成氧化铝,使其粒子生长,然后在含有氮气的非氧化气氛中烧制(氮化)其粒子,而得到平均粒子尺寸不小于3μm并且具有圆形形状的氮化铝粉末的方法。然而,存在的问题是,由于通过这种方法得到的氮化铝粉末具有椭圆形状,球形度低,并且涉及烧制气氛的变换,因此,难以控制氧化铝粒子的生长,即,难以控制得到的氮化铝粉末的粒子尺寸分布。另外,专利文献2(日本未审查专利申请公开no.h2005-162555)公开了一种通过在碳的存在下用氮气或氨气还原氮化球形氧化铝然后对其进行表面氧化,来制备平均粒子尺寸为50μm以下,球形度为0.8以上,并且具有优异的耐水性的球形氮化铝粉末的方法。然而,在上述制备方法中,由于作为原料的氧化铝的球形形状以原样被制成最终产品氮化铝粉末的形状,因此,必须使用粒子尺寸等于或大于所需要的粒子尺寸的氧化铝。在具有这样大的粒子尺寸的氧化铝的还原氮化中,需要长的反应时间来提高其转化率。另外,专利文献3(日本未审查专利申请公开no.h5-221618)公开了一种通过在含有氮气的非氧化气氛中烧制作为起始物料的氧化铝粉末、碳粉和稀土化合物的混合粉末来制备氮化铝粉末的方法。该方法利用碱土金属化合物或稀土化合物加速反应的功能,以在1500℃以下的低温下制备氮化铝。然而,通过这种方法得到的氮化铝粉末的粒子尺寸具体地为仅约1μm,并且得不到约数微米的相对大的粒子尺寸。另外,专利文献4(日本未审查专利申请公开no.h2002-179413)公开了一种在包含碱土金属、稀土金属等的化合物的助熔剂中烧制无定形粒子的氮化铝粉末以假定为球形,然后溶解助熔剂以分离氮化铝粉末的方法。该方法可以得到具有优异的流动性和填充性能的氮化铝粉末。然而,存在在热处理工艺的过程中诸如氧气等的杂质容易渗透到氮化铝粉末中的问题。另外,专利文献5(日本未审查专利申请公开no.h11-269302)公开了一种通过将成形助剂添加到通过预定方法制备的aln(氮化铝)粉末中,对其混合物进行湿法粉碎,使用喷雾干燥器使粉碎后的混合物颗粒化,将bn粉末混合进得到的颗粒化产物(颗粒)中,然后在氮气气氛中在高温下烧制和烧结所述混合物来制备球形氮化铝粉末的方法。然而,根据该方法,除了烧制使铝氮化之外,还需要烧制使得到的颗粒烧结,并且烧结温度非常高。因此,烧制必须在高温下进行两次,并且其颗粒化不容易。此外,由于aln易受水分的影响,因此,不能使用水作为溶剂进行喷雾干燥,由此,需要另外的表面改性用于水性喷雾干燥。为了解决这些问题,已经提出一种使用在水体系中稳定的前体如al2o3、al(oh)3和勃姆石进行喷雾干燥,将干燥后的产物与碳混合,然后在氮气气氛中在1200℃至1800℃下进行热处理的方法。然而,当使用α-al2o3相作为前体时,ain转化率为100%,但是当使用al(oh)3或勃姆石和其它al2o3相作为前体时,ain转化率低,因此,存在前体的使用受限的问题。因此,非常需要一种能够有效地制备具有最适合用作填料的球形形状并且平均粒子尺寸为数十微米的球形氮化铝粉末的制备方法。技术实现要素:技术问题做出本发明以解决现有技术中出现的上述问题以及过去遇到的技术问题。具体地,本发明的一个目的是提供一种方法,该方法即使在使用常规的喷雾干燥装置时也能够通过使用水性喷雾方法由稳定的水性起始物料高转化成ain,能够在相对低的温度下合成ain,从而能够有效地制备平均粒子尺寸为数十微米同时具有最适合用作填料的球形形状的球形氮化铝粉末。技术方案为了实现上述目的,本发明提供一种球形氮化铝粉末的制备方法,包括以下步骤:(i)在溶剂中混合al前体和助熔剂以制备混合溶液;(ii)对在步骤(i)中制备的所述混合溶液进行喷雾干燥;(iii)将喷雾干燥后的粉末与碳基物质混合;(iv)在氮气气氛中对步骤(iii)的混合物进行热处理;以及(v)在空气气氛中对步骤(iv)的所述热处理后的化合物进行脱碳处理,其中,所述助熔剂是选自cu2o、tio2、bi2o3和cuo中的至少一种;或者是选自cu2o、tio2、bi2o3和cuo中的至少一种与选自caf2和y2o3中的至少一种的混合物。换言之,根据本发明,当如上所述将al前体与助熔剂混合、喷雾干燥、与碳基物质混合、并进行热处理时,不仅由于al前体与助熔剂的低共熔点而可以在相对低的温度下合成aln,而且可以具有99.5%以上的转化率,这是非常高的转化率,并且可以有效地得到平均粒子尺寸为数十微米且具有最适合用作填料的球形形状的球形氮化铝粉末。在这种情况下,所述al前体可以是选自al(oh)3、勃姆石(alo(oh))和al2o3中的至少一种。这些前体在水中高度稳定,并且如下文将要描述的,在喷雾干燥的过程中不需要预处理,因此,可以减少工艺步骤的数目,这在工艺效率方面是优选的。al2o3包括具有α、γ、θ、δ、η、κ或χ的晶体结构的那些,但是不限于此。所述al前体的平均粒子尺寸(d50)可以为5微米以下,具体地为0.1微米至2微米,用于还原氮化反应。如果超过上述范围,则还原氮化反应难以进行至粒子的内部,并且氧化铝会残留在内部。此外,由于通过液相的质量传递的比率减小,因此,得到的氮化铝粒子的球形度降低。此外,如果平均粒子尺寸太小,则还原氮化反应倾向于在短时间内在低温下完成,粒子生长和质量传递困难,并且难以得到具有大粒子尺寸的氮化铝粉末。由于助熔剂优选能够与al前体形成低共熔点(1200℃至1800℃)的低共熔液相,因此,可以使用如上所述的助熔剂。然而,当单独使用caf2或y2o3时,合成转化率降低。因此,如上所述,使用选自cu2o、tio2、bi2o3和cuo中的至少一种助熔剂,或者可以使用上述物质和选自caf2和y2o3中的至少一种的混合物。更具体地,可以一起使用cu2o和其它物质中的一种。此时,助熔剂为颗粒状并且对粒子尺寸没有限制,但是平均粒子尺寸可以为0.01微米至50微米。对bet比表面积也没有特别地限制,但是可以为0.01m2/g至500m2/g,更具体地为0.1m2/g至100m2/g。这种al前体和助熔剂可以在溶剂中混合。在这种情况下,溶剂可以是极性溶剂,特别是水。如果溶剂是非极性溶剂如甲苯,它只能用于专门的喷雾干燥装置如防爆装置,这在生产和成本效益方面不优选。同时,由于本发明使用水作为溶剂,因此,即使使用常规喷雾干燥装置也可以容易地使用,因此非常有效。对在溶剂中混合没有限制,只要它是能够均匀地混合各个原料的方法即可。它可以使用在混合固体物质时通常使用的装置,例如,它可以通过搅拌机、混合器或球磨机进行。在这种情况下,当将al前体的重量认为是100%时,基于al前体的重量,al前体与助熔剂的混合物可以含有0.1重量%至10重量%的助熔剂。当助熔剂的含量太低以致低于上述范围时,在热处理过程中不能形成足够量的低共熔液相,向所得物氮化铝的转化率降低,并且存在不能得到具有所需要的粒子尺寸的粉末的问题。相反,当助熔剂的含量太高时,助熔剂会作为杂质残留,这会引起热导率降低。另一方面,在al前体与助熔剂的混合溶液中,根据需要,还可以包含粘合剂、分散剂或者粘合剂与分散剂,只要它们不损害本发明的效果即可,但是这不是必需的。粘合剂在喷雾干燥过程中可以用于促进粒子形状的保持,并且基于混合溶液的总重量,其含量可以为0.1重量%至5重量%。使用的粘合剂的实例为聚乙二醇、聚乙烯吡咯烷酮、聚偏二氟乙烯、聚乙烯醇、羧甲基纤维素(cmc)、淀粉、羟丙基纤维素、再生纤维素、聚乙烯吡咯烷酮、四氟乙烯、聚乙烯、聚丙烯、乙烯-丙烯-二烯三元共聚物(epdm)、磺化epdm、苯乙烯丁二烯橡胶、氟橡胶、各种共聚物、高分子量聚乙烯醇等。分散剂可以用于促进al前体与助熔剂在溶剂中均匀混合,并且基于混合溶液的总重量,其含量可以为0.1重量%至5重量%。所述分散剂可以是,例如,阳离子表面活性剂、阴离子表面活性剂、非离子表面活性剂、聚合物物质等。这种混合溶液可以经历各种方法以形成球形干燥粉末,并且从容易调节干燥粉末的粒子尺寸以及经济效率的观点来看,可以通过喷雾干燥方法进行。干燥粉末的粒子尺寸或比表面积可以通过调节混合溶液的固体含量浓度来控制,或者可以通过调节喷雾干燥的条件来控制。作为喷雾干燥方法,可以使用利用喷嘴、圆盘等的一种方法。喷雾干燥的条件可以根据使用的干燥器的尺寸和类型、混合溶液的浓度和粘度等适当地选择。将由此形成的干燥粉末与作为还原剂的碳基物质混合以在随后的热处理中还原。在这种情况下,碳基物质可以是炭黑、石墨粉等,并且具体地,可以是炭黑。炭黑的实例为炉黑、槽黑、科琴黑、乙炔黑等。碳基物质的bet比表面积可以为0.01m2/g至500m2/g。基于al前体的重量,这种碳基物质的含量可以为30重量%至70重量%,更具体地,其含量可以为40重量%至60重量%。当碳基物质以超出上述范围的过小的量包含时,不能发生充分的还原,由此,不能得到所需要的程度的氮化铝,即,转化率降低。当过量地含有碳基物质时,生产成本增加,这不是有效的。除了作为还原剂的作用之外,与碳基物质混合还可以通过与干燥粉末混合来使干燥粉末彼此分离,从而防止甚至在热处理之后粉末聚集。碳基物质与干燥粉末的混合也可以通过在将球形干燥粉末保持在搅拌器、搅拌机、混合器、球磨机等中的条件下将两者干燥混合来进行。同时,干燥粉末与碳基物质的混合物通过在氮气气氛中的热处理被还原氮化。在这种情况下,反应容器中的氮气气氛可以通过连续地或间歇地供应足以使用作原料的干燥粉末进行氮化反应的量的氮气来形成。另外,热处理可以在比原始氮化铝的烧制温度低的温度下进行,例如,在1200℃至1900℃,具体地在1300℃至1900℃的温度下进行1小时至10小时。当烧制温度低于上述温度范围时,氮化反应不能充分进行,并且不能得到需要的氮化铝粉末。如果热处理温度太高以致超过上述范围,则氮化反应充分进行,但是容易制得具有低热导率的氮氧化物(alon),并且倾向于容易发生粒子的聚集,因此,会难以得到具有所需要的粒子尺寸的氮化铝粉末。此外,当热处理温度太低时,向氮化铝的转化率低,因此,得到的粉末本身的热导率会降低。另外,如果热处理时间小于1小时,则氮化反应会不完全,如果热处理时间长于10小时,则形成的氮化铝粉末会聚集,这不是优选的。在本发明中,可以进行脱碳处理以除去在热处理之后得到的氮化铝粉末中存在的过量的碳基物质。所述脱碳处理使用氧化气体进行,用于氧化和除去碳。具体地,它可以在空气气氛中进行。在这种情况下,脱碳处理可以在600℃至800℃下进行1小时至3小时。如果脱碳处理温度太高或者如果长时间进行,则氮化铝粉末的表面被过度氧化并且氮化铝粉末的热导率降低,这是不合适的。此外,如果脱碳处理温度太低,或者如果短时间进行,则过量的碳基物质未被完全除去并且作为杂质残留,这是不优选的。当通过这种方法制备时,al前体向氮化铝粉末的转化率可以为90%以上,具体地为99%以上,更具体地为99.5%以上。制备的氮化铝粉末的平均粒子尺寸可以为5微米至200微米,具体地为10微米至100微米,更具体地为10微米至70微米。如果平均粒子尺寸超出上述范围,则不适合用作填料。因此,优选满足上述范围。在上述范围内,可以根据需要适当地调节尺寸并使用。另外,根据本发明制备的氮化铝粉末的球形度高达0.98以上,并且当与树脂混合时热导率可以具有2.7w/mk的高热导率。有益效果如上所述,在根据本发明的制备方法中,将稳定的水性al前体与助熔剂混合并在水体系中喷雾干燥以制备干燥粉末,并且将干燥粉末与碳基物质混合并热处理。由此,当使用喷雾干燥颗粒化为球形形状时,使用水作为溶剂,因此,它是有效的并且表现出99.5%以上的高aln转化率。因此,可以有效地制备尺寸为数十微米同时具有最适合用作填料的球形形状的球形的氮化铝粉末。附图说明图1是根据实施例1制备的氮化铝粉末(aln粉末)的xrd图;图2是根据实施例1制备的氮化铝粉末的sem照片。具体实施方式现在将参照实施例描述本发明,但是提供这些实施例用于更好地理解本发明,并且本发明的范围不限于此。在本发明中,根据bet单点法测量比表面积,并且通过使用激光衍射粒子尺寸分布计(horibala-960)通过将样品分散在乙醇中以测量平均粒子尺寸(d50)的方法来测量平均粒子尺寸。通过rietveld拟合方法计算ain转化率。以sem照片中的任意一个粒子的最长直径与最短直径的比率计算根据本发明的球形度。将硅橡胶与各个情况中的aln混合,将混合物模塑成100×60×3,然后在150℃下进行热处理1小时后测量热导率。<实施例1>使用氧化锆球将10g的al(oh)3(平均粒子尺寸:1μm)和0.3g的cu2o(平均粒子尺寸:1μm)与作为溶剂的水混合24小时。之后,将球分离并且在230℃的入口和60℃的出口的条件下对混合物进行喷雾干燥以得到干燥粉末。将得到的干燥粉末和4g的炭黑(比表面积:70m2/g)在研钵中混合,并且在n2气氛中在1600℃下对混合物热处理3小时。然后,在空气气氛中在700℃下对热处理后的氮化铝化合物进行脱碳2小时,以得到球形氮化铝粉末。由此得到的氮化铝粉末的xrd图示于图1中,并且sem照片示于图2中。参照图1和图2,可以确认,不仅得到高纯度的ain,而且其形状为球形,并且平均粒子尺寸为约20μm。<实施例2>除了还添加0.2g的tio2(平均粒子尺寸:1μm)并且与实施例1中的10g的al(oh)3(平均粒子尺寸:1μm)和0.3g的cu2o(平均粒子尺寸:1μm)混合之外,以与实施例1中相同的方式得到球形氮化铝粉末。<实施例3>除了使用0.3g的tio2(平均粒子尺寸:1μm)和0.2g的bi2o3(平均粒子尺寸:1μm)代替实施例1中的0.3g的cu2o(平均粒子尺寸:1μm)之外,以与实施例1中相同的方式得到球形氮化铝粉末。<实施例4>除了使用10g的勃姆石(平均粒子尺寸:1μm)代替实施例1中的10g的al(oh)3(平均粒子尺寸:1μm)之外,以与实施例1中相同的方式得到球形氮化铝粉末。<实施例5>除了使用10g的γ-al2o3(平均粒子尺寸:1μm)代替实施例1中的10g的al(oh)3(平均粒子尺寸:1μm)之外,以与实施例1中相同的方式得到球形氮化铝粉末。<比较例1>除了使用10g的勃姆石(平均粒子尺寸:1μm)代替10g的al(oh)3(平均粒子尺寸:1μm),并且不使用实施例1中的0.3g的cu2o(平均粒子尺寸:1μm)之外,以与实施例1中相同的方式得到球形氮化铝粉末。<比较例2>除了使用10g的γ-al2o3(平均粒子尺寸:1μm)代替10g的al(oh)3(平均粒子尺寸:1μm),并且不使用实施例1中的0.3g的cu2o(平均粒子尺寸:1μm)之外,以与实施例1中相同的方式得到球形氮化铝粉末。<比较例3>除了使用0.3g的y2o3(平均粒子尺寸:1μm)代替实施例1中的0.3g的cu2o(平均粒子尺寸:1μm)之外,以与实施例1中相同的方式得到球形氮化铝粉末。<比较例4>将10g的γ-al2o3(平均粒子尺寸:1μm)、4g的炭黑(比表面积:70m2/g)和0.3g的y2o3(平均粒子尺寸:1μm)混合。将混合的粉末在n2气氛下在1700℃下热处理10小时。然后,将热处理后的氮化铝化合物在空气气氛中在700℃下脱碳10小时,以得到氮化铝粉末。<比较例5>除了使用0.3g的cu2o(平均粒子尺寸:1μm)代替比较例4中的0.3g的y2o3(平均粒子尺寸:1μm)之外,以与比较例4中相同的方式得到球形氮化铝粉末。<实验例>测量在实施例1至实施例5和比较例1至比较例5中制备的氮化铝粉末的aln转化率、球形度和热导率,并且示于下面的表1中。[表1]aln转化率(%)球形度热导率(w/mk)实施例11000.992.8实施例21000.982.9实施例31000.992.8实施例41000.982.7实施例51000.992.8比较例1520.981.4比较例2780.972.7比较例3860.981.8比较例4820.99-比较例51000.98-参照表1,可以确认,如在实施例1至实施例5中,当根据本发明制备氮化铝粉末时,aln转化率非常高,同时具有高球形度和热导率,而在比较例1至比较例4中,aln转换率非常低。另一方面,在比较例4和比较例5中,由于在脱碳工艺中除去存在于aln中的炭黑,因此,不能保持球形形状,从而无法测量热导率。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1