一种高纯度大表比面积ε-MnO2的水热合成方法与流程
本发明涉及一种材料的制备方法,特别涉及一种ε-mno2的水热合成方法。
背景技术:
甲醛是最重要的室内污染物之一,主要来源于各种人造板和室内装饰材料。目前空气净化产品中的异味净化仍采用活性炭滤网吸附,其寿命短又常常因为滤网更换不及时造成二次污染。因此,研发能够将空气中的甲醛等污染物催化氧化成水和二氧化碳的催化剂,同时能够成功应用在家电产品或者新风系统中,实现无耗材高效率净化室内空气,则显得意义尤为重大。
二氧化锰是一种公知的室温下具有除甲醛功能的物质,被广泛用于制备除甲醛材料。研究表面,二氧化锰可以催化氧化甲醛,使其分解为二氧化碳和水。二氧化锰的晶型结构复杂,有研究表明其存在α、β、γ等5种主晶及30余种次晶,不同晶型的二氧化锰具有不同的特性。
已经报导的二氧化锰制备方法包括水热沉淀法、水热分解法、固相法、共沉淀法、溶胶-凝胶法、电化学法、微乳液法、流变相反应法、γ射线照射法、臭氧氧化法等。制备方法的不同对纳米二氧化锰的粒度分布、晶粒尺寸以及晶型的转变都具有不同程度影响,而纳米二氧化锰的性质、结构和形貌与制备方法和制备条件有很大关系。目前普遍需要采用复杂的工艺才可制备得到具有较高晶型纯度的二氧化锰,因此,开发出一种简便的高晶型纯度的二氧化锰制备方法,具有非常实际的意义。
技术实现要素:
本发明的目的在于克服现有技术的不足,提供一种二氧化锰的制备方法,该制备方法可以简便、高效地制备得到高晶型纯度的ε-mno2。
本发明所采取的技术方案是:
本发明的第一个方面,提供:
一种ε-mno2的水热合成方法,包括如下操作:
1)配制浓度为2g/(50~200ml)的高锰酸盐水溶液;
2)将高锰酸盐水溶液置于水热釜内,150~250℃下进行水热合成反应;
3)反应完毕后,固液分离,得到ε-mno2。
在一些水热合成方法的实例中,所述高锰酸盐水溶液的浓度为2g/(100~200ml)。
在一些水热合成方法的实例中,所述水热合成的反应温度为150~200℃。
在一些水热合成方法的实例中,所述水热合成的反应时间为10~18h。
在一些水热合成方法的实例中,所述水热合成的反应温度为150~180℃,反应时间为10~15h。
在一些水热合成方法的实例中,所述水热合成的过程中,水热釜内还添加有mno2载体。
在一些水热合成方法的实例中,所述载体包括但不限于在水热反应过程中稳定的活性炭、陶瓷片、铝基材、滤网。
在一些水热合成方法的实例中,所述高锰酸盐为高锰酸钾、高锰酸钠。
本发明的第二个方面,提供:
一种空气净化器件,包括载体,所述载体上负载有本发明第一个方面所述水热合成方法制备得到的ε-mno2。
在一些空气净化器件的实例中,所述载体包括但不限于活性炭、陶瓷片、铝基材、滤网。
本发明的有益效果是:
本发明的一个方面,使用的原料极少,可以简便、高效地制备得到高晶型纯度的ε-mno2。
本发明的一个方面,制备得到的ε-mno2具有大表比面积。
本发明的一个方面,制备得到的ε-mno2具有很好的甲醛降解活性,可以制备得到性能更为优异的除甲醛材料。
本发明的一个方面,通过在水热合成的过程中添加mno2载体,水热合成后可以得到负载有mno2的载体,简化了后续的处理。
本发明的空气净化器件,具有持久的除甲醛能力。
附图说明
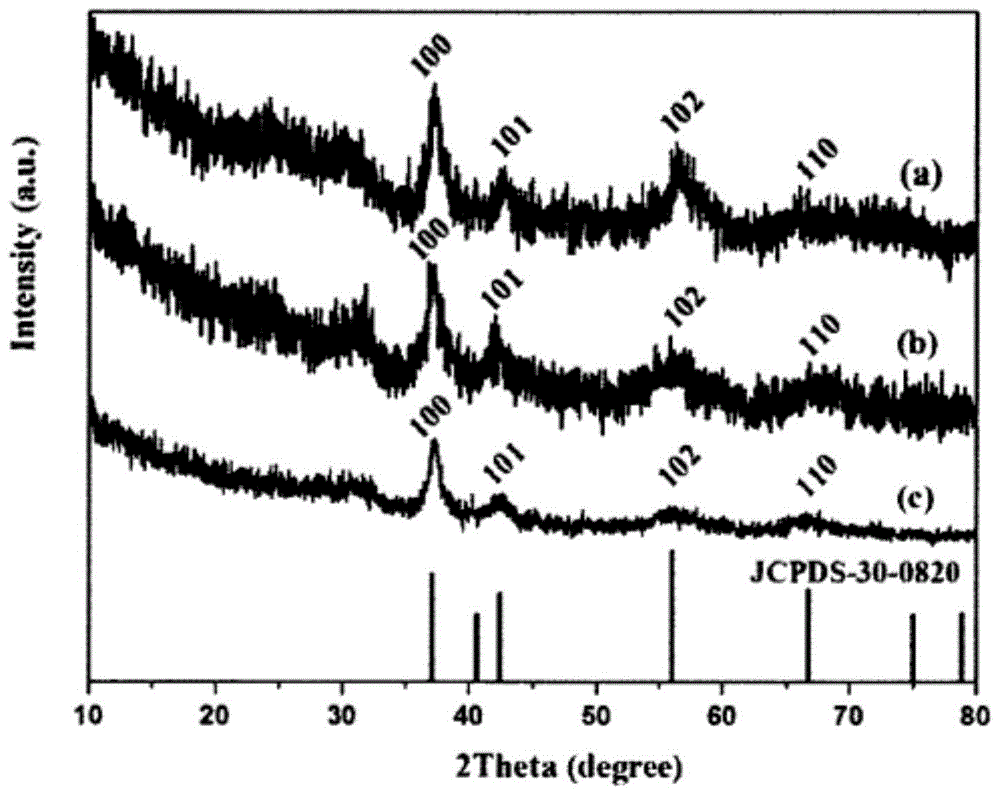
图1是实施例1合成得到的ε-mno2的xrd图谱;
图2是不同实施例合成的ε-mno2的除甲醛性能比较结果。
具体实施方式
本发明的第一个方面,提供:
一种ε-mno2的水热合成方法,包括如下操作:
1)配制浓度为2g/(50~200ml)的高锰酸盐水溶液;
2)将高锰酸盐水溶液置于水热釜内,150~250℃下进行水热合成反应;
3)反应完毕后,固液分离,得到ε-mno2。
水热合成的过程中,高锰酸盐发生复分解反应,生成-mno2。
在一些水热合成方法的实例中,所述高锰酸盐水溶液的浓度为2g/(100~200ml)。这种浓度可以得到纯度更高的ε-mno2。
在一些水热合成方法的实例中,所述水热合成的反应温度为150~200℃。
在一些水热合成方法的实例中,所述水热合成的反应时间为10~18h。
在一些水热合成方法的实例中,所述水热合成的反应温度为150~180℃,反应时间为10~15h。
具体的反应温度、反应时间,可以根据反应情况,在上述范围内进行相应的调整。
在一些水热合成方法的实例中,所述水热合成的过程中,水热釜内还添加有mno2载体。
载体的作用在于负载ε-mno2颗粒,本身没有特别的要求。在一些水热合成方法的实例中,所述载体包括但不限于在水热反应过程中稳定的活性炭、陶瓷片、铝基材、滤网。
在一些水热合成方法的实例中,所述高锰酸盐为高锰酸钾、高锰酸钠。
本发明的第二个方面,提供:
一种空气净化器件,包括载体,所述载体上负载有本发明第一个方面所述水热合成方法制备得到的ε-mno2。
在一些空气净化器件的实例中,所述载体包括但不限于活性炭、陶瓷片、铝基材、滤网等常用的载体材料。
实施例1:
1)配制浓度为2g/200ml的高锰酸盐水溶液;
2)将高锰酸盐水溶液置于水热釜内,150℃下进行水热合成反应12h;
3)反应完毕后,固液分离,得到ε-mno2。
图1是实施例1合成得到的ε-mno2的xrd图谱。从图中可以看出,制备得到的是ε-mno2。
实施例2:
1)配制浓度为2g/100ml的高锰酸盐水溶液;
2)将高锰酸盐水溶液置于水热釜内,200℃下进行水热合成反应15h;
3)反应完毕后,固液分离,得到ε-mno2。
实施例3:
1)配制浓度为2g/50ml的高锰酸盐水溶液;
2)将高锰酸盐水溶液置于水热釜内,250℃下进行水热合成反应10h;
3)反应完毕后,固液分离,得到ε-mno2。
实施例4:
1)配制浓度为2g/120ml的高锰酸盐水溶液;
2)将高锰酸盐水溶液置于水热釜内,180℃下进行水热合成反应12h;
3)反应完毕后,固液分离,得到ε-mno2。
不同实施例制备得到的ε-mno2部分物理特性如表1所示。
表1:不同实施例合成得到mno2的性质比较表
将水热反应的时间设定为12h,温度设定为180℃,比较不同高锰酸钾水溶液的浓度对水热合成制备ε-mno2的影响,实验结果如表2所示。
表2:高锰酸钾水溶液的浓度对水热合成制备ε-mno2的影响
实验结果表明,高锰酸钾水溶液的浓度为2g/(100~200)ml时,ε-mno2的纯度更高。
将高锰酸钾水溶液的浓度设定为2g/100ml,水热反应的时间设定为12h,比较不同水热合成温度对制备ε-mno2的影响,实验结果如表3所示。
表3:水热合成的反应温度对制备ε-mno2的影响
实验结果表明,水热反应温度为150~250℃时,可以得到纯度更高的ε-mno2,但是随着反应温度的升高,ε-mno2的粒径相对增加,导致其比表面积降低。
将高锰酸钾水溶液的浓度设定为2g/100ml,水热反应的温度设定为150℃,比较不同水热合成对时间制备ε-mno2的影响,实验结果如表4所示。
表4:水热合成的反应时间对制备ε-mno2的影响
实验结果表明,同一反应温度下,ε-mno2的粒径基本是相同的,反应时间在6h以上可以取得令人满意的结果,反应时间在10h或更长时,含量不再有显著变化,优选10~18h。
性能测试:
不同实施例制备的ε-mno2的除甲醛性能比较
1)将10gε-mno2配成浆料后负载于纸蜂窝上,制成10mm*15mm*60mm大小的除甲醛模块;
2)将模块置于100l的密闭舱中,舱中具有循环风扇、用于甲醛挥发的加热器以及可放置除甲醛模块的支架,支架带有风扇;
3)加入一定量的甲醛溶液于加热挥发器上,加热并开启循环风扇,甲醛检测仪器显示甲醛浓度稳定后,关闭舱内循环风扇和加热器,开启除甲醛模块装置的风扇;
4)记录初始甲醛浓度,以及1min,5min,10min,15min,20min,25min,30min的甲醛浓度,绘制除甲醛效率曲线。
实验结果如图2所示,结果表明本发明实施例1~4制备得到的ε-mno2,相对市售的二氧化锰具有更好的除甲醇性能。
长期除甲醛的性能测试:
参照上述不同实施例制备的ε-mno2的除甲醛性能比较的实验设计,分别测试不同二氧化锰材料多次除甲醇的能力。结果显示,本发明实施例合成得到的ε-mno2,多次的除甲醛效果基本相同,具有较为稳定的除甲醛效率。
- 还没有人留言评论。精彩留言会获得点赞!