碳阳极材料的制作方法
碳阳极材料
发明领域
1.本发明涉及某些新型含碳阳极材料,涉及制备这种含碳阳极材料的新方法,涉及包含这种新型含碳阳极材料的阳极电极,以及涉及这种阳极电极在例如诸如电池(尤其是可再充电电池)、电化学装置和电致变色装置的储能装置中的用途。
2.发明背景
3.钠离子电池在许多方面类似于现今常用的锂离子电池;它们都是包括阳极(负极)、阴极(正极)和电解质材料的可重复使用的二次电池,都能够储存能量,并且它们都经由类似的反应机理充电和放电。当钠离子(或锂离子)电池充电时,na
+
(或li
+
)离子从阴极脱嵌并且嵌入阳极。同时,电荷平衡电子从阴极通过包括充电器的外部电路并且进入电池的阳极。在放电期间发生相同的过程,但是方向相反。
4.锂离子电池技术近年来受到很多的关注,并且为现今使用的大多数电子设备提供优选的便携式电池;然而,锂不是廉价的金属来源,并且被认为对于大规模应用中的使用太昂贵。相比之下,钠离子电池技术仍然处于其相对初期,但是被认为是有利的;钠比锂是丰富得多的,并且一些研究者预测这将提供更便宜和更持久的方式来储存能量到未来,特别是对于诸如在电网上储存能量的大规模应用。然而,在钠离子电池成为商业现实之前,仍有大量工作要做。
5.在开发用于锂离子电池和钠离子电池两者的具有高电荷储存容量和倍率性能的阴极电极材料方面已经取得显著的研究进展,然而,需要更多关注的一个领域是新的和更有效的阳极电极材料的开发。
6.以石墨形式的碳由于其高的重量和体积容量在一段时间以来作为锂离子电池中的阳极材料被青睐;石墨电极提供大于360mah/g的可逆容量,与372mah/g的理论容量相当。电化学还原过程涉及将li
+
离子嵌入石墨烯层之间,以产生lic6。然而,不幸的是,石墨对钠的电化学活性低得多,并且这与钠与锂相比具有显著更大的原子半径的事实相结合,导致在钠离子电池中在石墨阳极中的石墨烯层之间的嵌入被严重限制。
7.另一方面,发现在钠离子电池中使用硬碳材料制成的阳极(诸如pct/gb2020/050872、us2002/0192553a1、us9,899,665b2、us2018/0287153a1中所述)表现的有利得多。
8.硬碳具有无序结构,这克服钠离子的许多嵌入问题。硬碳材料的确切结构仍有待解决,但一般而言,硬碳被描述为缺乏长程晶序的不可石墨化碳材料。硬碳具有层,但是这些层在长程中不是整齐地堆叠的,并且它是微孔材料。尽管缺乏确定的晶体结构,硬碳在宏观水平上是各向同性的。难以构建硬碳的通用结构模型的原因之一是短程有序、域尺寸、碳层和微孔的比例取决于诸如碳源、碳化和热解温度的合成条件。
9.另外,与具有其中碳层平面按层堆叠的石墨晶体结构的石墨不同,硬碳具有其中碳层平面以三维地错开的状态堆叠的乱层结构。因此,硬碳的热处理,即使在高温(如3000℃)下,也不会导致从乱层结构向石墨结构的转变或石墨微晶的发展。因此,硬碳在结构上与石墨完全不同,并且可以说包括一个或多个非石墨化区域以及一个或多个不可石墨化区域。
10.用于制备可在用于二次电池应用的电极中使用的硬碳材料的通常的方法涉及在无氧气氛中加热富碳起始材料至高于500℃的温度,所述富碳起始材料诸如例如石油焦炭和沥青焦炭的矿物;诸如蔗糖和葡萄糖的二次植物基材料;诸如聚合烃和诸如间苯二酚甲醛的较小的有机化合物的人造有机材料;诸如粪肥的动物衍生材料;以及诸如椰子壳、咖啡豆、稻草、竹子、稻壳、香蕉皮等一次植物衍生材料。在当植物衍生和动物衍生材料被碳化的情况下,产生“生物炭”或生物质炭,其可以被进一步加工以获得硬碳材料。
11.另一方面,软碳是碳的另一种形式,其在结构上也不同于石墨,但它是碳的可石墨化的形式,并且可以在高温(如3000℃)下转变成包括石墨结构的区域。然而,即使在该热处理之后,非石墨化碳材料的区域仍会存在,因为该转变不会导致完全石墨结构。因此,软碳可以说是包括一个或多个非石墨化区域,但不能说是包括一个或多个不可石墨化区域。
12.商业上有用的阳极材料的重要特征是包括在原始碱金属离子电池的首次充电循环期间由于液体电解质分解产物沉积在电解质和阳极表面之间的界面处自然形成的固体电解质中间相(sei)层。一段时间以来,已经认识到该sei层是碱金属离子电池的必要组分,首先因为它通过抑制电子从阳极向电解质的转移来保护阳极,以及其次因为它允许碱金属离子从电解质向阳极转移,并且这两个因素影响电池循环寿命。因此,理想的sei层既是离子导体又是电绝缘体。然而,sei层的形成必然消耗一部分在初始充电循环期间从阴极脱嵌的碱金属离子,这又意味着它们不能用于未来的充电/放电循环。由于在隔离的可再充电电池中存在固定的载荷子存量,可用的碱金属离子的该损耗导致容量的不可逆损失。目前的工作旨在控制sei层的形成(特别是控制sei层的稳定性),以便使其离子传导和电子绝缘性能最大化,并且使不可逆比容量最小化。
13.如下所述,本技术人已经设计阳极电极材料的表面化学、形态、晶体学、厚度和孔结构,以便控制sei层的稳定性和坚固性,以及从而使首次循环损失的不可逆容量最小化。
14.cn 108963252 a公开一种包括硬碳核的阳极材料,然后用备长炭涂覆该硬碳核并加热至1500℃,然而,该方法没有导致对硬碳材料的表面化学的任何设计,因为即使在该高温下,硬碳也不能化学键合到备长炭。
15.因此,并且特别是,本发明提供新型含碳阳极材料,其具有被设计为具有特定化学和/或物理特性的外表面,所述具有特定化学和/或物理特性的外表面可用于建立优化的、稳定的和坚固的sei层,同时使不可逆容量最小化。此外,本发明提供一种用于制备这种表面设计的含碳阳极材料的新方法。这种方法将是有成本效益的,尤其是在商业规模上,并且将使用容易得到的反应物。所得的表面设计的含碳阳极材料在诸如电池(尤其是二次(可再充电)电池)、碱金属离子电池(特别是钠离子电池)、电化学装置和电致变色装置的能量储存装置中将是有用的。重要的是,这些表面设计的含碳阳极材料将制备对于可逆比容量、阴极比能量、首次阴极脱钠比容量和首次放电容量效率(库仑效率,计算为在整个循环中从电池取出的总电荷与输入电池中的总电荷的比率)以及显著降低的不可逆容量(首次循环损失)提供优异结果的能量储存装置。此外,与类似的非表面设计的含碳阳极材料诸如cn 108963252 a中公开的阳极材料相比,本发明的新型表面设计的含碳阳极材料将提供令人惊讶的和有利的处理特性,所述令人惊讶的和有利的处理特性包括水分敏感性的降低和用于制备电极的浆料粘度的降低。
16.为了实现这些目的,本发明提供一种含碳阳极材料,其能够嵌入和脱嵌碱金属离
子并且其具有碳结构,所述碳结构包括含有一种或多种一次含碳材料的核和含有一种或多种碳化材料的外表面,所述一种或多种碳化材料优选地化学键合在所述一种或多种一次含碳材料上。
17.如本文所用,术语“核”是指碳结构的中心部分。
18.最优选地,所述核不由或基本上不由一种或多种选自石墨和具有完全石墨结构的材料的一次含碳材料组成。在一个实施方案中,所述核可基本上由所述一种或多种一次含碳材料组成,并且进一步优选地可由所述一种或多种一次含碳材料组成。
19.如本文所用,短语“化学键合”是指在一种或多种一次含碳材料和一种或多种碳化材料之间形成诸如共价键的化学键。因此,“强键”包括在该短语的含义内,但是诸如范德华相互作用的“弱键”不包括在该短语的含义内。
20.由于根据本发明碳化材料优选通过使用化学气相沉积“化学键合”到一次含碳材料上,这有利地允许对一次含碳材料的表面设计。此外,本发明的碳化材料在一种或多种一次含碳材料上热解分解,并且该“自下而上合成法”允许碳原子一个接一个地沉积在一种或多种一次含碳材料的外表面上。
21.因此,所述含碳阳极材料包含一种或多种一次含碳材料,所述一种或多种一次含碳材料具有被设计为表现出如下所述的特定表面特性的外表面,并且最理想地,根据本发明的所述含碳阳极材料包含一种或多种一次含碳材料,所述一种或多种一次含碳材料具有被设计为表现出使用氮气bet分析测定的0m2/g至5m2/g的开口微孔比表面积的外表面。优选地,使用氮气bet分析测定的大于0m2/g至5m2/g的开口微孔比表面积。
22.合适的一次含碳材料为任何颗粒(如粒状或粉末状)形式,并且能够嵌入和脱嵌钠离子。
23.在一个实施方案中,所述一种或多种一次含碳材料可以包括选自不可石墨化区域和非石墨化区域的区域。如上所讨论的,硬碳材料是包括不可石墨化区域以及非石墨化区域的含碳材料的实例。软碳材料是包括可石墨化区域和非石墨化区域的含碳材料的实例。
24.在一个实施方案中,所述一种或多种一次含碳材料可以包括可石墨化区域和/或非石墨化区域。其一个实例是软碳。
25.在一个实施方案中,所述一种或多种一次含碳材料可以包括不可石墨化区域和非石墨化区域。其一个实例是硬碳。
26.在一个实施方案中,所述一种或多种一次含碳材料包含无序的含碳材料,并且进一步优选地,它们包含选自常规碳阳极材料(如硬碳阳极材料);非完全石墨化的高温硬碳(例如,当完全石墨形成时退火到高于2000℃但低于3000℃的温度的硬碳);碳-金属、碳-半金属或碳-非金属复合材料(例如碳-sb、碳-sn、碳-si、碳-pb、碳-ti和碳-p)(这些材料的硬碳类似物是尤其优选的);软碳材料(例如热解的磨碎的碳纤维);碳-导电添加剂混合物(例如硬碳-碳黑混合物,合适的碳黑可以是从imerys商业上可得的super c65
tm
材料);碳-氧化物复合材料(例如硬碳-fe2o3、硬碳-sb氧化物、硬碳-sn氧化物、硬碳-sb/sn氧化物);碳-碳化物复合材料(例如硬碳-sic复合材料);和活性碳材料(例如bet表面积>100m2/g的活性硬碳)中的一种或多种材料。方便地,所述一次含碳材料可以通过碳基起始材料的热解(高温处理,一般大于700℃至2500℃并且一般在包含选自氮气、二氧化碳、另一种非氧化性气体和诸如氩气的惰性气体的一种或多种的非氧化性气氛下)制备,所述碳基起始材料诸如
植物基材料、动物衍生材料(包括在食物已经通过动物的消化道并且已经从动物的消化道排泄之后获得的“动物衍生废料”)、烃材料(包括诸如煤、煤沥青、煤焦油、石油沥青、石油焦油和油的化石燃料材料)、碳水化合物材料和其它含碳有机材料。优选地,理想地在热解之前,使用可以包括选自炭化(一般在150℃至≤700℃的温度)、洗涤、分解、化学消化(例如使用酸性和/或碱性条件)、过滤、离心、“重介质分离”或“沉浮分离法”、使用离子交换材料、色谱分离技术、电泳分离技术、使用络合剂或化学沉淀技术和研磨(一般至约8-25μm的d
50
粒度并通过15-25μm的筛过滤以排除较大颗粒)的一种或多种的方法步骤纯化所述碳基起始材料以除去不需要的不含碳的材料(例如含金属的离子(诸如过渡金属、碱金属或碱土金属)和不含金属的离子(如磷、氧、氢))。
27.在一个实施方案中,所述一种或多种一次含碳材料的粒度分布为从约1nm至约30μm,优选从约1nm至20μm。特别地,申请人理解,本发明的表面处理基本上不改变所述一种或多种一次含碳材料的粒度分布。因此,该范围适用于在所述碳化材料化学键合到一种或多种一次含碳材料上之前以及在该处理发生之后的所述一种或多种一次含碳材料的粒度分布。
28.在一个实施方案中,所述一种或多种一次含碳材料具有约0.01μm至约4μm的d
10
粒度。
29.在一个实施方案中,所述一种或多种一次含碳材料具有约4μm至约15μm的d
50
粒度。在另一实施方案中,所述一种或多种一次含碳材料具有从约1至约25μm的d
50
粒度,优选为从约8至约25μm的d
50
粒度。
30.在一个实施方案中,所述一种或多种一次含碳材料具有约15μm至约30μm的d
90
粒度。
31.理想地,用于本发明的含碳阳极材料的一次含碳材料包含硬碳和/或软碳材料,并且进一步理想地,该硬碳和/或软碳材料具有非完全石墨结构,即,其包括非石墨化区域。
32.其它优选的一次含碳材料包括与一种或多种元素和/或化合物组合的碳(例如如上所述的硬碳、软碳)。特别优选的示例性组合包括碳/x材料,其中x可以是诸如锑、锡、磷、硫、硼、铝、镓、铟、锗、铅、砷、铋、钛、钼、硒、碲、硅、碳或镁的一种或多种元素。碳/sb、碳/sn、碳/sb
x
sny、碳/磷、碳/硅、碳/碳化硅(hc/sic)或碳/硅酸钠是合适的含碳材料。一种或多种这些材料的硬碳类似物是尤其优选的。进一步优选的示例性组合包括碳/x材料,其中x可以是一种或多种选自锑、锡、磷、硫、硼、铝、镓、铟、锗、铅、砷、铋、钛、钼、硒、碲、硅、碳和镁的元素的氧化物。
33.在一些实施方案中,所述一次含碳材料可含有可在最终含碳阳极材料中充当掺杂剂的一种或多种金属离子和/或非金属离子。这些金属离子和/或非金属离子可以在用如下所述的碳化材料处理之前添加到一次含碳材料中,或者在热解之前添加到用于制备一次含碳材料的碳基起始材料中。供选择地,一种或多种金属离子和/或非金属离子可以在热解之前选择性地保留在碳基起始材料中,并将因此被携带进入一次含碳材料。
34.已经使用bet技术研究根据本发明的含碳阳极材料的表面特性,以确定开口微孔的比表面积,所述开口微孔是具有在含碳阳极材料的表面处形成的开着的入口的微孔。在本文中,“表面”字面上在含碳阳极颗粒的外部,并且没有深入到含碳阳极颗粒的主体中。表示为“微孔”的孔是具有小于2nm的直径的那些,并且它们不同于为具有约2nm至50nm的直径
的孔的“中孔”。
35.本技术人已经发现,在使用根据本发明的表面设计的含碳阳极材料的电化学电池的情况下,可以实现显著改善的电化学性能,所述表面设计的含碳阳极材料具有如使用氮气bet分析测定的大于0m2/g最高达最大值5m2/g、优选最高达最大值0.9、特别优选最高达最大值0.5m2/g、高度优选最高达最大值0.3m2/g、最优选最高达最大值0.15m2/g的开口微孔比表面积。
36.如上所述,当一种或多种一次含碳材料(其为固体形式,并且优选颗粒、粒状或粉末状形式)用碳化材料处理时,方便地制备根据本发明的表面设计的含碳阳极材料。该处理导致优选化学键合到一次含碳材料上的碳化材料,更优选化学沉积到一次含碳材料上的碳化材料,根据本发明优选通过使用化学气相沉积化学沉积到一次含碳材料上的碳化材料。
37.然而,本发明不限于使用化学气相沉积。实际上,技术人员将意识到将材料化学键合到一次基材的替代方法。这些方法的实例可以包括等离子体增强沉积、原子层沉积和物理气相沉积。
38.这里所指的“碳化材料”是优选衍生自一种或多种二次含碳材料的富碳固体物质。最特别地,本发明采用这种碳化材料作为一种或多种一次含碳材料外表面上的极薄沉积物。尽管碳化材料优选基本均匀地沉积在内核表面上,重要的是注意到沉积物可以不必是完整层或均匀涂层的形式(即一次含碳材料和沉积的碳化材料可以不必是核/全壳型排列)。然而,沉积的材料优选具有1nm至小于500nm,更优选从10nm至小于500nm,并且高度优选从10nm至250nm的厚度。理想地,一种或多种一次含碳材料的外表面的表面积的10%至90%将被衍生自一种或多种二次含碳材料的碳化材料覆盖。沉积物的质量也极小(一般每30分钟沉积2.2
±
0.8重量%)。因此,碳化材料基本上不改变如上所讨论的一种或多种一次含碳材料的粒度分布。
39.优选衍生碳化材料的合适的二次含碳材料可以选自一种或多种有机和/或烃材料例如烷烃、烯烃、炔烃或芳烃,其可以是直链、支链或环状的。所述二次含碳材料本身可衍生自煤基或石油基的焦油或沥青、油或植物基材料。包含一种或多种具有以下通式的气态烃的二次含碳材料的是特别优选的:c
nh2n+2
,其中1≤n≤10。
40.在一个实施方案中,优选衍生碳化材料的二次含碳材料可以包括在从约950℃或更低的至少一个温度下的蒸气相和/或液相和/或气相。优选地,在约200℃或更高至约950℃或更低的至少一个温度下的蒸气相和/或液相和/或气相。
41.发现本发明的含碳阳极材料的开口微孔的比表面积显著低于在用例如衍生自一种或多种二次含碳材料(如上所述)的碳化材料处理之前的一次含碳材料的开口微孔的比表面积。据信这是由于至少一部分的含碳阳极材料的开口微孔(即表面处的开口微孔)的入口被沉积的碳化材料“掩蔽”或“堵塞”。优选地,与用碳化材料处理之前的一次含碳材料的开口微孔的表面积相比,衍生自一种或多种二次含碳材料的化学沉积的碳化材料的存在导致含碳阳极材料的表面微孔的表面积减少至少40%,进一步优选至少50%,以及特别优选至少85%。开口微孔表面积的高度减少似乎支持申请人目前的理解,即沉积的碳化材料仅堵塞表面(开口)微孔,此外,该观点进一步被以下事实支持:在用碳化材料处理后,没有测量到一次含碳材料的显著的重量增加。
42.如上所公开的,本发明提供一种含碳阳极材料,其包括沉积或部分沉积在一次含
碳材料的外表面上的碳化材料。
43.碳化材料可以是“软”含碳物质,其在某种程度上将通过碳化过程石墨化,并且石墨化材料的存在可以通过例如拉曼光谱、x射线衍射或高分辨率透射电子显微镜来证实。然而,重要的是控制含碳阳极材料的形成,使得其具有适合于其所用于的特定电池的化学性质的石墨化程度。例如,在na离子电池的情况下,石墨化高度优选地限于在常规的硬碳材料中经常观察到的水平,即,因为石墨对钠的电化学活性低得多,出于可逆嵌钠的目的,期望避免在一次含碳材料的表面上的高度石墨化的含软碳物质。然而,对于锂离子电池,情况将是相反的。
44.必须小心以避免形成高度石墨区域,因为这些催化各种寄生反应(如当在电解质组合物中使用碳酸丙烯酯(pc)时)。因此,发现极端退火不会提高碳阳极效率。另一方面,发现根据本发明的表面处理系统地改善含碳阳极材料的效率,而与电解质体系无关。然而,本发明的方法不影响封闭的孔的体积。这从以下事实是明显的:用碳化材料处理前和处理后的一次含碳材料产生类似的(脱)嵌钠电位曲线。
45.根据本发明的含碳阳极材料的表面的另一优选特性是极低的表面氧化程度。已知在含碳材料的表面上具有含氧基团(例如c-o、c=o和c(=o)oh官能团)的化合物的存在易于充当用于引入的载荷子的永久锚定点和充当用于不期望的寄生反应的平台;当这些含碳材料用作阳极材料时,这两个因素都将潜在地有助于首次循环损失。有利地,根据本发明的含碳阳极材料具有使用x射线光电子能谱(xps)测量的从0原子百分比(atm.%)至小于2.5atm.%、优选从0atm.%至小于1.5atm.%、以及高度优选从0atm.%至小于1atm.%的表面氧含量。因此,用例如根据本发明的衍生自一种或多种二次含碳材料的碳化材料处理一种或多种一次含碳材料,具有将一次含碳材料的表面氧含量降低至少30atm.%、优选至少50atm.%、以及进一步优选至少90atm.%的效果。在一些实施方案中,可以降低接近100atm.%的表面氧原子。
46.含碳阳极材料的比表面积总体上也通常被认为是影响首次循环损失的不可逆容量程度的另一个有用因素;比表面积越高,阳极材料使sei层过度稳定的敏感性越高,从而增加不可逆容量。然而,在本发明的情况下,尽管用例如衍生自一种或多种二次含碳材料的碳化材料处理一种或多种一次含碳材料确实使含碳阳极材料的比表面积降低约30%,这种降低并不像可以最高达87%之多的表面微孔表面积的降低那样显著。本技术中给出的所有比表面积值都是使用bet n2分析测定的。图1在以下实验部分详细讨论以解释根据本发明的含碳阳极材料的表面如何能够产生所观察到的开口(表面)微孔表面积的显著减小的机理,同时记录总表面积的最小降低。
47.根据本发明,通过使一种或多种一次含碳材料与碳化材料(例如衍生自一种或多种二次含碳材料)接触,用一种或多种二次含碳材料处理一种或多种一次含碳材料,以获得期望的表面设计的含碳阳极材料。
48.使一次含碳材料与碳化材料接触可以使用任何合适的方法实现,诸如使一次含碳材料直接与碳化材料接触或使一次含碳材料与一种或多种二次含碳材料接触,然后促进由一种或多种二次含碳材料形成碳化材料。
49.合适地,使一次含碳材料与一种或多种二次含碳材料接触可以涉及溶剂介导的步骤,其中将固体一次碳基材料与二次含碳材料溶解/分散于其中的一种或多种溶剂和/或其
它液体混合,然后在二次含碳材料的碳化之前除去溶剂/分散剂。供选择地,在二次含碳材料碳化之前,可以使用机械化学步骤,其中将一种或多种一次和二次含碳材料混合在一起(没有溶剂或其它分散剂或具有有助于混合的试剂)。或者进一步供选择地,使用基于扩散的系统,其中使一种或多种以固体形式的一次含碳材料与一种或多种以蒸气和/或气态形式的二次含碳材料接触,随后加热以碳化二次含碳材料。
50.在第二方面,本发明提供一种用于制备能够嵌入和脱嵌碱金属离子并且具有碳结构的含碳阳极材料的方法,所述方法包括:在最高达950℃的温度下,使包含一种或多种以固体形式的一次含碳材料的核与碳化材料接触,从而产生具有如使用氮气bet分析测定的0m2/g至5m2/g的开口微孔比表面积的含碳阳极材料。
51.在一个实施方案中,外表面可以被设计成表现出如使用氮气bet分析测定的大于0m2/g至5m2/g的开口微孔比表面积。
52.理想地,所述核不由或基本上不由一种或多种选自石墨和具有完全石墨结构的材料的一次含碳材料组成。在一个实施方案中,所述核可基本上由所述一种或多种一次含碳材料组成,并且优选可由所述一种或多种一次含碳材料组成。
53.所述一种或多种固体一次含碳材料优选地为如上所述的任何颗粒形式(例如颗粒或粉末)。在一个实施方案中,所述一种或多种一次含碳材料的粒度分布为从约1nm至约30μm,也如上所述。用于本发明的方法的合适的一次含碳材料是上文参照根据本发明的含碳阳极材料描述的那些。
54.加热条件将被选择为i)(在当碳化材料在与一次含碳材料接触之前预先形成的情况下)以促进碳化材料在一次含碳材料的表面上的气相沉积,或ii)以促进已经在一次含碳材料的表面上的一种或多种二次含碳材料的碳化,或iii)以促进一种或多种二次含碳材料的碳化和随后的所得碳化材料在一次含碳材料的表面上的沉积。
55.在每种情况下,最终结果将是在一种或多种一次含碳材料和一种或多种碳化材料之间形成诸如共价键的化学键。因此,一种或多种碳化材料将化学键合在一种或多种一次含碳材料的表面上,优选化学沉积在一种或多种一次含碳材料的表面上。
56.优选地,所使用的温度低于将导致碳化材料过度石墨化的温度,尤其是(如上所讨论的)当所得含碳阳极材料用于钠离子电池中时。然而,重要的是,根据本发明的方法所使用的温度将导致碳化材料化学键合到一次含碳材料上。
57.如上所述,因此,优选衍生碳化材料的二次含碳材料可以包括在从约950℃或更低的至少一个温度下的蒸气相和/或液相和/或气相。优选地,在约200℃或更高至约950℃或更低的至少一个温度下的蒸气相和/或液相和/或气相。
58.930℃的最高温度是优选的,900℃的最高温度是高度优选的,以及880℃的最高温度是特别优选的。最低加热温度是将能够发生碳化的任何温度,并且其将取决于所使用的二次含碳材料。200℃的最低温度通常是足够的,但是如果使用催化剂或其它试剂来降低热催化分解和碳化二次含碳材料所需的活化能,更低的温度也可以是可能的。可能的催化剂包括少量的一种或多种诸如过渡金属或过渡金属氧化物的金属化合物或金属氧化物化合物。
59.如上所述,优选衍生碳化材料的合适的二次含碳材料可以选自一种或多种有机和/或烃材料例如烷烃、烯烃、炔烃或芳烃,其可以是直链、支链或环状的。所述二次含碳材
料本身可衍生自煤基或石油基的焦油或沥青、油或植物基材料。包含一种或多种具有以下通式的气态烃的二次含碳材料是特别优选的:c
nh2n+2
,其中1≤n≤10。
60.在本发明的优选方法中,当一次含碳材料与流体的(液体、蒸气或气体)二次含碳材料或流体的(液体、蒸气或气体)预形成的碳化材料接触时,反应物的总压力、总流速以及单独的分压和单独的流速被优化以确保正确量的碳化材料沉积在一次含碳材料上。二次含碳材料的优选的总压力、总流速和单独的分压以及单独的流速分别在10-6
至3
×
107pa、0.001至1000l/min、10-6
至3
×
107pa和0.001至1000l/min的范围内,并且进一步优选在104至106pa、0.01至100l/min、104至106pa和0.01至100l/min的范围内,并且高度优选分别在5
×
104至5
×
105pa、0.1至10l/min、5
×
104至5
×
105pa和0.1至10l/min的范围内。
61.注射碳气相沉积(cvd)系统和气溶胶辅助反应器是设置的实例,其中单独的流体前体的压力和流速可被控制。
62.在本发明的进一步优选的方法中,用于与一种或多种一次含碳材料接触的碳化材料的浓度和/或一种或多种二次含碳材料的浓度在用于气态二次含碳材料的载气中优选在0.001-100体积%,优选0.01-10体积%,进一步优选0.01至5体积%和高度优选0.05-0.1体积%的范围内,并且在用于液体和半固体(如沥青、焦油、油)二次含碳材料的溶剂或载体液体中优选在0.001-100体积%的范围内。
63.在本发明的另一进一步优选方法中,加热步骤的持续时间(退火时间)也优选调节为i)最小化,以及优选防止碳化材料的过度石墨化;加热时间越长,碳化材料越可能过度石墨化;和ii)确保其足够长以化学沉积足够的碳化材料以堵塞至少一部分的开口微孔,如上所讨论的。
64.如上所述,本发明的方法不限于使用化学气相沉积。实际上,技术人员将意识到将材料化学键合到一次基材的替代方法,并且这些方法包括在本发明的范围内。这些方法的实例可以包括等离子体增强沉积、原子层沉积和物理气相沉积。
65.5分钟至120分钟的退火时间是优选的,30分钟至90分钟的退火时间是尤其优选的。退火时间是碳化材料沉积在一次含碳材料上所需的时间。
66.在本发明的特别优选的方法中,使一种或多种以固体形式的一次含碳材料与碳化材料接触的步骤是使用确保一次含碳材料的每个颗粒的表面的至少一部分与碳化材料接触所需的任何方法进行。合适的方法包括:当与碳化材料接触时搅拌或搅动一次含碳材料,将一次含碳材料的颗粒喷入含有气化的碳化材料的气氛中,和在引入碳化材料之前在平板或广口反应容器上铺展一次含碳材料。
67.此外,在本发明的特别优选的方法中,期望在本发明的方法的最后阶段进行使一种或多种以固体形式的一次含碳材料与碳化材料接触的步骤。更特别地,高度期望的是,在对一种或多种一次含碳材料进行任何研磨处理(如碾磨、研磨、压碎等)之后进行该步骤。这有利地避免包括化学键合在一种或多种一次含碳材料上的一种或多种碳化材料的外表面被干扰。例如,包括研磨处理的后表面处理可使钝化表面裂开并暴露微孔。
68.为了避免任何疑问,在该短语的含义内,诸如将活性材料与粘合剂混合、电极印刷(如涂覆)和电极压延(如轧制)的后表面处理步骤不被认为是“研磨处理”。
69.根据本发明的含碳阳极材料适合用作二次电池应用中的电极活性材料,尤其是在碱金属离子电池中,并且特别是在钠离子电池中。
70.在第三方面,本发明提供一种碱金属离子电池,其包括至少一个如上所述的负极(阳极)。优选地,所述负极(阳极)具有使用氮气bet分析测定的从大于0m2/g至5m2/g的开口微孔比表面积。
71.所述碱金属离子电池将还包括正极(阴极),其优选包含一种或多种能够嵌入和脱嵌碱金属的正极活性材料,并且其优选选自氧化物基材料、聚阴离子材料和普鲁士蓝类似物基材料。特别优选地,所述一种或多种正极活性材料包含一种或多种选自含碱金属的氧化物基材料和含碱金属的聚阴离子材料,其中碱金属是选自钠和/或钾的一种或多种碱金属,并且任选地与锂结合。某些正极活性材料含有作为少量碱金属成分的锂,即锂的量小于总碱金属含量的50重量%,优选小于总碱金属含量的10重量%,以及理想地小于总碱金属含量的5重量%,
72.最优选的正极活性材料是以下通式的化合物:
73.a1±
δm1vm2wm3xm4ym5zo2-c
74.其中
75.a为选自钠、钾和锂的一种或多种碱金属;
76.m1包括一种或多种+2氧化态的氧化还原活性金属,
77.m2包括氧化态大于0至小于或等于+4的金属;
78.m3包括+2氧化态的金属;
79.m4包括氧化态大于0至小于或等于+4的金属;
80.m5包括+3氧化态的金属;
81.其中
82.0≤δ≤1;
83.v>0;
84.w≥0;
85.x≥0;
86.y≥0;
87.w和y中至少一个>0
88.z≥0;
89.c在0≤c《2的范围内;
90.其中选择v、w、x、y、z和c以保持电化学中性。
91.为了避免疑问,术语“选自钠、钾和锂的一种或多种碱金属”应解释为包括:na、k、li、na+k、na+li、k+li和na+k+li。
92.理想地,金属m2包括一种或多种过渡金属,并且是优选选自锰、钛和锆;m3优选为选自镁、钙、铜、锡、锌和钴中的一种或多种;m4包括一种或多种过渡金属,优选选自锰、钛和锆;以及m5优选为选自铝、铁、钴、锡、钼、铬、钒、钪和钇中的一种或多种。可使用具有任何晶体结构的阴极活性材料,并且优选该结构将为o3或p2或其衍生物,但具体地,还可能的是,阴极材料将包括相的混合物,即其将具有由几种不同晶体形式组成的非均匀结构。
93.高度优选的正极活性材料包括含钠和/或钾的含过渡金属的化合物,其中钠过渡金属镍酸盐化合物是尤其优选的。特别有利的实例包括碱金属-层状氧化物,单相和混合相o3、p2和p3碱金属-层状氧化物,含碱金属的聚阴离子材料,金属氧酸盐普鲁士蓝类似物
(oxymetallates prussion blue analogs)和普鲁士山白色类似物(prussioan white analogs)。具体实例包括o3/p2-a
0.833
ni
0.317
mn
0.467
mg
0.1
ti
0.117
o2,o3-a
0.95
ni
0.3167
mn
0.3167
mg
0.1583
ti
0.2083
o2,p2-型a
2/3
ni
1/3
mn
1/2
ti
1/6
o2,p2-a
2/3
(fe
1/2
mn
1/2
)o2,p’2-a
2/3
mno2,p3或p2-a
0.67
mn
0.67
ni
0.33
o2,a
3v2
(po4)3,avpo4f,avpo4f,a
3v2
(po4)3a
3v2
(po4)2f3,a
3v2
(po4)2f3,a
x
feymny(cn)6.nh2o(0≤x,y,z≤2;0≤n≤10),o3,p2和/或p3-a
x
mnynizo2(0≤x≤1和0≤y,z≤1),a2fe2(so4)3,a2ni2sbo6和a3ni2sbo6,其中“a”是选自li、na和k的一种或多种碱金属的这些化合物,优选为na和/或k,最优选为na。
94.有利地,根据本发明的碱金属离子电池可以使用以任何形式的电解质,即,可以使用固体、液体或凝胶组合物,并且合适的实例包括;1)液体电解质,诸如>0至10摩尔的碱金属盐,诸如napf6、nabf4、双(草酸)钠(nabob)、三氟甲磺酸钠(naotf)、lipf6、liasf6、libf4、libob、liclo4、lifsi、litfsi、三氟甲磺酸锂及其混合物,其在一种或多种选自碳酸亚乙酯(ec)、碳酸二乙酯(dec)、碳酸亚丙酯(pc)、(优选比例为1:2:1重量/重量的ec:dec:pc作为混合物)、γ-丁内酯(gbl)环丁砜、二甘醇二甲醚、三甘醇二甲醚、四甘醇二甲醚、二甲基亚砜(dmso)、二氧戊环及其混合物的溶剂中,所有这些物质都具有/不具有诸如hfe(1,1,2,2-四氟乙基2,2,3,3-四氟丙基醚)或d2(1,1,2,2-四氟乙基2,2,2-三氟乙基醚))的稀释剂;2)基于单独或彼此结合使用的以下基体材料中的任一种的凝胶电解质;或3)固体电解质,诸如:诸如na3zr2si2po
12
的nasicon型,诸如na3ps4或na3sbs4的硫化物基,诸如na2b
10h10-na2b
12h12
的氢化物基或诸如na2o.(8-11)al2o3的β-氧化铝基或诸如na2o.(5-7)al2o3的相关的β"-氧化铝基)。诸如1,3-丙二醇环硫酸酯(pcs)、p123表面活性剂、三(三甲基甲硅烷基)亚磷酸酯(tmsp)、三(三甲基甲硅烷基)硼酸酯(tmsb)、1-丙烯-1,3-磺内酯、1,3-丙磺酸内酯的已知的电解质添加剂也可以包括在电解质中,诸如聚偏二氟乙烯(pvdf)、聚偏二氟乙烯-六氟丙烯(pvdf-hfp)、聚(甲基丙烯酸甲酯)(pmma)、羧甲基纤维素钠(cmc)和苯乙烯-丁二烯橡胶(sbr)的粘合剂也可以包括在电解质中。
95.应注意,除了是优异的阳极材料之外,本发明的表面设计的含碳材料还提供另外的商业的优点。
96.这些优点中的第一个涉及改善的水分敏感性。由于本发明的表面设计的含碳阳极材料极低水平的开口微孔性,本发明的表面设计的含碳阳极材料在暴露时比非表面设计的一次含碳材料吸收显著更少的大气水分。这不仅使得在阳极制备期间更容易处理申请人的阳极材料,而且还降低所得阳极涂层和成品电池的水分含量。
97.第二个意想不到的优点涉及电极浆料粘度的改善,所述电极浆料含有根据本发明的含碳阳极材料。在电池制备期间,电极浆料的粘度不应被忽略,因为这将对过程的平稳运行和所得电极的质量控制产生重要差异。电极材料(活性物质、粘合剂和添加剂)是一般混合并分散在有机或水性溶剂中,使得它们可以涂覆在集流体上。在涂覆过程中,溶剂蒸发并留下干组分。粘度不足导致浆料太松软,并且这可能导致未对准的涂层边缘;同时,过度粘稠的浆料将造成过程问题,因为浆料将不能如其应该的那样平稳地运行。这不利地影响干燥涂层的质量。一般地,具有减小的表面积的电极材料需要较少的溶剂以实现给定的最优粘度。从成本的观点来看,这是有利的。因此,由于根据本发明的表面设计的含碳阳极材料较低的微孔表面积,根据本发明的表面设计的含碳阳极材料对于相同的固体含量表现出较低的粘度,并且这产生更平滑的表面形态和更纯的表面化学。通过使用较少的溶剂可以节
省成本,以获得良好质量的电极。
98.如以下讨论的具体实例中所证明的,使用根据本发明的含碳阳极材料可以实现有利的电化学性能改善,可以总结如下:i)以含碳材料为特征的na离子全电池的不可逆容量和首次循环损失是分别低至25.2mah/g和8.6%。与从以常规硬碳阳极和其它相同化学和组分为特征的基准电池分别获得的54.9mah/g和16.8%的值相比,这是显著的降低;ii)以本发明的含碳阳极材料为特征的na离子全电池在最高达
±
3c的更快充电和放电速率下显示出显著改善的容量保持和循环稳定性;iii)根据本发明的含碳阳极材料具有降低的水分吸附速率,并且以这些含碳阳极材料为特征的na离子全电池由于其降低的总水分含量而具有改善的循环稳定性。
99.附图简述
100.现在将参考以下附图描述本发明,其中:
101.图1示出原始一次含碳材料的颗粒和根据本发明的表面设计的含碳阳极材料的颗粒的示意图表示。
102.图2示出说明本发明优选方法的流程图。
103.图3是柱状图,其说明与根据本发明的用碳化材料处理的相同的含硬碳材料相比,在原始含硬碳材料上存在的表面氧的量(atm.%)。
104.图4是柱状图,其说明与根据本发明的用碳化材料处理的相同的含硬碳材料相比,原始的含硬碳材料的bet比表面积(m2/g)。
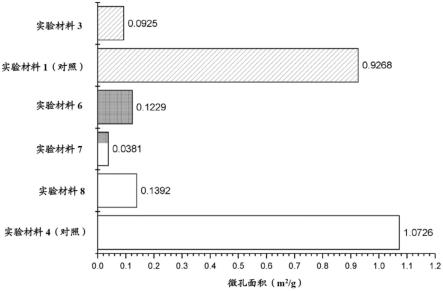
105.图5是柱状图,其说明与根据本发明的用碳化材料处理的相同的含硬碳材料相比,原始的含硬碳材料的bet微孔表面积(m2/g)。
106.图6示出根据本发明的样品材料8的代表性t曲线图。
107.图7示出对于使用根据本发明的含碳阳极材料3的na离子半电池获得的电压相对于na
+
/na容量曲线。
108.图8示出对于使用根据本发明的含碳阳极材料8的na离子半电池获得的电压相对于na
+
/na容量曲线。
109.图9示出对于使用含碳阳极材料4(对照)的na离子半电池获得的电压相对于na
+
/na容量曲线。
110.图10示出对于使用根据本发明的含碳阳极材料7的三电极全电池获得的电压相对于容量曲线。
111.图11示出对于使用根据本发明的含碳阳极材料8的三电极全电池获得的电压相对于容量曲线。
112.图12示出对于使用根据本发明的含碳阳极材料6的三电极全电池获得的电压相对于容量曲线。
113.图13说明包括含碳阳极材料8的全钠离子电池在快速放电时的阴极比容量、循环寿命性能和库仑效率。
114.图14说明包括含碳阳极材料8的全钠离子电池在快速放电时的阴极比容量、循环寿命性能和库仑效率。
115.图15说明包括含碳阳极材料6和8的全钠离子电池在快速放电时的阴极比容量、循环寿命性能和库仑效率。
116.图16说明包括含碳阳极材料8的全钠离子电池在快速充电时的阴极比容量。
117.图17示出水分含量相对于空气暴露时间的曲线图,以说明与材料4(对照)相比,通过根据本发明制备的材料6、7、8、9和10的含碳阳极材料表现出的降低的对水分的敏感性。
118.图18是柱状图,以说明与材料4(对照)相比,使用根据本发明制备的含碳阳极材料7、8和10制备的电极对水分的敏感性。
119.图19示出使用一次含硬碳材料的激光衍射获得的各种粒度分布。
120.图20示出一次含硬碳材料的扫描电子显微图像。
121.详述
122.对根据本发明的含碳阳极材料的结构提出的模型
123.图1示出包括含有一次含碳材料1的核的原始含碳材料的颗粒的示意图表示。图1进一步示出包括含有一次含碳材料1的核和含有化学键合在一次含碳材料1上的碳化材料35的外表面15的根据本发明的表面设计的含碳阳极材料10(即非原始的)的颗粒的示意图表示。更特别地,图1提供帮助以解释所提出的机理,该机理用于解释根据本发明的表面设计的含碳阳极材料10如何可能表现出显著降低的开口微孔表面积,同时记录总表面积的最小降低。图1也可以帮助解释,与包括含有一次含碳材料1的核的原始含碳材料相比,根据本发明的表面设计的含碳阳极材料10如何具有更大的耐水分吸附性。
124.如图1所描绘的,包括含有具有开口孔隙率的一次含碳材料1的核的原始含碳材料的代表性颗粒具有有多个开口中孔20和多个开口微孔25形成的不规则且不均匀的外表面15。在例如根据本发明的方法处理包括含有一次含碳材料1的核的原始含碳材料之后,将碳化材料35(例如衍生自二次含碳材料)的颗粒的不均匀、不完整和极薄层30沉积在包括含有一次含碳材料1的核的原始含碳材料的外表面15上,以制备根据本发明的表面设计的含碳阳极材料10。
125.如图1所示,许多开口微孔25的入口被形成极薄层30的碳化材料35的沉积颗粒堵塞。在图1中,表面设计的含碳阳极材料10上的堵塞的微孔用55表示。应理解,不均匀、不完整的层30的极薄度将使足以覆盖/堵塞较大中孔20的入口是高度不可能的,但层30可改为部分地涂覆中孔的内部,这可降低这些孔的表面积,但仅是轻微地。
126.根据本发明的表面设计的含碳阳极材料增加的疏水性还可通过以下事实来解释,即与能够进入原始的一次含碳材料1中的开口微孔25的水分子40的数量相比,能够进入堵塞或阻塞的微孔55的水分子40a的数量减少,从而使得根据本发明的表面设计的含碳材料10比非表面设计的材料更耐水分。这在下面研究。
127.根据本发明制备含碳阳极材料的普通方法
128.图2提供说明本发明的普通方法的示意性流程图。在一般的方法中,一种或多种以颗粒形式的一次含碳材料在200至950℃下用碳化材料处理30-120分钟,如上所讨论的,所述碳化材料可以是预先制备的碳化材料,或者其可以是衍生自一种或多种二次含碳材料的碳化材料。理想地,处理过程在惰性气体气氛中进行。进一步理想地,一种或多种二次含碳材料以所需浓度提供(如上所讨论的),并且气态二次含碳材料优选在载气(优选惰性载气)中提供,并且液态二次含碳材料优选在载体溶剂或其它载体液体中提供。
129.测试的含碳阳极材料的细节在下表1中给出:
130.表1
[0131][0132][0133]
一次含碳材料尺寸的测量
[0134]
使用激光衍射和扫描电子显微镜进行一次含硬碳材料的尺寸测量。获得的结果分别示于图19和20中。结果表明以下一次含碳材料的优选粒度分布:
[0135]
参数优选的下端点优选的上端点d10[μm]0.014d50[μm]415d90[μm]1530
[0136]
当所述一种或多种一次含碳材料包括一种或多种由(碳)-x表示的碳复合材料时,如本文所公开的,在一些情况下,粒度分布可以是不同于上面指出的那些。这是因为一些复合材料的尺寸可以是在纳米级范围内。因此,在一个实施方案中,本发明的一次含碳材料的粒度分布为从约1nm至约30μm,优选为从约1nm至约20μm。
[0137]
就申请人所知,本发明的表面处理基本上不改变一次含碳材料的粒径粒度分布。在本发明的一个实例中,发现二次含碳材料的质量沉积物是非常少的(每30分钟的沉积2.2
±
0.8重量%)。因此,表面处理后的一次含碳材料的粒度分布可被认为与表面处理前的一次含碳材料的粒度分布基本相同。
[0138]
根据本发明的含碳阳极材料的图形化特性的测量
[0139]
如上所讨论的,控制沉积在一次含碳材料外表面上的碳化材料的石墨化水平以匹配使用阳极材料的电池化学的要求是重要的。下表3比较根据本发明的表面设计的含碳阳极材料的石墨化特性(在堆叠(lc)和平面内(la)方向上的石墨间距和微晶尺寸)与非表面设计的一次含碳材料(即用于制备一次含碳材料的起始材料)的石墨化特性。
[0140]
从表3的结果可以看出,根据本发明的表面设计的存在对石墨化程度没有显著影响,因此,预期阳极材料3、6-11和14是高度适用于钠离子电池的。
[0141]
表面氧含量(atm.%)的测量
[0142]
使用xps测量i)根据本发明的含碳阳极材料和ii)与碳化材料接触之前的一次含碳材料的表面上存在的氧的量,分析规格总结在下表2中。表面氧含量结果示于图3中。
[0143]
表2
[0144][0145]
bet表面积的测量(m2/g)
[0146]
使用micromeritics gemini vii 2390表面积分析仪、使用氮气作为吸附物在液氮温度下进行bet分析。在分析前,所有样品在250℃下在流动的氮气下脱气过夜。获得的结果示于图4中。
[0147]
bet微孔表面积的测量(m2/g)
[0148]
通过应用模型,从被材料吸附的气体体积,可以估算气体可进入的微孔(开口微孔,也称为含碳阳极材料表面的微孔)的表面积,计算为每克含碳阳极材料(或在对照样品的情况下,原始的含硬碳材料)的微孔表面积。这是从't-曲线'分析中获得的。一般的t-曲线由在标准温度和压力下吸附的气体的量相对于harkins和jura根据harkins和jura厚度方程(t=[13.99/(0.034-log(p/p
°
))]^0.5)统计的厚度(nm))组成。外表面积与bet(总)表面积之差为估计的微孔表面积。获得的结果示于图5中。材料8的代表性t-曲线示于图6中。
[0149]
水分含量(ppm)的测量
[0150]
活性材料和阳极电极(涂层)的水分含量使用来自mitsubishi chemical analytech滴定器的ca-200型水分测量仪(库仑滴定)在没有任何暴露(0分钟)的情况下和暴露于具有20-50%相对湿度的大气中30和60分钟之后测量。
[0151]
结果
[0152]
下表3总结如上所述获得的石墨化特性、表面氧含量、bet表面积、微孔表面积和水分含量结果。
[0153]
表3
[0154][0155]
使用xrd的产物分析
[0156]
使用siemens(rtm)d5000粉末衍射仪进行x射线衍射分析,以确认已经制备所需的目标材料,确定产物材料的相纯度并确定存在的杂质类型。从该信息可以确定晶胞的晶格参数。
[0157]
用于分析材料的普通xrd操作条件如下:
[0158]
狭缝尺寸:1mm
[0159]
量程:2θ=10
°‑
60
°
[0160][0161]
速度:1.0秒/步
[0162]
增量:0.025
°
[0163]
电化学结果
[0164]
通过溶剂浇铸包含重量比为92:6:2的实验含碳材料(如上所述)、粘合剂和溶剂的浆料制备包括根据本发明制备的含碳材料的阳极。诸如c5
tm
碳(timcal)(rtm)的导电碳可以包括在浆料中。pvdf和丁苯橡胶/羧甲基纤维素(sbr/cmc)是合适的粘合剂,并且n-甲基-2-吡咯烷酮(nmp)或水可以用作溶剂。然后将浆料浇铸到集电箔(如原始的涂覆碳的铝箔)上并加热,直到大部分溶剂蒸发并形成电极膜。然后在约120℃的动态真空下进一步干燥阳极电极,并压延至所需厚度。
[0165]
电池测试
[0166]
对于半电池测试,实验含碳阳极电极与作为参比和对电极的一个钠金属盘配对。玻璃纤维gf/a用作隔板,并且还使用合适的电解质。可以使用任何合适的na离子电解质,优选其可以包含一种或多种盐,例如napf6、naasf6、naclo4、nabf4、nascn和三氟甲磺酸钠,与一种或多种有机溶剂,例如ec、pc、dec、dmc、emc、甘醇二甲醚、酯、乙酸酯等组合。还可以加入诸如碳酸亚乙烯酯和碳酸氟代亚乙酯的其它添加剂。优选的电解质组合物包含0.5m napf6/ec:pc:dec。
[0167]
所有电池在循环前静置24小时。对于三电极测试,根据本发明的含碳阳极材料作为负极,标准氧化物材料作为正极,并且使用一片钠作为参比,所有三个电极都通过相同的电解质润湿。两个24.5μm厚的聚乙烯膜作为隔板。
[0168]
使用恒定电流循环技术测试半电池,并且使用恒定电流-恒定电压技术测试三电极电池。
[0169]
电池在预设电压极限之间的给定电流密度下循环。使用来自mti inc.(richmond,ca,usa)或maccor(tulsa,ok,usa)的商业电池循环仪。在充电时,碱离子嵌入含碳阳极材料中。在放电期间,碱离子从阳极被脱嵌并重新嵌入到阴极活性材料中。
[0170]
结果
[0171]
实验含碳阳极材料3-半电池(相对于na
+
/na)的电化学测试
[0172]
图7示出作为阳极比容量的函数的阳极嵌钠和脱钠电位曲线。使用根据本发明的实验含碳阳极材料3作为实例,可实现315mah/g的可逆脱钠容量与36.0mah的不可逆比容量以及89.8%的首次循环库伦效率。
[0173]
实验含碳阳极材料8-半电池(相对于na
+
/na)的电化学测试
[0174]
图8示出作为阳极比容量的函数的阳极嵌钠和脱钠电位曲线。使用根据本发明的实验含碳阳极材料8作为实例,可实现大于330mah/g的可逆比容量与29.1mah的不可逆比容量以及91.9%的首次循环库伦效率。
[0175]
对照阳极材料4(对照)-半电池(相对于na
+
/na)的电化学测试
[0176]
图9示出作为阳极比容量的函数的阳极嵌钠和脱钠电位曲线。使用根据本发明的对照阳极材料4作为实例,获得281mah/g的可逆比容量与58.6mah的不可逆比容量以及
82.8%的首次循环库伦效率。比较这些值与实验含碳阳极材料8的那些值(图7相对于图8),显然根据本发明的表面处理导致显著改善的电化学性能。
[0177]
实验含碳阳极材料6、7和8的三电极全电池的电化学测试
[0178]
图10-12示出在三个电压窗口:1.0-4.2v、1.0-4.1v和1.0-4.0v下阳极和阴极嵌钠和脱钠电位曲线以及作为电池容量的函数的电池电压。电池分别以实验含碳阳极材料7、8和6为特征。三电极全电池研究的目的是测量用最大电荷的阳极电位,并研究阳极表面上枝晶形成的可能性。在所有电压窗口中用最大电荷的阳极电位是安全地正的这一事实表明,以含碳材料为特征的na离子电池没有枝晶形成的风险。由于在阳极和阴极之间存在na金属参比,这种三电极全电池设计对于实现最高的首次循环库伦效率不是最优的。因此,在0.1ah全电池中进一步测试含碳阳极材料以验证真实的首次循环库伦效率值。
[0179]
实验含碳阳极材料6-11和4(对照)-全电池的电化学测试
[0180]
图13和14示出以实验含碳阳极材料8作为阳极为特征的两个可比的电池的库伦效率和阴极放电比容量作为循环次数的函数。在c/10充电和放电的四个形成循环之后,图13中的电池以c/5充电,并以从c/5直到3c的各种速率放电,而图14中的电池按照相同的形成方案以从c/5至3c的各种速率充电,并以c/5放电。两个电池均具有》90%的首次循效率,并且在快速充电/放电循环之后表现出》98%的容量保持率。这表明根据本发明的含碳阳极材料具有优异的快速充电和快速放电能力。这可能是由于本发明的材料的增强的电荷载流子特性。
[0181]
图15比较在三个不同电压窗口下的以实验含碳阳极材料6和8为特征的三个电池的循环稳定性。在c/10充电和放电的四个形成循环之后,所有三个电池以c/5和c/2充电和放电(每次四个循环),然后以1c充电和放电。所有三个电池都具有约89%的首次循环效率。以实验含碳阳极材料6为特征的电池在1.0-4.0v和1.0-4.1v下循环。以实验含碳阳极材料8为特征的电池在1.0-4.2v下循环。
[0182]
表4总结以各种实验含碳阳极材料为特征的全电池的fcl、阳极不可逆比容量和阴极可逆比容量。
[0183]
表4
[0184][0185]
为了理解真正的性能改善(降低的阳极不可逆比容量和首次循环损失),按照与用于以实验含碳阳极材料6-11为特征的全电池相同的方案对四个以含碳阳极材料4(对照)为
特征的同类的基准全电池进行充电和放电,首次循环损失、阳极不可逆比容量和阴极可逆比容量值总结于表4中。
[0186]
从表4可以看出,以含碳阳极材料4为特征的基准全电池(对照)的fcl和阳极不可逆比容量是显著且系统地高于在以实验含碳阳极材料6-10为特征的全电池中所观察到的那些。与从以实验含碳阳极材料6-9为特征的电池中看到的阴极可逆比容量值相比,较高的fcl导致对照电池显示出少约10mah/g的阴极可逆比容量值。
[0187]
实验含碳阳极材料11未表现出与实验含碳阳极材料6-10所获得的那些一样低的fcl和阳极不可逆比容量值,然而,阳极材料11的结果仍低于对照样品4的结果。据信,将一次含碳材料表面处理至最高达最大值900℃是最有利的,以避免碳物质石墨化至抑制可逆(脱)嵌钠的程度。总之,当根据本发明并且在780-900℃的温度下处理一次含碳材料时,示出获得最大效率。
[0188]
包括以实验材料8为特征的阳极的全电池以c/5的恒定放电速率从c/5逐渐充电到10c。在整个测试中展示大于60%的放电容量保持率。在完成快速充电测试后,获得接近100%的额定容量,即当电池以c/5充电和放电时的阴极放电容量。结果总结在表5和图16中。
[0189]
表5
[0190][0191]
*近似的
[0192]
根据本发明证明含碳阳极材料降低的水分敏感性的实验
[0193]
高度优选的是降低包括电极、隔板和电解质的所有电池部件的残留水分含量。根据本发明的含碳阳极材料(实验材料6-11)的关键优点在于,发现它们对水分暴露的敏感性显著低于未用碳化材料处理的原始一次含碳材料(实验材料4(对照))。
[0194]
在不同的暴露持续时间下实验性含碳阳极材料6-11以及对照材料4的水分含量详述于表3和图17中,显然对照材料4在暴露时吸附大量水分,而根据本发明的含碳阳极材料具有显著降低的水分吸附速率。如上所述,据信该降低的水分吸附是由于在碳化材料存在下处理一次硬碳材料后表面微孔降低的可用性。
[0195]
图18示出以对照材料4为特征的阳极电极(涂层)以及以根据本发明的含碳材料
(实验材料7-10)为特征的阳极电极(涂层)的残留水分含量。包含实验含碳材料10的阳极电极(涂层)表现出最低(最有利的)残留水分含量。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1