一种密脉木生物碱的合成方法与流程
本发明属于有机合成技术领域,具体涉及密脉木生物碱的制备方法。
背景技术:
丙型肝炎是一种世界性的疾病,根据世界卫生组织的统计,全球有1.3亿至1.5亿人患有慢性丙肝感染,大量慢性感染者会出现肝硬化或者肝癌,其中每年大约有50万人死于丙肝相关的肝脏疾病。但是治疗丙肝的抗病毒药物的价格却很高,人们一直在不断研制新型药物确保全球更多丙肝患者得到治疗。近年来,从密脉木属植物中分离获得了大量结构新颖并且活性显著的天然产物,其中许多可作为新药研究的先导化合物。密脉木碱A(α,β-MyrifabralA)和密脉木碱B(α,β-MyrifabralB)由中国科学院昆明植物研究所的郝小江研究员对采自四川的密脉木的化学成分进行分析时首次分离获得。初步的生理学研究发现,密脉木碱A和B及其部分衍生物对丙肝病毒有着显著的的抑制作用,并且细胞毒性低于现有的丙肝治疗药物特拉匹韦(telaprevir)。但是,30公斤的天然密脉木植物中仅仅分离得到了30毫克的密脉木碱A和2毫克的密脉木碱B。这增加了对其生理学和药理学活性方面的研究难度,阻碍了对该物质的进一步研究和应用。
技术实现要素:
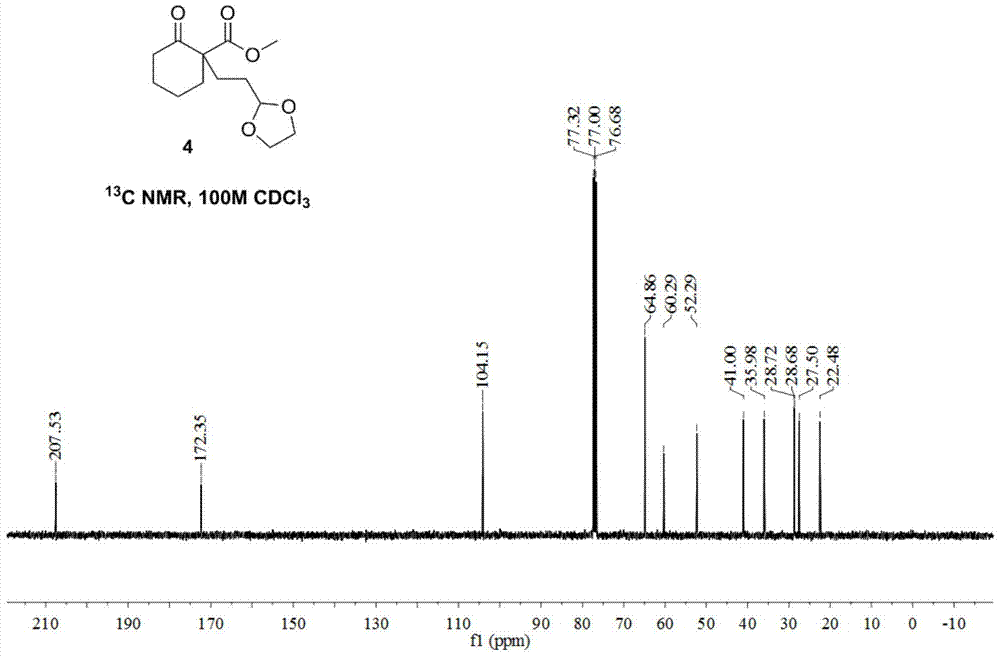
针对天然产物密脉木碱A和B的获取量少,阻碍了对该物质的进一步研究和应用方面存在的不足,本发明提供一种密脉木碱A和B的合成方法。该方法能够从廉价易得的原料出发,实现了密脉木碱A和B的首次人工合成,并能持续、大量地合成密脉木碱A和B,为后续实现该天然产物的规模化生产及构效关系研究提供良好的技术支持。本发明提供一种新的制备密脉木碱A和B的方法,该方法以丙烯醛为起始原料,通过5步化学反应最终制备得到密脉木碱A和B,具体包括以下步骤:(1)化合物3的合成(2)化合物4的合成(3)化合物5的合成(4)化合物6的合成(5)密脉木生物碱A的合成(6)密脉木生物碱B的合成本发明的益处在于,突破密脉木碱A和B只能从生物中提取,获取量少的缺陷,将密脉木碱A和B人工合成,可以大规模生产。同时,化学流程短,损耗低,操作方便,条件简单。附图说明:图1化合物4的1氢核磁谱图。图2化合物4的13碳核磁谱图。图3化合物5的1氢核磁谱图。图4化合物5的13碳核磁谱图。图5化合物6的1氢核磁谱图。图6化合物6的13碳核磁谱图。图7密脉木碱A的1氢核磁谱图。图8密脉木碱A的13碳核磁谱图。图9密脉木碱B的1氢核磁谱图。图10密脉木碱B的1氢核磁谱图。具体实施方式:本发明提供一种新的制备密脉木碱A和B的方法,该方法以丙烯醛为起始原料,通过5步化学反应最终制备得到密脉木碱A和B,具体包括以下步骤:(1)化合物3的合成5.6g(100mmol)丙烯醛溶于250ml乙腈中,加入18g(120mmol)碘化钠,缓慢滴入15.3ml(120mmol)氯代三甲基硅烷,反应20分钟。随后缓慢滴入6.7ml(120mmol)乙二醇,继续反应20分钟。反应完毕后,加入100ml5%的碳酸氢钠水溶液淬灭反应,加入100ml石油醚,体系分为三相,使用饱和硫代硫酸钠溶液洗涤一次,再用饱和食盐水洗涤数次至体系分为两相为止,分出上层有机相,无水硫酸钠干燥,旋除溶剂,得到的化合物直接进行下一步。其中丙烯醛、碘化钠、氯代三甲基硅烷和乙二醇的最佳摩尔比为1:1.2:1.2:1.2。(2)化合物4的合成2.88g(72mmol)60%的氢化钠悬浮在60ml四氢呋喃和60mlN,N-二甲基甲酰胺的混合溶剂中,0℃下缓慢滴入9.371g(60mmol)2-氧环己烷羧酸甲酯。搅拌10分钟后升至室温继续搅拌1小时。随后缓慢加入16.418g(72mmol)的化合物3,室温反应18小时。饱和氯化铵淬灭反应,水相用乙醚萃取3次,食盐水洗涤有机相,无水硫酸钠干燥。过滤,旋除溶剂,柱层析分离(石油醚:乙酸乙酯=5:1)得到12.611g(49.3mmol)无色油状液体即化合物4,产率82%。其中溶剂为四氢呋喃与N,N-二甲基甲酰胺的混合溶剂,最佳体积比为1:1。2-氧环己烷羧酸甲酯与氢化钠及化合物3的最佳摩尔比为1:1.2:1.2。1HNMR(400MHz,CDCl3)δ4.84(t,J=4.3Hz,1H),3.97-3.90(m,2H),3.86-3.78(m,2H),3.72(s,3H),2.54-2.46(m,1H),2.45-2.41(m,2H),2.04-1.93(m,2H),1.74(m,1H),1.70-1.58(m,4H),1.56-1.41(m,2H).13CNMR(100MHz,CDCl3)δ207.5,172.3,104.2,64.9,60.3,52.3,41.0,36.0,28.7,28.7,27.5,22.5;(3)化合物5的合成10.792g(42.1mmol)的化合物4溶于80ml甲醇中,加入4.548g(84.2mmol)甲醇钠,随后加入5.243g(63.2mmol)2,3,4,5-四氢哌啶,反应升至85℃回流反应72小时。反应完毕,加水淬灭,旋除甲醇后水相用乙酸乙酯萃取,食盐水洗涤有机相,无水硫酸钠干燥。过滤,旋除溶剂,柱层析分离(石油醚:乙酸乙酯=5:1),得到5.042g(16.4mmol)白色固体即化合物5,产率39%。其中化合物4与2,3,4,5-四氢哌啶及甲醇钠的最佳摩尔比为1:1.5:2。1HNMR(400MHz,CDCl3)δ4.85(t,J=5.0Hz,1H),4.78(d,J=13.6Hz,1H),3.93-3.87(m,2H),3.83-3.77(m,2H),3.33(dt,J=9.9,4.8Hz,1H),2.59(brs,1H),2.48-2.41(m,1H),2.30-2.27(m,1H),2.18-2.15(m,1H),1.97-1.95(m,1H),1.84-1.81(m,2H),1.77-1.64(m,5H),1.61-1.43(m,6H);13CNMR(100MHz,CDCl3)δ209.9,170.2,104.7,64.7,64.6,60.4,55.4,50.0,43.2,42.0,30.6,29.5,28.9,27.0,25.1,24.6,19.8;(4)化合物6的合成3.470g(11.3mmol)的化合物5溶于30ml干燥的四氢呋喃溶液中,0℃下缓慢加入2.144g(56.5mmol)四氢铝锂,随后升温回流反应6小时。反应完毕,冷至0℃,依次缓慢滴入2.1ml水,4.2ml10%NaOH水溶液和6.3ml水。过滤,乙酸乙酯洗涤滤饼,滤液用无水硫酸钠干燥。随后旋除溶剂,柱层析分离(石油醚:乙酸乙酯:二乙胺=100:20:1),得到2.702g(9.16mmol)无色或红色油状液体即化合物6,产率81%。其中化合5与四氢铝锂最佳摩尔比为1:5。1HNMR(400MHz,CD3OD)δ4.76(t,J=4.6Hz,1H),3.94-3.88(m,2H),3.85-3.79(m,2H),3.34(brs,1H),2.74(d,J=9.7Hz,1H),2.61(d,J=10.9Hz,1H),2.55-2.43(m,1H),1.94(brs,2H),1.83-1.74(m,2H),1.69-1.49(m,9H),1.45-1.21(m,7H);13CNMR(100MHz,CD3OD)δ106.5,76.9,67.2,66.9,66.0,58.0,43.2,38.1,33.9,31.7,31.4,28.6,27.4,25.9,21.9,21.1;(5)密脉木生物碱A的合成2.702g(9.2mmol)化合物6溶于10ml四氢呋喃溶液中,加入11.5ml2N盐酸,升温至回流反应4小时。反应完毕,冷却至0℃,使用10%NaOH水溶液调节体系pH至10,旋除四氢呋喃。水相用氯仿萃取,饱和食盐水洗涤有机相,无水硫酸钠干燥。过滤,旋除溶剂,柱层析分离得到2.114g(8.4mmol)白色固体密脉木碱A,产率92%。其中化合物6与盐酸的最佳摩尔比为1:2.5,进一步的纯化可以使用甲醇重结晶。密脉木碱A主要构型的1HNMR(400MHz,Pyr)δ5.71(t,J=3.6Hz,1H),4.21(d,J=3.2Hz,1H),2.74(m,1H),2.68(m,1H),2.54(d,J=10.8Hz,1H),2.28(m,1H),2.07(m,1H),1.99-1.92(m,3H),1.76(m,1H),1.67-1.59(m,4H),1.55-1.45(m,4H),1.25-1.20(m,2H),1.16-1.13(m,1H),1.07(m,1H);13CNMR(100MHz,Pyr)δ92.3,72.4,69.6,66.8,57.1,40.1,33.0,30.6,29.5,28.7,26.8,25.4,21.3,21.1;(6)密脉木生物碱B的合成1.113g(3.8mmol)化合物6溶于4ml四氢呋喃溶液中,加入4.8ml2N盐酸,升温至回流反应4小时。随后加入2.210g(18.9mmol)化合物7,继续回流反应6小时。反应完毕,冷却至0℃,使用10%NaOH水溶液调节体系pH至10,旋除四氢呋喃。水相用氯仿萃取,饱和食盐水洗涤有机相,无水硫酸钠干燥。随后旋除溶剂,柱层析分离得到白色固体即203mg(0.81mmol)密脉木碱A与537mg(1.6mmol)密脉木碱B,产率分别为21%和42%。其中化合物6与盐酸及化合物7的最佳摩尔比为1:2.5:5,进一步的纯化可以使用甲醇重结晶。密脉木碱B主要构型的1HNMR(400MHz,Pyr)δ5.73(s,1H),4.23(d,J=2.6Hz,1H),2.78(m,2H),2.71(m,1H),2.61(m,1H),2.52(m,4H),2.44-2.36(m,3H),2.33-2.26(m,1H),2.07-1.94(m,3H),1.72(overlap,m,1H),1.72-1.64(overlap,m,3H),1.56-1.44(m,4H),1.35-1.24(m,3H),1.16(m,1H),1.02(overlap,t,J=7.1Hz,4H);13CNMR(100MHz,Pyr)δ94.1,72.5,69.7,66.8,57.1,57.0,48.4,40.0,35.2,35.1,33.7,30.6,29.8,26.8,25.4,21.5,21.2,12.8。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1