治疗抑郁症和重性抑郁障碍的方法与流程
本申请要求2014年3月5日提交的美国临时专利申请No.61/948,529和2014年10月8日提交的美国临时专利申请No.62/061,417的优先权和权益。前述临时申请全文以引用方式并入本文。
技术领域:
本发明涉及治疗个体的抑郁症诸如重性抑郁障碍(MDD)以及鉴定罹患抑郁症诸如MDD的个体对沃替西汀的治疗将产生有利反应和/或在接受沃替西汀治疗时经历增强的治疗效果的可能性的方法和试剂盒。这些方法和试剂盒基于检测以下各者的多态性的存在:XXVI型胶原α1(COL26A1)基因和/或L型电压依赖性钙通道α1C亚单位(CACNA1C)基因和/或CUB和Sushi多结构域1(CSMD1)基因和/或锌指蛋白494(ZSCAN4)基因和/或锌指蛋白551(ZNF551)基因和/或迪格弗-梅尔基奥尔-克劳森综合征蛋白(dymeclin)(DYM)基因和/或LINC00348基因和/或FOXL2NB基因和/或基因间区。
背景技术:
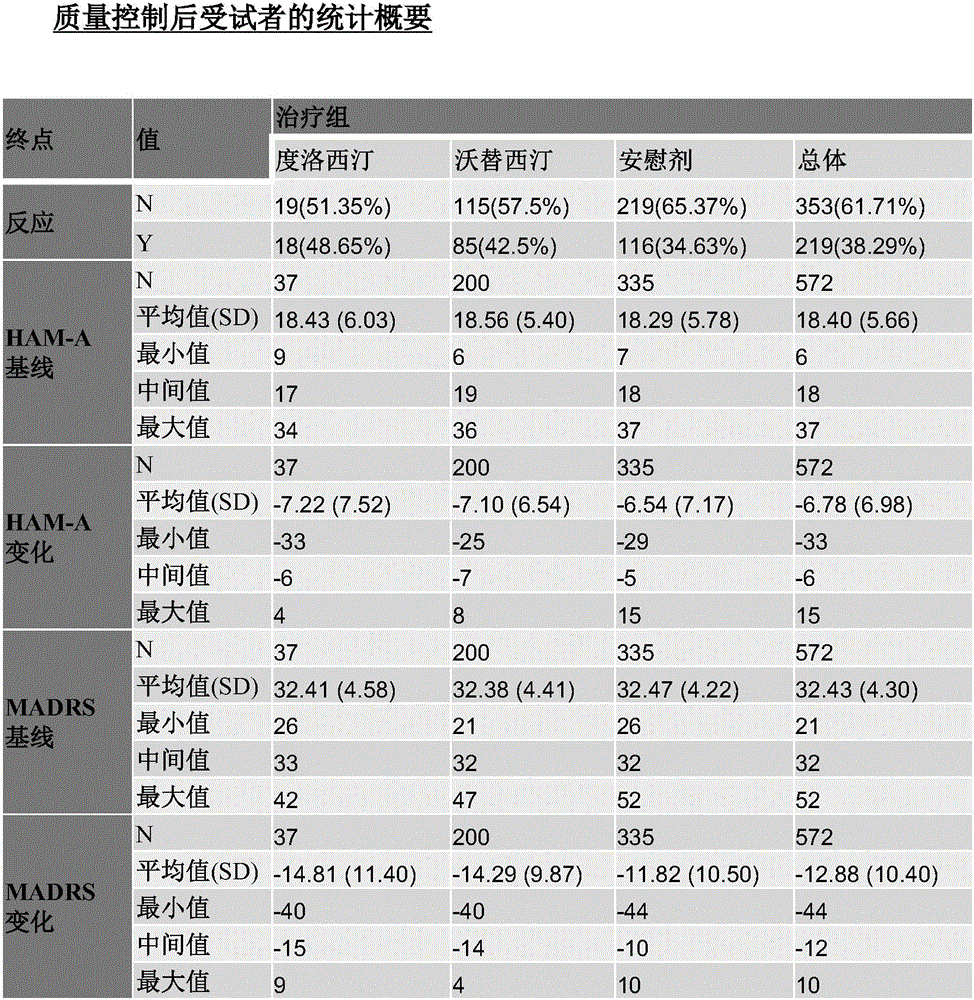
:抑郁症是情绪低落且厌恶活动的状态,其可能影响个人的思想、行为、感觉和幸福感。抑郁的人可能感觉悲伤、焦虑、空虚、没希望、担忧、无助、无价值、罪恶、易激怒、伤心或不安宁。许多精神病综合征的特征是作为主要症状的抑郁情绪。情绪障碍是被视为原发性情绪紊乱的一群病变,诸如重性抑郁障碍(MDD;通常称为重性抑郁症或临床抑郁症),其中病人具有至少两周抑郁情绪或在几乎所有活动中均丧失兴趣或乐趣。更明确地讲,重性抑郁障碍(MDD)是一种失能的严重心智障碍,其特征在于持续性情绪低落发作,伴随自我评价低落,以及对平时应该感到愉快的活动丧失兴趣或乐趣。这种疾病倾向于慢性的,并会反复发作。MDD的其他症状可包括易激怒或挫折感、睡眠紊乱、疲倦及缺乏活力、食欲改变、焦虑、激动、不安宁、无价值感或罪恶感、无法思考与集中注意力以及无原由的身体问题,诸如背痛或头痛。该障碍成为造成全球疾病负担的重要原因,并影响全世界所有社区人群(Ferrari,2013)。MDD是一种极普遍发生的精神障碍,在双胞胎研究中显示,高达40%MDD病例由遗传决定(Kendler,2006)。虽然MDD的确切原因仍未知,但据信其可涉及多种因素,诸如脑部化学与物理性脑差异、激素、遗传特质和生活事件。许多类型的抗抑郁剂药物可用来治疗MDD和与抑郁症一起出现的其他情绪障碍。一些可用的药物包括选择性血清素再吸收抑制剂(SSRI)、血清素和去甲肾上腺素再吸收抑制剂(SNRI)、去甲肾上腺素和多巴胺再吸收抑制剂(NDRI)、三环类抗抑郁剂、单胺氧化酶抑制剂(MAOI)和非典型抗抑郁剂(诸如沃替西汀)。然而,尽管有许多种治疗选项可以采用,但个体对抗抑郁剂药物的反应仍欠佳且多变。即,并非所有个体均对给定的抗抑郁剂产生同等反应。有多达一半的患者无法接受适当的MDD治疗且许多患者仅对治疗出现部分反应或完全没有反应。沃替西汀是一种适用于治疗MDD的双-芳基-硫烷基胺精神药物。虽然沃替西汀的抗抑郁剂效应机制尚未完全了解,但已知沃替西汀可通过抑制血清素再吸收(例如,通过作为5-HT受体拮抗剂)来增强中枢神经系统中的血清素活性。据信,此活性会影响沃替西汀的抗抑郁效应。沃替西汀还具有数种其他活性,包括5-HT3受体拮抗性和5-HT1A受体激动性。然而,这些活性对沃替西汀的抗抑郁剂效应的贡献仍未确立。据信,遗传特质可在抗抑郁剂如何影响个体的过程中扮演某种角色,但除了遗传以外的其他变量也会影响对药物的反应。因此,不容易预测哪一种药物才是对给定患者最佳的治疗选项。因此,若能设计一种鉴定对特定MDD药物诸如沃替西汀可能产生最有利反应的罹患抑郁症和/或MDD的患者亚群的方法将是有益的。技术实现要素:本发明的一个方面提供治疗个体的抑郁症和/或MDD的方法,该个体经鉴定为(i)COL26A1rs4045阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045阳性和CACNA1C变体阳性,(vii)COL26A1rs4045、CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045、CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性,该方法包括对该个体施用沃替西汀。本发明的另一方面提供治疗个体的抑郁症和/或MDD的方法,其包括确定个体为(i)COL26A1rs4045阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045阳性和CACNA1C变体阳性,(vii)COL26A1rs4045、CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045、CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性,并对该个体施用沃替西汀。本发明的另一方面提供确定罹患抑郁症和/或MDD的个体对沃替西汀的治疗将产生有利反应的可能性的方法。一些方面包括从个体取得生物样品。一些方面包括分析来自该个体的生物样品,以确定来自该个体的核酸中COL26A1rs4045和/或CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体的存在。一些方面包括当个体为(i)COL26A1rs4045纯合的;(ii)具有CACNA1C变体;(iii)具有CSMD1变体,(iv)具有ZSCAN4变体,(v)具有ZNF551变体,(vi)为COL26A1rs4045纯合的且具有CACNA1C变体,(vii)为COL26A1rs4045纯合的且具有CACNA1C变体和CSMD1变体,或(viii)为COL26A1rs4045纯合的且具有CACNA1C变体、CSMD1变体和ZSCAN4变体,(ix)为COL26A1rs4045纯合的且具有CACNA1C变体、CSMD1变体、ZSCAN4变体和ZNF551变体,(x)为COL26A1rs4045纯合的且具有CACNA1C变体、CSMD1变体、ZSCAN4变体、DYM变体和基因间变体,或(x)为COL26A1rs4045纯合的且具有CACNA1C变体、CSMD1变体、ZSCAN4变体、DYM变体、LINC00348变体、FOXL2NB变体和基因间变体时,则确定该个体可能对沃替西汀的治疗产生有利反应。在一些实施方案中,该方法还包括分析生物样品,以确定来自该个体的核酸中COL26A1rs4045和/或CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体的存在,且当该个体为(i)COL26A1rs4045纯合的;(ii)具有CACNA1C变体;或(iii)具有CSMD1变体,(iv)具有ZSCAN4变体,(v)具有ZNF551变体,(vi)为COL26A1rs4045纯合的且具有CACNA1C变体,(vii)为COL26A1rs4045纯合的且具有CACNA1C变体和CSMD1变体,(viii)为COL26A1rs4045纯合的且具有CACNA1C变体、CSMD1变体和ZSCAN4变体,(ix)为COL26A1rs4045纯合的且具有CACNA1C变体、CSMD1变体、ZSCAN4变体和ZNF551变体,(x)为COL26A1rs4045纯合的且具有CACNA1C变体、CSMD1变体、ZSCAN4变体、DYM变体和基因间变体,或(ix)为COL26A1rs4045纯合的且具有CACNA1C变体、CSMD1变体、ZSCAN4变体、DYM变体、LINC00348变体、FOXL2NB变体和基因间变体时,则确定该个体可能对沃替西汀的治疗产生有利反应。在一些实施方案中,具有CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体的个体经确定为该变体纯合的。本发明的又一方面提供确定罹患抑郁症和/或MDD的个体在接受沃替西汀治疗时将经历增强的治疗效果的可能性的方法,其包括分析来自该个体的生物样品,以确定来自该个体的核酸中是否存在COL26A1rs4045和/或CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体;以及当在样品中检测到COL26A1rs4045和/或CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体时,则确定该个体是否可能在接受沃替西汀治疗时经历增强的治疗效果。在本发明方法的在一些实施方案中,该个体罹患和/或曾经经临床诊断患有重性抑郁障碍(MDD)。在本发明的一些实施方案中,沃替西汀可用于治疗认知损害的个体,其中该个体经确定或经鉴定为(i)COL26A1rs4045阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045阳性和CACNA1C变体阳性,(vii)COL26A1rs4045、CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045、CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性。一些实施方案包括在罹患认知损害的个体经确定为(i)COL26A1rs4045阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045阳性和CACNA1C变体阳性,(vii)COL26A1rs4045、CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045、CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性时,确定该个体在接受沃替西汀治疗时将经历增强的治疗效果的可能性的方法。同样地,本文还描述在罹患认知损害的个体为(i)COL26A1rs4045纯合的阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045纯合的及CACNA1C变体阳性,(vii)COL26A1rs4045纯合的及CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045纯合的及CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045纯合的及CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045纯合的及CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045纯合的及CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性时,确定该个体对沃替西汀的治疗将产生有利反应的可能性的方法。在本发明的一些方面,该公开的方法考虑使用沃替西汀治疗以改善认知功能。在一些实施方案中,该接受治疗、对治疗产生有利反应和/或经历增强的治疗效果的个体被鉴定为COL26A1rs4045纯合的及CACNA1C变体阳性、CSMD1变体阳性和ZSCAN4变体阳性。在一些方面,患有认知损害的个体还罹患或经诊断为患有抑郁症和/或MDD。在一些方面,该公开的方法考虑使用沃替西汀治疗经诊断为罹患抑郁症和/或MDD的个体,以改善认知功能。在一些实施方案中,该公开的方法包括确定该个体为CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体杂合的。在其他实施方案中,该方法包括确定该个体为CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体纯合的。在一些实施方案中,该公开的方法包括确定该个体为COL26A1rs4045纯合的。在一些实施方案中,该CACNA1C变体选自:rs7297992、rs7297582(位置2355806,等位基因C/T)、rs2239042(位置2428487,等位基因G/A)、rs3819532、rs2239079、rs2239080、kgp5074525、rs4765961、kgp1052923、kgp1390211、rs7311147(位置2707821,等位基因G/A)、rs12312322、rs2108636、rs2238043、rs7295089、kgp3964892、rs10848664、kgp2586442、rs4765700、rs2238095、rs12312322、rs7972947、rs10848664、rs1006737(位置2345295,等位基因G/A)、rs2370602及其组合。在一个特定实施方案中,该CACNA1C变体选自:rs7297582(位置2355806,等位基因C/T)、rs2239042、rs7311147(位置2707821,等位基因G/A)及其组合。在一些实施方案中,该CSMD1变体为rs59420002。在一些实施方案中,该ZSCAN4变体选自:rs9304796、rs73064580、rs12983596、rs12984275、rs9749513、rs12609579、rs4239480、rs9676604、rs12162232及其组合。在一些实施方案中,该ZNF551变体为rs12162230。在一些实施方案中,该DYM变体为rs62104612。在一些实施方案中,该LINC00348变体为rs145136593。在一些实施方案中,该FOXL2NB变体为rs116191388。在一些实施方案中,该基因间变体选自:rs1998609、rs4142192及其组合。本发明的方法可包括分析来自个体的样品,以确定该个体基因组中rs4045变体和/或CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体的存在。该样品可选自:体液、组织样品、细胞和分离的核酸。分离核酸的样品可包括来自个体的DNA和/或RNA。在一些实施方案中,来自个体的样品的分析涉及RNA的逆转录,以产生cDNA。本发明的一个方面提供试剂盒,诸如包含以下各者的试剂盒:(i)与本文所公开的遗传变体特异性杂交的至少一对引物,以及(ii)与该遗传变体杂交的以可检测的方式标记的探针。在一些实施方案中,该遗传变体独立选自:rs4045、rs59420002、rs7297582、rs2239042和rs7311147。在一些实施方案中,该试剂盒包含与rs4045特异性杂交的一对引物;与rs59420002特异性杂交的一对引物;与rs7297582特异性杂交的一对引物;与rs2239042特异性杂交的一对引物;与rs7311147特异性杂交的一对引物;与rs12983596特异性杂交的一对引物;与rs9749513特异性杂交的一对引物。在一些实施方案中,该试剂盒包含与rs4045特异性杂交的一对引物;与rs59420002特异性杂交的一对引物;与rs7297582特异性杂交的一对引物;与rs2239042特异性杂交的一对引物;与rs7311147特异性杂交的一对引物;与rs12983596特异性杂交的一对引物;与rs9749513特异性杂交的一对引物;与rs62104612特异性杂交的一对引物;与rs1998609特异性杂交的一对引物;以及与rs4142192特异性杂交的一对引物。在一些实施方案中,该试剂盒包含与rs4045特异性杂交的一对引物;与rs59420002特异性杂交的一对引物;与rs7297582特异性杂交的一对引物;与rs2239042特异性杂交的一对引物;与rs7311147特异性杂交的一对引物;与rs12983596特异性杂交的一对引物;与rs9749513特异性杂交的一对引物;与rs62104612特异性杂交的一对引物;与rs1998609特异性杂交的一对引物;与rs145136593特异性杂交的一对引物;以及与rs116191388特异性杂交的一对引物。在一些实施方案中,该试剂盒包含与rs4045特异性杂交的一对引物;与rs59420002特异性杂交的一对引物;与rs7297582特异性杂交的一对引物;与rs2239042特异性杂交的一对引物;与rs7311147特异性杂交的一对引物;与rs9304796特异性杂交的一对引物;与73064580特异性杂交的一对引物;与rs12983596特异性杂交的一对引物;与rs12984275特异性杂交的一对引物;与rs9749513特异性杂交的一对引物;与rs12609579特异性杂交的一对引物;与rs4239480特异性杂交的一对引物;与rs9676604特异性杂交的一对引物;以及与rs12162232特异性杂交的一对引物。附图说明图1显示研究中的个体在质量控制(QC)过程之后的基因型的概要。QC过程评价了变体细胞率(每种变体,采用所有样品)、次要等位基因频率(每种变体,采用所有样品)和哈温平衡检验(Hardy-WeinbergEquilibriumtest)p值(每种变体,每种人种采用所有样品)。图2提供质量控制后的统计分析的概要。图3汇总亚组鉴定结果。具有rs4045和CACNA1C变体的MDD个体对沃替西汀的治疗经历显著增强的反应,如通过MADRS和HAM-A得分来度量。图4提供从沃替西汀相对于安慰剂亚组鉴定研究所得的数据的图形结果。图5示出具有指定rs1006737等位基因(GG=G等位基因纯合的;GA=杂合的;而AA=A纯合的)的个体的MADRS得分(5(B))、HAM-A得分(5(C))和总体反应(RESP)得分(5(D))的最小二乘(LS)均值图。对于每个图表(B至D),最左边3个数据点代表治疗组(20mg沃替西汀),而最右边3个数据点代表安慰剂组。图6示出具有指定rs7297582等位基因(CC=C等位基因纯合的;CT=杂合的;而TT=T等位基因纯合的)的个体的MADRS得分(6(B))、HAM-A得分(6(C))和总体反应(RESP)得分(6(D))的最小二乘(LS)均值图。对于每个图表(B至D),最左边3个数据点代表治疗组(20mg沃替西汀),而最右边3个数据点代表安慰剂组。图7示出具有指定rs2239042等位基因(AA=A等位基因纯合的;AG=杂合的;而GG=G等位基因纯合的)的个体的MADRS得分(7(B))、HAM-A得分(7(C))和总体反应(RESP)得分(7(D))的最小二乘(LS)均值图。对于每个图表(B至D),最左边3个数据点代表治疗组(20mg沃替西汀),而最右边3个数据点代表安慰剂组。图8示出具有指定rs7311147等位基因(AA=A等位基因纯合的;AG=杂合的;而GG=G等位基因纯合的)的个体的MADRS得分(8(B))、HAM-A得分(8(C))和总体反应(RESP)得分(8(D))的最小二乘(LS)均值图。对于每个图表(B至D),最左边3个数据点代表治疗组(20mg沃替西汀),而最右边3个数据点代表安慰剂组。图9提供得自以下的数据的图形或表格结果:(i)所有受试者(9(A))、非西班牙裔白人受试者(9(B))和初始426位受试者亚组内的所有受试者(9(C))的沃替西汀相对于安慰剂的5变体模型亚组鉴定研究;(ii)采用5变体模型的研究中受试者的基线和人口学特征概要(9(D));(iii)由LOCF确定的第8周时的有反应者和缓解率(9E和9F);(iv)在5变体模型中使用20mg沃替西汀相对于安慰剂治疗后的MADRS得分离基线的变化(9G-I),(v)5变体模型中的CGI-I得分(9J),(vi)两个5变体模型在第8周时的HAM-A总得分离基线的变化(图9K),(vii)在5变体模型中,基于人种的有反应者比例(图9L),(viii)在5变体模型中,施用20mg沃替西汀后的恶心比例(9M),(ix)所有受试者的沃替西汀相对于度洛西汀相对于安慰剂的5变体模型亚组鉴定研究(9(N));以及(iii)具有A/GEMID2等位基因(9(O))、A/Grs2239042等位基因(9(P))、C/Trs7297582等位基因(9(Q))、A/Grs1006737等位基因(9(R))和A/Grs7311147等位基因(9(S))的个体的总体反应状态图。在图中,PK<LLQ表示该药物动力学低于定量下限。图10提供得自以下的数据的图形或表格结果:(i)所有受试者(10(A))、非西班牙裔白人受试者(10(B))和初始426位受试者亚群中的所有受试者(10(C))的沃替西汀相对于安慰剂的7变体模型亚组鉴定研究,以及(ii)所有个体的沃替西汀相对于安慰剂的5变体模型亚组鉴定研究(10(D)),(iii)采用7变体模型的研究中受试者的基线和人口学特征概要(10D),(iv)由LOCF确定的第8周时的有反应者比例和缓解率(10E和10F),(v)在7变体模型中使用20mg沃替西汀相对于安慰剂治疗后的MADRS得分离基线的变化(10G-I),(vi)在5变体模型和7变体模型中MADRS总得分离基线的变化的比较在(10J)中示出,(vii)在7变体模型中的CGI-I得分(10K),(viii)两个7变体模型在第8周时的HAM-A总得分离基线的变化(10L),(ix)在7变体模型中,基于人种的有反应者比例(10M),以及(x)所有受试者的沃替西汀相对于度洛西汀相对于安慰剂的7变体模型亚组鉴定研究(10N)。图11提供得自所有受试者的沃替西汀相对于安慰剂的14变体模型亚组鉴定研究的数据的图形结果。图12提供得自10mg沃替西汀相对于20mg沃替西汀相对于安慰剂的5变体和7变体模型亚组鉴定研究(即TAK-316研究)的图形结果,且该图包括下列各项的图形或表格结果:(i)10mg沃替西汀相对于20mg沃替西汀相对于安慰剂的7变体模型亚组鉴定研究(12A和12D),(ii)10mg沃替西汀相对于安慰剂的7变体模型亚组鉴定研究(12B),(iii)10mg沃替西汀相对于20mg沃替西汀相对于安慰剂的5变体模型亚组鉴定研究(12C),以及(iv)样品可说明性(accountability)数据(12E)。图13显示认知的改善,其在施用10mg/天和20mg/天的沃替西汀相对于施用安慰剂后,通过认知与身体功能问卷(CognitiveandPhysicalFunctioningQuestionnaire)(CPFQ)确定。结果以表格形式示于图13A,并以图形形式示于图13B。图13C显示相对于安慰剂数据计算的10mg/天和20mg/天沃替西汀数据的图形结果。图14显示在10变体模型亚组鉴定研究中,(i)相对于安慰剂施用60mg度洛西汀和20mg沃替西汀(14A和14B),(ii)相对于安慰剂施用10mg沃替西汀和20mg沃替西汀(14C和14D),以及(iii)相对于安慰剂施用10mg沃替西汀(14E和14F)后MADRS总得分离基线的变化。图15提供得自11变体模型亚组鉴定研究的数据的图形结果,且显示(i)施用20mg沃替西汀、10mg沃替西汀和/或60mg度洛西汀后MADRS得分离基线的变化(15A-D),以及(ii)(a)相对于安慰剂施用60mg度洛西汀和20mg沃替西汀(15E和15F),(b)相对于安慰剂施用10mg沃替西汀和20mg沃替西汀(15G和15H),和(c)相对于安慰剂施用10mg沃替西汀(15I和15J)后MADRS总得分离基线的变化。具体实施方式本文提供治疗罹患抑郁症或重性抑郁障碍(MDD)的个体中的抑郁症诸如MDD的方法。在一些实施方案中,该个体经临床诊断为患有抑郁症或抑郁症相关情绪障碍,诸如MDD。本文还描述鉴定将可能对沃替西汀的治疗产生有利反应的罹患抑郁症诸如MDD的个体的方法。还描述鉴定对沃替西汀将可能经历比另一个体更强的治疗反应的罹患抑郁症诸如MDD的个体的方法。本文还提供治疗罹患认知损害的个体中的认知损害的方法。本文还描述鉴定将可能对沃替西汀的治疗产生有利反应的罹患认知损害的个体的方法。还描述鉴定对沃替西汀将可能经历比另一个体更强的治疗反应的罹患认知损害的个体的方法。在一些实施方案中,该罹患认知损害的个体还罹患抑郁症和/或MDD。目标群体本发明人惊人地发现,罹患MDD的为COL26A1rs4045纯合的且具有CACNA1C变体、CSMD1变体、ZSCAN4变体、ZNF551变体、DYM变体、LINC00348变体、FOXL2NB变体和/或基因间变体的个体比不为COL26A1rs4045纯合的且不具有CACNA1C变体、CSMD1变体、ZSCAN4变体、ZNF551变体、DYM变体、LINC00348变体、FOXL2NB变体和/或基因间变体的个体更可能经历对沃替西汀的增强的治疗反应。具有此基因型的个体可能对沃替西汀的治疗产生有利反应,这意味着,该个体在对为减轻抑郁症而施用的特定治疗方案的反应中,其MADRS得分相较于其基线得分产生≥50%的改善。在一些实施方案中,该治疗是施用沃替西汀。如本文所用,“COL26A1”是指XXVI型胶原α1基因,其位于人类第7号染色体上。COL26A1也称为EMID2。转录起始和终止位置分别位于101,006,001和101,202,304。COL26A1的示例性基因序列为基因ID:136227,其序列以引用方式并入本文中。如本文所用,“COL26A1rs4045”变体或多态性描述出现在第7号染色体的位置101067089处的COL26A1基因中的单核苷酸多态性。包含rs4045的一部分COL26A1基因序列如下:TGTTCTGTTTTGGCCTCCGAACTCC[A/G]AGGAGTGAGTGAGAAGAACTCCCTG(SEQIDNO:1)其中[A/G]代表变异。具有至少一个COL26A1rs4045变体拷贝的个体称为“COL26A1rs4045阳性”或“rs4045阳性”。另外的COL26A1变体包括kgp3405169(第7号染色体位置101,071,257,等位基因=A,等位基因=G)和rs6949799(第7号染色体位置101,067,526,等位基因=C,等位基因=T)。在一些实施方案中,该COL26A1变体选自:rs4045、rs6949799、kpg3405169及其组合。如本文所用,“CACNA1C”基因是指L型电压依赖性钙通道α1C亚单位基因,其细胞遗传学位置在12p13.3(即,位于第12号染色体的短(p)臂上位置13处)。基于基因组参照序列联盟(GenomeReferenceConsortium)人类基因组组装第38版(GRCh38),转录起始和终止位置分别位于1,970,786和2,697,949。由CACNA1C基因产生的钙通道称为CaV1.2。这些通道出现在许多细胞类型中,但它们似乎对心脏和脑部细胞的正常功能尤其重要。CACNA1C基因的示例性核苷酸序列为NCBI基因ID:775,其序列以引用方式并入本文中。已报导此基因产生超过23种转录变体,且对应于各种mRNA转录物的示例性cDNA序列是已知的且可公开获得。已在CACNA1C基因中鉴定出超过528种SNP。如本文所用,“CACNA1C变体”是其序列与NCBI基因ID:775的序列的同一性低于100%的CACNA1C基因。在一些实施方案中,该变体的序列与NCBI基因ID:775的序列的同一性为约75%至约99%,诸如与NCBI基因ID:775的序列的同一性为约75%、约80%、约85%、约90%、约95%或约99%。因此,与NCBI基因ID:775的序列相比具有单一核苷酸变异的CACNA1C基因即为CACNA1C变体。在一些实施方案中,CACNA1C变体为相较于NCBI基因ID:775的编码区,在CACNA1C编码区中表现出至少一种多态性的CACNA1C多核苷酸。在一些实施方案中,与个体对沃替西汀的反应有关的CACNA1C变体为CACNA1C错义突变(也称为非同义突变)。在一些实施方案中,与对沃替西汀产生有利反应或增强治疗效果有关的CACNA1C变体位于区间3内(位置2333638至2436522)或区间6内(位置2538549至2565920)。在一些实施方案中,与对沃替西汀产生有利反应或增强治疗效果有关的CACNA1C变体选自:rs7297992、rs7297582(位置2355806,等位基因C/T)、rs2239042(位置2428487,等位基因G/A)、rs3819532、rs2239079、rs2239080、kgp5074525、rs4765961、kgp1052923、kgp1390211、rs7311147(位置2707821,等位基因G/A)、rs12312322、rs2108636、rs2238043、rs7295089、kgp3964892、rs10848664、kgp2586442、rs4765700、rs2238095、rs12312322、rs7972947、rs10848664、rs1006737(位置2345295,等位基因G/A)、rs2370602及其组合。在一个特定实施方案中,该CACNA1C变体选自:rs7297582(位置2355806,等位基因C/T)、rs2239042、rs7311147(位置2707821,等位基因G/A)及其组合。在一些实施方案中,与对沃替西汀产生有利反应或增强治疗效果有关的CACNA1C变体选自:rs7297582、rs2239042、rs7311147及其组合。为CACNA1C变体杂合的或纯合的个体为“CACNA1C变体阳性的”。如本文所用,“CSMD1”基因是指CUB和Sushi多结构域1蛋白基因,其位于第8号染色体上。基于GRCh38,转录起始和终止位置位于2,935,353和4,994,806,它们是互补的。CSMD1的示例性基因序列为NCBI基因ID:64478,其序列以引用方式并入本文中。如本文所用,“CSMD1变体”是其序列与NCBI基因ID:64478的序列的同一性低于100%的CSMD1基因。在一些实施方案中,该变体的序列与NCBI基因ID:64478的序列的同一性为约75%至约99%,诸如与NCBI基因ID:64478的序列的同一性为约75%、约80%、约85%、约90%、约95%或约99%。在一些实施方案中,CSMD1变体为相较于NCBI基因ID:64478的编码区,在CSMD1编码区中表现出至少一种多态性的CSMD1多核苷酸。在一些实施方案中,CSMD1变体与对沃替西汀产生有利反应有关。在一些实施方案中,与对沃替西汀产生有利反应有关的CSMD1变体为rs59420002(等位基因A/G)。为CSMD1变体杂合的或纯合的个体为“CSMD1变体阳性的”。如本文所用,“ZSCAN4”基因是指锌指蛋白494基因,其位于第19号染色体上。基于GRCh38,转录起始和终止位置位于57,668,935和57,679,152。ZSCAN4的示例性基因序列为NCBI基因ID:201516,其序列以引用方式并入本文中。如这里所用,“ZSCAN4变体”是其序列与NCBI基因ID:201516的序列的同一性低于100%的ZSCAN4基因。在一些实施方案中,该变体的序列与NCBI基因ID:201516的序列的同一性为约75%至约99%,诸如约75%、约80%、约85%、约90%、约95%或约99%。在一些实施方案中,ZSCAN4变体为相较于NCBI基因ID:201516的编码区,在ZSCAN4编码区中表现出至少一种多态性的ZSCAN4多核苷酸中。在一些实施方案中,ZSCAN4变体与对沃替西汀产生有利反应有关。在一些实施方案中,与对沃替西汀产生有利反应有关的ZSCAN4变体选自:rs9304796(等位基因G/T)、rs73064580(等位基因C/T)、rs12983596(等位基因C/T)、rs12984275(等位基因C/G)、rs9749513(等位基因C/T)、rs12609579(等位基因A/C)、rs4239480(等位基因A/G)、rs9676604(等位基因C/T)、rs12162232(等位基因A/G)、rs10417057(等位基因T/C)、rs10403851(等位基因G/A)、rs56066537(等位基因G/T)、rs112783430(等位基因G/T)、rs9749360(等位基因A/G)及其组合。为ZSCAN4变体杂合的或纯合的个体为“ZSCAN4变体阳性的”。如本文所用,“ZNF551”基因是指锌指蛋白551基因,其位于第19号染色体上。基于GRCh38,转录起始和终止位置位于57,681,969和57,689,811。ZNF551的示例性基因序列为NCBI基因ID:90233,其序列以引用方式并入本文中。如这里所用,“ZNF551变体”是其序列与NCBI基因ID:90233的序列的同一性低于100%的ZNF551基因。在一些实施方案中,该变体的序列与NCBI基因ID:90233的序列的同一性为约75%至约99%,诸如与NCBI基因ID:90233的序列的同一性为约75%、约80%、约85%、约90%、约95%或约99%。在一些实施方案中,ZNF551变体为相较于NCBI基因ID:90233的编码区,在ZNF551编码区中表现出至少一种多态性的ZNF551多核苷酸。在一些实施方案中,ZNF551变体与对沃替西汀产生有利反应有关。在一些实施方案中,与对沃替西汀产生有利反应有关的ZNF551变体为rs12162230(等位基因G/A)。为ZNF551变体杂合的或纯合的个体为“ZNF551变体阳性的”。如本文所用,“DYM”基因是指迪格弗-梅尔基奥尔-克劳森综合征蛋白基因,其位于第18号染色体上。基于GRCh38,转录起始和终止位置位于49,043,026和49,460,709。示例性基因序列为NCBI基因ID:54808,其序列以引用方式并入本文中。如本文所用,“DYM变体”是其序列与NCBI基因ID:54808的序列的同一性低于100%的DYM基因。在一些实施方案中,该变体的序列与NCBI基因ID:54808的序列的同一性为约75%至约99%,诸如与NCBI基因ID:54808的序列的同一性为约75%、约80%、约85%、约90%、约95%或约99%。在一些实施方案中,DYM变体为相较于NCBI基因ID:54808的编码区,在DYM编码区中表现出至少一种多态性的DYM多核苷酸。在一些实施方案中,DYM变体与对沃替西汀产生有利反应有关。在一些实施方案中,与对沃替西汀产生有利反应有关的DYM变体为rs62104612。为DYM变体杂合的或纯合的个体为“DYM变体阳性的”。如本文所用,“LINC00348”基因是指长基因间非蛋白编码RNA348基因(LongIntergenicNon-ProteinCodingRNA348gene),其位于第13号染色体上。基于GRCh38,转录起始和终止位置位于71,143,183和71,168,417。示例性基因序列为NCBI基因ID:100885781,其序列以引用方式并入本文中。如本文所用,“LINC00348变体”是其序列与NCBI基因ID:100885781的序列的同一性低于100%的LINC00348基因。在一些实施方案中,该变体的序列与NCBI基因ID:100885781的序列的同一性为约75%至约99%,诸如与NCBI基因ID:100885781序列的同一性为约75%、约80%、约85%、约90%、约95%或约99%。在一些实施方案中,LINC00348变体为相较于NCBI基因ID:100885781的编码区,在LINC00348编码区中表现出至少一种多态性的LINC00348多核苷酸。在一些实施方案中,该LINC00348变体与对沃替西汀产生有利反应有关。在一些实施方案中,与对沃替西汀产生有利反应有关的LINC00348变体是rs145136593。为LINC00348变体杂合的或纯合的个体为“LINC00348变体阳性的”。如本文所用,“FOXL2NB”基因(也称为C3orf72基因)是指FOXL2近邻基因,其位于第3号染色体上。基于GRCh38,转录起始和终止位置位于138,947,234和138,953,988。示例性基因序列为NCBI基因ID:401089,其序列以引用方式并入本文中。如本文所用,“FOXL2NB变体”是指其序列与NCBI基因ID:401089序列的同一性低于100%的FOXL2NB基因。在一些实施方案中,该变体的序列与NCBI基因ID:401089的序列的同一性为约75%至约99%,诸如与NCBI基因ID:401089的序列的同一性为约75%、约80%、约85%、约90%、约95%或约99%。在一些实施方案中,FOXL2NB变体为相较于NCBI基因ID:401089的编码区,在FOXL2NB编码区中表现出至少一种多态性的FOXL2NB多核苷酸。在一些实施方案中,FOXL2NB变体与对沃替西汀产生有利反应有关。在一些实施方案中,与对沃替西汀产生有利反应有关的FOXL2NB变体为rs116191388。为FOXL2NB变体杂合的或纯合的个体为“FOXL2NB变体阳性的”。如本文所用,“基因间区”是指两个基因之间的区。如本文所用,“基因间变体”为两个基因之间的相较于野生型基因间区表现出至少一种多态性的区。在一些实施方案中,基因间变体与对沃替西汀产生有利反应有关。在一些实施方案中,与对沃替西汀产生有利反应有关的基因间变体选自:rs1998609、rs4142192及其组合。为基因间变体杂合的或纯合的个体为“基因间变体阳性的”。如本文所用,罹患MDD的个体是符合MDD的精神疾病诊断与统计手册(DiagnosticandStatisticalManualofMentalDisorders)(DSM-IV-TR)标准的个体。在一些实施方案中,罹患MDD的个体已经历重性抑郁障碍发作(MDE)至少3个月。在一些实施方案中,该个体在治疗之前的MADRS总分≥26和/或CGI-S得分≥4。抑郁症症状和经历治疗后的改善程度采用标准抑郁症症状量表来评估,诸如汉密尔顿抑郁量表(HamiltonDepressionRatingScale)(HAM-A)、蒙哥马利抑郁量表(Montgomery-AsbergDepressionRatingScale)(MADRS)和/或临床总体印象改善心理学量表(ClinicalGlobalImpressionImprovementpsychologicalscale)(CGI量表)。治疗效力基于由HAM-A总得分、MADRS总得分和/或CGIS总得分离基线的平均变化所度量的一种或多种抑郁症状的改善来确定。如本文所用,对药物诸如沃替西汀产生“增强的治疗反应”的个体在接受治疗时,其抑郁症状比罹患抑郁症和/或MDD的已接受治疗但不是COL26A1rs4045纯合的且不是rs7297582、rs2239042,或rs7311147CACNA1C变体;和/或rs59420002CSMD1变体;和/或rs9304796、rs73064580、rs12983596、rs12984275、rs9749513、rs12609579、rs4239480、rs9676604、rs12162232、rs10417057、rs10403851、rs56066537、rs112783430或rs9749360ZSCAN4变体;和/或rs12162230ZNF551变体;和/或rs62104612DYM变体;和/或rs145136593LINC00348变体;和/或rs116191388FOXL2NB变体;和/或rs1998609或rs4142192基因间变体纯合的个体经历更大的改善。治疗方法在一个实施方案中,如本文所提供的治疗经鉴定为(i)COL26A1rs4045阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045阳性和CACNA1C变体阳性,(vii)COL26A1rs4045、CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045、CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性的个体中的抑郁症和/或MDD的方法包括对该个体施用沃替西汀。在另一个实施方案中,治疗个体的抑郁症和/或MDD的方法包括确定个体为(i)COL26A1rs4045阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045阳性和CACNA1C变体阳性,(vii)COL26A1rs4045、CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045、CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性,并对该个体施用沃替西汀或类似的双-芳基-硫烷基胺精神药物。沃替西汀可以按包含具有以下结构式的氢溴酸沃替西汀(1-[2-(2,4-二甲基-苯基硫烷基)-苯基]-哌嗪氢溴酸盐)的片剂形式施用或摄入:在一些实施方案中,沃替西汀的施用或摄入剂量为每天5、10、15或20mg。在一些实施方案中,起始剂量为10mg/天,最后提高至20mg/天。治疗可持续至少5、6、7或8周。经口施用是优选的,但可采用其他施用模式。若在本发明中鉴定的患者群体可能对沃替西汀作出反应而经历增强的治疗效果时,可施用较低剂量。例如,可每天施用低于5mg的剂量,诸如每天2.5、3、3.5、4或4.5mg的剂量。在再一个实施方案中,公开了确定罹患抑郁症和/或MDD的个体在接受沃替西汀治疗时可能经历增强的治疗效果的可能性的方法。在一些实施方案中,该方法包括分析来自罹患抑郁症和/或MDD的个体的样品,以确定来自该个体的核酸中是否存在COL26A1rs4045变体和/或CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体。若来自该个体的核酸中存在COL26A1rs4045和/或CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体时,则确定该个体可能在用沃替西汀治疗时经历增强的治疗效果。预测对沃替西汀的反应的方法本文还提供确定罹患抑郁症和/或MDD的个体对沃替西汀的治疗将产生有利反应的可能性的方法。在一些实施方案中,该方法包括分析来自个体的样品,以确定来自该个体的核酸中是否存在COL26A1rs4045变体和/或CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体,以及当该个体为CACNA1C变体和/或CSMD1变体和/或ZSCAN4变体和/或ZNF551变体和/或DYM变体和/或LINC00348变体和/或FOXL2NB变体和/或基因间变体纯合的时,则确定该个体可能对沃替西汀的治疗产生有利反应。在一些实施方案中,本发明的方法还包括对呈COL26A1rs4045、CACNA1C变体阳性、CSMD1变体阳性、ZSCAN4变体阳性、ZNF551变体阳性、DYM变体阳性、LINC00348变体阳性、FOXL2NB变体阳性和/或基因间变体阳性的个体施用沃替西汀。在一些实施方案中,确定个体为COL26A1rs4045阳性和/或CACNA1C变体阳性和/或CSMD1变体阳性和/或ZSCAN4变体阳性和/或ZNF551变体阳性和/或DYM变体阳性和/或LINC00348变体阳性和/或FOXL2NB变体阳性和/或基因间变体阳性的方法涉及取得个体的生物样品及分析该样品,以确定该个体的基因组中是否存在COL26A1rs4045和/或CACNA1C序列变体和/或CSMD1序列变体和/或ZSCAN4序列变体和/或ZNF551序列变体和/或DYM序列变体和/或LINC00348序列变体和/或FOXL2NB序列变体和/或基因间序列变体。所分析的样品可以是从个体取得的任何物质的样品,其中该物质包含来自该个体的核酸。示例性样品类型包括体液样品、组织样品、粪便样品、个体的细胞和得自个体的分离核酸。示例性体液样品包括血液、血浆、血清、脑脊髓液和唾液。示例性组织样品包括组织活检样品。示例性细胞样品包括口腔拭子或从取自个体的任何生物样品得到的细胞。从样品中提取核酸的方法是本领域中熟知的且可容易地适于获得与所用的系统相容的样品。从测试样品中提取核酸的自动化样品制备系统可商购获得,例如,RocheMolecularSystems的COBASAmpliPrepSystem、Qiagen的BioRobot9600和AppliedBiosystems的PRISMTM6700样品制备系统。如本文所用,“分离的核酸”意指已从其来源的细胞材料中移出达到至少一定程度的核酸。然而,“分离的”并不要求该核酸是完全纯的且不含任何其他组分。分离的核酸的实例为使用商业核酸提取试剂盒获得的那些。在一些实施方案中,来自个体的样品包含来自该个体的DNA和/或RNA。在一些实施方案中,样品的分析涉及从生物样品提取核酸,以确定该个体为COL26A1rs4045阳性和CACNA1C变体阳性和/或CSMD1变体阳性和/或ZSCAN4变体阳性和/或ZNF551变体阳性和/或DYM变体阳性和/或LINC00348变体阳性和/或FOXL2NB变体阳性和/或基因间变体阳性的。各种提取方法均适合分离DNA或RNA。合适的方法包括苯酚及氯仿提取法。参见Maniatis等人,MolecularCloning,ALaboratoryManual,第2版,ColdSpringHarborLaboratoryPress,第16.54页(1989)。许多种商业试剂盒还可产生DNA和/或RNA。然而,不一定要采用核酸提取,并且比如血液或唾液的样品可以直接分析,不需要从样品中提取核酸即可用以确定个体为COL26A1rs4045阳性和CACNA1C变体阳性和/或CSMD1变体阳性和/或ZSCAN4变体阳性和/或ZNF551变体阳性和/或DYM变体阳性和/或LINC00348变体阳性和/或FOXL2NB变体阳性和/或基因间变体阳性的。在一些实施方案中,样品的分析包括将RNA逆转录产生cDNA。在一些实施方案中,样品的分析包括扩增样品中的核酸或由样品中的核酸衍生的核酸(例如,cDNA)。可使用的扩增方法包括RT-PCR的变动形式,包括定量RT-PCR,例如,采用由Wang,A.M.等人,Proc.Natl.Acad.Sci.USA86:9717-9721,(1989)或由Karet,F.E.等人,AnalyticalBiochemistry220:384-390(1994)描述的方法。另一种可采用的核酸扩增或突变检测方法为连接酶链式反应(LCR),如由Wiedmann等人,PCRMethodsAppl.3:551-564,(1994)所述。另一种扩增或突变检测方法为等位基因特异性PCR(ASPCR)。利用模板与引物3′末端碱基之间的匹配或错配的ASPCR是本领域熟知的。参见例如美国专利No.5,639,611,其以引用方式并入本文中且成为本文的一部分。另一种分析样品以确定存在遗传变体的方法包括核酸测序。测序可采用本领域已知的任何方法、试剂盒或系统进行。一个实例是使用染料终止剂化学法(dyeterminatorchemistry)和ABI测序仪(AppliedBiosystems,FosterCity,Calif.)。测序还可涉及单碱基确定法,诸如单核苷酸引物延伸(测序法)或等位基因或突变特异性PCR。多重系统(MultiplexSystem)是基于引物延伸的方法,该方法可让多达10种SNP(单核苷酸多态性)进行多重反应。该化学基于一种未标记的寡核苷酸引物(或多种引物)的二脱氧单碱基延伸。每个引物在荧光标记的ddNTP和DNA聚合酶(DNAPolymerase,FS)的存在下与互补模板结合。该聚合酶将引物延伸一个核苷酸,从而在其3′末端增加单个ddNTP。多重系统可商购获得(ABIPRISM.多重试剂盒,AppliedBiosystemsFosterCity,Calif.)。使用ABI多重试剂盒产生的产物可用分析软件3.1版或更高版本,利用ABI310遗传分析仪(GeneticAnalyzer)、ABI3100遗传分析仪或ABI3700DNA分析仪分析。本领域的技术人员将认识到,基于本文所公开的SNP和相关序列信息,可以开发检测试剂并可将其单独或组合用于分析本技术的任何SNP,并且这样的检测试剂可并入试剂盒中。本文在SNP检测试剂的背景中所用的术语“试剂盒”是指多种SNP检测试剂的组合,或一种或多种SNP检测试剂与一种或多种其他类型的元件或组分(例如,其他类型的生化试剂、容器、包装诸如旨在用于商业规模的包装、欲附连SNP检测试剂的底物、电子硬件部件等)的组合等等。因此,本技术还提供SNP检测试剂盒和系统,其包括但不限于:已包装的探针和引物组(例如,TaqMan探针/引物组),核酸分子的阵列/微阵列,以及包含一种或多种探针、引物或其他用于检测本文所述的一种或多种SNP的检测试剂的珠粒。该试剂盒可任选地包括各种电子硬件部件。例如,各种制造商所提供的阵列(“DNA芯片”)和微流体系统(“芯片实验室(lab-on-a-chip)”系统)通常包括硬件部件。一些试剂盒(例如,TaqMan探针/引物组)可以不包括电子硬件部件,但可由例如包装在一个或多个容器内的一种或多种SNP检测试剂(连同其他任选的生化试剂)组成。在一些实施方案中,SNP检测试剂盒包含一种或多种检测试剂和其他组分(例如,缓冲剂、试剂、具有聚合酶活性的酶、具有聚合酶活性且缺乏5′→3′外切核酸酶活性或5′→3′与3′→5′两者的外切核酸酶活性的酶、连接酶、酶辅因子(诸如镁或锰)、盐、链延伸核苷酸(诸如脱氧核苷三磷酸(dNTP)或生物素化dNTP)、和在Sanger型DNA测序反应情况下的链终止核苷酸(即,二脱氧核苷三磷酸(ddNTP))、阳性对照序列、阴性对照序列等等)来进行分析或反应,诸如扩增和/或检测含SNP的核酸分子。在一些实施方案中,试剂盒包含用于以下方面的装置:确定目标核酸的量,对于多态性而言或当检测基因转录物时确定个体是杂合的还是纯合的,和/或将所述量与标准进行比较。在一些实施方案中,该试剂盒包含使用该试剂盒来检测所关注的含SNP核酸分子的说明。在一些实施方案中,该试剂盒包含用于执行一种或多种分析来检测一种或多种本文所公开的SNP的试剂。在一些实施方案中,SNP检测试剂盒呈核酸阵列或以隔板分开的试剂盒的形式,包括微流体/芯片实验室系统。该试剂盒还可包含以下一者或多者:洗涤缓冲剂和/或试剂、杂交缓冲剂和/或试剂、标记缓冲剂和/或试剂和检测装置。可针对该试剂盒旨在用于的特定扩增/检测技术来优化缓冲剂和/或试剂。将这些缓冲剂和试剂用于执行不同过程步骤的方案也可包括在试剂盒内。在一些实施方案中,该SNP检测试剂盒包含:至少一组引物(例如,包含一个匹配的等位基因特异性引物和一个错配的等位基因特异性引物),和任选地不可延伸的寡核苷酸探针。每个试剂盒可包含使该过程为特异性的试剂。因此,旨在用于检测特定SNP的试剂盒可包含:特异性检测该特定SNP的匹配和错配的等位基因特异性引物组,和任选地不可延伸的寡核苷酸探针。旨在用于多重检测多种SNP的试剂盒包含:多个引物组,每组均对检测一种特定SNP有特异性;和任选地多个对应的不可延伸的寡核苷酸探针。在一些实施方案中,该SNP检测试剂盒包含针对一个或多个目标SNP基因座的多对引物,其中所述引物的设计使得来自不同SNP基因座或来自相同SNP基因座的不同等位基因的所述PCR产物的长度足以在毛细管电泳分析中彼此加以区分,因而使其适于多重PCR。SNP检测试剂盒还可包含荧光标记的单碱基延伸/终止试剂,即ddNTP,以在多重PCR反应期间标记引物(例如,SNaPshotMultiplex)。SNP检测试剂盒的化学可基于未标记的引物的二脱氧单碱基延伸。每个引物均可在荧光标记的ddNTP的存在下与其目标SNP基因座结合,且聚合酶将引物延伸一个核苷酸,从而在其3′末端增加单个ddNTP。可通过读取荧光颜色来确定所并入的核苷酸的种类。在一些实施方案中,该试剂盒包含多对引物,以用于同时检测至少一个具有两个或更多个不同等位基因的SNP基因座。在一些实施方案中,该试剂盒包含多对引物,以用于在1至8种不同的SNP基因座中同时检测不同的基因型。在一些实施方案中,该SNP检测试剂盒包含多对引物,该引物具有被设计成用于单个扩增反应的退火温度。在一些实施方案中,该试剂盒还包含内部对照多核苷酸和/或多种对照引物,以使用内部对照多核苷酸作为模板来进行多重PCR。在一些实施方案中,SNP检测试剂盒可包含例如在各目标SNP位置处或附近与核酸分子杂交的一个或多个探针,或多对探针。该试剂盒可包含多对等位基因特异性探针,以同时分析多个SNP,其中至少一个为本文所公开的SNP。在某些实施方案中,该试剂盒包含多对等位基因特异性探针,以同时分析本文所述的所有SNP。在一些实施方案中,该试剂盒包含捕获引物和任选地延伸引物,以用于检测选自COL26A1、CACNA1C、CSMD1、ZSCAN4、ZNF551、DYM、LINC00348和FOXL2NB的一种或多种基因的一个或多个SNP。在一些实施方案中,该SNP检测试剂盒包含至少一组预先选择的核酸序列,该序列充当延伸产物的捕获探针。该预先选择的核酸序列(等位基因特异性探针)可以固定在阵列或珠粒(例如,编码珠粒)上,且可用于检测至少1、4、10、11个、所有的本文所公开的SNP、或其任何组合。仅供举例说明,该试剂盒可包含聚苯乙烯微球,该微球内部经过两种不同光谱的荧光染料染色(例如,x-MAPTM微珠,LuminexCorp.(Austin,Tex.))。使用准确比例的这些荧光团,即可产生大量不同的荧光珠粒组(例如,一组100个)。每一组珠粒可通过其编码(或光谱特征)区分,并可用于检测单一反应容器中大量不同的延伸产物。这些具有可区分的编码的荧光珠粒组可用于标记延伸产物。可通过任何合适的方式在珠粒上标记(或附接)延伸产物,该方式包括但不限于:化学或亲和捕获、交联、静电附接等等。在一些实施方案中,延伸产物的标记通过等位基因特异性引物和标签探针序列的杂交来进行。可采用充当报告子(reporter)的第三种荧光染料(例如,生物素化dNTP),来测量在微球表面上发生的生物分子相互作用的程度。由于每一种不同的延伸产物均经过荧光珠粒而被独特标记,因此所捕获的延伸产物(指示所关注的SNP的一个等位基因)可与其他不同的延伸产物(包括指示相同SNP的其他等位基因的延伸产物和指示其他所关注的SNP的延伸产物)区分。杂交后,可使用诸如流式细胞术的方法分析微珠。在引物延伸反应在生物素化dNTP的存在下进行的实施方案中,可在与荧光标记的链霉亲和素(例如,Cy5-链霉亲和素偶联物)反应后,使用诸如100TMTotalSystem、100TMISTotalSystem、LuminexTM高通量筛选系统(HighThroughputScreeningSystem))等仪器,由荧光来定量珠粒与延伸产物之间的反应。一些实施方案提供在生物样品中鉴定本文所公开的SNP的方法,其包括:将得自受试者的核酸的测试样品与包含对应于本文所公开的至少一个SNP位置的一种或多种探针的阵列一起温育,并分析来自该测试样品的核酸与一种或多种探针的结合。将测试样品与来自采用一种或多种SNP检测试剂的试剂盒中的此类SNP检测试剂一起温育的条件可以变化。温育条件取决于诸如分析所采用的格式、所采用的检测方法和分析所采用的检测试剂的类型及性质等因素。本领域的技术人员将认识到,任一种常用的杂交、扩增和阵列分析格式均可容易地适于检测本文所公开的SNP。在一些实施方案中,本技术的SNP检测试剂盒包含加至样品中的对照分析物、缓冲剂(包括结合、洗涤和洗脱缓冲剂)、固相载体(诸如珠粒、蛋白A或G或亲和素包被的琼脂糖(sepharose或agarose)等)以及基质辅助激光解吸/电离(MALDI)样品板。该试剂盒还可包含数据库,该数据库可以呈包含选自COL26A1、CACNA1C、CSMD1、ZSCAN4、ZNF551、DYM、LINC00348和FOXL2NB的一种或多种基因的一个或数个SNP的信息的表格、纸张或电子媒介的形式。在一些实施方案中,该试剂盒包含编程,以允许机器人系统执行本方法,例如,编程以指导机器人移液器或者接触式或喷墨式打印机来添加、混合和移除试剂。该试剂盒的各种部件可存在于分开的容器中或某些相容的部件可根据需要预先在单一容器中组合。在一些实施方案中,该试剂盒包含用于制备或处理基质辅助激光解吸/电离飞行时间质谱(MALDI-TOF)的分析物样品的一种或多种其他试剂。该试剂可包括一种或多种基质、溶剂、样品制备试剂、缓冲剂、脱盐试剂、酶试剂、变性试剂,其中也可提供校准标准品,诸如阳性和阴性对照。因此,该试剂盒可包括一个或多个容器,诸如小瓶或瓶子,其中每个容器包含用于执行样品处理或准备步骤和/或用于执行MALDI-TOF方案的一个或多个步骤的分开的部件。除了上述部件外,该试剂盒还包括使用该试剂盒的部件来准备MALDI-TOF样品板和/或评估样品的说明。该说明(诸如用于制备样品或经由MALDI-TOF来分析样品)通常记录在合适的记录媒介上。例如,该说明书可印刷在基材上,诸如纸张或塑料等。因此,该说明可作为包装插页、试剂盒的容器或其部件上的标签(即,与包装或小包装相连)等而存在于试剂盒中。在一些实施方案中,该说明作为存在于合适的计算机可读存储介质上的电子存储数据文件而存在。在一些实施方案中,实际的说明不存在于试剂盒中,但提供可从远程来源获得该说明(例如,经由互联网)的方式。此实施方案的实例为包括网址的试剂盒,在该网址中可以查看该说明和/或可以从该网址下载该说明。与该说明一样,获得说明的该方式也记录在合适的基材上。除了数据库、编程和说明外,该试剂盒还可以包含一种或多种对照分析混合物,例如,用于测试该试剂盒的两种或更多种对照样品。还可采用下一代测序(NGS)来确定个体的基因型。下一代测序是一种高通量的大量并行测序方法(例如,使用大量处理器或分开的计算机的方法),其可让经过克隆扩增的分子和单一核酸分子并行产生多个测序反应。此作法可以提高通量和数据产量。NGS方法包括例如使用可逆转的染料终止剂进行的合成测序法,和连接酶测序法。常用的NGS平台的非限制性实例包括miRNABeadArray(Illumina,Inc.)、Roche454TMGSFLXTM-Titanium(RocheDiagnostics)、(LuminexCorp.)、IONTORRENTTM(LifeTechnologiesCorp.)和ABISOLiDTM系统(AppliedBioSystems,FosterCity,CA)。认知在本发明的一个实施方案中,沃替西汀可用于治疗经鉴定为(i)COL26A1rs4045阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045阳性和CACNA1C变体阳性,(vii)COL26A1rs4045、CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045、CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性的认知损害的个体。在另一个实施方案中,一种在罹患认知损害的个体经确定为(i)COL26A1rs4045阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045阳性和CACNA1C变体阳性,(vii)COL26A1rs4045、CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045、CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性时,确定该个体将在接受沃替西汀治疗时经历增强的治疗效果的可能性的方法。同样地,本文还描述在罹患认知损害的个体经确定为(i)COL26A1rs4045纯合的阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045纯合的及CACNA1C变体阳性,(vii)COL26A1rs4045纯合的及CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045纯合的及CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045纯合的及CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045纯合的及CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045纯合的及CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性时,确定该个体对沃替西汀的治疗将产生有利反应的可能性的方法。在本发明的一些方面,该公开的方法考虑使用沃替西汀治疗经诊断为患有认知功能损害的个体。在一个最优选的实施方案中,该接受治疗、对治疗产生有利反应和/或经历增强治疗效果的个体经鉴定为COL26A1rs4045纯合的及CACNA1C变体阳性、CSMD1变体阳性和ZSCAN4变体阳性。在本发明的一个实施方案中,沃替西汀可用于治疗患有认知损害的个体,其中该个体罹患抑郁症和/或MDD且经确定或经鉴定为(i)COL26A1rs4045阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045阳性和CACNA1C变体阳性,(vii)COL26A1rs4045、CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045、CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性。在另一个实施方案中,一种在罹患认知损害且还罹患抑郁症和/或MDD的个体经确定为(i)COL26A1rs4045阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045阳性和CACNA1C变体阳性,(vii)COL26A1rs4045、CACNA1C和CSMD1变体阳性,(viii)COL26A1rs4045、CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045、CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性时,确定该个体在接受沃替西汀治疗时将经历增强的治疗效果的可能性的方法。同样地,本文还描述一种当罹患认知损害的个体在罹患抑郁症和/或MDD且经确定为(i)COL26A1rs4045纯合的阳性,(ii)CACNA1C变体阳性,(iii)CSMD1变体阳性,(iv)ZSCAN4变体阳性,(v)ZNF551变体阳性,(vi)COL26A1rs4045纯合的及CACNA1C变体阳性,(vii)COL26A1rs4045纯合的及CACNA1C与CSMD1变体阳性,(viii)COL26A1rs4045纯合的及CACNA1C、CSMD1和ZSCAN4变体阳性,(ix)COL26A1rs4045纯合的及CACNA1C、CSMD1、ZSCAN4和ZNF551变体阳性,(x)COL26A1rs4045纯合的及CACNA1C、CSMD1、ZSCAN4、DYM和基因间变体阳性,或(xi)COL26A1rs4045纯合的及CACNA1C、CSMD1、ZSCAN4、DYM、LINC00348、FOXL2NB和基因间变体阳性时,确定该个体对沃替西汀的治疗将产生有利反应的可能性的方法。在本发明的一些方面,所公开的方法考虑使用沃替西汀治疗经诊断患有抑郁症和/或MDD的个体,以改善认知功能。在一个最优选的实施方案中,该接受治疗、对治疗产生有利反应和/或经历增强治疗效果的个体经鉴定为COL26A1rs4045纯合的及CACNA1C变体阳性、CSMD1变体阳性和ZSCAN4变体阳性。根据CDC,认知损害是指一个人在记忆、学习新事物、集中注意力或下决定时出现困难而影响其日常生活。认知损害的范围为轻度至重度。对于轻度损害,患者可能开始注意到认知功能的变化,但仍然可以进行其日常活动。重度损害可导致丧失理解某些事物的意义与重要性的能力及谈话或书写的能力,以致无法独立生活。认知能力可通过例如麻省总医院认知与身体功能问卷(MassachusettsGeneralHospitalCognitiveandPhysicalFunctioningQuestionnaire)(参见例如,Fava等人,J.Clin.Psychiatry,67:11(2006))和/或数字符号替换测验(DigitSymbolSubstitutionTest)(DSST)(参见Mahableshwarker等人,Neuropsychopharmacology,出版中2015)来评估。认知障碍是一种常见类型的神经病变。例如,痴呆是一种由脑功能障碍造成的认知损害形式。阿尔茨海默氏痴呆(以及一些其他形式的痴呆)的特征在于记忆功能的破坏。在若干称为痴呆的病症中,最常见的是阿尔茨海默病和轻度认知损害(MCI)(其为阿尔茨海默病的临床前形式),以及帕金森病痴呆和路易体痴呆。如本文所述,认知损害与精神分裂症、注意力缺陷多动症、躁郁症、中风后认知缺陷、闭合性脑外伤、术后认知缺陷、亨丁顿氏病、广泛性焦虑症(GAD)和创伤后压力障碍(PTSD)有关。一些实施方案包括治疗与本文所公开的疾病或病症有关的认知损害。参考文献:FavaM,GravesLM,BenazziF,ScaliaMJ,IosifescuDV,AlpertJE,&PapakostasGI.Across-sectionalstudyoftheprevalenceofcognitiveandphysicalsymptomsduringlong-termantidepressanttreatment,J.Clin.Psychiatry,67:11(2006)Ferrari,AJ,CharlsonFJ,NormanRE,FlaxmanAD,PattenSB,VosT&WhitefordHATheEpidemiologicalModellingofMajorDepressiveDisorder:ApplicationfortheGlobalBurdenofDiseaseStudy2010.PlosOne8(7):e69637,2013.KendlerKS,GatzM,GardnerCOandPedersenNL.ASwedishNationalTwinSmdyofLifetimeMajorDepression.AmJPsychiatry163:109-114,2006.Mahableshwarker,AR,Zajecka,J,JacobsenW,ChenY&KeefeRSARandomized,Placebo-Controlled,Active-Reference,Double-Blind,Flexible-DoseStudyoftheEfficacyofVortioxetineonCognitiveFunctioninMajorDepressiveDisorder.Neuropharmacology,Fen.17,2015;出版中。本申请中所公开的所有参考文献的主题全文以引用方式并入本文中。实施例实施例1研究设计-治疗组进行多中心、随机、双盲、平行组、安慰剂对照、药物参考、固定剂量研究来评估沃替西汀(10、15和20mg/天)在急性治疗患有MDD的成年患者中的效力和安全性。本研究包括总共595位符合复发型MDD的DSM-IV-TR诊断标准的个体。通过DSM病症结构性临床访谈(StructuredClinicalInterviewforDSMDisorders)(SCID)确认每位个体的当前重性抑郁障碍。个体报告其当前MDE已持续至少3个月。个体还在筛选和基线访视时得到≥26的总MADRS得分和≥4的CGI-S得分。个体每天接受10、15或20mg沃替西汀、或不同药物、或安慰剂治疗,持续8周。参见图1。在治疗的前2周内每周观察受试者,然后每2周一次,直到8周治疗期结束为止。主要结局测量指标为治疗8周后的MADRS总得分离基线的变化。蒙哥马利抑郁量表(Montgomery-DepressionRatingScale)(MADRS)是由10个项目组成的抑郁症量表,每一项均分成0级(无症状)至6级(严重症状)。这10个项目代表抑郁症的核心症状。基于与患者临床访谈最近7天内与症状有关的一般广泛性问题到更详细的问题来分级,以便为严重性准确分级。总得分为0至60,得分越高表示越严重。次要结局测量指标包括在第8周时有反应者的比例(有反应者定义为MADRS总得分比基线降低50%);第8周时的MADRS总得分离基线的变化;以及第8周时使用CGI-I得分的临床状态变化。临床总体印象-总体改善(TheClinicalGlobalImpression-GlobalImprovement)(CGI-I)量表为分成1级(极大改善)至7级(极大恶化)的7级量表。研究者相对于基线来评定患者的总体改善,根据研究者的意见,不论是否有改善,均完全归因于药物治疗。研究设计-基因型测定将来自个体的核酸样品在IlluminaTMHumanOmni5EXOME全基因组珠粒-芯片阵列上根据制造商的方案运行。在质量控制(QC)后,将595个样品乘以4,641,218个变体的原始数据集缩减至473个样品乘以3,923,897个变体。参见图1。分析经由惩罚回归法,使用一组被关注的基因组区来计算综合得分(或遗传得分)。然后鉴定达到最大治疗特异性效果的遗传得分的截止点。然后确定由最佳截点所限定的该亚组的治疗效果的统计显著性(经由参数自助法(parametricbootstrapmethod))。结果CACNA1C、COL26A1rs4045、CSMD1、ZSCAN4和ZNF551显示出治疗特异性效果的统计上显著的证据。经由基于CACNA1C+rs4045的遗传特征而鉴定的亚组显示出统计上显著增强的治疗效果。参见图2-4。经由基于CACNA1C、COL26A1rs4045和CSMD1的遗传特征而鉴定的亚组也显示出统计上显著增强的治疗效果。参见图9。经由基于CACNA1C、COL26A1rs4045、CSMD1和ZSCAN4的遗传特征而鉴定的亚组也显示出统计上显著增强的治疗效果。参见图10和图11。实施例2下表证实具有COL26A1rs4045和CACNA1C变体的个体在接受20mg/天的沃替西汀施用持续8周时表现出改善的认知。表1.根据治疗和亚组的反应率。每个表元为“有反应者数量/样品数量”COL26A1rs4045和CACNA1C变体阳性变体阴性N/A总计Lu20mg14/176/2528/7840/120安慰剂5/176/3021/8148/128总计19/3412/5549/28232/371表2.所有组合并的亚组反应无反应有反应不在亚组内4312在亚组内1519<NA>19389表3.仅接受Lu20mg的亚组反应无反应有反应不在亚组内196在亚组内314<NA>5028表4.仅接受安慰剂的亚组反应无反应有反应不在亚组内246在亚组内125<NA>6021实施例3表5显示其表达水平可在多基因模型中加以组合的基因和基因组合,所述基因和基因组合与接受20mg/天沃替西汀治疗的成年MDD患者中的总体反应率显著相关。在表中,B等位基因表示次要等位基因,而A等位基因表示主要等位基因。表5:遗传特征中所用的5种变体MAF=次要等位基因频率该5变体(5-SNP)模型显示出治疗特异性效果的统计上显著的证据。经由表5所示的遗传特征组而鉴定的亚组显示出统计上显著增强的治疗效果。参见图9。此外,该亚组外的受试者显示出统计上显著的无反应效应。参见图9。使用组合式弹性网(elasticnet)/自助(bootstrapping)法鉴定了显示出增强治疗效果的亚组,类似于Li等人,“Amulti-markermolecularsignatureapproachfortreatment-specificsubgroupidentificationwithsurvivaloutcomes,”ThePharmacogenomicsJournal,14(5):439-45(2014)中所述,该文献以引用方式并入本文中且成为本文的一部分。具体地讲,数据集经自助抽样处理1000次,并将每个自助抽样的数据集用于采用弹性网重新估算得分。采用此方法,使用1000个估算值的2.5%和97.5%百分位数,以95%置信区间(CI)估算各SNP的系数范围。95%CI系数范围示于表5。对于每种特征,使用这些系数,将患者得分计算为:其中j表示第j个SNP,且患者的关系为在此公式中,G为0、1或2,具体取决于患者的等位基因组合(参见表5),而系数β选自为每个特定变体提供的范围内(也参见表5)。采用此公式,使用下式鉴定有反应者,其中最佳截止值为τ*=-0.6:得分i=(rs4045系数)*rs4045+(rs59420002系数)*rs59420002+(rs7297582系数)*rs7297582+(rs2239042系数)*rs2239042+(rs7311147系数)*rs7311147此实施例中采用的具体算法如下:得分i=-0.9*rs4045+1.6*rs59420002-0.3*rs7297582-0.8*rs2239042+0.3*rs7311147本研究中5变体模型的受试者人口统计学和基线人口统计学与特征示于图9D,其中SNP5=1对应于由5变体模型鉴定的亚组内的患者,而SNP5=0对应于不在该亚组内的患者。由这些研究,经由LOCF(末次观察推进法(lastobservationcarriedforward))确定第8周时的有反应者比例(图9E)和第8周时的缓解率(图9F)。此外,经由MMRM(重复测量混合模型)确定第8周时和每次访视时的基线MADRS总得分变化(图9G-I)。还计算了第8周时CGI-I得分(9J)和HAM-A总得分离基线的变化(9K)。经由LOCF,基于人种计算了第8周时的有反应者比例,且示于图9L。在5变体模型中,在施用20mg沃替西汀后测定恶心比例(图9M)。图9N比较在5变体模型中使用沃替西汀20mgQD、度洛西汀60mgQD和安慰剂QD的治疗效果(即,优势比(OR))。沃替西汀相对于度洛西汀的增强治疗效果示于表6,而度洛西汀相对于安慰剂的治疗效果示于表7。表6:使用沃替西汀相对于度洛西汀的治疗治疗OR(95%CL)不在亚组内0.24(0.07-0.86)在亚组内4.17(1.15-16.67)总体0.82(0.36-1.85)表7:使用度洛西汀相对于安慰剂的治疗治疗OR(95%CL)不在亚组内2.29(0.68-7.71)在亚组内1.54(0.46-5.17)总体1.44(0.65-3.18)图9O-S示出具有A/GEMID2等位基因(9O)、A/Grs2239042等位基因(9P)、C/Trs7297582等位基因(9Q)、A/Grs1006737等位基因(9R)和A/Grs7311147等位基因(9S)的个体的总体反应状态图。实施例4表8显示其表达水平可在多基因模型中加以组合的基因和基因组合,所述基因和基因组合与接受20mg/天沃替西汀治疗的成年MDD患者中的总体反应率显著相关。在表中,B等位基因表示次要等位基因,而A等位基因表示主要等位基因。表8:遗传特征中所用的7种变体MAF=次要等位基因频率该7变体(7-SNP)模型显示出治疗特异性效果的统计上显著的证据。经由表8所示的遗传特征而鉴定的亚组显示出统计上显著增强的治疗效果。参见图10。此外,该亚组外的受试者显示出统计上显著的无反应效应。参见图10。采用实施例3所示的弹性网/自助法鉴定了显示出增强治疗效果的亚组。具体地讲,采用下式鉴定有反应者,其中最佳截止值为τ*=-0.6;得分i=(rs4045系数)*rs4045+(rs59420002系数)*rs59420002+(rs7297582系数)*rs7297582+(rs2239042系数)*rs2239042+(rs7311147系数)*rs7311147+(rs12983596系数)*rs12983596+(rs9749513系数)*rs9749513此实施例中采用的具体算法如下:得分i=-0.8*rs4045+1.3*rs59420002-0.1*rs7297582-0.6*rs2239042+0.4*rs7311147-0.5*rs12983596-0.4*rs9749513本研究中7变体模型的受试者人口统计学和基线人口统计学与特征示于图10D,其中SNP7=1对应于由7变体模型鉴定的亚组内的患者,而SNP7=0对应于不在该亚组内的患者。由这些研究,经由LOCF确定第8周时的有反应者比例(图10E)和第8周时的缓解率(图10F)。此外,经由MMRM确定第8周时和每次访视时的基线MADRS总得分变化(图10G-I)。5变体模型和7变体模型中MADRS总得分离基线的变化的比较示于图10J。还计算了第8周时的CGI-I得分(10K)和HAM-A总得分离基线的变化(10L)。经由LOCF,基于人种计算了第8周时的有反应者比例,且示于图10M。图10N比较使用沃替西汀20mgQD、度洛西汀60mgQD和安慰剂QD的治疗效果。增强的治疗效果的比较示于表9和表10。表9:使用沃替西汀相对于度洛西汀的治疗治疗OR(95%CL)不在亚组内0.30(0.09-0.98)在亚组内6.25(1.41-33.33)总体0.82(0.36-1.85)表10:使用度洛西汀相对于安慰剂的治疗治疗OR(95%CL)不在亚组内1.51(0.51-4.42)在亚组内1.87(0.49-7.15)总体1.44(0.65-3.18)实施例5表11显示其表达水平可在多基因模型中加以组合的基因和基因组合,所述基因和基因组合与接受20mg/天沃替西汀治疗的成年MDD患者中的总体反应率显著相关。在表中,B等位基因表示次要等位基因,而A等位基因表示主要等位基因。表11:遗传特征中所用的14种变体该14变体模型显示出治疗特异性效果的统计上显著的证据。经由表11所示的遗传特征而鉴定的亚组显示出统计上显著增强的治疗效果。参见图11。此外,该亚组外的受试者显示出统计上显著的无反应效应。参见图11。采用实施例3所示的弹性网/自助法鉴定了显示出增强治疗效果的亚组。具体地讲,采用下式鉴定有反应者,其中最佳截止值为τ*=-1.4:得分i=(rs4045系数)*rs4045+(rs59420002系数)*rs59420002+(rs7297582系数)*rs7297582+(rs2239042系数)*rs2239042+(rs7311147系数)*rs7311147+(rs9304796系数)*rs9304796+(rs73064580系数)*rs73064580+(rs12983596系数)*rs12983596+(rs12984275系数)*rs12984275+(rs9749513系数)*rs9749513+(rs12609579系数)*rs12609579+(rs4239480系数)*rs4239480+(rs9676604系数)*rs9676604+(rs12162232系数)*rs12162232此实施例中采用的具体算法如下:得分i=-0.8*rs4045+1.2*rs59420002-0.1*rs7297582-0.7*rs2239042+0.3*rs7311147-0.1*rs9304796+0.1*rs73064580-0.4*rs12983596-0.1*rs12984275-0.3*rs9749513+0.1*rs12609579+0.1*rs4239480+0.1*rs9676604-0.05*rs12162232实施例6表12显示其表达水平可在多基因模型中加以组合的基因和基因组合,所述基因和基因组合与接受20mg/天沃替西汀治疗的成年MDD患者中的总体反应率显著相关。经证实表12所列的SNP可与上文所示的7基因和14基因模型中的SNP交换,在治疗反应效应或无反应效应中无任何显著变化。表12:第19号染色体上的SNP:ZSCAN4和ZNF551实施例7上文讨论的5变体和7变体模型显示了10mg沃替西汀和20mg沃替西汀两者的治疗特异性效果的证据。该效果由20mg沃替西汀和10mg沃替西汀治疗期间所得的MADRS得分证实。参见图12A,其显示了7-SNP模型中所得的MADRS得分。在10mg沃替西汀治疗期间,使用7变体模型得到的MADRS得分的最小二乘均值图在图12B中示出。利用5变体模型对20mg沃替西汀、10mg沃替西汀和安慰剂的治疗效果的比较示于图12C,而7变体模型中治疗的比较示于图12D。图12E显示了本实施例中提及的3项单独研究在排除对应于20位依从性差患者的数据后的样品可说明性。实施例8上文实施例4中所讨论的7变体模型显示了成年MDD患者在接受10mg/天和20mg/天沃替西汀施用后认知力均得到改善的证据。该效果由图13A中所示的认知与身体功能问卷(CognitiveandPhysicalFunctioningQuestionnaire)(CPFQ)结果证实。该数据在图13B中以图形方式表示为CPFQ总得分离基线的变化。图13C显示了10mg/天和20mg/天沃替西汀数据相对于安慰剂数据的图形表示。在图13中,术语“SNP7=1”对应于由7变体模型鉴定的亚组内的患者;术语“SNP7=0”对应于不在该亚组内的患者。实施例9表13显示其表达水平可在多基因模型中加以组合的基因和基因组合,所述基因和基因组合与接受20mg/天沃替西汀治疗的成年MDD患者中的总体反应率显著相关。在表中,B等位基因表示次要等位基因,而A等位基因表示主要等位基因。表13:遗传特征中所用的10种变体该10变体模型显示出治疗特异性效果的统计上显著的证据。经由表13所示的遗传特征而鉴定的亚组显示出统计上显著增强的治疗效果。参见图14。此外,该亚组外的受试者显示出统计上显著的无反应效应。参见图14。采用实施例3所示的弹性网/自助法鉴定了显示出增强治疗效果的亚组。具体地讲,采用下式鉴定有反应者,其中最佳截止值为τ*=-0.9:得分i=(rs4045系数)*rs4045+(rs59420002系数)*rs59420002+(rs7297582系数)*rs7297582+(rs2239042系数)*rs2239042+(rs7311147系数)*rs7311147+(rs12983596系数)*rs12983596+(rs9749513系数)*rs9749513+(rs62104612系数)*rs62104612+(rs1998609系数)*rs1998609+(rs4142192系数)*rs4142192此实施例中采用的具体算法如下:得分i=-1.0*rs4045+1.5*rs59420002-0.3*rs7297582-0.7*rs2239042+0.5*rs7311147-0.5*rs12983596-0.4*rs9749513+0.6*rs62104612-0.9*rs1998609+0.5*rs4142192在采用10变体模型鉴定为有反应者和无反应者的患者中,经由MMRM确定了MADRS总得分的变化。图14A-F显示了3个单独的研究组在施用度洛西汀、10mg沃替西汀和/或20mg沃替西汀后MADRS总得分离基线的变化。在图中,“SNP10阳性”对应于在该亚组内的患者,而“SNP10阴性”对应于不在该亚组中的患者。实施例10表14显示其表达水平可在多基因模型中加以组合的基因和基因组合,所述基因和基因组合与接受20mg/天沃替西汀治疗的成年MDD患者中的总体反应率显著相关。在表中,B等位基因表示次要等位基因,而A等位基因表示主要等位基因。表14:遗传特征中所用的11种变体该11变体模型显示出治疗特异性效果的统计上显著的证据。经由表14所示的遗传特征而鉴定的亚组显示出统计上显著增强的治疗效果。此外,该亚组外的受试者显示出统计上显著的无反应效应。使用实施例3所示的弹性网/自助法鉴定了显示出增强治疗效果的亚组。具体地讲,使用下式鉴定有反应者,其中最佳截止值为τ*=-1.3:得分i=(rs4045系数)*rs4045+(rs59420002系数)*rs59420002+(rs7297582系数)*rs7297582+(rs2239042系数)*rs2239042+(rs7311147系数)*rs7311147+(rs12983596系数)*rs12983596+(rs9749513系数)*rs9749513+(rs62104612系数)*rs62104612+(rs1998609系数)*rs1998609+(rs145136593系数)*rs145136593+(rs116191388系数)*rs116191388此实施例中采用的具体算法如下:得分i=-1.1*rs4045+2.2*rs59420002-0.1*rs7297582-0.8*rs2239042+0.5*rs7311147-0.4*rs12983596-0.5*rs9749513+0.7*rs62104612-1.2*rs1998609+2.5*rs145136593+1.4*rs116191388经由MMRM确定了第8周时和每次访视时的基线MADRS得分的变化(图15A-D)。MADRS总得分离基线的变化的比较示于图15E-J。在图中,“SNP11阳性”对应于在该亚组内的患者,而“SNP11阴性”对应于不在该亚组内的患者。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1