新颖的N2,N4,N7,6‑四取代的蝶啶‑2,4,7‑三胺和2,4,6,7‑四取代的蝶啶化合物及其合成和使用方法与流程
相关申请本申请要求2014年8月22日提交的美国临时专利申请号62/040,824和2014年9月15日提交的美国临时专利申请号62/050,321的权益和优先权,它们的内容特此通过引用整体并入。本发明一般地涉及药物科学领域。更具体地,本发明涉及可用作改变免疫功能的药物的组合物。更具体地,本发明涉及2,4,6,7-四取代的蝶啶化合物,包括n2,n4,n7,6-四取代的蝶啶-2,4,7-三胺化合物,和它们在用于影响由toll样受体(tlr)分子介导的免疫刺激的方法中的应用。
背景技术:
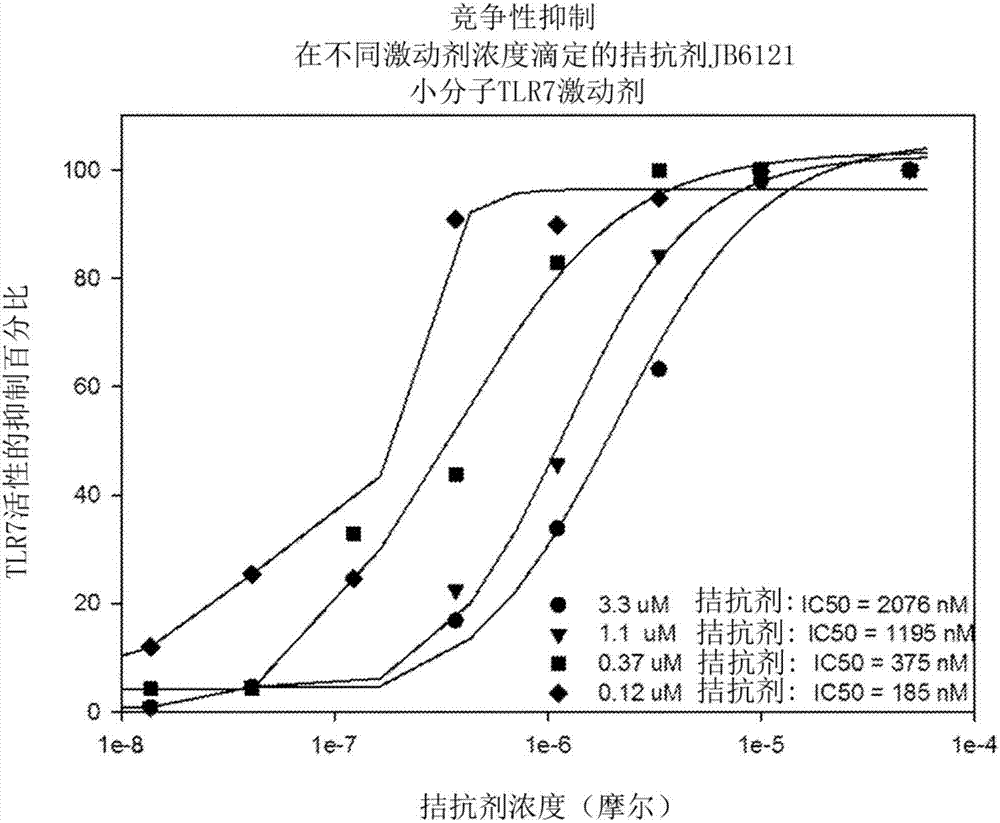
:免疫系统的刺激(其包括先天性免疫和适应性免疫中的任一种或两种的刺激)是可对宿主产生保护性或不利的生理学结果的复杂现象。近年来对构成先天性免疫基础的机制的兴趣增加,先天性免疫被认为引发和支持适应性免疫。以下近期发现部分地推动了这种兴趣:高度保守模式识别受体蛋白(被称为toll样受体(tlr))的家族被认为作为病原体相关分子模式(pamp)和危险相关分子模式(damp)的受体参与先天性免疫。因此对调节先天性免疫有用的组合物和方法引起极大兴趣,因为它们可能影响对病况的治疗方案,所述病况包括自身免疫、炎症、动脉粥样硬化、变态反应、哮喘、移植物排斥、移植物抗宿主病(gvhd)、感染、癌症和免疫缺陷。toll样受体(tlr)是参与先天性免疫的模式识别和信号传递分子的家族。这个家族包括至少十二个成员,命名为tlr1-tlr13,对于其中大部分但非全部成员而言,功能和特异性是已知的。已知这些tlr中的某些响应于遇到特定类型的核酸分子而发信号。例如,tlr9响应于含cpg的dna而发信号,tlr3响应于双链rna而发信号,tlr7和tlr8响应于某种单链rna而发信号。已经有许多报道描述了某些类型的核酸分子(包括cpg核酸和双链rna)的免疫刺激效应。值得注意的是,据报道toll样受体9(tlr9)识别细菌dna和cpgdna,而tlr7和8识别单链rna(hemmi等人(2000),nature408:740-5;bauer等人(2001),procnatlacadsciusa98:9237-42;heil等人(2004),science,303:1526)。除它们的天然配体外,这些核酸响应性tlr的某些合成或人工配体也是已知的。这些包括某些cpg寡脱氧核糖核苷酸(cpgodn)、寡核糖核苷酸(orn)和某些orn类似物及某些小分子,包括咪喹莫特(imiquimod)(r-837)和瑞喹莫德(resiquimod)(r-848)。将咪喹莫特和瑞喹莫德分类为咪唑并氨基喹啉-4-胺;前者目前作为艾达乐tm由3mpharmaceuticals在市场上销售用于局部治疗与乳头状瘤病毒感染相关的肛门生殖器疣。除它们在治疗某些病毒感染诸如乳头状瘤病毒中的用途外,还认为某些tlr激动剂可用作佐剂、抗肿瘤剂和抗变态反应剂。因为许多疾病和病况可以通过增强先天性免疫来治疗,所以继续需要另外的且改善的tlr激动剂。最近还报道,含有igg和核酸的免疫复合物可以刺激tlr9并参与某些自身免疫性疾病中的b细胞活化(leadbetter等人(2002),nature416:595-8)。已经对tlr7、8和9做了这些权利要求的类似且额外的记录(综述在sun等人(2007),inflammationandallergy-drugtargets6:223-235)。技术实现要素:描述了可用作免疫系统调节剂的包含2,4,6,7-四取代的蝶啶核心的化合物,包括n2,n4,n7,6-四取代的蝶啶-2,4,7-三胺化合物。本文描述的分子可以通过抑制tlr信号传递而改变tlr介导的免疫刺激性信号传递,且因而可用作免疫刺激的抑制剂。本文还描述了合成这些化合物的方法。本文描述的组合物和方法可用于在体外和在体内抑制免疫刺激。这样的组合物和方法因而可用在许多临床应用中,包括作为用于治疗涉及不希望的免疫活性的病况(包括炎症性和自身免疫性病症)的药学试剂和方法。本发明的组合物也可用在制备药物的方法中,所述药物用于治疗涉及不希望的免疫活性的病况(包括多种炎症性和自身免疫性病症)。在一个方面,描述了式i的化合物或其药学上可接受的盐,其中每次出现的d独立地是-o-或-n(me)-;且r5是h、f或cl。在本文描述的任一个实施方案中,所述化合物具有选自以下的结构:或其药学上可接受的盐。在本文描述的任一个实施方案中,所述化合物具有选自以下的结构:或其药学上可接受的盐。在本文描述的任一个实施方案中,所述化合物具有以下结构:或其药学上可接受的盐。在本文描述的任一个实施方案中,所述化合物具有以下结构:或其药学上可接受的盐。在本文描述的任一个实施方案中,所述化合物在标准人类果蝇相关基因(humanether-a-go-gorelatedgene,herg)膜片箝测定中具有超过10、15、20、25或30μm的ic50。在本文描述的任一个实施方案中,在肝细胞已经暴露于100μm的化合物24h以后,所述化合物在肝细胞生存力测定中产生超过75%的肝细胞生存力。在另一个方面,描述了式ia的化合物或其药学上可接受的盐,其中r1是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环或烷基杂环;x1和x2各自独立地不存在或者是o;r2是卤素、ora、sra、os(=o)2ra、oc(=o)ra、nrbrc或nra(ch2)pnrbrc,其中p是2-4;r3和r4各自是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc;每次出现的ra独立地是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;且每次出现的rb和rc独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环、芳基;或所述rb和rc与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;或所述ra和rb与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;其中形成的杂环任选地被(c1-c4)烷基取代,且形成的杂环中的一个或多个碳原子任选地被o、nr8或s替换,其中r8是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;前提条件是,当r2是ora、sra、nrbrc或nra(ch2)pnrbrc时,x1和x2中的至少一个是o。在本文描述的任一个实施方案中,r1是烷基、任选地被取代的芳基或任选地被取代的杂芳基。在本文描述的任一个实施方案中,x1和x2都是o。在本文描述的任一个实施方案中,r2是cl或br。在本文描述的任一个实施方案中,r2是os(=o)2ra或oc(=o)ra。在本文描述的任一个实施方案中,r2是nrbrc或nra(ch2)pnrbrc。在本文描述的任一个实施方案中,r4是nrbrc或nra(ch2)pnrbrc。在本文描述的任一个实施方案中,r2和r4是相同的或不同的。在本文描述的任一个实施方案中,r2和r4各自独立地选自:在另一个方面,描述了合成具有式ii的结构的化合物的方法,所述方法包括:(a)将具有式iii的结构的化合物转化成具有式iv的结构的化合物:(b)将具有式iv的结构的化合物转化成具有式ii的结构的化合物:其中每次出现的x独立地不存在或者是烷基、环烷基、芳基或杂环;每次出现的q独立地是h、(ch2)qnrbrc、nra(ch2)pnrbrc、or1、sr1、或crarbrc,其中q是0或1且p是2-4;且x1和x2各自独立地不存在或者是o;r1是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环、烷基杂环;r2”是卤素、ora、os(=o)2ra或oc(=o)ra;r2’是oh、nrbrc或nra(ch2)pnrbrc;a是芳基或杂芳基;每次出现的r9和r10各自独立地是氢、os(=o)2ra、ch2c(=o)ora、c(=o)c(=o)ora、oc(=o)ra、oc(=o)ora或ra’,或者可替换地r9和r10与它们所连接的氮原子一起形成单环或二环碳环或杂环,其中所述碳环或杂环任选地被氧代取代;r3和r4各自独立地是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、ora、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc,其中p是2-4;且每次出现的ra独立地是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;每次出现的rb和rc独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环、芳基;或所述rb和rc与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;或所述ra和rb与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;其中形成的杂环任选地被(c1-c4)烷基取代,且形成的杂环中的一个或多个碳原子任选地被o、nr8或s替换,其中r8是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基。在本文描述的任一个实施方案中,x不存在且q是(ch2)qnrbrc、nra(ch2)pnrbrc、or1、sr1或在本文描述的任一个实施方案中,r2’和r4是相同的。在本文描述的任一个实施方案中,r2’和r4是不同的。在本文描述的任一个实施方案中,r9和r10选自fmoc-、cbz-、boc-、ac-、cf3(c=o)-、苄基、三苯基甲基和对甲苯磺酰基;或r9和r10与它们所键合的氮原子一起形成在本文描述的任一个实施方案中,a是苯基。在本文描述的任一个实施方案中,所述方法还包括(a1)的步骤:(a1)其中每次出现的r2”独立地是卤素、ora、os(=o)2ra或oc(=o)ra。在本文描述的任一个实施方案中,所述步骤(a1)还包括(a2)和(a3)的步骤:(a2)和(a3)其中r9和r10中的至少一个不是氢。在本文描述的任一个实施方案中,步骤(b)还包括(b1)和(b2)的步骤:(b1)和(b2)其中x3是o或不存在,x4是oh或不存在,且ra是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基。在本文描述的任一个实施方案中,r9是h且r10是-(c=o)ora。在本文描述的任一个实施方案中,所述方法还包括(b3)和(b4)的步骤:(b3)和(b4)其中每次出现的rd独立地是h、卤素、os(=o)2ra或oc(=o)ra。在另一个方面,描述了合成具有式ii的结构的化合物的方法,所述方法包括:(a)将具有式x的结构的化合物转化成具有式xi的结构的化合物:和(b)将具有式xi的结构的化合物转化成具有式ii的结构的化合物:其中每次出现的x独立地不存在或者是烷基、环烷基、芳基或杂环;每次出现的q独立地是h、rd、(ch2)qnrarb、nra(ch2)pnrbrc、or1、sr1、或crarbrc,其中q是0或1且p是2-4;且x1和x2各自独立地不存在或者是o;r1是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环、烷基杂环;每次出现的rd独立地是卤素、os(=o)2ra或oc(=o)ra;r2’是oh、nrbrc或nra(ch2)pnrbrc;r3和r4各自独立地是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、ora、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc,其中p是2-4;且每次出现的ra独立地是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;每次出现的rb和rc独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环、芳基;或所述rb和rc与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;或所述ra和rb与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;其中形成的杂环任选地被(c1-c4)烷基取代,且形成的杂环中的一个或多个碳原子任选地被o、nr8或s替换,其中r8是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;前提条件是,如果在式xi的化合物的6位处的rd和r3是相同的,步骤(b)可以被省略。在本文描述的任一个实施方案中,r2’和r4是相同的。在本文描述的任一个实施方案中,r2’和r4是不同的。在本文描述的任一个实施方案中,步骤(a)还包括步骤(a1)和(a2):(a1)和(a2)其中步骤(a1)还包括纯化具有式xii的结构的化合物。在本文描述的任一个实施方案中,所述纯化是柱色谱法纯化或hplc纯化。在本文描述的任一个实施方案中,步骤(a)还包括步骤(a1’)和(a2’):(a1’)和(a2’)其中步骤(a1’)还包括纯化具有式xiii的结构的化合物。在本文描述的任一个实施方案中,所述纯化是柱色谱法纯化或hplc纯化。在本文描述的任一个实施方案中,步骤(a)包括一锅合成步骤(a1x):(a1x)其中步骤(a1x)还包括纯化具有式xi的结构的化合物。在本文描述的任一个实施方案中,所述纯化是柱色谱法纯化或hplc纯化。在本文描述的任一个实施方案中,式x和xi中的取代基-x-q是rd,且步骤(a)包括将具有式x’的结构的化合物转化成具有式xi’的结构的化合物:在本文描述的任一个实施方案中,所述方法还包括步骤(a’):(a’)将具有式xi’的结构的化合物转化成具有式xi”的结构的化合物:其中-x-q不是rd。在本文描述的任一个实施方案中,-x-q是nrarb、nra(ch2)pnrbrc、or1或sr1。在本文描述的任一个实施方案中,-x-q是在本文描述的任一个实施方案中,r2’和r4是相同的。在本文描述的任一个实施方案中,r2’和r4都是在本文描述的任一个实施方案中,rd和r3都是cl。在本文描述的任一个实施方案中,所述方法包括以下2个步骤:(1)和(2)在本文描述的任一个实施方案中,所述方法还包括通过以下步骤制备具有的结构的化合物:(1’)(2’)在本文描述的任一个实施方案中,所述方法还包括通过以下步骤制备具有的结构的化合物:(1”)和(2”)在另一个方面,描述了一种化合物,其选自:在本文描述的任一个实施方案中,描述了选自表1的化合物。在另一个方面,描述了一种药物组合物,其包含至少一种根据本文描述的任一个实施方案的化合物和药学上可接受的载体或稀释剂。在另一个方面,描述了一种治疗有此需要的哺乳动物物种中的自身免疫疾病的方法,其包括给所述哺乳动物物种施用治疗有效量的至少一种根据本文描述的任一个实施方案的化合物。在本文描述的任一个实施方案中,所述哺乳动物物种是人。在本文描述的任一个实施方案中,所述自身免疫疾病选自皮肤和系统性红斑狼疮、胰岛素依赖性的糖尿病、类风湿性关节炎、多发性硬化、动脉粥样硬化、银屑病、银屑病关节炎、炎性肠病、强直性脊柱炎、自身免疫性溶血性贫血、behget氏综合征、古德帕斯彻氏综合征、格雷夫斯病、格-巴二氏综合征、桥本甲状腺炎、特发性血小板减少症、io重症肌无力、恶性贫血、结节性多动脉炎、多肌炎/皮肌炎、原发性胆道硬化、结节病、硬化性胆管炎、舍格伦综合征、系统性硬化症(硬皮病和肢端硬皮综合征(crestsyndrome))、高安动脉炎、颞动脉炎和韦格纳氏肉芽肿病。在另一个方面,描述了一种在有此需要的哺乳动物物种中抑制tlr介导的免疫刺激的方法,其包括给所述哺乳动物物种施用治疗有效量的至少一种根据本文描述的任一个实施方案的化合物。在本文描述的任一个实施方案中,所述哺乳动物物种是人。在另一个方面,描述了一种抑制tlr介导的免疫刺激性信号传递的方法,其包括使表达tlr的细胞与有效量的至少一种根据本文描述的任一个实施方案的化合物接触。在另一个方面,描述了治疗有效量的至少一种根据本文描述的任一个实施方案的化合物用于制备药物的用途,所述药物用于治疗有此需要的哺乳动物物种中的自身免疫疾病。在本文描述的任一个实施方案中,所述哺乳动物物种是人。在本文描述的任一个实施方案中,所述自身免疫疾病选自皮肤和系统性红斑狼疮、胰岛素依赖性的糖尿病、类风湿性关节炎、多发性硬化、动脉粥样硬化、银屑病、银屑病关节炎、炎性肠病、强直性脊柱炎、自身免疫性溶血性贫血、behget氏综合征、古德帕斯彻氏综合征、格雷夫斯病、格-巴二氏综合征、桥本甲状腺炎、特发性血小板减少症、io重症肌无力、恶性贫血、结节性多动脉炎、多肌炎/皮肌炎、原发性胆道硬化、结节病、硬化性胆管炎、舍格伦综合征、系统性硬化症(硬皮病和肢端硬皮综合征)、高安动脉炎、颞动脉炎和韦格纳氏肉芽肿病。在另一个方面,描述了治疗有效量的至少一种根据本文描述的任一个实施方案的化合物用于制备药物的用途,所述药物用于在有此需要的哺乳动物物种中抑制tlr介导的免疫刺激。在本文描述的任一个实施方案中,所述哺乳动物物种是人。在另一个方面,描述了用于治疗有此需要的哺乳动物物种中的自身免疫疾病的、治疗有效量的至少一种根据本文描述的任一个实施方案的化合物。在本文描述的任一个实施方案中,所述哺乳动物物种是人。在本文描述的任一个实施方案中,所述自身免疫疾病选自皮肤和系统性红斑狼疮、胰岛素依赖性的糖尿病、类风湿性关节炎、多发性硬化、动脉粥样硬化、银屑病、银屑病关节炎、炎性肠病、强直性脊柱炎、自身免疫性溶血性贫血、behget氏综合征、古德帕斯彻氏综合征、格雷夫斯病、格-巴二氏综合征、桥本甲状腺炎、特发性血小板减少症、io重症肌无力、恶性贫血、结节性多动脉炎、多肌炎/皮肌炎、原发性胆道硬化、结节病、硬化性胆管炎、舍格伦综合征、系统性硬化症(硬皮病和肢端硬皮综合征)、高安动脉炎、颞动脉炎和韦格纳氏肉芽肿病。在另一个方面,描述了用于治疗有此需要的哺乳动物物种中的不希望的tlr介导的免疫刺激的、治疗有效量的至少一种根据本文描述的任一个实施方案的化合物。在本文描述的任一个实施方案中,所述哺乳动物物种是人。在另一个方面,公开了如说明书中所述的化合物、方法或组合物。附图说明图1显示了根据一个或多个实施方案,某些蝶啶化合物的herg膜片箝研究。图2a显示了根据一个或多个实施方案,jb6121的竞争性抑制研究。图2b显示了根据一个或多个实施方案,使用递增的激动剂攻击剂量的jb6121的拮抗剂ic50研究。图3a显示了根据一个或多个实施方案,jb6121的体内tlp9拮抗作用研究。图3b显示了根据一个或多个实施方案,使用递增的激动剂攻击剂量的jb6121的体内tlp7拮抗作用研究。图4显示了根据一个或多个实施方案,与它的全血暴露有关的jb6121的体内tlp9活性。图5显示了根据一个或多个实施方案,与它的口服给药剂量有关的jb6121的cmax。具体实施方式定义下面是在本说明书中使用的术语的定义。除非另外指出,为本文的基团或术语提供的初始定义适用于贯穿本说明书中单独地或作为另一基团的组成部分的基团或术语。除非另有定义,在本文中使用的所有技术和科学术语具有本领域普通技术人员通常理解的相同含义。术语“烷基”和“alk”表示含有1-12个碳原子、优选1-6个碳原子的直链或支链烷烃(烃)基。示例性的“烷基”基团包括甲基、乙基、丙基、异丙基、正丁基、叔丁基、异丁基、戊基、己基、异己基、庚基、4,4-二甲基戊基、辛基、2,2,4-三甲基戊基、壬基、癸基、十一烷基、十二烷基等。术语“(c1-c4)烷基”表示含有1-4个碳原子的直链或支链烷烃(烃)基,诸如甲基、乙基、丙基、异丙基、正丁基、叔丁基和异丁基。“被取代的烷基”表示在任何可利用的连接点处被一个或多个取代基、优选1-4个取代基取代的烷基。示例性的取代基包括、但不限于以下基团中的一个或多个:氢、卤素(例如,单个卤素取代基或多个卤素取代基,在后一种情况下,形成基团诸如cf3或携带ccl3的烷基)、氰基、硝基、氧代(即,=o)、cf3、ocf3、环烷基、烯基、环烯基、炔基、杂环、芳基、ora、sra、s(=o)re、s(=o)2re、p(=o)2re、s(=o)2ore、p(=o)2ore、nrbrc、nrbs(=o)2re、nrbp(=o)2re、s(=o)2nrbrc、p(=o)2nrbrc、c(=o)ord、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ore、nrdc(=o)nrbrc、nrds(=o)2nrbrc、nrdp(=o)2nrbrc、nrbc(=o)ra或nrbp(=o)2re,其中每次出现的ra独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环或芳基;每次出现的rb、rc和rd独立地是氢、烷基、环烷基、杂环、芳基,或所述rb和rc与它们所键合的n一起任选地形成杂环;且每次出现的re独立地是烷基、环烷基、烯基、环烯基、炔基、杂环或芳基。在前述示例性的取代基中,基团诸如烷基、环烷基、烯基、炔基、环烯基、杂环和芳基本身可以任选地被取代。术语“烯基”表示含有2-12个碳原子和至少一个碳-碳双键的直链或支链烃基。示例性的这样的基团包括乙烯基或烯丙基。术语“c2-c6烯基”表示含有2-6个碳原子和至少一个碳-碳双键的直链或支链烃基,诸如乙烯基、丙烯基、2-丙烯基、(e)-丁-2-烯基、(z)-丁-2-烯基、2-甲基(e)-丁-2-烯基、2-甲基(z)-丁-2-烯基、2、3-二甲基-丁-2-烯基、(z)-戊-2-烯基、(e)-戊-1-烯基、(z)-己-1-烯基、(e)-戊-2-烯基、(z)-己-2-烯基、(e)-己-2-烯基、(z)-己-1-烯基、(e)-己-1-烯基,(z)-己-3-烯基、(e)-己-3-烯基和(e)-己-1,3-二烯基。“被取代的烯基”表示在任何可利用的连接点处被一个或多个取代基、优选1-4个取代基取代的烯基。示例性的取代基包括、但不限于以下基团中的一个或多个:氢、卤素(例如,单个卤素取代基或多个卤素取代基,在后一种情况下,形成基团诸如cf3或携带ccl3的烷基)、氰基、硝基、氧代(即,=o)、cf3、ocf3、环烷基、烯基、环烯基、炔基、杂环、芳基、ora、sra、s(=o)re、s(=o)2re、p(=o)2re、s(=o)2ore、p(=o)2ore、nrbrc、nrbs(=o)2re、nrbp(=o)2re、s(=o)2nrbrc、p(=o)2nrbrc、c(=o)ord、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ore、nrdc(=o)nrbrc、nrds(=o)2nrbrc、nrdp(=o)2nrbrc、nrbc(=o)ra或nrbp(=o)2re,其中每次出现的ra独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环或芳基;每次出现的rb、rc和rd独立地是氢、烷基、环烷基、杂环、芳基,或所述rb和rc与它们所键合的n一起任选地形成杂环;且每次出现的re独立地是烷基、环烷基、烯基、环烯基、炔基、杂环或芳基。所述示例性的取代基本身可以任选地被取代。术语“炔基”表示含有2-12个碳原子和至少一个碳-碳三键的直链或支链烃基。示例性的这样的基团包括乙炔基。术语“c2-c6炔基”表示含有2-6个碳原子和至少一个碳-碳三键的直链或支链烃基,诸如乙炔基、丙-1-炔基、丙-2-炔基、丁-1-炔基、丁-2-炔基、戊-1-炔基、戊-2-炔基、己-1-炔基、己-2-炔基、己-3-炔基。“被取代的炔基”表示在任何可利用的连接点处被一个或多个取代基、优选1-4个取代基取代的炔基。示例性的取代基包括、但不限于以下基团中的一个或多个:氢、卤素(例如,单个卤素取代基或多个卤素取代基,在后一种情况下,形成基团诸如cf3或携带ccl3的烷基)、氰基、硝基、氧代(即,=o)、cf3、ocf3、环烷基、烯基、环烯基、炔基、杂环、芳基、ora、sra、s(=o)re、s(=o)2re、p(=o)2re、s(=o)2ore、p(=o)2ore、nrbrc、nrbs(=o)2re、nrbp(=o)2re、s(=o)2nrbrc、p(=o)2nrbrc、c(=o)ord、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ore、nrdc(=o)nrbrc、nrds(=o)2nrbrc、nrdp(=o)2nrbrc、nrbc(=o)ra或nrbp(=o)2re,其中每次出现的ra独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环或芳基;每次出现的rb、rc和rd独立地是氢、烷基、环烷基、杂环、芳基,或所述rb和rc与它们所键合的n一起任选地形成杂环;且每次出现的re独立地是烷基、环烷基、烯基、环烯基、炔基、杂环或芳基。所述示例性的取代基本身可以任选地被取代。术语“环烷基”表示含有1-4个环和3-8个碳/环的完全饱和的环状烃基。“c3-c7环烷基”表示环丙基、环丁基、环戊基、环己基或环庚基。“被取代的环烷基”表示在任何可利用的连接点处被一个或多个取代基、优选1-4个取代基取代的环烷基。示例性的取代基包括、但不限于以下基团中的一个或多个:氢、卤素(例如,单个卤素取代基或多个卤素取代基,在后一种情况下,形成基团诸如cf3或携带ccl3的烷基)、氰基、硝基、氧代(即,=o)、cf3、ocf3、环烷基、烯基、环烯基、炔基、杂环、芳基、ora、sra、s(=o)re、s(=o)2re、p(=o)2re、s(=o)2ore、p(=o)2ore、nrbrc、nrbs(=o)2re、nrbp(=o)2re、s(=o)2nrbrc、p(=o)2nrbrc、c(=o)ord、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ore、nrdc(=o)nrbrc、nrds(=o)2nrbrc、nrdp(=o)2nrbrc、nrbc(=o)ra或nrbp(=o)2re,其中每次出现的ra独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环或芳基;每次出现的rb、rc和rd独立地是氢、烷基、环烷基、杂环、芳基,或所述rb和rc与它们所键合的n一起任选地形成杂环;且每次出现的re独立地是烷基、环烷基、烯基、环烯基、炔基、杂环或芳基。所述示例性的取代基本身可以任选地被取代。示例性的取代基还包括螺-连接的或稠合的环状取代基,特别是螺-连接的环烷基、螺-连接的环烯基、螺-连接的杂环(不包括杂芳基)、稠合的环烷基、稠合的环烯基、稠合的杂环或稠合的芳基,其中前述环烷基、环烯基、杂环和芳基取代基本身可以任选地被取代。术语“环烯基”表示含有1-4个环和3-8个碳/环的部分不饱和的环状烃基。示例性的这样的基团包括环丁烯基、环戊烯基、环己烯基等。“被取代的环烯基”表示在任何可利用的连接点处被一个或多个取代基、优选1-4个取代基取代的环烯基。示例性的取代基包括、但不限于以下基团中的一个或多个:氢、卤素(例如,单个卤素取代基或多个卤素取代基,在后一种情况下,形成基团诸如cf3或携带ccl3的烷基)、氰基、硝基、氧代(即,=o)、cf3、ocf3、环烷基、烯基、环烯基、炔基、杂环、芳基、ora、sra、s(=o)re、s(=o)2re、p(=o)2re、s(=o)2ore、p(=o)2ore、nrbrc、nrbs(=o)2re、nrbp(=o)2re、s(=o)2nrbrc、p(=o)2nrbrc、c(=o)ord、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ore、nrdc(=o)nrbrc、nrds(=o)2nrbrc、nrdp(=o)2nrbrc、nrbc(=o)ra或nrbp(=o)2re,其中每次出现的ra独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环或芳基;每次出现的rb、rc和rd独立地是氢、烷基、环烷基、杂环、芳基,或所述rb和rc与它们所键合的n一起任选地形成杂环;且每次出现的re独立地是烷基、环烷基、烯基、环烯基、炔基、杂环或芳基。所述示例性的取代基本身可以任选地被取代。示例性的取代基还包括螺-连接的或稠合的环状取代基,特别是螺-连接的环烷基、螺-连接的环烯基、螺-连接的杂环(不包括杂芳基)、稠合的环烷基、稠合的环烯基、稠合的杂环或稠合的芳基,其中前述环烷基、环烯基、杂环和芳基取代基本身可以任选地被取代。术语“芳基”表示具有1-5个芳族环的环状芳烃基,特别是单环或二环基团诸如苯基、联苯基或萘基。在含有两个或更多个芳族环(二环等)的情况下,所述芳基的芳族环可以在单个点处连接(例如,联苯基)或稠合(例如,萘基、菲基等)。“被取代的芳基”表示在任何可利用的连接点处被一个或多个取代基、优选1-3个取代基取代的芳基。示例性的取代基包括、但不限于以下基团中的一个或多个:氢、卤素(例如,单个卤素取代基或多个卤素取代基,在后一种情况下,形成基团诸如cf3或携带ccl3的烷基)、氰基、硝基、氧代(即,=o)、cf3、ocf3、环烷基、烯基、环烯基、炔基、杂环、芳基、ora、sra、s(=o)re、s(=o)2re、p(=o)2re、s(=o)2ore、p(=o)2ore、nrbrc、nrbs(=o)2re、nrbp(=o)2re、s(=o)2nrbrc、p(=o)2nrbrc、c(=o)ord、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ore、nrdc(=o)nrbrc、nrds(=o)2nrbrc、nrdp(=o)2nrbrc、nrbc(=o)ra或nrbp(=o)2re,其中每次出现的ra独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环或芳基;每次出现的rb、rc和rd独立地是氢、烷基、环烷基、杂环、芳基,或所述rb和rc与它们所键合的n一起任选地形成杂环;且每次出现的re独立地是烷基、环烷基、烯基、环烯基、炔基、杂环或芳基。所述示例性的取代基本身可以任选地被取代。示例性的取代基还包括稠合的环状基团,特别是稠合的环烷基、稠合的环烯基、稠合的杂环或稠合的芳基,其中前述环烷基、环烯基、杂环和芳基取代基本身可以任选地被取代。术语“碳环”表示含有1-4个环和3-8个碳/环的完全饱和的或部分饱和的环状烃基,或具有1-5个芳族环的环状芳烃基,特别是单环或二环基团诸如苯基、联苯基或萘基。术语“碳环”包括如在上文中定义的环烷基、环烯基、环炔基和芳基。术语“被取代的碳环”表示在任何可利用的连接点处被一个或多个取代基、优选1-4个取代基取代的碳环或碳环基团。示例性的取代基包括、但不限于上面关于被取代的环烷基、被取代的环烯基、被取代的环炔基和被取代的芳基描述的那些。示例性的取代基还包括在任何可利用的一个或多个连接点处螺-连接的或稠合的环状取代基,特别是螺-连接的环烷基、螺-连接的环烯基、螺-连接的杂环(不包括杂芳基)、稠合的环烷基、稠合的环烯基、稠合的杂环或稠合的芳基,其中前述环烷基、环烯基、杂环和芳基取代基本身可以任选地被取代。术语“杂环”和“杂环的”表示完全饱和的、或部分或完全不饱和的,包括芳族(即,“杂芳基”)环状基团(例如,4-7元单环、7-11元二环或8-16元三环环系),其在至少一个含碳原子的环中具有至少一个杂原子。含有杂原子的杂环基团的每个环可以具有1、2、3或4个选自氮原子、氧原子和/或硫原子的杂原子,其中所述氮和硫杂原子可以任选地被氧化,且所述氮杂原子可以任选地被季铵化(术语“杂芳基鎓(heteroarylium)”表示携带季氮原子且因而携带正电荷的杂芳基)。所述杂环基团可以在环或环系的任何杂原子或碳原子处连接至所述分子的其余部分。示例性的单环杂环基团包括氮杂环丁基、吡咯烷基、吡咯基、吡唑基、氧杂环丁基、吡唑啉基、咪唑基、咪唑啉基、咪唑烷基、噁唑基、噁唑烷基、异噁唑啉基、异噁唑基、噻唑基、噻二唑基、噻唑烷基、异噻唑基、异噻唑烷基、呋喃基、四氢呋喃基、噻吩基、噁二唑基、哌啶基、哌嗪基、2-氧代哌嗪基、2-氧代哌啶基、2-氧代吡咯烷酮基(oxopyrrolodinyl)、2-氧代氮杂环庚三烯基、氮杂环庚三烯基、六氢二氮杂环庚三烯基、4-哌啶酮基、吡啶基、吡嗪基、嘧啶基、哒嗪基、三嗪基、三唑基、四唑基、四氢吡喃基、吗啉基、硫吗啉基、硫吗啉基亚砜、硫吗啉基砜、1,3-二氧杂环戊烷和四氢-1,1-二氧代噻吩基等。示例性的二环杂环基团包括吲哚基、异吲哚基、苯并噻唑基、苯并噁唑基、苯并噁二唑基、苯并噻吩基、苯并[d][1,3]二氧杂环戊烯基、2,3-二氢苯并[b][1,4]二氧杂环己烯基、奎宁环基、喹啉基、四氢异喹啉基、异喹啉基、苯并咪唑基、苯并吡喃基、吲嗪基、苯并呋喃基、苯并呋咱基、色酮基、香豆素基、苯并吡喃基、噌啉基、喹喔啉基、吲唑基、吡咯并吡啶基、呋喃并吡啶基(诸如呋喃并[2,3-c]吡啶基、呋喃并[3,2-b]吡啶基]或呋喃并[2,3-b]吡啶基)、二氢异吲哚基、二氢喹唑啉基(诸如3,4-二氢-4-氧代-喹唑啉基)、三嗪基氮杂环庚三烯基、四氢喹啉基等。示例性的三环杂环基团包括咔唑基、benzidolyl、菲咯啉基、吖啶基、菲啶基、呫吨基等。“被取代的杂环”和“被取代的杂环的”(诸如“被取代的杂芳基”)表示在任何可利用的连接点处被一个或多个取代基、优选1-4个取代基取代的杂环或杂环基团。示例性的取代基包括、但不限于以下基团中的一个或多个:氢、卤素(例如,单个卤素取代基或多个卤素取代基,在后一种情况下,形成基团诸如cf3或携带ccl3的烷基)、氰基、硝基、氧代(即,=o)、cf3、ocf3、环烷基、烯基、环烯基、炔基、杂环、芳基、ora、sra、s(=o)re、s(=o)2re、p(=o)2re、s(=o)2ore、p(=o)2ore、nrbrc、nrbs(=o)2re、nrbp(=o)2re、s(=o)2nrbrc、p(=o)2nrbrc、c(=o)ord、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ore、nrdc(=o)nrbrc、nrds(=o)2nrbrc、nrdp(=o)2nrbrc、nrbc(=o)ra或nrbp(=o)2re,其中每次出现的ra独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环或芳基;每次出现的rb、rc和rd独立地是氢、烷基、环烷基、杂环、芳基,或所述rb和rc与它们所键合的n一起任选地形成杂环;且每次出现的re独立地是烷基、环烷基、烯基、环烯基、炔基、杂环或芳基。所述示例性的取代基本身可以任选地被取代。示例性的取代基还包括在任何可利用的一个或多个连接点处螺-连接的或稠合的环状取代基,特别是螺-连接的环烷基、螺-连接的环烯基、螺-连接的杂环(不包括杂芳基)、稠合的环烷基、稠合的环烯基、稠合的杂环或稠合的芳基,其中前述环烷基、环烯基、杂环和芳基取代基本身可以任选地被取代。术语“烷基氨基”表示具有结构-nhr’的基团,其中r’是氢、烷基或被取代的烷基、环烷基或被取代的环烷基,如本文中所定义。烷基氨基的例子包括、但不限于甲基氨基、乙基氨基、正丙基氨基、异丙基氨基、环丙基氨基、正丁基氨基、叔丁基氨基、新戊基氨基、正戊基氨基、己基氨基、环己基氨基等。术语“二烷基氨基”表示具有结构-nrr’的基团,其中r和r’各自独立地是烷基或被取代的烷基、环烷基或被取代的环烷基、环烯基或被取代的环烯基、芳基或被取代的芳基,杂环基或被取代的杂环基,如本文中所定义。r和r’在二烷基氨基部分中可以是相同的或不同的。二烷基氨基的例子包括、但不限于二甲基氨基、甲基乙基氨基、二乙基氨基、甲基丙基氨基、二(正丙基)氨基、二(异丙基)氨基、二(环丙基)氨基、二(正丁基)氨基、二(叔丁基)氨基、二(新戊基)氨基、二(正戊基)氨基、二(己基)氨基、二(环己基)氨基等。在某些实施方案中,r和r’连接以形成环状结构。得到的环状结构可以是芳族的或非芳族的。环状二氨基烷基的例子包括、但不限于氮杂环丙基、吡咯烷基、哌啶基、吗啉基、吡咯基、咪唑基、1,3,4-三唑基(trianolyl)和四唑基。术语“卤素”或“卤”表示氯、溴、氟或碘。除非另有说明,假定具有不满价的任何杂原子具有足以满价的氢原子。本发明的化合物可以形成也在本发明的范围内的盐。对本发明的化合物的提及被理解为包括对其盐的提及,除非另外指明。如本文所采用的术语“盐”表示与无机和/或有机酸和碱形成的酸式和/或碱式盐。另外,当本发明的化合物含有碱性部分(诸如但不限于吡啶或咪唑)和酸性部分(诸如但不限于羧酸)时,可以形成两性离子(“内盐”)并且其被包括在如本文所使用的术语“盐”中。药学上可接受的(即,无毒的、生理上可接受的)盐是优选的,尽管其它盐也是有用的,例如,在制备过程中可能采用的分离或纯化步骤中。可以如下形成本发明的化合物的盐:例如,在介质(例如,盐沉淀于其中的介质)中或在水性介质中使本文描述的化合物与一定量(诸如等量)的酸或碱在反应,接着低压冻干。含有碱性部分(诸如但不限于胺或吡啶或咪唑环)的本发明的化合物可以与多种有机和无机酸形成盐。示例性酸加成盐包括乙酸盐(诸如与乙酸或三卤乙酸(例如三氟乙酸)形成的乙酸盐)、己二酸盐、海藻酸盐、抗坏血酸盐、天冬氨酸盐、苯甲酸盐、苯磺酸盐、硫酸氢盐、硼酸盐、丁酸盐、柠檬酸盐、樟脑酸盐、樟脑磺酸盐、环戊烷丙酸盐、二葡萄糖酸盐、十二烷基硫酸盐、乙磺酸盐、富马酸盐、葡萄糖庚酸盐、甘油磷酸盐、半硫酸盐、庚酸盐、己酸盐、盐酸盐、氢溴酸盐、氢碘酸盐、羟基乙磺酸盐(例如,2-羟基乙磺酸盐)、乳酸盐、马来酸盐、甲磺酸盐、萘磺酸盐(例如,2-萘磺酸盐)、烟酸盐、硝酸盐、草酸盐、果胶酸盐、过硫酸盐、苯基丙酸盐(例如,3-苯基丙酸盐)、磷酸盐、苦味酸盐、新戊酸盐、丙酸盐、水杨酸盐、琥珀酸盐、硫酸盐(诸如与硫酸形成的硫酸盐)、磺酸盐、酒石酸盐、硫氰酸盐、甲苯磺酸盐诸如甲苯磺酸盐、十一烷酸盐等。含有酸性部分(例如但不限于羧酸)的本发明的化合物可以与多种有机和无机碱形成盐。示例性碱式盐包括铵盐、碱金属盐(诸如钠、锂和钾盐)、碱土金属盐(诸如钙和镁盐)、与有机碱(例如,有机胺)诸如苄星青霉素(benzathine)、二环己胺、哈胺(hydrabamine)(用n,n-双(去氢松香基)乙二胺形成)、n-甲基-d-还原葡糖胺、n-甲基-d-葡糖酰胺(glycamide)、叔丁基胺形成的盐、和与氨基酸诸如精氨酸、赖氨酸等形成的盐。碱性含氮基团可以用试剂诸如低级烷基卤化物(例如,甲基、乙基、丙基和丁基的氯化物、溴化物和碘化物)、二烷基硫酸酯(例如,二甲基、二乙基、二丁基和二戊基硫酸酯)、长链卤化物(例如,癸基、月桂基、肉豆蔻基和硬脂酰基的氯化物、溴化物和碘化物)、芳烷基卤化物(例如,苄基溴和苯乙基溴)等季铵化。本文中也预见到本发明的化合物的前药和溶剂合物。如本文所采用的术语“前药”表示这样的化合物:其在施用给受试者后通过代谢或化学过程发生化学转化以产生本发明的化合物或其盐和/或溶剂合物。本发明的化合物的溶剂合物包括例如水合物。本发明的化合物及其盐或溶剂合物可以以它们的互变异构形式(例如,作为酰胺或亚氨基醚)存在。在本文中预见到所有这样的互变异构形式作为本发明的组成部分。在本发明范围内涵盖本发明的化合物的所有立体异构体(例如,由于不同取代基上的不对称碳可能存在的那些),包括对映异构形式和非对映异构形式。本发明的化合物的单一立体异构体可能例如基本上不含其它异构体(例如,作为具有指定活性的纯的或基本上纯的光学异构体),或可能混合,例如,作为外消旋体或与所有其它的或其它选择的立体异构体混合。本发明的手性中心可以具有如国际纯粹与应用化学联合会(iupac)1974年推荐所定义的s或r构型。通过物理方法例如非对映异构的衍生物的分步结晶、分离或结晶,或通过手性柱色谱法分离,可以拆分外消旋形式。可以通过任意合适的方法从外消旋体获得单一光学异构体,所述方法包括、但不限于常规方法,例如与光学活性的酸形成盐,随后结晶。在其制备之后,优选地分离并纯化本发明的化合物以获得组合物,按重量计,所述组合物含有等于或大于90%、例如等于或大于95%、等于或大于99%的量的化合物(“基本上纯的”化合物),然后将其如本文所述使用或配制。本文将本发明的此类“基本上纯的”化合物也预见为本发明的组成部分。预见到本发明的化合物的所有构型异构体,无论是混合物形式还是纯的或基本上纯的形式。本发明的化合物的定义包括顺式(z)和反式(e)烯烃异构体以及环状烃或杂环的顺式和反式异构体。在本说明书中,可以选择基团及其取代基以提供稳定的部分和化合物。在下面更详细地描述了具体官能团和化学术语的定义。为了本发明的目的,根据元素周期表(cas版本,handbookofchemistryandphysics,第75版,内封面)来鉴别化学元素,且具体官能团一般如本文所述进行定义。另外,有机化学的一般原理,以及具体的官能部分和反应性,描述于“organicchemistry”,thomassorrell,universitysciencebooks,sausalito(1999),其整个内容通过引用并入本文。本发明的某些化合物可以以特定几何或立体异构形式存在。本发明预见到所有这样的化合物,包括顺式-和反式-异构体、r-和s-对映异构体、非对映异构体、(d)-异构体、(l)-异构体、它们的外消旋混合物和它们的其它混合物,它们都落入本发明的范围内。其它不对称的碳原子可以存在于诸如烷基等取代基中。所有这样的异构体以及它们的混合物,都意图包括在本发明中。可以根据本发明利用含多种异构体比例中的任一种的异构体混合物。例如,在仅组合两种异构体的情况下,本发明预见到全部含50:50、60:40、70:30、80:20、90:10、95:5、96:4、97:3、98:2、99:1或100:0异构体比例的混合物。本领域普通技术人员容易地认识到,对更复杂的异构体混合物预见到类似比例。本发明还包括同位素标记的化合物,除了以下事实以外其与本文中公开的化合物相同:一个或多个原子被其原子质量或质量数与通常在自然界中发现的原子质量或质量数不同的原子替换。可以掺入本发明的化合物中的同位素的例子包括氢、碳、氮、氧、磷、硫、氟和氯的同位素,分别例如2h、3h、13c、11c、14c、15n、18o、17o、31p、32p、35s、18f和36cl。含有前述同位素和/或其它原子的其它同位素的本发明的化合物或其对映异构体、非对映异构体、互变异构体或药学上可接受的盐或溶剂合物是在本发明的范围内。本发明的某些同位素标记的化合物,例如在其中掺入了放射性同位素(诸如3h和14c)的那些,在药物和/或底物组织分布测定中是有用的。氚化(即3h)和碳-14(即14c)同位素因为它们的容易制备和可检测性是特别优选的。此外,用较重的同位素诸如氘(即,2h)替换可以获得由较大的代谢稳定性产生的某些治疗优点,例如增加的体内半衰期或减少的剂量需求,并且因此可以在某些情况下是优选的。通过进行在下面的方案和/或实施例中公开的操作,通过用容易得到的同位素标记的试剂替换非同位素标记的试剂,通常可以制备同位素标记的化合物。例如,如果需要本发明的化合物的特定对映异构体,可以通过不对称合成或通过用手性助剂衍生化来制备它,其中分离得到的非对映体混合物,并切割辅助基团,以提供纯的所需对映体。可替换地,在所述分子含有碱性官能团(诸如氨基)或酸性官能团(诸如羧基)的情况下,用适当的光学活性的酸或碱形成非对映异构的盐,随后经本领域公知的分级结晶法或色谱法拆分由此形成的非对映异构体,并随后回收纯的对映异构体。应当理解,如本文中所述的化合物可以被任何数量的取代基或官能部分取代。一般而言,术语“取代”(不论前面是否有术语“任选地”)和在本发明的式中所含的取代基表示,用指定的取代基的残基替代给定结构中的氢残基。当任意给定结构中的超过一个位置可以被超过一个选自指定集合的取代基取代时,在每个位置的所述取代基可以是相同的或不同的。预见到本文中使用的术语“取代”包括有机化合物的所有可允许的取代基。在一个广泛方面,容许的取代基包括有机化合物的无环的和环状的、支链的和非支链的、碳环的和杂环的、芳族的和非芳族的取代基。就本发明的目的而言,诸如氮等杂原子可以具有本文描述的有机化合物的氢取代基和/或任意可允许的取代基,所述取代基满足所述杂原子的化合价。此外,本发明无意以任何方式受到有机化合物的容许的取代基的限制。本发明预见到的取代基和变量的组合优选地是导致稳定化合物的形成的那些,所述稳定化合物可用在例如感染性疾病或增殖性障碍的治疗中。本文中使用的术语“稳定的”优选地表示这样的化合物:其具有足以允许制造的稳定性,并在足够长的待检测时段内及优选地在对本文详述的目的而言有用的足够长时段内维持化合物的完整性。本文中使用的术语“适应性免疫应答”表示任何类型的抗原特异性的免疫应答。在本领域中也称为特异性免疫应答的适应性免疫应答涉及特征还在于免疫记忆的淋巴细胞,由此对第二次或随后暴露于抗原的应答比对第一次向抗原的暴露的应答更有力。术语适应性免疫应答包括体液(抗体)免疫和细胞介导的(细胞的)免疫。本文中使用的“变态反应(allergy)”表示对物质(变应原)的获得性超敏反应。变应性病况包括湿疹、变应性鼻炎或鼻伤风、花粉热、哮喘、风疹(荨麻疹)和食物变态反应及其它特应性病况。本文中使用的术语“抗原物质”表示诱导适应性(特异性)免疫应答的任何物质。抗原通常是可以被t-细胞抗原受体、抗体或b-细胞抗原受体特异性地结合的任何物质。抗原物质包括、但不限于肽、蛋白、碳水化合物、脂质、磷脂、核酸、自身活性物质和激素。抗原物质进一步具体地包括分类为变应原、癌症抗原和微生物抗原的抗原。本文中使用的“哮喘”表示特征在于炎症、气道变窄和气道对吸入的试剂的反应性增加的呼吸系统病症。哮喘经常(尽管非排它地)与特应性或变应性征状相关。例如,哮喘可以由暴露于变应原、暴露于冷空气、呼吸道感染和劳累促成。本文中使用的术语“自身免疫疾病”和等同的“自身免疫病症”和“自身免疫”表示对源自宿主的组织或器官的免疫学上介导的急性或慢性损伤。所述术语包括细胞和抗体介导的自身免疫现象以及器官特异性的和器官非特异性的自身免疫。自身免疫疾病包括胰岛素依赖性的糖尿病、类风湿性关节炎、系统性红斑狼疮、多发性硬化、动脉粥样硬化、银屑病和炎性肠病。自身免疫疾病也包括、但不限于,强直性脊柱炎、自身免疫性溶血性贫血、beget氏综合征、古德帕斯彻氏综合征、格雷夫斯病、格-巴二氏综合征、桥本甲状腺炎、特发性血小板减少症、重症肌无力、恶性贫血、结节性多动脉炎、多肌炎/皮肌炎、原发性胆道硬化、结节病、硬化性胆管炎、舍格伦综合征、系统性硬化症(硬皮病和肢端硬皮综合征)、高安动脉炎、颞动脉炎和韦格纳氏肉芽肿病。自身免疫疾病还包括某些免疫复合物相关疾病。本文中使用的术语“癌症”和等同的“肿瘤”表示这样的病况:其中宿主起源的异常复制细胞以可检测量存在于受试者体内。癌症可以是恶性的或非恶性的癌症。癌症或肿瘤包括、但不限于:胆道癌;脑癌;乳腺癌;宫颈癌;绒毛膜癌;结肠癌;子宫内膜癌;食管癌;胃癌;上皮内肿瘤;白血病;淋巴瘤;肝癌;肺癌(例如,小细胞肺癌和非小细胞肺癌);黑素瘤;神经母细胞瘤;口癌;卵巢癌;胰腺癌;前列腺癌;直肠癌;肾脏(肾)癌;肉瘤;皮肤癌;睾丸癌;甲状腺癌;以及其它癌和肉瘤。癌症可以是原发性的或转移性的。本文中使用的术语“cpgdna”表示含有胞嘧啶-鸟嘌呤(cg)二核苷酸(其c残基未甲基化)的免疫刺激性核酸。在美国专利诸如美国专利号6,194,388、美国专利号6,207,646、美国专利号6,239,116和美国专利号6,218,371和公布的国际专利申请诸如w098/37919、w098/40100、w098/52581和w099/56755中已经广泛地描述了cpg核酸对免疫调节的影响。这些专利和公布的专利申请中的每一个的整个内容特此通过引用并入。整个免疫刺激性核酸可以是未甲基化的,或部分可以是未甲基化的,但是至少5'-cg-3'的c必须是未甲基化的。在一个实施方案中,所述cpgdna是具有由5'-tcgtcgttttgtcgttttgtcgtt-3'(odn2006;seqidno:1)提供的碱基序列的cpgodn。已经按结构和功能将cpgodn进一步分类为至少以下三个类别或类型,它们都意图被包括在本文中使用的术语cpgdna内:b类cpgodn(诸如odn2006)包括最初描述的免疫刺激性cpgodn并且特征性地活化b细胞和nk细胞,但是不会诱导或仅微弱地诱导i型干扰素(例如,ifn-a)的表达。在公布的pct国际申请wo01/22990中描述的a类cpgodn包含cpg基序,包括嵌合的磷酸二酯/硫代磷酸酯主链,并且特征性地活化nk细胞和诱导浆细胞样树突细胞以表达大量ifn-α,但是不活化或仅微弱地活化b细胞。a类cpgodn的一个例子是5'-g*g*gggacgatcgtcg*g*g*g*g*g-3'(odn2216,seqidno:2),其中“*”代表硫代磷酸酯且“”代表磷酸二酯。c类cpgodn包含cpg,包括整个硫代磷酸酯主链,包括富含gc的回文或近回文区域,并且能够活化b细胞和诱导ifn-α的表达。例如,在公布的美国专利申请us2003/0148976中已经描述了c类cpgodn。c类cpgodn的一个例子是5'-tcgtcgttttcggcgcgcgccg-3'(odn2395;seqidno:3)。关于各类cpgodn的综述,也参见vollmer等人(2004),eurjimmunol34:251-62。本文中使用的“细胞因子”表示通过特定受体对免疫细胞起作用以影响免疫细胞的活化状态和功能的许多可溶性蛋白或糖蛋白中的任一种。细胞因子包括干扰素、白介素、肿瘤坏死因子、转化生长因子β、集落刺激因子(csf)、趋化因子等。各种细胞因子影响先天性免疫、获得性免疫或二者。细胞因子具体地包括、但不限于ifn-α、ifn-β、ifn-γ、il-1、il-2、il-3、il-4、il-5、il-6、il-9、il-10、il-12、il-13、il-18、tnf-α、tgf-β、粒细胞集落刺激因子(g-csf)和粒细胞-巨噬细胞集落刺激因子(gm-csf)。趋化因子具体地包括、但不限于il-8、ip-10、i-tac、rantes、mip-lα、mip-1β、gro-α、gro-β、gro-γ、mcp-1、mcp-2和mcp-3。大多数成熟的cd4+t辅助细胞可以分类为细胞因子相关的、交叉调节亚类或表型:thl、th2、th17或treg。th1细胞与il-2、il-3、ifn、gm-csf和高水平的tnf-α相关。th2细胞与il-3、il-4、il-5、il-6、il-9、il-10、il-13、gm-csf和低水平的tnf-α相关。thl亚类在小鼠中促进细胞介导的免疫和特征在于免疫球蛋白类别转变为igg2a的体液免疫。thl应答也可以与迟发型超敏反应和自身免疫疾病相关。th2亚类在小鼠中主要诱导体液免疫并且诱导免疫球蛋白类别转变为ige和igg1。与thl应答相关的抗体同种型通常具有良好的中和和调理能力,而与th2应答相关的抗体同种型更多地与变应性应答相关。已经证实几个因素影响对thl或th2谱的定型。最佳地表征的调节剂是细胞因子。il-12和ifn-γ是阳性的thl和阴性的th2调节剂。il-12促进ifn-γ生成,并且ifn-γ为il-12提供正反馈。为了建立th2细胞因子谱并下调thl细胞因子生成,似乎需要il-4和il-10;il-4的作用在某些情况下比il-12的作用显著。证实了il-13通过lps诱导的单核细胞以类似于il-4的方式抑制炎症性细胞因子(包括il-12和tnf-α)的表达。本文中使用的“有效量”表示达到或促进预期结果所需或足够的任何量。在某些情况下,有效量是治疗有效量。治疗有效量是在受试者中促进或实现期望的生物应答所需或足够的任何量。用于任何特定应用的有效量可以根据诸如以下因素变化:正在治疗的疾病或病症、正在施用的特定药剂、受试者的大小或疾病或病症的严重程度。本领域普通技术人员可以经验地确定特定药剂的有效量,不需要过度实验。本文中使用的“移植物排斥”表示对源自除宿主以外的来源的组织或器官的免疫学上介导的超急性、急性或慢性损伤。所述术语因此包括细胞和抗体介导的排斥,以及同种异体移植物和异种移植物的排斥。本文中使用的术语“免疫细胞”表示属于免疫系统的细胞。免疫细胞包括t淋巴细胞(t细胞)、b淋巴细胞(b细胞)、自然杀伤(nk)细胞、粒细胞、嗜中性粒细胞、巨噬细胞、单核细胞、树突细胞和前述任一种的特化形式,例如浆细胞样树突细胞、浆细胞、nkt、t辅助细胞和细胞毒性t淋巴细胞(ctl)。本文中使用的术语“免疫复合物”表示包括抗体和所述抗体特异性地结合的抗原的任何缀合物。在一个实施方案中,所述抗原是自身抗原。本文中使用的术语“包含核酸的免疫复合物”表示包括抗体和所述抗体特异性地结合的含核酸的抗原的任何缀合物。所述含核酸的抗原可以包括染色质、核糖体、小核蛋白、组蛋白、核小体、dna、rna或它们的任意组合。所述抗体可以但是不一定特异性地结合含核酸的抗原的核酸组分。在某些实施方案中,术语“包含核酸的免疫复合物”还表示非抗体复合物诸如hmgb1、ll-37,及其它核酸结合蛋白诸如组蛋白、转录因子和与核酸形成复合物的酶。本文中使用的术语“免疫复合物相关疾病”表示特征在于免疫复合物生成和/或组织沉积的任何疾病,包括、但不限于系统性红斑狼疮(sle)和有关的结缔组织疾病、类风湿性关节炎、丙型肝炎-和乙型肝炎-相关的免疫复合物疾病(例如,冷球蛋白血症)、beget氏综合征、自身免疫性肾小球性肾炎和与ldl/抗-ldl免疫复合物的存在相关的血管病变。本文中使用的“免疫缺陷”表示这样的疾病或病症:其中受试者的免疫系统不在正常能力范围内起作用,或其中提高受试者的免疫应答会有用,例如以消除受试者中的肿瘤或癌症(例如,脑、肺(例如,小细胞和非小细胞)、卵巢、乳房、前列腺、结肠的肿瘤以及其它癌和肉瘤)或感染。所述免疫缺陷可以是获得性的,或它可以是先天性的。本文中使用的“受试者中免疫刺激性核酸相关的应答”表示受试者中与免疫刺激性核酸向受试者的施用相关的可测量的应答。这样的应答包括、但不限于,细胞因子、趋化因子、生长因子或免疫球蛋白的加工;免疫细胞表面活化标志物的表达;thl/th2偏移;和临床疾病活动性。本文中使用的术语“感染”和等同的“传染性疾病”表示这样的病况:其中传染性生物体或介质以可检测的量存在于受试者的血液或通常无菌的组织或通常无菌的腔室中。传染性生物体或介质包括病毒、细菌、真菌和寄生生物。所述术语包括急性和慢性感染、以及脓毒症。本文中使用的术语“先天性免疫应答”表示对某些病原体相关分子模式(pamp)或危险相关分子模式(damp)的任何类型的免疫应答。先天性免疫(其在本领域中也被称为自然或天然免疫)主要涉及嗜中性粒细胞、粒细胞、单核吞噬细胞、树突细胞、nkt细胞和nk细胞。先天性免疫应答可以包括、但不限于i型干扰素生成(例如,ifn-α)、嗜中性粒细胞活化、巨噬细胞活化、吞噬作用、调理作用、补体激活和它们的任意组合。本文中使用的术语“自身dna”表示源自宿主受试者的基因组的任何dna。在一个实施方案中,自身dna包括源自宿主受试者的互补dna(cdna)。自身dna包括完整的和降解的dna。本文中使用的术语“自身rna”表示源自宿主受试者的基因组的任何rna。在一个实施方案中,自身rna是源自宿主受试者的信使rna(mrna)。在另一实施方案中,自身rna是调节rna,诸如微rna。在一个实施方案中,自身rna包括源自宿主受试者的核糖体rna(rrna)。自身rna包括完整的和降解的rna。本文中使用的术语”受试者”表示脊椎动物。在一个实施方案中,所述受试者是哺乳动物。在一个实施方案中,所述受试者是人。在其它实施方案中,所述受试者是非人脊椎动物,包括、但不限于,非人灵长类动物、实验动物、家畜、赛马、驯化的动物和未驯化的动物。本文中使用的“具有tlr介导的免疫刺激或处于发展tlr介导的免疫刺激的危险中的受试者”表示暴露于pamp、damp或其它tlr配体或处于暴露于pamp、damp或其它tlr配体的危险中的受试者。本文中使用的术语“toll样受体”和等同的“tlr”表示识别pamp、damp并且在先天性免疫中作为关键信号传递元件起作用的至少十三种高度保守的哺乳动物模式识别受体蛋白(tlr1-tlr13)的家族的任何成员。tlr多肽共有特征性结构,其包括具有富亮氨酸重复序列的细胞外(细胞质外)结构域、跨膜结构域和参与tlr信号传递的细胞内(细胞质)结构域。tlr包括、但不限于人tlr。所有十种目前已知的人tlr的核酸和氨基酸序列可从公开数据库诸如genbank得到。类似地,众多非人物种的各种tlr的核酸和氨基酸序列也可从包括genbank在内的公开数据库得到。例如,人tlr9(htlr9)的核酸和氨基酸序列可以分别作为genbank登录号af245704(跨核苷酸145-3243的编码区)和aaf78037被找到。鼠tlr9(mtlr9)的核酸和氨基酸序列可以分别作为genbank登录号af348140(跨核苷酸40-3138的编码区)和aak29625被找到。推导出的人tlr9蛋白含有1,032个氨基酸并且与小鼠tlr9共有75.5%的总氨基酸同一性。象其它tlr蛋白一样,人tlr9含有细胞外富亮氨酸重复序列(lrr)和细胞质toll/白介素-1r(tir)结构域。它还具有信号肽(残基1-25)和跨膜结构域(残基819-836)。人tlr8(htlr8)的核酸和氨基酸序列可以分别作为genbank登录号af245703(跨核苷酸49-3174的编码区)和aaf78036被找到。鼠tlr8(mtlr8)的核酸和氨基酸序列可以分别作为genbank登录号ay035890(跨核苷酸59-3157的编码区)和aak62677被找到。人tlr7(htlr7)的核酸和氨基酸序列可以分别作为genbank登录号af240467(跨核苷酸135-3285的编码区)和aaf60188被找到。鼠tlr7(mtlr7)的核酸和氨基酸序列可以分别作为genbank登录号ay035889(跨核苷酸49-3201的编码区)和aak62676被找到。人tlr3(htlr3)的核酸和氨基酸序列可以分别作为genbank登录号nm003265(跨核苷酸102-2816的编码区)和np003256被找到。鼠tlr3(htlr3)的核酸和氨基酸序列可以分别作为genbank登录号af355152(跨核苷酸44-2761的编码区)和aak26117被找到。尽管htlr1普遍地表达,但是htlr2、htlr4和htlr5存在于单核细胞、多形核吞噬细胞和树突细胞中。muzio等人(2000),jleukocbiol67:450-6。近期的出版物报道,htlr1、htlr6、htlr7、htlr9和htlr10存在于人b细胞中。人tlr7和htlr9存在于浆细胞样树突细胞(pdc)中,而髓样树突细胞表达htlr7和htlr8,但是不表达htlr9。但是,人tlr8似乎在pdc中不表达。与促炎性的白介素-1受体(il-1r)家族的成员一样,tlr在它们的被称为toll/il-lr同源性(tir)结构域的细胞质结构域中共有同源性。参见pct公开申请pct/us98/08979和pct/us01/16766。由tlr介导的细胞内信号传递机制通常似乎是类似的,认为myd88和肿瘤坏死因子受体相关因子6(traf6)具有关键作用。wesche等人(1997),immunity7:837-47;medzhitov等人(1998),molcell2:253-8;adachi等人(1998),immunity9:143-50;kawai等人(1999),immunity11:115-22);cao等人(1996),nature383:443-6;lomaga等人(1999),genesdev13:1015-24。已知myd88和traf6之间的信号传递涉及丝氨酸-苏氨酸激酶il-1受体-相关的激酶(irak)家族的成员,至少包括irak-1和irak-2。muzio等人(1997),science278:1612-5。简而言之,认为myd88作为tlr或il-1r的tir结构域与irak(其至少包括irak-1、irak-2、irak-4和irak-m中的任一种)之间的衔接分子起作用。myd88包括c-端toll同源结构域和n-端死亡结构域。myd88的toll同源结构域结合tlr或il-1r的tir结构域,并且myd88的死亡结构域结合丝氨酸激酶irak的死亡结构域。irak与traf6相互作用,所述traf6作为至少两个途径的入口通道起作用,一个途径导致转录因子nf-kb活化,而另一个导致jun和fos(活化蛋白-1(ap-1)转录因子家族的成员)的活化。nf-kb的活化涉及tak-1(map3激酶(mapk)家族的成员)和ikb激酶的活化。iob激酶使ikb磷酸化,导致其降解和nf-kb向细胞核的易位。认为jun和fos的活化涉及map激酶激酶(mapkk)和map激酶erk、p38和jnk/sapk。nf-kb和ap-1都参与控制许多关键免疫应答基因的转录,所述基因包括各种细胞因子和共刺激分子的基因。参见aderem等人(2000),nature406:782-7;hacker等人(1999),emboj18:6973-82。本文中使用的术语“tlr配体”和等同的“tlr的配体”和“tlr信号传递激动剂”表示,除了根据本文描述的式i的小分子以外,通过除tir结构域以外的tlr结构域与tlr直接地或间接地相互作用并且诱导tlr介导的信号传递的分子。在一个实施方案中,tlr配体为天然配体,即在自然界中发现的tlr配体。在一个实施方案中,tlr配体表示除tlr的天然配体以外的分子,例如通过人类活动制备的分子。在一个实施方案中,所述tlr是tlr9,且所述tlr信号激动剂是cpg核酸。已经描述了许多、但并非全部tlr的配体。例如,已经报道tlr2响应于肽聚糖和脂肽而发信号。yoshimura等人(1999),jimmunol163:1-5;brightbill等人(1999),science285:732-6;aliprantis等人(1999),science285:736-9;takeuchi等人(1999),immunity11:443-51;underhill等人(1999),nature401:811-5。已经报道tlr4响应于脂多糖(lps)而发信号。参见hoshino等人(1999),immunol.162:3749-52;poltorak等人(1998),science282:2085-8;medzhitov等人(1997),nature388:394-7。已经报道细菌鞭毛蛋白是tlr5的天然配体。参见hayashi等人(2001),nature410:1099-1103。已经报道tlr6连同tlr2一起响应于蛋白聚糖而发信号。参见ozinsky等人(2000),procnatlacadsciusa97:13766-71;takeuchi等人(2001),intimmunol13:933-40。最近,据报道tlr9是cpgdna的受体。hemmih等人(2000)nature408:740-5;bauers等人(2001)procnatlacadsciusa98:9237-42。本文在别处更详细地描述了cpgdna,其包括具有cg二核苷酸(其中胞嘧啶未被甲基化)的细菌dna和合成dna。marshak-rothstein和同事最近也报道了他们的发现:tlr9信号传递可以响应于含有igg和染色质的免疫复合物而出现在某些自身免疫疾病中。leadbetterea等人(2002)nature416:595-8。因此,在更宽的意义上,当核酸在合适环境下呈现例如作为免疫复合物的组成部分时,似乎tlr9可以响应于自身或非自身核酸(dna或rna)而发信号。最近,据报道某些具有抗病毒活性的咪唑并喹啉化合物是tlr7和tlr8的配体。hemmih等人(2002)natimmunol3:196-200;jurkm等人(2002)natimmunol3:499。咪唑并喹啉是具有抗病毒和抗肿瘤性质的免疫细胞的有效合成活化剂。使用来自野生型和myd88-缺陷型小鼠的巨噬细胞,hemmi等人最近报道称,两种咪唑并喹啉,咪喹莫特和瑞喹莫德(r848),诱导肿瘤坏死因子(tnf)和白介素-12(il-12)并且仅在野生型细胞中活化nf-kb,这与通过tlr实现的活化一致。hemmih等人(2002)natimmunol3:196-200。来自缺乏tlr7而非其它tlr的小鼠的巨噬细胞未响应于这些咪唑并喹啉而产生可检测的细胞因子。另外,咪唑并喹啉诱导脾脏b细胞的剂量依赖性增殖和来自野生型而非tlr7-/-小鼠的细胞中细胞内信号传递级联的活化。荧光素酶分析确定,在人胚胎肾细胞中人tlr7、而非tlr2或tlr4的表达导致响应于瑞喹莫德的nf-kb活化。因此hemmi等人的发现提示,这些咪唑并喹啉化合物是可以通过tlr7诱导信号传递的tlr7的非天然配体。最近,据报道r848也是人tlr8的配体。参见jurkm等人(2002)natimmunol3:499.natimmunol3:499。还已经报道,ssrna是天然配体并且在自身免疫中涉及rna:复合物对tlr7和/或tlr8的异常刺激。最近据报道,tlr3的配体包括聚(i:c)和双链rna(dsrna)。为了本发明的目的,将聚(i:c)和双链rna(dsrna)分类为寡核苷酸分子。通过刺激表达一系列具有聚(i:c)的tlr中的一种的肾细胞,alexopoulou等人报道,仅表达tlr3的细胞通过活化nf-ab而作出应答。参见alexopouloul等人(2001)nature413:732-8。alexopoulou等人还报道,用聚(i:c)刺激过的野生型细胞会活化nf-kb并产生炎症性细胞因子il-6、il-12和tnf-α,而tlr3-/-细胞的相应应答明显受损。相反,tlr3-/-细胞与野生型细胞等同地响应于脂多糖、肽聚糖和cpg二核苷酸作出应答。myd88-/-细胞的分析指示,尽管nf-kb和map激酶的活化未受影响,但是这种衔接蛋白参与dsrna诱导的细胞因子生成和增殖应答,表明这些细胞应答的不同途径。alexopoulou等人提出,tlr3可能在针对病毒的宿主防御中起作用。本文中使用的“表达tlr的细胞”表示天然地或人工地表达功能性tlr的任何细胞。功能性tlr是能够响应于与其配体的相互作用而诱导信号的全长tlr蛋白或其片段。通常,功能性tlr将包括全长tlr的细胞外结构域的至少一个tlr配体结合片段和能够与另一个含toll同源结构域的多肽(例如,myd88)相互作用的tir结构域的至少一个片段。在不同的实施方案中,所述功能性tlr是选自tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9和tlr10的全长tlr。化合物描述了新颖的蝶啶化合物。申请人已经令人惊讶地发现了新颖的作为免疫系统调节剂的n2,n4,n7,6-四取代的蝶啶-2,4,7-三胺和2,4,6,7-四取代的蝶啶。意外的是,如本文中公开的蝶啶化合物在用于体外和体内抑制免疫应答的方法中是有用的,所述方法包括用于治疗免疫复合物相关疾病和自身免疫病症的方法。在另一个方面,本发明提供了新颖的蝶啶组合物。如下面进一步所述,已经发现这些组合物和其它蝶啶组合物在用于体外和体内抑制免疫应答的方法中是有用的,所述方法包括用于治疗免疫复合物相关疾病和自身免疫病症的方法。还认为,如本文中所述的新颖的蝶啶组合物可以用于预防和治疗疟疾、以及用于治疗其它疾病。在一个方面,描述了式i的化合物或其药学上可接受的盐,其中每次出现的d独立地是-o-或-n(me)-;且r5是h、f或cl。在某些实施方案中,所述化合物具有选自以下的结构:在其它实施方案中,所述化合物具有选自以下的结构:在某些具体实施方案中,所述化合物具有结构(6-氯-2-(4-甲基哌嗪-1-基)-n4,n7-双(2-吗啉代乙基)蝶啶-4,7-二胺;“jb6121”)。在某些具体实施方案中,所述化合物具有结构(6-氯-2-(4-甲基哌嗪-1-基)-n7-(2-(4-甲基哌嗪-1-基)乙基)-n4-(2-吗啉代乙基)蝶啶-4,7-二胺)。对于要视作适当药物候选物的小分子化合物,所述化合物的均衡的总药理学特性是合乎需要的。例如,除了针对疾病靶标的有效体外和体内活性以外,所述药物候选物需要表现出可接受的安全性,例如,低毒性和良好的生物利用度。申请人已经令人惊讶地和意外地发现,具有式(i)的结构的化合物(例如,jb6121)表现出合乎需要的总pk/pd特性,包括在体外和在体内针对tlr的有效拮抗剂活性、在体内低或无毒性、合乎需要的细胞吸收、合乎需要的体内稳定性和/或在体内施用化合物以后合乎需要的生物利用度和全身暴露。例如,申请人意外地发现,6-氯-2-(4-甲基哌嗪-1-基)-n4,n7-双(2-吗啉代乙基)蝶啶-4,7-二胺表现出合乎需要的体内和体外tlr拮抗剂活性、可接受的体内生物利用度(>20%)、在大鼠中在ames试验中无毒性、低心血管毒性、低药物-药物相互作用活性和低受体交叉活性。更具体地,已经意外地发现,具有式(i)的结构的化合物(例如,jb6121)具有低心血管毒性或基本上没有心血管毒性。许多药物由于这些心脏毒性效应已经从晚期临床试验中撤出,因此重要的是,在药物发现的早期鉴别和避免具有心脏毒性效应的化合物。使用标准的人类果蝇相关基因(herg)测定,可以测量化合物的心血管毒性。人类果蝇相关基因(herg)在心脏中编码向内整流电压门控性钾通道(ikr),后者参与心脏复极化。herg电流的抑制会造成qt间期延长,从而导致可能致命的室性快速型心律失常(被称作尖端扭转型室性心动过速)。在herg测定中具有超过10μm的ic50的化合物可以被视作不具有任何心血管毒性。在某些实施方案中,式(i)的化合物在标准的膜片箝herg测定中具有超过10、15、20、25或30μm的ic50。例如,在30μm或超过30μm的6-氯-2-(4-甲基哌嗪-1-基)-n4,n7-双(2-吗啉代乙基)蝶啶-4,7-二胺没有表现出可测量的herg抑制。与此相比,jb6059、jb6116和jb6131在herg测定中分别表现出等于6.2μm、13.1μm和8.1μm的ic50。jb6059、jb6116和jb6131是与式(i)的化合物密切相关的类似物,但是没有落入式(i)的种类内(参见下面方案1)。式(i)的化合物的这种心血管毒性缺乏是惊人的和意外的,特别考虑到密切相关的类似物jb6059、jb6116和jb6131都具有某种程度的心血管毒性。另外,已经意外地发现,具有式(i)的结构的化合物(例如,jb6121)具有低肝细胞毒性或基本上没有肝细胞毒性。可以将肝细胞毒性测量为肝细胞暴露于所述化合物以后肝细胞生存力的百分比。在某些实施方案中,在将肝细胞暴露于100μm的化合物24h以后,式(i)的化合物(例如,jb6121)导致超过75%、80%、85%、90%、95%、97%、98%或99%的肝细胞生存力,或导致在以本文中公开的任意2个值为边界的范围内的肝细胞生存力。在另一个方面,描述了式ia的化合物或其药学上可接受的盐,其中r1是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环或烷基杂环;x1和x2各自独立地不存在或者是o;r2是卤素、ora、sra、os(=o)2ra、oc(=o)ra、nrbrc或nra(ch2)pnrbrc,其中p是2-4;r3和r4各自是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc;每次出现的ra独立地是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;且每次出现的rb和rc独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环、芳基;或所述rb和rc与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;或所述ra和rb与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;其中形成的杂环任选地被(c1-c4)烷基取代,且形成的杂环中的一个或多个碳原子任选地被o、nr8或s替换,其中r8是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;前提条件是,当r2是ora、sra、nrbrc或nra(ch2)pnrbrc时,x1和x2中的至少一个是o。在某些实施方案中,r1是烷基、任选地被取代的芳基或任选地被取代的杂芳基。在本文描述的任一个实施方案中,x1和x2可以都是o。在某些实施方案中,r1是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环或烷基杂环。烷基的非限制性例子包括me、et、pr、i-pr、n-bu、i-bu、t-bu或sec-bu。在某些实施方案中,x1和x2各自独立地不存在或者是o,前提条件是,当r2是ora、sra、nrbrc或nra(ch2)pnrbrc时,x1和x2中的至少一个是o。在某些实施方案中,r2选自卤素、ora、sra、os(=o)2ra、oc(=o)ra、nrbrc和nra(ch2)pnrbrc,其中p是2-4。在某些实施方案中,r3和r4各自选自氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环和nra(ch2)pnrbrc。在本文描述的任一个实施方案中,r2可以选自卤素、os(=o)2ra、oc(=o)ra、nrbrc和nra(ch2)pnrbrc。在某些实施方案中,r2是cl或br。在某些实施方案中,r2是os(=o)2ra或oc(=o)ra。在某些实施方案中,r2是nrbrc或nra(ch2)pnrbrc。在本文描述的任一个实施方案中,r4可以是nrbrc或nra(ch2)pnrbrc。r2和r4可以是相同的或不同的。在某些实施方案中,r2和r4各自独立地选自:在另一个方面,描述了一种化合物,其选自:在另一个方面,本发明提供了如表1中所述的选自实施例1至74的式(ia)的化合物。在表1中列举的化合物是本发明的代表性的和非限制性的蝶啶化合物。表1.选择的式(ia)的化合物,其中x1和x2各自独立地是o或不存在.在pct公开号wo2012/167046所公开的不同方面和实施方案中描述了另外的蝶啶类似物,其内容明确地通过引用并入。在另一个方面,本发明提供了一种药物组合物,其包含至少一种如本文中所述的式i和ia的化合物和药学上可接受的载体或稀释剂。在另一个方面,本发明提供了一种用于治疗有此需要的哺乳动物物种中的自身免疫疾病的方法,所述方法包括给所述哺乳动物物种施用治疗有效量的至少一种式i的化合物,其中每次出现的d独立地是-o-或-n(me)-;且r5是h、f或cl。在某些具体实施方案中,所述化合物具有结构在另一个方面,本发明提供了一种用于治疗有此需要的哺乳动物物种中的自身免疫疾病的方法,所述方法包括给所述哺乳动物物种施用治疗有效量的至少一种式ia的化合物,其中r1是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环或烷基杂环;x1和x2各自独立地不存在或者是o;r2是卤素、ora、sra、os(=o)2ra、oc(=o)ra、nrbrc或nra(ch2)pnrbrc,其中p是2-4;r3和r4各自是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc;每次出现的ra独立地是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;且每次出现的rb和rc独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环、芳基;或所述rb和rc与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;或所述ra和rb与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;其中形成的杂环任选地被(c1-c4)烷基取代,且形成的杂环中的一个或多个碳原子任选地被o、nr8或s替换,其中r8是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;前提条件是,当r2是ora、sra、nrbrc或nra(ch2)pnrbrc时,x1和x2中的至少一个是o。在某些实施方案中,所述蝶啶组合物呈水合物或药学上可接受的盐的形式。所述蝶啶组合物可以通过任意合适的施用途径施用给受试者,所述施用途径包括、但不限于口服和胃肠外。胃肠外施用途径如上面关于被取代的4-伯氨基蝶啶所述。在某些实施方案中,所述自身免疫疾病选自皮肤和系统性红斑狼疮、胰岛素依赖性的糖尿病、类风湿性关节炎、多发性硬化、动脉粥样硬化、银屑病、银屑病关节炎、炎性肠病、强直性脊柱炎、自身免疫性溶血性贫血、behget氏综合征、古德帕斯彻氏综合征、格雷夫斯病、格-巴二氏综合征、桥本甲状腺炎、特发性血小板减少症、io重症肌无力、恶性贫血、结节性多动脉炎、多肌炎/皮肌炎、原发性胆道硬化、结节病、硬化性胆管炎、舍格伦综合征、系统性硬化症(硬皮病和肢端硬皮综合征)、高安动脉炎、颞动脉炎和韦格纳氏肉芽肿病。在某些实施方案中,所述自身免疫疾病选自系统性红斑狼疮、类风湿性关节炎、银屑病、炎性肠病、舍格伦综合征、多肌炎、血管炎、韦格纳氏肉芽肿病、结节病、强直性脊柱炎、莱特尔综合症、银屑病关节炎和behyet氏综合征。在一个特定实施方案中,所述自身免疫疾病是系统性红斑狼疮。在另一个特定实施方案中,所述自身免疫疾病是类风湿性关节炎。在一个特定实施方案中,所述自身免疫疾病是银屑病。在另一个特定实施方案中,所述自身免疫疾病是舍格伦综合征。在一个实施方案中,所述受试者是人。在一个实施方案中,所述自身免疫病症是如上所述的免疫复合物相关疾病。在另一个方面,本发明提供了一种在有此需要的哺乳动物物种中抑制tlr介导的免疫刺激的方法,所述方法包括给所述哺乳动物物种施用治疗有效量的至少一种式i的化合物,其中每次出现的d独立地是-o-或-n(me)-;且r5是h、f或cl。在某些具体实施方案中,所述化合物具有结构在另一个方面,本发明提供了一种在有此需要的哺乳动物物种中抑制tlr介导的免疫刺激的方法,所述方法包括给所述哺乳动物物种施用治疗有效量的至少一种式ia的化合物,其中r1是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环或烷基杂环;x1和x2各自独立地不存在或者是o;r2是卤素、ora、sra、os(=o)2ra、oc(=o)ra、nrbrc或nra(ch2)pnrbrc,其中p是2-4;r3和r4各自是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc;每次出现的ra独立地是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;且每次出现的rb和rc独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环、芳基;或所述rb和rc与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;或所述ra和rb与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;其中形成的杂环任选地被(c1-c4)烷基取代,且形成的杂环中的一个或多个碳原子任选地被o、nr8或s替换,其中r8是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;前提条件是,当r2是ora、sra、nrbrc或nra(ch2)pnrbrc时,x1和x2中的至少一个是o。在某些实施方案中,所述影响受试者中tlr介导的免疫刺激的方法包括,给具有tlr介导的免疫刺激或处于发生tlr介导的免疫刺激的风险中的受试者施用有效量的如本文中提供的式i-ia的化合物,以抑制受试者中tlr介导的免疫刺激。在另一个方面,本发明提供了一种抑制tlr介导的免疫刺激性信号传递的方法,所述方法包括使表达tlr的细胞与有效量的至少一种式i的化合物接触,其中每次出现的d独立地是-o-或-n(me)-;且r5是h、f或cl。在某些具体实施方案中,所述化合物具有结构在另一个方面,本发明提供了一种抑制tlr介导的免疫刺激性信号传递的方法,所述方法包括使表达tlr的细胞与有效量的至少一种式ia的化合物接触,其中r1是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环或烷基杂环;x1和x2各自独立地不存在或者是o;r2是卤素、ora、sra、os(=o)2ra、oc(=o)ra、nrbrc或nra(ch2)pnrbrc,其中p是2-4;r3和r4各自是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc;每次出现的ra独立地是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;且每次出现的rb和rc独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环、芳基;或所述rb和rc与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;或所述ra和rb与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;其中形成的杂环任选地被(c1-c4)烷基取代,且形成的杂环中的一个或多个碳原子任选地被o、nr8或s替换,其中r8是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;前提条件是,当r2是ora、sra、nrbrc或nra(ch2)pnrbrc时,x1和x2中的至少一个是o。在某些实施方案中,所述抑制tlr介导的免疫刺激性信号传递的方法包括,使表达tlr的细胞与有效量的如上提供的式i-ia的化合物接触,以抑制响应于tlr配体的tlr介导的免疫刺激性信号传递。在某些实施方案中,所述抑制tlr介导的免疫刺激性信号传递的方法包括,使表达功能性tlr的免疫细胞与以下物质接触:(a)有效量的tlr信号激动剂,以刺激在没有蝶啶组合物存在下由tlr实现的信号传递,和(b)有效量的如本文中所述的具有结构式i或ia的蝶啶组合物,以与在没有蝶啶组合物存在下响应于tlr信号激动剂由tlr实现的信号传递相比,抑制响应于tlr信号激动剂由tlr实现的信号传递。在某些具体实施方案中,用于抑制tlr介导的免疫刺激性信号传递的蝶啶组合物具有式i的结构。在某些具体实施方案中,所述蝶啶组合物呈水合物或药学上可接受的盐的形式。在某些具体实施方案中,在体外或在体内执行用于抑制tlr介导的免疫刺激性信号传递的方法。在某些实施方案中,所述tlr是tlr9,且所述tlr信号激动剂是tlr9信号激动剂。在这些实施方案中,所述方法是抑制响应于tlr9信号激动剂由tlr9实现的细胞内信号传递的方法。在一个实施方案中,所述tlr信号激动剂是cpgdna,其可以是寡脱氧核苷酸(odn)。在某些实施方案中,cpgodn是odn2006。在其它实施方案中,cpgodn属于任一类cpgodn,包括a类(例如,odn2216)、b类(例如,odn2006)或c类(例如,odn2395)。在某些实施方案中,所述tlr信号激动剂是包括核酸的免疫复合物。在某些实施方案中,如本文中所述的方法可用于改变tlr介导的信号传递。所述方法用于改变响应于合适的tlr配体或tlr信号传递激动剂的tlr介导的信号传递。例如,所述方法可以用于治疗涉及自身免疫、炎症、变态反应、哮喘、移植物排斥、移植物抗宿主病(gvhd)、感染、脓毒症、癌症和免疫缺陷的任意病症种类。通常,在涉及自身免疫、炎症、变态反应、哮喘、移植物排斥和gvhd的病况的治疗中有用的方法将采用小分子,其抑制响应于合适的tlr配体或tlr信号传递激动剂的tlr介导的信号传递。通常,在涉及感染、癌症和免疫缺陷的病况的治疗中有用的方法将采用小分子,其增强响应于合适的tlr配体的tlr介导的信号传递。在某些实施方案中,所述方法用于抑制或促进响应于tlr配体或tlr信号传递激动剂的tlr介导的信号传递。在某些实施方案中,所述方法用于抑制响应于tlr配体或tlr信号传递激动剂的tlr介导的免疫刺激性信号传递。在某些实施方案中,所述方法用于抑制或促进受试者中的tlr介导的免疫刺激。在某些实施方案中,所述方法用于抑制受试者中的tlr介导的免疫刺激。在某些实施方案中,所述方法用于抑制受试者中的免疫刺激性核酸相关的应答。在某些实施方案中,可用于改变tlr介导的信号传递的方法使用式i和ia的化合物的小分子组合物。本发明的组合物用于改变响应于合适的tlr配体或tlr信号传递激动剂的tlr介导的信号传递。例如,所述小分子可以用在治疗涉及自身免疫、炎症、变态反应、哮喘、移植物排斥、gvhd、感染、脓毒症、癌症和免疫缺陷的多种病况中的任一种的方法中。通常,在涉及自身免疫、炎症、变态反应、哮喘、移植物排斥和gvhd的病况的治疗中有用的方法将采用小分子,其抑制响应于合适的tlr配体或tlr信号传递激动剂的tlr介导的信号传递。通常,在涉及感染、癌症和免疫缺陷的病况的治疗中有用的方法将采用小分子,其增强响应于合适的tlr配体的tlr介导的信号传递。在某些情况下,所述分子可以用在抑制或促进响应于tlr配体或tlr信号传递激动剂的tlr介导的信号传递的方法中。在某些情况下,所述小分子可以用在抑制响应于tlr配体或tlr信号传递激动剂的tlr介导的免疫刺激性信号传递的方法中。在某些实施方案中,所述小分子用在抑制或促进受试者中tlr介导的免疫刺激的方法中。在某些实施方案中,所述小分子用在抑制受试者中tlr介导的免疫刺激的方法中。在某些实施方案中,所述小分子用于抑制受试者中的免疫刺激性核酸相关的应答。此外,如本文中所述的方法可以与额外试剂的施用相组合以实现对tlr介导的免疫刺激的协同效应。更具体地,鉴于已经发现本文描述的试剂直接影响tlr并且因而直接影响携带tlr的细胞,例如抗原呈递细胞(apc),可以将这样的试剂与影响非apc免疫细胞(例如t淋巴细胞(t细胞))的额外试剂一起使用。这样的方案有效地引入在两个水平的免疫调节干预:先天性免疫和获得性免疫。因为先天性免疫被认为会引发和支持获得性免疫,所以所述联合干预是协同性的。在另一个方面,提供了一种抑制受试者中免疫刺激性核酸相关的应答的方法。所述方法包括给需要这种治疗的受试者施用有效量的如上面提供的式i和ia的化合物,以抑制所述受试者中的免疫刺激性核酸相关的应答。在某些实施方案中,用如本文中所述的蝶啶化合物治疗的受试者具有指示免疫系统疾病的征状。在其它实施方案中,用如本文中所述的蝶啶化合物治疗的受试者不具有指示免疫系统疾病的任何征状。在某些实施方案中,所述tlr是tlr9。在某些具体实施方案中,所述tlr的配体是免疫刺激性核酸。在其它具体实施方案中,所述免疫刺激性核酸是cpg核酸。在其它具体实施方案中,所述免疫刺激性核酸是含有dna的免疫复合物。在某些实施方案中,所述tlr是tlr8。在某些具体实施方案中,所述tlr的配体是tlr8的天然配体。在其它具体实施方案中,所述tlr的配体是rna。在其它具体实施方案中,所述tlr的配体是免疫刺激性核酸。在其它具体实施方案中,所述免疫刺激性核酸是含有rna的免疫复合物。在其它具体实施方案中,所述tlr的配体是免疫刺激性的咪唑并喹啉。在其它具体实施方案中,所述tlr的配体是瑞喹莫德(r848)。在某些实施方案中,所述tlr是tlr7。在某些具体实施方案中,所述tlr的配体是tlr7的天然配体。在其它具体实施方案中,所述tlr的配体是免疫刺激性核酸。在一个实施方案中,所述tlr的配体是rna。在其它具体实施方案中,所述免疫刺激性核酸是含有rna的免疫复合物。在其它具体实施方案中,所述tlr的配体是免疫刺激性的咪唑并喹啉。在其它具体实施方案中,所述tlr的配体是r848。在某些实施方案中,所述tlr是tlr3。在某些具体实施方案中,所述tlr的配体是双链rna。在其它具体实施方案中,所述tlr的配体是如本文中所述的免疫复合物。在其它具体实施方案中,所述tlr的配体是聚(i:c)。在其它具体实施方案中,所述tlr是tlr9,且所述tlr信号激动剂是tlr9信号激动剂。在其它具体实施方案中,所述tlr信号激动剂是cpgdna,其可以是寡脱氧核苷酸(odn)。在某些实施方案中,所述tlr信号激动剂是包含核酸的免疫复合物。在另一个方面,提供了一种用于抑制对抗原物质的免疫应答的方法。所述方法包括使表达功能性toll样受体的免疫细胞与以下物质接触:(a)有效量的抗原物质,以刺激在没有蝶啶组合物存在下对所述抗原物质的免疫应答,和(b)有效量的如上定义的具有结构式i和ia的蝶啶组合物,以与在没有蝶啶组合物存在下对所述抗原物质的免疫应答相比,抑制对所述抗原物质的免疫应答。在某些实施方案中,所述免疫应答是先天性免疫应答。在其它实施方案中,所述免疫应答包括适应性免疫应答。在某些具体实施方案中,所述蝶啶组合物呈水合物或药学上可接受的盐的形式。在某些具体实施方案中,在体外或在体内执行用于抑制对抗原物质的免疫应答的方法。在某些实施方案中,所述抗原物质是变应原。在其它实施方案中,所述抗原物质是抗原,所述抗原是或源自微生物介质,包括细菌、病毒、真菌或寄生生物。在其它实施方案中,所述抗原物质是癌抗原。在某些实施方案中,所述功能性tlr由细胞天然地表达。表达tlr的细胞的非限制性例子包括rpmi8226细胞系。在一个实施方案中,所述细胞天然地表达功能性tlr并且是来自人多发性骨髓瘤细胞系rpmi8226(atccccl-155;美国典型培养物保藏中心(atcc),manassas,va)的分离细胞。在诊断多发性骨髓瘤(iggλ型)时,从61岁男性的外周血建立该细胞系。matsuokay等人(1967)procsocexpbiolmed125:1246-50。如il-6蛋白和il-12p40mrna的诱导所证明,先前报道rpmi8226对cpg核酸有应答。takeshitaf等人(2000)eurjimmunol30:108-16;takeshitaf等人(2000)eurjimmunol30:1967-76。takeshita等人仅使用所述细胞系研究了启动子构建体,以便鉴别对cpg核酸信号传递重要的转录因子结合位点。现在已知,rpmi8226细胞响应于免疫刺激性核酸而分泌许多其它趋化因子和细胞因子,包括il-8、il-10和ip-10。因为该细胞系表达tlr9,免疫刺激性核酸(例如cpg核酸)通过所述tlr9来介导其效应,所以它是用在本发明的涉及作为参考和试验化合物的cpg核酸以及其它tlr9配体的方法中的合适细胞系。与外周血单核细胞(pbmc)类似,已经观察到rpmi8226细胞系响应于cpg核酸暴露而上调其标志物(诸如cd71、cd86和hla-dr)的细胞表面表达。这已经通过细胞系的流式细胞计数分析观察到。因此,可以将本文提供的方法构造为使用适当地选择的细胞表面标志物表达作为读出,用于补充或代替趋化因子或细胞因子生成或本文别处描述的其它读出。还已发现rpmi8226细胞系对某些小分子(包括咪唑并喹啉化合物)有应答。例如,将rpmi8226细胞与咪唑并喹啉化合物r848(瑞喹莫德)一起孵育会诱导il-8、il-10和ip-10生成。最近已经报道,r848通过tlr7和tlr8介导其免疫刺激效应。rpmi8226对r848做出应答的能力提示,与先前关于正常人b细胞报道的一样,rpmi8226细胞系也表达tlr7。rpmi细胞系可以以未修饰形式或经修饰形式使用。在一个实施方案中,用报告构建体转染rpmi8226细胞。优选地,用报告构建体稳定地转染细胞。所述报告构建体通常包括启动子、编码序列和多腺苷酸化信号。所述编码序列可以包括报告序列,其选自酶(例如,萤光素酶、碱性磷酸酶、β-半乳糖苷酶、氯霉素乙酰基转移酶(cat)、分泌型碱性磷酸酶等)、生物发光标志物(例如,绿色荧光蛋白(gfp,美国专利号5,491,084)等)、表面表达的分子(例如,cd25)、分泌分子(例如,il-8、il-12p40、tnf-α等)和本领域技术人员已知的其它可检测的蛋白产物。优选地,所述编码序列编码具有可计量的水平或活性的蛋白。在某些实施方案中,所述功能性tlr由细胞人工地表达(包括过表达),例如通过向细胞中引入带有功能性tlr的编码序列的表达载体,其中所述编码序列与基因表达序列可操作地连接。如本文中使用的,编码序列和基因表达序列在以下情况下说成可操作地连接:它们以使编码序列的表达或转录和/或翻译置于基因表达序列的影响或控制下的方式共价地连接。在以下情况下说两个dna序列是可操作地连接的:5'基因表达序列中的启动子的诱导导致编码序列的转录,并且所述两个dna序列之间的连接的性质不会(1)导致移码突变的引入,(2)干扰启动子区域的指导编码序列转录的能力,或(3)干扰对应的rna转录物翻译成蛋白的能力。因此,如果基因表达序列能够实现编码序列的转录,使得得到的转录物翻译成期望的蛋白或多肽,则基因表达序列将与编码序列可操作地连接。在某些实施方案中,编码序列表示编码功能性tlr的核酸序列。在某些实施方案中,编码序列表示编码报告物的核酸序列。人工地表达功能性tlr的细胞可以是如果没有tlr表达载体就不表达功能性tlr的细胞。例如,人293成纤维细胞(atcccrl-1573)不表达tlr3、tlr7、tlr8或tlr9。如在以下实施例中所述,这样的细胞可以用合适的表达载体(或多种载体)瞬时地或稳定地转染,从而产生确实表达tlr3、tlr7、tlr8、tlr9或它们的任意组合的细胞。可替换地,人工地表达功能性tlr的细胞可以是这样的细胞:与在没有tlr表达载体存在下的表达水平相比,所述细胞在有tlr表达载体存在下以显著更高的水平表达功能性tlr。为了用在本发明的方法中,人工地表达功能性tlr的细胞优选地是表达功能性tlr的稳定地转染的细胞。也可以用合适的报告构建体稳定地转染这样的细胞。关于有效性的测定使用基于tlr/il-1r信号转导途径的许多可能读出系统中的任一种,可以评估本发明的方法。在某些实施方案中,所述方法的读出是基于天然基因的使用,或者可替换地,基于转染的或以其它方式人工引入的报道基因构建体,所述报道基因构建体对涉及myd88、traf、p38和/或erk的tlr/il-1r信号转导途径有应答。h等人(1999)emboj18:6973-82。这些途径会活化激酶,包括κb激酶复合物和c-junn-端激酶。因而,对于所述测定而言特别有用的报道基因和报道基因构建体包括:例如,与对nf-κb敏感的启动子可操作地连接的报道基因。这样的启动子的例子包括、但不限于,nf-κb、il-1β、il-6、il-8、il-12p40、ip-10、cd80、cd86和tnf-α的启动子。与tlr-敏感型启动子可操作地连接的报道基因可以包括,但不限于,酶(例如,萤光素酶、碱性磷酸酶、β-半乳糖苷酶、氯霉素乙酰基转移酶(cat)等)、生物发光标志物(例如,绿色荧光蛋白(gfp,例如,美国专利号5,491,084)、蓝色荧光蛋白(bfp,例如,美国专利号6,486,382)等)、表面表达的分子(例如,cd25、cd80、cd86)或分泌的分子(例如,il-1、il-6、il-8、il-12p40、tnf-α)。在某些实施方案中,所述报道物选自il-8、tnf-α、nf-κb-萤光素酶(nf-κb-luc;h等人(1999)emboj18:6973-82)、il-12p40-luc(murphytl等人(1995)molcellbiol15:5258-67)和tnf-luc(h等人(1999)emboj18:6973-82)。在依赖于酶活性读出的测定中,底物可以作为测定的一部分来提供,并且检测可以涉及化学发光、荧光、彩色显影、放射性标记掺入、药物抗性或酶活性的另一种标志物的测量。对于依赖于分子的表面表达的测定,使用流式细胞计量术(例如,facs)分析或功能测定可以完成检测。使用酶联免疫吸附测定(elisa)或生物测定,可以测定分泌的分子。这些和其它适当的读出系统中的许多是本领域众所周知的并且是商购可得的。报告构建体在某些实施方案中,表达功能性tlr并且对本发明的方法有用的细胞具有包括分离的核酸的表达载体,所述分离的核酸编码可用于检测tlr信号传递的报告构建体。所述表达载体(其包括编码可用于检测tlr信号传递的报告构建体的分离的核酸)可以包括在启动子应答元件(增强子元件)控制下的报道基因。在某些实施方案中,所述启动子应答元件与对由于tlr信号传递而被活化的转录因子有应答的最小启动子相关。这样的最小启动子的例子包括、但不限于下述基因的启动子:ap-1、nf-κb、atf2、irf3和irf7。这些最小启动子含有分别对ap-1、nf-κb、atf2、irf3和irf7敏感的相应启动子应答元件。在其它实施方案中,所述表达载体(包括编码可用于检测tlr信号传递的报告构建体的分离的核酸)可以包括在启动子应答元件控制下的基因,所述启动子应答元件选自对il-6、il-8、il-12p40亚基、i型ifn、rantes、tnf、ip-10、i-tac敏感的应答元件和干扰素刺激的应答元件(isre)。所述启动子应答元件通常以多个拷贝存在,例如作为串联重复。例如,在一种报告构建体中,荧光素酶的编码序列是在nf-κb应答元件的上游6x串联重复的控制下。在某些实施方案中,在本发明中有用的isre-萤光素酶报告构建体(例如,目录号219092,stratagene,inc.,lajolla,ca)包括与萤光素酶报道基因的上游tata盒连接的5xisre串联重复。如本文中所述的,报道基因本身可以是适合通过本领域公认的方法检测的任何基因产物。这样的检测方法可以包括,例如,自发的或刺激的发光、酶活性、可溶性分子的表达和细胞表面分子的表达等的测量。读出通常涉及toll/il-1r信号传递的普通元件,例如,myd88、traf和irak分子,尽管在tlr3的情况下,myd88的作用不如对于其它tlr家族成员清楚。如本文中所述的,这样的应答包括在特定启动子(诸如nf-κb启动子)控制下的基因的诱导,特定细胞因子水平的增加,特定趋化因子水平的增加等。在nf-κb启动子控制下的基因可以是天然地包括nf-κb启动子的基因,或它可以是其中已经插入nf-κb启动子的构建体中的基因。包括nf-κb启动子的基因和构建体包括、但不限于il-8、il-12p40、nf-κb-luc、il-12p40-luc和tnf-luc。细胞因子水平的增加可以源自响应于tlr介导的信号传递的细胞因子的生成增多、稳定性增加、分泌增多或前述任意组合。细胞因子通常包括、但不限于il-1、il-2、il-3、il-4、il-5、il-6、il-7、il-10、il-11、il-12、il-13、il-15、il-18、ifn-α、ifn-β、ifn-γ、tnf-α、gm-csf、g-csf、m-csf。th1细胞因子包括、但不限于il-2、ifn-γ和il-12。th2细胞因子包括、但不限于il-4、il-5和il-10。趋化因子水平的增加可以源自响应于tlr介导的信号传递的趋化因子的生成增多、稳定性增加、分泌增多或前述任意组合。在本发明中特别重要的趋化因子包括、但不限于ccl5(rantes)、cxcl9(mig)、cxcl10(ip-10)和cxcl11(i-tac)、il-8和mcp-1。缩写acn乙腈ea乙酸乙酯dmf二甲基甲酰胺pe石油醚dcm二氯甲烷thf四氢呋喃hobt1-羟基苯并三唑edci1-乙基-3-(3-二甲基氨基丙基)碳二亚胺hbtu2-(1h-苯并三唑-1-基)-1,1,3,3-四甲基脲鎓六氟磷酸盐hatun-[(二甲基氨基)(3h-1,2,3-三唑lo(4,4-b)吡啶-3-基氧基)亚甲基]-n-甲基甲烷铵(aminium)六氟磷酸盐pybop1h-苯并三唑-1-基氧基三吡咯烷子基(pyrrolidino)鏻六氟磷酸盐bopcl双(2-氧代-3-噁唑烷基)膦(phosphinic)氯化物bop苯并三唑-1-基氧基三(二乙基氨基)鏻六氟磷酸盐tea三乙胺dipea二异丙基乙胺dmap4-二甲基氨基吡啶pcc吡啶鎓氯铬酸盐pdc吡啶鎓重铬酸盐nbsn-溴琥珀酰亚胺ncsn-氯琥珀酰亚胺nisn-碘琥珀酰亚胺9-bbn9-硼杂二环[3.3.1]壬烷tsoh对甲苯磺酸tfa三氟乙酰胺cdi羰基二咪唑制备方法下面是制备本发明的化合物的一般合成方案。这些方案是示例性的,且无意限制本领域技术人员可以用于制备本文中公开的化合物的可能技术。不同的方法将是本领域的技术人员显而易见的。另外,合成中的各个步骤可以按替代次序或顺序执行以产生期望的化合物。本文引用的所有文件通过引用整体并入本文。例如,下列反应是本文中公开的一些起始原料和化合物的制备的说明而非限制。合成途径1下面的方案描述了合成途径1,其可以用于合成本发明的化合物,例如,具有式i、ia或ii的结构的化合物。本领域技术人员可以预见到对这些方法的各种修改,以实现与下面给出的发明人的结果类似的结果。在下面的实施方案中,使用具有式ii的结构的化合物作为一个实施例描述了合成途径。但是,该合成途径同样可以用于制备具有式i或ia的结构的化合物。在另一个方面,描述了合成具有式ii的结构的化合物的方法,所述方法包括:(a)将具有式iii的结构的化合物转化成具有式iv的结构的化合物:和(b)将具有式iv的结构的化合物转化成具有式ii的结构的化合物:其中每次出现的x独立地不存在或者是烷基、环烷基、芳基或杂环;每次出现的q独立地是h、(ch2)qnrbrc、nra(ch2)pnrbrc、or1、sr1、或crarbrc,其中q是0或1且p是2-4;且x1和x2各自独立地不存在或者是o;r1是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环、烷基杂环;r2”是卤素、ora、os(=o)2ra或oc(=o)ra;r2’是oh、nrbrc或nra(ch2)pnrbrc;a是芳基或杂芳基;每次出现的r9和r10各自独立地是氢、os(=o)2ra、ch2c(=o)ora、c(=o)c(=o)ora、oc(=o)ra、oc(=o)ora或ra’,或者可替换地r9和r10与它们所连接的氮原子一起形成单环或二环碳环或杂环,其中所述碳环或杂环任选地被氧代取代;r3和r4各自独立地是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、ora、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc,其中p是2-4;且每次出现的ra独立地是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;每次出现的rb和rc独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环、芳基;或所述rb和rc与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;或所述ra和rb与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;其中形成的杂环任选地被(c1-c4)烷基取代,且形成的杂环中的一个或多个碳原子任选地被o、nr8或s替换,其中r8是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基。在某些实施方案中,在方案2中的步骤(a)包含式iv中的r2’基团对式iii中的r2”基团的取代反应。r2”可以是离去基团诸如卤素、ora、os(=o)2ra或oc(=o)ra。r2’可以是oh、nrbrc或nra(ch2)pnrbrc。步骤(a)可以使用亲核试剂r2’h进行。任意合适的有机碱或无机碱可以用在步骤(a)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。在某些实施方案中,在方案3中的步骤(b)包括式iv中的保护基的除去和环化反应以形成式ii中的蝶啶环体系。a可以是任何任选地被取代的芳基或杂芳基。在某些实施方案中,a是任选地被取代的苯基。用于除去保护基的条件的非限制性例子包括氢化,例如,在有催化剂诸如pd存在下使用氢。可以使用本领域已知的任意其它条件。一旦除去保护基,可以将合适的nr9r10环化在除去保护基以后新形成的nh2基团上。这样的合适的、可环化的nr9r10取代基包括、但不限于nhch2c(=o)ora和nhc(=o)c(=o)ora。这样的合适的、可环化的nr9r10取代基可以在合成的任何阶段(例如,在式iii、iv的化合物中)或在即将环化以形成蝶啶环之前安装至中间体。用于环化的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。在某些实施方案中,可以在环化过程中形成非芳族环,且步骤(b)还包括使用芳构化试剂或脱氢试剂来形成芳族蝶啶体系。这样的芳构化试剂和脱氢试剂的非限制性例子包括在某些实施方案中,r9和r10是选自fmoc-、cbz-、boc-、ac-、cf3(c=o)-、苄基、三苯基甲基和对甲苯磺酰基的保护基;或r9和r10与它们所键合的氮原子一起形成在这些实施方案中,可以除去保护基r9和r10并然后可以安装合适的环化基团(例如,r9或r10是ch2c(=o)ora或c(=o)c(=o)ora)。在某些实施方案中,所述合成途径还包括(a1)的步骤:(a1)其中每次出现的r2”独立地是卤素、ora、os(=o)2ra或oc(=o)ra。在某些实施方案中,在方案4中的步骤(a1)包括nr9nr10基团对式v中的r2”基团的取代反应以形成式iii的化合物。r2”可以是离去基团诸如卤素、ora、os(=o)2ra或oc(=o)ra。步骤(a1)可以使用亲核试剂hnr9nr10进行。任意合适的有机或无机碱可以用在步骤(a1)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。在某些实施方案中,所述步骤(a1)还包括(a2)和(a3)的步骤:(a2)和(a3)其中r9和r10中的至少一个不是氢。在步骤a2中,nh3可以用作亲核试剂以替代式v中的离去基团r2”。任意合适的有机或无机碱可以用在步骤(a2)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。在某些实施方案中,在步骤a3中,使用本领域已知的条件和试剂可以引入r9和/或r10取代基作为上述的保护基或可环化基团。这样的试剂的非限制性例子包括clos(=o)2ra、卤素-ch2c(=o)ora、clc(=o)c(=o)ora、hoc(=o)ra、clc(=o)ra、clc(=o)ora和卤素-ra’。任意合适的有机或无机碱可以用在步骤(a3)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。在某些实施方案中,步骤(b)还包括(b1)和(b2)的步骤:(b1)和(b2)其中x3是o或不存在,x4是oh或不存在,且ra是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基。因而,在某些实施方案中,在步骤b1中,式iv中的r9和/或r10取代基可以是将使用本领域已知的任意条件和试剂除去的保护基。然后可以使用合适的试剂诸如rao(c=o)c(=x3)cl引入可环化的取代基rao(c=o)c(=x3),以使用本领域已知的条件和试剂形成式vii的化合物。x3可以是o或不存在。任意合适的有机或无机碱可以用在可环化的取代基rao(c=o)c(=x3)的引入中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。保护基可以在该步骤中除去,在除去保护基r9和/或r10之前或之后除去,或者在引入可环化的取代基rao(c=o)c(=x3)之前或之后除去。然后形成准备好环化的式vii的化合物。在某些实施方案中,在步骤b2中,将式vii的化合物环化以形成式viii的化合物。任意合适的有机或无机碱可以用在可环化的取代基rao(c=o)c(=x3)的引入中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。所述环化反应可以在室温或升高的温度进行。在某些实施方案中,可以在环化过程中形成非芳族环,且所述步骤(b)还包括使用芳构化试剂或脱氢试剂以形成芳族蝶啶体系。这样的芳构化试剂和脱氢试剂的非限制性例子包括在某些具体实施方案中,r9是h且r10是-(c=o)ora。在某些实施方案中,所述方法还包括(b3)和(b4)的步骤:(b3)和(b4)其中每次出现的rd独立地是卤素、os(=o)2ra或oc(=o)ra。在某些实施方案中,在步骤b3中,使用本领域已知的任意合适的条件和试剂,可以将在式viii的化合物中的oh和/或x4基团转化成离去基团rd。合适的试剂的非限制性例子包括cl2、br2、socl2、pocl3、clos(=o)2ra、hoc(=o)ra和clc(=o)ra。任意合适的有机或无机碱可以用在该步骤中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。所述反应可以在室温或升高的温度进行。在某些实施方案中,x4不存在于式viii的化合物中,且因而式ix的化合物中的rd和式ii的化合物中的r4可以是h。在该途径中,因为r2’和r4可以在合成的不同阶段引入,r2’和r4可以是两个不同的基团。所述合成途径能够容易地且方便地合成式ii的化合物(其中r2’和r4是不同的),不需要位置异构体的不同柱和/或hplc分离。当然,使用该合成途径同样可以制备式ii的化合物(其中r2’和r4是相同的)。在某些实施方案中,x不存在。在其它实施方案中,x选自烷基、环烷基、芳基和杂环。在某些实施方案中,x是-(ch2)m-,其中m是2-4。在其它实施方案中,x是芳基。芳基的非限制性例子包括任选地被取代的苯基和萘基。在其它实施方案中,x是杂环。在某些实施方案中,x是饱和的杂环。饱和杂环的非限制性例子包括哌嗪。在其它实施方案中,x是不饱和的杂环。不饱和杂环的非限制性例子包括吡啶、吡嗪、嘧啶和哒嗪。在某些实施方案中,q是h、(ch2)qnr1r2、nr1(ch2)pnrbrc、or1、sr1、cr1r2r2’或chr1r2,其中q是0或1且p是2-4。r1、r2和r2’各自独立地是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环、烷基杂环,或r1和r2与它们所键合的氮原子一起形成杂环,所述杂环可以任选地被1-4个基团取代,所述基团可以是相同的或不同的且选自(c1-c4)烷基、苯基、苄基、c(=o)r12、(ch2)pora和(ch2)pnrbrc,其中p是2-4。在某些实施方案中,q是h、or1、sr1或chr1r2。在其它实施方案中,q是-(ch2)qnr1r2。在某些具体实施方案中,q是-(ch2)2nr1r2。在某些具体实施方案中,q是在其它实施方案中,q是其中r12是烷基、芳基或杂环。在某些实施方案中,c(=o)r12是在其它实施方案中,q是nh(ch2)pnrbrc。在某些具体实施方案中,q是nh(ch2)2n(ch3)2、nh(ch2)2n(ch2ch3)2或nh(ch2)2n(ch3)(ch2ch3)。在其它实施方案中,q是烷基。烷基的非限制性例子包括甲基、乙基、丙基、异丙基、丁基、仲丁基和叔丁基。在某些实施方案中,x不存在且q是(ch2)qnrbrc、nra(ch2)pnrbrc、or1、sr1或在某些实施方案中,x是苯基。在这些实施方案中,q在相对于蝶啶核心的邻位、间位或对位处连接至苯基。在某些具体实施方案中,q是在某些具体实施方案中,q是在相对于蝶啶核心的对位处连接至苯基的在某些具体实施方案中,-x-q是在其它具体实施方案中,-x-q是在其它具体实施方案中,-x-q是在其它具体实施方案中,-x-q是在这些实施方案中,y是nh、s或o且l是-(ch2)m-,其中m是2-6。其它取代基如本文中所述。合成途径2下面的方案描述了合成途径2,其可以用于合成本发明的化合物,例如,具有式i、ia或ii的结构的化合物。本领域技术人员可以预见到对这些方法的各种修改,以实现与下面给出的发明人的结果类似的结果。在下面的实施方案中,使用具有式ii的结构的化合物作为一个实施例描述了合成途径。但是,该合成途径同样可以用于制备具有式i或ia的结构的化合物。在另一个方面,描述了合成具有式ii的结构的化合物的方法,所述方法包括:(a)将具有式x的结构的化合物转化成具有式xi的结构的化合物:和(b)将具有式xi的结构的化合物转化成具有式ii的结构的化合物:其中每次出现的x独立地不存在或者是烷基、环烷基、芳基或杂环;每次出现的q独立地是h、rd、(ch2)qnrarb、nra(ch2)pnrbrc、or1、sr1、或crarbrc,其中q是0或1且p是2-4;且x1和x2各自独立地不存在或者是o;r1是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环、烷基杂环;每次出现的rd独立地是卤素、os(=o)2ra或oc(=o)ra;r2’是oh、nrbrc或nra(ch2)pnrbrc;r3和r4各自独立地是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、ora、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc,其中p是2-4;且每次出现的ra独立地是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;每次出现的rb和rc独立地是氢、烷基、环烷基、烯基、环烯基、炔基、杂环、芳基;或所述rb和rc与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;或所述ra和rb与它们所键合的氮原子一起任选地形成包含1-4个杂原子的杂环;其中形成的杂环任选地被(c1-c4)烷基取代,且形成的杂环中的一个或多个碳原子任选地被o、nr8或s替换,其中r8是氢、任选地被取代的烷基、任选地被取代的环烷基、任选地被取代的烯基、任选地被取代的环烯基、任选地被取代的炔基、任选地被取代的杂环或任选地被取代的芳基;前提条件是,如果在式xi的化合物的6位处的rd和r3是相同的,步骤(b)可以被省略。在某些实施方案中,在方案11中的步骤(a)包括r2’和r4基团分别对式x中的4和7位处的rd基团的取代反应以形成式xi的化合物。r2’可以是oh、nrbrc或nra(ch2)pnrbrc;r3和r4各自可以独立地是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、ora、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc,其中p是2-4。步骤(a)可以使用亲核试剂r2’h和r4h以任意次序依次进行或在一个锅中进行。任意合适的有机或无机碱可以用在步骤(a)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。当r2’和r4是相同的时,区域异构体的分离不是必要的。但是,当r2’和r4是不同的时,柱色谱法纯化和/或hplc纯化可能是分离位置异构体所必需的。这主要是由于蝶啶环的4和7位的类似反应性。在某些实施方案中,在方案11中的步骤(a)还可以包括步骤(a1)和(a2):(a1)和(a2)其中步骤(a1)还包括纯化具有式xii的结构的化合物。因而,使用亲核试剂r2’h,可以首先用r2’替换在4位处的rd基团。任意合适的有机或无机碱可以用在方案13的步骤(a1)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。该反应可以产生副产物,其中在7位处的rd基团被r2’替代。因而,通过hplc和/或柱的进一步纯化可能是必要的。随后,使用亲核试剂r4h可以用r4替换在7位处的rd基团。任意合适的有机或无机碱可以用在方案14的步骤(a2)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。在某些实施方案中,在方案11中的步骤(a)可以还包括步骤(a1)和(a2):(a1)和(a2)其中步骤(a1)还包括纯化具有式xii的结构的化合物。因而,可以首先使用亲核试剂r4h用r4替换在7位处的rd基团。任意合适的有机或无机碱可以用在方案15的步骤(a1)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。该反应可以产生副产物,其中在4位处的rd基团被r4替换。因而,通过hplc和/或柱的进一步纯化可能是必要的。随后,使用亲核试剂r2’h可以用r2’替换在4位处的rd基团。任意合适的有机或无机碱可以用在方案16的步骤(a2)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。在某些实施方案中,在方案11中的步骤(a)包括一锅合成步骤(a1x):(a1x)其中步骤(a1x)还包括纯化具有式xi的结构的化合物。因而,所述一锅合成可以在本文关于亲核取代描述的条件下一起使用亲核试剂r2’h和r4h。可能需要通过柱色谱法纯化或hplc纯化进行的纯化。在某些实施方案中,在式x和xi中的取代基-x-q是rd,且在方案11中的步骤(a)包括将具有式x’的结构的化合物转化成具有式xi’的结构的化合物:因而,如在方案18中所示,r2’和r4基团分别对式x’中的4和7位处的rd基团的取代反应形成式xi’的化合物。r2’可以是oh、nrbrc或nra(ch2)pnrbrc;r3和r4各自可以独立地是氢、卤素、氰基、硝基、cf3、ocf3、烷基、环烷基、烯基、任选地被取代的芳基、杂环、ora、sra、s(=o)ra、s(=o)2ra、nrbrc、s(=o)2nrbrc、c(=o)ora、c(=o)ra、c(=o)nrbrc、oc(=o)ra、oc(=o)nrbrc、nrbc(=o)ora、nrbc(=o)ra、烷芳基、烷基杂环或nra(ch2)pnrbrc,其中p是2-4。可以使用亲核试剂r2’h和r4h以任一种次序依次或在一个锅中进行在方案18中的反应。任意合适的有机或无机碱可以用在步骤(a)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。在某些具体实施方案中,r2’和r4是相同的。在一个实施方案中,r2’和r4都是在某些实施方案中,所述方法还包括步骤(a’):将具有式xi”的结构的化合物转化成具有式xi”’的结构的化合物,如在方案19中所示。在某些具体实施方案中,-x-q是nrarb、nra(ch2)pnrbrc、or1或sr1。在一个实施方案中,-x-q是使用亲核试剂q-x-h可以进行在方案19中的反应。任意合适的有机或无机碱可以用在步骤(a)中。合适的碱的非限制性例子包括na2co3、k2co3、naoh、koh、csoh、氢化钠、碳酸钾、三乙胺和二异丙基乙胺。用于该反应的合适溶剂包括dmso、乙醇、水、thf、二氯甲烷、乙腈、氯仿或甲苯。在某些具体实施方案中,r2’和r4是相同的。在某些具体实施方案中,r2’和r4都是在某些具体实施方案中,rd和r3都是cl。在某些具体实施方案中,所述方法包括以下两个步骤:(1)和(2)在某些具体实施方案中,所述方法还包括通过以下步骤制备具有的结构的化合物:(1’)(2’)在某些具体实施方案中,所述方法还包括通过以下步骤制备具有的结构的化合物:(1”)和(2”)在某些实施方案中,在方案1-25中的任一个中描述的任意反应可以在室温或在0℃进行。在其它实施方案中,在方案1-19中的任一个中描述的任意反应可以在升高的温度进行。升高的温度的非限制性例子包括约30、35、40、45、50、55、60、65、70、75、80、90、100、110、120、130、140、150、160、170、180、190或200℃,或在以本文中公开的任意两个值为边界的范围内。在某些实施方案中,x不存在。在其它实施方案中,x选自烷基、环烷基、芳基和杂环。在某些实施方案中,x是-(ch2)m-,其中m是2-4。在其它实施方案中,x是芳基。芳基的非限制性例子包括任选地被取代的苯基和萘基。在其它实施方案中,x是杂环。在某些实施方案中,x是饱和的杂环。饱和杂环的非限制性例子包括哌嗪。在其它实施方案中,x是不饱和的杂环。不饱和杂环的非限制性例子包括吡啶、吡嗪、嘧啶和哒嗪。在某些实施方案中,q是h、(ch2)qnr1r2、nr1(ch2)pnrbrc、or1、sr1、cr1r2r2’或chr1r2,其中q是0或1且p是2-4。r1、r2和r2’各自独立地是氢、烷基、烯基、环烷基、烷基环烷基、芳基、烷基芳基、杂环、烷基杂环,或r1和r2与它们所键合的氮原子一起形成杂环,所述杂环可以任选地被1-4个基团取代,所述基团可以是相同的或不同的且选自(c1-c4)烷基、苯基、苄基、c(=o)r12、(ch2)pora和(ch2)pnrbrc,其中p是2-4。在某些实施方案中,q是h、or1、sr1或chr1r2。在其它实施方案中,q是-(ch2)qnr1r2。在某些具体实施方案中,q是-(ch2)2nr1r2。在某些具体实施方案中,q是在其它实施方案中,q是其中r12是烷基、芳基或杂环。在某些实施方案中,c(=o)r12是在其它实施方案中,q是nh(ch2)pnrbrc。在某些具体实施方案中,q是nh(ch2)2n(ch3)2、nh(ch2)2n(ch2ch3)2或nh(ch2)2n(ch3)(ch2ch3)。在其它实施方案中,q是烷基。烷基的非限制性例子包括甲基、乙基、丙基、异丙基、丁基、仲丁基和叔丁基。在某些实施方案中,x是苯基。在这些实施方案中,q在相对于蝶啶核心的邻位、间位或对位处连接至苯基。在某些具体实施方案中,q是在某些具体实施方案中,q是在相对于蝶啶核心的对位处连接至苯基的在某些具体实施方案中,-x-q是在其它具体实施方案中,-x-q是在其它具体实施方案中,-x-q是在其它具体实施方案中,-x-q是在这些实施方案中,y是nh、s或o和l是-(ch2)m-,其中m是2-6。其它取代基如本文中所述。另外,通过本领域技术人员通常已知的操作,可以制备式i、ia和ii的其它化合物。具体地,下述实施例提供了用于制备本发明的化合物的另外方法。现在将由以下工作实施例进一步描述本发明,所述工作实施例是本发明的优选实施方案。这些实施例是示例性的而不是限制性的,并且应当理解,可能存在落入所附权利要求所定义的本发明的精神和范围内的其它实施方案。药物组合物本发明也提供了一种药物组合物,其包含至少一种如本文中所述的化合物或其药学上可接受的盐或溶剂合物、和药学上可接受的载体。在另一个方面,描述了一种药物组合物,其包含至少一种式i、ia或ii的化合物或其药学上可接受的盐、和药学上可接受的载体或稀释剂。在某些具体实施方案中,所述化合物具有结构本文使用的短语“药学上可接受的载体”是指,这样的药学上可接受的材料、组合物或媒介物,诸如液体或固体填充剂、稀释剂、赋形剂、溶剂或包封材料:其参与将主题药学试剂从一个器官或身体部分携带或运输至另一个器官或身体部分。每种载体必须是“可接受的”,其含义是,与制剂的其它成分相容,且对患者无害。可以充当药学上可接受的载体的材料的一些例子包括:糖类,诸如乳糖、葡萄糖和蔗糖;淀粉类,诸如玉米淀粉和马铃薯淀粉;纤维素和它的衍生物,诸如羧甲基纤维素钠、乙基纤维素和醋酸纤维素;黄蓍胶粉末;麦芽;明胶;滑石;赋形剂,诸如可可脂和栓剂蜡;油,诸如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;二醇类,诸如丁二醇;多元醇,诸如甘油、山梨醇、甘露醇和聚乙二醇;酯类,诸如油酸乙酯和月桂酸乙酯;琼脂;缓冲剂,诸如氢氧化镁和氢氧化铝;海藻酸;无热原水;等张盐水;林格氏溶液;乙醇;磷酸盐缓冲溶液;和在药物制剂中采用的其它无毒的相容物质。术语“载体”表示天然的或合成的有机或无机成分,活性成分与所述成分组合以促进应用。所述药物组合物的组分还能够以使得不存在实质上损害期望的药物效率的相互作用的方式与本发明的化合物和与彼此混合。如上所述,本发明的药学试剂的某些实施方案可以以药学上可接受的盐的形式提供。在这方面,术语“药学上可接受的盐”表示本发明的化合物的相对无毒的无机和有机酸加成盐。这些盐可以在本发明的化合物的最终分离和纯化过程中原位制备,或者通过使处于它的游离碱形式的纯化的本发明的化合物与合适的有机或无机酸反应并分离如此形成的盐而单独地制备。代表性的盐包括:氢溴酸盐、盐酸盐、硫酸盐、硫酸氢盐、磷酸盐、硝酸盐、乙酸盐、戊酸盐、油酸盐、棕榈酸盐、硬脂酸盐、月桂酸盐、苯甲酸盐、乳酸盐、磷酸盐、甲苯磺酸盐、柠檬酸盐、马来酸盐、富马酸盐、琥珀酸盐、酒石酸盐、萘酸盐(napthylate)、甲磺酸盐、葡庚糖酸盐、乳糖酸盐和月桂基磺酸盐等(参见,例如,berge等人,(1977)“pharmaceuticalsalts”,j.pharm.sci.66:1-19.)主题化合物的药学上可接受的盐包括所述化合物的常规无毒盐或季铵盐,例如,来自无毒的有机或无机酸。例如,这样的常规无毒的盐包括:从无机酸衍生出的那些,所述无机酸例如盐酸、氢溴酸、硫酸、氨基磺酸、磷酸、硝酸等;以及从有机酸制备的盐,所述有机酸例如乙酸、丁酸、琥珀酸、羟乙酸、硬脂酸、乳酸、苹果酸、酒石酸、柠檬酸、抗坏血酸、棕榈酸、马来酸、羟基马来酸、苯乙酸、谷氨酸、苯甲酸、水杨酸、对氨基苯磺酸、2-乙酰氧基苯甲酸、富马酸、甲苯磺酸、甲磺酸、乙烷二磺酸、草酸、羟乙磺酸等。在其它情况下,本发明的化合物可以含有一个或多个酸性官能团且因而能够与药学上可接受的碱形成药学上可接受的盐。术语“药学上可接受的盐”在这些情况下表示本发明的化合物的相对无毒的无机和有机碱加成盐。这些盐同样可以在所述化合物的最终分离和纯化过程中原位制备,或通过单独地使处于它的游离酸形式的经纯化的化合物与以下物质反应来制备:合适的碱,诸如药学上可接受的金属阳离子的氢氧化物、碳酸盐或碳酸氢盐;氨;或药学上可接受的有机伯、仲或叔胺。代表性的碱金属或碱土金属盐包括锂、钠、钾、钙、镁和铝盐等。可用于形成碱加成盐的代表性的有机胺包括:乙胺、二乙胺、乙二胺、乙醇胺、二乙醇胺、哌嗪等。(参见,例如,berge等人,出处同上.)润湿剂、乳化剂和润滑剂,诸如月桂基硫酸钠、硬脂酸镁和聚氧化乙烯-聚氧化丁烯共聚物以及着色剂、脱模剂、包衣剂、甜味剂、调味剂和芳香剂、防腐剂和抗氧化剂,也可以存在于所述组合物中。本发明的制剂包括适合于口服、经鼻、局部(包括含服的和舌下)、直肠、阴道和/或胃肠外施用的那些。所述制剂可以方便地以单位剂型呈现,且可以通过药学领域众所周知的任意方法制备。可以与载体材料组合以产生单一剂型的活性成分的量将随正在治疗的宿主、特定施用模式而变化。可以与载体材料组合以产生单一剂型的活性成分的量通常将是产生治疗效果的化合物的量。通常,在100%中,该量的范围将是约1%至约99%的活性成分,优选约5%至约70%,最优选约10%至约30%。制备这些制剂或组合物的方法包括使本发明的化合物与载体和任选的一种或多种助剂结合的步骤。一般而言,如下制备所述制剂:使本发明的化合物与液体载体或精细粉碎的固体载体或两者均匀地且密切地结合,然后,如果必要的话,使产品成形。本发明的适合用于口服施用的制剂可以呈胶囊剂、扁囊剂、丸剂、片剂、锭剂(使用经调味的基质,通常为蔗糖和阿拉伯胶或黄蓍胶)、粉剂、颗粒剂的形式,或者作为在水性或非水性液体中的溶液或混悬液,或者作为水包油或油包水液体乳剂,或者作为酏剂或糖浆剂,或者作为软锭剂(pastille)(使用惰性基质,诸如明胶和甘油、或蔗糖和阿拉伯胶)和/或作为漱口液等,每种含有预定量的本发明的化合物作为活性成分。本发明的化合物也可以作为大丸剂、药糖剂或糊剂施用。在本发明的用于口服施用的固体剂型(胶囊剂、片剂、丸剂、糖衣丸、粉剂、颗粒等)中,将所述活性成分与一种或多种药学上可接受的载体(诸如柠檬酸钠或磷酸二钙)和/或下述物质中的任一种混合:填充剂或增量剂(extender),诸如淀粉、乳糖、蔗糖、葡萄糖、甘露醇和/或硅酸;粘合剂,例如,羧甲基纤维素、海藻酸盐、明胶、聚乙烯吡咯烷酮、蔗糖和/或阿拉伯树胶;保湿剂,诸如甘油;崩解剂,诸如琼脂、碳酸钙、马铃薯或木薯淀粉、海藻酸、某些硅酸盐、碳酸钠和淀粉羟乙酸钠;溶液阻滞剂,诸如石蜡;吸收促进剂,诸如季铵化合物;润湿剂,例如,鲸蜡醇、单硬脂酸甘油酯和聚氧化乙烯-聚氧化丁烯共聚物;吸收剂,诸如高岭土和膨润土;润滑剂,诸如滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、月桂基硫酸钠,及其混合物;和着色剂。在胶囊剂、片剂和丸剂的情况下,所述药物组合物还可以包含缓冲剂。也可以使用类似类型的固体组合物,作为在软和硬填充的明胶胶囊中的填充剂,并使用诸如乳糖(lactose)或乳糖(milksugar)以及高分子量聚乙二醇等的赋形剂。通过任选地与一种或多种助剂一起压缩或模塑,可以制备片剂。使用粘合剂(例如,明胶或羟基丁基甲基纤维素)、润滑剂、惰性稀释剂、防腐剂、崩解剂(例如,淀粉羟乙酸钠或交联的羧甲基纤维素钠)、表面活性剂或分散剂,可以制备压制的片剂。通过在合适的机器中模塑用惰性液体稀释剂润湿的粉末状化合物的混合物,可以制备模塑的片剂。本发明的药物组合物的片剂和其它固体剂型(诸如糖衣丸、胶囊剂、丸剂和颗粒)可以任选地刻痕,或者用包衣剂和壳(诸如肠溶包衣和药物配制领域中众所周知的其它包衣剂)制备。还可以使用例如不同比例的羟基丁基甲基纤维素(以提供期望的释放特性)、其它聚合物基质、脂质体和/或微球配制它们,从而提供其中的活性成分的缓慢释放或控制释放。它们可以如下灭菌:例如,通过细菌截留滤器而过滤,或在即将使用之前掺入无菌固体组合物(其可以溶解在无菌水中)形式的灭菌剂或一些其它的无菌可注射介质。这些组合物也可以任选地含有遮光剂并且可以具有仅释放活性成分的组成,或优选地在胃肠道的某些部分中,任选地,以延迟方式释放。可以使用的包埋组合物的例子包括聚合物质和蜡类。活性成分也可以微囊形式存在,如果合适的话,与一种或多种上述赋形剂一起。本发明的化合物的口服给药液体剂型包括药学上可接受的乳剂、微乳剂、溶液、混悬液、糖浆剂和酏剂。除活性成分以外,所述液体剂型可以含有本领域中常用的惰性稀释剂,例如,水或其它溶剂、增溶剂和乳化剂,诸如乙醇、异丁醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苄酯、丁二醇、1,3-丁二醇、油(具体地,棉籽油、花生油、玉米油、胚芽油、橄榄油、蓖麻油和芝麻油)、甘油、四氢糠醇(tetrahydrofurylalcohol)、聚乙二醇和脱水山梨糖醇的脂肪酸酯、及其混合物。另外,环糊精(例如,羟基丁基-β-环糊精)可以用于溶解化合物。除惰性稀释剂以外,口服组合物还可以包含佐剂诸如润湿剂、乳化和助悬剂、甜味剂、调味剂、着色剂、芳香剂和防腐剂。除活性化合物以外,混悬液还可以含有助悬剂,例如,乙氧基化的异硬脂醇、聚氧乙烯山梨醇和脱水山梨糖醇酯、微晶纤维素、铝金属氢氧化物(aluminummetahydroxide)、膨润土、琼脂--琼脂和黄蓍胶、及其混合物。本发明的用于直肠或阴道给药的药物组合物的制剂可以呈现为栓剂,其可以如下制备:将一种或多种本发明的化合物与一种或多种合适的无刺激性的赋形剂或载体混合,所述赋形剂或载体包括,例如可可脂、聚乙二醇、栓剂蜡或水杨酸盐,并且其在室温为固体,但在体温为液体,且因此,将在直肠或阴道腔中熔化并释放本发明的活性药学试剂。适合阴道施用的本发明的制剂还包括子宫托、卫生栓、乳膏剂、凝胶、糊剂、泡沫或喷雾制剂,其含有本领域已知为适合的载体。用于本发明的化合物的局部或透皮施用的剂型包括粉剂、喷雾剂、软膏剂、糊剂、乳膏剂、洗剂、凝胶剂、溶液剂、贴剂和吸入剂。可以在无菌条件下将所述活性化合物与药学上可接受的载体和与可能需要的任何防腐剂、缓冲剂或推进剂混合。除本发明的活性化合物以外,所述软膏剂、糊剂、乳膏剂和凝胶剂还可以含有赋形剂,诸如动物和植物脂肪、油、蜡、石蜡、淀粉、黄蓍胶、纤维素衍生物、聚乙二醇、有机硅、膨润土、硅酸、滑石和氧化锌、或其混合物。除本发明的化合物以外,粉剂和喷雾剂还可以含有赋形剂诸如乳糖、滑石、硅酸、氢氧化铝、硅酸钙和聚酰胺粉末或者这些物质的混合物。喷雾剂可以另外含有常规推进剂(诸如氯氟烃)和挥发性的未被取代的烃(诸如丁烷和丁烷)。透皮贴剂具有给身体提供本发明的化合物的受控递送的额外优点。这样的剂型可以通过将药学试剂溶解或分散在适当介质中来制备。还可以使用吸收增强剂来增加本发明的药学试剂穿过皮肤的通量。通过提供控速膜或将所述化合物分散在聚合物基质或凝胶中,可以控制这样的通量的速率。在本发明的范围内也涵盖眼用制剂、眼软膏剂、粉剂、溶液等。适于胃肠外施用的本发明的药物组合物包含与一种或多种药学上可接受的无菌的等渗水性或非水性溶液、分散体、混悬液或乳剂,或无菌粉剂(其可以在临用前重构成无菌的可注射的溶液或分散体)组合的一种或多种本发明的化合物,其可含有抗氧化剂、缓冲剂、抑菌剂、使所述制剂与预定的接受者的血液等渗的溶质或者助悬剂或增稠剂。在某些情况下,为了延长药物的作用,需要减慢来自皮下或肌肉内注射的药物的吸收。这可以通过使用具有差水溶性的结晶或无定形物的液体混悬液来完成。药物的吸收速率则取决于它的溶解速率,所述溶解速率又可以取决于晶体大小和晶型。可替换地,通过将药物溶解或悬浮在油媒介物中,实现胃肠外施用的药物形式的延迟吸收。用于贮库注射剂的一种策略包括使用聚氧化乙烯-聚氧化丙烯共聚物,其中所述媒介物在室温为流体且在体温固化。通过形成主题化合物在可生物降解的聚合物(诸如聚丙交酯-聚乙醇酸交酯)中的微胶囊基体,制备可注射的贮库形式。取决于药物与聚合物的比率以及采用的特定聚合物的性质,可以控制药物释放速率。其它可生物降解的聚合物的例子包括聚原酸酯和聚酸酐。还通过将药物包封在与身体组织相容的脂质体或微乳剂中来制备贮库可注射制剂。当将本发明的化合物作为药物施用给人类和动物时,它们可以单独地或作为药物组合物施用,所述药物组合物含有例如与药学上可接受的载体组合的0.1%至99.5%(更优选地,0.5%至90%)的活性成分。可以在联合疗法中采用本发明的化合物和药物组合物,也就是说,所述化合物和药物组合物可以与一种或多种其它期望的治疗剂或医疗操作同时地、在其之前或之后施用。在联合方案中采用的治疗(疗法或操作)的特定组合将考虑期望的疗法和/或操作与要达到的期望治疗效果的相容性。还应当理解,采用的疗法可以对相同病症达到预期效应(例如,本发明的化合物可以与另一种抗炎或免疫抑制剂同时施用;例如但不限于nsaids、dmards、类固醇或生物制品诸如抗体疗法)或者它们可以实现不同的效应(例如,任何不良作用的控制)。本发明的化合物可以静脉内地、肌肉内地、腹膜内地、皮下地、局部地、口服地或通过其它可接受的方式施用。所述化合物可以用于治疗哺乳动物(例如,人类、家畜和家养动物)、赛马、禽类、蜥蜴和可以耐受所述化合物的任何其它生物中的关节炎病况。本发明还提供了药物包或试剂盒,其包含一个或多个容器,所述容器装有本发明的药物组合物的一种或多种成分。任选地,这样的容器可以伴有管理药品或生物制品的制造、使用或销售的政府机构规定的形式的告示,所述告示反映了所述机构关于人施用而生产、使用或销售的批准。施用给受试者本发明的一些方面涉及给受试者施用有效量的组合物以达到特定结果。因此可以以适合药用的任何方式配制根据本发明的方法有用的小分子组合物。在药学上可接受的溶液中施用本发明的制剂,所述溶液可以常规地含有药学上可接受的浓度的盐、缓冲剂、防腐剂、相容的载体、佐剂和任选的其它治疗成分。为了用于治疗,可以通过允许所述化合物被适当靶细胞摄取的任何模式给受试者施用有效量的化合物。可以通过技术人员已知的任何方式完成“施用”本发明的药物组合物。特定施用途径包括、但不限于口服、透皮(例如,经由贴剂)、胃肠外注射(皮下、真皮内、肌肉内、静脉内、腹膜内、鞘内等)或粘膜(鼻内、气管内、吸入、直肠内、阴道内等)。注射可以是推注或连续输注。例如,根据本发明的药物组合物经常通过静脉内、肌肉内或其它胃肠外方式施用。它们也可以通过鼻内应用、吸入、局部、口服或作为植入物施用,并且甚至直肠或阴道使用是可能的。合适的液体或固体药物制剂形式是例如用于注射或吸入的水溶液或盐水溶液,其被微囊化、螺卷化(encochleated)、包被到微小金颗粒表面上,包含在脂质体、经雾化的气雾剂、用于植入皮肤的小粒中,或干燥到要刮入皮肤中的锋利物体上。所述药物组合物还包括颗粒、粉剂、片剂、包衣片剂、(微)胶囊剂、栓剂、糖浆剂、乳剂、混悬液、乳膏剂、滴剂或延长活性化合物释放的制品,在它们的制备中,赋形剂和添加剂和/或助剂诸如崩解剂、粘合剂、包衣剂、膨胀剂、润滑剂、调味剂、甜味剂或增溶剂如上所述按惯例使用。所述药物组合物适合用于多种药物递送系统。关于药物递送的现有方法的简要综述,参见langerr(1990)science249:1527-33,其通过引用并入本文。在用于本发明的方法中的组合物中包括的化合物的浓度可以在约1nm至约100μm的范围内。据信有效剂量是在约10皮摩尔/kg至约100微摩尔/kg范围内。药物组合物优选地以剂量单位制备和施用。液体剂量单位是用于注射或其它胃肠外施用的小瓶或安瓿。固体剂量单位是片剂、胶囊剂、粉剂和栓剂。为了治疗患者,根据化合物的活性、施用方式、施用目的(即,预防或治疗)、病症的性质和严重程度、患者的年龄和体重,不同的剂量可能是必要的。通过以单个剂量单位或几个较小剂量单位的形式单次施用,可以进行给定剂量的施用。本发明还预见到以相隔数天、数周或数月的特定间隔重复和多次施用剂量。所述组合物可以单独地(纯的)或以药学上可接受的盐的形式施用。当用在药物中时,所述盐应当是药学上可接受的,但是非药学上可接受的盐可以方便地用于制备其药学上可接受的盐。这样的盐包括、但不限于从以下酸制备的那些盐:盐酸、氢溴酸、硫酸、硝酸、磷酸、马来酸、乙酸、水杨酸、对甲苯磺酸、酒石酸、柠檬酸、甲磺酸、甲酸、丙二酸、琥珀酸、萘-2-磺酸和苯磺酸。并且,这样的盐可以制备为碱金属或碱土金属盐,诸如羧酸基团的钠、钾或钙盐。合适的缓冲剂包括:乙酸和盐(1-2%w/v);柠檬酸和盐(1-3%w/v);硼酸和盐(0.5-2.5%w/v);和磷酸和盐(0.8-2%w/v)。合适的防腐剂包括苯扎氯铵(0.003-0.03%w/v);三氯叔丁醇(0.3-0.9%w/v);对羟基苯甲酸酯(0.01-0.25%w/v)和硫柳汞(0.004-0.02%w/v)。适合用于胃肠外施用的组合物方便地包括可以与接受者的血液等渗的无菌水性制剂。可接受的媒介物和溶剂包括水、林格氏溶液、磷酸盐缓冲盐水和等渗氯化钠溶液。此外,无菌的不挥发油常用作溶剂或悬浮介质。为此目的,可以采用任何温和的不挥发的矿物油或非矿物油,包括合成的甘油单酯或甘油二酯。此外,诸如油酸这类脂肪酸可以用于制备注射剂。可以在remington’spharmaceuticalsciences,mackpublishingcompany,easton,pa中找到适合皮下、肌肉内、腹膜内、静脉内等施用的载体制剂。在本发明中有用的化合物可以以超过两种这样的化合物的混合物递送。除了化合物的组合外,混合物还可以包括一种或多种佐剂。多种施用途径是可用的。当然,选择的特定模式将取决于选择的特定化合物、受试者的年龄和总体健康状况、正在治疗的特定病况和治疗效果所需的剂量。一般而言,使用医学上可接受的任何施用模式(意指产生有效的反应水平且不造成临床上不可接受的不良作用的任何模式),可以实践本发明的方法。在上面讨论了优选的施用模式。所述组合物可以方便地以单位剂型呈现并且可以通过制药领域众所周知的任何方法制备。所有方法包括以下步骤:使所述化合物与构成一种或多种助剂的载体混合。一般而言,如下制备所述组合物:使所述化合物与液体载体、精细粉碎的固体载体或或二者均匀地且密切地混合,然后,如果必要的话,使产品成形。其它递送系统可以包括延时释放、延迟释放或持续释放递送系统。这样的系统可以避免所述化合物的重复施用,从而为受试者和医师增加方便。许多类型的释放递送系统是本领域普通技术人员可得到的和已知的。它们包括基于聚合物的系统诸如聚(丙交酯-乙交酯)、共聚草酸酯、聚己内酯、聚酰胺酯、聚原酸酯、聚羟基丁酸和聚酸酐。在例如美国专利号5,075,109中描述了含有前述聚合物的药物的微胶囊。递送系统还包括非聚合物系统,即:脂质,其包括甾醇类诸如胆固醇、胆固醇酯和脂肪酸或中性脂肪诸如甘油单酯、甘油二酯和甘油三酯;水凝胶释放系统;硅橡胶系统;基于肽的系统;蜡包衣;使用常规粘合剂和赋形剂的压制片剂;部分熔合的植入物;等。具体例子包括、但不限于:(a)侵蚀系统,其中本发明的试剂以在基质内的形式包含在其中,诸如在美国专利号4,452,775、4,675,189和5,736,152中描述的那些;和(b)扩散系统,其中活性组分以受控速率从聚合物渗透,诸如在美国专利号3,854,480、5,133,974和5,407,686中描述的那些。另外,可以使用基于泵的硬件递送系统,其中的一些适合植入。等同方案下面的代表性实施例旨在帮助举例说明本发明,并且无意、也不应将其解释为限制本发明的范围。实际上,本领域技术人员从本文件的完整内容会明白除了在本文中显示和描述的那些以外的、本发明的各种修改及其许多其它实施方案,包括以下实施例和对在本文中所引用的科学和专利文献的提及。还应当理解,那些引用的参考文献的内容通过引用并入本文以帮助说明技术水平。下述实施例含有重要的额外信息、例证和指导,其可以适合本发明在各个实施方案及其等同方案中的实践。实施例实施例1.使用合成途径1合成溶液1:将2-甲硫基-4,6-二羟基嘧啶(15.8gm,0.10摩尔)溶解在含有氢氧化钠(24gm,0.60摩尔)的水(200ml)中。一旦溶解结束,将溶液在冰上冷却并加入碎冰(100gm)。溶液2:将苯胺(9.3gm,0.10摩尔)和浓盐酸(20ml)加入水(150ml)和冰(150gm)中。向该溶液中加入亚硝酸钠(6.9gm,0.10摩尔)溶解在水(50ml)中的溶液。所述加入在搅拌下使用分液漏斗逐滴进行,出料口位于苯胺溶液的表面以下。一旦加入结束,将重氮鎓溶液在0℃搅拌10分钟。然后在搅拌下在0℃将溶液2加入溶液1中。将得到的红色溶液搅拌30分钟并然后用浓盐酸酸化,从而造成偶氮基嘧啶(azopyrimidine)分离为亮黄色固体。将固体通过过滤进行分离,并用水充分洗涤,然后干燥。产量为25gm(95.3%)。将偶氮基嘧啶(25gm,9.53x10-2摩尔)在磷酰氯(150ml)中搅拌并缓慢地加入二异丙基乙胺(35ml)。将溶液温热至约50℃。将该溶液加热至回流保持5分钟,并然后在室温搅拌过夜。将多余的磷酰氯在减压下除去。将残余的红色固体溶解在氯仿(250ml)中,并将该溶液与水(200ml)一起搅拌。将固体碳酸氢钠分份加入,直到停止产生二氧化碳。搅拌另外15分钟以后,将氯仿溶液分离并经硫酸镁干燥。过滤以除去干燥剂以后,将氯仿在减压下蒸发。将得到的固体在水(400ml)中搅拌并将固体碳酸氢钠分份加入直到停止产生二氧化碳且ph保持在7.0-8.0。将固体4,6-二氯-2-甲硫基-5-苯基偶氮基嘧啶通过过滤进行分离,用水洗涤和干燥。以28gm(98%)的产量得到红色产物。将4,6-二氯-2-甲硫基-5-苯基偶氮基嘧啶(5.98gm,0.02摩尔)和甘氨酸乙酯盐酸盐(2.79gm,0.02摩尔)的混合物在乙醇(100ml)中搅拌。向其中加入二异丙基乙胺(5.17gm,6.97ml,0.04摩尔)。这造成深黄色溶液的形成。搅拌几分钟以后,固体开始分离。在室温搅拌1小时以后,将反应物在冰柜中储存过夜。将已经结晶的固体通过过滤进行分离并先后用乙醇和己烷洗涤,然后干燥。黄色产物的产量是6.3gm(86.1%)。将氯代嘧啶(17.36gm,4.75x10-2摩尔)和n-(2-氨基乙基)吗啉(12.36gm,9.5x10-2摩尔)在2-丁醇(100ml)中组合并使混合物达到回流。回流30分钟以后,将溶液冷却至室温,从而造成产物从溶液中结晶。在冰上冷却以后,将产物通过过滤进行分离并用2-丙醇洗涤,然后干燥。黄色产物的产量是18.7gm(85.7%)。将甲硫基嘧啶(39.54gm,8.6x10-2摩尔)的溶液溶解在氯仿(200ml)中。将该溶液在冰上冷却,同时通过滴液漏斗缓慢地加入间氯过氧苯甲酸(40.1gm的77%酸/23%水,0.172摩尔)溶解在氯仿(450ml)中的溶液。加入结束后,将反应物在室温搅拌过夜。向其中加入碳酸钾细粉(30gm)并继续搅拌2小时。将固体通过经硅藻土过滤除去,并将硅藻土用氯仿充分洗涤。将合并的滤液在减压下蒸发。将剩余物与2-丙醇(200ml)一起搅拌并加入n-甲基哌嗪(17.23gm,19.1ml,0.172摩尔)。回流搅拌1小时以后,将反应物在室温搅拌过夜。将2-丙醇通过减压蒸发除去,并将剩余物在氯仿(400ml)和20%碳酸钾溶液(200ml)之间分配。将氯仿溶液经硫酸镁干燥。过滤以除去干燥剂以后,将滤液减压蒸发。将得到的固体在乙醚中搅拌,然后通过过滤进行分离并干燥。产物的产量是36.0gm(81.8%)。将偶氮基嘧啶(25gm,5.44x10-2摩尔)溶解在甲醇(150ml)和thf(100ml)的混合物中。向其中加入10%炭载钯(50%水,15gm)。将其在50psi的氢气下在parr振荡器上氢化。4小时以后,氢气消耗已经停止,且溶液已经从深黄色变成无色。将反应在50psi的氢气下保持24小时以允许闭环完成。然后将催化剂通过过滤除去并将滤液在减压下蒸发。将乙醚(100ml)加入剩余物中并将其搅拌30分钟,从而造成产物结晶。将固体产物通过过滤进行分离,用乙醚洗涤并干燥。产量是14.1gm(78%)。将二氢蝶啶酮(1.5gm,4.0x10-3摩尔)在温暖的40%甲醇于四氢呋喃中的溶液(100ml)中的溶液搅拌,同时通过加料漏斗缓慢地加入o-氯醌(984mg,4.0x10-3摩尔)在四氢呋喃(60ml)中的溶液。加入结束后,将黄色溶液搅拌15分钟,并然后加入4m的氯化氢在二噁烷中的溶液(1.0ml,4.0x10-3摩尔)。将其在室温搅拌1小时,在该时间中固体分离。将反应物在冰柜中冷却,然后将固体通过过滤进行收集。用二乙醚洗涤以后,将固体干燥。产量是1.05gm,70.1%。将6-羟基蝶啶(385mg,1.03x10-3摩尔)在亚硫酰氯(10ml)和二甲基甲酰胺(1ml)中回流加热。3小时以后,将反应物冷却并将亚硫酰氯在减压下除去。将剩余物在二氯甲烷(100ml)和饱和碳酸氢钠(100ml)之间分配。将二氯甲烷溶液经硫酸镁干燥,然后过滤和在减压下蒸发。向剩余物中加入2-丁醇(5ml)和n-(2-氨基乙基)吗啉(269mg,2.06x10-3摩尔)。将得到的溶液回流加热2小时。冷却后,将反应物在二氯甲烷(50ml)和2%碳酸钾(50ml)之间分配。将二氯甲烷溶液经硫酸镁干燥,然后过滤和在减压下蒸发。使用25%的甲醇在氯仿中的溶液作为洗脱液,将剩余物通过硅胶上的色谱法纯化。将含有产物的级分合并和在减压下蒸发。以300mg(55.9%)的产量分离产物,jb6121。实施例2.使用合成途径2第一次合成步骤1.作为制备5,6-二氨基-4-羟基-2-甲硫基嘧啶的一锅反应的烷基化、亚硝基化和还原向氢氧化钠(30gm,0.75摩尔)在水(280ml)中的溶液中加入4-氨基-6-羟基-2-巯基嘧啶一水合物(60gm,0.37摩尔)。一旦嘧啶已经溶解,将溶液在冰上搅拌并冷却至<10℃。通过滴液漏斗历时1小时加入硫酸二甲酯(32.6gm,24.5ml,0.258摩尔),保持温度低于10℃。一旦加入结束,将反应物缓慢地温热至90℃并在该温度保持过夜。在25%的甲醇在氯仿中的溶液中运行tlc以跟踪反应。加入更多的硫酸二甲酯,迅速形成期望的2-甲硫基-4-氨基-6-羟基嘧啶,但是也造成更多的2-甲硫基-4-甲氧基-6-氨基嘧啶的形成。使用小于1摩尔的硫酸二甲酯并加热反应物以利用甲基硫酸钠,从而减少副产物形成。该反应是缓慢的,且因此可能需要延长的加热时间段。为了运行tlc,将几滴反应混合物加入1.0ml甲醇和一滴乙酸中。将该溶液印迹在硅胶板上,干燥,并在25%的甲醇在氯仿中的溶液中运行。4-氨基-6-羟基-2-巯基嘧啶,rf=0.26,2-甲硫基-4-羟基-6-氨基嘧啶,rf=0.51,2-甲硫基-4-甲氧基-6-氨基嘧啶,rf=0.66。一旦冷却至室温,一些固体已经分离。将反应物过滤,并将固体在氢氧化钠(10gm,0.25摩尔)在水(100ml)中的溶液中搅拌。将少量剩余的固体通过过滤除去,并将组合的水性滤液用于亚硝基化,无需分离2-甲硫基-4-氨基-6-羟基嘧啶。将来自上面的4-氨基-6-羟基-2-甲硫基-嘧啶溶液(0.37摩尔)搅拌,同时加入亚硝酸钠(29.2gm,0.42摩尔)在水(100ml)中的溶液。将该溶液在冰上冷却至15℃并搅拌,同时通过滴液漏斗缓慢地加入乙酸(65gm,0.1.08摩尔),保持温度低于20℃。白色固体立即开始分离,但是随着继续加入乙酸,混悬液变得更稠且变成蓝色。一旦所有的乙酸已经加入,将蓝色混悬液在室温搅拌过夜。tlc(在硅胶板上在25%的甲醇在氯仿中的溶液中运行,样品准备如在注解1中所述)表明,亚硝基化反应在乙酸加入以后是缓慢的,并执行搅拌过夜以允许反应进行至结束。向该混悬液中加入氢氧化钠(59.8gm,1.5摩尔)在水(200ml)中的溶液。浆从蓝色变成粉红色。将浆加热至45℃。向该温暖的浆中历时30分钟加入连二亚硫酸钠(165gm,0.95摩尔),保持温度低于55℃,在必要时使用冷却。一旦所有的连二亚硫酸钠已经加入,淡黄色混悬液已经形成。将其加热至70℃保持30分钟,然后将其冷却至室温过夜。将得到的浆过滤,并将固体用水洗涤。干燥以后,以34.5gm(54.1%)的产量得到作为褐色固体的产物,2-甲硫基-4,5-二氨基-6-羟基嘧啶(通过hplc确定纯度为91%,ms,分子量=173)。将该物质从沸水重结晶为黄色针状物。步骤1a.制备5,6-二氨基-4-羟基-2-甲硫基嘧啶的替代方法向氢氧化钠(25.3gm,0.63摩尔)在水(250ml)中的溶液中加入5,6-二氨基-4-羟基-2-巯基嘧啶(50gm,0.32moles,aldrich#d17807)。一旦嘧啶已经溶解,将溶液在冰上搅拌并冷却至<10℃。通过滴液漏斗历时1小时加入硫酸二甲酯(27.9gm,20.9ml,0.22摩尔),保持温度低于10℃。一旦加入结束,将反应物温热至室温,然后缓慢地温热至90℃并在该温度保持15小时。一旦冷却至室温,将得到的浆用乙酸(20ml)处理至ph5。将反应浆加热至沸腾并过滤以除去少量不溶性的固体。将热滤液在冰上冷却,并将结晶的固体通过过滤进行分离,用水洗涤和干燥。5,6-二氨基-4-羟基-2-甲硫基嘧啶的产量是29.5gm,54.2%。步骤2:蝶啶形成将粉末状2-甲硫基-4-羟基-5,6-二氨基嘧啶(48.2gm,2.80x10-1摩尔)和n-甲基吡咯烷酮(150ml)的混合物在65℃加热直到嘧啶已经溶解。将溶液在冷水浴中搅拌,且当温度已经达到40℃时,加入吡啶(26.4gm,27ml,3.34x10-1摩尔),然后通过加料漏斗缓慢地加入乙基草酰氯(45.6gm,37.2ml,3.34x10-1摩尔)(当冷却至45℃时,一些固体分离,但是这在加入吡啶和一些乙基草酰氯后迅速溶解)。通过加入速率和通过使用冷却浴使温度保持在40℃至50℃之间。加入结束后,将反应物在室温搅拌1小时。tlc(硅胶,25%甲醇/chcl3)表明二胺的损失(rf=0.35),形成单一产物(rf=0.69)。使溶液在油浴中达到115℃。约2小时以后,固体开始分离。将反应物在115℃浴温度(108℃锅温度)保持4小时。tlc(硅胶,25%甲醇/chcl3)表明化合物的完全损失(在rf=0.69),形成新产物(在rf=0.24)。加热阶段以后,将反应物在室温搅拌过夜。在室温搅拌过夜不是必需的,且外部冷却至10℃保持30分钟是足够的。将固体通过过滤进行分离并先后用nmp和丙酮(200ml)洗涤,然后干燥。2-甲硫基-4,6,7-三羟基蝶啶的产量是46.6gm(73.6%)。通过hplc确定纯度是88%。ms,分子量=225。步骤3:jb6136的形成将2-甲硫基-4,6,7-三羟基蝶啶(15.7gm,6.94x10-2摩尔)、亚硫酰氯(75ml)和二甲基甲酰胺(4.8ml)的混合物在室温搅拌30分钟。将该浆加热至回流。2小时以后,深黄色溶液已经形成。继续加热另外4小时。将一些亚硫酰氯(20ml)在减压下在50℃除去,然后分离固体。向剩余的混合物中加入氯仿(100ml),并将其搅拌直到溶液已经形成。然后将溶液倒在冰和水上,并将该混合物搅拌以分解剩余的亚硫酰氯。分离各层,并将氯仿溶液先后用冷水(100ml)和饱和碳酸氢钠洗涤。然后将溶液经硫酸镁干燥,然后过滤以除去干燥剂。将滤液不经进一步纯化地用于下一步。将来自上面的2-甲硫基-4,6,7-三氯蝶啶在氯仿中的溶液在冰上冷却和搅拌,同时通过滴液漏斗缓慢地加入硫酰氯(16.4gm,9.8ml,1.22x10-1摩尔)。然后将溶液在室温搅拌过夜。将挥发物在减压下蒸发至20ml的体积。向剩余物中加入庚烷(100ml),其造成固体分离。将浆在减压下浓缩至25ml的体积。加入另外的庚烷(100ml),并将浆再次在减压下浓缩至25ml的体积。将剩余的庚烷从固体倾析,将所述固体用少量庚烷洗涤。将固体溶解在氯仿(100ml)中,并将该含有2,4,6,7-四氯蝶啶的溶液不经纯化地用于下一步。将来自上面的四氯蝶啶溶液在冰上搅拌和冷却。在搅拌下通过滴液漏斗向其中加入n-(2-氨基乙基)吗啉(18.1gm,0.139摩尔)溶解在氯仿(50ml)中的溶液。将得到的溶液在室温搅拌过夜。将溶液先后用10%碳酸钾(100ml)和水(100ml)洗涤。经硫酸镁干燥以后,将氯仿溶液过滤并在减压下浓缩至约25ml的体积。向剩余的溶液中加入乙酸乙酯(100ml)。将该溶液在减压下浓缩至约25ml。再次加入乙酸乙酯(100ml)并将溶液在减压下浓缩至约50ml。将该浓缩物在室温搅拌,从而造成二氯蝶啶结晶。所述化合物缓慢地结晶,且在室温搅拌过夜有助于使产量最大化。将固体通过过滤进行分离,用冷乙酸乙酯洗涤并干燥以13.0gm(从2-甲硫基-4,6,7-三羟基蝶啶开始,41%)的量得到作为褐色粉末的jb6136(该物质可以从乙酸乙酯重结晶)。通过hplc确定的纯度是99.4%。ms,分子量=457。步骤4:jb6121三盐酸盐的制备使二氯蝶啶(34.7gm,7.58x10-2摩尔)和n-甲基哌嗪(9.1gm,10.1ml,9.1x10-2摩尔)在甲醇(375ml)中的混合物达到回流,这会产生橙色溶液。回流15小时以后,tlc(硅胶,15%的甲醇在氯仿中的溶液)表明起始原料的损失(rf=0.45)和蓝色荧光化合物的形成(rf=0.15)。将溶液冷却至85℃并加入浓盐酸(31.4ml,3.6x10-1摩尔)。冷却至室温后,盐酸盐结晶。在冰上冷却以后,将固体通过过滤进行分离,先后用冷甲醇(100ml)、二乙醚(100ml)洗涤,然后在真空下在45℃干燥。产量是32.5gm(从二氯蝶啶开始,总体上68.0%)作为白色固体。蒸发滤液得到水性油,将其与2-丙醇(200ml)一起搅拌。静置过夜以后,半固体块已经形成。将2-丙醇从所述块倾析,将所述块溶解在沸腾的甲醇(200ml)中。在冰箱中冷却过夜以后,以6.0gm(12.6%)的产量得到第二批jb6121盐酸盐。使用无水hcl在甲醇中的溶液可以增加第一批jb6121盐酸盐的产量。通过hplc确定的纯度是99.5%。ms,分子量=521。tlc:(硅胶,25%的甲醇在二氯甲烷中的溶液)-一个斑点,rf=0.65。实施例3.使用合成途径2第二次合成将粉末状2-甲硫基-4-羟基-5-亚硝基-6-氨基嘧啶(12.6gm,6.77x10-2摩尔)在氢氧化钠(8.1gm,2.03x10-2摩尔)在水(150ml)中的溶液中搅拌。将该蓝色混悬液搅拌,同时历时30分钟分份加入连二亚硫酸钠(25gm)。加入结束后,蓝色已经褪去并已经形成白色混悬液。在室温搅拌过夜以后,将固体通过过滤进行分离,用水洗涤并干燥。产物的产量是11.4gm(98%)。将2-甲硫基-4-羟基-5,6-二氨基嘧啶(31.4gm,0.183摩尔)和吡啶(500ml)的混合物加热直到嘧啶已经溶解。将溶液在冷水浴中搅拌,且当温度已经达到40℃时,通过加料漏斗缓慢地加入乙基草酰氯(34.9gm,28.5ml,0.256摩尔)。加入结束后,将反应物在室温搅拌1小时。tlc(硅胶,25%甲醇/chcl3)表明二胺的完全损失(rf=0.35),并形成单一产物(rf=0.69)。使溶液达到回流。约15分钟以后,固体开始分离。将反应物在回流保持2小时。tlc(硅胶,25%甲醇/chcl3)表明化合物的完全损失(rf=0.69),并形成新产物(rf=0.24)。冷却至室温以后,将固体通过过滤进行分离并用丙酮洗涤,然后干燥。将粗制的固体(其含有吡啶盐酸盐)溶解在含有氢氧化钠(15gm,0.375摩尔)的水(300ml)中。向该溶液中加入浓盐酸(60ml)至ph3。将沉淀的固体通过过滤进行分离,用水洗涤并干燥。蝶啶的产量是27.5gm(66.4%)将2-甲硫基-4,6,7-三羟基蝶啶(2.0gm,8.84x10-3摩尔)、亚硫酰氯(20ml)和二甲基甲酰胺(4ml)的混合物在室温搅拌过夜。将得到的浆加热至75℃保持4小时。将得到的黄色溶液冷却,并将多余的亚硫酰氯在减压下除去。将剩余的固体溶解在二氯甲烷中,并加入冰的同时搅拌溶液。将冷却的(冰)混合物搅拌,同时加入碳酸氢钠直到水溶液的ph为7-8。将二氯甲烷经硫酸镁干燥,然后过滤并在减压下蒸发。将剩余物在二乙醚中搅拌,这造成少量深色物质的沉淀。将其通过过滤除去并将乙醚在减压下蒸发以2.12gm(85%)的产量得到作为亮黄色固体的2-甲硫基-4,6,7-三氯蝶啶。将2-甲硫基-4,6,7-三氯蝶啶(2.12.gm,7.53x10-3摩尔)在二氯甲烷(50ml)中的溶液搅拌,同时加入n-(2-氨基乙基)吗啉(3.45gm,2.65x10-2摩尔)。将得到的溶液在室温搅拌过夜。将反应溶液用二氯甲烷(50ml)稀释并用5%碳酸钾溶液(50ml)洗涤。将二氯甲烷溶液经硫酸镁干燥,然后过滤并在减压下蒸发。剩余的油在冷却后迅速固化。将该固体从2-丙醇(50ml)重结晶以2.4gm(69%)的产量得到产物。将甲硫基嘧啶(3.75gm,8.0x10-3摩尔)溶解在乙酸(4.6ml)中并在冰上冷却。向其中加入过氧化氢(30%,3.4ml)和钨酸钠二水合物(792mg,2.40x10-3摩尔)。将该溶液在冰上搅拌2小时,在此时加入更多的乙酸(4.6ml)和过氧化氢(30%,3.4ml)。将得到的溶液在冰柜中保持过夜。将反应物在冷水中稀释,并通过小心地加入碳酸钾进行中和。一旦中和,将产物砜萃取进二氯甲烷(2x100ml)中。将有机溶液经硫酸镁干燥,然后过滤并在减压下蒸发。将砜不经进一步纯化地用于下一步。在正丁醇(10ml)中组合蝶啶砜(677mg,1.35x10-3摩尔)和n-甲基哌嗪(203mg,225μl,2.0x10-3摩尔)。将其回流加热10小时。tlc(硅胶,15%的甲醇在二氯甲烷中的溶液)表明砜的损失,具有与jb6121一致的主要产物以及几种次要产物。冷却后,将反应物在二氯甲烷(50ml)和5%碳酸钾之间分配。将二氯甲烷溶液经硫酸镁干燥,然后过滤并在减压下蒸发。将剩余物溶解在沸腾的乙醇(10ml)中并加入浓盐酸(382μl)。冷却后,分离固体,将其通过过滤进行分离。用乙醇洗涤以后,将固体干燥以400mg(47%)的产量得到jb6121三盐酸盐。实施例4.herg膜片箝测定和蝶啶类似物针对tlr的体外ic50herg(自动化的膜片箝)herg抑制测定使用高通量单细胞平坦膜片箝方案。将用herg基因转染的中国仓鼠卵巢细胞(cho-herg)分配在patchplate中。使用两性霉素作为穿孔剂以获得向细胞的电通道。在通过穿孔的膜片箝加入试验化合物之前,测量herg尾电流。以确定的浓度或浓度范围加入试验化合物以后,执行herg电流的第二次记录。如下得到抑制程度(%):在药物孵育之前和之后测量尾电流振幅,其由达到+20mv的两秒脉冲以后的达到-40mv的一秒试验脉冲诱导(将差分电流相对于对照归一化,并乘以100以得到抑制百分比)。将浓度(log)应答曲线拟合至逻辑方程(三个参数假定在非常高的试验化合物浓度电流的完全阻断)以产生50%抑制浓度(ic50)的估计值。从电流的减小百分比构建每种化合物的浓度-应答关系。经常将数据分类成以下分类区间:tlr7、-8和-9是跨膜蛋白的tlr家族的亚类的成员,其识别微生物-相关的核酸基序以刺激转录因子(诸如nf-κb)和炎症性细胞因子的产生。由浆细胞样树突细胞(pdc)表达的tlr7被ssrna寡核苷酸活化以产生尤其是1型干扰素,ifnα。类似地,tlr9也由pdc以及b-细胞表达,并诱导ifnα的表达,但是不同于tlr7,tlr9由cpg-dna刺激。尽管由ssrna活化,tlr8在定位和下游信号传递方面不同于tlr7;tlr8定位至髓样树突细胞(mdc)并导致炎症性细胞因子(诸如tnfα)的产生。通过为目标tlr定制刺激/读出,我们能够在原代人外周血单核细胞(pbmc)中测量小分子拮抗剂针对tlr7、-8或-9的活性。toll样受体(tlr)是与果蝇蛋白toll相关的跨膜蛋白家族,并通过识别病原体-相关的微生物模式(pamp)作为先天性免疫应答的关键介质起作用。tlr对pamp(诸如脂多糖(lps)、微生物dna或rna)的识别会通过myd88活化toll/白介素-1受体(il-1r)信号传递级联,从而导致转录因子(包括nf-κb)的产生,其随后造成免疫应答基因(诸如白介素(il)-6、il-8、1型干扰素(ifn)和肿瘤坏死因子(tnf))的转录/翻译。尽管在tlr的功能和活化中存在一些冗余,然而各种tlr可以通过它们的独特表达谱以及它们识别的具体pamp来区分开。tlr7、-8、-9与tlr3一起构成tlr的亚家族,其尽管在结构上类似于tlr1-6,但是定位在核内体内而不是在细胞表面上,并且主要存在于富免疫的组织(诸如脾和周围血细胞)中。在该亚组中的tlr对病原体相关的寡核苷酸(dna或rna)做出应答,并且可以基于识别的具体核酸基序、表达谱和下游效应物信号传递来区分开。人tlr7和-9都在浆细胞样树突细胞(pdc)中表达,而tlr8存在于髓样树突细胞(mdc)中。tlr9也由外周b细胞表达。已经证实嗜中性粒细胞(人血液中的最丰富的免疫细胞)表达除tlr3以外的所有人tlr。单链rna寡核苷酸或脱氧胞苷酸-磷酸-脱氧鸟苷酸(cpg)dna分别对tlr7或tlr9的活化导致ifnα的产生。类似于tlr7,tlr8也由单链rna活化,从而导致jun-n末端激酶(jnk)信号传递的活化和tnfα的产生。以前的研究已经提示,抗-疟疾药物(具体地喹啉)可以抑制人外周血单核细胞(pbmc)中的tlr7、-8和-9活性。为了确定我们的小分子拮抗剂化合物针对tlr7、-8和-9的效力,我们开发了体外测定以筛查在pbmc中的拮抗剂活性。通过利用独特的tlr信号传递途径,我们能够明确地确定我们的拮抗剂相对于其它小-分子拮抗剂且针对tlr7、-8或-9的相对活性。从来自健康人供体(bloodresearchcomponents,llc)的未纯化的血沉棕黄层分离pbmc。对于拮抗剂试验,将细胞以3x106个细胞/ml铺板在96-孔u-底板上。将拮抗剂化合物加给一式两份孔中的细胞,并以1:3系列稀释度从10μm开始滴定(共试验了8种拮抗剂浓度)。大约30分钟以后,用激动剂化合物刺激细胞(关于激动剂浓度参见表2)。刺激以后,将细胞在37℃孵育过夜。为了增加ssrna的稳定性,将3μg/mldotap(roche)加入orn1075激动剂溶液中。在rpmi-1640培养基(sigma,目录号r7388)+5%人雄性ab血清(sigma,目录号h4522)+1x青霉素/链霉素溶液(vwr,目录号82026-730)中进行所有稀释。表2:用于人pbmc测定的tlr激动剂的总结.用于原代人细胞中的拮抗剂试验的、用于刺激tlr7、-8或-9活性的激动剂的总结.elisa使用对目标tlr特异性的细胞因子读出,通过elisa测量pbmc和嗜中性粒细胞中的tlr活性。tnfαelisa.使用elisamaxtmdeluxesethumantnfα试剂盒(biolegend,目录号430206),使用tnfα作为用orn1075(关于浓度参见表3)刺激的pbmc和嗜中性粒细胞中的tlr8活性的读出。在1xassaydiluent(biolegend)中将来自pbmc的上清液1:50稀释,并将来自嗜中性粒细胞的上清液1:3稀释。根据试剂盒产品说明书运行elisa。使用moleculardevicesspectramax340pc平板读数器记录在450nm的吸光度。随后按照下述的方法计算每种拮抗剂的ic50。表3:用于试验每种tlr-激动剂组合的elisa总结表.**tlr7和tlr8被单链rna活化,分别发出i型干扰素或肿瘤坏死因子的产生的信号。tlr9被未甲基化的双链cpg-dna基序活化,并导致i型干扰素(诸如ifnα)的产生。ifnαelisa使用人pan-ifnαelisa试剂盒(mabtech,目录号3425-1h-20),将ifnα测量为分别用orn1075或odn2395刺激的pbmc中的tlr7和tlr9活性的读出。将pbmc上清液在pbs+0.05%tween-20+0.1%bsa中1:3稀释。使用moleculardevicesspectramax340pc平板读数器记录在450nm的吸光度。随后按照下述的方法计算每种拮抗剂的ic50。从elisa数据集和生物学特性对比计算拮抗剂的ic50首先将每个96-孔板的原始elisa数据集(其由在450nm的吸光度读出组成)输入microsoftexcel中以计算每种标准或拮抗剂浓度的平均吸光度。然后将平均数据输入sigmaplotv.11.0,其中计算标准曲线并用于外推产生的tlr读出(tnfα、ifnα等)的相对浓度。然后用sigmaplotv.11.0在对数标度上绘制每种拮抗剂的剂量-应答曲线。在microsoftexcel中将tlr读出的浓度转化成相对于该elisa板的平均最大浓度的百分比。然后使用4-参数hill方程式用sigmaplot回归向导确定每种拮抗剂的ic50。在最少3个独立实验中试验每种拮抗剂,并使用microsoftexcel编译ic50结果和求平均值。试验了化合物jb6059、jb6116、jb6131和6-氯-2-(4-甲基哌嗪-1-基)-n4,n7-双(2-吗啉代乙基)蝶啶-4,7-二胺。6-氯-2-(4-甲基哌嗪-1-基)-n4,n7-双(2-吗啉代乙基)蝶啶-4,7-二胺直到30μm没有表现出可测量的herg抑制。但是,jb6059、jb6116和jb6131分别表现出等于6.2μm、13.1μm和8.1μm的ic50,参见图1。在tlr抑制测定中,证实了jb6121(6-氯-2-(4-甲基哌嗪-1-基)-n4,n7-双(2-吗啉代乙基)蝶啶-4,7-二胺)比tlr9、tlr8和tlr7的总和更有效。参见,表4a和方案18。表4a.蝶啶化合物针对tlr的ic50.表4b.herg和%肝细胞生存力.方案18.各种化合物的结构如上所示,已经令人惊讶地发现,与其它化合物相比,式(i)的化合物(例如,jb6121)表现出惊人的优良心脏安全性(在herg膜片箝测定中)和优良肝细胞安全性(在肝细胞生存力试验中)。参见,表4b和方案18。根据mosmann,t.,1983,j.immunol.met.65:55-62,由cerep,seattle,wa执行肝细胞细胞生存力测定。实施例5.6-氯-2-(4-甲基哌嗪-1-基)-n4,n7-双(2-吗啉代乙基)蝶啶-4,7-二胺的药理学数据.拮抗剂/激动剂竞争性抑制在初步结果(即,进行中的一个测定结果-重复测定)中,执行拮抗剂相对于激动剂的交叉滴定以确定拮抗剂结合的形式。针对不同浓度的攻击激动剂,滴定从10um至4nm的jb6121。使用了小分子tlr7激动剂jb6011。下面的图(尽管是粗制的)暗示,jb6121对tlr7激动剂的抑制在性质上是竞争性的,因为随着激动剂剂量增加曲线的迹线是平行的。用于该实验的激动剂范围是在0.12至3.3μm之间或约30倍范围内。这些结果(尽管仅代表一个测定)似乎得到多种拮抗剂支持。与jb6121相比,用拮抗剂jb6140已经实现了一个可比较的结果,所述jb6140是一种相对于jb6011具有更高logd和更高效能的类似的拮抗剂分子(参见,图2a和2b)。体内药理学在体内试验了jb6121的tlr9敲减(knockdown)活性。用于ip注射的id50被确定为55.27μg注射剂量,且po管饲法是59.99μg递送剂量。这大致转换成对于25克小鼠2.4mg/kg剂量的id50。在t=0小时用不同剂量的试验拮抗剂处理小鼠。在1小时以后(t=1小时,对于ip组)和2小时以后(t=2小时,对于po组)施用激动剂处理(cpg-dna)。在激动剂处理后3小时、t=4小时(ip组)或t=5小时(po组)执行尸检。通过elisa测量由tlr激动剂诱导的血清细胞因子。每个剂量的组大小,n=3。绘制在不同血清稀释度的2个独立elisa的平均值±sd。还利用tlr7小分子激动剂jb6011作为激动剂攻击,在体内试验了jb6121的tlr7敲减活性。用于ip注射的id50被确定为98.34μg注射剂量,且po管饲法是286μg递送剂量,参见下面的图3a和3b。这大致转换成对于25克小鼠3.92mg/kgip剂量和11.44mg/kgpo剂量。cerep初步admet数据由cerep进行初步筛选测量。所有值落入可接受的限度内(表5)。根据lipinski,c.a.等人,1997,adv.drugdel.rev.,46:3-26,由cerep,seattle,wa执行溶解度测定。根据banker,m.j.等人,2003,j.pharm.sci.,92:967-974,由cerep,seattle,wa执行蛋白结合测定。根据hildalgo,i.j.,1998,gastroenterology,96:736-749,由cerep,seattle,wa执行渗透性测定。根据obach,r.s.等人,1997,j.pharmacol.exp.ther.,283:46-58,由cerep,seattle,wa执行代谢稳定性测定。根据polli,j.w.等人,2001,j.pharm.exp.ther.,299:620-628,由cerep,seattle,wa执行p-糖蛋白抑制测定。根据mosmann,t.,1983,j.immunol.met.65:55-62,由cerep,seattle,wa执行细胞生存力测定。根据mathes,c.,2006,expertopin.ther.targets,10:230-241,由cerep,seattle,wa执行herg自动化的膜片箝测定。表5.关于jb6121的体外admet数据.水溶性,pbs,ph7.4,μm>200μm水溶性,模拟的胃液,μm>200μm水溶性,模拟的肠液,μm194.9μmlogd,ph7.40.995蛋白结合,人血浆,%结合87%a-b渗透性,caco-2细胞,ph6.5/7.4,10-6cm/sec1.2p-糖蛋白,在100μm的%抑制1.0%代谢稳定性,在60min的人肝微粒体,%剩余75%细胞生存力,hep-g2细胞,在100μm的%抑制8.5%herg,自动化的膜片箝,在10μm的%抑制11.0%jb6121细胞色素p450抑制还针对cyp抑制试验了jb6121,参见下面表6。根据atkinson,a等人,2005,drugmetab.dispos.33:1637-1647,由cerep,seattle,wa执行测定。表6.细胞色素p450试验浓度平均%对照cyp1a210μm97.0cyp2b610μm58.2cyp2c810μm87.7cyp2c910μm46.7cyp2c1910μm92.9cyp2d610μm80.9cyp2e110μmntcyp3a4,bfc底物10μm94.1cyp3a4,bzres底物10μm104.8jb6121受体交叉反应性受体交叉反应性谱由71个结合和27个酶测定组成。结合测定组由大致相等数目的选择性的、中央的和周围的治疗上有关的靶标广泛地定义。酶测定组包括来自不同酶家族的最有代表性的靶标,特别聚焦于磷酸酶和参与细胞周期调节的特定酶。由cerep,seattle,wa执行测定,采用与cordeaux,y.等人,2004brit.j.pharmacol.,143:705-714类似的方案。对于大约100个受体和酶,在10μm试验了jb6121的受体交叉反应性。在下面在表7中突出显示了大于50%的任何%抑制(ic50<10μm)。表7以上数据暗示,jb6121可以能够阻断与m非选择性的毒蕈碱受体和comt的放射性配体结合。对于非选择性的毒蕈碱受体,活性最可能是ic50>5.0μm,且对于comt,非常接近10μm。jb6121药代动力学由charlesriverwilmingtonma在大鼠中执行药代动力学研究,且剂量是2mg/kgiv和10mg/kgpo,并测量全血水平72h。在下面在表8中给出了24h的计算的药代动力学参数。六(6)只雄性sprague-dawley大鼠选自试验机构(testingfacility)的啮齿动物群体。基于由试验机构兽医确定的可接受的健康和基于股骨和颈静脉导管的开放性,招选动物进入研究。在给药之前禁食至少16小时。还扣发食物,直到4小时时间点收集以后。将动物放入2个3只动物/组的组中。组1中的每只动物通过静脉内剂量施用以2mg/kg的靶剂量水平和以1ml/kg的剂量体积接受制备的jb6121。在静脉内给药以后,立即用0.5ml盐水冲洗内置导管。组2中的每只动物通过经口管饲法剂量施用以10mg/kg的靶剂量水平和以10ml/kg的剂量体积接受制备的jb6121。在给药过程中和在所有样品收集时间点,观察动物任何临床上有关的异常;没有注意到异常。通过颈静脉导管从每只动物收集全血样品(0.300ml;k2edta抗凝血)。在给药后30分钟和1、2、4、6、12、24、48和72小时,从所有动物收集全血样品。将全血样品转移至charleriverbioanalyticalscienceslaboratory,wilmingtonma用于分析。使用与iv或po施用途径一致的非房室方案,使用watson药代动力学软件(versionno.7.2)估计药代动力学参数。表8.jb6121pk/pd该研究的目的是收集odncpg1668施用以后的血清和确定给sprague-dawley大鼠口服施用7天以后jb6121的药代动力学。使用血清il-12作为监测的细胞因子,在大鼠中进行预试验以确立tlr9配体的适当激动剂(cpgdnaodn1668)剂量,组1-3,参见表6。在施用odncpg1668以后3小时,从每只动物末端收集血清全血样品。通过elisa确定血清il-12,数据未显示。选择1mg/kg的激动剂剂量用于下一研究阶段。对于施用jb6121的组(组4-7),针对基础/盐组分校正制剂,且不针对纯度进行校正。在剂量施用的第一天,使用无菌pbs至调节的靶剂量浓度制备jb6121制剂,使用0.8265的因数来校正盐含量。如下表9中所述执行给药。表9.实验设计ip=腹膜内,po=经口管饲法a给组1-3施用并收集血清样品进行分析,然后给组4-7进行剂量施用。这些血清数据用于指定odncpg1668制剂的剂量(和浓度)(组4-7)。b将调节仅应用于jb6121制剂。通过0.8265的因数调节剂量浓度以校正盐含量。将动物分配至四组(组4-7),并通过经口管饲法每天一次以10mg/ml的体积施用0.39、1.56、6.25或25mg/kg的jb6121持续7天。在第7天,在jb6121施用(接近cmax)以后2小时,以1ml/kg的体积以1mg/kg作为单个ip剂量施用odncpg1668。在t=2、3、4和5h,通过尾静脉出血或通过心脏穿刺在末端收集用于生物分析的全血样品和用于血清细胞因子分析的血清样品。在下面表10中呈现了关于jb6121的生物分析测量的结果。表10.jb6121在sprague-dawley大鼠中的平均全血浓度.在激动剂攻击后3小时监测血清il-12作为药效动力学jb6121活性的量度,参见图4。7-天暴露后的表观id50是大约11ng*h/mlauc或大致0.5mg/kg剂量。考虑到大约2倍的7-天积累(参见7天毒物动力学量度相对于24hpk全血暴露)和大鼠与小鼠之间2的异速生长定标(如果合适),该值与在体内tlr9敲减测定(上面第4.2部分,体内药理学)中确定的2.4mg/kgid50大致相关。这将导致相对于1-天小鼠在7-天大鼠中大4倍(0.5mg/kg相对于2.4mg/kg)的预期活性。但是,由于在0.4mg/kg剂量处全血暴露的强可变性,人们可以简单地声称,在该研究中在1.56mg/kg剂量实现>80%的tlr9抑制。1.56mg/kg剂量导致第7个剂量后10.9ng/mljb6121的平均cmax血液暴露。我们还使用多路分析来测量血清样品中的另外细胞因子和趋化因子。所述测量递送mip-1a、mip-2、mcp-1和ip-10的结果。ip-10产生id50的最高量估计,≈2.8mg/kg,与上面详述的il-12elisa结果合理一致。jb6121毒理学遗传毒性根据maron,d.m.和ames,b.n.,1983,mutationres.,113:173-215,由biorelienceinc,md执行非-glpames试验研究。在5个细菌菌株(含或不含s9级分)中执行试验至5000μg。心血管由cyprotecinc.在它的watertown,ma实验室中进行herg测定。试验的浓度范围是0.0096-30μm。没有观察到浓度依赖性的抑制,ic50>30μm。herg抑制测定使用高通量单个细胞平坦膜片箝方案。将用herg基因转染的中国仓鼠卵巢细胞(cho-herg)分配在patchplate中。使用两性霉素作为穿孔剂以获得向细胞的电通道。在通过穿孔的膜片箝加入试验化合物之前,测量herg尾电流。加入试验化合物(n=4个细胞/浓度,最终的dmso浓度=0.25%)以后,执行herg电流的第二次记录。将复合后herg电流表达为复合前herg电流的百分比(%对照电流),并相对于每种化合物的浓度绘图。在观察到浓度依赖性的抑制的情况下,使用hill方程式将s形线拟合至数据并确定ic50(观察到50%抑制时的浓度)。根据haverkamp,w.等人,2000,eurheartj.,21:1216-1231,kiss,l.等人,2003,assaydrugdev.technol.,1:127-135和schroeder,k.等人,2003,j.biomolscreen,8:50-64执行测定。体内毒性在大鼠中执行7-天非-glp毒性研究。给药是通过经口管饲法每天1次。存在4个剂量组:0、10、30和100mg/kg。在该研究中评价了下述参数和端点:临床征象、体重、体重变化、食物消耗、临床病理学参数(血液学、凝固、临床化学和尿分析)、毒物动力学参数、肉眼尸检发现、器官重量和组织病理学检查。对死亡率、临床观察、体重、体重变化、食物消耗、血液学参数、凝固参数、临床化学参数、尿分析参数或肉眼尸检观察不存在试验物相关的效应。相对于脾重量,当在雄性中测量绝对脾重量(p=0.444)、体重的%脾(p=0.278)或脑重量的%脾(p=0.502)时,剂量组之间的平均值的差异不是统计上不同的。但是,存在平均脾重量随着剂量增加而增加的趋势。在≥30mg/kg/天雄性中脾重量的剂量相关的增加与在≥30mg/kg/天时增加的血细胞生成发生相一致。在100mg/kg/天还存在雄性的肝脏中的血细胞生成的轻微增加。增加的血细胞生成经常是适应性的(非不利的)应答,其在除去起始刺激以后复原。但是,因为在检查的有限组织中没有观察到可以引发这样的应答的变化,不可排除这是jb6121的直接作用的可能性。在10、30和100mg/kg/天的水平,在大鼠中较好地耐受每天1次口服施用jb6121持续7天。在≥30mg/kg/天,雄性中的平均脾重量增加了至少10%,这与脾中增加的血细胞生成相一致。因为增加的血细胞生成对血液学参数、肝酶或脾或肝组织不存在明显的不良作用,认为没有观察到不利作用水平(noael)为100mg/kg/天(对于雄性和雌性),而认为没有观察到作用水平(noel)在雄性中为10mg/kg/天且在雌性中为100mg/kg/天。毒物动力学结果tk动物中的临床征象和体重变化通常类似于主要毒理学阶段动物。选择来自第1和7天的毒物动力学参数并包括在下面表11中。表11.毒物动力学参数的总结-第1天表12.毒物动力学参数的总结-第7天当剂量从10mg/kg增加至100mg/kg时,在第1天和第7天观察到cmax和auc的超过剂量比例增加。在第1天,剂量的10倍增加导致雄性和雌性cmax分别增加32倍和43倍以及雄性和雌性auc0-24h分别增加59倍和113倍。类似地,在第7天,剂量的10倍增加导致雄性和雌性cmax分别增加24倍和20倍以及雄性和雌性auc0-24h分别增加48倍和38倍。全身暴露的不成比例增加可能是由于“首过”代谢的饱和和/或胃肠道、肝细胞和/或肾小管细胞(取决于消除的途径)中的流出转运蛋白的抑制。每天口服施用7-天以后,jb6121在所有3个剂量以后积累在全血中,具有1.71的平均d7/d1cmax比率和2.79的auc0-24h比率;但是,由于jb6121的半衰期和每天1次给药预见到一些或所有积累。存在这样的趋势:雄性大鼠具有与雌性大鼠相比稍微更高的cmax和auc0-24h,这与iv施用以后更低的清除率一致。由于当经口剂量从10mg/kg增加至100mg/kg时auc0-24h的超过剂量比例增加,在第1天计算的经口绝对生物利用度(假定iv施用以后的剂量比例是在5mg/kg至100mg/kg之间)是剂量依赖性的,10、30和100mg/kg的剂量以后平均值分别为13.3%、28.0%和78.5%。汇集的7-天全血暴露数据如果人们汇集来自pk/pd研究和毒物动力学研究的7-天暴露数据,将cmax相对于剂量绘图会产生在0-30mg/kg施用剂量之间的剂量比例线性曲线。所述线具有0.986的相关系数和28.24ng/ml/mg/kg的斜率。100mg/kg剂量与以前的较低剂量30mg/kg没有2.36的因数的剂量比例,且没有描绘。将cmax用于该分析,因为auc在研究之间不是可比较的(由于在pk/pd研究中较短的血液取样持续时间)(参见,图5)。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1