一种多维串联凝胶电泳系统、电泳方法及试剂盒与流程
本发明属于蛋白凝胶电泳分离领域,具体涉及了一种多维串联凝胶电泳系统、电泳方法及试剂盒。
背景技术:
聚丙烯酰胺凝胶是电泳分离蛋白质的经典支持介质,聚合反应前,通过调节丙烯酰胺和n,n'甲叉双丙烯酰胺单体的浓度比,形成具有不同程度交链结构、网孔大小和形状的高分子聚合物,施加直流电压后,具有不同分子量和电荷的蛋白质具有不同的泳动速度因而在聚丙烯酰胺凝胶上得以分离。
现有的凝胶电泳技术中,通过等电点聚焦技术首先按照电荷进行第一维分离,再采用十二烷基磺酸钠-聚丙烯酰胺凝胶电泳按照蛋白质的质量差异进行第二维分离。常规等电点聚焦和聚丙烯胺酰胺凝胶电泳的缺点主要表现在六个方面:(1)等电点聚焦不适合于碱性或酸性蛋白,进行等电点聚焦需要价格昂贵的胶条和特殊仪器;(2)现有聚丙烯酰胺凝胶的结构单一,只有丙烯酰胺和n,n'甲叉双丙烯酰胺两种单体,因此制备的凝胶性质单一,仅仅只靠网孔大小和形状进行分离,不能满足分析复杂蛋白质混合物的需求;(3)不适合于碱性蛋白的分离,现有催化剂过硫酸铵aps和temed只能再碱性条件下引发聚合反应,而碱性蛋白在碱性条件下溶解度降低,容易产生沉淀。碱性蛋白质通常溶解于酸性溶液,但是aps和temed在酸性条件下发生质子化,降低了引发丙烯酰胺聚合反应的能力,导致聚合不完全、聚合时间长、制得的凝胶弹性差等缺点;(4)对具有相似结构和分子量的蛋白质分离能力差,特别不适合于组蛋白的分离;(5)对具有不同翻译后修饰的蛋白质异构体分离能力差。以碱性组蛋白为例,由于大量翻译后修饰的存在,其不同异构体的分子量非常相似,这使得常规聚丙烯酰胺凝胶电泳只能分离得到有限的几条蛋白质带;(6)常规聚丙烯酰胺凝胶电泳结束后所使用的固定液和脱色液不适合于碱性蛋白,因为酸性的固定液和脱色液使碱性蛋白流失。
技术实现要素:
本发明针对现有技术中存在的不足,目的在于提供一种用于分离碱性蛋白的多维串联凝胶电泳系统、电泳方法及试剂盒,实现对生物样品中碱性蛋白的分离和质谱鉴定。
为实现上述发明目的,本发明所采用的技术方案为:
一种用于分离碱性蛋白的多维串联凝胶电泳系统,包括:第一维tio2-聚丙烯酰胺复合凝胶电泳、第二维n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶电泳和第三维固定化zr4+聚丙烯酰胺凝胶电泳;所述多维串联凝胶电泳系统的电泳凝胶是由tio2-聚丙烯酰胺复合凝胶、n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶、固定化zr4+聚丙烯酰胺凝胶和样品浓缩胶依次填充于电泳槽内制备所得。
上述方案中,所述tio2-聚丙烯酰胺复合凝胶由如下方法制备得到,具体包括:
(1)凝胶制备液的配制:将尿素、60%丙烯酰胺/0.4%n,n’-亚甲双丙烯酰胺、冰醋酸、蒸馏水以及10%(体积浓度)tritonx-100溶液混合均匀后,加入锐钛矿型纳米tio2,漩涡混合均匀,使纳米颗粒均匀地分散在溶液中;
(2)tio2-聚丙烯酰胺复合凝胶的制备:将步骤(1)配制的凝胶制备液灌入凝胶槽两片玻璃之间的空隙中,使其高度为凝胶槽总高度的1/3,避免产生气泡;利用波长为365nm的紫外灯照射使聚合反应进行完全,待凝胶制备液凝固,得到用于第一维tio2-聚丙烯酰胺复合凝胶电泳的tio2-聚丙烯酰胺复合凝胶。
上述方案中,所述n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶由如下方法制备得到,具体包括:
(1)凝胶制备液的配制:将尿素、30%丙烯酰胺和30%n-羟乙基丙烯/0.4%n,n’-亚甲双丙烯酰胺、冰醋酸、蒸馏水以及10%tritonx-100溶液混合均匀后,加入锐钛矿型纳米tio2,漩涡混合均匀,使纳米颗粒均匀地分散在溶液中;
(2)n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶的制备:将步骤(1)配制的凝胶制备液灌入凝胶槽内、tio2-聚丙烯酰胺复合凝胶之上,使其高度为凝胶槽总高度的1/3,避免产生气泡,利用波长为365nm的紫外灯照射使聚合反应进行完全,待凝胶制备液凝固,制得用于第二维n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶电泳的n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶。
上述方案中,所述固定化zr4+聚丙烯酰胺凝胶由如下方法制备得到,具体包括:
(1)螯合zr4+的新型单体的制备:将腺嘌呤核苷三磷酸二钠盐(atpna2)、烯丙基缩水甘油醚(age)加入到蒸馏水中,于40℃条件下搅拌3小时,得到能够螯合zr4+的单体;
(2)凝胶制备液的配制:将尿素、60%丙烯酰胺/0.4%n,n’-亚甲双丙烯酰胺、冰醋酸、蒸馏水以及10%tritonx-100溶液混合均匀后,加入zrcl4溶液,漩涡混合均匀,再加入步骤(1)所得螯合zr4+的新型单体,混合均匀后依次加入10wt%过硫酸铵和四甲基二乙胺;
(3)固定化zr4+聚丙烯酰胺凝胶的制备:将步骤(2)配制的凝胶制备液灌入凝胶槽内、n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶之上,高度为凝胶槽总高度的1/6,避免产生气泡,待凝胶制备液凝固后,得到用于固定化zr4+聚丙烯酰胺凝胶电泳的固定化zr4+聚丙烯酰胺凝胶;
上述方案中,所述样品浓缩胶由如下方法制备得到,具体包括:
(1)凝胶制备液的配制:将尿素、60%丙烯酰胺/0.4%n,n’-亚甲双丙烯酰胺、冰醋酸、蒸馏水以及10wt%过硫酸铵和四甲基二乙胺,漩涡混合均匀;
(2)样品浓缩凝胶的制备:将步骤(1)配制的凝胶制备液灌入凝胶槽内、固定化zr4+聚丙烯酰胺凝胶之上,使其淹没整个凝胶槽,小心插入干净的配套梳子,避免气泡的产生,待凝胶制备液充分凝固,取出梳子,得到样品浓缩凝胶。
一种用于分离碱性蛋白的多维串联凝胶电泳分离方法,包括如下步骤:
(1)配制样品缓冲溶液;配制辅助样品缓冲液;配制电泳液;
(2)将待分析蛋白质溶解于样品缓冲溶液中得到待测样品液,所述待测样品液中待分析蛋白质的浓度为5μg/μl;再将辅助样品缓冲液与待测样品液按比例混合后得到混合液;
(3)将所述电泳凝胶置于电泳槽内,加入电泳液,再将步骤(2)所得混合液加样到电泳凝胶的泳道内,施加直流电压,进行电泳分离;
(4)电泳分离结束后,取出凝胶,进行coomassieblue染色、脱色;
(5)将电泳分离所得蛋白胶条切下,用胰蛋白酶切,利用质谱分析并搜索蛋白质数据库,鉴定分离所得碱性蛋白。
用于上述多维串联凝胶电泳分离方法的试剂盒,包括:
(1)螯合zr4+新型单体,其各组分的配比为:蒸馏水、腺嘌呤核苷三磷酸二钠盐(atpna2)、烯丙基缩水甘油醚(age)的比值为20ml:1g:190μl;
(2)tio2-聚丙烯酰胺复合凝胶,其各组分配比为:尿素、60%丙烯酰胺/0.4%n,n’-亚甲双丙烯酰胺、冰醋酸、蒸馏水、10%(体积浓度)tritonx-100溶液和锐钛矿型纳米tio2的比值为3.6g:2.5ml:500μl:3.73ml:370μl:10mg;
(3)n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶,其各组分的配比为:尿素、30%丙烯酰胺和30%n-羟乙基丙烯/0.4%n,n’-亚甲双丙烯酰胺、冰醋酸、蒸馏水、10%(体积浓度)tritonx-100溶液和锐钛矿型纳米tio2的比值为3.6g:2.5ml:500μl:3.73ml:370μl:10mg;
(4)固定化zr4+聚丙烯酰胺凝胶,其各组分的配比为:尿素、60%丙烯酰胺/0.4%n,n’-亚甲双丙烯酰胺、冰醋酸、蒸馏水、10%(体积浓度)tritonx-100溶液、1mol/l的zrcl4溶液、螯合zr4+新型单体100μl、10wt%过硫酸铵溶液和四甲基二乙胺的比值为1.8g:1.25ml:250μl:1.86ml:186μl:10μl:100μl:140μl:30μl;
(5)样品浓缩胶,其各组分的配比为:尿素、60%丙烯酰胺/0.4%n,n’-亚甲双丙烯酰胺、冰醋酸、蒸馏水、四甲基二乙胺和10wt%过硫酸铵溶液的比值为1.8g:0.5ml:250μl:2.8ml:30μl:140μl;
(6)样品缓冲溶液,其各组分的配比为:尿素、冰醋酸、0.2%pyroniny和纯净水的比值为0.36g:50μl:60μl:490μl;
(7)辅助样品缓冲溶液,配方为:浓度为4μg/μl的cuso4溶液;
(8)电泳液,配方为:体积浓度为5%的醋酸水溶液;
(9)coomassiebluer250染色液,其各组分的配比按质量百分比计为:甲醇50%、0.1%coomassiebluer250、碳酸氢铵0.5%和水49.4%;
(10)脱色液,各组分的配比按质量百分比计为:甲醇50%、nh4hco30.5%和水49.5%。
本发明的技术方案中,所述多维串联凝胶电泳系统和试剂盒应用于分离碱性组蛋白的电泳分离方法如下所述:对生物组织样品分析,先将生物组织用冰冷却的生理盐水洗去血液,剪碎后放入玻璃匀浆器,加入酶抑制剂和核分离试剂b并在冰上匀浆,离心(500g,4℃,20min)后用不含np40的核分离试剂a清洗直到无血色,分离得到的细胞核用0.2m硫酸溶液抽提,加入三氯乙酸沉淀蛋白质,离心后用冰丙酮洗涤,然后冷冻干燥。将蛋白冻干粉溶解于本发明配制的样品缓冲溶液,蛋白混合物采用本发明多维串联凝胶电泳系统进行分离,然后再用质谱鉴定所分离的蛋白异构体。当所述生物样品为小鼠大脑组织,所述的核分离试剂a包括15mmtris-hcl、60mmkcl、11mmcacl2、5mmnacl、5mmmgcl2、250mm蔗糖、1mmdtt、10mm丁酸钠、0.02%nan3,用naoh调ph至7.4。所述的核分离试剂b的配制方法:在10ml核分离试剂a中加np-40,使其浓度为0.3%,并加入酶抑制剂。
本发明的有益效果:
(1)本发明所述多维串联凝胶电泳系统可采用常规十二烷基磺酸钠-聚丙烯酰胺凝胶电泳系统的直流电源和电泳槽进行相关凝胶电泳实验,使用简单,操作方便;本发明所述试剂盒绿色环保、安全实用、配制简单、保存容易、成本较低;其中的染色剂更加适合碱性蛋白,可减少洗涤过程中碱性蛋白的流失;
(2)本发明所述多维串联凝胶电泳分离方法适用于碱性蛋白质混合物的分离,分离效果好,质量稳定;整个操作过程简单,一步完成,电泳电压容易控制,三维电泳分离连续进行,中间无需进行样品转移;与下游质谱鉴定相容,干扰较小;适用于大规模蛋白质组的研究,特别适用于碱性组蛋白异构体的分离,便于质量控制和产业化。
(3)与现有等电点聚焦-十二烷基磺酸钠聚丙烯酰胺二维凝胶电泳相比,本发明所述多维串联凝胶电泳系统适用于碱性蛋白,克服了聚丙烯酰胺凝胶结构单一的缺点;本发明中,首先利用zr4+与磷酸化基团的相互作用增强对磷酸化修饰蛋白的分离效果;然后利用n-羟乙基丙烯酰胺与丙烯酰胺和n,n’-亚甲双丙烯酰胺共聚物增强了不同性质蛋白质之间的分离效果;最后在酸性条件下、利用半导体纳米颗粒二氧化钛在紫外光照射下产生的oh自由基引发丙烯酰胺和n,n’-亚甲双丙烯酰胺的聚合反应,使聚合反应更加完全,克服了过硫酸铵和四乙基二胺在酸性条件下质子化所引起的聚合不完全缺点,而且纳米二氧化钛的存在还增强了凝胶的强度和弹性以及对磷酸化修饰蛋白的分离效果;利用本发明所述电泳系统,当施加直流电压时,不同蛋白质异构体在酸性条件下进行分离,蛋白质携带的电荷、大小、形状和翻译后修饰的差异均对分离效果产生影响,大大提高了对相似蛋白异构体的分辨能力,克服了等电点聚焦容易发生蛋白质沉淀以及对碱性蛋白分析的局限性。
附图说明
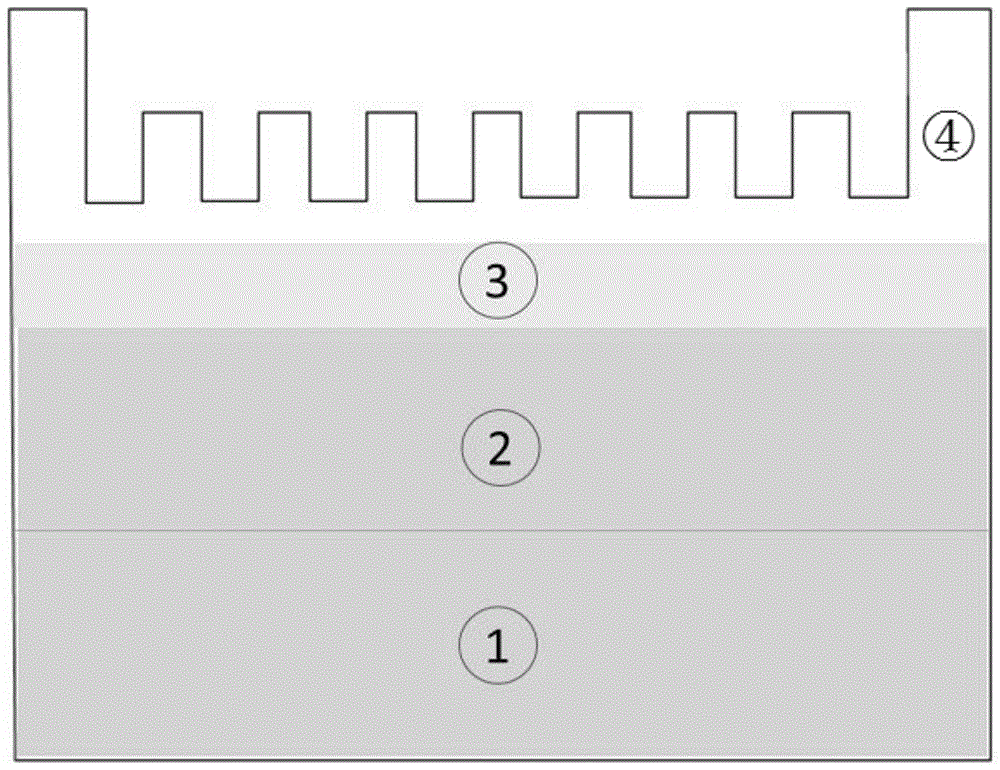
图1是多维串联凝胶的串联方式,其中①为tio2-聚丙烯酰胺复合凝胶,②为n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶,③为固定化zr4+聚丙烯酰胺凝胶电泳,④为样品浓缩胶。
图2是具有螯合zr4+能力的新型单体结构及制备工艺。
图3是实施例1所得电泳图,其中(a)是采用常规聚丙烯酰胺凝胶电泳获得的电泳图,其中左边是酪蛋白,右边是去磷酸化酪蛋白;(b)是采用本发明所述三维串联凝胶电泳系统电泳后得到的电泳图,其中左边是酪蛋白,右边是去磷酸化酪蛋白。
图4是实施例2所得的高分辨多维串联凝胶电泳图,图中从左到右表示不同发育时期的小鼠大脑组蛋白异构体。
图5是实施例2中经多维串联凝胶电泳分离后,切下其中一个蛋白质条带(小鼠大脑组蛋白)的典型质谱图。
具体实施方式
为了更好地理解本发明,下面结合实施例进一步阐明本发明的内容,但本发明的内容不仅仅局限于下面的实施例。
以下实施例中,用于分离碱性蛋白的多维串联凝胶电泳系统,包括:第一维tio2-聚丙烯酰胺复合凝胶电泳、第二维n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶电泳和第三维固定化zr4+聚丙烯酰胺凝胶电泳;所述多维串联凝胶电泳系统的电泳凝胶是由tio2-聚丙烯酰胺复合凝胶、n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶、固定化zr4+聚丙烯酰胺凝胶和样品浓缩胶依次填充于电泳槽内制备所得。
所述tio2-聚丙烯酰胺复合凝胶由如下方法制备得到,具体包括:
(1)凝胶制备液的配制:将尿素3.6g、60%丙烯酰胺/0.4%n,n’-亚甲双丙烯酰胺2.5ml、冰醋酸500μl、蒸馏水3.73ml以及10%(体积浓度)tritonx-100溶液370μl混合均匀后,加入锐钛矿型纳米tio210mg,漩涡混合均匀,使纳米颗粒均匀地分散在溶液中;
(2)tio2-聚丙烯酰胺复合凝胶的制备:将步骤(1)配制的凝胶制备液灌入凝胶槽两片玻璃之间的空隙中,使其高度为凝胶槽总高度的1/3,避免产生气泡;将波长为365nm的紫外灯放置在距离10cm处,照射大约20分钟,使聚合反应进行完全,待溶液凝固,制得tio2-聚丙烯酰胺复合凝胶。
所述n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶由如下方法制备得到,具体包括:
(1)凝胶制备液的配制:将尿素3.6g、30%丙烯酰胺和30%n-羟乙基丙烯/0.4%n,n’-亚甲双丙烯酰胺2.5ml、冰醋酸500μl、蒸馏水3.73ml以及10%tritonx-100溶液370μl混合均匀后,加入锐钛矿型纳米tio210mg,漩涡混合均匀,使纳米颗粒均匀地分散在溶液中;
(2)n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶的制备:将步骤(1)配制的凝胶制备液灌入凝胶槽内、tio2-聚丙烯酰胺复合凝胶之上,使其高度为凝胶槽总高度的1/3,避免产生气泡,将波长为365nm的紫外灯放置在距离10cm处,照射大约20分钟,使聚合反应进行完全,待溶液凝固,制得n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶。
所述固定化zr4+聚丙烯酰胺凝胶由如下方法制备得到,具体包括:
(1)螯合zr4+的新型单体的制备:将腺嘌呤核苷三磷酸二钠盐(atpna2)1g、烯丙基缩水甘油醚(age)190μl加入到20ml蒸馏水中,于40℃条件下搅拌3小时,得到能够螯合zr4+的单体;
(2)凝胶制备液的配制:将尿素1.8g、60%丙烯酰胺/0.4%n,n’-亚甲双丙烯酰胺1.25ml、冰醋酸250μl、蒸馏水1.86ml以及10%tritonx-100溶液186μl混合均匀后,加入zrcl4溶液10μl,漩涡混合均匀,再加入步骤(1)所得螯合zr4+的新型单体100μl,混合均匀后依次加入10wt%过硫酸铵140μl和30μl四甲基二乙胺;
(3)固定化zr4+聚丙烯酰胺凝胶的制备:将步骤(2)配制的凝胶制备液灌入凝胶槽内、n-羟乙基丙烯酰胺-丙烯酰胺共聚凝胶之上,使其高度为凝胶槽总高度的1/6,避免产生气泡,待凝胶制备液凝固后,得到固定化zr4+聚丙烯酰胺凝胶。
所述样品浓缩胶由如下方法制备得到,具体包括:
(1)凝胶制备液的配制:将尿素1.8g、60%丙烯酰胺/0.4%n,n’-亚甲双丙烯酰胺0.5ml、冰醋酸250μl、蒸馏水2.8ml以及10wt%过硫酸铵30μl和四甲基二乙胺140μl,漩涡混合均匀;
(2)样品浓缩凝胶的制备:将步骤(1)配制的凝胶制备液灌入凝胶槽内、固定化zr4+聚丙烯酰胺凝胶之上,使其淹没整个凝胶槽,小心插入干净的配套梳子,避免气泡的产生,待凝胶制备液充分凝固,取出梳子,得到样品浓缩凝胶。
实施例1
酪蛋白和去磷酸化酪蛋白的电泳分离和质谱鉴定,首先进行多维串联凝胶电泳,操作步骤依次如下:
(1)酪蛋白和去磷酸化酪蛋白的样品制备:将标准样品分别溶解于样品缓冲溶液,该样品缓冲溶液呈酸性,可使样品中碱性氨基酸残基质子化,从而使样品带上正电荷;样品缓冲溶液的组成成分为:尿素(0.36g),冰醋酸(50μl),0.2%pyroniny(60μl)和纯净水490μl,使其浓度大约为5μg/μl;
(2)将步骤1)所得样品溶液与辅助样品缓冲溶液按照1:1进行混合,辅助样品缓冲溶液的组成成分为cuso4(4μg/μl);
(3)将电泳液(体积浓度为5%的醋酸水溶液)加入到多维串联凝胶电泳系统,将步骤(2)所得加入到多维串联凝胶电泳系统的电泳凝胶的泳道内,施加直流电压,蛋白质在多维串联凝胶不同区域的泳动速度与蛋白质和凝胶性质有关,电荷、大小、形状和修饰差异等因素均影响其泳动速度,样品首先在30v下运行0.5小时,等待样品浓缩成一直线后,在100v下运行135分钟;
(4)将步骤(3)所得电泳图进行拷蓝染色,具体步骤是将凝胶取出后放入染色液,染色液的用量以完全浸泡凝胶为准,染色液的组成成分为:甲醇(50%)、0.1%coomassiebluer250、碳酸氢铵(0.5%)和水(49.4%),在震荡摇床上染色1-2小时;
(5)将步骤(4)所得凝胶进行脱色,具体步骤是将凝胶取出后放入脱色液,脱色液的用量以完全浸泡凝胶为准,脱色液的组成成分为:甲醇(50%)、nh4hco3(0.5%)和水(49.5%),在震荡摇床上脱色1-2小时。
将步骤(5)所得凝胶取出,扫描,图像如图3(b)所示,其中图3(a)为常规聚丙烯酰胺凝胶电泳对照。由图3可见,酪蛋白去磷酸化的程度并不相同,不同程度去磷酸化的酪蛋白异构体在本发明所述多维串联凝胶电泳系统中得到了高分辨分离。
实施例2
小鼠大脑组蛋白的分离和质谱鉴定,复杂蛋白混合物首先在本发明所述多维串联凝胶电泳系统上按照不同性质进行分离,然后利用质谱鉴定电泳分离后的蛋白条带,具体操作步骤依次如下:
(1)重复实施例1操作步骤(1)至(5),将步骤(5)所得凝胶取出,扫描,图像如图4所示;
(2)将多维串联凝胶电泳分离所得凝胶取出,并切下相关泳道;
(3)将步骤(2)所得蛋白胶条用胰蛋白酶进行胶内胰蛋白酶解,提取出的肽段采用maldi-ms进行分析,所得质谱图如图5所示。
图4和图5的结果说明了:本发明所述多维串联凝胶电泳分离方法特别适用于碱性组蛋白异构体的分离,分离效果好,质量稳定;整个操作过程简单,一步完成,电泳电压容易控制,三维电泳分离连续进行,中间无需进行样品转移;与下游质谱鉴定相容,干扰较小。
显然,上述实施例仅仅是为清楚地说明所作的实例,而并非对实施方式的限制。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而因此所引申的显而易见的变化或变动仍处于本发明创造的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!