从辣椒植物体分离的PseudozymachurashimaensisRGJ1菌株及其用途的制作方法
本发明涉及:pseudozymachurashimaensisrgj1菌株,其从辣椒植物
背景技术:
目前,主要用于抑制植物致病菌产生和防治植物致病菌的方法是使用化学合成的农药。然而,这些合成农药破坏生态系统,并且由于其残留物而导致人中毒问题。因此,引起多种疾病(例如癌症、畸形等)的可能性非常高,并且因此其使用受到限制。因此,正在积极研究能够替代化学合成农药的环境友好型生物农药的开发。许多研究人员为解决化学防治方法的问题而已经尝试的方法之一是使用微生物的生物防治方法。由于最近消费者对食品安全的意识提高并且对环境友好型农产品的偏好迅速提高,已经研究了使用微生物的生物防治方法作为防治作物病害的化学防治方法的替代方案。
辣椒的重要病害包括炭疽病、白粉病、细菌斑点病和在地上部分中发生的病毒性病害,包括作为土壤感染性病害的辣椒晚疫病。这些被认为是威胁辣椒生产的经济上危重的病害。由于不仅辣椒的栽培时间长,而且根据天气的变化,辣椒病害的模式也非常不同。因此难以防治辣椒的病害。在这方面,辣椒是在栽培期期间经常用杀菌剂处理的作物之一。因此,为了产生环境友好的清洁辣椒,需要利用用于病害防治的微生物,其被选择以具有优异的病害防治作用。大多数为防治辣椒病害而开发的微生物已被开发用于防治辣椒晚疫病。普城沙雷菌(serratiaplymuthica)已被报道可有效地防治辣椒晚疫病(shen等,plantpathol,j.,21,64-67,2005)。然而,很少有对辣椒之地上部分的病害具有优异防治作用的微生物的报道。
韩国专利申请公布no.2009-0105726公开了“防治红辣椒的细菌性斑点和炭疽病的巨大芽孢杆菌分离株22-5”。韩国专利申请公布no.2012-0075936公开了“从土壤分离的芽孢杆菌属pb25菌株及其用途”。除原核细菌之外,上述专利文献未公开根据本发明的pseudozymachurashimaensisrgj1的真核酵母菌株,其从辣椒植物分离并且导致针对植物病原体或植物病毒的诱导性全身抗性。
技术实现要素:
[技术问题]
本发明源于上述需求。本发明通过确定从辣椒叶分离和鉴定的pseudozymachurashimaensis菌株rgj1导致针对辣椒植物的细菌病原体或植物病毒的诱导性全身抗性并因此具有植物病害防治作用而完成。
[技术方案]
在本发明的一个方面,提供了从辣椒植物分离的pseudozymachurashimaensis菌株rgj1,其中pseudozymachurashimaensisrgj1菌株导致针对植物病原体或植物病毒的诱导性全身抗性。
在本发明的另一个方面,提供了用于防治植物病害的微生物制剂,其中所述制剂包含pseudozymachurashimaensis菌株rgj1或其培养物作为活性成分。
在本发明的另一个方面,提供了用于提高植物产量的微生物制剂,其中所述制剂包含pseudozymachurashimaensis菌株rgj1或其培养物作为活性成分。
在本发明的另一个方面,提供了用于制备微生物制剂的方法,所述方法包括培养pseudozymachurashimaensis菌株rgj1。
在本发明的另一个方面,提供了用于防治植物病害的方法,所述方法包括用pseudozymachurashimaensis菌株rgj1或其培养物对植物幼苗进行处理,其中所述处理包括浸渍处理、土壤浇灌处理或向地上叶上的喷洒处理。
[有益效果]
经确定,从辣椒叶分离和鉴定的本发明pseudozymachurashimaensis菌株rgj1导致针对辣椒植物的细菌病原体或植物病毒的诱导性全身抗性并因此具有植物病害防治作用。根据本发明的菌株可消除由化学农药的副作用引起的环境污染和由残留农药引起的人中毒的风险,并因此可用作生态友好的植物保护剂。根据本发明的菌株具有防治辣椒植物上感染性细菌和提高植物的病害抗性的作用,并因此可以是在工业上可用的。
附图说明
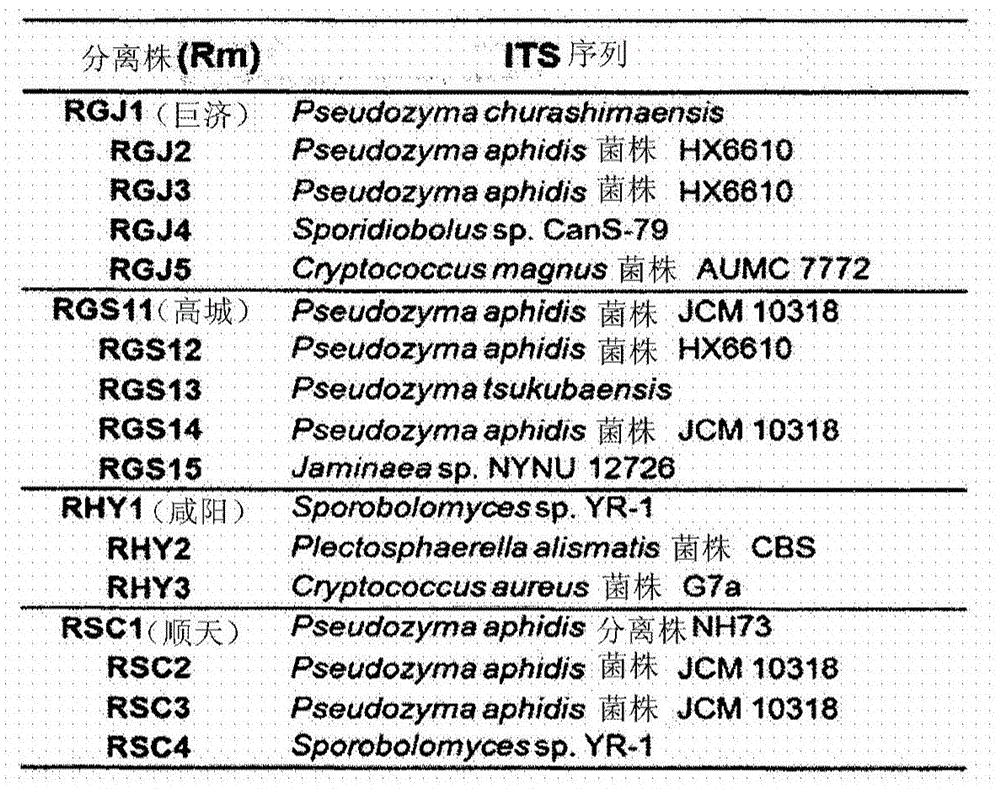
图1示出了为从辣椒分离活酵母而从取样区域分离的酵母物种。
图2示出了对在辣椒中存活的酵母菌株的诱导性抗性的初步分析的结果:rgj1:pseudozymachurashimaensis;rgj5:cryptococcusmagnus;gs5:pseudozymaaphidis;gs6:pseudozymatsukubaensis。
图3示出了对作为从辣椒分离的酵母菌株的rgj1的诱导性抗性的二次分析的结果。bth(苯并噻二唑):诱导性抗性阳性对照;卡那霉素:直接细菌杀伤剂(广谱抗生素)。
图4示出了检查经根据本发明的酵母rgj1在田地中处理的辣椒针对细菌性斑点病原体地毯草黄单胞菌辣椒斑点病致病变种(x.axonopodispv.vesicatoria)的诱导性抗性的结果。
图5示出了通过症状检查经根据本发明的酵母rgj1在田地中处理的辣椒针对病毒的诱导性抗性的结果。
图6示出了通过使用qrt-pcr对病毒进行量测量检查经根据本发明的酵母rgj1在田地中处理的辣椒针对病毒的诱导性抗性的结果。cmv:黄瓜花叶病毒(cucumbermosaicvirus);bbwv:蚕豆萎蔫病毒(broadbeanwiltvirus)。
图7示出了通过使用qrt-pcr对病毒进行量测量检查经根据本发明的酵母rgj1在田地中处理的辣椒针对病毒的诱导性抗性的结果。pepmov:辣椒斑驳病毒(peppermottlevirus);pmmov:辣椒轻微斑驳病毒(peppermildmottlevirus)。
图8示出了辣椒pr4和pr5的表达水平的分析结果,所述辣椒pr4和pr5作为与经根据本发明的酵母rgj1处理的辣椒在田地条件下针对病原体侵染的诱导性抗性相关的基因。
图9示出了通过在田地中用根据本发明的酵母rgj1进行处理的辣椒产量的提高。
图10示出了检测酵母rgj1在温室中定植于叶上之能力的结果。
具体实施方式
为了实现本发明的目的,提供了从辣椒植物分离的pseudozymachurashimaensisrgj1菌株,其中pseudozymachurashimaensisrgj1菌株导致针对植物病原体或植物病毒的诱导性全身抗性。pseudozymachurashimaensisrgjl于2016年6月24日保藏在韩国生命工学研究院
在根据本发明一个实施方案的菌株中,植物病原体或植物病毒可以是多种植物的病原体或病毒。优选地,在根据本发明一个实施方案的菌株中,植物病原体或植物病毒可以是但不限于辣椒植物病原体或辣椒植物病毒。植物病原体可以是细菌病原体,优选辣椒细菌性斑点的致病细菌。更优选地,细菌病原体可以是地毯草黄单胞菌辣椒斑点病致病变种(xanthomonasaxonopodispv.vesicatoria),但可以不限于此。辣椒植物病毒可包括黄瓜花叶病毒(cmv)、烟草花叶病毒(tmv)、蚕豆萎蔫病毒(bbwv)、菊花轻微斑驳病毒(cmmv)、马铃薯病毒y(pvy)、番茄斑萎病毒(tswv)、辣椒斑驳病毒(pepmov)、辣椒轻微斑驳病毒(pmmov)等。优选地,辣椒植物病毒可以是黄瓜花叶病毒(cmv)、蚕豆萎蔫病毒(bbwv)、辣椒斑驳病毒(pepmov)、辣椒轻微斑驳病毒(pmmov)等,但是可以不限于此。
在本发明的另一方面,提供了用于防治植物病害的微生物制剂,其中所述制剂包含pseudozymachurashimaensis菌株rgj1或其培养物作为活性成分。植物病害可由植物病原体或植物病毒引起。优选地,植物病害可由辣椒植物病原体或辣椒植物病毒引起。本发明不限于此。辣椒植物病原体或辣椒植物病毒如上所述。
用于防治植物病害的微生物制剂可包含pseudozymachurashimaensis菌株rgj1或其培养物作为活性成分,其中该菌株从辣椒植物分离,其中pseudozymachurashimaensis菌株rgj1导致针对植物病原体或植物病毒的诱导性全身抗性。根据本发明的微生物制剂可以以液体肥料形式制备。可通过向微生物制剂添加增量剂来以粉末形式使用微生物制剂。可配制微生物制剂并使其粒化。然而,制剂没有特别限制。换言之,在化学肥料供应有限的环境友好型有机农业中,可将微生物制剂配制成生物肥料以克服这样的限制。
在本发明的另一个方面,提供了用于提高植物产量的微生物制剂,其中所述制剂包含pseudozymachurashimaensis菌株rgj1或其培养物作为活性成分。植物可以是但不限于辣椒植物。当用根据本发明的菌株处理辣椒植物时,与未经处理的对照相比,辣椒果实产量提高约30%。
在本发明的另一个方面,提供了用于制备微生物制剂的方法,所述方法包括培养pseudozymachurashimaensis菌株rgj1。酵母菌株可通过本领域中已知的任何方法进行培养,并且可不限于特定方法。
在本发明的另一个方面,提供了用于防治植物病害的方法,所述方法包括用pseudozymachurashimaensis菌株rgj1或其培养物对植物幼苗进行处理,其中所述处理包括浸渍处理、土壤浇灌处理或者向地上叶或地下土壤上的喷洒处理。植物病害可由植物病原体或植物病毒引起。优选地,植物病害可由辣椒植物病原体或辣椒植物病毒引起。本发明不限于此。辣椒植物病原体或辣椒植物病毒如上所述。
用于防治植物病害的方法可包括用pseudozymachurashimaensis菌株rgj1、其培养物或使用该菌株的微生物制剂对植物幼苗进行处理,包括浸渍处理、土壤浇灌处理或向地上叶上的喷洒处理。在浸渍处理的情况下,可将培养基和微生物制剂倒入植物周围的土壤中,或者可将植物种子浸入培养基和制剂中。
在下文中,参照实施例对本发明进行详细说明。然而,本发明实施例仅是本发明的一些实例,并且本发明的内容不限于所呈现的实施例。
实施例1.在辣椒上存活的酵母菌株的分离
为了分离在辣椒中发挥有用作用并且在辣椒叶上存活的酵母,从忠清南道和全罗道收集辣椒叶。从2013年9月至11月,在巨济
此后,辣椒叶从全罗道、巨济、高城、咸阳、济南、南海、顺天的辣椒田收集。通过对来自收获的叶的分离的酵母进行测序来鉴定酵母。多种酵母在辣椒的叶上存活。其中,pseudozyma属的酵母占主导,并且其大量酵母在辣椒叶上存活(参见图1)。
实施例2.在辣椒中存活的酵母菌株的诱导性抗性的初步分析
为了确定分离的酵母的诱导性抗性能力,在温室中进行初步菌株选择实验。本发明人在50孔盆中种植了7日龄辣椒(新pr辣椒:弘农幼苗
在病原体接种之后7天检查症状。根据检查结果,pseudozymachurashimaensisrgj1酵母,即从巨济岛分离的酵母,显示出最优异的病害抗性作用。与水对照相比,该酵母处理显示出70%的症状减轻。这与作为阳性对照的化学bth对照显示出相同的显著性(参见图2)。
实施例3.从辣椒分离的酵母菌株的诱导性抗性的二次分析
对于作为在初步诱导性抗性测定中使用的数种分离的酵母菌株中最有效菌株的pseudozymachurashimaensisrgj1菌株,确定基于处理方法的变化的诱导性抗性差异。将在其中培养酵母rgj1的培养基调节至o.d.600=1。在与第一诱导性抗性实验相同的实验条件下,在将培养基喷洒在辣椒地上部分的叶面上时与在将培养物直接通过沟槽到土壤中进入辣椒根时之间比较抗性差异。作为阳性对照,使用诱导诱导性抗性的化学物质bth,并且作为阴性对照,使用水对照。实验在温室中进行。此外,为了确定酵母rgj1是否存在直接灭菌作用,将辣椒细菌性斑点病原体黄单胞菌(xav.)调节至o.d.600=0.5,并将黄单胞菌涂抹到直径为90mm的板中。然后,在板上布置直径为10mm的纸盘。然后,以相同的量用酵母rgj1(浓度调节至o.d.600=1,且量为20微升)、bth(1mm)、抗生素卡那霉素25和水进行处理。然后,将经处理的产物在30℃下培养。通过观察出现杀菌作用的透明区来比较其作用(参见图3)。
病害抗性以与初步抗性测试的结果类似的结果诱导。在对叶进行喷洒处理与直接土壤浇灌之间不存在作用差异。此外,根据置换培养的结果,在酵母rgj1周围没有透明环。因此确定,酵母rgj1不具有直接杀伤病原体的灭菌作用,而是具有诱导抗性的作用(参见图3)。
实施例4.如由用根据本发明的酵母rgj1在田地中处理辣椒诱导的针对细菌性斑点病原体的诱导性抗性的鉴定
对于通过在实验室和温室中进行鉴定选择的酵母菌株,在辣椒田中验证其诱导性抗性能力。验证测试在位于忠清南道锦山郡geonbuk-myeon,oebuli
根据田地测试结果,确定通过以与温室实验中相同的方式进行酵母喷洒处理诱导了抗性,并且细菌性斑点病害的症状减轻50%(参见图4)。
实施例5.经根据本发明的酵母rgj1在田地中处理的辣椒针对病毒的诱导性抗性的鉴定
从在室外田地实验中酵母处理之后已经过去60天的辣椒收集5个新鲜幼叶。将叶立即放入液氮中并迅速冷冻。此后,使用研钵将叶研磨。从经粉碎或研磨的叶中使用rna提取试剂盒(rneasy试剂盒;qiagen)提取rna。将提取的rna合成为cdna。使用qpcr(cfx连接实时系统;bio-rad)对合成的cdna进行rt-qpcr,作为用于量化病毒量的方法。
使用天然存在的cmv(黄瓜花叶病毒)和bbwv(蚕豆萎蔫病毒)特异性引物量化感染程度。使用的qpcr条件和引物如下。cmv包被蛋白正向:5′-cgttgccgctatctctgctat-3′(seqidno.:3),cmv包被蛋白反向:5′-ggatgctgcatactgacaaaca-3′(seqidno.:4),bbwv正向:5′-aatgaagtggtgctcaactacaca-3′(seqidno.:5),bbwv反向:5′-ttttggagcattcaaccatttgga-3′(seqidno.:6)。此外,使用pepmov(辣椒斑驳病毒)和pmmov(辣椒轻微斑驳病毒)特异性引物,量化感染程度。使用的qpcr条件和引物如下。pepmov:5′-aagatcagacacatgga-3′(seqidno.:7),pepmov反向:5′-caagcaagggtatgcatgt-3′(seqidno.:8),pmmov正向:5′-acagtttccagtgccaatca-3′(seqidno.:9),pmmov反向:5′-aagcgtctcggcagttg-3′(seqidno.:10)。
[表1]
qpcr条件
在病毒症状研究中,从在水对照和酵母处理之间比较辣椒新叶的结果确定,在水对照中,病毒症状严重,而在酵母处理中,症状较弱(参见图5)。此外,根据使用qpcr量化病毒的结果,对于代表性cmv和bbwv病毒二者,与水对照相比,在酵母处理中病毒量降低10倍。因此,确定,通过酵母处理,辣椒植物被较少的病毒感染(参见图6)。此外,对于这两种病毒pepmov和pmmov,发现,通过酵母处理,辣椒植物更不易受病毒感染(参见图7)。
实施例6.与经根据本发明的酵母rgj1处理的辣椒针对病原体侵染的诱导性抗性相关的基因的表达水平分析
为了研究用于研究酵母的作用机制的基因表达水平,在田地实验期间接种细菌性斑点病原体中,在以下三个时间点收集辣椒叶:①接种病原体之前、②接种病原体之后立即、③接种病原体之后6小时时。然后,将叶放入液氮中并在其中迅速冷冻。以与病毒量化方法中相同的方式,从叶中提取rna,并将rna合成为cdna。然后,使用qpcr检测与辣椒的诱导性抗性相关的基因的表达水平。具体地,确定作为与辣椒的诱导性抗性相关的代表性基因的pr基因的表达。qpcr的条件与上述病毒量化方法中相同。关于所使用引物的信息如下。capr4正向:5′-aactgggatttgagaactgccagc-3′(seqidno.:11),反向:5′-atccaaggtacatatagagcttcc-3′(seqidno.:12),capr5正向:5′-ctccacaagaaacaaggca-3′(seqidno.:13),反向:5′-gtacgaagcacgcacacaa-3′(seqidno.:14)。
在酵母处理中,抗性基因pr4和pr5的表达水平在6小时之后显著提高。这导致抗性引发效应,导致对病原体侵入的更快响应时间(参见图8)。
实施例7.基于根据本发明的酵母rgj1的处理的田地辣椒产量的研究
在确定田地中的诱导性抗性之后,研究了每个处理单元中20个辣椒植物的辣椒产量。这些调查总共重复四次。与未经处理的单元相比,在具有酵母rgj1处理的处理单元中,产量提高约30%(参见图9)。
实施例8.rgj1酵母在温室中留下的固定能力的鉴定
为了确定从辣椒叶分离的酵母菌株pseudozymachurashimaensisrgjl在叶上沉降的能力,本发明人在温室中对辣椒幼苗进行了实验。在发芽之后三周,将酵母悬液以两种浓度o.d.600=1和2接种在辣椒叶上。将其中含有分散的细菌的悬液以50ml喷洒在辣椒的地上部分上。此后,对叶进行取样。本发明人通过使用直径为10mm的木塞穿孔器进行冲孔获得三个叶盘。将盘形叶置于含有1ml经灭菌水的1.5ml管中。然后,使用珠充分地进行涡旋。将充分地涡旋的溶液以1/10浓度稀释。将经稀释的溶液以100微升涂抹在作为酵母专用培养基的ypd琼脂板上。计数由此产生的菌落的数目以测量cfu值。从喷洒当天(第0天)开始每10天进行取样(参见图10)。根据初始喷洒时的o.d.600值没有显著差异。确定了沉降在10mm叶盘上的酵母菌株从第0天开始在第20天至第30天的时间段内维持在104或更高计数。该结果表明,分离的酵母菌株在辣椒叶上生活良好。可认为104的密度是酵母菌株的最合适生长浓度。此外,当将酵母菌株喷洒在作物上时,酵母菌株由于其固定在叶上的优异能力而在叶中很好地存活,并且长时间保持作物的诱导性抗性。因此,作物对细菌性或病毒性病害具有抗性。
[登记号]
保藏机构名称:韩国生命工学研究院
登记号:kctc13051bp
保藏日期:2016年06月24日
<110>韩国生命工学研究院
<120>从辣椒植物分离的pseudozymachurashimaensisrgj1菌株及其用途
<130>pct1619
<160>14
<170>kopatentin2.0
<210>1
<211>20
<212>dna
<213>人工序列
<220>
<223>引物
<400>1
tccgtaggtgaaccttgcgg20
<210>2
<211>20
<212>dna
<213>人工序列
<220>
<223>引物
<400>2
tcctccgcttattgatatgc20
<210>3
<211>21
<212>dna
<213>人工序列
<220>
<223>引物
<400>3
cgttgccgctatctctgctat21
<210>4
<211>22
<212>dna
<213>人工序列
<220>
<223>引物
<400>4
ggatgctgcatactgacaaaca22
<210>5
<211>24
<212>dna
<213>人工序列
<220>
<223>引物
<400>5
aatgaagtggtgctcaactacaca24
<210>6
<211>24
<212>dna
<213>人工序列
<220>
<223>引物
<400>6
ttttggagcattcaaccatttgga24
<210>7
<211>17
<212>dna
<213>人工序列
<220>
<223>引物
<400>7
aagatcagacacatgga17
<210>8
<211>19
<212>dna
<213>人工序列
<220>
<223>引物
<400>8
caagcaagggtatgcatgt19
<210>9
<211>20
<212>dna
<213>人工序列
<220>
<223>引物
<400>9
acagtttccagtgccaatca20
<210>10
<211>17
<212>dna
<213>人工序列
<220>
<223>引物
<400>10
aagcgtctcggcagttg17
<210>11
<211>24
<212>dna
<213>人工序列
<220>
<223>引物
<400>11
aactgggatttgagaactgccagc24
<210>12
<211>24
<212>dna
<213>人工序列
<220>
<223>引物
<400>12
atccaaggtacatatagagcttcc24
<210>13
<211>19
<212>dna
<213>人工序列
<220>
<223>引物
<400>13
ctccacaagaaacaaggca19
<210>14
<211>19
<212>dna
<213>人工序列
<220>
<223>引物
<400>14
gtacgaagcacgcacacaa19
- 还没有人留言评论。精彩留言会获得点赞!