四种GypenosideL和GypenosideLI乙酰化衍生物及其制备抗肿瘤药物的用途的制作方法
本发明涉及四种由绞股蓝皂苷gypenosidel和gypenosideli乙酰化产生的化合物,以及这四种乙酰化衍生物在制备治疗肿瘤药物中的用途,属于中药现代化领域。
背景技术:
“绞股蓝”(gynostemmapentaphyllum(thunb.)makino.),为葫芦科绞股蓝属草质多年生攀援植物,壮族医学称为“国虾薄”,为我国中医及壮医常用药材[1]。其分布广泛,易于种植管理,在我国秦岭以南地区均可种植,以陕西,福建,广西,湖北居多。绞股蓝叶中具有丰富的与人参皂苷结构相似的绞股蓝皂苷成分,且一年内可多次采集,相对于人参而言,绞股蓝皂苷更加廉价易得,故其极具经济开发价值[2]。
经高温高压方法处理后,绞股蓝热处理产物与原植物相比,具有更强的抗肿瘤活性。热处理过程中产生了原药材中没有的gypenosidel和gypenosideli两种皂苷类化合物,并具有良好的抗肿瘤细胞活性[3]。不同肿瘤细胞所处环境不同对于药物分子的吸收效率不同,如脑部肿瘤由于血脑屏障的用对于脂溶性大的分子吸收效率更高,故对于有较强活性的抗肿瘤化合物而言,如何提高生物利用率成为现代药学研究的重点之一[4]。
利用乙酰化方法,产生的四种gypenosidel和gypenosideli乙酰化衍生物与gypenosidel和gypenosideli分子相比,具有更强的脂溶性,而仍保留抗肿瘤活性。乙酰化产生的gypenosidel和gypenosideli衍生物为抗癌药物提供了新的备选方案。
参考文献:
[1]梁启成,钟鸣.中国壮药学[m].广西民族出版社,2005.
[2]张涛,袁弟顺.中国绞股蓝种植资源研究进展[j].云南农业大学学报,2009,23(3):459-469.
[3]xiang-lanpiao,qianwu,jingyang,etal.dammarane-typesaponinsfromheat-processedgynostemmapentaphyllumshowfortifiedactivityagainsta549cells[j].archivesofpharmacalresearch,2013,vol.36(7):874-879.
[4]denoran,trapania,laquintanav,etal.recentadvancesinmedicinalchemistryandpharmaceuticaltechnology-strategiesfordrugdeliverytothebrain[j].currtopmedchem,2009,9:182-196.
技术实现要素:
本发明的目的在于合成四种gypenosidel和gypenosideli乙酰化衍生物,该乙酰化衍生物的制备方法,以及这四种乙酰化衍生物在制备治疗肿瘤药物中的用途。
本发明的四种gypenosidel和gypenosideli乙酰化衍生物的制备方法如下:
取gypenosidel和gypenosideli混合物,加入100倍量冰醋酸,105℃条件下加热3小时。将反应后的混合物减压浓缩,干燥得到gypenosidel和gypenosideli及其乙酰化衍生物的混合物。
所述的四种gypenosidel和gypenosideli乙酰化衍生物的分离及鉴定如下:
将干燥的gypenosidel和gypenosideli及其乙酰化衍生物的混合物用甲醇超声溶解后,过0.45μm微孔滤膜,通过半制备液相色谱分离。分离得到4个化合物,用nmr及ms技术手段,根据文献,最终被鉴定为6′-acetyl-gypenosidel、6′-acetyl-gypenosideli、4′-acetyl-gypenosidel、4′-acetyl-gypenosideli(表1、表2、附图1、附图2)。
表1.四种gypenosidel和gypenosideli乙酰化衍生物1hnmr数据表(600mhz,溶剂cd3od)
表2.四种gypenosidel和gypenosideli乙酰化衍生物13cnmr数据表(150mhz,溶剂cd3od)
我们还发现,本发明制备得到的四种化合物对于肝癌、肺癌、胃癌和前列腺癌细胞均具有抑制作用,因此,本发明还提供这四种化合物在制备治疗肿瘤药物中的用途。
附图说明
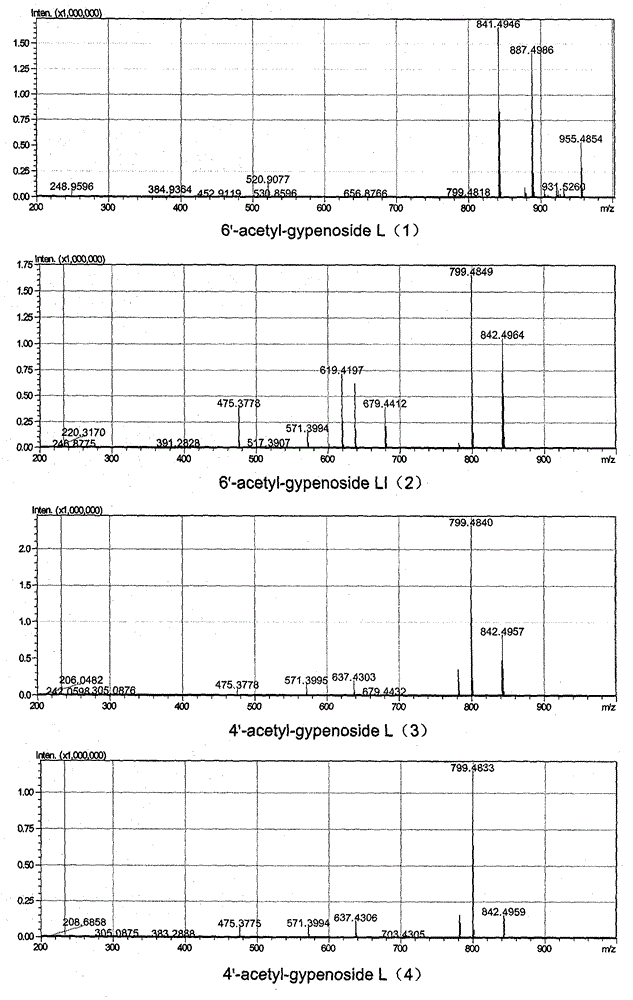
1.附图1为四种四种gypenosidel和gypenosideli乙酰化衍生物质谱图,由这四种化合物的质谱信息可以发现,四种化合物可能是在绞股蓝皂苷gypenosidel和gypenosideli的化学结构基础之上发生乙酰化,增加了一个乙酰化基团。
2.附图2为四种gypenosidel和gypenosideli乙酰化衍生物结构图,通过结合这四种乙酰化衍生物的质谱信息和核磁信息,可推断其发生乙酰化的位置为4’位和6’位,按化学命名法,这四种化合物命名为6′-acetyl-gypenosidel、6′-acetyl-gypenosideli、4′-acetyl-gypenosidel、4′-acetyl-gypenosideli。
3.附图3为乙酰化反应完成后gypenosidel和gypenosideli与其乙酰化化合物的混合物半制备液相分离图,从色谱图可发现,发生乙酰化后生成的这四种化合物相比gypenosidel和gypenosideli而言,保留时间延长,及说明乙酰化产物极性更小,脂溶性更大。
具体实施方式
实施例1gypenosidel和gypenosideli乙酰化衍生物制备实验
4.gypenosidel和gypenosideli乙酰化实验
取gypenosidel和gypenosideli混合物,加入100倍量冰醋酸,105℃条件下加热3h。将所得混合物减压浓缩至干燥状态,即得gypenosidel和gypenosideli与其乙酰化化合物的混合物。
5.gypenosidel和gypenosideli乙酰化衍生物分离及鉴定实验
将获得的gypenosidel和gypenosideli与其乙酰化化合物的混合物加入适量甲醇溶液溶解,过0.45μm微孔滤膜,利用半制备色谱仪进行分离,具体色谱条件如下:
hplc型号:岛津6ad
检测器:uv检测器
检测波长:203nm
色谱柱:thermoc18色谱柱(250×10mm,5μm)
柱温:30℃
流速:5ml/min
流动相:纯水(a)-乙腈(b)
洗脱条件:47%(b)等度洗脱
gypenosidel和gypenosideli与其乙酰化化合物的混合物,分离结果见附图3。
获得四个乙酰化衍生物单体,利用nmr,ms检测获得其核磁数据和质谱数据。
实施例2抗肿瘤实验
1.细胞系及细胞培养
人肺癌细胞a549、肝癌细胞hepg2、胃癌细胞sgc7901、前列腺癌细胞pc-3,以含10%胎牛血清的dmem培养基,与37℃、饱和湿度下、5.0%co2的培养箱中培养,细胞呈单层贴壁生长。实验取对数生长期细胞。
2.cck8法药物肿瘤活性抑制实验
取对数生长期的癌细胞,0.25%胰酶消化,10%胎牛血清的dmem培养基重悬成单细胞悬液。调细胞液浓度为5×104个/ml,接种导96孔板,100μl/孔。24h细胞贴壁后,弃去原有培养基;加入用dmem培养基稀释的质量浓度梯度(0、6.25、12.5、25、50、100μg/ml)的6′-acetyl-gypenosidel、6′-acetyl-gypenosideli、4′-acetyl-gypenosidel、4′-acetyl-gypenosideli100μl/孔,每个质量浓度设5个复孔。孵育24h后,弃去原培养基,按100μl/孔加入含10%cck8的dmem培养基,导37℃,5%co2培养箱孵育3h,用酶标仪于450nm检测吸光度。进行三次平行实验。计算肿瘤细胞半数抑制浓度ic50.计算公式如下:
寇氏改良法计算半数:igic50=xm-i(p-(3-pm-pn)/4)
1)实验材料及仪器
培养基:dmem培养基(gibco,美国);
fbs(gibco,美国);
胎牛血清(gibco,美国);
胰酶(1∶250,活性>250u/mg)(gibco,美国);
96孔板(corning,usa);
cck8试剂盒(东仁化学科技,上海);
倒置显微镜(optec,重庆光电仪器有限公司)
酶标仪(伯乐,美国)
xp205电子天平(梅特勒,瑞士)
细胞培养箱(thermoforma,美国)
人肺癌细胞a549、肝癌细胞hepg2、胃癌细胞sgc7901、前列腺癌细胞pc-3(北京协和细胞资源中心)
2)实验方法
人肺癌细胞a549、肝癌细胞hepg2、胃癌细胞sgc7901、前列腺癌细胞pc-3的抑制活性实验实验均采用cck8法。
3)供试样品
阳性对照药物选用人参皂苷rg3;四种gypenosidel和gypenosideli乙酰化衍生物6′-acetyl-gypenosidel、6′-acetyl-gypenosideli、4′-acetyl-gypenosidel、4′-acetyl-gypenosideli。
4)实验结果
对人肺癌细胞a549、肝癌细胞hepg2、胃癌细胞sgc7901、前列腺癌细胞pc-3均具有不同程度抑制活性,实验结果见表3
表3四种四种gypenosidel和gypenosideli乙酰化衍生物ic50值
- 还没有人留言评论。精彩留言会获得点赞!