3-羟基异戊酸氨基酸盐的晶体及其制造方法与流程
本发明涉及例如作为健康食品、药品、化妆品等的制品、原料或中间体等有用的3-羟基异戊酸(β-hydroxy-β-methylbutyrate)(以下称为hmb)的氨基酸盐的晶体以及该晶体的制造方法。
背景技术:
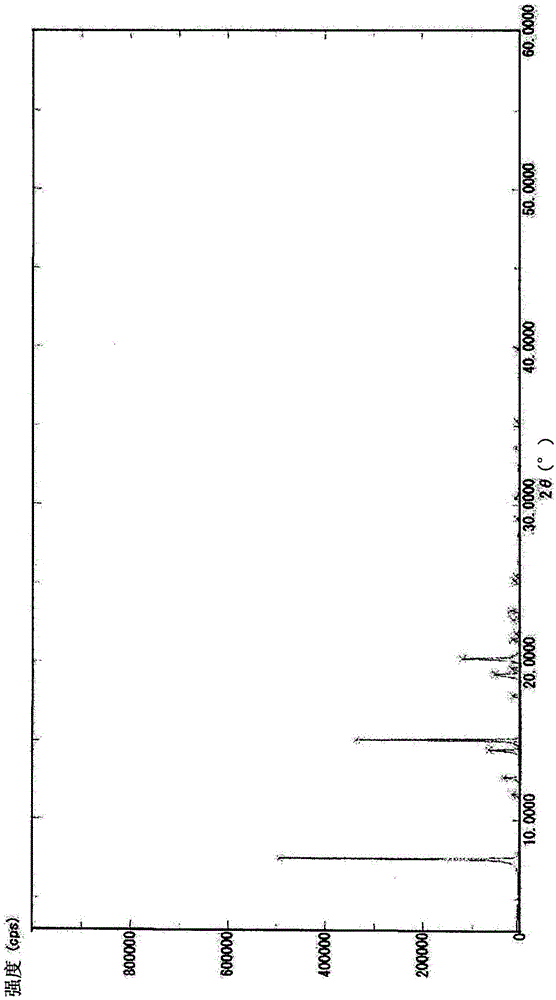
:hmb例如作为健康食品、药品、化妆品等的制品、原料或中间体等是有用的。hmb是通过体内的亮氨酸代谢得到的有机酸,被认为对肌肉的增强效果或分解抑制有效(非专利文献1以及2)。在商业上,hmb仅以游离羧酸体或钙盐中的任一种形态在市场上流通。特别是作为补充剂、健康食品用途,由于钙盐为操作性优良的粉末而几乎都使用钙盐(非专利文献3)。专利文献4中有已获得精氨酸盐的晶体的记载,但关于获得的晶体的性质没有记载。钙是在体内承担骨形成、神经活动、肌肉运动等的重要的矿物质。但是,最近有报道指出,过量摄取钙会使由心血管疾病、缺血性心脏病引起的死亡的风险增加(非专利文献4)。现有技术文献专利文献专利文献1:国际公开第2014/166273号公报专利文献2:美国专利第6248922号说明书专利文献3:国际公开第2013/025775号公报专利文献4:美国专利申请公开第2004/0176449号说明书非专利文献非专利文献1:journalofappliedphysiology,vol.81,p2095,1996非专利文献2:nutrition&metabolism,vol.5,p1,2008非专利文献3:journaloftheinternationalsocietyofsportsnutritionvol.10,p6,2013非专利文献4:thebmj.,vol.346,p228,2013技术实现要素:发明所要解决的问题在制剂领域中,存在来自钙盐的钙容易与磷酸等其它成分结合而形成不溶性盐、不能制备高浓度的溶液等问题。在专利文献1-3、专利文献1以及专利文献4中,分别记载了hmb钙盐(专利文献1-3)、hmb镁盐(专利文献1)以及hmb精氨酸盐(专利文献4)的制造方法,但是,在任一种方法中都无法获得晶体。即,对于任何盐形态都不知晓晶体,需要产业上有用的hmb盐的晶体及制造方法。本发明的课题在于提供溶解性优良、易于处理的hmb氨基酸盐的晶体及其制造方法。用于解决问题的方法本发明涉及以下的(1)~(25)。(1)一种3-羟基异戊酸(以下称为hmb)的氨基酸盐的晶体。(2)如上述(1)所述的晶体,其中,hmb氨基酸盐为hmb碱性氨基酸盐。(3)如上述(2)所述的晶体,其中,hmb碱性氨基酸盐为hmb精氨酸盐。(4)如上述(2)所述的晶体,其中,hmb碱性氨基酸盐为hmb赖氨酸盐。(5)如上述(2)所述的晶体,其中,hmb碱性氨基酸盐为hmb鸟氨酸盐。(6)如上述(3)所述的晶体,其中,在粉末x射线衍射中,在衍射角(2θ)为7.5±0.2°、14.5±0.2°、15.1±0.2°、19.2±0.2°以及20.2±0.2°处具有峰。(7)如上述(6)所述的晶体,其中,在粉末x射线衍射中,进一步在衍射角(2θ)为11.6±0.2°、12.7±0.2°、17.9±0.2°、21.5±0.2°以及23.3±0.2°处具有峰。(8)如上述(7)所述的晶体,其中,在粉末x射线衍射中,进一步在衍射角(2θ)为19.6±0.2°、21.9±0.2°、25.2±0.2°、25.5±0.2°以及33.6±0.2°处具有峰。(9)如上述(4)所述的晶体,其中,在粉末x射线衍射中,在衍射角(2θ)为8.5±0.2°、17.0±0.2°、18.1±0.2°、18.5±0.2°以及19.5±0.2°处具有峰。(10)如上述(9)所述的晶体,其中,在粉末x射线衍射中,进一步在衍射角(2θ)为22.2±0.2°、25.5±0.2°、25.8±0.2°、26.6±0.2°以及34.4±0.2°处具有峰。(11)如上述(10)所述的晶体,其中,在粉末x射线衍射中,进一步在衍射角(2θ)为4.8±0.2°、20.4±0.2°、31.0±0.2°、33.8±0.2°以及36.5±0.2°处具有峰。(12)如上述(5)所述的晶体,其中,在粉末x射线衍射中,在衍射角(2θ)为5.1±0.2°、14.0±0.2°、15.3±0.2°、20.4±0.2°以及21.9±0.2°处具有峰。(13)如上述(12)所述的晶体,其中,在粉末x射线衍射中,进一步在衍射角(2θ)为16.4±0.2°、16.8±0.2°、19.4±0.2°、21.4±0.2°以及25.5±0.2°处具有峰。(14)如上述(13)所述的晶体,其中,在粉末x射线衍射中,进一步在衍射角(2θ)为10.9±0.2°处具有峰。(15)一种hmb氨基酸盐的晶体的制造方法,其包括:使hmb氨基酸盐的无定形物溶解于含有醇类的溶剂中的工序、通过静置或搅拌该溶剂而使hmb氨基酸盐的晶体析出的工序、以及从该溶剂中收集hmb氨基酸盐的晶体的工序。(16)一种hmb氨基酸盐的晶体的制造方法,其包括:通过对ph为2.5~11.0的含有含氨基酸的化合物的hmb的水溶液进行浓缩而使hmb氨基酸盐的晶体析出的工序、以及从该水溶液中收集hmb氨基酸盐的晶体的工序。(17)如上述(16)所述的制造方法,其中,在使hmb氨基酸盐的晶体析出的工序中,进一步包括添加或滴加选自由醇类、腈类以及酮类组成的组中的至少一种溶剂的工序。(18)如上述(15)或(17)所述的制造方法,其中,醇类为选自由c1~c6的醇组成的组中的至少一种醇类。(19)如上述(17)或(18)所述的制造方法,其中,腈类为乙腈。(20)如上述(17)~(19)中任一项所述的制造方法,其中,酮类为选自由丙酮、甲乙酮、甲基异丁基酮以及二乙基酮组成的组中的至少一种酮类。(21)如上述(15)~(20)中任一项所述的制造方法,其中,hmb氨基酸盐为hmb碱性氨基酸盐。(22)如上述(21)所述的制造方法,其中,hmb碱性氨基酸盐为hmb精氨酸盐、hmb赖氨酸盐或hmb鸟氨酸盐。(23)如上述(5)所述的晶体,其中,在粉末x射线衍射中,在衍射角(2θ)为4.9±0.2°、5.2±0.2°、5.5±0.2°、10.9±0.2°以及15.5±0.2°处具有峰。(24)如上述(23)所述的晶体,其中,在粉末x射线衍射中,进一步在衍射角(2θ)为15.9±0.2°、16.4±0.2°、17.4±0.2°、19.2±0.2°以及20.4±0.2°处具有峰。(25)如上述(24)所述的晶体,其中,在粉末x射线衍射中,进一步在衍射角(2θ)为20.8±0.2°、21.3±0.2°、21.8±0.2°、22.2±0.2°以及22.8±0.2°处具有峰。发明效果根据本发明,可提供易于处理的hmb氨基酸盐的晶体及其制造方法。本发明的hmb氨基酸盐的晶体与hmb钙盐相比显示高溶解度,不形成不溶性盐,不诱发电解质异常等,是具有优势的盐晶体。另外,本发明的hmb氨基酸盐的晶体与hmb钙盐相比溶解性高,改善风味的效果优良。附图说明图1示出实施例2中得到的hmb精氨酸盐无水物的晶种的粉末x射线衍射的结果。图2示出实施例3中得到的hmb精氨酸盐无水物的晶体的粉末x射线衍射的结果。图3示出实施例3中得到的hmb精氨酸盐无水物的晶体的红外光谱(ir)分析的结果。图4示出实施例4中得到的hmb赖氨酸盐无水物的晶体的粉末x射线衍射的结果。图5示出实施例4中得到的hmb赖氨酸盐无水物的晶体的红外光谱(ir)分析的结果。图6示出实施例6中得到的hmb鸟氨酸盐无水物的晶体的粉末x射线衍射的结果。图7示出实施例6中得到的hmb鸟氨酸盐无水物的晶体的红外光谱(ir)分析的结果。图8示出实施例7中得到的hmb鸟氨酸盐无水物的晶体的粉末x射线衍射的结果。具体实施方式1.本发明的晶体本发明的晶体为hmb氨基酸盐的晶体(以下也称为“本发明的晶体”。)。作为hmb氨基酸盐的晶体,可以列举优选为hmb的碱性氨基酸盐的晶体,更优选为hmb精氨酸盐的晶体、hmb赖氨酸盐的晶体、hmb组氨酸盐的晶体以及hmb鸟氨酸盐的晶体,最优选为hmb精氨酸盐的晶体、hmb赖氨酸盐的晶体以及hmb鸟氨酸盐的晶体。本发明的晶体为hmb的晶体这一点可以通过使用后述的分析例中记载的hplc的方法来确认。作为本发明的晶体中的氨基酸,可以为l体、d体中的任一种,优选为l体。本发明的晶体为氨基酸盐的晶体这一点可以通过使用后述的分析例中记载的hplc对该晶体中所含的氨基酸的含量进行测定来确认。例如,本发明的晶体为单精氨酸盐的晶体这一点可以通过该晶体中的精氨酸含量通常为59.6±5.0重量%、优选为59.6±4.0重量%、最优选为59.6±3.0重量%来确认。另外,例如,本发明的晶体为单赖氨酸盐的晶体这一点可以通过该晶体中的赖氨酸含量通常为55.3±5.0重量%、优选为55.3±4.0重量%、最优选为55.3±3.0重量%来确认。另外,例如,本发明的晶体为单鸟氨酸盐的晶体这一点可以通过该晶体中的鸟氨酸含量通常为52.8±5.0重量%、优选为52.8±4.0重量%、最优选为52.8±3.0重量%来确认。本发明的晶体为无水物的晶体这一点可以通过使用后述的分析例中记载的卡尔费休法测定的水分含量通常为2.5重量%以下、优选为2.3重量%以下、最优选为2.0重量%以下来确认。作为hmb精氨酸盐无水物的晶体,可以列举使用cukα作为x射线源的粉末x射线衍射图案由图1及2、以及表1及2所示的值规定的hmb精氨酸盐无水物的晶体。需要说明的是,图1及表1、以及图2及表2对应于各hmb精氨酸盐无水物的晶体的衍射结果。作为上述粉末x射线衍射图案由图2以及表2所示的值规定的hmb精氨酸盐无水物的晶体,可以列举在供于后述的分析例中记载的红外(ir)分析时显示图3所示的红外吸收光谱的hmb精氨酸盐无水物的晶体。作为hmb精氨酸盐无水物的晶体,具体而言,在使用cukα作为x射线源的粉末x射线衍射中优选在下述(i)中记载的衍射角(2θ)处具有峰的hmb精氨酸盐无水物的晶体,更优选除了下述(i)中记载的衍射角(2θ)以外还在下述(ii)中记载的衍射角(2θ)处具有峰的hmb精氨酸盐无水物的晶体,进一步优选除了下述(i)以及(ii)中记载的衍射角(2θ)以外还在下述(iii)中记载的衍射角(2θ)处具有峰的hmb精氨酸盐无水物的晶体。(i)7.5±0.2°、优选7.5±0.1°;14.5±0.2°、优选14.5±0.1°;15.1±0.2°、优选15.1±0.1°;19.2±0.2°、优选19.2±0.1°;以及20.2±0.2°、优选20.2±0.1°(ii)11.6±0.2°、优选11.6±0.1°;12.7±0.2°、优选12.7±0.1°;17.9±0.2°、优选17.9±0.1°;21.5±0.2°、优选21.5±0.1°;以及23.3±0.2°、优选23.3±0.1°(iii)19.6±0.2°、优选19.6±0.1°;21.9±0.2°、优选21.9±0.1°;25.2±0.2°、优选25.2±0.1°;25.5±0.2°、优选25.5±0.1°;以及33.6±0.2°、优选33.6±0.1°作为hmb赖氨酸盐无水物的晶体,可以列举使用cukα作为x射线源的粉末x射线衍射图案由图4以及表4所示的值规定的hmb赖氨酸盐无水物的晶体。作为上述粉末x射线衍射图案由图4以及表4所示的值规定的hmb赖氨酸盐无水物的晶体,可以列举在供于后述的分析例中记载的红外光谱(ir)分析时显示图5所示的红外吸收光谱的hmb赖氨酸盐无水物的晶体。作为hmb赖氨酸盐无水物的晶体,具体而言,在使用cukα作为x射线源的粉末x射线衍射中优选在下述(i)中记载的衍射角(2θ)处具有峰的hmb赖氨酸盐无水物的晶体,更优选除了下述(i)中记载的衍射角(2θ)以外还在下述(ii)中记载的衍射角(2θ)处具有峰的hmb赖氨酸盐无水物的晶体,进一步优选除了下述(i)以及(ii)中记载的衍射角(2θ)以外还在下述(iii)中记载的衍射角(2θ)处具有峰的hmb赖氨酸盐无水物的晶体。(i)8.5±0.2°、优选8.5±0.1°;17.0±0.2°、优选17.0±0.1°;18.1±0.2°、优选18.1±0.1°;18.5±0.2°、优选18.5±0.1°;以及19.5±0.2°、优选19.5±0.1°(ii)22.2±0.2°、优选22.2±0.1°;25.5±0.2°、优选25.5±0.1°;25.8±0.2°、优选25.8±0.1°;26.6±0.2°、优选26.6±0.1°;以及34.4±0.2°、优选34.4±0.1°(iii)4.8±0.2°、优选4.8±0.1°;20.4±0.2°、优选20.4±0.1°;31.0±0.2°、优选31.0±0.1°;33.8±0.2°、优选33.8±0.1°;以及36.5±0.2°、优选36.5±0.1°作为hmb鸟氨酸盐无水物的晶体,可以列举使用cukα作为x射线源的粉末x射线衍射图案由图6以及表6所示的值规定的hmb鸟氨酸盐无水物的晶体、以及由图8以及表9所示的值规定的hmb鸟氨酸盐无水物的晶体。需要说明的是,图6及表6、以及图8及表9对应于各hmb鸟氨酸盐无水物的晶体的衍射结果。作为上述粉末x射线衍射图案由图6以及表6所示的值规定的hmb鸟氨酸盐无水物的晶体,可以列举在供于后述的分析例中记载的红外光谱(ir)分析时显示图7所示的红外吸收光谱的hmb鸟氨酸盐无水物的晶体。作为hmb鸟氨酸盐无水物的晶体,具体而言,在使用cukα作为x射线源的粉末x射线衍射中优选在下述(i)中记载的衍射角(2θ)处具有峰的hmb鸟氨酸盐无水物的晶体,更优选除了下述(i)中记载的衍射角(2θ)以外在下述(ii)中记载的衍射角(2θ)处具有峰的hmb鸟氨酸盐无水物的晶体,进一步优选除了下述(i)以及(ii)中记载的衍射角(2θ)以外还在下述(iii)中记载的衍射角(2θ)处具有峰的hmb鸟氨酸盐无水物的晶体。(i)5.1±0.2°、优选5.1±0.1°;14.0±0.2°、优选14.0±0.1°;15.3±0.2°、优选15.3±0.1°;20.4±0.2°、优选20.4±0.1°;以及21.9±0.2°、优选21.9±0.1°(ii)16.4±0.2°、优选16.4±0.1°;16.8±0.2°、优选16.8±0.1°;19.4±0.2°、优选19.4±0.1°;21.4±0.2°、优选21.4±0.1°;以及25.5±0.2°、优选25.5±0.1°(iii)0.9±0.2°、优选0.9±0.1°另外,作为hmb鸟氨酸盐无水物的晶体,具体而言,在使用cukα作为x射线源的粉末x射线衍射中优选在下述(i)中记载的衍射角(2θ)处具有峰的hmb鸟氨酸盐无水物的晶体,更优选除了下述(i)中记载的衍射角(2θ)以外还在下述(ii)中记载的衍射角(2θ)处具有峰的hmb鸟氨酸盐无水物的晶体,进一步优选除了下述(i)以及(ii)中记载的衍射角(2θ)以外还在下述(iii)中记载的衍射角(2θ)处具有峰的hmb鸟氨酸盐无水物的晶体。(i)4.9±0.2°、优选4.9±0.1°;5.2±0.2°、优选5.2±0.1°;5.5±0.2°、优选5.5±0.1°;10.9±0.2°、优选10.9±0.1°;以及15.5±0.2°、优选15.5±0.1°(ii)15.9±0.2°、优选15.9±0.1°;16.4±0.2°、优选16.4±0.1°;17.4±0.2°、优选17.4±0.1°;19.2±0.2°、优选19.2±0.1°;以及20.4±0.2°、优选20.4±0.1°(iii)20.8±0.2°、优选20.8±0.1°;21.3±0.2°、优选21.3±0.1°;21.8±0.2°、优选21.8±0.1°;22.2±0.2°、优选22.2±0.1°;以及22.8±0.2°、优选22.8±0.1°2.本发明的晶体的制造方法本发明的晶体的制造方法为以下的(1)或(2)记载的制造方法(以下也称为“本发明的晶体的制造方法”。)。(1)本发明的晶体的制造方法-1作为本发明的晶体的制造方法,可以列举如下所述的hmb氨基酸盐的晶体的制造方法,其包括:使hmb氨基酸盐的无定形物溶解于含有醇类的溶剂中的工序、通过将该溶剂进行静置或搅拌而使hmb氨基酸盐的晶体析出的工序、以及从该溶剂中收集hmb氨基酸盐的晶体的工序。作为氨基酸,可以列举优选为碱性氨基酸,更优选为精氨酸、鸟氨酸、赖氨酸以及组氨酸,进一步优选为精氨酸、鸟氨酸以及赖氨酸,最优选为精氨酸。氨基酸可以使用l体、d体中的任一种,优选为l体。作为醇类,可以列举优选为选自由c1~c6的醇组成的组中的至少一种醇类,更优选为选自由c1~c3的醇类组成的组中的至少一种醇类,进一步优选为选自由甲醇、乙醇、正丙醇以及异丙醇组成的组中的至少一种醇类,更进一步优选为选自由甲醇以及乙醇组成的组中的至少一种醇类,最优选为乙醇。上述醇类可以混合使用一种以上。另外,在含有上述醇类的溶剂中可以含有水。作为含有醇类的溶剂的含水量,可以列举通常为40重量%以下、优选为20重量%以下、进一步优选为10重量%以下、最优选为5重量%以下。作为使hmb氨基酸盐的无定形物溶解于含有醇类的溶剂中的方法,可以列举使hmb氨基酸盐的无定形物悬浮在该溶剂中后进行加热而得到溶解液的方法、或者将该溶剂进行过滤而得到滤液的方法。使hmb氨基酸盐的无定形物悬浮在上述溶剂中后进行加热而得到溶解液的方法中,作为加热温度,可以列举通常为0~80℃、优选为20~70℃、最优选为40~60℃。作为加热时间,可以列举通常为10分钟~6小时、优选为20分钟~4小时、最优选为30分钟~2小时。hmb氨基酸盐的无定形物可以通过后述的实施例1中记载的方法获得。通过将使hmb氨基酸盐的无定形物溶解而得到的上述溶剂进行静置或搅拌,可以使hmb氨基酸盐的晶体析出。作为溶解于含有醇类的溶剂中的hmb氨基酸盐的无定形物的浓度,可以列举优选为50g/l以上、更优选为100g/l以上、进一步优选为150g/l以上。可以在使hmb氨基酸盐的无定形物溶解后的含有醇类的溶剂中添加作为晶种的hmb氨基酸盐的晶体后,将该溶剂进行静置或搅拌,由此使hmb氨基酸盐的晶体析出。通过在该溶剂中添加该晶种,能够加快析出速度。该晶种按照在该溶剂中的浓度通常为0.05~15重量%、优选为0.5~10重量%、最优选为2~7重量%的方式添加。hmb氨基酸盐的晶体可以通过后述的实施例2、4或5中记载的方法获得。作为将上述溶剂进行静置或搅拌的温度,可以列举通常为0~80℃、优选为5~50℃、最优选为10~30℃。作为进行静置或搅拌的时间,可以列举通常为1~100小时、优选为3~48小时、最优选为5~24小时。作为从上述溶剂中收集hmb氨基酸盐的晶体的方法,没有特别限定,可以列举滤取、加压过滤、抽滤或离心分离等。进而,为了减少母液的附着、提高晶体的品质,可以适当洗涤晶体。晶体的洗涤中使用的溶液没有特别限制,可以使用将选自水、甲醇、乙醇、丙酮、正丙醇以及异丙醇中的一种或多种以任意的比例混合而成的溶液。通过将由此得到的湿晶干燥,可以获得hmb氨基酸盐的晶体。作为干燥条件,只要能够保持hmb氨基酸盐的晶体的形态的方法则可以为任一种,可以应用减压干燥、真空干燥、流化床干燥或通风干燥等。作为干燥温度,只要是能够除去附着水分、溶剂的范围则可以为任意温度,可以列举优选为80℃以下、更优选为60℃以下。通过上述晶析条件,可以获得高纯度的hmb氨基酸盐的晶体。作为该晶体的纯度,可以列举通常为95%以上、优选为96%以上、更优选为97%以上、最优选为97.5%以上。作为可以通过上述制造方法制造的hmb氨基酸盐的晶体,例如可以列举使用cukα作为x射线源的粉末x射线衍射图案由图1及2、以及表1及2所示的值规定的hmb精氨酸盐无水物的晶体。(2)本发明的晶体的制造方法-2作为本发明的晶体的制造方法,可以列举如下所述的hmb氨基酸盐的晶体的制造方法,其包括:对含有含氨基酸的化合物的ph为2.5~11.0的hmb的水溶液进行浓缩而使hmb氨基酸盐的晶体在该水溶液中析出的工序、以及从该水溶液中收集hmb氨基酸盐的晶体的工序。hmb的水溶液中所含有的hmb可以是通过发酵法、酶法、从天然物中提取的方法或化学合成法等中的任一制造方法制造的hmb。在hmb的水溶液中含有妨碍结晶化的固态物的情况下,可以使用离心分离、过滤或陶瓷过滤器等除去固态物。另外,在hmb的水溶液中含有妨碍结晶化的水溶性的杂质、盐的情况下,可以通过从填充有离子交换树脂等的柱中通过等来除去水溶性的杂质或盐。另外,在hmb的水溶液中含有妨碍结晶化的疏水性的杂质的情况下,可以通过从填充有合成吸附树脂或活性炭等的柱中通过等来除去疏水性的杂质。该水溶液可以按照hmb的浓度达到通常为500g/l以上、优选为600g/l以上、更优选为700g/l以上、最优选为800g/l以上的方式来制备。作为含氨基酸的化合物,可以列举优选为含碱性氨基酸的化合物,更优选为含精氨酸的化合物、含赖氨酸的化合物、含鸟氨酸的化合物以及含组氨酸的化合物,最优选为含精氨酸的化合物、含赖氨酸的化合物以及含鸟氨酸的化合物。含氨基酸的化合物中的氨基酸可以使用l体、d体中的任一种,优选为l体。作为含精氨酸的化合物,例如可以列举游离体的精氨酸以及精氨酸盐酸盐。在使用游离体的精氨酸作为含精氨酸的化合物的情况下,通过使用精氨酸对hmb的水溶液的ph进行调整,能够获得ph通常为2.5~11.0、优选为2.8~10.5、最优选为3.0~10.0的含有含精氨酸的化合物的hmb的水溶液。作为含赖氨酸的化合物,例如可以列举游离体的赖氨酸以及赖氨酸盐酸盐。在使用游离体的赖氨酸作为含赖氨酸的化合物的情况下,通过使用赖氨酸对hmb的水溶液的ph进行调整,可以获得ph通常为2.5~11.0、优选为2.8~10.5、最优选为3.0~10.0的含有含赖氨酸的化合物的hmb的水溶液。作为含鸟氨酸的化合物,例如可以列举游离体的鸟氨酸以及鸟氨酸盐酸盐。在使用游离体的鸟氨酸作为含鸟氨酸的化合物的情况下,通过使用鸟氨酸对hmb的水溶液的ph进行调整,可以获得ph通常为2.5~11.0、优选为2.8~10.5、最优选为3.0~10.0的含有含鸟氨酸的化合物的hmb的水溶液。作为对hmb的水溶液进行浓缩而使hmb氨基酸盐的晶体在该水溶液中析出的方法,可以列举对该水溶液进行减压浓缩的方法等。作为对hmb的水溶液进行减压浓缩的方法中的该水溶液的温度,可以列举通常为0~100℃、优选为10~90℃、最优选为20~60℃。作为对该水溶液进行减压浓缩的方法中的减压时间,可以列举通常为1~120小时、优选为2~60小时、最优选为3~50小时。在使hmb氨基酸盐的晶体在该水溶液中析出的工序中,可以在hmb的水溶液中添加hmb氨基酸盐的晶体作为晶种。晶种按照在水溶液中的浓度通常为0.05~15重量%、优选为0.5~10重量%、最优选为2~7重量%的方式添加。具体而言,hmb氨基酸盐的晶体例如可以通过后述的实施例2、4或5中记载的方法获得。在使hmb氨基酸盐的晶体在该水溶液中析出的工序中,可以通过向hmb的水溶液中添加或滴加选自由醇类、腈类以及酮类组成的组中的至少一种溶剂而使hmb氨基酸盐的晶体析出。醇类、腈类以及酮类可以单独使用一种,也可以组合使用多种。此外,在添加或滴加上述溶剂时,可以在hmb氨基酸盐的晶体析出之前添加上述晶种。作为添加上述晶种的时间,可以列举开始滴加或添加该溶剂后通常0~5小时以内、优选0~4小时以内、最优选0~3小时以内。另外,可以在向hmb的水溶液中添加或滴加该溶剂之前添加上述晶种。作为醇类,可以列举与上述2.(1)所记载相同的例子。作为腈类,可以列举优选为乙腈。作为酮类,可以列举优选为选自由丙酮、甲乙酮、甲基异丁基酮以及二乙基酮组成的组中的至少一种酮类,更优选为选自由丙酮以及甲乙酮组成的组中的至少一种酮类,最优选为丙酮。作为向hmb的水溶液中添加或滴加上述溶剂时的该水溶液的温度,只要是hmb不发生分解的温度则可以为任一温度,但是,为了降低溶解度而提高hmb氨基酸盐无水物的晶体的结晶化率,可以列举通常为80℃以下、优选为70℃以下、更优选为60℃以下、最优选为50℃以下。作为温度的下限值,可以列举通常为0℃以上、优选为10℃以上。作为向hmb的水溶液中添加或滴加上述溶剂的量,可以列举该水溶液的通常0.5~30倍量、优选为0.5~25倍量、最优选为0.5~10倍量。作为向hmb的水溶液中添加或滴加上述溶剂的时间,可以列举通常为30分钟~48小时、优选为2~30小时、最优选为3~20小时。如此使hmb氨基酸盐的晶体析出后,可以进一步将析出的晶体进行通常为1~48小时、优选为1~24小时、最优选为1~12小时的熟化。熟化是指将使hmb氨基酸盐无水物的晶体析出的工序暂时停止而使晶体生长。使晶体熟化后,可以再次开始使hmb氨基酸盐的晶体析出的工序。作为收集hmb氨基酸盐的晶体的方法,没有特别限定,例如可以列举滤取、加压过滤、抽滤以及离心分离等。进而,为了减少母液的附着、提高晶体的品质,可以适当洗涤晶体。作为晶体洗涤中使用的溶液,没有特别限制,可以使用将选自水、甲醇、乙醇、丙酮、正丙醇、异丙醇、乙腈、丙酮、甲乙酮、甲基异丁基酮以及二乙基酮中的一种或多种以任意的比例混合后的溶液。通过将由此得到的湿晶干燥,可以获得hmb氨基酸盐的晶体。作为干燥条件,可以应用减压干燥、真空干燥、流化床干燥或通风干燥。作为干燥温度,只要是能够除去附着水分、溶剂的范围则可以为任意温度,可以列举优选为80℃以下、更优选为60℃以下。利用上述晶析条件,能够获得高纯度的hmb氨基酸盐的晶体。作为hmb氨基酸盐的晶体的纯度,可以列举通常为93%以上、优选为94%以上、更优选为95%以上、最优选为96%以上。作为可以通过上述制造方法制造的hmb氨基酸盐的晶体,例如可以列举使用cukα作为x射线源的粉末x射线衍射图案由图4以及表4所示的值规定的hmb赖氨酸盐无水物的晶体、由图6以及表6所示的值规定的hmb鸟氨酸盐无水物的晶体、以及由图8以及表9所示的值规定的hmb鸟氨酸盐无水物的晶体。[分析例](1)粉末x射线衍射使用粉末x射线衍射装置(xrd)ultimaiv(理学公司制造),测定按照使用说明书来进行。(2)浓度和纯度测定使用以下的hplc分析条件来测定hmb浓度以及各种盐的纯度。保护柱:shodexsugarsh-gφ6.0×50mm柱:sugarsh1011φ8.0×300mm×2根串联柱温:60℃缓冲液:0.005mol/l的硫酸水溶液流速:0.6ml/分钟检测器:uv检测器(波长210nm)(3)利用卡尔费休法的晶体的水分含量的测定使用自动水分测定装置aqv-2200(平沼产业公司制造),按照使用说明书测定晶体的水分含量。(4)晶体的氨基酸含量的测定使用具有荧光检测器的hplc,通过邻苯二甲醛(opa)法测定氨基酸含量。(5)熔点的测定使用meltingpointm-565(buchi公司制造),按照使用说明书利用以下条件测定熔点。100℃~250℃、2℃/分钟(6)红外光谱(ir)分析使用ftir-8400型(岛津制作所制造),按照使用说明书来进行。[参考例1]hmb游离体溶液的制作使以游离体换算计为76.5g的hmb钙盐试剂溶解于850ml的水中。将该水溶液从640ml的强阳离子性交换树脂xus-40232.01(h+)(陶氏化学公司制造)通过来进行脱ca,获得含有76.4g的hmb游离体的溶液1.25l。[参考例2]hmb精氨酸盐的结晶化研究参考美国专利申请公开第2004/0176449号说明书的记载尝试了hmb精氨酸盐的结晶化。根据与参考例1同样的方法,获得含有hmb游离体2.31g的水溶液48ml。对所得到的水溶液进行浓缩而使其为12ml后,添加异丁醇24ml,进而添加精氨酸游离体2.41g,在室温下搅拌1小时,结果,以双相的形式得到白色透明的溶液。只取水相,将水相在50℃、15mbar的条件下浓缩20小时,结果得到6.5g白色的析出物。利用偏光显微镜对该粉末进行观察,结果确认到,其为不显示偏光的无定形的饴糖状固体,可知其为非晶性无定形物(熔点:98~126℃、10℃/分钟)。由上所述,利用美国专利申请公开第2004/0176449号说明书记载的方法无法得到hmb精氨酸盐的晶体。实施例以下示出实施例,但本发明不受下述实施例限定。[实施例1]hmb精氨酸盐的非晶性无定形物的获得向参考例1中得到的hmb游离体水溶液200ml中加入128g/l的l-精氨酸水溶液160ml,将ph调整为7.05。将得到的水溶液供于下一工序。将该水溶液360ml在50℃、15mbar下减压浓缩而除去溶剂,由此得到31.1g的白色粉末。利用偏光显微镜对该粉末进行观察,结果没有显示偏光,因此可知,该粉末为非晶性无定形物。[实施例2]hmb精氨酸盐无水物的晶种的获得向参考例1中得到的hmb精氨酸盐的非晶性无定形物150mg中添加1.5ml的100%-etoh(乙醇),加热至50℃使其完全溶解。将该水溶液在25℃搅拌12小时,由此使晶体自然结晶。使该晶体浆液进一步熟化12小时后,滤取该晶体,在25℃通风干燥12小时,由此得到60mg的晶体。将该晶体的粉末x射线衍射的结果示于图1以及表1中。表中,“2θ”表示衍射角(2θ°),“相对强度”表示相对强度比(i/i0)。另外,显示相对强度比为1以上的结果。[表1]2θ相对强度7.510011.6412.7814.51415.16917.9419.21119.6420.22521.5421.8222.7423.3525.2325.5229.1230.4333.6235.3239.91[实施例3]hmb精氨酸盐无水物的晶体的获得向参考例1中得到的hmb精氨酸盐的非晶性无定形物27.8g中添加160ml的100%-etoh,加热至50℃使其完全溶解。向该水溶液中添加0.1g按照实施例2得到的hmb精氨酸盐的晶种,使晶体结晶。将该晶体浆液在25℃搅拌12小时,使其熟化后,滤取该晶体,在25℃进行通风干燥,由此得到23.6g的晶体。使所得到的晶体中的11.6g进一步在减压(15mbar)下于40℃干燥4小时,由此得到9.0g的晶体。在利用hplc的纯度测定中,能够获得97.8%(面积%)以上的hmb精氨酸盐无水物的晶体。将该晶体的粉末x射线衍射的结果示于图2以及表2中,将红外光谱(ir)分析的结果示于图3中。表中,“2θ”表示衍射角(2θ°),“相对强度”表示相对强度比(i/i0)。另外,显示相对强度比为5以上的结果。[表2]2θ相对强度7.58111.61412.73313.5514.55715.14917.91519.25519.61420.210021.51521.91023.31725.21325.5926.3729.1630.5633.61035.3739.96通过hplc测定该晶体的l-精氨酸含量,结果为61.7重量%,与单精氨酸盐的理论值(59.6重量%)基本一致。另外,通过卡尔费休法测定该晶体中所含的水分量,结果为0.5重量%。根据以上可知,该晶体为hmb精氨酸盐无水物的晶体。将实施例3中获得的晶体的各种物性示于表3中。[表3]水分精氨酸含量熔点%%℃0.561.7177.9[实施例4]hmb赖氨酸盐无水物的晶体的获得向参考例1中得到的hmb游离体水溶液200ml中添加200g/l的l-赖氨酸水溶液94ml,将ph调整为6.03。将得到的水溶液供于下一工序。将该水溶液在50℃、15mbar的条件下浓缩至浓缩液重量为33.4g,结果使晶体自然结晶,得到白色浆液。向该浆液中添加乙腈20ml,在50℃搅拌1小时使其熟化后,滤取该晶体。将所得到的晶体用乙腈20ml进行洗涤后,在减压(15mbar)下于40℃干燥24小时,由此得到5.0g的晶体。在利用hplc的纯度测定中,能够获得97.4%(面积%)以上的hmb赖氨酸盐无水物的晶体。将该晶体的粉末x射线衍射的结果示于图4以及表4中,将红外光谱(ir)分析的结果示于图5中。表中,“2θ”表示衍射角(2θ°),“相对强度”表示相对强度比(i/i0)。另外,显示相对强度比为2以上的结果。[表4]通过hplc测定该晶体的l-赖氨酸含量,结果为54.8重量%,与单赖氨酸盐的理论值(55.3重量%)基本一致。另外,通过卡尔费休法测定该晶体中所含的水分量,结果为0.1重量%。根据以上可知,该晶体为hmb赖氨酸盐无水物的晶体。将实施例4中获得的晶体的各种物性示于表5中。[表5]水分赖氨酸含量熔点%%℃0.154.8186.2[实施例5]hmb鸟氨酸盐无水物的晶种的获得向参考例1中得到的hmb游离体水溶液20ml中添加510g/l的l-鸟氨酸水溶液,将ph调整为7.80。将得到的水溶液供于下一工序。将该水溶液在50℃、15mbar的条件下进行浓缩,得到2.8g白色析出物。将该粉末利用偏光显微镜进行观察,结果显示出偏光,因此可知,该粉末为晶体。[实施例6]hmb鸟氨酸盐无水物的晶体的获得-1向参考例1中得到的hmb游离体水溶液20ml中添加510g/l的l-鸟氨酸水溶液2.1ml,将ph调整为7.08。将得到的水溶液供于下一工序。将该水溶液在50℃、15mbar的条件下浓缩至浓缩液重量为3.9g后,添加0.1g按照实施例5得到的hmb鸟氨酸盐无水物的晶种后,用30分钟滴加添加9ml的100%-乙醇,使晶体析出。使晶体浆液熟化12小时后,滤取该晶体,用100%乙醇水溶液进行洗涤后,在25℃进行通风干燥,进一步在减压(15mbar)下于室温干燥24小时,由此得到250mg的晶体。在利用hplc的纯度测定中,能够获得96.3%(面积%)以上的hmb鸟氨酸盐无水物的晶体。将该晶体的粉末x射线衍射的结果示于图6以及表6中,将红外光谱(ir)分析的结果示于图7中。表中,“2θ”表示衍射角(2θ°),“相对强度”表示相对强度比(i/i0)。另外,显示相对强度比为1以上的结果。[表6]2θ相对强度5.110010.5110.9214.0215.3816.4216.8219.4220.4321.4221.9323.9124.9125.5226.1128.1130.7134.7135.41通过hplc测定该晶体的l-鸟氨酸含量,结果为53.6重量%,与单鸟氨酸盐的理论值(52.8重量%)基本一致。另外,通过卡尔费休法测定该晶体中所含的水分量,结果为2.0重量%。根据以上可知,该晶体为hmb鸟氨酸盐无水物的晶体。将实施例6中获得的晶体的各种物性示于表7中。[表7]水分鸟氨酸含量熔点%%℃2.053.6171.6[实施例7]hmb鸟氨酸盐无水物的晶体的获得-2根据与参考例1同样的方法获得含有hmb游离体280.3g的水溶液4.6l。向所得到的水溶液中添加510g/l的鸟氨酸水溶液615ml,将ph调整为6.2。将该水溶液在50℃、15mbar的条件下浓缩至浓缩液重量为696g。在将该溶液维持于室温下的同时,添加按照实施例5得到的hmb鸟氨酸盐无水物的晶种1.8g,使晶体析出。使晶体浆液在室温下熟化24小时后,对该晶体进行离心分离,由此滤取晶体,进一步将该晶体在30hpa、40℃的条件下真空干燥24小时,由此得到180g的晶体。通过hplc测定该晶体的鸟氨酸含量,结果为51.6重量%,与单鸟氨酸盐的理论值(52.8重量%)基本一致。另外,通过卡尔费休法测定该晶体中所含的水分量,结果为0.5重量%。根据以上可知,该晶体为hmb鸟氨酸盐无水物的晶体。将实施例7中获得的晶体的各种物性示于表8中。[表8]水分鸟氨酸含量熔点%%℃0.551.6169-172将该晶体的粉末x射线衍射的结果示于图8以及表9中。表中,“2θ”表示衍射角(2θ°),“相对强度”表示相对强度比(i/i0)。另外,显示相对强度比为2以上的结果。[表9]将作为实施例7中获得的晶体的图表的图8与作为实施例6中获得的晶体的图表的图6进行比较,结果,它们不一致。由此确认到,该晶体为与实施例6中获得的晶体不同的晶型。[实施例8]溶解度的测定分别添加实施例3中得到的hmb精氨酸盐无水物的晶体、hmb钙盐水合物(东京化成工业公司制造)直至在室温下在水中有溶解残留,搅拌保持充分时间后,收集不含晶体的上清液,使用hplc测定hmb浓度。将其结果示于表10中。[表10]※1从东京化成工业株式会社购入如表10所示,可知:获得的hmb精氨酸盐无水物的晶体与现有的hmb钙盐相比,在水中的溶解度大幅提高。[实施例9]hmb精氨酸盐的晶体、hmb赖氨酸盐的晶体与磷酸缓冲液的混合将实施例3中得到的hmb精氨酸盐无水物的晶体、实施例4中得到的hmb赖氨酸盐无水物的晶体、hmb钙盐水合物(东京化成工业公司制造)分别制成以游离体换算计为100g/l的溶液,与0.2m的磷酸缓冲液(ph6.80)以任意的混合比率混合。对混合后的液体的透光率(660nm)进行测定,对不溶性盐的形成有无进行评价。将其结果示于表11中。[表11]透射率t%(660nm)(※1)体积/体积=hmb100g/l水溶液(体积)/0.2m磷酸缓冲液(体积)如表11所示,可知:在与磷酸缓冲液的混合中,现有的hmb钙盐生成不溶性的盐,与此相对,获得的hmb精氨酸盐无水物以及hmb赖氨酸盐无水物的晶体没有形成不溶性盐。[实施例10]hmb精氨酸盐的晶体与糖氨基酸电解质输液制剂的混合将实施例3中得到的hmb精氨酸盐无水物、hmb钙盐水合物(东京化成工业公司制造)分别按照以游离体换算计终浓度达到0重量/体积%、0.11重量/体积%、0.21重量/体积%以及0.42重量/体积%的方式混合到外周静脉营养用糖氨基酸电解质输液剂[ph约6.7,制品名:aminofluid输液(株式会社大塚制药工厂)]中,通过紫外可见分光光度计测定刚混合后及室温放置24小时后的透光率t%(660nm),对不溶性盐的形成有无进行评价。将其结果示于表12中。[表12]透射率t%(660nm)如表12所示,可知:在与aminofluid输液的混合中,现有的hmb钙盐形成不溶性盐,与此相对,获得的hmb精氨酸盐无水物没有形成不溶性盐。[实施例11]含有hmb精氨酸盐的晶体的糖电解质输液制剂给药时对体内电解质的影响将实施例3中得到的hmb精氨酸盐无水物、hmb钙盐水合物(东京化成工业公司制造)分别按照以游离体换算计终浓度达到0重量/体积%以及0.42重量/体积%的方式混合到不含磷酸根离子的糖电解质输液制剂[制品名:solita-t3号输液(aypharmaceuticals株式会社)]中,对通过肠道擦伤术施加手术侵入后的大鼠以标准的用量(240ml/kg/天)持续给药3天。在最终给药日收集蓄积了24小时的尿,测定尿中电解质浓度。将其结果示于表13以及表14中。[表13]尿中钙排泄量(mg/天)[表14]尿中磷排泄量(mg/天)如表13以及表14所示,可知:在与solita-t3号输液的混合给药中,现有的hmb钙盐会诱发尿中钙的升高以及尿中磷排泄的减少,与此相对,获得的hmb精氨酸盐无水物的晶体没有诱发上述电解质异常。[实施例12]感官评价试验-1[饮料(1)的制备]向水200ml中添加实施例7中得到的hmb鸟氨酸盐无水物6g、麦芽糖醇(三菱商事foodtech公司制造)4g、苹果香料(高田香料公司制造)120μl、糖香精(小川香料公司制造)120μl、阿斯巴甜(味之素公司制造)200mg使其溶解。向该溶液中添加适量柠檬酸(三菱foodspecialties公司制造),将ph调整为3.70后,每100ml分注于玻璃瓶中,施加铝盖。将该玻璃瓶在90℃加热5分钟后,通过室温放置进行冷却,制作出饮料(1)。室温放置后立即通过目视确认有无沉淀以及浑浊,结果没有确认到沉淀以及浑浊。[比较饮料(1)的制备]使用hmb钙盐(hmb协和、协和发酵生化株式会社制造)代替hmb鸟氨酸盐无水物,除此以外,与饮料(1)同样地制备比较饮料(1)。室温放置后立即通过目视确认有无沉淀以及浑浊。其结果是,确认到大量白色沉淀。由8名评审员通过两点识别法来评价上述饮料(1)以及比较饮料(1)的风味哪个更好。其结果是,8名中8名评价为:与比较饮料(1)相比,饮料(1)明显风味更好。根据该结果可知,与hmb钙盐相比,获得的hmb鸟氨酸盐的改善溶解性以及风味的效果更优良。[实施例13]感官评价试验-2[饮料(2)的制备]向水200ml中添加实施例3中得到的hmb精氨酸盐无水物6g、麦芽糖醇(三菱商事foodtech公司制造)4g、黑醋栗香料(小川香料公司制造)120μl、糖蜜香精(三井制糖公司制造)60mg、甜菊(物产foodscience公司制造)200mg使其溶解。向该溶液中添加适量75%磷酸(大洋化学工业公司制造),将ph调整为3.70后,各100ml分注于玻璃瓶中,施加铝盖。将该玻璃瓶在90℃加热5分钟后,通过室温放置进行冷却,立即通过目视确认有无沉淀以及浑浊,其结果是,没有确认到沉淀以及浑浊。[比较饮料(2)的制备]使用hmb钙盐(hmb协和、协和发酵生化株式会社制造)代替hmb精氨酸盐无水物,除此以外,与饮料(2)同样地制备比较饮料(2)。室温放置后立即通过目视确认有无沉淀以及浑浊。其结果是,确认到与加热前同样的白色沉淀。由8名评审员通过两点识别法来评价饮料(2)与比较饮料(2)的风味哪个更好。其结果是,8名中8名评价为:与比较饮料(2)相比,饮料(2)明显风味更好。根据该结果可知,与hmb钙盐相比,获得的hmb精氨酸盐的改善溶解性以及风味的效果更优良。参照特定方式对本发明详细地进行了说明,但是,对于本领域技术人员显而易见的是,在不脱离本发明的精神和范围的情况下能够进行各种变更以及修正。需要说明的是,本申请基于2016年6月24日提出的日本专利申请(日本特愿2016-125280),通过引用而援引其整体。此外,本申请中所引用的全部参考均作为整体并入。产业上的可利用性根据本发明,可提供例如作为健康食品、药品、化妆品等的制品、原料或中间体等有用的hmb氨基酸盐无水物的晶体及其制造方法。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1