不对称模板和核酸测序的不对称方法与流程
本发明涉及核酸测序的领域,且更具体地,涉及制备用于核酸测序的环状模板。
发明背景
环状模板用于测序的用途是本领域已知的。例如,pacificbiosciences使用smrtbell™衔接子来产生此类模板。参见美国专利号7,302,146和8,153,375。环状单链模板在边合成边测序中具有若干优点:如果测序聚合酶可以进行滚环复制,则将多次读取模板并且将读取watson链和crick链。配对链的多重读取允许更准确的共有序列输出。然而,现有的环状模板被设计为使两个测序聚合酶结合各模板。两个聚合酶有可能相互干扰并引起合成的停滞或终止,产生次优的测序数据。本发明改进现有技术以实现更准确的测序读取。
发明概述
在一些实施方案中,本发明是测定样品中双链靶核酸的序列的方法,其包括:使包含双链靶核酸的样品与包含双链茎区域和单链环区域的发夹衔接子分子接触;将靶核酸分子的每个末端连接至衔接子分子的双链区域,由此形成环状接合分子,其包含靶核酸且具有双链区域和与双链区域共价连接的近端单链环区域和远端单链环区域;使样品与栓系至固体支持物的限定浓度的阻断寡核苷酸接触,其中所述阻断寡核苷酸不可通过核酸聚合酶延伸,并且与近端和远端单链环区域互补,由此将所述环状接合分子捕获在固体支持物上并阻断近端单链环区域;使所述样品和与近端和远端单链环区域互补的寡核苷酸引物接触,由此使所述引物与所述远端单链环区域杂交;用测序聚合酶延伸所述引物,由此测定双链靶核酸的序列。在一些实施方案中,所述靶核酸和所述衔接子的末端是平端的。在一些实施方案中,通过酶促处理使所述靶核酸和所述衔接子的末端粘性。酶促处理可以是核苷酸添加和用限制性内切核酸酶消化所述靶核酸和所述衔接子。所述阻断寡核苷酸可以经由选自与支持物分子的共价键或与支持物分子的非共价键的方式栓系至固体支持物。与支持物分子的非共价键可以是选自以下的特异性相互作用:生物素-链霉抗生物素蛋白、抗体-抗原或阻断寡核苷酸与共价或非共价连接至固体支持物的互补寡核苷酸的杂交。所述阻断寡核苷酸不可通过核酸聚合酶延伸。通过选自3’-h、2’-磷酸酯和3’-磷酸酯的化学修饰,可以使所述阻断寡核苷酸不可通过核酸聚合酶延伸。所述阻断寡核苷酸可以具有防止核酸聚合酶的结合的修饰。凭借经由其3’-末端连接至固体支持物,所述阻断寡核苷酸不可通过核酸聚合酶延伸。所述阻断寡核苷酸可以包含一种或多种双链体稳定化修饰,诸如lna、pna和非天然核苷酸。所述阻断寡核苷酸包含一种或多种阻断核酸酶消化的修饰,诸如硫代磷酸酯骨架。固体支持物的每个颗粒连接至多个阻断寡核苷酸。在一些实施方案中,所述方法可以进一步包括去除未捕获在固体支持物上的环状分子的步骤。测序可以是单分子测序、边合成边测序、纳米孔测序或隧道识别测序。在一些实施方案中,延伸引物是通过链置换聚合酶或通过滚环复制。在一些实施方案中,所述双链靶核酸在体外由单链靶核酸生成。
在一些实施方案中,本发明是测定样品中双链靶核酸的序列的方法,其包括:使包含双链靶核酸的样品与第一和第二发夹衔接子分子的混合物接触,所述第一和第二发夹衔接子分子各自包含双链茎区域和第一单链环区域或第二单链环区域;将靶核酸分子的每个末端连接至衔接子分子的双链区域,由此形成环状接合分子,其包含靶核酸且具有双链区域和与双链区域共价连接的在一个末端的第一单链环区域和在另一末端的第二单链环区域;使样品与栓系至固体支持物的限定浓度的阻断寡核苷酸接触,其中所述阻断寡核苷酸不可通过核酸聚合酶延伸,并且与第一单链环区域互补,由此将所述环状分子捕获在固体支持物上并阻断第一单链环区域;使所述样品和与第二单链环区域互补的寡核苷酸引物接触,由此使所述引物与第二单链环区域杂交;用测序聚合酶延伸所述引物,由此测定双链靶核酸的序列。所述靶核酸和所述衔接子的末端可以是平端的,或通过可以选自核苷酸添加和用限制性内切核酸酶消化所述靶核酸和所述衔接子的酶促处理来使其粘性。在一些实施方案中,所述阻断寡核苷酸经由选自与支持物分子的共价键或与支持物分子的非共价键的方式栓系至固体支持物。与支持物分子的非共价键可以是选自以下的特异性相互作用:生物素-链霉抗生物素蛋白、抗体-抗原或阻断寡核苷酸与共价或非共价连接至固体支持物的互补寡核苷酸的杂交。由于例如选自3’-h、2’-磷酸酯和3’-磷酸酯的化学修饰,所述阻断寡核苷酸不可通过核酸聚合酶延伸。所述阻断寡核苷酸可以具有防止核酸聚合酶的结合的修饰。凭借经由其3’-末端连接至固体支持物,所述阻断寡核苷酸不可通过核酸聚合酶延伸。所述阻断寡核苷酸可以包含一种或多种双链体稳定化修饰,诸如例如锁核酸(lna)、肽核酸(pna)和非天然核苷酸。所述阻断寡核苷酸可以包含一种或多种阻断核酸酶消化的修饰,例如硫代磷酸酯骨架。在一些实施方案中,固体支持物的每个颗粒连接至多个阻断寡核苷酸。在一些实施方案中,所述方法进一步包括去除未捕获在固体支持物上的核酸。在一些实施方案中,测序是单分子测序、边合成边测序、纳米孔测序或隧道识别测序。在一些实施方案中,延伸引物是通过链置换聚合酶或通过滚环复制。在一些实施方案中,所述双链靶核酸在体外由单链靶核酸生成。
在一些实施方案中,本发明是测定样品中双链靶核酸的序列的方法,其包括:使包含具有两个5’-末端和两个可延伸的3’-末端的双链靶核酸的样品与末端转移酶、单一可延伸的核苷酸种类接触,和提供用于控制通过末端转移酶的核苷酸并入的方式,通过并入单一核苷酸的多个单元延伸可延伸的3’-末端,由此形成线性接合分子,其包含靶核酸且具有双链区域和近端和远端单链同聚物区域;使样品与栓系至固体支持物的限定浓度的捕获寡核苷酸接触,其中所述捕获寡核苷酸与近端和远端单链同聚物区域互补,由此将线性分子捕获在固体支持物上;使所述样品和与近端和远端单链同聚物区域互补的寡核苷酸引物接触,由此使所述引物与所述远端单链同聚物区域杂交;用测序聚合酶延伸所述引物,由此测定双链靶核酸的序列。用于控制通过末端转移酶的核苷酸并入的方式是在反应中存在其比率有利于可延伸的核苷酸的终止子核苷酸种类,或并入反应的时间。在一些实施方案中,所述捕获寡核苷酸是可延伸的,且所述方法进一步包括延伸捕获寡核苷酸以到达靶核酸的末端。所述方法可以进一步包括将延伸的捕获寡核苷酸与靶核酸的末端连接以产生连续核酸链的步骤。所述阻断寡核苷酸可以经由选自与支持物分子的共价键或与支持物分子的非共价键的方式栓系至固体支持物。与支持物分子的非共价键可以是选自以下的特异性相互作用:生物素-链霉抗生物素蛋白、抗体-抗原或阻断寡核苷酸与共价或非共价连接至固体支持物的互补寡核苷酸的杂交。在一些实施方案中,所述阻断寡核苷酸包含一种或多种双链体稳定化修饰,诸如锁核酸(lna)、肽核酸(pna)和非天然核苷酸。在一些实施方案中,所述阻断寡核苷酸包含一种或多种阻断核酸酶消化的修饰,例如硫代磷酸酯骨架。在一些实施方案中,固体支持物的每个颗粒连接至多个阻断寡核苷酸。在一些实施方案中,所述方法进一步包括去除未捕获在固体支持物上的核酸的步骤。在一些实施方案中,每种线性分子具有通过如下产生的两种不同的同聚物:阻断靶核酸的近端末端,同时用包含第一非终止子核苷酸的混合物延伸远端末端,解开近端末端并用包含第二种非终止子核苷酸的混合物延伸近端末端。在一些实施方案中,所述测序是单分子测序、边合成边测序、纳米孔测序或隧道识别测序。在一些实施方案中,所述双链靶核酸在体外由单链靶核酸生成。
在一些实施方案中,本发明是用于测定双链靶核酸的序列的组合物,其包含:环状接合分子,其包含在每个末端连接至包含双链茎区域和单链环区域的衔接子分子的靶核酸,所述环状接合分子具有双链区域和与双链区域共价连接的近端单链环区域和远端单链环区域;栓系至固体支持物的阻断寡核苷酸,其中所述阻断寡核苷酸不可通过核酸聚合酶延伸,并且其与近端单链环区域杂交,由此将所述环状接合分子捕获在固体支持物上并阻断近端单链环区域;与远端单链环区域杂交的寡核苷酸引物;和测序聚合酶。
在一些实施方案中,本发明是用于测定双链靶核酸的序列的组合物,其包含:线性接合分子,其包含靶核酸且具有双链区域和近端和远端单链同聚物区域;捕获寡核苷酸,其拴系至固体支持物且与近端单链同聚物区域杂交,由此将线性分子捕获在固体支持物上;与远端单链同聚物区域杂交的寡核苷酸引物;和测序聚合酶。
附图简述
图1显示制备和测序环状模板的现有技术方法。与衔接子杂交的捕获探针包含如seqidno:7所示的序列加上与衔接子的发夹区域互补的额外序列。
图2显示本发明的方法的一个实施方案。与衔接子杂交的捕获探针包含如seqidno:8所示的序列加上与衔接子的发夹区域互补的额外序列。
图3显示图2中图示的结构的核苷酸序列细节的细节。发夹衔接子a包含seqidno:1中所示的序列。发夹衔接子b包含seqidno:2中所示的序列。捕获探针如seqidno:4所示。测序引物如seqidno:5所示。
图4显示具有同聚物的对称线性模板(seqidno:9)。
图5显示具有测序聚合酶的不对称加载的对称线性模板。(如seqidno:9所示的同聚物。)
图6显示图2中图示的结构的另一个实施方案的核苷酸序列细节的细节。发夹衔接子a包含seqidno:1中所示的序列。发夹衔接子c包含seqidno:3中所示的序列。珠粒连接的捕获序列如seqidno:10所示。测序引物如seqidno:5所示。
图7显示图2中图示的结构的另一个实施方案的核苷酸序列细节的细节。发夹衔接子a包含seqidno:1中所示的序列。发夹衔接子b包含seqidno:2中所示的序列。捕获探针/测序引物如seqidno:6所示。
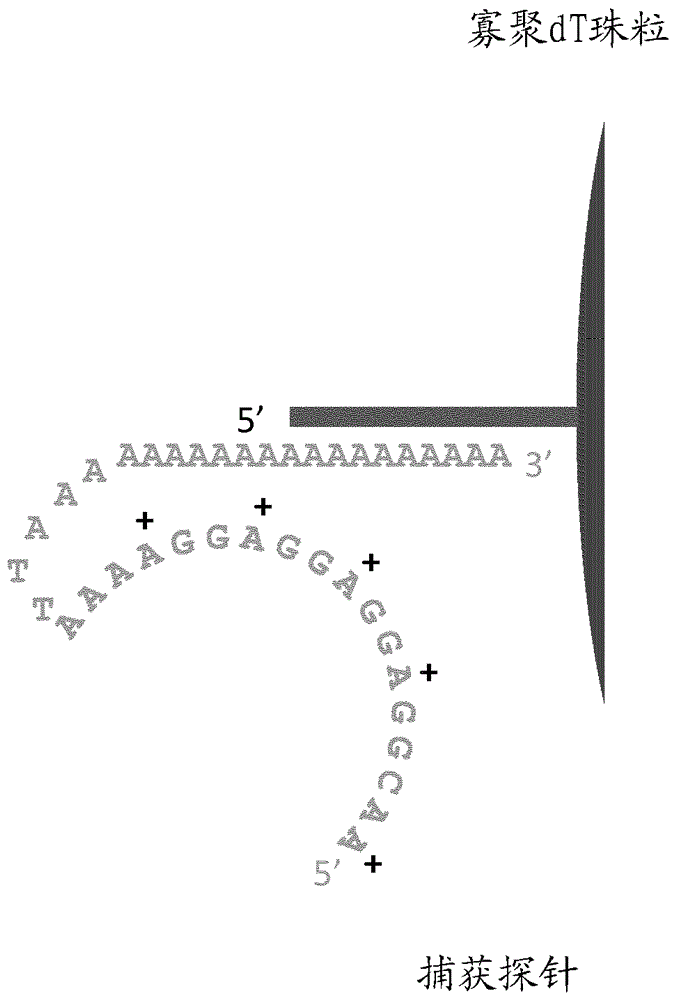
图8a-8f显示用于制备用于根据本发明的方法测序的测序文库的系列组装工作流程。工作流程用寡聚-dt捕获珠粒开始(图8a)。将捕获探针(seqidno:4)添加至捕获珠粒以形成捕获探针-捕获珠粒复合物(图8b)。使包含双链靶核酸分子和两个发夹衔接子(发夹衔接子a和b,分别包含seqidno:1和2)的环状测序模板与捕获探针-捕获珠复合物接触(图8c),以形成捕获珠粒、捕获探针和环状测序模板的复合物。然后添加测序引物(seqidno:5)(图8d)和测序聚合酶(图8e)。图8f显示当如图8a-8e中所示添加组分时组装的测序文库的组分的分析。仅当全部包括珠粒、捕获探针和文库分子时,才在最终组装的复合物中检测到所有三者。
发明详述
定义
术语“样品”是指含有或假定含有靶核酸的任何组合物。这包括从个体分离的组织或液体的样品,例如皮肤、血浆、血清、脊髓液、淋巴液、滑液、尿液、泪液、血细胞、器官和肿瘤,以及由取自个体的细胞建立的体外培养物的样品,包括福尔马林固定的石蜡包埋的组织(ffpet)和从其分离的核酸。样品还可以包括无细胞材料,诸如含有无细胞dna(cfdna)或循环肿瘤dna(ctdna)的无细胞血液级分。
术语“核酸”是指核苷酸(例如,天然和非天然的核糖核苷酸和脱氧核糖核苷酸)的聚合物,包括dna、rna及其亚类,诸如cdna、mrna等。核酸可以是单链或双链的并且将通常含有5'-3'磷酸二酯键,尽管在一些情况下,核苷酸类似物可以具有其它键。核酸可以包括天然存在的碱基(腺苷、鸟苷、胞嘧啶、尿嘧啶和胸苷)以及非天然碱基。非天然碱基的一些实例包括在例如seela等人,(1999)helv.chim.acta82:1640中描述的那些。非天然碱基可以具有特定功能,例如,增加核酸双链体的稳定性,抑制核酸酶消化或阻断引物延伸或链聚合。
术语“多核苷酸”和“寡核苷酸”可互换使用。多核苷酸是单链或双链核酸。寡核苷酸是有时用于描述较短多核苷酸的术语。寡核苷酸可以由至少6个核苷酸或约15-30个核苷酸构成。寡核苷酸通过本领域已知的任何合适的方法,例如,通过涉及直接化学合成的方法来制备,如以下所述:narang等人(1979)meth.enzymol.68:90-99;brown等人(1979)meth.enzymol.68:109-151;beaucage等人(1981)tetrahedronlett.22:1859-1862;matteucci等人(1981)j.am.chem.soc.103:3185-3191。
术语“引物”是指与靶核酸中的序列(“引物结合位点”)杂交且能够在适合于这种合成的条件下充当沿着核酸的互补链的合成起始点的单链寡核苷酸。
术语“衔接子”意指可以被添加至另一序列、以便将额外的特性输入该序列的核苷酸序列。衔接子通常是这样的寡核苷酸,其可以是单链或双链的,或者可以同时具有单链部分和双链部分。
术语“连接”是指接合两条核酸链的缩合反应,其中一个分子的5'-磷酸酯基团与另一个分子的3'-羟基基团反应。连接通常是由连接酶或拓扑异构酶催化的酶促反应。连接可以接合两条单链以产生一个单链分子。连接还可以接合两条链(每条链属于双链分子),因此接合两个双链分子。连接还可以将双链分子的两条链接合至另一双链分子的两条链,因此接合两个双链分子。连接还可以接合双链分子内的链的两个末端,因此修复双链分子中的切口。
术语“条形码”是指可以检测和标识的核酸序列。条形码可被并入其它核酸中。条形码足够长,例如2、5、10个核苷酸,使得在样品中,并入条形码的核酸可以根据条形码区分或分组。
术语“多重标识符”或“mid”是指标识靶核酸来源(例如,衍生出核酸的样品)的条形码。来自相同样品的所有或基本上所有靶核酸将共享相同的mid。可以将来自不同来源或样品的靶核酸混合并同时测序。使用mid,可以将序列读取分配至靶核酸来源的单个样品。
术语“独特分子标识符”或“uid”是指标识与其附接的核酸的条形码。来自相同样品的所有或基本上所有靶核酸将具有不同的uid。源自相同原始靶核酸的所有或基本上所有后代(例如,扩增子)将共享相同的uid。
术语“通用引物”和“通用引发结合位点”或“通用引发位点”是指存在于(通常,体外添加至)不同靶核酸的引物和引物结合位点。使用衔接子或使用具有5'-部分中的通用引发位点的靶特异性(非通用)引物将通用引发位点添加至多种靶核酸。所述通用引物可以结合通用引发位点并指导从通用引发位点的引物延伸。
如本文所用,术语“靶序列”、“靶核酸”或“靶标”是指待检测或分析的样品中核酸序列的一部分。术语靶标包括靶序列的所有变体,例如,一种或多种突变型变体和野生型变体。
术语“测序”是指确定靶核酸中核苷酸序列的任何方法。
本发明提供了测定样品中双链靶核酸的序列的方法,其包括:
(a)使包含双链靶核酸的样品与包含双链茎区域和单链环区域的发夹衔接子分子接触;
(b)将靶核酸分子的每个末端连接至衔接子分子的双链区域,由此形成环状接合分子,其包含靶核酸且具有双链区域和与双链区域共价连接的近端单链环区域和远端单链环区域;
(c)使样品与栓系至固体支持物的限定浓度的阻断寡核苷酸接触,其中所述阻断寡核苷酸不可通过核酸聚合酶延伸,并且与近端单链环区域互补,由此将所述环状接合分子捕获在固体支持物上并阻断近端单链环区域;
(d)使所述样品和与远端单链环区域互补的寡核苷酸引物接触,由此使所述引物与远端单链环区域杂交;
(e)用测序聚合酶延伸所述引物,由此测定双链靶核酸的序列。
或者,本发明提供了测定样品中双链靶核酸的序列的方法,其包括:
(a)使包含双链靶核酸的样品与第一和第二发夹衔接子分子的混合物接触,所述第一和第二发夹衔接子分子各自包含双链茎区域和第一单链环区域或第二单链环区域;
(b)将靶核酸分子的每个末端连接至衔接子分子的双链区域,由此形成环状接合分子,其包含靶核酸且具有双链区域和与双链区域共价连接的在一个末端的第一单链环区域和在另一末端的第二单链环区域;
(c)使样品与栓系至固体支持物的限定浓度的阻断寡核苷酸接触,其中所述阻断寡核苷酸不可通过核酸聚合酶延伸,并且与第一单链环区域互补,由此将所述环状分子捕获在固体支持物上并阻断第一单链环区域;
(d)使所述样品和与第二单链环区域互补的寡核苷酸引物接触,由此使所述引物与第二单链环区域杂交;
(e)用测序聚合酶延伸所述引物,由此测定双链靶核酸的序列。
在步骤(c)之后,可以去除未捕获在所述固体支持物上的接合分子。
所述靶核酸和所述衔接子的末端可以通过酶促处理变平或为粘性的。所述酶促处理可以选自核苷酸添加和用限制性内切核酸酶消化所述靶核酸和所述衔接子。所述阻断寡核苷酸可以经由选自与支持物分子的共价键或与支持物分子的非共价键的方式栓系至固体支持物。与支持物分子的非共价键可以是选自以下的特异性相互作用:生物素-链霉抗生物素蛋白、抗体-抗原或阻断寡核苷酸与共价或非共价连接至固体支持物的互补寡核苷酸的杂交。所述阻断寡核苷酸可以不可通过核酸聚合酶延伸,并且可以通过选自3’-h、2’-磷酸酯和3’-磷酸酯的化学修饰使得不可延伸。所述阻断寡核苷酸可以具有防止核酸聚合酶的结合的修饰。凭借经由其3’-末端连接至固体支持物,所述阻断寡核苷酸不可通过核酸聚合酶延伸。所述阻断寡核苷酸可以包含一种或多种双链体稳定修饰,其可以选自锁核酸(lna)、肽核酸(pna)和非天然核苷酸。所述阻断寡核苷酸可以包含一种或多种阻断核酸酶消化的修饰,例如硫代磷酸酯骨架。所述固体支持物可以由颗粒构成,并且每个颗粒可以连接至多种阻断寡核苷酸。
测序可以是单分子测序、边合成边测序、纳米孔测序或隧道识别测序。引物延伸可以通过链置换聚合酶和/或通过滚环复制进行。所述双链靶核酸可以在体外由单链靶核酸生成。
本发明还提供了测定样品中双链靶核酸的序列的方法,其包括:
(a)使包含具有两个5’-末端和两个可延伸的3’-末端的双链靶核酸的样品与末端转移酶和单一可延伸的核苷酸种类接触,和提供用于控制通过末端转移酶的核苷酸并入的方式;
(b)通过并入单一核苷酸的多个单元延伸可延伸的3’-末端,由此形成线性接合分子,其包含靶核酸且具有双链区域、近端单链同聚物区域和远端单链同聚物区域;
(c)使样品与栓系至固体支持物的限定浓度的捕获寡核苷酸接触,其中所述捕获寡核苷酸与近端和远端单链同聚物区域互补,由此将线性分子捕获在固体支持物上;
(d)使所述样品和与近端和远端单链同聚物区域互补的寡核苷酸引物接触,由此使所述引物与所述远端单链同聚物区域杂交;
(e)用测序聚合酶延伸所述引物,由此测定双链靶核酸的序列。
在步骤(c)之后,可以去除未捕获在所述固体支持物上的核酸。
用于控制通过末端转移酶的核苷酸并入的方式可以是在反应中存在其比率有利于可延伸的核苷酸的终止子核苷酸种类,或并入反应的时间。
如果捕获寡核苷酸不可延伸,则所述方法可以进一步包括在步骤(c)之后,延伸捕获寡核苷酸以到达靶核酸的末端。然后,所述方法可以进一步包括将延伸的捕获寡核苷酸与靶核酸的末端连接以产生连续核酸链的步骤。
所述阻断寡核苷酸可以经由选自与支持物分子的共价键或与支持物分子的非共价键的方式栓系至固体支持物。与支持物分子的非共价键可以是选自以下的特异性相互作用:生物素-链霉抗生物素蛋白、抗体-抗原或阻断寡核苷酸与共价或非共价连接至固体支持物的互补寡核苷酸的杂交。所述阻断寡核苷酸可以包含一种或多种双链体稳定修饰,诸如锁核酸(lna)、肽核酸(pna)或非天然核苷酸。所述阻断寡核苷酸可以包含一种或多种阻断核酸酶消化的修饰,诸如硫代磷酸酯骨架。所述固体支持物可以由颗粒构成,并且每个颗粒可以连接至多种阻断寡核苷酸。
每种线性分子可以具有通过如下产生的两种不同的同聚物:阻断靶核酸的近端末端,同时用包含第一非终止子核苷酸的混合物延伸远端末端,解开近端末端并用包含第二种非终止子核苷酸的混合物延伸近端末端。
测序可以是单分子测序、边合成边测序、纳米孔测序或隧道识别测序。所述双链靶核酸可以在体外由单链靶核酸生成。
在一些实施方案中,本发明是将双链靶核酸转化为可用于测序中的环状锁定链模板结构的方法。环状模板的使用是本领域已知的,并且在边合成边测序应用中具有若干优点。参见美国专利号7,302,146和8,153,375和图1。如果使用链置换聚合酶,它将参与滚环复制,即连续置换新生链,并进行多轮复制环状模板。对靶标进行多次测序(通读)并比较连接至环状结构中的靶核酸的watson链和crick链的能力允许生成无误差或低误差的共有序列。
然而,现有的环状模板被设计成具有与靶核酸的两个末端连接的衔接子。(图1)。每个衔接子具有用于测序引物的结合位点,其允许两个测序引物和两个测序dna聚合酶结合每个环状模板。一旦已经开始测序反应,两种聚合酶有可能相互干扰并引起合成的停滞或终止、降低测序数据的读取长度和产量。对于较短模板,这尤其有问题。在一些应用、诸如单分子边合成边测序中,每个检测点存在两个聚合酶(例如,纳米孔或零分子波导(zmw))将降低测序数据的质量。
本发明通过确保仅单一测序聚合酶与每种测序模板结合且仅在一个方向上进行合成而改进现有技术。(图2)。本发明是可以增加测序质量、读取长度和效率的新型方法。在本发明的实施方案中,双链靶核酸与两个衔接子(分子的每个末端一个)缀合。每个衔接子序列具有在该处起始测序的引物结合位点(例如,通用引物结合位点)。所得接合分子在一个末端被捕获,而第二末端仍然可用于测序聚合酶。(图2)。
本发明是产生用于测序靶核酸或靶核酸文库的模板的方法。在一些实施方案中,在第一步中,使靶核酸与包含双链茎区域和单链环区域的茎-环衔接子分子接触。将靶核酸的每个末端连接至衔接子,由此形成接合分子。如果衔接子具有茎-环结构,则所得接合分子具有双链区(包含靶核酸)和与双链区域共价连接的近端单链环区域和远端单链环区域。所述接合分子是由单一连续链构成的拓扑学闭合的环状分子。在一些实施方案中,在进一步处理前,从样品去除未连接的衔接子和未连接的靶核酸。
在一些实施方案中,所有衔接子分子都是相同的。在其它实施方案中,存在两种衔接子分子的混合物。在两种衔接子(例如,a和b)的相等混合物的情况下,50%的接合分子将具有所需不对称衔接子结构(例如,a-b)。
然后使接合分子与栓系至固体支持物的限定浓度的阻断寡核苷酸接触。阻断寡核苷酸也可以称为“捕获寡核苷酸”,因为它们可以用于捕获接合分子,例如在溶液中或在固体支持物上。捕获可以包括简单地与捕获寡核苷酸形成杂交复合物,或者捕获可以包括捕获在寡核苷酸可以栓系的固体支持物。限定浓度的阻断寡核苷酸用于确保两个衔接子-末端中仅一个被捕获或阻断,而另一个衔接子-末端仍可进入进一步酶促步骤。在每个接合分子具有两个不同衔接子的实施方案中,捕获寡核苷酸仅与一个衔接子互补,而不与另一个衔接子互补,确保仅捕获一个衔接子-末端。在每个接合分子在两个末端具有相同衔接子的实施方案中,阻断寡核苷酸与衔接子互补。限定浓度的阻断寡核苷酸的使用确保仅捕获一个衔接子-末端,而另一个衔接子-末端仍可接近。为方便起见,在本公开中,捕获的衔接子-末端被指定为近端,而游离衔接子-末端被指定为远端。
如从下面描述的下一步骤可以明显看出,阻断捕获寡核苷酸必须在其3’-末端不可通过核酸聚合酶延伸。捕获寡核苷酸与近端衔接子-末端至少部分互补,并与衔接子-末端的单链部分杂交,由此阻断衔接子-末端。因为阻断寡核苷酸的3’-末端是不可延伸的,所以在核酸聚合酶存在的情况下其不能充当链聚合的开始。任选地,可以在下一步骤前去除未捕获的接合分子。
接下来,使样品和与衔接子的单链区域中的引物结合位点互补的寡核苷酸引物接触。因为近端末端被阻断,所以只有远端末端可用于引物结合和杂交。所述引物可以用测序聚合酶延伸,由此测定双链靶核酸的序列。所述测序是边合成边测序,包括单分子测序或核酸或核酸衍生物的任何测序。测序技术可以包括pacbio®rs系统、纳米孔测序系统或隧道识别测序系统或其中可能和期望连续读取模板的任何测序系统。
在一些实施方案中,引物延伸通过链置换聚合酶进行。在一些实施方案中,引物延伸经由滚环复制发生,使得每个模板能够被单个聚合酶多次读取。
在该方法的一些实施方案中,侧接靶核酸的末端的衔接子是单链同聚物区域。不是如上述实施方案中所述将衔接子连接至靶核酸的末端,而是通过使样品与合适的酶和单一可延伸的核苷酸种类接触来延伸靶核酸的可延伸的3’-末端。合适的酶是模板非依赖性dna聚合酶,诸如例如,末端脱氧核苷酸转移酶(tdt)。依次添加一种核苷酸种类在靶核酸的两侧生成同聚物区域。在一些实施方案中,所述方法包括用于控制同聚物区域的尺寸的方式。控制可以通过在反应中存在其比率有利于可延伸的核苷酸的终止子核苷酸种类或并入反应的时间来完成。合适的酶可以是末端转移酶。
在该实施方案中,所述接合分子是包含靶核酸且具有双链区域和近端和远端单链同聚物区域的线性分子。在该实施方案中,捕获寡核苷酸可以与同聚物区域互补并且能够捕获单链同聚物区域,由此将线性接合分子捕获在固体支持物上。捕获在固体支持物上的同聚物区域被称为近端区域,且游离区域为远端区域。如在本发明的其它实施方案中,所述测序引物能够结合游离的远端同聚物区域并与游离的远端同聚物区域杂交并引发引物延伸。在一些实施方案中,所述方法进一步包括去除未捕获在固体支持物上的核酸的步骤。
在一些实施方案中,每个线性分子具有两个不同的同聚物,其通过依次阻断靶核酸的一个末端,同时用不同的核苷酸延伸另一个末端而产生。在此类实施方案中,所述捕获寡核苷酸和所述引物与所述接合分子的相对侧上的同聚物互补。
本发明包括检测样品中的靶核酸。在一些实施方案中,所述样品来源于受试者或患者。在一些实施方案中,所述样品可以包含例如通过活检来源于受试者或患者的实体组织或实体瘤的片段。所述样品还可以包括体液(例如,尿液、痰液、血清、血浆或淋巴液、唾液、痰液、汗液、泪液、脑脊髓液、羊水、滑液、心包液、腹膜液、胸膜液、囊液、胆汁、胃液、肠液和/或粪便样品)。所述样品可以包括可存在肿瘤细胞的全血或血液级分。在一些实施方案中,所述样品,尤其是液体样品,可以包含无细胞材料,诸如无细胞dna或rna,包括无细胞肿瘤dna或肿瘤rna。在一些实施方案中,所述样品是无细胞样品,例如无细胞血液来源的样品,其中存在无细胞肿瘤dna或肿瘤rna。在其它实施方案中,所述样品是含有或怀疑含有感染病原体或源自感染病原体的核酸的培养的样品,例如,培养物或培养上清液。在一些实施方案中,所述感染病原体是细菌、原生动物、病毒或支原体。
靶核酸是可以存在于样品中的目标核酸。在一些实施方案中,所述靶核酸是基因或基因片段。在其它实施方案中,所述靶核酸含有遗传变体,例如,多态性,包括单核苷酸多态性或单核苷酸变体(snp或snv),或导致例如基因融合的遗传重排。在一些实施方案中,所述靶核酸包含生物标志物。在其它实施方案中,所述靶核酸是特定生物体特征性的,例如,有助于鉴定病原生物体或病原生物体的特征,例如,药物敏感性或药物抗性。在还有其它实施方案中,所述靶核酸是人受试者特征性的,例如,定义受试者的独特hla或kir基因型的hla或kir序列。在还有其它实施方案中,样品中的所有序列都是靶核酸,例如,在鸟枪基因组测序中。
在本发明的一个实施方案中,将双链靶核酸转化为本发明的模板构型。在一些实施方案中,所述靶核酸在自然界中以单链形式(例如,rna,包括mrna、微小rna、病毒rna;或单链病毒dna)存在。将单链靶核酸转化为双链形式以实现请求保护的方法的另外的步骤。尽管在一些应用中可能需要更长的靶核酸以实现更长的读取,但可以将更长的靶核酸片段化。在一些实施方案中,所述靶核酸是天然片段化的,例如,循环的无细胞dna(cfdna)或化学降解的dna,诸如在保存的样品中发现的dna。
在本发明的一些实施方案中,所述衔接子分子连接至所述靶核酸。所述连接可以是平末端连接或更有效的粘性末端连接。可以通过链填充,即通过dna聚合酶延伸3'-端以消除5'-突出端,使靶核酸或衔接子末端变平。在一些实施方案中,通过将单个核苷酸添加至衔接子的3'-末端并将单个互补核苷酸添加至靶核酸的3'-末端,例如通过dna聚合酶或末端转移酶,可以使平末端的衔接子和靶核酸粘性。在还有其它实施方案中,所述衔接子和所述靶核酸可以通过用限制性内切核酸酶消化而获得粘性末端(突出端)。后一种选择对于已知含有限制性酶识别位点的已知靶序列更有利。在每个上述实施方案中,所述衔接子分子可以通过下文进一步描述的合成衔接子寡核苷酸的设计获得所需末端(平端、单碱基延伸或多碱基突出端)。在一些实施方案中,可能需要其它酶促步骤来完成连接。在一些实施方案中,可以使用多核苷酸激酶将5'-磷酸酯添加至靶核酸分子和衔接子分子。
本发明包括待连接至所述靶核酸的一个或两个末端的衔接子分子的用途。在一些实施方案中,衔接子是采用茎-环二级结构的核酸的单链,所述茎-环二级结构包含至少一个双链区域和至少一个单链区域。双链区域包含具有至少部分自身互补性的区域,确保二级结构在本文所用的反应条件下的稳定性。在一些实施方案中,所述衔接子分子是体外合成的人工序列。在其它实施方案中,所述衔接子分子是已知具有所需二级结构的体外合成的天然存在的序列。在还有其它实施方案中,所述衔接子分子是分离的天然存在的分子或分离的非天然存在的分子。
在一些实施方案中,所述衔接子包含至少一个双链区域和至少一个单链区域。在一些实施方案中,所述衔接子形成具有至少一个双链茎和至少一个单链环的茎-环二级结构。在一些实施方案中,双链茎用于连接至双链靶核酸。在其它实施方案中,衔接子的单链部分被连接至靶核酸的单链部分。在一些实施方案中,使用夹板寡核苷酸进行连接单链核酸,参见例如美国申请公开号20120003657。在其它实施方案中,使用5'-和3'-末端单链区域(突出端)进行连接单链核酸或部分单链核酸,参见例如美国申请公开号20140193860。
在一些实施方案中,所述衔接子包含一个或多个条形码:多重样品id(mid)、独特id(uid)或uid和mid的组合。在一些实施方案中,单一条形码用作uid和mid两者。
在一些实施方案中,所述衔接子包含通用引物(例如通用测序引物)的引物结合位点。在一些实施方案中,所述衔接子包含捕获寡核苷酸的结合位点。在一些实施方案中,本发明的方法中使用的衔接子是包含引物的结合位点的衔接子和包含捕获寡核苷酸的结合位点的衔接子的混合物。
在一些实施方案中,本发明包括捕获寡核苷酸的用途。在一些实施方案中,捕获寡核苷酸直接与固体支持物结合。在该实施方案中,捕获寡核苷酸包含在一个末端的结合部分和在另一个末端的游离末端。捕获寡核苷酸经由结合部分栓系至固体支持物(例如,珠粒、微球体)。在一些实施方案中,寡核苷酸的栓系末端包含生物素,且固体支持物用链霉抗生物素蛋白包被。在其它实施方案中,寡核苷酸的栓系末端包含捕获分子,且固体支持物包含对捕获分子特异性的抗体。例如,可以使用洋地黄毒苷和抗洋地黄毒苷抗体。
在一些实施方案中,捕获寡核苷酸不与固体支持物直接结合,但与通过上述任何方法直接连接至固体支持物的另一寡核苷酸(“珠粒寡核苷酸”)杂交。捕获寡核苷酸和珠粒寡核苷酸共享至少一个互补区域。例如,珠粒寡核苷酸可以包含dt的同聚物(寡聚-dt),而捕获寡核苷酸的一部分是da的同聚物(寡聚-da)。(图3、6和7)。
在一些实施方案中,所述阻断寡核苷酸不可通过核酸聚合酶在3’-末端延伸。通过化学修饰可使3’-末端不可延伸。例如,3’-h、2’-磷酸酯和3’-磷酸酯是此类修饰。所述阻断寡核苷酸可以具有防止核酸聚合酶的结合的修饰,例如在空间上阻断3’-末端的大体积加合物。凭借经由其3’-末端连接至固体支持物,可使所述阻断寡核苷酸不可延伸。所述阻断寡核苷酸还可以包含一种或多种阻断核酸酶消化的修饰,诸如硫代磷酸酯骨架。
在一些实施方案中,所述寡核苷酸包含游离的5’-末端且具有与固体支持物栓系的3’-末端。在其它实施方案中,所述寡核苷酸包含游离的3’-末端且具有与固体支持物栓系的5’-末端。游离的5’-末端或3’-末端的至少一部分与衔接子中的序列互补。在一些实施方案中,游离末端与衔接子的单链部分互补,例如与环结构互补。经由该互补部分,栓系至固体支持物的捕获寡核苷酸与包含连接至至少一个衔接子的靶核酸的接合分子杂交。捕获寡核苷酸可以包含一种或多种稳定所述杂交体的修饰。在一些实施方案中,所述修饰选自锁核酸(lna)、肽核酸(pna)、非天然核苷酸,诸如7-氮杂嘌呤(例如,7-氮杂鸟嘌呤、7-氮杂腺嘌呤等)、吡唑并[3,4-d]嘧啶、丙炔基-dn(例如,丙炔基-du、丙炔基-dc等)等,如例如美国专利号5,990,303中所述。
在一些实施方案中,所述方法涉及产生接合分子。所述接合分子包含与一个或多个衔接子分子连接的双链靶核酸。在一些实施方案中,所述接合分子是拓扑学环状(闭合)单链,其包含双链区域(包含靶核酸),其在每个末端侧接闭环单链区域(包含衔接子序列)。
在一些实施方案中,所述接合分子具有相同的末端,即连接至两个相同的衔接子。在其它实施方案中,所述接合分子包含不同的末端,每个末端连接至不同的衔接子分子。在一些实施方案中,所述衔接子分子是两种类型的衔接子(例如,a和b)的混合物。然后,所述样品包含特定比率的具有衔接子aa、ab和bb的接合分子的混合物。在一些实施方案中,使用相等比率的a和b。50%的所得接合分子将具有所需结构a-b。25%将是a-a,即没有测序引物的结合位点,且25%将是b-b,如用于现有技术中的测序引物的两个位点。在此类情况下,本发明将提供相对于现有技术的改进,因为将根据改进的方法处理2/3的接合分子(a-b)以生成改进的读取。
在一些实施方案中,所述接合分子是包含双链区域的线性分子,所述双链区域包含在每个末端侧接衔接子或类似序列的靶核酸。在一些实施方案中,所述衔接子是线性双链分子。在其它实施方案中,所述衔接子可以是线性单链分子。在还有其它实施方案中,包含靶核酸的双链区域侧接一个或两个同聚物。
在一些实施方案中,本发明利用酶。所述酶包括dna聚合酶(包括测序聚合酶)、dna连接酶和末端转移酶。
在一些实施方案中,所述dna聚合酶具有链置换活性并且不具有5'-3-外切核酸酶活性。在一些实施方案中,使用phi29聚合酶及其衍生物。参见美国专利号5,001,050、5576204、7858747和8921086。
在一些实施方案中,本发明还利用dna连接酶。在一些实施方案中,使用t4dna连接酶或大肠杆菌dna连接酶。
在一些实施方案中,本发明还利用模板非依赖性dna聚合酶,例如末端转移酶。在一些实施方案中,本发明使用哺乳动物末端转移酶。
在一些实施方案中,本发明是用于测定双链靶核酸的序列的组合物,其包含:环状接合分子,其包含靶核酸且具有双链区域和与双链区域共价连接的近端单链环区域和远端单链环区域,所述近端区域与不可通过核酸聚合酶延伸的阻断寡核苷酸杂交。所述阻断寡核苷酸可以栓系至固体支持物。在一些实施方案中,所述组合物进一步包含与近端和远端单链环区域互补的寡核苷酸引物和任选核酸聚合酶。
在一些实施方案中,本发明是用于测定双链靶核酸的序列的组合物,其包含:线性接合分子,其包含靶核酸且具有双链区域和近端和远端单链同聚物区域,其中所述近端同聚物区域与不可通过核酸聚合酶延伸的阻断寡核苷酸杂交。所述阻断寡核苷酸可以栓系至固体支持物。在一些实施方案中,所述组合物进一步包含与近端和远端单链环区域互补的寡核苷酸引物和任选核酸聚合酶。
实施例
实施例1(预测性)制备对称调整的环状接合分子,用于用测序聚合酶的不对称加载的测序
在该实验中,获得双链靶dna。dna在体外片段化成合适的大小或者是天然片段化的。衔接子是具有双链部分和环部分的发夹分子。将相同的衔接子连接至靶dna的每个末端以产生接合分子,如pacificbiosciences®templatepreparationandsequencingguide(2012)pacificbiosciencesofcalifornia,inc.和美国专利8,153,375中所述。参见图2a。捕获寡核苷酸与衔接子分子的单链部分互补(图2b)。捕获寡核苷酸还包含与结合至聚苯乙烯包被的磁珠(dynabeads®,thermofisher,waltham,mass.)的多聚-dt寡核苷酸互补的多聚-da部分(参见图2a)。捕获寡核苷酸具有几个lna碱基,其稳定与衔接子的复合物(参见图2a和图2b)。因此,另一衔接子可用于聚合酶加载和测序起始。测序引物与衔接子的单链部分互补,且测序聚合酶能够延伸引物,由此进行测序反应。以图2所示的顺序添加组分。
与珠粒结合的捕获寡核苷酸的浓度相比过量的接合分子(高文库:珠粒比率)确保仅在一端捕获足够量的接合分子且一端可用于测序。
测序如仪器的制造商所预期进行。
实施例2(预测性)制备不对称调整的环状接合分子用于测序
在该实验中,获得双链靶dna。dna在体外片段化成合适的大小或者是天然片段化的。衔接子是具有双链部分和环部分的发夹分子。添加等量的两种衔接子的混合物。衔接子至少在环序列中不同。将衔接子连接至靶dna的每个末端以产生接合分子,如pacificbiosciences®templatepreparationandsequencingguide(2012)pacificbiosciencesofcalifornia,inc.和美国专利8153375中所述。参见图2a。捕获寡核苷酸与衔接子分子的单链部分互补(图2b)。捕获寡核苷酸还包含与结合至聚苯乙烯包被的磁珠(dynabeads®,thermofisher,waltham,mass.)的多聚-dt寡核苷酸互补的多聚-da部分(参见图2a)。捕获寡核苷酸具有几个lna碱基,其稳定与衔接子的复合物(参见图2a和图2b)。因此,另一衔接子可用于聚合酶加载和测序起始。测序引物与衔接子的单链部分互补,且测序聚合酶能够延伸引物,由此进行测序反应。以图2所示的顺序添加组分。测序如仪器的制造商所预期进行。
实施例3(预测性)制备不对称调整的线性接合分子用于测序
在该实验中,获得双链靶dna。dna在体外片段化成合适的大小或者是天然片段化的靶dna的每个3’-末端用末端转移酶和与少量二脱氧核苷酸(例如,ddctp)混合的单一核苷酸(例如,datp)延伸。靶dna在每个末端都具有同聚物。(图4、5)捕获寡核苷酸与固体支持物直接结合,并与同聚物互补(例如,具有寡聚-dt)(图4、5)。所述固体支持物包括聚苯乙烯包被的磁珠(dynabeads®,thermofisher,waltham,mass.)。所述同聚物可用于聚合酶加载和测序起始。
为了防止两个聚合酶加载在相同模板上(图4),用dttp和dna聚合酶延伸捕获寡核苷酸的3’-末端,使其不能用于测序引物。捕获寡核苷酸用dttp和ddttp的混合物延伸,以使延伸产物不可进一步延伸。或者,捕获寡核苷酸用dttp延伸并经由连接与靶标的5’-末端接合。
实施例4:用于测序的不对称调整的线性接合分子的工作流程组装
在该实验中,如图8a-8f中显示,使用系列组装工作流程来制备用于根据本发明的方法测序的测序文库。工作流程用如上所述的寡聚-dt捕获珠粒开始(图8a)。将捕获探针(seqidno:4)添加至捕获珠粒以形成捕获探针-捕获珠粒复合物(图8b)。使包含双链靶核酸分子和两个发夹衔接子(发夹衔接子a和b,分别包含seqidno:1和2)的环状测序模板与捕获探针-捕获珠复合物接触(图8c),以形成捕获珠粒、捕获探针和环状测序模板的复合物。然后添加测序引物(seqidno:5)(图8d)和测序聚合酶(图8e)。图8f显示当如图8a-8e中所示添加组分时组装的测序文库的组分的分析的结果。仅当珠粒、捕获探针和文库分子全部包括时,才在最终组装的复合物中检测到所有三者。
同聚物现在两种同聚物中仅一种可用于聚合酶加载和测序起始。测序引物与同聚物互补(例如,具有寡聚-dt),且测序聚合酶能够延伸引物,由此进行测序反应。以图2所示的顺序添加组分。测序如仪器的制造商所预期进行。
- 还没有人留言评论。精彩留言会获得点赞!