多肽及结合多肽的抗体的制作方法
本发明属于生物医药领域,具体涉及pro-bdnf的多肽片段及结合多肽片段的蛋白,还涉及pro-bdnf的多肽片段的用途。
背景技术:
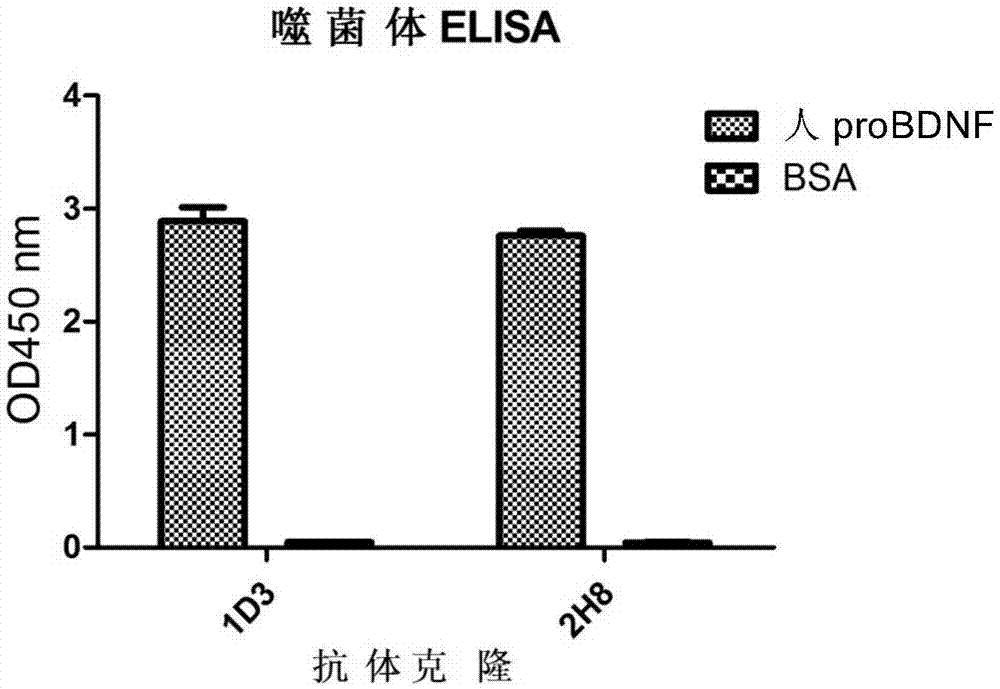
:自身免疫性疾病(aid)是指自身免疫耐受被打破,激活免疫系统攻击自身抗原,引起组织器官损害的一类疾病。其病因和发病机制尚不清楚,目前认为是由自身抗体,自身反应性t淋巴细胞或者二者共同引起的针对自身抗原的超敏反应性疾病。临床尚无根治药物,传统的糖皮质激素和免疫抑制剂适时应用能够控制病情,提高患者生存率,但长期使用会带来一系列副反应,严重时可影响患者生活质量,甚或威胁生命,而且还有部分患者对糖皮质激素和免疫抑制剂治疗不敏感。近年来随着对aid分子机制的深入了解,新的治疗策略不断被提出,包括基因治疗、表观遗传干预、小分子toll样受体抑制剂、抗炎症因子抗体、干细胞和调节性t细胞自体回输、树突状细胞疫苗等。这些治疗药物或方法有些已经用于临床,有些还处于临床研究阶段(如干细胞自体回输治疗等)甚至动物实验阶段(如表观遗传调控等)。但是,这些药物无法取代糖皮质激素成为一线药物,因此迫切需要新的安全有效治疗药物和方法应用于临床。技术实现要素:本发明的目的在于提供一种多肽,利用该多肽能够获得与其特异性结合的抗体;而所述抗体能够有效用于自身免疫性疾病的治疗。在第一方面,本发明提供一种多肽,所述多肽包含seqidno:41所示的氨基酸序列。在优选的实施方式例中,所述多肽的氨基酸序列如seqidno:41所示。在第二方面,本发明提供一种多肽,所述多肽包含seqidno:44所示的氨基酸序列。在优选的实施方式中,所述多肽的氨基酸序列如seqidno:44所示。在第三方面,本发明提供一种多肽,所述多肽包含seqidno:47所示的氨基酸序列。在优选的实施方式中,所述多肽的氨基酸序列如seqidno:47所示。在具体的实施方式中,本发明提供本发明第一-第三方面任一所述的多肽的编码多核苷酸。在具体的实施方式中,本发明提供一种表达载体,包含本发明的编码多核苷酸。在具体的实施方式中,本发明提供本发明第一-第三方面任一所述的多肽在筛选或制备其特异性抗体中的用途。在第四方面,本发明提供特异性结合本发明第一-第三方面任一所述的多肽的蛋白。在具体的实施方式中,所述蛋白与人pro-bdnf的结合亲和力<10nm。在具体的实施方式中,所述蛋白是抗体。在优选的实施方式中,所述抗体为单克隆抗体、多克隆抗体、或抗体片段。在优选的实施方式中,所述抗体可选自嵌合抗体、人源化抗体或全人抗体。在具体的实施方式中,所述抗体的轻链可变区具有:seqidno:4或seqidno:14所示的cdr1;seqidno:5或seqidno:15所示的cdr2;和seqidno:6或seqidno:16所示的cdr3。在具体的实施方式中,所述抗体的轻链可变区具有:seqidno:4所示的cdr1、seqidno:5所示的cdr2、和seqidno:6所示的cdr3;或seqidno:14所示的cdr1、seqidno:15所示的cdr2、和seqidno:16所示的cdr3。在具体的实施方式中,所述抗体的重链可变区具有:seqidno:1或seqidno:11所示的cdr1;seqidno:2或seqidno:12所示的cdr2;和seqidno:3或seqidno:13所示的cdr3。在具体的实施方式中,所述抗体的重链可变区具有:seqidno:1所示的cdr1、seqidno:2所示的cdr2、和seqidno:3所示的cdr3;或seqidno:11所示的cdr1、seqidno:12所示的cdr2、和seqidno:13所示的cdr3。在具体的实施方式中,所述抗体选自:抗体(a):重链可变区含有seqidno:1、seqidno:2和seqidno:3所示的序列,轻链可变区含有seqidno:4、seqidno:5和seqidno:6所示的序列;抗体(b):重链可变区含有seqidno:11、seqidno:12和seqidno:13所示的序列,轻链可变区含有seqidno:14、seqidno:15和seqidno:16所示的序列;抗体(c):抗体(a)或抗体(b)的变体,其具有或基本上具有抗体(a)或抗体(b)的活性。在优选的实施方式中,所述抗体(c)是在抗体(a)的seqidno:1、seqidno:2、seqidno:3、seqidno:4、seqidno:5或seqidno:6所示的序列中通过一个或多个,例如1-3,优选1个氨基酸的添加、缺失或取代(优选取代)得到的,并且具有或基本上具有抗体(a)的活性;或者所述抗体(c)是在抗体(b)的seqidno:11、seqidno:12、seqidno:13、seqidno:14、seqidno:15、seqidno:16所示的序列中通过一个或多个,例如1-3,优选1个氨基酸的添加、缺失或取代(优选取代)得到的,并且具有或基本上具有抗体(b)的活性。在优选的实施方式中,所述氨基酸取代是保守性氨基酸取代。在具体的实施方式中,所述抗体选自:抗体(d):具有seqidno:7所示的重链可变区和seqidno:8所示的轻链可变区;抗体(e):具有seqidno:17所示的重链可变区和与seqidno:18所示的轻链可变区;抗体(f):抗体(d)或抗体(e)的变体,其具有或基本上具有抗体(d)或抗体(e)的活性。在优选的实施方式中,所述抗体(f)是在抗体(d)的seqidno:7或seqidno:8所示的序列中通过一个或多个,例如1-10,优选1-6,更优选1-3,最优选1个氨基酸的添加、缺失或取代(优选取代)得到的,并且具有或基本上具有抗体(f)的活性;或者所述抗体(f)是在抗体(e)的seqidno:17或seqidno:18所示的序列中通过一个或多个,例如1-10,优选1-6,更优选1-3,最优选1个氨基酸的添加、缺失或取代(优选取代)得到的,并且具有或基本上具有抗体(f)的活性。在优选的实施方式中,所述抗体具有以下一种或多种特性:i)以10nm或更低的kd结合pro-bdnf多肽;ii)竞争性抑制pro-bdnf与p75的结合;和iii)依赖pro-bdnf的活性在具体的实施方式中,所述蛋白利用本发明第一-第三方面任一所述的多肽免疫动物得到或者采用本发明第一-第三方面任一所述的多肽进行噬菌体库的筛选得到。在第五方面,本发明提供一种药物组合物,所述药物组合物包含本发明第四方面所述的蛋白以及任选的一种或多种药学上可接受的赋形剂、稀释剂或运载体。在第六方面,本发明提供本发明第四方面所述的蛋白的用途,用于制备预防、治疗或诊断自身免疫性疾病的药物。在优选的实施方式中,所述自身免疫疾病是pro-bdnf介导的自身免疫疾病。在第七方面,本发明提供本发明第四方面所述的蛋白的用途,用于制备预防、治疗或诊断pro-bdnf介导的疾病的药物。在具体的实施方式中,所述疾病为关节炎、类风湿性关节炎、强直性脊柱炎、再生不良性贫血、银屑病、胰岛素依赖型糖尿病、多发性硬化症、冷球蛋白血症、慢性阻塞性肺疾病、系统性红斑狼疮(sle)、狼疮性肾炎、哮喘、多发性硬化或囊性纤维化。在第八方面,本发明提供本发明第四方面所述的蛋白的用途,用于制备通过抑制tnf-α、il-2、il-6或il-4分泌来预防、治疗或诊断的疾病的药物。在第九方面,本发明提供本发明第四方面所述的蛋白的用途,用于制备缓解疼痛的药物。在第十方面,本发明提供编码本发明第四方面所述的蛋白的核酸。在第十一方面,本发明提供一种抗体的筛选方法,采用本发明第一-第三方面任一所述的多肽免疫动物或者采用本发明第一-第三方面任一所述的多肽进行噬菌体库的筛选。应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。附图说明图1为1d3和2h8对人probdnf前体蛋白的结合能力的elisa结合图;图2为纯化的重组单克隆抗体1d3和2h8(人igg1形态);图3为1d3在biacore亲和力测定实验中的动力学曲线;图4为2h8在biacore亲和力测定实验中的动力学曲线;图5a为给予2h8治疗实验性自身免疫性脑脊髓炎(eae)的实验,图5b为2h8治疗eae的累积治疗评分;图6a为给予1d3治疗实验性自身免疫性脑脊髓炎(eae)的实验,图6b为1d3治疗eae的累积治疗评分;图7a显示炎症因子tnf-α基因表达情况,图7b显示了ab-prob对eae小鼠脾脏白细胞介素(il)-6的作用,图7c显示了ab-prob对eae小鼠脾脏il-2的作用,图7d显示了ab-prob对eae小鼠脾脏il-4的作用;图8显示了1d3和2h8与多肽e2和多肽e5的elisa结果;图9显示了1d3和2h8与多肽dh的elisa结果。具体实施方式发明人经过广泛而深入的研究,出乎意料地发现特异性结合pro-bdnf的抗体,这些抗体能够在体内实验性自身免疫性脑脊髓炎模型中降低tnf-α、il-2、il-6、或il-4分泌,同时对这些抗体的结合表位进行了分析,在此基础上完成了本发明。术语本文采用的科技术语具有与本领域技术人员常规理解的相同或相似的含义。为便于理解本发明,一些术语定义如下。术语“probdnf”(precursorforbrain-derivedneurotrophicfactor)为“脑源性神经营养因子的前体”,是bdnf基因的前体产物。除非另外描述,否则术语“pro-bdnf”是指序列如seqidno:27所示的人pro-bdnf。probdnf的分子氨基酸序列第1-18位点是信号肽序列,在分泌的过程中在这个位点产生2个片段,其中一个片段是包含序列第19-129位氨基酸即前体结构域的多肽片段,称为前体结构域(probdnfpro-domain),另一个片段则是氨基酸序列第130-247即成熟结构域所编码的片段,经加工后形成有生物活性的成熟bdnf。术语“p75”为神经营养因子受体(p75neurotrophinreceptor,p75ntr),也称cd271,是probdnf的配体。本文所用的术语“本发明的蛋白”或“本发明蛋白”表示与本发明的多肽结合的蛋白。本发明的多肽具体是指包含seqidno:41所示氨基酸序列或氨基酸序列如seqidno:41所示的多肽;包含seqidno:44所示氨基酸序列或氨基酸序列如seqidno:44所示的多肽;或包含seqidno:47所示氨基酸序列或氨基酸序列如seqidno:47所示的多肽。因此,在具体的实施方式中,本发明的蛋白可以是抗体或其抗原结合部分;本发明的蛋白也可以是包含抗体或其抗原结合部分的融合蛋白。术语“抗体”在本文中包括完整的抗体和任何抗原结合片段。天然存在的“抗体”是包含通过二硫键链间连接的至少2个重(h)链和2个轻(l)链的糖蛋白。每一条重链由重链可变区(在本文中缩写为vh)和重链恒定区组成。重链恒定区由3个结构域ch1、ch2和ch3组成。每一条轻链由轻链可变区(在本文中缩写为vl)和轻链恒定区组成。轻链恒定区由一个结构域cl组成。vh和vl区可被进一步细分为称为互补决定区(cdr)的具有高可变性的区域,其间隔以更保守的称为框架区(er)的区域。每一个vh和vl由按下列顺序:fr1、cdr1、fr2、cdr2、fr3、cdr3、fr4从氨基末端至羧基末端排列的3个cdr和4个fr组成。重链和轻链的可变区含有与抗原相互作用的结合结构域。抗体的恒定区可介导免疫球蛋白对宿主组织或因子(包括免疫系统的各种细胞(例如效应细胞)和经典补体系统的第一组分(c1q))的结合。术语“互补决定区”和“cdr”是指抗体可变区内赋予抗原特异性和结合亲和力的氨基酸的序列。一般而言,在每一个重链可变区中存在3个cdr(hcdr1、hcdr2、hcdr3)并且在轻链可变区中存在3个cdr(lcdr1、lcdr2、lcdr3)。给定的cdr的氨基酸序列边界可使用许多公知的方案的任何方案来确定,包括由kabat等(1991),“sequencesofproteinsofimmunologicalinterest,”第5版。publichealthservice,nationalinstitutesofhealth,bethesda,md(“kabat”编号方案)、al-lazikani等,(1997)jmb273,927-948(“chothia”编号方案)描述的那些方案。如本文中所用,术语“抗体”是指保留特异性结合抗原(例如,pro-bdnf的部分)的能力的抗体的全长或一个或多个片段、或者其他具有类似抗体结合活性的多肽。已显示抗体的抗原结合功能可通过全长抗体的片段来进行。包含在术语抗体的“抗原结合片段”的实例包括fab片段、由vl、vh、cl和ch1结构域组成的单价片段;f(ab)2片段、包含通过铰链区上的二硫桥连接的两个fab片段的双价片段;由vh和ch1结构域组成的fd片段;由抗体的单臂的vl和vh结构域组成的fv片段;由vh结构域组成的dab片段(ward等,1989,nature341:544-546);和分离的互补决定区(cdr)或包含这样的抗原结合部分的任何融合蛋白。如本文中所用,“具有类似抗体结合活性的多肽”可以为具有抗体抗原结合部位的蛋白,如单域抗体、微抗体、二聚体、三聚体,也可以是非抗体结构的亲和蛋白。虽然fv片段的两个结构域vl和vh由分开的基因编码,但它们可使用重组方法,通过合成接头来进行联接,所述接头使得它们被产生为其中vl和vh区域配对形成的单链蛋白(scfv)(参见:例如,bird等,1988,science242:423-426;和huston等,1988,proc.natl.acad.sci.85:5879-5883)。此类单链抗体也意欲包括在术语抗体的“抗原结合片段”内。这些抗体片段使用本领域普通技术人员已知的常规技术来获得,并且可以以与对于完整抗体使用的方式相同的方式筛选所述片段的功用。如本文中所用,“分离的抗体”是指大体上不含具有不同抗原特异性的其它抗体的抗体(例如,特异性结合pro-bdnf,诸如人pro-bdnf的分离的抗体,大体上不含特异性结合除pro-bdnf外的其它抗原的抗体)。然而,特异性结合pro-bdnf的分离的抗体可具有与其它抗原(诸如来自其它物种的pro-bdnf分子)的交叉反应性。此外,分离的抗体可大体上不含其它细胞材料和/或化学药品。术语“表位”意指能够特异性结合抗体的蛋白质决定簇。表位通常由分子的化学活性表面分组诸如氨基酸或糖侧链组成,通常具有特定的结构特征和电荷特征。术语“同种型”是指由重链恒定区基因提供的抗体种类(例如,igm、ige、igg,例如igg1或igg4)。同种型还包括这些种类之一的修饰形式,其中修饰已被产生来改变fc功能,例如以增强或减弱效应子功能或对fc受体的结合。如本文中所用,术语“全人抗体”意欲包括具有其中框架区和cdr区都来源于人来源的序列的可变区的抗体。此外,如果抗体含有恒定区,则所述恒定区也来源于这样的人序列,例如,人种系序列,或人种系序列或含有来源于人框架序列分析(例如knappik等,2000,jmolbiol296:57-86中所描述的)的共有框架序列的抗体的突变形式。本公开内容的全人抗体可包括不由人序列编码的氨基酸残基(例如,通过体外随机或定点诱变或通过体内体细胞突变引入的突变)。然而,如本文中所用,术语“全人抗体”无意包括其中来源于另一种哺乳动物物种诸如小鼠的种系的cdr序列已被移植至人框架序列上的抗体。如本文中所用,术语“重组人抗体”包括通过重组手段制备、表达、生成或分离的所有人抗体。诸如从人免疫球蛋白基因的转基因或转染色体动物(例如小鼠)或从其制备的杂交瘤分离的抗体,从经转化表达人抗体的宿主细胞,例如从转染瘤分离的抗体、从重组组合人抗体文库分离的抗体、以及通过包括将人免疫球蛋白基因序列的全部或部分与其它dna序列拼接的任何其它手段制备、表达、生成或分离的抗体。此类重组人抗体具有其中框架区和cdr区都来源于人种系免疫球蛋白序列的可变区。然而,在某些实施方案中,可将此类重组人抗体经历体外诱变(或,当使用人ig序列的转基因动物时,体内体细胞诱变),从而重组抗体的vh和vl区的氨基酸序列是虽然来源于人种系vh和vl序列并与所述序列相关,但在体内可以不天然存在于人抗体种系库内的序列。如本文中所用,“同种型”是指由重链恒定区基因提供的抗体种类(例如,igm、ige、igg,诸如igg1或igg4)。短语“识别抗原的抗体”和“对于抗原是特异性的抗体”在本文中可与术语“特异性结合抗原的抗体”互换使用。如本文中所用,“特异性结合pro-bdnf多肽”的抗体或蛋白质意欲指以100nm或更低、10nm或更低、5nm或更低的kd结合人pro-bdnf多肽的抗体或蛋白质。“与除pro-bdnf外的抗原交叉反应”的抗体意欲指以10nm或更低、5nm或更低kd结合该抗原的抗体。“不与特定抗原交叉反应”的抗体意欲指以200nm或更大的kd或1μm或更大的kd或10μm或更大的kd结合该抗原的抗体。在某些实施方案中,不与抗原交叉反应的此类抗体在标准结合测定中展现基本上不可检测的针对这类蛋白质的结合。如本文中所用,术语“kd”意指从kd对ka的比率(即kd/ka)获得的并且表达为摩尔浓度(m)的解离常数。抗体的kd值可使用本领域中良好建立的方法来测定。用于测定抗体的kd的方法是通过使用对于本领域普通技术人员来说是公知的并且如例如实施例中所述操作的表面等离子体共振或使用生物传感系统诸如biacoretm系统。如本文中所用,术语“亲和力”或“亲和活性”是指在单个抗原位(antigenicsite)上抗体与抗原之间的相互作用的强度。如本文中所用,术语对于igg抗体或其片段(例如,fab片段)的“高亲和力”是指对于靶抗原具有10-8m或更低、10-9m或更低的kd的抗体。然而,高亲和力结合对于其它抗体同种型可变化。如本文中所用,术语对于本公开内容的抗体或蛋白质的“选择性”是指结合某些靶多肽,但不结合密切相关的多肽的抗体或蛋白质。短语“识别抗原的抗体”和“对于抗原是特异性的抗体”在本文中可与术语“特异性结合抗原的抗体”互换使用。术语“核酸”或“多核苷酸”是指脱氧核糖核酸(dna)或核糖核酸(rna)及其呈单链或双链形式的聚合物。除非明确地限制,否则术语包括具有与参照核酸相似的结合性质并且以与天然存在的核苷酸相似的方式被代谢的含有已知的天然核苷酸的类似物的核酸。除非另有所指,否则特定核酸序列还隐含地包括其保守修饰的变体(例如,简并密码子取代)、等位基因、直系同源物、snp和互补序列以及明确指出的序列。具体地,简并密码子取代可通过生成其中一个或多个选择的(或全部)密码子的第三位被混合碱基和/或脱氧肌苷残基取代的序列来实现(batzer等,nucleicacid)。如本文中所用,术语“疾病”(如类风湿关节炎)的“治疗”,在一个实施方案中是指改善疾病或病症(即减缓或阻止或减少疾病的进展或其临床症状的至少一个)。在另一个实施方案中,“治疗”是指缓解或改善至少一个身体参数,包括可能不能被患者辨别出的那些物理参数。在另一个实施方案中,“治疗”是指在身体上(例如可辨别的症状的稳定)、生理上(例如身体参数的稳定)或在这两方面调节疾病或病症。除非在本文中明确描述,否则用于评估疾病的治疗和/或预防的方法在本领域中通常是已知的。两个核苷酸序列之间的百分比同一性还可使用例如算法诸如用于核酸序列的blastn程序,使用为11的字长(w)、为10的期望值(e)、m=5、n=4以及两条链的比较作术语“交叉阻断”、“交叉阻断的”、“交叉阻止”在本文中可互换使用,用于指抗体或其它结合剂在标准竞争性结合测定中干扰其它抗体或结合剂对pro-bdnf的结合的能力。抗体或其它结合剂诸如包含抗体的抗原结合部分的蛋白质能够干扰另一种抗体或结合分子对pro-bdnf的结合的能力或程度,和从而其是否可被认为是根据本公开内容的交叉阻断可使用标准竞争性结合测定来测定。一个合适的测定包括使用biacoretm技术(例如通过使用biacoretm3000仪(biacoretm,uppsala,sweden)),所述技术可使用表面等离子体共振技术来测量相互作用的程度。术语“变体”是指编码本公开内容的抗体的其它核酸包括已通过核苷酸缺失、插入或取代突变的,但仍然与本文公开的cdr、vl、vh、或者轻链、或重链、或scfv等对应的编码核酸序列具有至少60、70、80、90、91、92、93、94、95、96、97、98、99或100%同一性的核酸。在一些实施方案中,其包括变异核酸,在所述变异核酸中,相较于本文描绘的cdr编码区,在cdr编码区中已通过核苷酸缺失、插入或取代改变的核苷酸不超过1、2、3、4或5个。对于结合相同表位的抗体,可将vh、vl、全长轻链和全长重链序列(核苷酸序列和氨基酸序列)“混合和匹配”以生成本公开内容的其它抗pro-bdnf结合分子。此类“混合和匹配”的抗体的pro-bdnf结合可使用上述结合测定和其它常规结合测定(例如elisa)来进行测试。当将这些链混合和匹配时,应当用结构上相似的vh序列替代来自特定vh/vl配对的vh序列。同样地,应当用结构上相似的全长重链序列替代来自特定全长重链/全长轻链配对的全长重链序列。同样地,应当用结构上相似的vl序列替代来自特定vh/vl配对的vl序列。同样地,应当用结构上相似的全长轻链序列替代来自特定全长重链/全长轻链配对的全长轻链序列。鉴于这些抗体的每一个可结合pro-bdnf以及抗原结合特异性主要由cdr1、2和3区提供,因此可将vhcdr1、2和3序列与vlcdr1、2和3序列“混合和匹配”(即:可将来自不同抗体的cdr混合和匹配,含有vhcdr1、2和3以及vlcdr1、2和3的每一个抗体生成本公开内容的其它抗pro-bdnf结合分子)。可使用上文中所述的和实施例中的结合测定或其它常规测定(例如elisa)来测试此类“混合和匹配”抗体的pro-bdnf结合。当将vhcdr序列混合和匹配时,应当用结构上相似的cdr序列替代来自特定vh序列的cdr1、cdr2和/或cdr3序列。同样地,当将vlcdr序列混合和匹配时,应当用结构上相似的cdr序列替代来自特定vl序列的cdr1、cdr2和/或cdr3序列。对本领域普通技术人员来说显而易见的是,可通过用来自本文中显示的本公开内容的单克隆抗体的cdr序列的结构上相似序列取代一个或多个vh和/或vlcdr区序列来生成新型vh和vh。如本文中所用,如果抗体的可变区链或全长链获自使用人种系免疫球蛋白基因的系统,则人抗体包含作为特定种系序列“的产物”或“从其衍生”的重链或轻链可变区或全长重链或轻链。此类系统包括用目标抗原免疫具有人免疫球蛋白基因的转基因小鼠,或用目标抗原筛选在噬菌体上展示的人免疫球蛋白基因文库。可通过将人抗体的氨基酸序列与人种系免疫球蛋白的氨基酸序列相比较和选择在序列上与人抗体的序列最接近(即,最大百分比同一性)的人种系免疫球蛋白序列,来这样鉴定作为人种系免疫球蛋白序列“的产物”或“从其衍生”的人抗体。作为特定人种系免疫球蛋白序列“的产物”或“从其衍生”的人抗体可因例如天然存在的体细胞突变或定点突变的有意引入而含有不同于种系序列的氨基酸。然而,所选择的人抗体通常在氨基酸序列上与由人种系免疫球蛋白基因编码的氨基酸序列具有至少90%同一性,并且含有当与其它物种的种系免疫球蛋白的氨基酸序列(如,鼠类种系序列)相比较时,将人抗体鉴定为是人的氨基酸残基。在某些情况下,人抗体可在氨基酸序列上与由种系免疫球蛋白基因编码的氨基酸序列具有至少60%、70%、80%、90%或至少95%或甚至至少96%、97%、98%或99%的同一性。通常地,从特定人种系序列衍生的人抗体将显示与由人种系免疫球蛋白基因编码的氨基酸序列相异不超过10个氨基酸的差异。在某些情况下,人抗体可显示与由种系免疫球蛋白基因编码的氨基酸序列相差异不超过5个或甚至不超过4、3、2或1个氨基酸的差异。具有保守修饰的抗体在某些实施方案中,本公开内容的抗体(或包含其抗原结合片段)具有包含hcdr1、hcdr2和hcdr3序列(或hcdr1’、hcdr2’和hcdr3’)的重链可变区和包含lcdr1、lcdr2和lcdr3序列(或lcdr1’、lcdr2’和lcdr3’)的轻链可变区,其中这些cdr序列的一个或多个具有基于本文中描述的抗体1d3或者2h8的指定的氨基酸序列或其保守修饰,并且其中所述抗体或蛋白质保留本公开内容的抗pro-bdnf抗体的期望的功能性质。如本文中所用,术语“保守序列修饰”意欲指其中氨基酸残基被具有相似侧链的氨基酸残基替代的氨基酸取代。具有相似侧链的氨基酸残基的家族已在本领域中进行了定义。这些家族包括具有碱性侧链的氨基酸(例如,赖氨酸、精氨酸、组氨酸)、具有酸性侧链的氨基酸(例如,天冬氨酸、谷氨酸)、具有不带电荷的极性侧链的氨基酸(例如,甘氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸、酪氨酸、半胱氨酸、色氨酸)、具有非极性侧链的氨基酸(例如,丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、甲硫氨酸)、具有β-支链侧链的氨基酸(例如,苏氨酸、缬氨酸、异亮氨酸)和具有芳族侧链的氨基酸(例如,酪氨酸、苯丙氨酸、色氨酸、组氨酸)。因此,本公开内容的抗体的cdr区内的一个或多个氨基酸残基可用来自相同侧链家族的其它氨基酸残基来替代,并且可使用本文中描述的功能测定来测试改变的抗体的保留的功能。可通过本领域已知的标准技术诸如定点诱变和pcr介导的诱变将修饰引入本文中公开的抗体。另外,除本发明的重组抗体1d3和2h8外,本发明还涵盖了保留1d3和2h8抗体的理想的功能性质的同源抗体或蛋白质。特别地,所述根据本发明的同源抗体或蛋白质是包含针对pro-bdnf多肽的抗体的抗原结合部分的抗体或蛋白质,其特征是所述抗体或蛋白:i)以10nm或更低的kd结合pro-bdnf多肽,如在例如实施例中所述的biacoretm测定中测量的;(ii)pro-bdnf对p75的结合的竞争性抑制,(iii)依赖于pro-bdnf的活性。本文所述的“依赖pro-bdnf的活性”是指本发明的抗体或蛋白具有与pro-bdnf相关的活性。例如,probdnf与其配体结合促进某生物过程,则本发明的抗体或蛋白是该生物过程的抑制剂或拮抗剂;probdnf与其配体结合抑制某生物过程,则本发明的抗体或蛋白是该生物过程的促进剂或激动剂。编码本发明抗体的核酸分子本发明的另一方面涉及编码本发明抗体或蛋白质的核酸分子。本发明还涉及源自后者的序列的核酸分子,所述序列已被优化以用于在哺乳动物细胞例如cho细胞系中进行蛋白质表达。所述核酸可存在于完整细胞中,细胞裂解物中或可以是呈部分纯化或大体上纯的形式的核酸。当通过标准技术(包括碱性/sds处理、cscl分带、柱层析、琼脂糖凝胶电泳和本领域中公知的其它技术)从其它细胞组分或其它污染物(例如其它细胞核酸或蛋白质)纯化出来时,核酸是“分离的”或“变得大体上纯的”。参见,f.ausubel等编,1987,currentprotocolsinmolecularbiology,greenepublishingandwileyinterscience,newyork。本发明的核酸可使用标准分子生物学技术获得。一旦获得编码例如vh和vl区段的dna片段,可通过标准重组dna技术进一步操纵这些dna片段,例如以将可变区基因转变成全长抗体链基因、fab片段基因或scfv基因。在这些操纵中,vl-或vh-编码dna片段被有效地连接于另一个dna分子或编码另一种蛋白质(诸如抗体恒定区或柔性接头)的片段。术语“有效连接的”,如本说明中所用,意欲指以功能性方式联接两个dna片段,例如以便由这两个dna片段编码的氨基酸序列保留在框内或以便在期望的启动子控制下表达蛋白质。可通过将vh-编码dna有效地连接于编码重链恒定区(ch1、ch2和ch3)的另一个dna分子来将编码vh区的分离的dna转变成全长重链基因。人重链恒定区基因的序列在本领域是已知的(参见,例如,kabat,e.a.等,1991,sequencesofproteinsofimmunologicalinterest,第5版,美国卫生和人类服务部,nihpublicationno.91-3242)。并且编码这些区域的dna片段可通过标准pcr扩增来获得。重链恒定区可以是igg1、igg2、igg3、igg4、iga、ige、igm或igd恒定区。在一些实施方案中,在igg1同种型中选择重链恒定区。对于fab片段的重链基因,可将vh-编码dna有效地连接于仅编码重链ch1恒定区的另一个dna分子。可通过将vl-编码dna有效地连接于编码轻链恒定区cl的另一个dna分子来将编码vl区的分离的dna转变成全长轻链基因(以及fab轻链基因)。人轻链恒定区基因的序列在本领域是已知的(参见,例如,kabat,e.a.等,1991,sequencesofproteinsofimmunologicalinterest,第5版,美国卫生和人类服务部,nihpublicationno.91-3242)。并且包含这些区域的dna片段可通过标准pcr扩增来获得。所述轻链恒定区可以是κ或λ恒定区。为了生成scfv基因,将vh-和vl-编码dna片段有效地连接于编码柔性接头例如编码氨基酸序列(gly4-ser)3的另一个片段,以便vh和vl序列可被表达为连续单链蛋白质,vl与vh区通过所述柔性接头联接(参见例如,bird等,1988,science242:423-426;huston等,1988,proc.natl.acad.sci.usa85:5879-5883;mccafferty等,1990,nature348:552-554)。本发明的重组抗体的分离多种筛选抗体和包含其抗原结合部分的蛋白质的方法已在本领域中进行了描述。此类方法可被分成体内系统和体外系统,所述体内系统诸如能够在抗原免疫后产生全长人抗体的转基因小鼠,所述体外系统由产生抗体dna编码文库。这些体外技术被称为展示技术,包括但不限于噬菌体展示、rna或dna展示、核糖体展示、酵母或哺乳动物细胞展示。它们在本领域中已进行了详尽描述(关于综述参见例如:nelson等,2010,naturereviewsdrugdiscovery,“developmenttrendsforhumanmonoclonalantibodytherapeutics”)。在一个具体实施方案中,使用用于筛选人重线抗体文库的文库,诸如文库的噬菌体展示方法分离本公开内容的人重组抗体。vh和vl基因或相关的cdr区的库可通过聚合酶链式反应(pcr)来单独克隆或通过dna合成仪来合成,以及在噬菌体文库中被随机重组,随后可筛选其的抗原结合克隆。此类用于分离人抗体的噬菌体展示法在本领域中已被建立或在下面的实施例中进行了描述。参见例如:us5,223,409;us5,403,484;us5,427,908;us5,580,717;us6,521,404等。制备产生单克隆抗体的转染瘤可使用例如本领域中公知的重组dna技术与基因转染方法的组合(例如,morrison,s.1985,science229:1202)在宿主细胞转染瘤中产生本公开内容的抗体。例如,为了表达抗体或其抗体片段,编码部分或全长轻链和重链的dna可利用标准分子生物学或生物化学技术(例如,dna化学合成、pcr扩增或使用表达目标抗体的杂交瘤的cdna克隆)来获得,并且可将所述dna插入表达载体,以便所述基因被有效地连接于转录和翻译控制序列。在本说明书中,术语“有效连接的”意欲指将抗体基因连接进入载体,以使载体内的转录和翻译控制序列行使它们的调节抗体基因的转录和翻译的预定功能。选择可与所使用的表达宿主细胞相容的表达载体和表达调控序列。可将抗体轻链基因和抗体重链基因插入至不同的载体中,或者更通常地,将两个基因插入至同一表达载体中。通过标准方法将抗体基因插入至表达载体中(例如,连接抗体基因片段和载体上互补的限制性位点,或者如果不存在限制性位点,则进行平端连接)。可以使用本文所述抗体的轻链和重链可变区来生成任何抗体同种型的全长抗体基因,其通过将它们插入已编码期望同种型的重链恒定区和轻链恒定区的表达载体中,从而使得vh区段与载体中的ch区段有效连接,vl区段与载体中的cl区段有效连接。为表达轻链和重链,应用标准技术来将编码重链和轻链的表达载体转染进宿主细胞中。各种形式的术语“转染”意欲涵盖多种通常用于将外源dna导入原核或真核宿主细胞的技术,例如电穿孔、磷酸钙沉淀、deae-右旋糖苷转染等。理论上在原核或真核宿主细胞中都有可能表达本公开内容的抗体。论述抗体在真核细胞例如哺乳动物宿主细胞、酵母或丝状真菌中的表达,因为此类真核细胞(特别是哺乳动物细胞)比原核细胞更有可能组装和分泌正确折叠且具有免疫学活性的抗体。双特异性分子在另一方面,本发明表征了包含本公开内容的抗probdnf的抗体或包含其抗原结合部分的蛋白质的双特异性或多特异性分子。本发明的抗体或蛋白可被衍生化或连接至另一功能性分子,例如另一种肽或蛋白质(例如,受体的另一种抗体或配体)以产生与至少两种不同的结合位点或靶分子结合的双特异性分子。本发明的抗体或蛋白质事实上可以进行衍生化或连接至不止一个其它功能性分子以产生与两个以上不同结合位点和/或靶分子结合的多特异性分子;此类多特异性分子还意欲为本文中所使用的术语“双特异性分子”所涵盖。为生成本发明的双特异性分子,可以将本发明的抗体或蛋白质功能性连接(例如通过化学偶联、基因融合、非共价缔合或其它方式)至一种或多种其它结合分子,诸如另一种抗体、抗体片段、肽或结合模拟物,以便产生双特异性分子。因此,本发明包括包含至少一个针对pro-bdnf或其片段(如seqidno:41、44、或47)的双特异性分子。例如,第二靶表位是与第一靶表位不同的pro-bdnf的另一个表位。另一个实例是包含至少一个针对pro-bdnf的第一结合特异性部分(例如,1d3或2h8的一个抗原结合部分)和针对pro-bdnf内的其它地方或另一个靶抗原内的表位的第二结合特异性部分的双特异性分子。多价抗体在另一个方面,本发明提供多价抗体,其包含至少两个相同或不同的结合pro-bdnf的本发明的抗体的抗原结合部分(例如,选自1d3或2h8的抗原结合部分)。在一个实施方案中,多价抗体提供至少2、3或4个抗体的抗原结合部分。可通过蛋白质融合或共价或非共价连接将抗原结合部分连接在一起。或者,已针对双特异性分子描述了连接方法。可以例如通过将本发明的抗体与结合本发明的抗体的恒定区例如fc或铰链区的抗体交联来获得四价化合物。药物组合物在另一方面,本发明提供了一种组合物,例如药物组合物,其包含与可药用的载体配制在一起的一种或一组本公开内容的抗体或包含其抗原结合部分的蛋白质(选自下组的抗体:1d3或2h8)。此类组合物可包含一种或一组(例如,两种或多种不同的)的本发明抗体。例如,本发明的药物组合物可包含一组结合靶抗原上的不同表位或者具有互补活性的抗体或蛋白质。本发明的药物组合物还可以以联合疗法(即,与其它药物组合)施用。例如,联合疗法可以包括与至少一种其它抗炎剂或另一种化疗剂(例如免疫抑制剂)组合的本发明的抗pro-bdnf抗体或蛋白质(例如选自下组的抗体:1d3或2h8)。如本文中所用,“可药用的载体”包括生理上相容的任何和所有溶剂、分散介质、包衣、抗细菌和抗真菌剂、等渗和吸收延迟剂等。载体应当适于静脉内、肌内、皮下、胃肠外、脊髓或表皮施用(例如通过注射或输注)。在一个实施方案中,载体应当适合于皮下途径。取决于施用途径,活性化合物,即抗体、免疫缀合物或双特异性分子,可被包被在一种物质中,以保护该化合物不受酸和可以使该化合物失活的其它天然条件的作用。本发明的药物组合物可包含一种或多种可药用的盐。“可药用的盐”指这样一种盐,其保留亲本化合物的期望生物学活性且不产生任何不利的毒物学效果(参见例如,berge,s.m.等,1977,j.pharm.sci.66:1-19)。此类盐的例子包括酸加成盐和碱加成盐。酸加成盐包括衍生自无毒无机酸,诸如盐酸、硝酸、磷酸、硫酸、氢溴酸、氢碘酸、亚磷酸等的盐,以及衍生自无毒有机酸,诸如脂肪族单羧酸和二羧酸、苯基取代的链烷酸、羟基链烷酸、芳香族酸、脂肪族和芳香族磺酸等的盐。碱加成盐包括衍生自碱土金属(诸如钠、钾、镁、钙等)的盐,以及衍生自无毒有机胺的盐,诸如n,n'-二苄乙二胺、n-甲基葡糖胺、氯普鲁卡因、胆碱、二乙醇胺、乙二胺、普鲁卡因等。本发明的药物组合物还可包含可药用的抗氧化剂。可药用的抗氧化剂的例子包括:水溶性抗氧化剂,诸如抗坏血酸、盐酸半胱氨酸、硫酸氢钠、焦亚硫酸钠、亚硫酸钠等;油溶性抗氧化剂,诸如抗坏血酸棕榈酸酯、丁基化羟基茴香醚(bha)、丁基化羟基甲苯(bht),卵磷脂、没食子酸丙酯、α-生育酚等;和金属螯合剂,诸如柠檬酸、乙二胺四乙酸(edta)、山梨醇、酒石酸、磷酸等。可以用于本发明的药物组合物的合适的含水和非含水载体的例子包括水、乙醇、多元醇(诸如甘油、丙二醇、聚乙二醇等)及其合适的混合物、植物油诸如橄榄油,和可注射的有机酯诸如油酸乙酯。通过例如使用包衣材料诸如卵磷脂,通过在分散体的情况下保持期望颗粒大小,以及通过使用表面活性剂,可维持适当的流动性。这些组合物还可包含佐剂,诸如防腐剂、湿润剂、乳化剂和分散剂。通过灭菌方法和通过包含各种抗细菌和抗真菌剂,诸如对羟基苯甲酸酯类、氯丁醇、酚、山梨酸等,可以确保对微生物存在的预防。可能还希望向组合物中加入等渗剂,诸如糖类、氯化钠等。此外,通过加入延迟吸收的药物,诸如单硬脂酸铝和明胶,可以导致可注射药物形式的延长吸收。可药用的载体包括无菌水溶液或分散体和用于即时制备无菌可注射溶液或分散体的无菌粉末。此类介质和试剂用于药物活性物质的用途在本领域是已知的。除了任何常规介质或药物与活性化合物不相容的情况之外,设想了其在本发明的药物组合物中的用途。还可以向组合物中掺入补充性的活性化合物。治疗性组合物在生产和贮存条件下通常必须是无菌的和稳定的。可将组合物配制成溶液、微乳液、脂质体或适于高药物浓度的其它有序结构。载体可以是含有例如水、乙醇、多元醇(例如甘油、丙二醇、和液体聚乙二醇等)及其合适混合物的溶剂或分散介质。可以例如通过使用包衣诸如卵磷脂,在分散体的情况中通过维持期望粒度,及通过使用表面活性剂,来保持适当的流动性。在许多情况中,可在组合物中包含等渗剂,例如糖类、多元醇诸如甘露醇、山梨醇、或氯化钠。通过在组合物中包含延迟吸收的试剂,例如单硬脂酸盐和明胶,可以造成可注射组合物的延长吸收。关于稳定的蛋白质(例如抗体)制剂的开发的综述可见于cleland等,1993,crit.reviews.ther.drugcarriersystems10(4):307-377和weiwang1999,int.j.pharmaceutcs185:129-88。关于抗体的另外的配制论述可见于,例如daugherty和mrsny2006,advanceddrugdeliveryreviews58:686-706;us6,171,586及其它已知的参考资料中。用于皮内或皮下施用的溶液或悬浮液通常包含以下组分的一种或多种:无菌稀释剂诸如注射用水、盐水溶液、不挥发油、聚乙二醇、丙三醇、丙二醇或其它合成溶剂、抗菌剂诸如苄醇或对羟基苯甲酸甲酯,抗氧化剂诸如抗坏血酸或亚硫酸氢钠,螯合剂如乙二胺四乙酸,缓冲剂诸如乙酸盐,柠檬酸盐或磷酸盐,和调节张力的试剂诸如氯化钠或葡萄糖。ph可以用酸或碱,诸如盐酸或氢氧化钠来调节。可将此类制剂封装在由玻璃或塑料制造的安瓿、一次性注射器或多剂量小瓶中。可通过将所需量的所述活性化合物与根据需要的一种或一组上文中列举的成分掺入合适的溶剂中,然后微量过滤灭菌,来制备无菌注射液。一般地,通过将本公开内容的抗体或蛋白质掺入含有基本分散介质和来自上文中列举的那些成分的所需其它成分的无菌媒介物中,来制备分散剂。在用于制备无菌注射液的无菌粉剂的情况下,制备方法是真空干燥和冷冻干燥(冻干),所述方法产生来自其先前过滤灭菌的溶液的活性成分加上任何另外的所需成分的粉剂。可与载体材料组合以产生单剂量形式的活性成分的量将根据待治疗的受试者及具体施用模式而变化。可与载体材料组合以产生单剂量形式的活性成分的量一般是产生治疗效果的组合物量。“治疗有效量”的本公开内容抗pro-bdnf抗体或蛋白质可导致疾病症状严重度的降低、无疾病症状期的频率和持续时间的增加或对患病所造成的损害或残疾的预防。可以利用本领域中已知的多种方法中的一种或多种经一种或多种施用途径来施用本公开内容的组合物。正如本领域普通技术人员将会理解的,施用的途径和/或模式将根据期望的结果而变化。本公开内容的抗体的施用途径包括静脉内、肌内、皮内、腹膜内、皮下、脊柱或其它胃肠外施用途径,例如通过注射或输注。如本文中所用,短语“胃肠外施用”意味着除了肠和局部施用之外的施用模式,通常通过注射,包括但不限于静脉内、肌内、动脉内、鞘内、囊内、眶内、心内、皮内、腹膜内、经气管、皮下、表皮下、关节内、囊下、蛛网膜下、脊柱内、硬膜外和胸骨内(intrastemal)注射和输注。或者,可以经非胃肠外途径来施用本公开内容的抗体或蛋白质,诸如局部、表皮或粘膜施用途径,例如鼻内、口服、阴道、直肠、舌下或局部。可用载体制备本公开内容的抗体或蛋白质,所述载体将保护抗体以免迅速释放,诸如受控释放制剂,包括植入物、透皮贴和微囊递送系统。可以使用生物可降解的、生物相容性的聚合物,诸如乙烯乙酸乙烯、聚酸酐类、聚乙醇酸、胶原、聚正酯类和聚乳酸。用于制备此类剂型的许多方法已经获得了专利或为本领域技术人员所公知。参见例如sustainedandcontrolledreleasedrugdeliverysystems,j.r.robinson编,marceldekker,inc.,newyork,1978。可以用本领域已知的医疗手段来施用治疗性组合物。例如,在一个实施方案中,可以用无针皮下注射手段来施用本公开内容的治疗性组合物,诸如us5,399,163;us5,383,851;us5,312,335等中所公开的手段。可用于本公开内容的公知的植入物和模块的实例包括:us4,487,603,其公开了可植入的微输注泵,用于以受控速率分配药物;us4,486,194,其公开了一种治疗用装置,用于通过皮肤施用药物;us4,447,233,其公开了一种药物输注泵,用于以精确输注速率递送药物;us4,447,224,其显示了一种变流可植入输注装置,用于持续的药物递送;us4,439,196,其公开了一种渗透性药物递送系统,它具有多室隔室;us4,475,196,其公开了一种渗透性药物递送系统。许多其它的此类植入物、递送系统、和模块对于本领域普通技术人员来说是已知的。在某些实施方案中,可配制本公开内容的抗体或蛋白质以确保在体内的适当分布。例如,血脑屏障(bbb)排除了许多高亲水性化合物。为了确保本公开内容的治疗化合物穿过bbb(如有需要),可以将它们配制在例如脂质体中。有关制造脂质体的方法,参见例如us4,522,811、us5,374,548和5,399,331。所述脂质体可包含被选择性地转运到特定细胞或器官、从而增强靶向药物递送的一个或多个部分(参见例如v.v.ranade1989,j.clinepharmacol.29:685)。示例性靶向部分包括叶酸或生物素(参见例如,low等的美国专利5,416,016)、甘露糖苷(umezawa等,1988,biochem.biophys.res.commun.153:1038);抗体(p.g.bloeman等,1995,febslett.357:140;m.owais等,1995,antimicrob.agentschernother.39:180);表面活性剂a蛋白受体(briscoe等,1995,am.j.physiol.1233:134);p120(schreier等,1994,j.biol.chem.269:9090);也参见keinanen和laukkanen,1994,febslett.346:123;killion和fidler,1994,immunomethods4:273。本发明的用途和方法本发明的抗体或蛋白质具有体外和体内诊断及治疗功用。例如,可将这些分子施用至培养中的(例如在体外或体内)或受试者中的(例如在体内)的细胞,以治疗、预防或诊断多种病症。所述方法特别适合用于治疗、预防或诊断pro-bdnf相关病症和/或自身免疫性和炎性病症,例如多发性硬化、类风湿关节炎或银屑病;或者用于镇痛。具体地,本发明提供治疗pro-bdnf相关病症和/或自身免疫性和炎性病症、或镇痛的方法。在某些实施方案中,所述方法包括向有此需要的受试者施用本发明的分离的抗体或包含其抗原结合部分的蛋白的步骤。本发明还提供了方法,所述方法通过将细胞与包含治疗有效剂量的本公开内容的抗体的组合物接触,来减弱或抑制pro-bdnf或pro-bdnf在靶细胞或组织中诱导的信号转导应答。在本说明书中,短语“pro-bdnf介导的疾病”或“pro-bdnf相关病症”包括其中pro-bdnf或pro-bdnf在疾病或医学病况中起作用(无论是直接还是间接地)的所有疾病和医疗病况,包括疾病或病况的原因、发展、进展、持续或病理学。因此,这些术语包括与异常pro-bdnf水平相关或以异常pro-bdnf水平为特征的病况和/或可通过减弱或抑制pro-bdnf在靶细胞或组织中诱导的活性(例如tnf-α、il-2、il-6或il-4的产生)来治疗的疾病或病况。这类疾病或病况包括炎性病况和自身免疫性疾病,诸如多发性硬化、哮喘、关节炎、类风湿性关节炎或银屑病。这类疾病还包括过敏症和过敏性病况、超敏反应、慢性阻塞性肺疾病、囊性纤维化以及器官或组织移植排斥。本发明的抗体或蛋白质可用于(然而不限于)治疗、预防或改善自身免疫性疾病或炎性病况,特别是病因学包括自身免疫组分的炎性病况,诸如关节炎(例如类风湿性关节炎、慢性进行性关节炎(arthritischronicaprogrediente)和变形性关节炎)和风湿性疾病,包括牵涉骨损失、炎症性疼痛的炎性病况和风湿性疾病、脊椎关节病变(包括强直性脊柱炎)、赖特尔综合征、反应性关节炎、银屑病关节炎、幼年型特发性关节炎和肠病性关节炎、起止点炎、超敏反应(包括气道超敏反应和皮肤超敏反应)和过敏。可对其使用本公开内容的抗体的特定自身免疫性疾病包括自身免疫性血液学障碍(包括例如溶血性贫血、再生障碍性贫血、纯红细胞贫血和特发性血小板减少)、系统性红斑狼疮(sle)、狼疮性肾炎、炎性肌肉疾病(皮肌炎)、牙周炎、多软骨炎、硬皮病、韦格纳肉芽肿、皮肌炎、慢性活动性肝炎、重症肌无力、银屑病、史蒂芬约翰逊综合征、自发性口炎性腹泻、自身免疫性炎性肠病(包括例如溃疡性结肠炎、克罗恩病和肠易激综合症)、内分泌性眼病、格雷夫斯病、结节病、多发性硬化、系统性硬化病、纤维变性疾病、原发性胆汁性肝硬化、幼年型糖尿病(i型糖尿病)、葡萄膜炎、干燥性角结膜炎和春季角结膜炎、间质性肺纤维化、假体周围骨溶解、肾小球肾炎(有和无肾病综合症,例如包括特发性肾病综合征或微小病变性肾病)、多发性骨髓瘤、其他类型的肿瘤、皮肤和角膜的炎性疾病、肌炎、骨植入物的松动、代谢紊乱(诸如肥胖、动脉粥样硬化和其它心血管疾病,包括扩张型心肌病、心肌炎、ii型糖尿病和血脂异常)和自身免疫性甲状腺疾病(包括桥本甲状腺炎)、中小血管原发性血管炎、大血管血管炎包括巨细胞性动脉炎、化脓性汗腺炎、视神经脊髓炎、斯耶格伦氏综合征、白塞氏病、特应性和接触性皮炎、细支气管炎、炎性肌肉疾病、自身免疫性外周神经病、免疫性肾脏、肝脏和甲状腺疾病、炎症和动脉粥样硬化、自身炎症发热综合征、免疫血液学紊乱以及皮肤和粘膜的大疱性疾病。在解剖学上,葡萄膜炎可以是前、中、后部或泛葡萄膜炎。其可以是慢性或急性的。葡萄膜炎的病因学可以是自体免疫或非感染性的、感染性的,与全身性疾病相关或白点综合征。本公开内容的抗体或蛋白质还可用于治疗、预防或改善哮喘、支气管炎、细支气管炎、特发性间质性肺炎、尘肺、肺气肿以及气道的其它阻塞性或炎性疾病。本公开内容的抗体或蛋白质还可用于骨代谢的疾病,包括骨关节炎、骨质疏松和其它炎性关节炎和一般性骨损失,包括年龄相关的骨损失,特别是牙周病。下列疾病包含用于利用本发明的抗体或包含其抗原结合部分的蛋白治疗的特别优选的靶点:多发性硬化、银屑病、哮喘、系统性红斑狼疮(sle)和狼疮性肾炎。可将本发明的抗体或蛋白质作为唯一的活性成分或与其它药物例如免疫抑制剂或免疫调节剂或其它抗炎剂或其它细胞毒性剂或抗癌剂结合(例如作为其佐剂或与其组合)施用,例如以治疗或预防上述疾病。例如,可将本发明的抗体与如下药物组合使用:dmard,例如金盐、柳氮磺吡啶、抗疟药、甲氨蝶呤、d-青霉胺、硫唑嘌呤、麦考酚酸、他克莫司、西罗莫司、二甲胺四环素、来氟米特、糖皮质激素;钙调神经磷酸酶抑制剂,例如环孢菌素a或fk506;淋巴细胞再循环的调节剂,例如fty720和fty720类似物;mtor抑制剂,例如雷帕霉素,40-o-(2-羟基乙基)-雷帕霉素、cci779、abt578、ap23573或tafa-93;具有免疫抑制性质的子囊霉素,例如abt-281、asm981等;皮质类固醇;环磷酰胺;硫唑嘌呤;来氟米特;咪唑立宾;吗替麦考酚酯;15-脱氧精胍菌素或其免疫抑制同系物、类似物或衍生物;免疫抑制单克隆抗体,例如,针对白细胞受体,例如,mhc、cd2、cd3、cd4、cd7、cd8、cd25、cd28、cd40。cd45、cd58、cd80、cd86或其配体的单克隆抗体;其它免疫调节化合物,例如具有ctla4或其突变体的细胞外结构域的至少一部分,例如联接于非ctla4蛋白序列的ctla4或其突变体的细胞外结构域的至少一部分的重组结合分子,例如ctla4ig(例如,指定为atcc68629)或其突变体,例如lea29y;粘附分子抑制剂,例如lfa-1拮抗剂、icam-1或-3拮抗剂、vcam-4拮抗剂或vla-4拮抗剂;或化疗剂,例如紫杉醇、吉西他滨、顺铂、阿霉素或5-氟尿嘧啶;抗tnf药物,例如针对tnf的单克隆抗体,例如英夫利昔单抗、阿达木单抗、cdp870或针对tnf-ri或tnf-rii的受体构建体,例如依那西普、peg-tnf-ri;促炎细胞因子的阻断剂、il1阻断剂,例如阿那白滞素或il1陷阱、卡那奴单抗、il13阻断剂、il4阻断剂、il6阻断剂,il17阻断剂(诸如secukinumab、broadalumab、ixekizumab);趋化因子阻断剂,例如蛋白酶例如金属蛋白酶的抑制剂或激活物、抗-il15抗体、抗-il6抗体、抗-il4抗体、抗-il13抗体、抗-cd20抗体、nsaid,诸如阿司匹林或抗-感染剂(不限定于提及的试剂)。下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件如j.萨姆布鲁克等编着,分子克隆实验指南,第三版,科学出版社,2002中所述的条件,或按照制造厂商所建议的条件。实施例1.人probdnf前体结构域蛋白的表达和纯化(1)pet22b-probdnf载体构建及鉴定以人肿瘤细胞u87mg的cdna为模板(购自raygene公司),以引物probdnf-f(seqidno:25)和probdnf-r(seqidno:26)进行pc扩增,获得两端带有酶切位点ecori/xhoi的probdnf基因片段(703bp),用ecori/xhoi双酶切(购自neb公司),得到目的基因片段probdnf。将载体质粒pet22b(购自novogen公司)用ecori/xhoi双酶切,琼脂糖凝胶电泳后回收载体片段,与前述目的基因片段probdnf在t4连接酶(购自neb公司)作用下连接,然后转化大肠杆菌top10(购自life公司),经氨苄抗性进行筛选,经ecori/xhoi酶切鉴定含插入片断的阳性克隆,并通过测序验证,得到含有正确的人probdnf基因序列的原核表达质粒pet22b-probdnf。(2)人probdnf蛋白的表达与纯化将pet22b-probdnf质粒转化于表达宿主菌bl21(de3)(购自novagen公司),并平铺于氨苄青霉素抗性的平皿上37℃倒置培养过夜,挑取单克隆进行诱导表达,挑取单克隆后振荡培养至od600为0.6-0.8,加入终浓度为1mm的iptg,30℃诱导4h后收集菌液。通过离心收集沉淀,加入1/10体积的缓冲液a(50mmnah2po4,300mmnacl,10mm咪唑,ph8.0)重悬,加入pmsf(终浓度为1mm)置冰上超声,离心(4℃,12000g)15min,离心收集上清,通过ni-ntaagarose(购自qiagen公司)亲和柱层析,纯化得到目的表达蛋白,然后对pbs溶液进行透析,再通过12%sds-page分析透析后的纯化蛋白的纯度,a280检测其含量,sdspage电泳检测其分子量,结果显示目的条带分子量在30kd附近,该分子量与probdnf分子的理论分子量27.8kd基本符合。(3)人probdnf前体结构域表达载体v5f-pro-domain的构建以上述得到的质粒pet22b-probdnf为模板,以引物bdnfprovf1(seqidno:28)和bdnfprovr1(seqidno:29)进行pcr扩增,获得两端带有酶切位点nhei/xhoi的人probdnf前体结构域基因片段(350bp)。将该pcr片段用限制性内切酶nhei/xhoi(购自neb公司)进行双酶切,获得的前体结构域基因片段和经同样nhei/xhoi(购自neb公司)双酶切的载体v5f(购自raygene公司)通过t4dna连接酶连接后,转化于宿主菌top10(购自life公司)中,挑取阳性克隆进行pcr鉴定,并通过测序验证正确,成功构建v5f-pro-domain质粒。(4)人probdnf前体结构域蛋白的表达与纯化将生长良好的hek293f细胞(hek293f,购自life公司)以1×106细胞/毫升的密度接种于细胞三角培养瓶,37℃,5%co2120rpm培养过夜备用;将上述步骤获得的v5f-pro-domain质粒与脂质体(293fectin,购自life公司)分别用dmem稀释并温和混合,室温孵育20min,将孵育好的dna-脂质体复合物加至hek293f细胞中,37℃5%co2120rpm培养72h。收集细胞培养液,4500g离心15min,除去细胞取上清。取1ml的flag抗体亲和填料(anti-flagagaroseaffinitygel,购自sigma-aldrich公司)装柱,将flag亲和柱用裂解缓冲液(50mmpb,0.3mnacl,5%甘油)平衡5-10个柱体积。将离心后的细胞培养液上清以1ml/min通过flag亲和柱收集流穿液4℃保存。用清洗缓冲液1(50mmpb,ph7.8,0.3mnacl,5%甘油)洗5-10个柱体积,收集洗杂液1,于4℃保存。用清洗缓冲液2(50mmpb,ph7.8,0.5mnacl,5%甘油)洗4-5个柱体积,收集洗杂液2,于4℃保存。用洗脱缓冲液(50mmglycine.hcl,ph3.0,0.3mnacl,5%甘油)洗4-5个柱体积,收集洗脱液加入中和缓冲液(1mtris.hclph8.0),在透析液(50mmpb,ph7.8,0.3mnacl,5%甘油)中4℃透析过夜,sdspage电泳显示目的条带的分子量与人probdnf前体结构域蛋白的理论分子量13kd相当。实施例2.人probdnf前体的单链抗体筛选2.1基于噬菌体展示的人probdnf前体蛋白特异性结合抗体的筛选利用噬菌体展示技术,从全人源天然抗体库中筛选人probdnf前体蛋白特异性抗体。为此目的,采用本领域常规的噬菌体展示方法制备噬菌体展示库,并针对生物素标记的人probdnf前体重组蛋白实施四轮定向筛选,噬菌体展示库的制备方法和展示方法采用本领域常规的操作进行,如pct/cn2016/096292、antibodyphagedisplay(editedbyrobertaitken)所披露的方法。2.2人probdnf前体特异性结合抗体的鉴定从第四轮筛选所得的克隆中随机挑选96个,并用单噬菌体elisa(酶联免疫吸附实验)分析其与人probdnf前体的结合能力。为此目的,每个单菌落接种300μl2×yt/氨苄青霉素培养基(含2%葡萄糖)于96孔深孔培养板,并在37℃和250rpm下振荡培养16小时。用20μl培养物接种到500μl2×yt/氨苄青霉素培养基(含0.1%葡萄糖),在37℃和250rpm下振荡培养1.5小时。准备辅助噬菌体溶液,取75μl的m13ko7(滴度为3×1012pfu/ml)混入到15ml2×yt培养基中,50μl/孔加到培养板中。在37℃和150rpm条件培养30分钟,然后加入准备好的卡那霉素溶液50μl/孔(取180μl的50mg/ml卡那霉素,加入到15ml2×yt培养基),在37℃和250rpm下振荡培养16小时。最后离心沉淀细胞(30分钟,5000×g,4℃),上清转移到新的96孔深孔培养板。为进行单噬菌体elisa,在96孔medisorpelisa板(购自nunc)上分别使用100ng/孔抗原人probdnf前体以及阴性对照蛋白bsa(100μl/孔),在4℃包被过夜。每个孔用含2%bsa(w/v)的pbst封闭。随后用pbst清洗孔三次并排净。然后加入100μl/孔上面制备的每种噬菌体溶液到板上各孔中。37℃保温2小时后,用pbst洗涤三次。为了检测结合的噬菌体,将抗m13抗体过氧化物歧化酶偶联物(购自gehealthcare)以1:5000稀释于pbst中,并取100μl加到每个孔中。37℃保温1小时后用pbst漂洗孔三次,然后用pbs漂洗三次。最后吸取50μltmb底物加入到孔中,并在室温下显色10分钟,随后加入每孔50μl的2mh2so4终止显色反应。用酶联免疫检测仪(bio-rad)在450nm测量消光值。结合测序分析,观察到单链抗体1d3(核苷酸序列见seqidno:22、氨基酸序列见seqidno:21)和2h8(核苷酸序列见seqidno:24、氨基酸序列见23),在elisa实验中对人probdnf前体蛋白的结合信号较强,对bsa无结合(图1)。这两个抗体对应的质粒为pcantab-1d3和pcantab-2h8。实施例3.人probdnf前体蛋白单克隆抗体的制备在本实施例中,单克隆抗体的表达使用双质粒系统,需要分别把抗体重链可变区基因构建到包含了人igg1ch基因的pih质粒,把抗体轻链可变区基因构建到包含了人iggcl基因的pik质粒(质粒购自上海锐劲生物技术有限公司)。使用引物对1d3-hf(seqidno:30)和1d3-hr(seqidno:31)从模板质粒pcantab-1d3中扩增出vh-1d3片段。使用引物对hf1f(seqidno:32)和hf1r(seqidno:33)从模板质粒pih中扩增出hf1片段;使用引物对hf3f(seqidno:34)和hf3r(seqidno:35)从模板质粒pih中扩增出hf3片段。三个片段等摩尔比混合后进行拼接pcr,片段回收后经限制性内切酶nhei/noti双酶切,以t4dna连接酶于同样以nhei/noti双酶切载体质粒pih连接并转化于宿主菌top10中,挑取克隆通过pcr鉴定阳性克隆并通过测序确认,获得pih-1d3真核表达质粒。以同样的方式也获得了pih-2h8真核表达质粒。为获得pik-1d3真核表达质粒,使用引物对1d3-lf(seqidno:36)和1d3-lr(seqidno:37)从模板质粒pcantab-2h8中扩增出vl-2h8片段;使用引物对lf1f(seqidno:38)和lf1r(seqidno:39)从模板质粒pik中扩增出lf1片段。两个片段等摩尔比混合后进行拼接pcr,片段回收后经限制性内切酶ecorv/bsiwi双酶切,以t4dna连接酶于同样以ecorv/bsiwi双酶切载体质粒pik连接并转化于宿主菌top10中,挑取克隆通过pcr鉴定阳性克隆并通过测序确认。以同样的方式也获得了pik-2h8真核表达质粒。将表达质粒pih-1d3和pik-1d3等摩尔混合,pih-2h8和pik-2h8等摩尔混合,分别转染生长良好的hek-293f细胞,37℃,5%co2,125rpm摇床连续培养7天,4000rpm离心10min,去除沉淀,收集上清,并用0.45μm滤膜过滤,将处理好的样品以proteina(购自ge)亲和柱进行亲和纯化,最终获得纯化的重组单克隆抗体1d3和2h8,鉴定结果如图2所示。实施例4.人probdnf前体蛋白单克隆抗体的亲和力使用biacoret200系统(购自ge)通过捕获法分别测量了1d3和2h8单克隆抗体的亲和力和动力学参数。操作可参见说明书采用人probdnf前体蛋白的浓度分别为0.25nm、0.5nm、1nm、2nm、4nm和8nm。用biacoret200evaluationsoftware评估所得作用曲线,并计算亲和力kd值。图3和图4分别显示了单克隆抗体1d3和2h8在biacore亲和力测定实验中的动力学曲线。1d3和2h8的单克隆抗体分别对人probdnf前体蛋白的结合数据总结在表1中。表1.1d3和2h8的单克隆抗体对人probdnf前体蛋白的亲和力参数抗体样品ka(1/ms)kd(1/s)kd(m)1d3单抗5.256e+067.994e-041.521e-102h8单抗3.103e+065.940e-031.914e-09实施例5.2h8及1d3治疗实验性自身免疫性脑脊髓炎(eae)的实验本实验采用spf级6-8周雌性c57bl/6小鼠,体重18-20g。eae模型制备:将mog35-55(3mg/ml)/ifa(h37ra4mg/ml)完全乳化后,于小鼠上背部左右两侧及左侧尾根部进行皮下注射,剂量为150μl/小鼠。同时予以腹腔注射百日咳毒素ptx(0.5μg/100μl),剂量为50μl/小鼠,48小时后再次注射同剂量的ptx。于第7天给予mog35-55(3mg/ml)/ifa(h37ra2mg/ml)免疫小鼠下背部左右两侧及右侧尾根部进行皮下注射,剂量为150μl/小鼠。20只小鼠随机分为全人源igg对照抗体组和2h8单克隆抗体干预组组。同源igg对照抗体组在eae造模后第17天、19天和23天,腹腔注射全人源igg对照抗体0.2ml/次。2h8单克隆抗体干预组在造模后第17天、19天和23天,给予腹腔注射2h8单克隆抗体200μl,5mg/kg每次。对空白对照组和实验组的小鼠每天进行eae模型临床评分,评分标准如下:0分,无临床症状;0.5分,尾部无力;1分,尾部瘫痪;2分,协调性运动消失;2.5分,单侧后肢瘫痪;3分,双侧后肢瘫痪;3.5分,双侧后肢瘫痪伴前肢无力;4分,前肢瘫痪;5分,濒死或者死亡。死亡鼠在发现死亡当日记为5分,次日起不再记分。结果如图5a和5b所示,给予与同源对照抗体的eae小鼠在造模后17天,临床评分显著增加,临床评分超过2分,且持续维持至造模后49天;给予2h8单克隆抗体eae小鼠临床评分在造模后17天只49天,临床评分均低于1.5分;临床累计评分显示在同源对照抗体干预的eae小鼠临床治疗累积评分(43.45±5.009分)显著高于2h8克隆治疗的eae小鼠临床评分(24.65±1.282分),结果提示2h8克隆具有改善eae小鼠的临床症状。参照本实施例上述操作,对抗体1d3进行eae模型临床评分,结果如图6a和6b所示,与同种igg对照抗体干预组相比,1d3克隆干预组eae小鼠临床评分显著下降;临床累积治疗评分组1d3治疗组为21.65±1.734分,而同源对照igg抗体组则为43.45±5.009分,提示1d3可以显著减轻eae小鼠进程。实施例6.probdnf抗体对eae小鼠发病早期炎症因子的表达的影响参照实施例5的操作进行eae建模,实验分组:(1)正常对照(con)组;(2)单纯给予ab-probdnf单抗(ab-prob)组:造模前1天给予5mg/kgab-probdnf(1d3)单克隆抗体组;(3)eae造模+给予同源igg抗体对照(eae)组;(4)eae造模+给予ab-probdnf单克隆抗体(eae+ab-prob)组。采用qpcr的方法检测各组脊髓和脾脏与疾病相关基因表达,结果如图7所示。图7a显示炎症因子tnf-α基因表达情况。ab-prob组与正常对照组相比,tnf-α的表达基本相似,而eae组的tnf-α表达相比正常对照组显著增高,说明probdnf抗体对早期炎症具有干预和预防作用。eae+ab-prob组与eae组相比较,tnf-αmrna水平显著下降,且和正常对照组相比没有显著性差别,说明给予1d3单克隆抗体可以显著降低tnf-α的水平,即说明probdnf抗体具有抗炎作用。图7b、7c、7d分别显示ab-prob对eae小鼠脾脏il-6、il-2、il-4的作用。结果显示:与正常对照组相比,ab-prob组的il-6、il-2、il-4基因表达没有显著性差别,而eae组的tnf-α表达相比正常对照组显著增高,说明probdnf抗体对早期炎症具有干预和预防作用;eae组脾脏il-6、il-2、il-4基因与对照组相比,表达显著上调;给予1d3干预后(eae+ab-prob组),il-6、il-2、和il-4基因水平较eae组显著降低。这些结果说明给予probdnf抗体,可以抑制eae早期脾脏上调的il-6、il-2、il-4mrna水平,即说明probdnf抗体具有抗炎作用。实施例7.抗体的表位结合实验westernblot的结果显示抗体1d3,2h8能够结合变性的hubdnfpro,提示着两个抗体的结合表位很可能是线性的。将hubdnfpro平均分成两个肽段(e1,e2)或者三个肽段(e3,e4,e5),氨基酸序列如下:e1:pmkeanirgqgglaypgvrthgtlesvngpkagsrgltsladtfehmieelldedq(seqidno:40)e2:kvrpneennkdadlytsrvmlssqvpleppllflleeyknyldaanmsmrvrrh(seqidno:41)e3:pmkeanirgqgglaypgvrthgtlesvngpkagsrgl(seqidno:42)e4:tsladtfehmieelldedqkvrpneennkdadlytsr(seqidno:43)e5:vmlssqvpleppllflleeyknyldaanmsmrvrrh(seqidno:44)将这五个肽段和gst融合表达后纯化。通过elisa检测抗体1d3和2h8的结合。结果如图8所示,抗体1d3和2h8和gst-hubdnfpro全长,gst-hubdnfpro-e2肽段,gst-hubdnfpro-e5肽段都结合,提示这两个抗体的结合表位位于e5肽段的这36个氨基酸内。实施例8.抗体的表位结合实验进一步将e5肽段三等分成三个包含12个氨基酸的肽段,分别是vp肽段(vmlssqvplepp,seqidno:45),ll肽段(llflleeyknyl,seqidno:46),dh肽段(daanmsmrvrrh,seqidno:47)。通过吉尔生化(上海)有限公司体外合成生物素化的vp肽段,ll肽段以及dh肽段并通过elisa检测抗体的结合。结果如图9所示,抗体1d3和dh肽段结合比较强,2h8和dh肽段结合比较弱,和其他两个肽段不结合,提示抗体1d3的表位在dh肽段,2h8的表位在dh肽段附近。本发明涉及的序列总结于下表在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。序列表<110>上海易乐生物技术有限公司<120>多肽及结合多肽的抗体<130>p2018-1613<150>cn201710752743.8<151>2017-08-28<160>47<170>siposequencelisting1.0<210>1<211>5<212>prt<213>人工序列(artificialsequence)<400>1glytyraspmethis15<210>2<211>16<212>prt<213>人工序列(artificialsequence)<400>2glyleuglymetgluglyaspsertyrtyrseralaservallysgly151015<210>3<211>7<212>prt<213>人工序列(artificialsequence)<400>3aspvalhisglypheaspval15<210>4<211>16<212>prt<213>人工序列(artificialsequence)<400>4argserserglnserleuleutyrserasnglytyrthrtyrleuasp151015<210>5<211>7<212>prt<213>人工序列(artificialsequence)<400>5metglyserasnargalaser15<210>6<211>9<212>prt<213>人工序列(artificialsequence)<400>6metglnalaleuglnthrproleuthr15<210>7<211>115<212>prt<213>人工序列(artificialsequence)<400>7glnvalglnleuvalgluserglyglyglyleuileglnproglygly151015sermetargleusercysalaalaserglypheserleuserglytyr202530aspmethistrpvalargglnilealaglylysglyleuglutrpval354045alaglyleuglymetgluglyaspsertyrtyrseralaservallys505560glyargphethrileserargglnaspalalysasnserleutyrleu65707580glumetlysaspleuglyglyglyaspthralavaltyrtyrcysleu859095argaspvalhisglypheaspvaltrpglyglnglythrthrvalthr100105110valserser115<210>8<211>113<212>prt<213>人工序列(artificialsequence)<400>8aspvalvalmetthrglnserproleuserleuprovalthrprogly151015gluproalaserilesercysargserserglnserleuleutyrser202530asnglytyrthrtyrleuasptrptyrleuglnargproglyglnser354045proglnleuleuiletyrmetglyserasnargalaserglyvalpro505560aspargpheserglyserglyserglythraspphethrleulysile65707580serargvalglualagluaspvalglyvaltyrtyrcysmetglnala859095leuglnthrproleuthrpheglyglyglythrlysleugluilelys100105110arg<210>9<211>442<212>prt<213>人工序列(artificialsequence)<400>9glnvalglnleuvalgluserglyglyglyleuileglnproglygly151015sermetargleusercysalaalaserglypheserleuserglytyr202530aspmethistrpvalargglnilealaglylysglyleuglutrpval354045alaglyleuglymetgluglyaspsertyrtyrseralaservallys505560glyargphethrileserargglnaspalalysasnserleutyrleu65707580glumetlysaspleuglyglyglyaspthralavaltyrtyrcysleu859095argaspvalhisglypheaspvaltrpglyglnglythrthrvalthr100105110valserseralaserthrlysglyproservalpheproleualapro115120125cysserargserthrsergluserthralaalaleuglycysleuval130135140lysasptyrpheprogluprovalthrvalsertrpasnserglyala145150155160leuthrserglyvalhisthrpheproalavalleuglnsersergly165170175leutyrserleuserservalvalthrvalproserserserleugly180185190thrlysthrtyrthrcysasnvalasphislysproserasnthrlys195200205valasplysargvalgluserlystyrglyproprocysprosercys210215220proalaproglupheleuglyglyproservalpheleuphepropro225230235240lysprolysaspthrleumetileserargthrprogluvalthrcys245250255valvalvalaspvalserglngluaspprogluvalglnpheasntrp260265270tyrvalaspglyvalgluvalhisasnalalysthrlysproargglu275280285gluglnpheasnserthrtyrargvalvalservalleuthrvalleu290295300hisglnasptrpleuasnglylysglutyrlyscyslysvalserasn305310315320lysglyleuproserserileglulysthrileserlysalalysgly325330335glnproarggluproglnvaltyrthrleuproproserglngluglu340345350metthrlysasnglnvalserleuthrcysleuvallysglyphetyr355360365proseraspilealavalglutrpgluserasnglyglnprogluasn370375380asntyrlysthrthrproprovalleuaspseraspglyserphephe385390395400leutyrserargleuthrvalasplysserargtrpglngluglyasn405410415valphesercysservalmethisglualaleuhisasnhistyrthr420425430glnlysserleuserleuserproglylys435440<210>10<211>219<212>prt<213>人工序列(artificialsequence)<400>10aspvalvalmetthrglnserproleuserleuprovalthrprogly151015gluproalaserilesercysargserserglnserleuleutyrser202530asnglytyrthrtyrleuasptrptyrleuglnargproglyglnser354045proglnleuleuiletyrmetglyserasnargalaserglyvalpro505560aspargpheserglyserglyserglythraspphethrleulysile65707580serargvalglualagluaspvalglyvaltyrtyrcysmetglnala859095leuglnthrproleuthrpheglyglyglythrlysleugluilelys100105110argthrvalalaalaproservalpheilepheproproseraspglu115120125glnleulysserglythralaservalvalcysleuleuasnasnphe130135140tyrproargglualalysvalglntrplysvalaspasnalaleugln145150155160serglyasnserglngluservalthrgluglnaspserlysaspser165170175thrtyrserleuserserthrleuthrleuserlysalaasptyrglu180185190lyshislysvaltyralacysgluvalthrhisglnglyleuserser195200205provalthrlysserpheasnargglyglucys210215<210>11<211>5<212>prt<213>人工序列(artificialsequence)<400>11sertyrglymethis15<210>12<211>5<212>prt<213>人工序列(artificialsequence)<400>12sertyrglymethis15<210>13<211>10<212>prt<213>人工序列(artificialsequence)<400>13glyileleuthrglytyrvalpheasptyr1510<210>14<211>16<212>prt<213>人工序列(artificialsequence)<400>14argserserglnserleuvalserasnaspglyasnthrtyrleuasn151015<210>15<211>7<212>prt<213>人工序列(artificialsequence)<400>15metvalserlystrpaspser15<210>16<211>9<212>prt<213>人工序列(artificialsequence)<400>16metglnserthrhistrpproprothr15<210>17<211>119<212>prt<213>人工序列(artificialsequence)<400>17gluvalglnleuvalgluthrglyglyglyleuvalglnproglygly151015serleuargleusercysalaalaserglyphethrphesersertyr202530glymethistrpvalargglnalaproglylysglyleuglutrpval354045servalileserglyserglyaspserthrtyrtyralagluserval505560lysglyargphethrileserargaspasnalaargasnthrvaltyr65707580leuglnmetasnserleuargalagluaspthralavaltyrtyrcys859095alaserglyileleuthrglytyrvalpheasptyrtrpglylysgly100105110thrmetvalthrvalserser115<210>18<211>113<212>prt<213>人工序列(artificialsequence)<400>18aspvalvalmetthrglnserproleuserleuprovalthrleugly151015glnproalaserilesercysargserserglnserleuvalserasn202530aspglyasnthrtyrleuasntrppheglnglnargproglyglnpro354045proargargleuiletyrmetvalserlystrpaspserglyvalpro505560aspargpheserglyserglyserglythraspphethrleuargile65707580serargvalglualagluaspvalglyvaltyrtyrcysmetglnser859095thrhistrpproprothrpheglyglyglythrlysleugluilelys100105110arg<210>19<211>446<212>prt<213>人工序列(artificialsequence)<400>19gluvalglnleuvalgluthrglyglyglyleuvalglnproglygly151015serleuargleusercysalaalaserglyphethrphesersertyr202530glymethistrpvalargglnalaproglylysglyleuglutrpval354045servalileserglyserglyaspserthrtyrtyralagluserval505560lysglyargphethrileserargaspasnalaargasnthrvaltyr65707580leuglnmetasnserleuargalagluaspthralavaltyrtyrcys859095alaserglyileleuthrglytyrvalpheasptyrtrpglylysgly100105110thrmetvalthrvalserseralaserthrlysglyproservalphe115120125proleualaprocysserargserthrsergluserthralaalaleu130135140glycysleuvallysasptyrpheprogluprovalthrvalsertrp145150155160asnserglyalaleuthrserglyvalhisthrpheproalavalleu165170175glnserserglyleutyrserleuserservalvalthrvalproser180185190serserleuglythrlysthrtyrthrcysasnvalasphislyspro195200205serasnthrlysvalasplysargvalgluserlystyrglypropro210215220cysprosercysproalaproglupheleuglyglyproservalphe225230235240leupheproprolysprolysaspthrleumetileserargthrpro245250255gluvalthrcysvalvalvalaspvalserglngluaspprogluval260265270glnpheasntrptyrvalaspglyvalgluvalhisasnalalysthr275280285lysproargglugluglnpheasnserthrtyrargvalvalserval290295300leuthrvalleuhisglnasptrpleuasnglylysglutyrlyscys305310315320lysvalserasnlysglyleuproserserileglulysthrileser325330335lysalalysglyglnproarggluproglnvaltyrthrleupropro340345350serglngluglumetthrlysasnglnvalserleuthrcysleuval355360365lysglyphetyrproseraspilealavalglutrpgluserasngly370375380glnprogluasnasntyrlysthrthrproprovalleuaspserasp385390395400glyserphepheleutyrserargleuthrvalasplysserargtrp405410415glngluglyasnvalphesercysservalmethisglualaleuhis420425430asnhistyrthrglnlysserleuserleuserproglylys435440445<210>20<211>219<212>prt<213>人工序列(artificialsequence)<400>20aspvalvalmetthrglnserproleuserleuprovalthrleugly151015glnproalaserilesercysargserserglnserleuvalserasn202530aspglyasnthrtyrleuasntrppheglnglnargproglyglnpro354045proargargleuiletyrmetvalserlystrpaspserglyvalpro505560aspargpheserglyserglyserglythraspphethrleuargile65707580serargvalglualagluaspvalglyvaltyrtyrcysmetglnser859095thrhistrpproprothrpheglyglyglythrlysleugluilelys100105110argthrvalalaalaproservalpheilepheproproseraspglu115120125glnleulysserglythralaservalvalcysleuleuasnasnphe130135140tyrproargglualalysvalglntrplysvalaspasnalaleugln145150155160serglyasnserglngluservalthrgluglnaspserlysaspser165170175thrtyrserleuserserthrleuthrleuserlysalaasptyrglu180185190lyshislysvaltyralacysgluvalthrhisglnglyleuserser195200205provalthrlysserpheasnargglyglucys210215<210>21<211>243<212>prt<213>人工序列(artificialsequence)<400>21glnvalglnleuvalgluserglyglyglyleuileglnproglygly151015sermetargleusercysalaalaserglypheserleuserglytyr202530aspmethistrpvalargglnilealaglylysglyleuglutrpval354045alaglyleuglymetgluglyaspsertyrtyrseralaservallys505560glyargphethrileserargglnaspalalysasnserleutyrleu65707580glumetlysaspleuglyglyglyaspthralavaltyrtyrcysleu859095argaspvalhisglypheaspvaltrpglyglnglythrthrvalthr100105110valserserglyglyglyglyserglyglyglyglyserglyglygly115120125glyseraspvalvalmetthrglnserproleuserleuprovalthr130135140proglygluproalaserilesercysargserserglnserleuleu145150155160tyrserasnglytyrthrtyrleuasptrptyrleuglnargprogly165170175glnserproglnleuleuiletyrmetglyserasnargalasergly180185190valproaspargpheserglyserglyserglythraspphethrleu195200205lysileserargvalglualagluaspvalglyvaltyrtyrcysmet210215220glnalaleuglnthrproleuthrpheglyglyglythrlysleuglu225230235240ilelysarg<210>22<211>729<212>dna<213>人工序列(artificialsequence)<400>22caggtgcagctggtggagtctgggggaggcctgatacagccgggggggtcgatgagactc60tcctgtgcagcctctggattcagcctcagtggatatgacatgcactgggtccgccaaatt120gcgggaaaaggtctggagtgggtcgccggtcttgggatggaaggtgactcatattattca180gcctccgtgaagggccgattcaccatctccagacaagatgccaagaattccctgtatctt240gaaatgaaggacctgggaggcggggacacggctgtctattactgtctaagagatgtccac300ggattcgacgtctggggccaagggaccacggtcaccgtctcgagtggtggaggcggttca360ggcggaggtggttctggcggtggcggatcggatgttgtgatgactcagtctccactctcc420ctgcccgtcacccctggagagccggcctccatctcctgcaggtctagtcagagcctcctg480tatagtaatggatacacctatttggattggtacctgcagaggccagggcagtctccacag540ctcctgatctatatgggttctaatcgggcctccggggtccctgacaggttcagtggcagt600ggatcaggcacagattttacactgaaaatcagcagagtggaggctgaggatgttggggtt660tattactgcatgcaagctctacaaactcccctcactttcggcggagggaccaagctggag720atcaaacgt729<210>23<211>247<212>prt<213>人工序列(artificialsequence)<400>23gluvalglnleuvalgluthrglyglyglyleuvalglnproglygly151015serleuargleusercysalaalaserglyphethrphesersertyr202530glymethistrpvalargglnalaproglylysglyleuglutrpval354045servalileserglyserglyaspserthrtyrtyralagluserval505560lysglyargphethrileserargaspasnalaargasnthrvaltyr65707580leuglnmetasnserleuargalagluaspthralavaltyrtyrcys859095alaserglyileleuthrglytyrvalpheasptyrtrpglylysgly100105110thrmetvalthrvalserserglyglyglyglyserglyglyglygly115120125serglyglyglyglyseraspvalvalmetthrglnserproleuser130135140leuprovalthrleuglyglnproalaserilesercysargserser145150155160glnserleuvalserasnaspglyasnthrtyrleuasntrpphegln165170175glnargproglyglnproproargargleuiletyrmetvalserlys180185190trpaspserglyvalproaspargpheserglyserglyserglythr195200205aspphethrleuargileserargvalglualagluaspvalglyval210215220tyrtyrcysmetglnserthrhistrpproprothrpheglyglygly225230235240thrlysleugluilelysarg245<210>24<211>741<212>dna<213>人工序列(artificialsequence)<400>24gaggtgcagctggtggagactgggggcggcttggtccagcctggggggtccctgagactc60tcctgtgcagcgtctggattcaccttcagtagctatggcatgcactgggtccgccaggct120ccagggaaggggctggagtgggtctcagttattagtggtagtggtgatagtacatactac180gcagagtccgtgaagggccgcttcaccatctccagagacaatgccaggaacacggtgtat240ctgcaaatgaacagtctgagagccgaggacacggctgtatattattgtgcaagtggcatt300ttgactggttatgtatttgactattggggcaaagggacaatggtcaccgtctcgagtggt360ggaggcggttcaggcggaggtggttctggcggtggcggatcggatgttgtgatgactcag420tctccactctccctgcccgtcacccttggacagccggcctccatctcctgcaggtctagt480caaagcctcgtatccaatgatggaaacacctacttgaattggtttcagcagaggccaggc540caacctccaaggcgcctaatttatatggtttctaagtgggactctggggtcccagacaga600ttcagcggcagtgggtcaggcactgatttcacactgagaatcagcagggtggaggctgag660gatgttggggtttattactgcatgcaaagtacacactggcctcccactttcggcggaggg720accaagctggagatcaaacgt741<210>25<211>30<212>dna<213>人工序列(artificialsequence)<400>25gcgaattccccatgaaagaagcaaacatcc30<210>26<211>35<212>dna<213>人工序列(artificialsequence)<400>26ccgctcgagttatcttccccttttaatggtcaatg35<210>27<211>330<212>dna<213>人工序列(artificialsequence)<400>27gcccccatgaaagaagcaaacatccgaggacaaggtggcttggcctacccaggtgtgcgg60acccatgggactctggagagcgtgaatgggcccaaggcaggttcaagaggcttgacatca120ttggctgacactttcgaacacatgatagaagagctgttggatgaggaccagaaagttcgg180cccaatgaagaaaacaataaggacgcagacttgtacacgtccagggtgatgctcagtagt240caagtgcctttggagcctcctcttctctttctgctggaggaatacaaaaattacctagat300gctgcaaacatgtccatgagggtccggcgc330<210>28<211>36<212>dna<213>人工序列(artificialsequence)<400>28gctggctagcacccatgaaagaagcaaacatccgag36<210>29<211>28<212>dna<213>人工序列(artificialsequence)<400>29ccgctcgaggtggcgccggaccctcatg28<210>30<211>39<212>dna<213>人工序列(artificialsequence)<400>30gcctttcctggtttcctgtctcaggtgcagctggtggag39<210>31<211>38<212>dna<213>人工序列(artificialsequence)<400>31atgggcccttggtggaggcactcgagacggtgaccgtg38<210>32<211>22<212>dna<213>人工序列(artificialsequence)<400>32ggctaactagagaacccactgc22<210>33<211>21<212>dna<213>人工序列(artificialsequence)<400>33agacaggaaaccaggaaaggc21<210>34<211>20<212>dna<213>人工序列(artificialsequence)<400>34gcctccaccaagggcccatc20<210>35<211>21<212>dna<213>人工序列(artificialsequence)<400>35gacaatcttagcgcagaagtc21<210>36<211>47<212>dna<213>人工序列(artificialsequence)<400>36ctttggtttccaggtgcaagatgtgatgttgtgatgactcagtctcc47<210>37<211>26<212>dna<213>人工序列(artificialsequence)<400>37caccgtacgtttgatctccagcttgg26<210>38<211>22<212>dna<213>人工序列(artificialsequence)<400>38ggctaactagagaacccactgc22<210>39<211>24<212>dna<213>人工序列(artificialsequence)<400>39acatcttgcacctggaaaccaaag24<210>40<211>56<212>prt<213>人工序列(artificialsequence)<400>40prometlysglualaasnileargglyglnglyglyleualatyrpro151015glyvalargthrhisglythrleugluservalasnglyprolysala202530glyserargglyleuthrserleualaaspthrphegluhismetile354045glugluleuleuaspgluaspgln5055<210>41<211>54<212>prt<213>人工序列(artificialsequence)<400>41lysvalargproasnglugluasnasnlysaspalaaspleutyrthr151015serargvalmetleuserserglnvalproleugluproproleuleu202530pheleuleugluglutyrlysasntyrleuaspalaalaasnmetser354045metargvalargarghis50<210>42<211>37<212>prt<213>人工序列(artificialsequence)<400>42thrserleualaaspthrphegluhismetileglugluleuleuasp151015gluaspglnlysvalargproasnglugluasnasnlysaspalaasp202530leutyrthrserarg35<210>43<211>37<212>prt<213>人工序列(artificialsequence)<400>43thrserleualaaspthrphegluhismetileglugluleuleuasp151015gluaspglnlysvalargproasnglugluasnasnlysaspalaasp202530leutyrthrserarg35<210>44<211>36<212>prt<213>人工序列(artificialsequence)<400>44valmetleuserserglnvalproleugluproproleuleupheleu151015leugluglutyrlysasntyrleuaspalaalaasnmetsermetarg202530valargarghis35<210>45<211>12<212>prt<213>人工序列(artificialsequence)<400>45valmetleuserserglnvalproleuglupropro1510<210>46<211>12<212>prt<213>人工序列(artificialsequence)<400>46leuleupheleuleugluglutyrlysasntyrleu1510<210>47<211>12<212>prt<213>人工序列(artificialsequence)<400>47aspalaalaasnmetsermetargvalargarghis1510当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1