一种Fe3+/2+-NO供体混价配位聚合物及其应用的制作方法
本发明属于生物医药技术和纳米科技领域,具体涉及一种fe3+/2+-no供体混价配位聚合物及其抗肿瘤应用。
背景技术:
一氧化氮(no)是一种重要的内源性信使物质和(或)效应分子,参与体内众多的生理和病理过程。近年来,no与肿瘤的发生、发展、凋亡、侵袭和转移的关系引起了人们的广泛关注,成为肿瘤预防和治疗的新方向。已有大量研究表明,no是一把“双刃剑”,对肿瘤具有双重作用。低浓度的no促进肿瘤的发展、血管生成和转移,而高浓度的no则可以抑制肿瘤的生长,加速肿瘤细胞凋亡,表现出抗瘤作用。因此,在肿瘤部位释放高浓度的no,能够有效实现抗肿瘤治疗。
然而no气体的半衰期极短、稳定性差,将体外no直接输送至体内肿瘤部位非常困难,尤其是高浓度的no。no供体,即能够在体内产生no的化合物,备受关注,已成为no用于肿瘤治疗的重要化合物。尽管no供体前药在一定程度上提高了no抗肿瘤的疗效,但这些no供体大部分分子质量较低,容易被网状内皮系统清除且本身稳定性有限等。因而,单独的no供体治疗仍然难以达到预期的治疗效果。
随着纳米科技的飞速发展,纳米技术和纳米材料被广泛应用于疾病的诊疗。其中,纳米药物兼具药物和纳米材料的双重身份,与传统药物相比有其独特的优点,如能提高药物的稳定性;高比表面积,能够负载大量的药物;具有高效的实体瘤高通透性和滞留效应(enhancedpermeabilityandretentioneffect,epr),能够被动靶向肿瘤;可通过调控纳米材料的光信号、温度、磁场或利用肿瘤微环境响应等,实现在肿瘤部位药物的可控释放等。
2008年发表于journalofmedicinalchemistry杂志题为arylbis(diazeniumdiolates):potentinducersofs-glutathionylationofcellularproteinsandtheirinvitroantiproliferativeactivities的文献公开了一种含有2个游离羧基的no供体化合物bpdb,其可以被肿瘤组织或细胞中过表达的gsh激活,释放出4分子的no,并对hl-60细胞表现出一定的的增殖抑制活性。但是,此no供体分子(bpdb),与前期报道的no供体分子js-k类似,均依靠gsh激活,而正常组织和血浆中也含有一定量的gsh,造成该类化合物血浆稳定性差,半衰期短。即化合物在未到达肿瘤组织或进入肿瘤细胞时,绝大部分已被降解并产生no,造成抗肿瘤活性大大降低,同时在非肿瘤部位产生的no,会对正常组织或细胞产生较大的毒副作用。因此,上述问题限制了该no供体作为抗肿瘤药物的进一步研发及临床应用。
技术实现要素:
基于上述研究背景,本发明从3个方面考虑,①提高bpdb的血浆稳定性,延长其发挥抗肿瘤作用的时间,使其具有体内应用的潜力;②bpdb单一适用,活性不够理想,以期设计新的分子,其同时可产生no及其他细胞毒药物,从而发挥协同抗肿瘤作用,提高抗肿瘤活性,使其具有临床前或临床应用的实际价值;③降低bpdb对正常组织或细胞的毒副作用,实现其增效减毒的目的,以期克服目前bpdb存在的问题,提高其成药性,使其具有进一步临床应用的价值和潜力。
本发明一方面利用金属铁离子与羧基(-cooh)有较强的配位能力,在较温和的条件下能与带有-cooh尤其是多个-cooh的有机配体形成配位聚合纳米材料;另一方面,利用fe2+作为芬顿试剂,能有效催化h2o2反应生成细胞毒性更大的活性氧簇(ros),以期实现化学动力学治疗(chemodynamictherapy,cdt),设计了一种基于no供体(bpdb)的fe3+/2+-no供体混价配位聚合物纳米颗粒,能在肿瘤组织部位累积,实现肿瘤微环境gsh和h2o2响应的no和cdt的协同抗肿瘤治疗。
本发明具体技术方案如下:
一种fe3+/2+-no供体混价配位聚合物,no供体1,5-二(l-脯氨酸偶氮翁-o2-)-2,4-二硝基苯(简称为bpdb)与fe3+和fe2+形成混价配位聚合物。bpdb结构如下:
上述fe3+/2+-no供体混价配位聚合物中fe3+和fe2+的比例因制备条件不同而发生变化。
本发明一个具体的技术方案中,fe3+/2+-no供体混价配位聚合物的分子式为fex+4(bpdb)(h2o)2,所述fex+代表fe3+和fe2+。优选fe3+的fe2+比例为2.3:1.7。
上述分子式中一分子bpdb可以与4个fex+离子形成配位,fex+为fe3+和fe2+的混合,这是因为制备方法中先制备fe3+-bpdb,再采用fe2+进行离子交换,交换达到平衡时,得到的是既有fe3+也有fe2+与bpdb配位的混价配位聚合物。
上述配位聚合物可以在特定条件下形成聚合纳米颗粒,粒径为270–530nm,优选270nm。fe3+/2+-no供体混价配位聚合物纳米颗粒的水溶性和体内稳定性优于单独的no供体,适合用于体内抗肿瘤治疗。
本发明另一目的在于提供上述fe3+/2+-no供体混价配位聚合物的制备方法,由所述no供体1,5-二(l-脯氨酸偶氮翁-o2-)-2,4-二硝基苯和fe3+配位形成聚合物,再进一步与fe2+经离子交换制得。
上述fe3+/2+-no供体混价配位聚合物纳米颗粒的制备方法如下:
(1)将no供体1,5-二(l-脯氨酸偶氮翁-o2-)-2,4-二硝基苯和fe3+(可使用水溶性三价铁盐,如fecl3.6h2o)分散于水溶液中,调节溶液ph值至弱酸性;
(2)在剧烈搅拌下加入不良溶剂诱导纳米颗粒的形成,继续搅拌直至颗粒生长完成、离心、洗涤得到fe3+-no供体混价配位聚合物纳米颗粒(fe3+-bpdb-ncp);
(3)将fe3+-bpdb-ncp与fe2+(可使用水溶性二价铁盐,如fecl2.4h2o)在水溶液中进行交换,交换达到平衡后,离心、洗涤、收集产品,即可得到fe3+/2+-no供体混价配位聚合物纳米颗粒(fe3+/2+-bpdb-ncp)。优选的,所述no供体和fe3+的摩尔比为1:15~1:10,优选为2:15。
上述不良溶剂选自无水甲醇、无水乙醇等醇类溶剂中的一种或几种,优选无水甲醇。
优选的,所述fe3+-bpdb-ncp与fe2+摩尔比为2:1~1:2,优选为1:1。
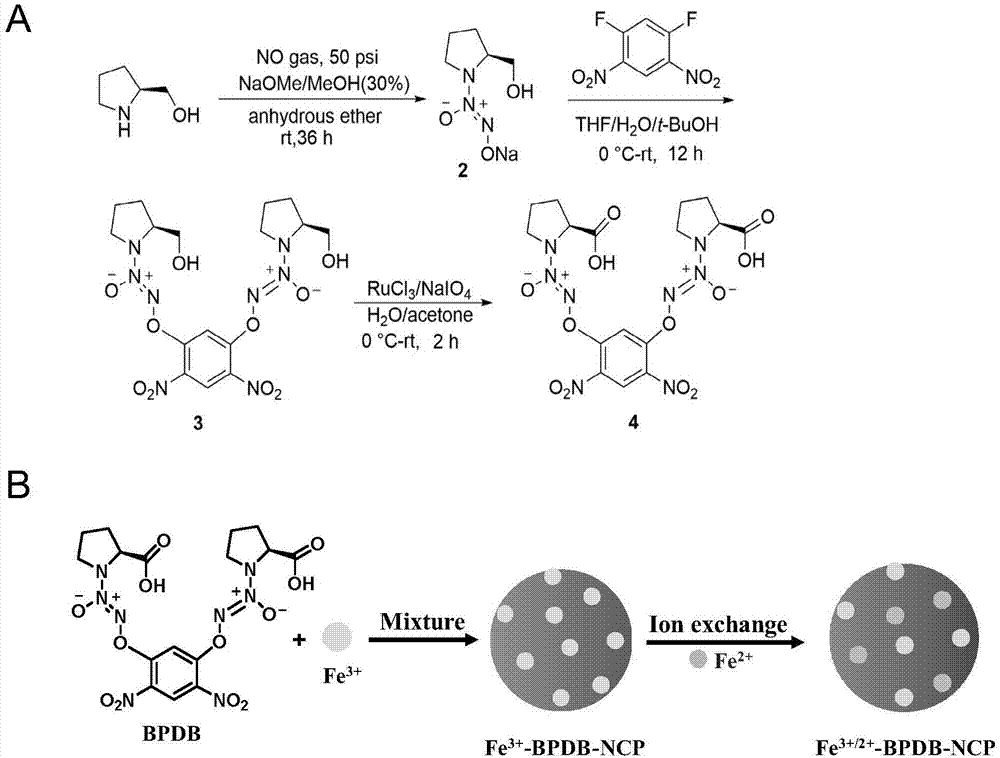
本发明所述no供体可采用发表于journalofmedicinalchemistry杂志题为arylbis(diazeniumdiolates):potentinducersofs-glutathionylationofcellularproteinsandtheirinvitroantiproliferativeactivities的文献中公开的方法制备而成。反应路线如图1a所示。
本发明的另一目的在于提供所述的fe3+/2+-no供体混价配位聚合物在制备抗肿瘤药物中的应用。进一步的,所述fe3+/2+-no供体混价配位聚合物可以作为前药受到肿瘤微环境高浓度gsh和h2o2响应分别释放no和产生ros。
本发明的另一目的在于提供一种药物制剂,含有本发明所述的fe3+/2+-no供体混价配位聚合物。
本发明优点:
(1)本发明所述的fe3+/2+-no供体混价配位聚合物通过实体瘤的高通透性和滞留效应(epr效应)被动靶向肿瘤;在肿瘤微环境高浓度gsh和高浓度h2o2响应下,释放no以及产生ros,实现肿瘤的高效、低毒、协同治疗。
(2)本发明研究中发现,直接使用no供体和fe2+制备fe2+-bpdb配位聚合物无法制成纳米颗粒,因此巧妙地先将no供体和fe3+配位形成络合物,进一步与fe2+经离子交换后制得fe3+/2+-no供体混价配位纳米颗粒。制得的纳米颗粒相对于单独的no供体具有更高的水溶性和稳定性,适合应用于体内治疗。
附图说明
图1(a)为本发明中no供体的合成路线图;(b)为本发明所述fe3+/2+-no供体混价配位聚合纳米颗粒的合成路线图。
图2为本发明实施例2中fe2+-bpdb配位聚合物的dls表征结果。
图3为本发明实施例1中各配位聚合纳米颗粒的(a)tem,(b)eds和(c)xps图。
图4为本发明实施例1制得的fe3+/2+-bpdb-ncp和no供体的水溶性(a)和体内稳定性(b)考察结果。
图5为本发明实施例5中各配位聚合纳米颗粒体外(a)gsh浓度与no释放的关系曲线,(b)羟自由基和超氧阴离子产生的荧光曲线,(c)活性氧簇产生的荧光曲线和(d)h2o2浓度与活性氧簇产生的关系曲线。
图6为本发明实施例6中各配位聚合纳米颗粒hepg2细胞内(a)no释放的共聚焦成像图和(b)ros产生的共聚焦成像图。
图7为本发明实施例7中(a)生理盐水,(b)no供体,(c)fe3+/2+-bpdb-ncp纳米颗粒制剂的药效学结果:(a)相对肿瘤体积,(b)小鼠体重,(c)生存期,(d)肿瘤重量,(e)肿瘤组织的h&e染色和tunel染色结果。
具体实施方式
在本发明中所使用的术语,除非另有说明,一般具有本领域普通技术人员通常理解的含义。
下面结合具体实施例并参照数据进一步详细描述本发明。应理解,该实施例只是为了举例说明本发明,而非以任何方式限制本发明的范围。
在以下实施例中,未详细描述的各种过程和方法是本领域中公知的常规方法。下述实例中所用的材料、试剂、装置、仪器、设备等,如无特殊说明,均可从商业途径获得。
本发明构建了一种fe3+/2+-no供体混价配位聚合纳米颗粒,其水溶性和体内稳定性优于单独no供体,更适合应用于体内抗肿瘤治疗。并对其体外表征,体外no的释放和ros的产生,细胞水平no的释放和ros的产生以及动物药效学进行了研究。
实施例1fe3+/2+-no供体混价配位聚合纳米颗粒(fe3+/2+-bpdb-ncp)的构建
一、no供体1,5-二(l-脯氨酸偶氮翁-o2-)-2,4-二硝基苯的合成,合成路线如图1a所示。
(a)
(b)
(c)
二、fe3+/2+-no供体混价配位聚合纳米颗粒(fe3+/2+-bpdb-ncp)的制备
分别采用不良溶剂法、溶剂热法对fe3+/2+-no供体混价配位聚合纳米颗粒的制备进行了研究。
1.不良溶剂法
fe3+/2+-bpdb-ncp的合成路线如图1b所示:
将no供体1,5-二(l-脯氨酸偶氮翁-o2-)-2,4-二硝基苯(bpdb)和fecl3.6h2o以摩尔比为2:15分散于水溶液中,并用稀naoh溶液调节ph值至5.5。然后,在剧烈搅拌下加入无水甲醇诱导纳米颗粒的形成,继续搅拌一段时间,直至颗粒生长完成。离心、洗涤即可得到fe3+-bpdb-ncp。该方法可通过调节加入无水甲醇的速度,调控合成不同尺寸的纳米颗粒。
基于离子交换的方法,将fe3+-bpdb-ncp纳米颗粒与等摩尔比的fecl2.4h2o在水溶液中进行交换,交换达到平衡后,离心、洗涤、收集产品,即可得到fe3+/2+-bpdb-ncp。
2.溶剂热法
将no供体1,5-二(l-脯氨酸偶氮翁-o2-)-2,4-二硝基苯(bpdb)和fecl3.6h2o以摩尔比为2:15分散于dmf中,然后加热至90℃保持8h。实验过程中发现,加热过程中no供体受热分解产生了no,不能有效形成所需的配位聚合物。上述实验说明,no供体合成配位聚合物需要温和的反应条件,如本发明中的不良溶剂法。
实施例2fe2+-bpdb配位聚合物的制备
将no供体1,5-二(l-脯氨酸偶氮翁-o2-)-2,4-二硝基苯(bpdb)和fecl2.4h2o以摩尔比为2:15分散于水溶液中,并用稀naoh溶液调节ph值至5.5。然后,在剧烈搅拌下加入无水甲醇诱导fe2+-bpdb颗粒的形成,继续搅拌一段时间,直至颗粒生长完成。离心、洗涤得到fe2+-bpdb颗粒。重复三次,三次样品的dls表征结果如图2所示。结果表明fe2+-bpdb的水合粒径大于1μm,无法进一步制备得到所需纳米级的颗粒。
dls表征:
取新鲜制备的fe2+-bpdb配位聚合物200μl,蒸馏水稀释至3ml,在粒径电位仪上对脂质体制剂进行其水合粒径的测定。
实施例3fe3+/2+-no供体混价配位聚合物纳米颗粒(fe3+/2+-bpdb-ncp)的表征
tem和eds测定:
取实施例1不良溶剂法新鲜制备的fe3+-bpdb-ncp和fe3+/2+-bpdb-ncp,稀释一定倍数后滴到铜网上,待自然风干后,于透射电子显微镜上表征材料的形貌、尺寸(tem)以及元素组成(eds)。
xps测定:
制备好的fe3+-bpdb-ncp和fe3+/2+-bpdb-ncp冷冻干燥后,收集粉末,用x射线光电子能谱分析仪表征材料表面铁离子,并通过软件分峰计算得到fe3+和fe2+的比例。
图3为本发明实施例1制得的各配位聚合纳米颗粒的(a)tem,(b)eds和(c)xps图。表明成功合成了以no供体bpdb为配体,以fe3+/2+混价为金属配位离子的配位聚合纳米颗粒。
根据上述tem,eds和xps结果,计算出fe3+/2+-no供体混价配位聚合物的分子式为fex+4(bpdb)(h2o)2,fex+为fe3+和fe2+,fe3+和fe2+比例为2.3:1.7。
实施例4no供体和fe3+/2+-no供体混价配位聚合纳米颗粒(fe3+/2+-bpdb-ncp)的水溶性和稳定性考察
水溶性:将no供体1,5-二(l-脯氨酸偶氮翁-o2-)-2,4-二硝基苯(bpdb)分别分散于无水甲醇和水中,fe3+/2+-bpdb-ncp分散于水中,制备得到1mg/ml的溶液。通过拍照记录它们在各溶剂中的分散性和溶解性。如图4a所示,bpdb只能溶解于甲醇溶液中,在水中分散性差,而fe3+/2+-bpdb-ncp能很好的溶解在水中。
稳定性:15mg/kg的bpdb和fe3+/2+-bpdb-ncp通过尾静脉注射入大鼠内体,通过血压计测量大鼠尾巴的舒张压来表征no在体内循环中的稳定性,如图4b所示。其结果表明fe3+/2+-bpdb-ncp在体内有较高的稳定性,而单独的no供体bpdb体内稳定性差,在未到达肿瘤部位就开始释放no了。
实施例5fe3+/2+-no供体混价配位聚合物纳米颗粒(fe3+/2+-bpdb-ncp)的体外释放行为研究
本发明的fe3+/2+-bpdb-ncp体外no释放和活性氧簇产生的检测方法如下:
一方面,由于多功能no供体是gsh响应的,因而配位聚合物纳米颗粒释放no也是gsh触发的。将fe3+/2+-bpdb-ncp与不同浓度的gsh共孵育2h,用griess试剂检测no的释放量。另一方面,no供体配位聚合物纳米颗粒中fe2+是有效的fenton试剂,能够催化h2o2产生活性氧簇包括羟自由基、超氧阴离子。将fe3+/2+-bpdb-ncp与h2o2共孵育30min,分别用对苯二甲酸、二氢乙锭和dcfh-da检测.oh、.o2-和ros的产生。结果如图5所示,表明本发明合成的fe3+/2+-no供体混价配位聚合纳米颗粒在gsh和h2o2响应下能分别释放出no和产生ros。
实施例6fe3+/2+-no供体混价配位聚合物纳米颗粒(fe3+/2+-bpdb-ncp)的细胞成像研究(a)no成像:将hepg2细胞接种于共聚焦培养皿内,接种密度为1×105个/孔,并在5%co2无菌培养箱(37℃,饱和湿度)内孵育过夜。24h后,将原培养液吸出,加入无血清含有5μmdaf-fmdano检测探针的dmem,于培养箱中培育20min。将dmem弃掉,用pbs溶液洗涤3次,分别加入5%血清-dmem溶液、含有20μg/mlbpdb的5%血清-dmem溶液和20μg/mlfe3+/2+-bpdb-ncp的5%血清-dmem溶液。继续孵育3h,弃掉上清用pbs洗涤3次,加入1μg/mlhoechst33342进行核染。核染15min,pbs洗涤3次后用4%的多聚甲醛固定细胞用于共聚焦成像观察。
(b)ros成像:将hepg2细胞接种于共聚焦培养皿内,接种密度为1×105个/孔,并在5%co2无菌培养箱(37℃,饱和湿度)内孵育过夜。24h后,将原培养液吸出,加入无血清含有10μmdcfh-daros检测探针的dmem,于培养箱中培育20min。将dmem弃掉,用pbs溶液洗涤3次,分别加入5%血清-dmem溶液、含有20μg/mlfe3+-bpdb-ncp的5%血清-dmem溶液和20μg/mlfe3+/2+-bpdb-ncp的5%血清-dmem溶液。继续孵育3h,弃掉上清用pbs洗涤3次,加入1μg/mlhoechst33342进行核染。核染15min,pbs洗涤3次后用4%的多聚甲醛固定细胞用于共聚焦成像观察。
结果如图6所示,表明本发明合成的fe3+/2+-no供体混价配位聚合纳米颗粒在细胞水平上能有效释放no和产生ros,且释放no的量较单独no供体bpdb多,产生ros的量也多于fe3+-bpdb-ncp,为体内no-cdt协同治疗提供依据。
实施例7fe3+/2+-no供体混价配位聚合物纳米颗粒(fe3+/2+-bpdb-ncp)的药效学研究
对健康icr小鼠进行腋下植瘤,每只小鼠注射heps瘤溶液(1×107个/ml)100μl,当瘤体积至约100~200mm3时,将移植瘤小鼠随机分成3组(n=8),将给药的第一天设为第0天,则分别于第0、2、4、6、8、10天注射生理盐水、no供体和fe3+/2+-bpdb-ncp制剂,剂量均为15mg/kg。同时隔天记录小鼠的体重和肿瘤的大小,最后一次给药后,将小鼠处死,剥离肿瘤,并称重。瘤体积的计算方法采用以下公式:volume=(w2×l)/2其中w为肿瘤最短的半径,l为肿瘤最长半径。
结果如图7所示,证明本发明合成的fe3+/2+-no供体混价配位聚合纳米颗粒在老鼠体内的抗肿瘤治疗效果明显优于单独的no供体bpdb,且没有明显的毒副作用。
- 还没有人留言评论。精彩留言会获得点赞!