大黄鱼清道夫受体基因MARCO基因及其免疫防御功能的制作方法
本发明涉及基因工程技术领域,尤其是涉及大黄鱼清道夫受体基因marco基因及其免疫防御功能。
技术背景
大黄鱼(larimichthyscrocea)广泛分布于我国东南沿海,俗称“黄花鱼”,肉质鲜嫩爽滑,营养价值高,是百姓餐桌上的常见食用鱼,在经历了从资源紧缺状态到后来大规模人工养殖以及大力开拓国内外市场后,大黄鱼的经济地位不断提升,其人工养殖也越来越受到广泛关注,但养殖大黄鱼通常离不开抵抗病原菌的问题,因而免疫相关基因的开发和利用尤显重要。基于大黄鱼的全基因组测序的完成,人们对大黄鱼的基因研究上了一个新台阶,大黄鱼先天性免疫基因特征也逐渐被解析,其中作为免疫防御第一防线的模式识别受体(patternrecognitionreceptors,prrs)尤为关键,该类分子通过两种模式防止感染和识别内部损伤:即病原相关分子模式(pathogen-associatedmolecularpatterns,pamps)和损伤相关分子模式(damage-associatedmolecularpatterns,damps)。清道夫受体(scavengerreceptors,srs)是第一个被描述的prrs,srs是多种结构功能各异的蛋白分子的统称,能结合、转移、在细胞内降解乙酰化/氧化修饰的低密度脂蛋白(acetylatedlowdensitylipoproteins,acldl/oxidisedlowdensitylipoproteinsoxldl),并能与多种配体结合发挥不同作用。目前发现的清道夫受体大致有a到h共8类,称为清道夫受体家族,另有i、j类仍处于探索阶段。该家族成员在内皮细胞、巨噬细胞、平滑肌细胞、血细胞、破骨细胞、脂肪细胞、树突状细胞、血小板等细胞中发现清道夫受体家族成员表达调控。其中a类清道夫受体的一种marco的胞外区缺少α-螺旋卷曲motif,为胶原样结构域,这些都跟受体三聚体的形成密切相关,在c末端含有6个保守的半胱氨酸,并都有一个srcr结构域,与sr-ai结构有较大的相似性。marco在脾脏边缘区的巨噬细胞中大量表达,而脾脏是人体最大的周围淋巴器官,该边缘区位于白髓和红髓的交界处,分布着丰富的巨噬细胞、树突状细胞和b淋巴细胞,边缘区的边缘窦是最早接触和识别抗原的部位,因此可以判断在边缘区高表达的marco参与机体的免疫反应,起到识别病原体的重要作用。marco与pamps的结合主要与srcr结构域有关,可以结合革兰氏阳性菌和革兰氏阴性菌,还能结合石英颗粒和乳胶微球等。有报道称,人和鼠的marco基因在敲除srcr结构域后,将不能正确识别和结合相应的配体。因此研究marco基因及其相关免疫功能对进一步阐明大黄鱼的固有免疫系统调控机制、掌握marco基因对大黄鱼免疫代谢的影响奠定基础。同时,为预防病原菌引起的疾病提供理论基础,也为揭示大黄鱼健康养殖提供理论指导。
技术实现要素:
本发明的目的之一在于提供一种大黄鱼清道夫受体基因marco基因,其采用同源克隆法与race技术克隆获得,克隆过程中总rna提取效果好,能灭活内源rna酶,不会引起rna的降解,保持rna的完整性,提高总rna的得率和纯度。
本发明的目的之二在于提供一种marco基因在大黄鱼免疫防御功能中的用途,为预防病原菌引起的疾病提供理论基础,也为揭示大黄鱼健康养殖提供理论指导。
本发明针对
背景技术:
中提到的问题,采取的技术方案为:
大黄鱼清道夫受体基因marco基因,marco基因开放阅读框序列采用同源克隆法与race技术克隆获得,其中marco基因开放阅读框序列如如seqidno:1所示。
作为优选,marco基因放阅读框序列全长为1218bp,编码405个氨基酸。
作为优选,marco基因克隆包括如下步骤:
以提取的总rna反转录合成的cdna为模板扩增marco基因片段,纯化;
将纯化后的扩增产物进行t-a克隆,测序,即得marco基因。
进一步优选,基因扩增用引物为:
marco–f:5'-atggagacgtaggtggagggcacc-3';
marco–r:5'-ctaggagccctccagtgccgg-3'。
进一步优选,扩增反应体系为:2.5μl10×pcrbuffer、0.4μldntps、0.8μlmarco-f、0.8μlmarco-r、0.6μltemplatecdna、0.4μltaqdnapolymerase(takara)、14.5μlrnasefreeddh2o。
进一步优选,扩增条件为:95℃预变性4min;94℃变性30s,55-65℃退火30s,72℃延伸2min,循环35次;最后72℃延伸10min。
进一步优选,总rna提取采用trizolregent、磷酸胍和硫脲进行提取。trizolregent、磷酸胍和硫脲能够发挥增益作用,一方面可迅速渗入组织,灭活内源rna酶,不会引起rna的降解,便于rna的后续提取,并且具有极强的裂解能力,可在短时间内裂解细胞和组织样本,能够使细胞释放出的蛋白质迅速发生变性并抑制细胞释放出的rna酶活性,有效抑制样本中rna的降解,保持rna的完整性;另一方面协助变性的蛋白质等物质溶解于后续加入的氯仿,使得rna能快速分布在上层水相中,提高总rna的得率和纯度。
更进一步优选,trizolregent中含有0.03-0.04%磷酸胍和0.01-0.02%硫脲。
本发明还公开了大黄鱼清道夫受体基因marco基因的用途,marco基因在大黄鱼免疫防御功能中的用途。marco基因在巨噬细胞膜外均含有胶原样结构域及富含半胱氨酸的结构域,这些结构域是与配基结合的重要部位,可以促进巨噬细胞的粘附,参与清除机体内的凋亡细胞,另外还可以抵抗病原菌的入侵,在机体防御方面也发挥着重要作用,为预防病原菌引起的疾病提供理论基础,也为揭示大黄鱼健康养殖提供理论指导。
与现有技术相比,本发明的优点在于:本发明克隆了marco基因,克隆过程中总rna提取效果好,能灭活内源rna酶,不会引起rna的降解,保持rna的完整性,提高总rna的得率和纯度;本发明克隆的marco基因在大黄鱼免疫防御功能中的用途,为预防病原菌引起的疾病提供理论基础,也为揭示大黄鱼健康养殖提供理论指导。
附图说明
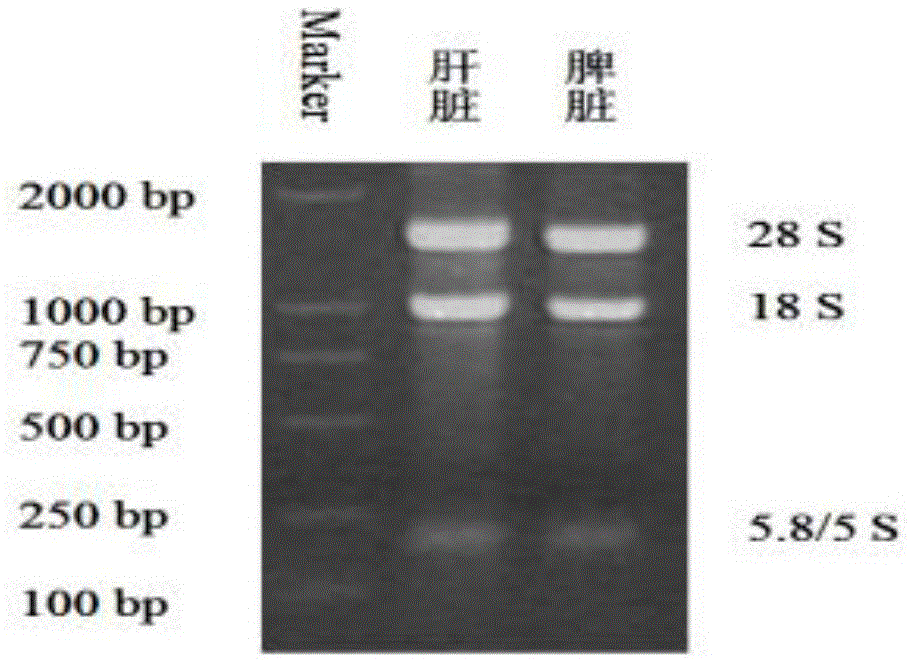
图1为本发明实施例1中大黄鱼肝脏和脾脏总rna电泳图;
图2为本发明实施例4中大黄鱼清marco基因表达量及对照组。
具体实施方式
下面通过实施例对本发明方案作进一步说明:
实施例1:
大黄鱼清道夫受体基因marco基因,marco基因开放阅读框序列采用同源克隆法与race技术克隆获得,marco基因开放阅读框序列为如seqidno:1所示,具体为:atggagacgtcggtggaccgcaccaacaaccgagtctcgtacacgcagagtaacccgctgttcgacatgtcgctcagcaggactgacctgtacaacttccagcctgacgatctgaagccggcgaggccgagacgacagtggtgtttaaacgtgatcatcgtttacctcgtcctgcagaccggcctgaacgccttcctcatttataaagttttcacgttggactcatcgtcgtcgaccctcggggctcagaagcagacgtccaatcacatgcctcagggaggagaaccgagcggcgatgacaccctccaaactctcgtccgcaacaacagtgaagaaaccaaaaccctgaggggtcagctgtgggcgctggacagccaggtcaagaacctctgtgcagaggagggtcagctgggcaggatgaggtctgacctgaagatgctcaactcaagcgcccgaaacctggaggacaaactgatcaacctcaaacaaggacctccaggtcctccgggaagagacgggctttcaggacagccgggcacacctggagacagaggcctcaaaggtgacatcggtgacgctggccctcaaggactaaagggtgacaacggacaacccggacagtcaggagctccgggtcccagaggaccacctggacctgcaggagccccagggaatcaaggaccaggagctaagggagagaaaggagcacctgggggcccaggccttcctggacccaaaggtgaccccggcaccgccgggcaaaaaggatcttctggatctcaaggtaccactgggctacaaggacagaaagcagattctggtccaccgggacctcaaggtgcattgggacctcctggtgccaaaggagatcaaggtccagctggaccaccaggtgccaaagcagagaggggagaccaggaagcgaatgtgcgtctcgtgccgtctggatcccgaggccgtgtggaggtgaaggtaaacggggcctggggcaccgtgtgtgacgacaactttggcaccccagacggcaaggtgatctgcaggatgctgggcttccagaccgctactgacaccttcactgcccccccaggcactggaaagatctggctggatgatctgaaatgtacaggagcagagttggatatcatggactgcccacatcctggagtcggcgtcaacaactgccaacacagcgaggacgccggagtgcagtgcgcctag。该marco基因放阅读框序列全长为1218bp,编码405个氨基酸。
marco基因克隆包括如下步骤:
1)总rna提取及检测
a)取30mg的组织样品于1.5ml的离心管中;
b)在离心管中加入200μltrizolregent;
c)用电研磨棒进行快速充分研磨后加入800μltrizolregent;
d)用移液枪反复吹吸沉淀,使其重悬,室温放置5min;
e)加入200μl氯仿,盖紧离心管,用手震荡剧烈混匀15s,室温放置10min;
f)在4℃环境下,12000×g离心15min,使溶液分为上、中、下三层;
g)小心吸取上层水相溶液至另一离心管中,加入500μl异丙醇,轻轻混匀;
h)将混合后的溶液置于-20℃环境下30min;
i)在4℃环境下,12000×g离心10min;
j)弃去溶液,加入750μl4℃预冷的75%乙醇进行洗涤;
k)在4℃环境下,12000×g离心10min;
l)重复步骤10和11;
m)弃溶液后短暂离心,吸尽残余液体,置室温中数分钟,彻底晾干;
n)向上述rna沉淀中加入30μlrnasefreeddh2o,轻微混匀使其溶解。
将获得的总rna以1.5%非变形琼脂糖凝胶电泳检测,并检测其浓度及a260/a280值,电泳图如图1所示,显示为3条带:28srrna、18srrna、5.8srrna,证明rna提取较完整,其a260/a280值符合要求,可以进行后续实验;
2)cdna第一条链的合成
对所提取的rna进行反转录,获得相应的cdna第一链,反转反应体系为:5.0μl模板rna、1.0μloligo(dt),混匀离心后置于pcr仪上,扩增条件为70℃10min后0℃10min,取出短暂离心后,按下述体系加入:6.0μl模板/引物混合液(上步产物)、2.0μl5×m-mlvbuffer、0.5μldntpmixture(10mm)、0.25μlrnaseinhibitor(40μ/μl)、0.25μlratasem-mlv(200μ/μl)、1.0μlrnasefreeddh2o,混匀离心后置于pcr仪上40℃1h,70℃15min,0℃5min,即可获得cdna第一链,同时反转3份,完成后置于-80℃超低温冰箱保存;
3)marco基因扩增与纯化
根据大黄鱼基因组数据库,通过primer5.0软件设计扩增完整清道夫受体家族基因orf的引物,以cdna为模板,克隆marco基因,反应完成后pcr产物通过1.2%的琼脂糖凝胶进行电泳检验,以dl2000dnamarker作为标准的分子量标记,经pcr反应获得的dna溶液用琼脂糖凝胶回收试剂盒(tiangen,china)进行纯化,具体步骤如下:
a)柱平衡:向吸附柱ca2(吸附柱放入收集管中)中,加入500μl平衡液bl,12000rpm离心1min,倒掉收集管中的废液,将吸附柱重新放回收集管中;
b)将单一的目的dna条带从琼脂糖凝胶中切下(尽量切除多余部分),放入干净的离心管中,称取重量;
c)向胶中加入3倍体积(0.1g视为100μl)溶胶液pn,50℃水浴放置约10min,其间不断温和地上下翻转离心管,以确保胶块充分溶解;
d)将上步所得溶液加入吸附柱ca2中,室温放置2min,12000rpm离心1min。超过800μl可分次加入,倒去收集管中的废液,将吸附柱ca2放入收集管中;
e)加入600μl漂白液pw,12000rpm离心1min,倒掉废液,将吸附柱ca2放入收集管中;
f)重复步骤5;
g)将吸附柱放回管中,12000rpm离心2min,尽量除尽漂洗液,将吸附柱ca2置于室温放置数分钟,彻底晾干,以防止残留的漂洗液影响下一步的实验;
h)将吸附柱放到一个干净的离心管中,向吸附膜中间位置悬空滴加30μl洗脱缓冲液eb,室温放置2min
i)12000rpm离心2min,收集dna溶液,置于-20℃低温冰箱保存;
纯化完成后pcr产物通过1.2%的琼脂糖凝胶进行电泳检验,以dl2000dnamarker作为标准的分子量标记,应与纯化前产物的分子量相当;;
4)t-a克隆
将纯化后的产物进行t-a克隆,首先利用连接反应试剂盒takarapmd18-tvector(takara,japan)进行重组载体的构建,连接体系(总体积10μl)为:5.0μlsolutioni、4.2μlpcr产物、0.8μltakarapmd18-tvector,在冰上按体系中顺序逐一加入各物质,轻轻混匀后16℃连接过夜,连接完成后进行热激转化,具体步骤为:
a)取感受态细胞dh5α(tiangen,china),冰下融解5min,其间将100μl的枪头在冰箱里冰冻(-20℃)预冷,最后将100μldh5α加入10μl连接产物中;
b)打开水浴锅,42℃热激90s,然后迅速置于冰上静置3min;
c)将pcr管中的液体(连接产物+dh5α)加入不含氨苄青霉素(amp-)的lb液体培养基中,然后在37℃以180rpm振荡培养1-2h;
d)在培养过程中,将40μl(20mg/ml)x-gal和7μl(200mg/ml)iptg均匀涂布在amp+lb固体平板上,使其充分吸收;
e)震荡培养结束后,将菌液以4000rpm离心5min,去除大部分上清液,吸取130μl菌液于步骤4准备好的amp+lb固体平板上,均匀涂布,并标记;
f)置于37℃培养过夜
(以上所有操作在超净工作台中进行)
将平板放于37℃恒温培养箱中培养过夜后即可出现菌落,培养后的平板再置于4℃下1h,用无菌牙签在每个平板中挑取白色单菌落(具体数量根据平板上实际菌落确定),置于装有800μlamp+的lb液体培养基的ep管中,编号,然后在37℃摇床以180rpm振荡培养约6h。以18t质粒载体通用引物m13r:5'-cgccagggttttcccagtcacgac-3'和m13f:5'-agcggataacaatttcacacagga-3'作为pcr反应的引物进行菌液pcr扩增,10μl反应体系为:5.0μlextaq(takara、1.0μl菌液、0.3μlm13f、0.3μlm13r、3.4μlddh2o,混匀离心后置于pcr仪上。扩增条件为95℃预变性4min;94℃变性30s,56℃退火30s,72℃延伸2min,循环35次;最后72℃延伸7min。反应完成后以dl2000dnamarker作为标准的分子量标记,1.2%琼脂糖凝胶电泳检测pcr产物,将含有合适片段大小的重组子送上海英潍捷基生物公司进行dna序列测序。
上述总rna提取采用trizolregent、磷酸胍和硫脲进行提取,trizolregent中含有0.03%磷酸胍和0.01%硫脲。trizolregent、磷酸胍和硫脲能够发挥增益作用,一方面可迅速渗入组织,灭活内源rna酶,不会引起rna的降解,便于rna的后续提取,并且具有极强的裂解能力,可在短时间内裂解细胞和组织样本,能够使细胞释放出的蛋白质迅速发生变性并抑制细胞释放出的rna酶活性,有效抑制样本中rna的降解,保持rna的完整性;另一方面协助变性的蛋白质等物质溶解于后续加入的氯仿,使得rna能快速分布在上层水相中,提高总rna的得率和纯度。
上述基因扩增用引物为:
marco–f:5'-atggagacgtaggtggagggcacc-3';
marco–r:5'-ctaggagccctccagtgccgg-3'。
上述扩增反应体系为:2.5μl10×pcrbuffer、0.4μldntps、0.8μlmarco-f、0.8μlmarco-r、0.6μltemplatecdna、0.4μltaqdnapolymerase(takara)、14.5μlrnasefreeddh2o;扩增条件为:95℃预变性4min;94℃变性30s,55-65℃退火30s,72℃延伸2min,循环35次;最后72℃延伸10min。
上述大黄鱼清道夫受体基因marco基因的用途,marco基因在大黄鱼免疫防御功能中的用途。
实施例2:
大黄鱼清道夫受体基因marco基因,marco基因采用同源克隆法与race技术克隆获得,所述marco基因cdna序列全长8275bp。
marco基因克隆包括如下步骤:
1)总rna提取及检测;
2)cdna第一条链的合成;
3)marco基因扩增与纯化;
4)t-a克隆。
总rna提取采用trizolregent、磷酸胍和硫脲进行提取,trizolregent中含有0.035%磷酸胍和0.015%硫脲。
基因扩增用引物为:
marco–f:5'-atggagacgtaggtggagggcacc-3';
marco–r:5'-ctaggagccctccagtgccgg-3'。
扩增反应体系为:2.5μl10×pcrbuffer、0.4μldntps、0.8μlmarco-f、0.8μlmarco-r、0.6μltemplatecdna、0.4μltaqdnapolymerase(takara)、14.5μlrnasefreeddh2o,扩增条件为:95℃预变性4min;94℃变性30s,55-65℃退火30s,72℃延伸2min,循环35次;最后72℃延伸10min。
上述大黄鱼清道夫受体基因marco基因的用途,marco基因在大黄鱼免疫防御功能中的用途。
实施例3:
大黄鱼清道夫受体基因marco基因,marco基因采用同源克隆法与race技术克隆获得,所述marco基因cdna序列全长8275bp。
marco基因克隆包括如下步骤:
1)总rna提取及检测;
2)cdna第一条链的合成;
3)marco基因扩增与纯化;
4)t-a克隆。
总rna提取采用trizolregent、磷酸胍和硫脲进行提取,trizolregent中含有0.04%磷酸胍和0.02%硫脲。
基因扩增用引物为:
marco–f:5'-atggagacgtaggtggagggcacc-3';
marco–r:5'-ctaggagccctccagtgccgg-3'。
扩增反应体系为:2.5μl10×pcrbuffer、0.4μldntps、0.8μlmarco-f、0.8μlmarco-r、0.6μltemplatecdna、0.4μltaqdnapolymerase(takara)、14.5μlrnasefreeddh2o,扩增条件为:95℃预变性4min;94℃变性30s,55-65℃退火30s,72℃延伸2min,循环35次;最后72℃延伸10min。
上述大黄鱼清道夫受体基因marco基因的用途,marco基因在大黄鱼免疫防御功能中的用途。
实施例4:
大黄鱼清道夫受体基因marco基因的免疫防御功能
实验大黄鱼(体长20-30cm,体重350-400g)取自浙江舟山东极养殖场,于25℃洁净海水中暂养1周,每天换新鲜海水。随后将大黄鱼随机分为2组,每组30条,其中实验组腹腔注射100μlpbs重悬的鳗弧菌菌液(ph7.4,1×108cfu/ml),对照组注射100μlpbs(ph7.4)。收集注射后0h、2h、6h、12h、24h、48h、72h的肝脏组织提取总rna。大黄鱼清道夫受体家族各基因mrna在感染溶藻弧菌后0、6、12、24、48和72h的表达量与对照组的结果如图2。marco基因均在24-72h有极高表达量,且在24h时表达量最高。
本发明操作步骤中的常规操作为本领域技术人员所熟知,在此不进行赘述。
以上所述的实施例对本发明的技术方案进行了详细说明,应理解的是以上所述仅为本发明的具体实施例,并不用于限制本发明,凡在本发明的原则范围内所做的任何修改、补充或类似方式替代等,均应包含在本发明的保护范围之内。
序列表
<110>浙江海洋大学
<120>大黄鱼清道夫受体基因marco基因及其免疫防御功能
<160>2
<170>siposequencelisting1.0
<210>1
<211>1218
<212>dna
<213>大黄鱼(larimichthyscrocea)
<400>1
atggagacgtcggtggaccgcaccaacaaccgagtctcgtacacgcagagtaacccgctg60
ttcgacatgtcgctcagcaggactgacctgtacaacttccagcctgacgatctgaagccg120
gcgaggccgagacgacagtggtgtttaaacgtgatcatcgtttacctcgtcctgcagacc180
ggcctgaacgccttcctcatttataaagttttcacgttggactcatcgtcgtcgaccctc240
ggggctcagaagcagacgtccaatcacatgcctcagggaggagaaccgagcggcgatgac300
accctccaaactctcgtccgcaacaacagtgaagaaaccaaaaccctgaggggtcagctg360
tgggcgctggacagccaggtcaagaacctctgtgcagaggagggtcagctgggcaggatg420
aggtctgacctgaagatgctcaactcaagcgcccgaaacctggaggacaaactgatcaac480
ctcaaacaaggacctccaggtcctccgggaagagacgggctttcaggacagccgggcaca540
cctggagacagaggcctcaaaggtgacatcggtgacgctggccctcaaggactaaagggt600
gacaacggacaacccggacagtcaggagctccgggtcccagaggaccacctggacctgca660
ggagccccagggaatcaaggaccaggagctaagggagagaaaggagcacctgggggccca720
ggccttcctggacccaaaggtgaccccggcaccgccgggcaaaaaggatcttctggatct780
caaggtaccactgggctacaaggacagaaagcagattctggtccaccgggacctcaaggt840
gcattgggacctcctggtgccaaaggagatcaaggtccagctggaccaccaggtgccaaa900
gcagagaggggagaccaggaagcgaatgtgcgtctcgtgccgtctggatcccgaggccgt960
gtggaggtgaaggtaaacggggcctggggcaccgtgtgtgacgacaactttggcacccca1020
gacggcaaggtgatctgcaggatgctgggcttccagaccgctactgacaccttcactgcc1080
cccccaggcactggaaagatctggctggatgatctgaaatgtacaggagcagagttggat1140
atcatggactgcccacatcctggagtcggcgtcaacaactgccaacacagcgaggacgcc1200
ggagtgcagtgcgcctag
<210>2
<211>24
<212>dna
<213>引物(artificialsequence)
<400>2
atggagacgtaggtggagggcacc24
<210>3
<211>24
<212>dna
<213>引物(artificialsequence)
<400>3
atggagacgtaggtggagggcacc24
- 还没有人留言评论。精彩留言会获得点赞!