一种(E)-1,2-二硫氰酸乙烯酯化合物的合成方法与流程
本发明涉及一种(e)-1,2-二硫氰酸乙烯酯化合物的合成方法,特别涉及一种室温及搅拌条件下,炔烃、硫氰酸盐和过硫酸氢钾复合盐在二氯甲烷溶液中一锅反应,高选择性合成(e)-1,2-二硫氰酸乙烯酯化合物,属于有机中间体合成技术领域。
背景技术:
含硫氰酸酯的化合物在药物研发[chem.res.toxicol.,2014,27,51;pharm.chem.j.,2013,47,422;j.med.chem.,2002,45,3984;chem.res.toxicol.,2014,27,51],有机合成([org.lett.,2011,13,454;tetrahedronlett.,1997,38,65]等领域发挥着重要的作用。
硫氰酸烷基酯的研究已经取代较好进展,但是(e)-1,2-二硫氰酸乙烯酯化合物的合成方法目前文献报道的仅有一例。
2001年,robertm.moriarty报道了0-5℃低温搅拌条件下,硫氰酸铅与二氯化碘代苯原位生成二硫氰酸化碘代苯与炔烃反应生成(e)-1,2-二硫氰酸乙烯酯化合物,反应中间体为碘嗡离子。(o.prakash,v.sharma,h.batraandr.m.moriarty,tetrahedronlett.,2001,42,553.),式1。
该方法存在以下不足:
1)该方法使用的化学当量的金属铅试剂,二氯化碘代苯(cas:932-72-9),两种试剂都是剧毒,价格昂贵,不仅增加反应成本,还污染环境。
2)需低温条件反应,增加反应成本。
技术实现要素:
为了克服现有技术中(e)-1,2-二硫氰酸乙烯酯化合物合成方法存在的不足,本发明的目的旨在提供一种反应产率高,成本低,反应条件温和、环境友好型的(e)-1,2-二硫氰酸乙烯酯化合物的合成方法。
为了实现上述技术目的,本发明提供了一种(e)-1,2-二硫氰酸乙烯酯化合物的合成方法,该方法是在室温及搅拌条件下,炔烃、硫氰酸盐和过硫酸盐在二氯甲烷溶液体系中一锅反应,生成(e)-1,2-二硫氰酸乙烯酯化合物;
所述炔烃具有式1结构:
所述(e)-1,2-二硫氰酸乙烯酯化合物具有式2结构:
其中,
r1为芳基、杂芳环基、烷基、环烷基、卤素取代基、含羟基取代基的烷基或含羧基取代基的烷基;
r2为氢、烷基或酯基。
本发明的炔烃两端的取代基团选择最好是选择不同的取代基团。r1选择芳基时,芳基选自苯基或取代苯基;取代苯基的苯环上至少包含c1~c6烷基(可以为直链烷基或带支链的烷基)、c1~c6烷氧基、卤素(如氟、氯、溴或碘)中一种取代基;取代苯基的苯环上最好是包含一个取代基。取代基在苯环上的位置不限。r1选择杂芳环基时,杂芳基选自五元或六元的含氧、硫、氮原子中至少一种杂原子的芳香性杂环基团,如噻吩、呋喃、吡啶等;r1为烷基时,所述烷基选自c1~c12的烷基,如甲基、乙基、辛基等;r1为环烷基时,所述烷基选自c3~c12的环烷基,如环丙基、环己基、环辛基等;r1为卤素取代基时,所述卤素取代基为氟、氯、溴或碘等;r1为含羟基取代基的烷基时,所述含羟基取代基的烷基碳原子数为c1~c6;具体如2-羟基乙基、5-羟基戊基、2-羟基丙基等;r1为含羧基取代基的烷基时,所述含羧基取代基的烷基碳原子数为c1~c6;如5-羧基戊基、2-羧基乙基等。
本发明的r2为烷基时,所述烷基为c1~c5的烷基,如甲基、乙基、丙基等。r2为酯基时,所述酯基为甲酯基(即甲氧酰基)、乙酯基、异丙酯基、丁酯基。
优选的方案,硫氰酸盐作为硫氰酸源,理论上只要氧化生成硫氰酸自由基的硫氰酸盐均适应本发明,优选为硫氰酸钠、硫氰酸钾、亚硫酸铵中至少一种;最优选为亚硫酸钠。
优选的方案,过硫酸盐作为氧化剂,优选为过硫酸钠、过硫酸钾、过硫酸铵过硫酸氢钾中至少一种;最优选为过硫酸氢钾。
优选的方案,炔烃、硫氰酸盐和过硫酸氢钾复合盐的摩尔比为1:2~2.5:1~1.5。。较优选为1:2.2:1.1。
优选的方案,所述一锅反应的条件为:室温搅拌反应1~3h。最优选为反应2h。
本领公知,硫氰酸铅是一种环境污染大、使用成本高的含铅试剂。而在本发明使用的硫氰酸钠具有成本低,稳定,环境副作用小等优势。
本发明以炔烃作为底物原料,廉价易得的硫氰酸钠等作为硫氰酸源,过硫酸盐作为氧化剂,二氯甲烷作为溶剂,在室温搅拌作用下进行炔烃双官能化反应合成(e)-1,2-二硫氰酸乙烯酯化合物,反应路线如下:
本发明的反应是自由基反应机理,具体反应的机理如下:以硫氰酸钠为原料为例进行说明:
硫氰酸钠在氧化剂过硫酸盐作用下生成硫氰酸自由基(a),一分子硫氰酸自由基先进攻炔烃,生成中间体自由基(b),中间体自由基(b)再与一分子硫氰酸自由基(a)结合,生成目标产物。
相对现有技术,本发明的技术方案带来的有益技术效果:
1)本发明采用硫氰酸钠替换硫氰酸铅作为硫氰酸源,硫氰酸钠原料来源丰富易得,价格远低于相应的硫氰酸源;
2)本发明通过过硫酸盐氧化硫氰酸钠生成硫氰酸自由基,与炔烃发生自由基加成反应,避免了使用的有毒,不稳定的二氯化碘代苯。
3)本发明可以高选择性获得(e)-1,2-二硫氰酸乙烯酯化合物,且产物收率高。
附图说明
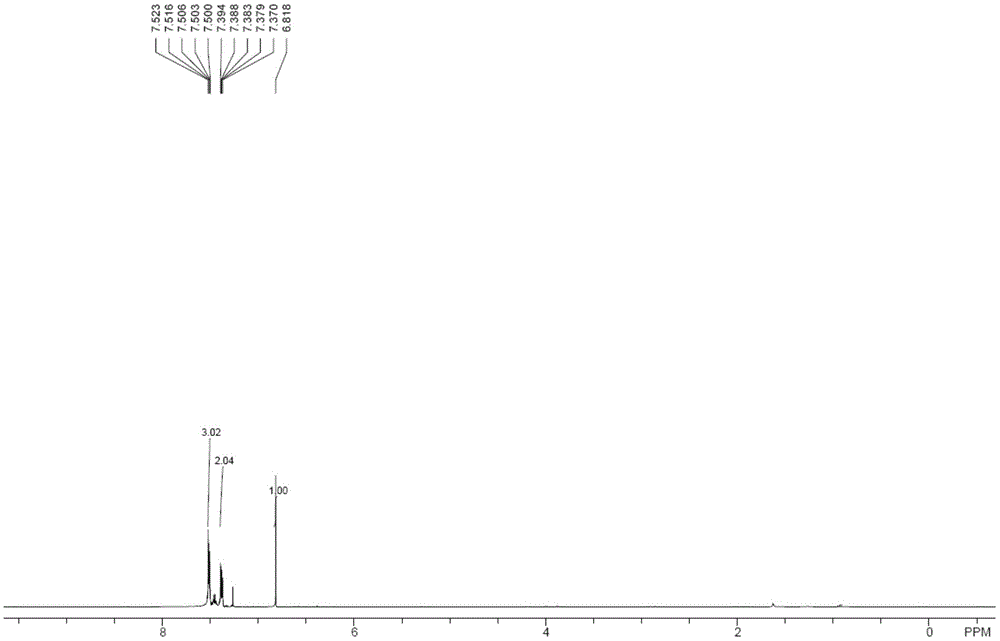
图1为实施例1的(e)-1,2-二硫氰酸乙烯基苯酯核磁氢谱图;
图2为实施例1的(e)-1,2-二硫氰酸乙烯基苯酯核磁碳谱图;
图3为实施例6的(e)-1,2-二硫氰酸乙烯基环己酯核磁氢谱图;
图4为实施例6的(e)-1,2-二硫氰酸乙烯基环己酯核磁碳谱图。
具体实施方式
以下具体实施例旨在进一步说明本发明内容,而不是限制本发明权利要求的保护范围。
实施例1
(e)-1,2-二硫氰酸乙烯基苯酯;(e)-(1,2-dithiocyanatovinyl)benzene:
在50ml圆底烧瓶中,依次加入苯乙炔1.02g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品1.85g,产率85%。
核磁数据:
1hnmr(400mhz,cdcl3)δ7.52–7.50(m,3h),7.39–7.37(m,2h),6.82(s,1h).13cnmr(100mhz,cdcl3)δ131.6,131.3,129.6,129.1,128.5,117.0,108.6,107.8.
对照实验组1:
以硫氰酸钾替代硫氰酸钠:
在50ml圆底烧瓶中,依次加入苯乙炔1.02g,硫氰酸钾2.14g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,液相色谱面积归一化法计算(e)-1,2-二硫氰酸乙烯基苯酯产率为32%。
对照实验组2:
以硫氰酸铵替代硫氰酸钠:
在50ml圆底烧瓶中,依次加入苯乙炔1.02g,硫氰酸铵1.67g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,液相色谱面积归一化法计算(e)-1,2-二硫氰酸乙烯基苯酯产率为26%。
对照实验组3:
以2化学当量的硫氰酸钠替代2.2化学当量的硫氰酸钠:
在50ml圆底烧瓶中,依次加入苯乙炔1.02g,硫氰酸钠1.62g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,液相色谱面积归一化法计算(e)-1,2-二硫氰酸乙烯基苯酯产率为72%。
对照实验组4:
以过硫酸钾代替过硫酸氢钾复合盐
在50ml圆底烧瓶中,依次加入苯乙炔1.02g,硫氰酸钠1.62g,过硫酸钾2.98g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,液相色谱面积归一化法计算(e)-1,2-二硫氰酸乙烯基苯酯产率为32%。
对照实验组5:
以过硫酸钠代替过硫酸氢钾复合盐
在50ml圆底烧瓶中,依次加入苯乙炔1.02g,硫氰酸钠1.62g,过硫酸钠2.62g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,液相色谱面积归一化法计算(e)-1,2-二硫氰酸乙烯基苯酯产率为7%。
对照实验组6:
过硫酸铵代替过过硫酸氢钾复合盐
在50ml圆底烧瓶中,依次加入苯乙炔1.02g,硫氰酸钠1.62g,过硫酸铵2.51g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,液相色谱面积归一化法计算(e)-1,2-二硫氰酸乙烯基苯酯产率为26%。
对照实验组7:
以1.0倍化学当量的过硫酸氢钾复合盐代替1.1倍化学当量的过硫酸氢钾复合盐
在50ml圆底烧瓶中,依次加入苯乙炔1.02g,硫氰酸钠1.62g,过硫酸氢钾复合盐1.39g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,液相色谱面积归一化法计算(e)-1,2-二硫氰酸乙烯基苯酯产率为68%。
对照实验组9:
以二氯乙烷作为反应介质代替二氯甲烷
在50ml圆底烧瓶中,依次加入苯乙炔1.02g,硫氰酸钠1.62g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,液相色谱面积归一化法计算(e)-1,2-二硫氰酸乙烯基苯酯产物产率为32%。
对照实验组10:
以乙酸乙酯作为反应介质代替二氯甲烷
在50ml圆底烧瓶中,依次加入苯乙炔1.02g,硫氰酸钠1.62g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。薄层层析分析没有(e)-1,2-二硫氰酸乙烯基苯酯产物生成。
实施例2
(e)-1,2-二硫氰酸乙烯基-4-甲基苯酯;
(e)-1-(1,2-dithiocyanatovinyl)-4-methylbenzene:
在50ml圆底烧瓶中,依次加入对甲基苯乙炔1.17g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品1.88g,产率81%。
核磁数据:
1hnmr(400mhz,cdcl3)δ7.34–7.28(m,4h),6.78(s,1h),2.43(s,3h).
13cnmr(100mhz,cdcl3)δ141.8,131.5,130.2,128.6,128.4,116.1,108.7,108.0,21.4.
实施例3
(e)-1,2-二硫氰酸乙烯基-4-甲氧基苯酯;
(e)-1-(1,2-dithiocyanatovinyl)-4-methoxybenzene:
在50ml圆底烧瓶中,依次加入对甲氧基苯乙炔1.32g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品1.94g,产率78%。
核磁数据:
1hnmr(400mhz,cdcl3)δ7.33(d,j=8.8hz,2h),7.00(d,j=8.8hz,2h),6.72(s,1h),3.86(s,3h).
13cnmr(100mhz,cdcl3)δ161.7,131.6,130.2,123.5,115.4,114.9,108.9,108.1,55.4
实施例4
(e)-1,2-二硫氰酸乙烯基-4-溴苯酯;
(e)-1-bromo-4-(1,2-dithiocyanatovinyl)benzene:
在50ml圆底烧瓶中,依次加入4-溴基苯乙炔1.80g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品2.29g,产率77%。
核磁数据:
1hnmr(400mhz,cdcl3)δ7.74(d,j=8.4hz,1h),7.35(d,j=8.4hz,1h),6.94(s,1h).
13cnmr(100mhz,cdcl3)δ132.9,130.5,130.2,130.0,125.9,118.3,108.1,107.5.
实施例5
(e)-3-(1,2-二硫氰酸乙烯基)噻吩酯;(e)-3-(1,2-dithiocyanatovinyl)thiophene:
在50ml圆底烧瓶中,依次加入3-乙炔噻吩1.08g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品1.92g,产率86%。
核磁数据:
1hnmr(400mhz,cdcl3)δ7.58–7.57(m,1h),7.52–7.50(m,1h),7.23–7.22(m,1h),6.79(s,1h).
13cnmr(100mhz,cdcl3)δ128.6,128.4,127.2,126.6,125.9,117.2,108.5,108.0
实施例6
(e)-1,2-二硫氰酸乙烯基环己酯;(e)-(1,2-dithiocyanatovinyl)cyclohexane:
在50ml圆底烧瓶中,依次加入1-乙炔基-环己烷1.06g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品1.68g,产率75%。
核磁数据:
1hnmr(400mhz,cdcl3)δ6.50(s,1h),2.79–2.73(m,1h),1.88–1.84(m,2h),1.74–1.70(m,2h),1.47–1.21(m,6h).
13cnmr(100mhz,cdcl3)δ140.8,112.7,109.0,108.5,42.6,30.5,25.6,25.1.
实施例7
(e)-1,2-二硫氰酸乙烯基辛酯;(e)-1,2-dithiocyanatooct-1-ene:
在50ml圆底烧瓶中,依次加入辛炔1.10g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品1.90g,产率84%。
核磁数据:
1hnmr(400mhz,cdcl3)δ6.50(s,1h),2.79–2.73(m,1h),1.88–1.84(m,2h),1.74–1.70(m,2h),1.47–1.21(m,6h).
13cnmr(100mhz,cdcl3)δ140.8,112.7,109.0,108.5,42.6,30.5,25.6,25.1.
实施例8
(e)-4-溴-1,2-二硫氰酸丁酯-1-烯;(e)-4-bromo-1,2-dithiocyanatobut-1-ene:
在50ml圆底烧瓶中,依次加入4-溴正丁炔1.33g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品1.94g,产率78%。
核磁数据:
1hnmr(400mhz,cdcl3)δ6.82(s,1h),3.65(t,j=6.4hz,2h),3.16(t,j=6.4hz,2h).13cnmr(100mhz,cdcl3)δ131.7,121.5,107.8,107.2,35.3,28.1
实施例9
(e)-3,4-二硫氰酸酯基-4-烯-1-醇;(e)-3,4-dithiocyanatobut-3-en-1-ol:
在50ml圆底烧瓶中,依次加入3-丁炔-1-醇0.7g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品1.37g,产率74%。
核磁数据:
1hnmr(400mhz,cdcl3)δ6.01(s,1h),3.91(t,j=5.6hz,2h),2.81(t,j=5.6hz,2h).13cnmr(100mhz,cdcl3)δ132.1,118.9,109.0,107.9,59.6,35.9.
实施例10
(e)-6,7-二硫氰酸-6-庚烯酯;(e)-6,7-dithiocyanatohept-6-enoicacid:
在50ml圆底烧瓶中,依次加入6-庚炔酸1.26g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品1.69g,产率70%。
核磁数据:
1hnmr(400mhz,cdcl3)δ6.54(s,1h),2.57(t,j=6.8hz,2h),2.43(t,j=6.8hz,2h),1.71–1.68(m,4h).13cnmr(100mhz,cdcl3)δ178.3,135.8,115.3,108.0,107.5,33.2,32.7,26.6,23.6
实施例11
(e)-2,3-二硫氰酸辛-2-烯酯;(e)-2,3-dithiocyanatooct-2-ene:
在50ml圆底烧瓶中,依次加入2-辛炔1.10g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品1.97g,产率87%。
核磁数据:
1hnmr(400mhz,cdcl3)δ2.67(t,j=7.6hz,2h),2.44(s,3h),1.67–1.59(m,2h),1.38–1.32(m,4h),0.95–0.91(m,2h).
13cnmr(100mhz,cdcl3)δ130.0,125.9,108.2,108.1,35.9,30.9,27.5,22.7,22.3,13.8.
实施例12
(e)-乙基-3-苯基-2,3-二硫氰酸乙烯基羧酸乙酯
(e)-ethyl3-phenyl-2,3-dithiocyanatoacrylate:
在50ml圆底烧瓶中,依次加入苯丙酸乙酯1.78g,硫氰酸钠1.79g,过硫酸氢钾复合盐1.85g,15ml二氯甲烷,室温条件下搅拌反应2小时。过滤,减压除去溶剂,硅胶柱层析分离的目标产品2.20g,产率76%。
核磁数据:
1hnmr(400mhz,cdcl3)δ7.53–7.49(m,3h),7.22–7.19(m,2h),4.40(q,j=7.2hz,2h),1.40(t,j=7.2hz,3h).13cnmr(100mhz,cdcl3)δ163.3,159.0,136.0,131.3,129.5,127.3,113.0,108.7,108.6,64.2,13.9。
- 还没有人留言评论。精彩留言会获得点赞!