一种快速的基于取代环丁醇氧化开环/环化反应制备萘满酮衍生物的方法与流程
本发明涉及一种萘满酮衍生物的合成方法,特别涉及一种基于取代环丁醇氧化开环/环化反应合成萘满酮衍生物的方法,属于医药中间体合成、精细有机合成领域。
背景技术:
萘满酮衍生物是重要的有机化合物之一,它广泛存在于生物活性分子(如下分子结构式)、有机合成中间体中。然而合成萘满酮衍生物的方法还极为有限,最主要的传统方法是haworth反应。该方法需要经过多步反应,需要使用到大量的路易斯酸、质子酸及还原剂,且对底物的官能团容忍性差,总产率低[(a)c.o.kangani,b.w.day,org.lett.2008,10,2645;(b)s.arai,y.sudo,a.nishida,tetrahedron2005,61,4639;(c)d.-m.cui,m.kawamura,s.shimada,t.hayashi,m.tanaka,tetrahedronlett.2003,44,4007;(d)t.yamato,c.hideshima,g.k.s.prakash,g.a.olah,j.org.chem.1991,56,3955;(e)a.silveira,e.j.mcwhorter,j.org.chem.1972,37,3687;(f)r.d.haworth,j.chem.soc.1932,1125.]。最近,有人报道了以苯乙烯为原料,光催化合成4-芳基萘满酮衍生物的方法,该方法仅限于合成4-芳基取代的产物,且产率不理想[k.wang,l.-g.meng,q.zhang,l.wang,green.chem.2016,18,2864]。另外,还有人报道了银催化的取代环丁醇开环/环化反应制备萘满酮衍生物的方法,该方法需要使用到贵金属银盐做催化剂,且产率不高[j.yu,h.zhao,s.liang,x.bao,c.zhu,org.biomol.chem.2015,13,7924]。以上三种方法均需要较长的反应时间,一般大于7小时。因此,开发一种操作简单、反应快速的合成萘满酮衍生物的新方法具有重要的理论意义和应用价值。
技术实现要素:
针对现有的合成萘满酮衍生物的方法存在的不足,如路易斯酸或质子酸的大量消耗,对环境影响大,反应步骤多,需要使用贵金属催化剂,反应时间长等问题,本发明的目的是在于提供一种基于取代环丁醇氧化开环/环化反应制备萘满酮衍生物的方法,该方法具有反应快速(30秒内完成反应),操作简单(敞口反应),反应条件温和、一步反应、不需使用贵金属催化、产率较高、可扩量反应等优点。因此,该方法在萘满酮衍生物的合成应用领域具有很好的应用前景。
为了实现上述技术目的,本发明提供了一种基于取代环丁醇氧化开环/环化反应制备萘满酮衍生物的方法,该方法是:在0-100℃,敞口条件下,式1取代环丁醇和硝酸铈铵一锅反应,得到式2萘满酮衍生物;
其中,
ar选自苯、稠环芳烃、噻吩、或苯并噻吩;
r1和r2独立选自氢或其他取代基。
优选的方案,式1芳烃取代环丁醇为1-(1-萘基)环丁-1-醇、1-(2-萘基)环丁-1-醇、1-(4-甲基萘-1-基)环丁-1-醇、1-(4-甲氧基萘-1-基)环丁-1-醇、1-(6-甲氧基萘-2-基)环丁-1-醇、1-(9-菲基)环丁-1-醇、1-(5-苊基)环丁-1-醇、1-(2-三氟甲基苯基)环丁-1-醇、1-(4-三氟甲基苯基)环丁-1-醇、1-(2,5-二三氟甲基苯基)环丁-1-醇、1-(噻吩-2-基)环丁-1-醇、1-(5-甲基噻吩-2-基)环丁-1-醇、1-(4-辛基噻吩-2-基)环丁-1-醇、1-(苯并噻吩-2-基)环丁-1-醇、1-(4-溴苯并噻吩-2-基)环丁-1-醇、1-(5-氯苯并噻吩-2-基)环丁-1-醇。
优选的方案,所述芳烃取代环丁醇通过氧化开环/环化反应后转化成式2萘满酮衍生物,这些萘满酮衍生物为2,3-二氢-4(1h)-菲酮、3,4-二氢-1(2h)-菲酮、3,4-二氢-1(2h)-蒽酮、9-甲基-2,3-二氢-4(1h)-菲酮、9-甲氧基-2,3-二氢-4(1h)-菲酮、7-甲氧基-3,4-二氢-1(2h)-菲酮、6-甲氧基-3,4-二氢-1(2h)-蒽酮、3,4-二氢-1(2h)-苯并菲酮、4,5,8,9-四氢-10(7h)苯并苊酮、8-三氟甲基-3,4-二氢-1(2h)-萘酮、6-三氟甲基-3,4-二氢-1(2h)-萘酮、5,8-二三氟甲基-3,4-二氢-1(2h)-萘酮、5,6-二氢-1-苯并噻吩-7(4h)-酮、2-甲基-5,6-二氢-1-苯并噻吩-7(4h)-酮、3-辛基-5,6-二氢-1-苯并噻吩-7(4h)-酮、9-溴-2,3-二氢二苯并[b,d]噻吩-4(1h)-酮、8-氯-2,3-二氢二苯并[b,d]噻吩-4(1h)-酮。
优选的方案,硝酸铈胺为氧化剂,其用量为2~4当量,时间为30秒~10分钟,反应温度0~100℃。进一步优选的方案,硝酸铈胺用量为2.5~3当量,时间为30秒~60秒,反应温度0~100℃。硝酸铈胺用量过低,反应物转化不完全,硝酸铈胺用量过大,副产物增加。反应时间过短产率降低,而反应时间过长,则副产物增加。在优选的反应时间和温度范围内可以达到最佳的反应效果。
优选的方案,溶剂为水或乙腈或水与乙腈混合物(1:1,体积比),最优选为水与乙腈混合物(1:1,体积比)。
优选的方案,所述硝酸铈胺在水与乙腈混合物(1:1,体积比)中的浓度为0.25~0.3mol/l。进一步优选的方案,硝酸铈胺在水与乙腈混合物(1:1,体积比)中的浓度为0.25mol/l。
优选的方案,所述芳烃取代的环丁醇在水与乙腈混合物(1:1,体积比)中的浓度为0.1~0.2mol/l。进一步优选的方案,芳烃取代的环丁醇在水与乙腈混合物(1:1,体积比)中的浓度为0.1mol/l。
本发明的甲酰胺衍生物合成中反应方程式如下。
基于大量的实验总结以及参考先前文献报道,本发明提出了如下合理的反应机制。首先芳烃取代环丁醇与4价铈发生单电子转移反应,得到氧自由基中间体a;然后a发生碳碳键的均裂,得到碳自由基中间体b。随后,碳自由基与芳环发生自由基加成反应,得到中间体c。中间体c再与4价铈发生单电子转移反应,得到芳构化的目标化合物萘满酮衍生物。
本发明的技术方案中,将所述芳烃取代环丁醇溶于水与乙腈混合溶剂中(1:1,体积比),在空气氛围下放入设定温度的热浴锅中,磁力搅拌下一次性加入所需硝酸铈胺,反应设定的时间后,立即加入饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1~4:1为洗脱剂对粗产物进行柱层析得到纯品。
本发明的萘满酮衍生物的合成方法,包括以下步骤:
称取芳烃取代环丁醇0.2毫摩尔,将其溶于2毫升水与乙腈混合溶剂中(1:1,体积比),在空气氛围下放入设定温度的热浴锅,磁力搅拌下一次性加入硝酸铈胺0.274克(0.5毫摩尔),反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1~4:1为洗脱剂对粗产物进行柱层析得到纯品。
相对现有技术,本发明的技术方案具有以下优点和效果:
1)本发明的技术方案首次以硝酸铈胺为氧化剂,经由芳烃取代环丁醇的开环/闭环反应一步实现了萘满酮衍生物的制备。
2)本发明的技术方案反应快速,仅需要30秒即可完成反应。
3)本发明的技术方案避免使用贵金属催化剂,成本低廉。
4)本发明的技术方案在温和条件下实现了萘满酮衍生物的一步合成,大多数产物的合成在0℃下即可完成,反应对空气及水兼容,具有步骤简单、成本低,操作简单等优点,克服了现有技术如反应试剂毒性大,催化剂昂贵、合成方法成本高昂、反应步骤多,副产物多等缺陷。
附图说明
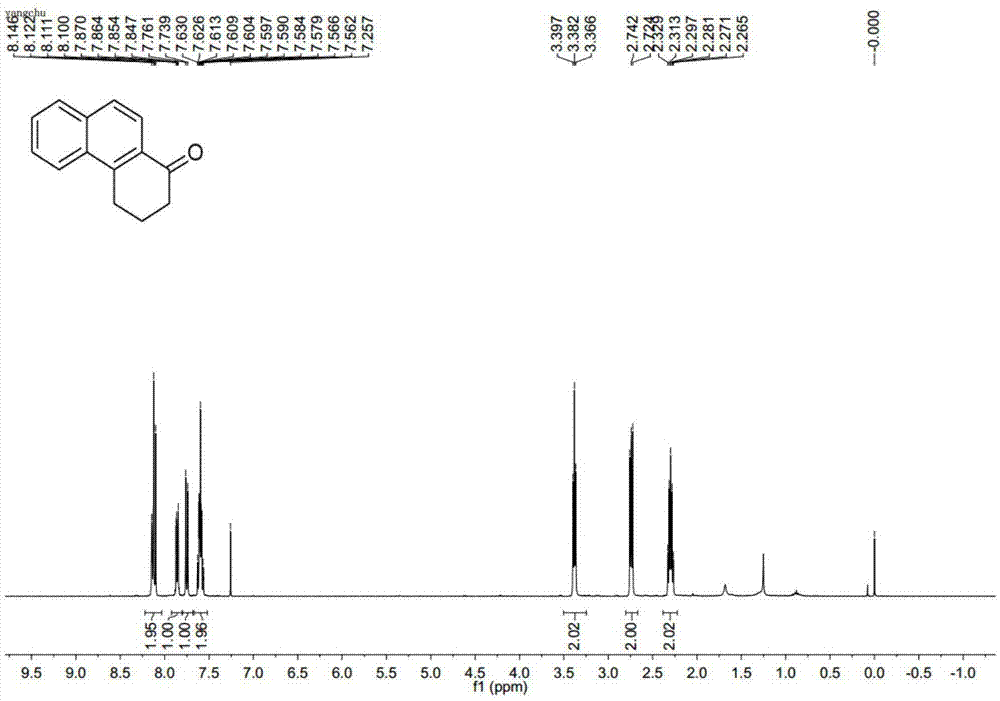
【图1】为实施例1所得产物的1hnmr图;
【图2】为实施例1所得产物的13cnmr图;
【图3】为实施例14所得产物的1hnmr图;
【图4】为实施例14所得产物的13cnmr图。
具体实施方式
结合以下具体实施例和附图,对本发明作进一步的详细说明。实施本发明的过程、条件、试剂、试验方法等,除以下专门提及的内容之外,均为本领域的普遍和公知常识,本发明没有特别限制内容。
实施例1
将1-(1-萘基)环丁-1-醇(39.6mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入0℃的水浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。白色固体,熔点70-72℃,产率70%。1hnmr(400mhz,cdcl3)δ9.41(d,j=8.7hz,1h),7.93(d,j=8.4hz,1h),7.81(d,j=8.0hz,1h),7.65–7.61(m,1h),7.51–7.47(m,1h),7.33(d,j=8.4hz,1h),3.13(t,j=6.1hz,2h),2.79(t,j=6.8hz,2h),2.23–2.17(m,2h);13cnmr(100mhz,cdcl3)δ200.6,146.9,134.3,132.9,131.5,128.9,128.4,127.4,127.1,126.8,125.9,41.2,31.7,23.1;ir(kbr):3140,2361,1664,1541,1401,1280,1113,889,740cm-1;hrms(esi)m/z[m+nh4]+calcdforc14h16no214.1226,found214.1230.
实施例2
将1-(2-萘基)环丁-1-醇(39.6mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入0℃的水浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。白色固体,熔点92-94℃,产率66%。1hnmr(400mhz,cdcl3)δ8.14–8.10(m,2h),7.87–7.84(m,1h),7.75(d,j=8.7hz,1h),7.63–7.56(m,2h),3.38(t,j=6.1hz,2h),2.74(t,j=6.8hz,2h),2.33–2.27(m,2h);13cnmr(100mhz,cdcl3)δ198.8,143.1,135.8,131.5,130.1,128.9,128.4,127.1,126.8,125.0,122.9,38.5,25.7,22.9;ir(kbr):3140,2365,1687,1654,1401,1109,1415,1326,1295,824,748cm-1;hrms(esi)m/z[m–h]–calcdforc14h11o195.0815,found195.0816.
实施例3
将1-(4-甲基萘-1-基)环丁-1-醇(42.5mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入0℃的水浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色油状物,产率73%。1hnmr(400mhz,cdcl3)δ9.47(d,j=8.6hz,1h),7.98(d,j=8.3hz,1h),7.62(t,j=7.7hz,1h),7.52(t,j=7.6hz,1h),7.18(s,3h),3.07(t,j=6.1hz,2h),2.76(t,j=6.6hz,2h),2.70(s,3h),2.20–2.14(m,2h);13cnmr(100mhz,cdcl3)δ200.3,146.7,141.4,132.1,131.7,128.5,128.1,127.4,126.1,125.8,124.2,41.3,31.7,23.2,20.3;ir(kbr):3184,2363,1668,1511,1401,1593,1213,1120,840,760cm-1;hrms(esi)m/z[m+nh4]+calcdforc15h18no228.1383,found228.1384.
实施例4
将1-(4-甲氧基萘-1-基)环丁-1-醇(45.7mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入0℃的水浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色油状物,产率72%。1hnmr(400mhz,cdcl3)δ9.49(d,j=8.7hz,1h),8.28–8.24(m,1h),7.66–7.61(m,1h),7.49–7.45(m,1h),6.59(s,1h),4.05(s,3h),3.08(t,j=6.1hz,2h),2.74(t,j=6.6hz,2h),2.18–1.12(m,2h);13cnmr(100mhz,cdcl3)δ199.2,159.4,149.3,133.2,129.4,126.8,125.4,125.0,121.9,121.2,104.6,55.9,41.1,32.6,23.1;ir(kbr):3138,2348,1640,1588,1401,1247,1113,769cm-1;hrms(esi)m/z[m+h]+calcdforc15h15o2227.1067,found227.1074.
实施例5
将1-(6-甲氧基萘-2-基)环丁-1-醇(45.7mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入0℃的水浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色固体,熔点94-96℃,产率71%。1hnmr(400mhz,cdcl3)δ8.06(dd,j=18.7,9.0hz,2h),7.64(d,j=8.7hz,1h),7.22(dd,j=9.2,2.6hz,1h),7.15(d,j=2.6hz,1h),3.95(s,3h),3.35(t,j=6.1hz,2h),2.72(t,j=6.6hz,2h),2.31–2.25(m,2h);13cnmr(100mhz,cdcl3)δ198.5,159.7,143.2,137.7,128.5,126.7,126.5,125.9,123.8,119.2,107.1,55.6,38.4,25.8,22.9;ir(kbr):3184,2344,1671,1619,1401,1282,1032,1282,852cm-1;hrms(esi)m/z[m+k]+calcdforc15h14ko2265.0625,found265.0632.
实施例6
将1-(9-菲基)环丁-1-醇(49.7mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入0℃的水浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色固体,熔点103-105℃,产率61%。1hnmr(400mhz,cdcl3)δ9.25(d,j=9.0hz,1h),8.69(dd,j=16.8,7.9hz,2h),8.22(d,j=8.2hz,1h),7.77(t,j=7.5hz,1h),7.69–7.64(m,3h),3.44(t,j=5.8hz,2h),2.85(t,j=6.4hz,2h),2.32–2.28(m,2h).13cnmr(100mhz,cdcl3)δ200.9,144.5,132.6,130.1,130.0,129.3,128.9,127.9,127.8,127.7,127.2,126.7,125.6,123.3,122.5,40.4,27.3,22.2;ir(kbr):3140,2372,1671,1492,1120,1401,883,810cm-1;hrms(esi)m/z[m+na]+calcdforc18h14nao269.0937,found269.0934.
实施例7
将1-(5-苊基)环丁-1-醇(44.9mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入0℃的水浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色固体,熔点144-147℃,产率67%。1hnmr(400mhz,cdcl3)δ9.05(d,j=8.5hz,1h),7.60(dd,j=8.5,7.0hz,1h),7.33(d,j=6.9hz,1h),7.14(s,1h),3.40–3.34(m,4h),3.11(t,j=6.1hz,2h),2.74(t,j=6.6hz,2h),2.20–2.14(m,2h);13cnmr(100mhz,cdcl3)δ200.3,153.7,149.8,146.0,138.6,131.1,130.0,124.2,123.1,120.7,120.1,40.9,32.4,30.5,30.3,23.5;ir(kbr):3138,2352,1602,1401,1174,1079,978,885cm-1;hrms(esi)m/z[m+h]+calcdforc16h15o223.1117,found223.1114.
实施例8
将1-(2-三氟甲基苯基)环丁-1-醇(43.2mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入60℃的油浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色油状物,产率47%。1hnmr(400mhz,cdcl3)δ7.70(d,j=7.7hz,1h),7.53(t,j=7.7hz,1h),7.47(d,j=7.7hz,1h),3.00(t,j=6.1hz,2h),2.75(t,j=6.7hz,2h),2.18–2.11(m,2h).13cnmr(100mhz,cdcl3)δ196.9,146.6,132.9,132.1,132.0,129.5(q,j=33.0hz,1c),129.3(q,j=6.7hz,1c),123.7(d,j=272.0hz,1c),40.2,30.7,22.7;19fnmr(377mhz,cdcl3)δ-59.25;ir(kbr):3138,2344,1687,1541,1401,1314,1097,879,801cm-1;hrms(esi)m/z[m+h]+calcdforc11h10f3o215.0678,found215.0679.
实施例9
将1-(4-三氟甲基苯基)环丁-1-醇(43.2mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入60℃的油浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色油状物,产率53%。1hnmr(400mhz,cdcl3)δ8.14(d,j=8.0hz,1h),7.57–7.54(m,2h),3.04(t,j=6.1hz,2h),2.72(t,j=6.4hz,2h),2.22–2.16(m,2h);13cnmr(100mhz,cdcl3)δ197.5,145.0,135.1,134.6(d,j=32.4hz),128.0,126.1(q,j=3.5hz,1c),123.5(q,j=3.6hz,1c),123.7(d,j=271.1hz,1c),39.2,29.8,23.1;19fnmr(377mhz,cdcl3)δ-63.18;ir(kbr):3138,2369,1707,1666,1316,1264,1126,850,805cm-1;hrms(esi)m/z[m–h]–calcdforc11h8f3o213.0533,found213.0532.
实施例10
将1-(2,5-二三氟甲基苯基)环丁-1-醇(56.8mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入90℃的油浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色油状物,产率45%。1hnmr(400mhz,cdcl3)δ7.90(d,j=8.2hz,1h),7.81(d,j=8.2hz,1h),3.11(t,j=5.9hz,2h),2.80(t,j=6.6hz,2h),2.21–2.15(m,2h);13cnmr(100mhz,cdcl3)δ:196.5,144.8,134.7,132.9(q,j=32.6hz,1c),132.0(q,j=30.1hz,1c),129.4(q,j=5.6hz,1c),126.3(q,j=6.5hz1c),124.6(d,j=39.2hz,1c),121.8(d,j=39.2hz,1c),39.4,26.5,22.0;19fnmr(377mhz,cdcl3)δ-57.76,-63.25;ir(kbr)3140,2344,1716,1507,1401,1319,1127,1168,1036,943,850cm-1;hrms(esi)m/z[m+hco2h–h]-calcdforc13h9f6o3327.0450,found327.0451.
实施例11
将1-(噻吩-2-基)环丁-1-醇(30.8mg,0.2mmol),10毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入60℃的油浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色油状物,产率58%。1hnmr(400mhz,cdcl3)δ7.62(d,j=4.9hz,1h),6.98(d,j=4.9hz,1h),2.89(t,j=6.1hz,2h),2.62(t,j=6.4hz,2h),2.22–2.16(m,2h);13cnmr(100mhz,cdcl3)δ192.6,152.8,136.6,134.0,128.4,38.4,26.2,24.5;ir(kbr):3140,2359,1660,1532,1401,1280,861,740cm-1;hrms(esi)m/z[m+h]+calcdforc8h9os153.0369,found153.0365.
实施例12
将1-(5-甲基噻吩-2-基)环丁-1-醇(33.7mg,0.2mmol),10毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入60℃的油浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色油状物,产率54%。1hnmr(400mhz,cdcl3)δ6.66(s,1h),2.79(t,j=6.1hz,2h),2.56(t,j=6.6hz,2h),2.51(s,3h),2.18–2.11(m,2h);13cnmr(100mhz,cdcl3)δ:192.0,153.6,150.1,134.8,127.1,38.2,26.1,24.5,16.4;ir(kbr)3138,2922,2851,1559,1401,1285,10956,991,884cm-1;hrms(esi)m/z[m+h]+calcdforc9h11os167.0525,found167.0526.
实施例13
将1-(4-辛基噻吩-2-基)环丁-1-醇(53.3mg,0.2mmol),10毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入60℃的油浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色油状物,产率63%。1hnmr(400mhz,cdcl3)δ7.28(s,1h),2.74(t,j=6.1hz,2h),2.61(t,j=6.6hz,2h),2.52(t,j=7.6hz,2h),2.22–2.16(m,2h),1.61–1.55(m,2h),1.40–1.24(m,10h),0.90–0.87(m,3h);13cnmr(100mhz,cdcl3)δ193.6,144.6,144.0,132.9,128.6,39.3,32.0,30.6,30.5,29.9,29.5,29.4,29.2,24.7,22.8,14.3.ir(kbr)3138,2930,2855,1667,1543,1401,1297,1137,924,872,723cm-1;hrms(esi)m/z[m+k]+calcdforc16h24kos303.1179,found303.1176.
实施例14
将1-(苯并噻唑-2-基)环丁-1-醇(40.9mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入0℃的水浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。白色固体,熔点118-120℃,产率61%。1hnmr(400mhz,cdcl3)δ7.87(d,j=8.1hz,1h),7.81(d,j=7.9hz,1h),7.48(t,j=7.4hz,1h),7.42(t,j=7.5hz,1h),3.06(t,j=6.1hz,2h),2.73(t,j=6.6hz2h),2.34–2.28(m,2h);13cnmr(100mhz,cdcl3)δ193.9,148.1,142.6,138.3,136.3,128.2,124.8,124.0,123.6,38.7,24.2,24.0;ir(kbr):3183,2959,2885,1859,1523,1401,1290,1140,1085,878,760cm-1;hrms(esi)m/z[m+h]+calcdforc12h11os203.0521,found203.0520.
实施例15
将1-(4-溴苯并噻唑-2-基)环丁-1-醇(56.6mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入0℃的水浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色固体,熔点137-139℃,产率70%。1hnmr(400mhz,cdcl3)δ7.81(d,j=8.0hz,1h),7.60(d,j=7.6hz,1h),7.28–7.24(m,1h),3.55(t,j=5.3hz,2h),2.70(t,j=5.8hz,2h),2.31–2.27(m,2h);13cnmr(100mhz,cdcl3)δ194.0,148.0,144.8,138.1,136.2,130.4,128.2,123.0,119.4,38.1,28.0,24.1;ir(kbr)3138,1664,1539,1401,1297,1117,1099,879,771cm-1;hrms(esi)m/zcalcdforc12h10bros280.9630,found[m+h]+280.9623.
实施例16
将1-(5-氯苯并噻唑-2-基)环丁-1-醇(47.7mg,0.2mmol),2毫升水与乙腈混合溶剂(1:1,体积比),及一粒搅拌子放入反应管中。将反应管放入0℃的水浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(0.274g,0.5mmol),敞口反应30秒后,立即加入2.5毫升饱和硫代硫酸钠溶液终止反应。然后用乙酸乙酯萃取3次,每次10ml;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品。黄色固体,熔点175-177℃,产率70%。1hnmr(400mhz,cdcl3)δ7.82–7.79(m,2h),7.45(dd,j=8.6,2.1hz,1h),3.03(t,j=6.1hz,2h),2.75(t,j=7.0hz,2h),2.36–2.31(m,2h);13cnmr(100mhz,cdcl3)δ193.6,146.9,140.6,139.6,138.1,131.3,128.6,124.7,123.5,38.7,24.1,24.0;ir(kbr):3153,2363,1559,1401,1257,1593,1080,937,803,741cm-1;hrms(esi)m/zcalcdforc12h10clos237.0135,found[m+h]+237.0134.
对照试验组1~18:
将1-(1-萘基)环丁-1-醇(19.8mg,0.1mmol),溶剂,及一粒搅拌子放入反应管中。将反应管放入设定温度的水/油浴锅中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺,敞口反应,产物采用1hnmr定量分析;各对照试验组的具体反应条件如表1所示。
从上表可以看出,反应温度对该反应有较大影响,但对于该底物最好是在0℃反应。
从上表可以看出,溶剂的类型及用量对该反应也有较大影响,反应效果最好的溶剂是乙腈和水的混合溶剂,其用量分别为0.5毫升和0.5毫升。
从上表还可以看出,氧化剂硝酸铈胺的用量对该反应有较大影响,用量偏低,产率也较低;用量偏高,产率也会降低;最佳的用量是2.5当量,即0.25毫摩尔。
从上表还可以看出,该反应在0.5~2分钟内可顺利进行。反应0.5分钟即可以达到最高产率,而进一步延长反应时间,产率会有所降低。
对照试验组19:
将1-(1-萘基)环丁-1-醇(1g,5.0毫摩尔),水(25毫升),乙腈(25毫升),及一粒搅拌子放入反应管中。将反应管放入0℃的冰水浴中,开动搅拌,恒温10分钟。然后一次性加入硝酸铈胺(6.85克),敞口反应60秒,然后立即加入20毫升饱和硫代硫酸钠溶液终止反应。再用乙酸乙酯萃取3次,每次30毫升;合并萃取液,并用无水硫酸钠干燥,过滤,滤液经减压浓缩后,以石油醚:乙酸乙酯=8:1为洗脱剂对粗产物进行柱层析得到纯品603毫克,产率61%。
由此可见,该反应扩量至克级后,仍然可以迅速的完成,具有好的工业化应用前景。
- 还没有人留言评论。精彩留言会获得点赞!