一种聚乙二醇化酚红及其制备方法和用途与流程
本发明属于医药领域,涉及聚乙二醇化酚红及其制备方法和医药用途,具体涉及新颖的酚红聚合物聚乙二醇化酚红及其制备方法和在在体肠吸收试验的水分校正中的用途。
背景技术:
在体单向肠灌流和在体肠循环是目前最常用、最接近于体内真实吸收状态的在体动物药物吸收研究方法,可用于考察药吸收程度、吸收机制、辅料对药物的透过影响,药物吸收促进剂的转运能力、机制及毒性等各个方面的研究。在研究药物的肠吸收机制时,由于小肠不仅吸收药物也吸收或分泌水分,使灌流液的体积发生改变,故不能直接采用计算药物浓度的方法来计算药量的变化。为校正灌流液体积改变带来的误差,常用的方法有水分校正剂校正法和重量法。重量法存在水分蒸发,肠道壁细胞溶蚀,黏膜脱落等问题。常用的水分校正剂有酚红和14c标记的聚乙二醇4000。
酚红为酸碱指示剂,属于离子型化合物,传统肠吸收的理论认为离子型的化合物在体内不吸收,因此广泛采用酚红来标示在体小肠吸收模型中灌肠液的体积变化,进行药物的小肠吸收研究。但大量的实验结果表明,酚红在一定条件下会被肠道吸收,而且是p-糖蛋白的底物,这将对实验结果产生较大误差。尤其是对于肠道吸收差的药物,酚红校正水分不准确的影响会十分明显。
聚乙二醇4000是渗透性试验中公认的零渗透药物。但14c标记的聚乙二醇4000具有放射性,而且其检测方法特殊,在实验室中难以被广泛采用。对于正常的、未被标记的、分子量大于400的聚乙二醇(peg)是无毒、无致畸性、无免疫原性,价廉易得的。该物质重复单元为氧乙烯基,端基为两个羟基,呈线性或支化链状结构,具有非常好的水溶性和生物相容性,peg修饰药物分子时,可以将其许多优良性能赋予修饰后的药物,如增加被修饰药物的生物相容性、提高溶解性、减小血药浓度波动、增强疗效、降低毒性等。大分子修饰药物这一领域是近年来研究的热点,聚乙二醇是迄今为止已知的大分子聚合物中细胞和蛋白吸收水平最低的分子。
查阅相关文献发现,对于酚红衍生物的研究目前相对较少,将酚红连接在高分子骨架上是目前很新颖且有意义的做法。
现有技术中未见有关于将酚红结构改造制成聚乙二醇化酚红的报道。目前国内对于聚乙二醇修饰小分子技术的研究相对较少,在现有的缺乏相关技术的情况下,研制出一种具有生物相容性好、稳定性高、肠道渗透性低、适用于大规模生产等优点的聚乙二醇化酚红仍然是一个有挑战性和应用价值的难题。
技术实现要素:
针对上述现有技术,本发明提供了一种聚乙二醇化酚红,化学性质稳定,肠道渗透性更低,可提高将其应用于在体肠吸收试验中水分校正的准确性,本发明还提供了其制备方法。
本发明是通过以下技术方案实现的:
一种聚乙二醇化酚红,在不同的ph条件下其结构式分别如下:
n为50-910中的整数,优选为80-250。
r为c1-c6烷基,c3-c6环烷基,苯基,c1-c6烷氧基,含有取代基团的c1-c6烷基、c3-c6环烷基、苯基、c1-c6烷氧基,所述取代基为c1-c4烷基,c1-c4烷氧基。
优选地,
r为c1-c4烷基,c3-c6环烷基,苯基,c1-c4烷氧基,含有取代基团的c1-c4烷基、c3-c6环烷基、苯基、c1-c4烷氧基,所述取代基为c1-c4烷基,c1-c4烷氧基。
优选地,
r为甲氧基。
本发明还提供了所述聚乙二醇化酚红的制备方法如下:
先活化聚乙二醇单甲醚的端羟基,活化的聚乙二醇单甲醚再与酚红反应,得到聚乙二醇修饰的酚红化合物粗品,然后提纯聚乙二醇化酚红的粗品,制得聚乙二醇化酚红的精制品。
具体地,所述的聚乙二醇化酚红的制备方法包括如下步骤:
第一步聚乙二醇单甲醚活化物的制备
原料聚乙二醇单甲醚端羟基活化物的合成,需要根据分子的特性选择活化所需的功能基团。对聚乙二醇单甲醚的一端进行活化,常见活性基团包括对甲基苯磺酸酯基、碘基、甲基磺酸酯基、溴基、氯基等。最优选对甲基苯磺酸酯基。合成步骤如下:
1.制备对甲基苯磺酰基聚乙二醇单甲醚粗品
将聚乙二醇单甲醚溶于溶剂a中,再加入对甲基苯磺酰氯,氮气保护,置于0~5℃条件下滴加缚酸剂,室温反应,得到对甲基苯磺酰基聚乙二醇单甲醚粗品。
所述的聚乙二醇单甲醚的分子量为2~40kda,优选分子量为4~10kda。
所述的聚乙二醇单甲醚可为直链、支链或多臂的聚乙二醇单甲醚中的任意一种,优选为直链的聚乙二醇单甲醚。
所述的聚乙二醇单甲醚、对甲基苯磺酰氯和三乙胺物质的量比为1:1~5:2~10;所述室温下反应时间为3~24h。
所述溶剂a为四氢呋喃、二氯甲烷、三氯甲烷、甲苯、苯、二甲基甲酰胺、二甲亚砜、四氢呋喃、1,4-二氧六环中至少一种,优选为二氯甲烷、四氢呋喃。用量为10~50ml/g。
所述缚酸剂为,但不限有机碱性化合物:吡啶、三乙胺、叔丁醇钾、2,6-二甲基吡啶、二异丙胺、四甲基胍、四甲基乙二胺、二氮杂二环、1,8-二氮杂二环十一碳-7-烯;无机碱性化合物:氢氧化钠、碳酸钾、氢化钠、氢化钙、氢氧化钾中的一种。优选为三乙胺。
2.反应液后处理及产物纯化
先加入1m盐酸至反应液呈酸性,再加入二氯甲烷,水相用二氯甲烷萃取,合并有机相,饱和食盐水洗涤,干燥,减压浓缩,乙醚重结晶,得白色固体,真空干燥至恒重,制得对甲基苯磺酰基聚乙二醇单甲醚精制品,产物为白色固体粉末。收率为80~90%。
第二步单甲氧基聚乙二醇化酚红产物的制备:
1.制备单甲氧基聚乙二醇化酚红粗品
将缚酸剂溶于溶剂b中,氮气保护,0~5℃下搅拌;将酚红溶于溶剂b中,滴加至上述缚酸剂的溶剂中,于0~5℃下反应一段时间后,室温搅拌反应;再将已经溶于溶剂b的聚乙二醇单甲醚活化物滴加至上述反应瓶中,0~5℃下搅拌,室温反应一段时间,油浴下加热进行该反应。
所述反应中聚乙二醇单甲醚活化物:酚红:缚酸剂的物质的量比为1:1.2~3:1.5~5;
所述溶剂b为甲醇、n,n-二甲基甲酰胺、乙腈、二甲基亚砜、甲酰胺中至少一种,优选为n,n-二甲基甲酰胺。
所述缚酸剂为,但不限有机碱性化合物:吡啶、三乙胺、叔丁醇钾、2,6-二甲基吡啶、二异丙胺、四甲基胍、四甲基乙二胺、二氮杂二环、1,8-二氮杂二环十一碳-7-烯;无机碱性化合物:氢氧化钠、氢化钠中的一种。优选为氢化钠。
所述0~5℃下搅拌反应时间为0.2~1h,室温反应时间为0.2~1h。
所述油浴反应温度为80~90℃,反应时间为12~36h。
以薄层色谱检测反应过程,薄层色谱的展开剂为石油醚、乙酸乙酯、正己烷、甲醇、氯仿、二氯甲烷、丙酮、四氢呋喃、水或者其中的两者或三者的混合液。
2.反应液后处理及产物纯化:
反应完毕后用水淬灭,水相用二氯甲烷萃取,合并有机相,饱和食盐水洗涤,干燥,过滤后浓缩得粗产物,粗产物硅胶柱层析,纯化后的产物真空干燥,得到精制品,产物为黄色固体粉末。收率为60~70%。其1hnmr谱,13cnmr谱信号归属见表1,相关谱图见附图1-8。
所述的硅胶柱层析过程中,洗脱剂为乙腈、甲醇、乙醇、丙酮、四氢呋喃、乙酸乙酯、二氯甲烷、石油醚中的两种混合,优选为甲醇和二氯甲烷体积比1:10的混合溶剂。硅胶柱的固定相为200~300目的硅胶。
本发明中,将酚红用聚乙二醇修饰后,可以达到增加其溶解性,增大其分子量的目的。聚乙二醇在酚红周围形成的空间屏障,产生了大分子的空间位阻作用,避免酚红的肠道的吸收,而且避免p-糖蛋白对酚红的识别,使得聚乙二醇化酚红作为水分校正剂更加精确。
本发明具有以下特点:
1.本发明中的原料聚乙二醇单甲醚、活化剂和酚红廉价易得,为聚乙二醇化酚红产品的推广应用提供保障。
2.本发明制备过程简单、产率高、应用性广、生产成本低、对环境无污染。
3.本发明采用的分离纯化容易,产物纯度高。
4.本发明酚红的聚乙二醇修饰物中通过醚键连接,物理化学性质稳定。
5.本发明用于修饰酚红的聚乙二醇是中性、无毒且具有独特理化性质和良好生物相容性的高分子聚合物。
6.本发明利用酚红的酚羟基结构与具有活性基团的聚乙二醇单甲醚进行共价连接,增加酚红的水溶性,降低酚红的肠道透过性。此外,聚合物的链状结构能够有效增加酚红周围环境的空间位阻,避免p-糖蛋白的转运,减少酚红的肠道吸收,增加酚红作为水分矫正剂的准确性。
下面通过实施例对本发明作进一步的描述,这些描述并不是本发明内容进一步的限定。本领域的技术人员应理解,对本发明的技术特征所作的等同替换,或相应的改进,仍属于本发明的保护范围之内。
附图说明
图1是实施实例1聚乙二醇化酚红的凝胶渗透色谱图。
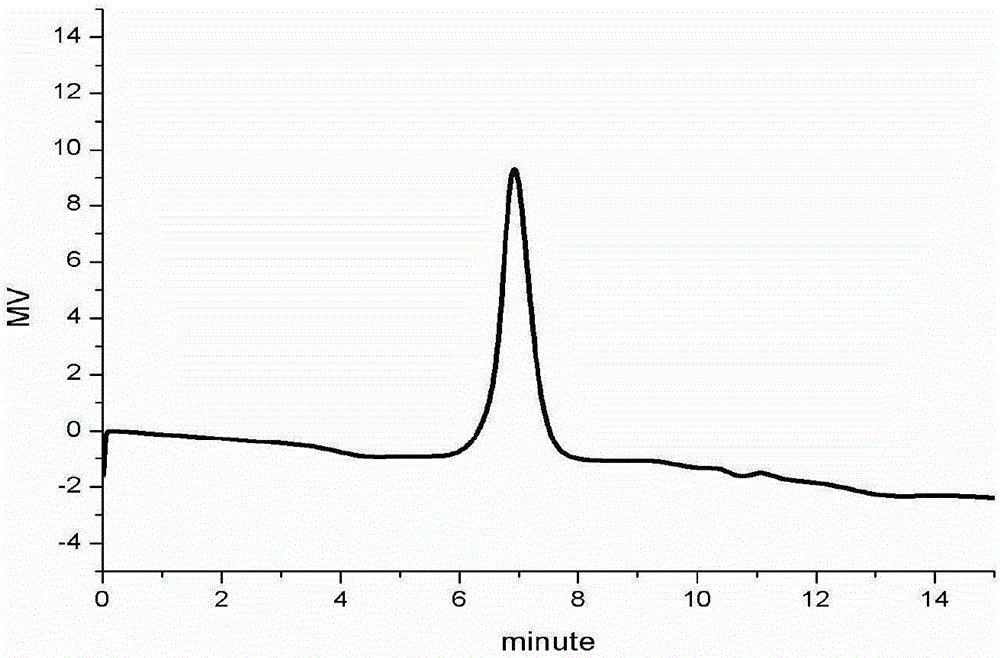
图2是实施实例1聚乙二醇化酚红的hplc图谱。
图3是实施实例1聚乙二醇化酚红的1h-nmr。
图4是实施实例1聚乙二醇化酚红的13c-nmr。
图5是实施实例1聚乙二醇化酚红的hsqc。
图6是实施实例1聚乙二醇化酚红的hmbc。
图7是实施实例1聚乙二醇化酚红的cosy。
图8是实施实例1聚乙二醇化酚红的noesy。
图9是实施实例7中甲氧基聚乙二醇化酚红(4100)与酚红校正模型药物应用于单向在体肠灌流实验中吸收系数比较柱状图。
具体实施方式
实施例1
1.使用甲氧基聚乙二醇-对甲苯磺酸酯(平均分子量4100)为起始原料以制备甲氧基聚乙二醇化酚红
甲氧基聚乙二醇-对甲苯磺酸酯的制备及纯化
取聚乙二醇单甲醚(平均分子量4000)2g溶于10ml二氯甲烷中,再加入0.2g对甲苯磺酰氯,氮气保护下磁力搅拌,冰浴上缓慢滴加三乙胺0.8ml,滴加完毕后室温反应12小时,停止反应。加入1m盐酸10ml至反应液呈酸性,水相用二氯甲烷萃取(40ml*3),合并有机相,饱和食盐水洗涤(20ml*2),干燥,减压浓缩,乙醚重结晶,得白色固体,真空干燥至恒重,得到白色固体粉末,即为对甲苯磺酰化聚乙二醇单甲醚。收率为85%。
2.甲氧基聚乙二醇化酚红的制备及纯化
将0.024g的氢化钠溶于5mlml的二甲基甲酰胺,氮气保护,冰浴下搅拌10分钟。将0.13g酚红溶于4ml二甲基甲酰胺中,滴加至上述冰浴下的氢化钠反应瓶中,冰浴下搅拌10分钟,再将1g对甲苯磺酰化聚乙二醇单甲醚溶于4ml二甲基甲酰胺中,滴加至上述反应瓶中,冰浴下搅拌10分钟,室温下反应10分钟,油浴加热至80℃反应24h。反应结束后,加水淬灭反应,水相用二氯甲烷进行萃取(30ml*3),合并有机相,饱和食盐水洗涤(10ml*2),干燥过滤后,减压浓缩得到粗产物,用甲醇比二氯甲烷为1:10比例的展开剂进行硅胶柱层析,纯化后的产物真空干燥,得到黄色固体粉末0.78g。收率为75%。
实施例2
1.甲氧基聚乙二醇-对甲苯磺酸酯(平均分子量8100)的制备及纯化
取聚乙二醇单甲醚(平均分子量8000)2g溶于10ml二氯甲烷中,再加入0.1g对甲苯磺酰氯,氮气保护下磁力搅拌,冰浴上缓慢滴加三乙胺0.4ml,滴加完毕后室温反应12小时,停止反应。加入1m盐酸6ml至反应液呈酸性,水相用二氯甲烷萃取(40ml*3),合并有机相,饱和食盐水洗涤(20ml*2),干燥,减压浓缩,乙醚重结晶,得到白色固体,真空干燥至恒重,得到白色固体粉末,即为对甲苯磺酰化聚乙二醇单甲醚。收率为90%。
2.甲氧基聚乙二醇化酚红的制备及纯化
将0.012g的氢化钠溶于2.5ml的二甲基甲酰胺,氮气保护,冰浴下搅拌10分钟。将0.06g酚红溶于2ml二甲基甲酰胺中,滴加至上述冰浴下的氢化钠反应瓶中,冰浴下搅拌10分钟,再将1g对甲苯磺酰化聚乙二醇单甲醚溶于4ml二甲基甲酰胺中,滴加至上述反应瓶中,冰浴下搅拌10分钟,室温下反应10分钟,油浴下加热至80℃反应24h。反应结束后,水相用二氯甲烷进行萃取(20ml*3),合并有机相,饱和食盐水洗涤(10ml*2),干燥过滤后,减压浓缩得到粗产物,用甲醇比二氯甲烷为1:10比例的展开剂进行硅胶柱层析,纯化后的产物真空干燥,得到黄色固体粉末0.65g。收率为62%。
实施例3
1.甲氧基聚乙二醇甲基磺酸酯(平均分子量5100)的制备及纯化
取聚乙二醇单甲醚(平均分子量5000)2g溶于10ml二氯甲烷中,再加入0.1g甲基磺酰基氯,氮气保护下磁力搅拌,冰浴上缓慢滴加三乙胺0.4ml,滴加完毕后室温反应12小时,停止反应。加入1m盐酸6ml至反应液呈酸性,水相用二氯甲烷萃取(40ml*3),合并有机相,饱和食盐水洗涤(20ml*2),干燥,减压浓缩,乙醚重结晶,得到白色固体,真空干燥至恒重,得到白色固体粉末,即为甲氧基聚乙二醇-甲基磺酸酯。收率为83%。
2.甲氧基聚乙二醇化酚红的制备及纯化
将0.024g的氢化钠溶于5ml的二甲基甲酰胺,氮气保护,冰浴下搅拌10分钟。将0.13g酚红溶于4ml二甲基甲酰胺中,滴加至上述冰浴下的氢化钠反应瓶中,冰浴下搅拌10分钟,再将1g甲氧基聚乙二醇-甲基磺酸酯溶于4ml二甲基甲酰胺中,滴加至上述反应瓶中,冰浴下搅拌10分钟,室温下反应10分钟,油浴下加热至80℃反应24h。反应结束后,水相用二氯甲烷进行萃取(20ml*3),合并有机相,饱和食盐水洗涤(10ml*2),干燥过滤后得到粗产物,用甲醇比二氯甲烷为1:10比例的展开剂进行硅胶柱层析,纯化后的产物真空干燥,得到黄色固体粉末0.66g。收率为63%。
实施例4
1.甲氧基聚乙二醇甲基磺酸酯(平均分子量10100)的制备及纯化
取聚乙二醇单甲醚(平均分子量10000)2g溶于10ml二氯甲烷中,再加入0.05g甲基磺酰基氯,氮气保护下磁力搅拌,冰浴上缓慢滴加三乙胺0.2ml,滴加完毕后室温反应12小时,停止反应。加入1m盐酸4ml至反应液呈酸性,水相用二氯甲烷萃取(40ml*3),合并有机相,饱和食盐水洗涤(20ml*2),干燥,减压浓缩,乙醚重结晶,得到白色固体,真空干燥至恒重,得到白色固体粉末,即为甲氧基聚乙二醇-甲基磺酸酯。收率为81%。
2.甲氧基聚乙二醇化酚红的制备及纯化
将0.012g的氢化钠溶于2.5ml的二甲基甲酰胺,氮气保护,冰浴下搅拌10分钟。将0.06g酚红溶于2ml二甲基甲酰胺中,滴加至上述冰浴下的氢化钠反应瓶中,冰浴下搅拌10分钟,再将1g甲氧基聚乙二醇-甲基磺酸酯溶于4ml二甲基甲酰胺中,滴加至上述反应瓶中,冰浴下搅拌10分钟,室温下反应10分钟,油浴下加热至80℃反应24h。反应结束后,水相用二氯甲烷进行萃取(20ml*3),合并有机相,饱和食盐水洗涤(10ml*2),干燥过滤后,减压浓缩得到粗产物,用甲醇比二氯甲烷为1:10比例的展开剂进行硅胶柱层析,纯化后的产物真空干燥,得到黄色固体粉末0.70g。收率为67%。
实施例5
甲氧基聚乙二醇化酚红(平均分子量4100)和酚红的肠透性比较。
甲氧基聚乙二醇化酚红(由实施实例1的方法制备得到)和酚红肠吸收的实验比较。分别配制30μmol/ml甲氧基聚乙二醇化酚红与30μmol/ml酚红溶解于k-r液中,测定以上两种指示剂的渗透量。
通过外翻肠囊法对两种指示剂肠渗透性进行比较,用hplc方法来确定指示剂的渗透量。实验前将健康合格,体重在200±15g的wistar雄性大鼠禁食过夜,腹腔注射20%乌拉坦溶液,剂量为5ml/kg。沿腹中线打开腹腔,剥离肠段,取10cm左右肠段,立即置于冰冷的k-r营养液中,冲洗肠段,小心翻转肠段,使粘膜侧向外,细线结扎一端,小肠上端固定于取样口,向肠内注满空白k-r营养液,然后放入含有指示剂溶液的容器中,37℃恒温并通入混合气体(5%co2,95%o2)。分别于15min、30min、45min、60min、75min、90min、105min吸取受药体系溶液300μl,同时补加等量的k-r试液。测定表明:同等摩尔量浓度下,甲氧基聚乙二醇修饰的酚红几乎不透过肠道,显著降低了酚红的吸收。
实施例6
甲氧基聚乙二醇化酚红(平均分子量8100)和酚红的肠透性比较。
甲氧基聚乙二醇化酚红(由实施例2的方法制备得到)和酚红肠吸收的试验比较。利用与实施例5相同的方法,分别配制相当于30μmol/ml甲氧基聚乙二醇化酚红(平均分子量8100)与30μmol/ml酚红溶解于k-r液中,测定以上两种指示剂的渗透量。测定表明:同等摩尔量浓度下,甲氧基聚乙二醇修饰的酚红几乎不透过肠道,显著降低了酚红的吸收。
以上结果表明:甲氧基聚乙二醇修饰的酚红的肠渗透性几乎为零,同酚红比较肠透性显著降低,这样更有利于作为在体肠吸收的水分校正剂使用。
上述实施例5、6的指示剂吸收情况示于表2。
表2外翻肠囊实验中聚乙二醇化酚红与酚红渗透性数据
实施例7
甲氧基聚乙二醇化酚红(平均分子量4100)应用于单向在体肠灌流实验研究。
甲氧基聚乙二醇化酚红(由实施例1的方法制备得到)和酚红应用于在体单向肠灌流实验中的比较。分别配制30μmol/ml甲氧基聚乙二醇化酚红与30μmol/ml酚红溶解于k-r液中,测定模型药物硝酸异山梨酯的有效渗透系数和吸收速率。
通过单向在体肠灌流对两种指示剂应用进行比较,用hplc方法来确定模型药物和指示剂的浓度。实验前将健康合格,体重在200±15g的wistar雄性大鼠禁食过夜,腹腔注射20%乌拉坦溶液,剂量为5ml/kg。沿腹中线打开腹腔3.0~4.0cm的开口,分离出空肠段约10cm(空肠段为自幽门下15cm开始),两端切口,用预热至37℃的灌流液将肠内容物清洗干净。之后插管结扎于出口处。用浸有生理盐水的纱布将大鼠伤口处覆盖,于红外灯下保温。实验前用灌流液饱和管路30min后收集灌流液,流速为0.2ml/min,每隔15min在出口收集一次灌流液,实验进行105min,样品进hplc进行检测。实验结束后,测量并记录被灌流肠段的长度和内径,计算模型药物硝酸异山梨酯的表观渗透系数。测定表明:同等摩尔量浓度下,甲氧基聚乙二醇修饰的酚红校正结果更加稳定,结果更加可靠。两种水分校正剂校正模型药物硝酸异山梨酯吸收情况见附图9。
表1聚乙二醇化酚红1h(600mhz)and13c(150mhz)nmr数据(dmso-d6)
- 还没有人留言评论。精彩留言会获得点赞!