用于肺癌的诊断的生物标志物的制作方法
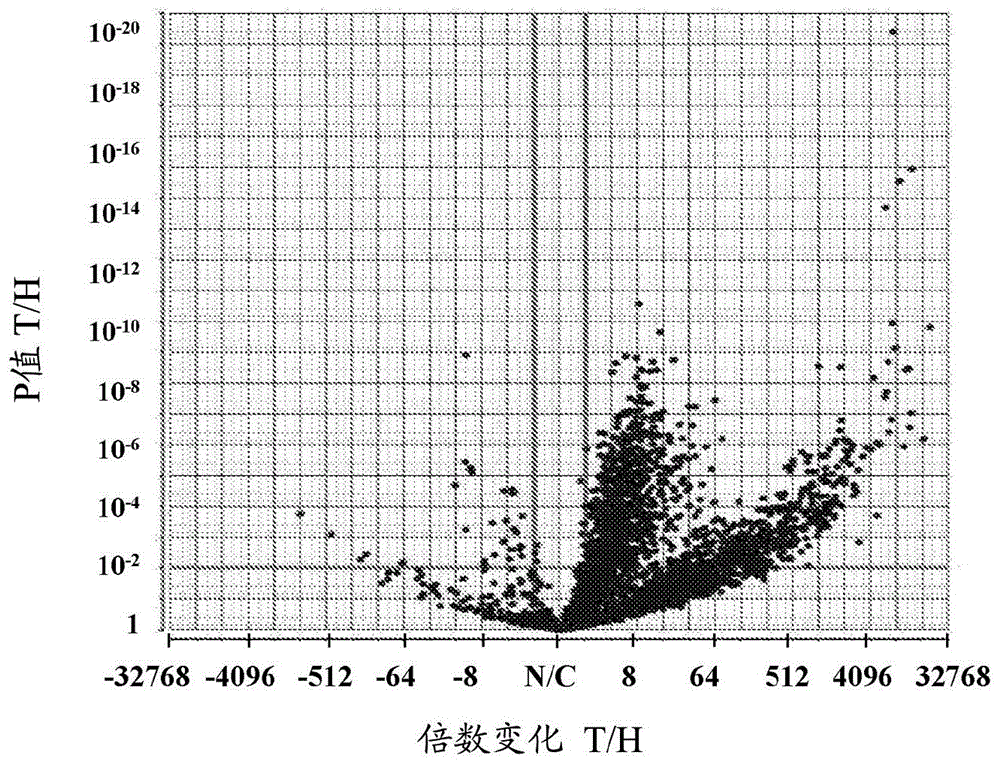
发明领域本发明涉及肺癌的生物标志物,特别是能够区分非小细胞肺癌(nsclc)的亚型,特别是区分腺癌(ac)和鳞状细胞癌(scc)的标志物。特别地,本发明涉及用于诊断、评估nsclc的严重程度的水平和治疗nsclc的组合物和方法。发明背景非小细胞肺癌(nsclc)是肺癌的最普遍形式,并且代表了全世界男性和女性二者中癌症死亡的主要原因。因为大多数被诊断为nsclc的患者是在疾病的晚期,在用基于铂的化学疗法、放射和/或手术进行标准治疗后,总体生存仍然少于12个月。然而,通过以不同的组合实施免疫疗法的新型策略,中位总体生存期可以增加;或如果存在驱动突变,那么通过靶向的酪氨酸激酶抑制疗法,中位总体生存期可以增加到4年。nsclc可以被分为许多亚型,而两个主要的亚型是腺癌(ac)和鳞状细胞癌(scc),一起占nsclc病例的绝大多数(代表几乎80%的原发性肺癌病例),并且是所有癌症死亡的30%的原因。特别地,ac是非吸烟者中肺癌的最普遍亚型,并且构成所有肺癌类型的病例的约50%。在ac中,肿瘤发展于肺的腺细胞,所述腺细胞位于肺的周围处,负责产生粘蛋白和表面活性物质。scc构成约30%的nsclc病例,其通常发展于肺的支气管的中央区域,并且与吸烟紧密关联。虽然这两种nsclc亚型二者具有独特的和共有的临床表现和组织病理学特征,但对遗传学研究的需要和治疗策略可能有显著差异。为了确保适当的治疗策略,因此在诊断期间能够区分两种nsclc亚型是至关重要的(jankuf等人natrevclinoncol2010;7:401-14;kawasea等人jpnjclinoncol2012;42:189-95)。目前的组织学鉴别(histologicaldiscrimination)是基于组织可利用度,其中约15%-20%的病例,在最终组织学可以被定义前,组织被耗尽,或多达7.2%被不良地区分并且不以其他方式表现为指定的nsclc。肺癌和许多其他癌症一样,通过包括遗传或获得性遗传异常的累积的肿瘤生物发生(tumorbiogenesis)的多步骤过程发展(tomasettic等人science.2017;355:1330-4)。这些可以通过深度测序方法检测(meldrumc等人clinbiochemrev2011;32:177-95),然而它由于恶性肿瘤的异质性和复杂性而变得复杂(marusyka等人-biochimbiophysacta.2010;1805:105-17)。然而,与癌症相关的其他变化与突变不相关,而是表现为蛋白表达的增加或减少,或表现为标志物蛋白的差异翻译后修饰(tainskyma.biochimbiophysacta2009;1796:176-93)。因此,除突变之外的生物标志物应当作为疾病的早期标志物、作为疾病状态的指示物和作为治疗有效性的预测和预后度量被鉴定和探索(tainsky2009,同上)。最近的努力已经集中在肺ac和scc中的基因组、表观基因组、转录组和蛋白组内出现的变化,其可以用于区分这两种nsclc亚型(campbelljd等人natgenet2016;48:607-16)。据报道目前约17种生物标志物在ac和scc中差异表达(下文表1)。这些中的11种生物标志物被报道以检测ac,而仅5种生物标志物被提出用于诊断scc。目前4种标志物在临床中使用以区分两种亚型,并且6种标志物被用于指导靶向的疗法(表1)。它们中包括microrna,在ac中检测到mir21,而mir205与scc相关(campbell2016,同上)。ttf1(甲状腺转录因子1)、napsa(天冬氨酸蛋白酶a(napsina))和cd141(凝血调节蛋白)被发现在ac中与scc相比高度表达,而tp63(肿瘤蛋白63)及其同种型p40(δnp63)的高表达水平被报道为scc的标志物(kimmj等人anndiagnpathol2013;17:85-90)。仍然存在对适当生物标志物的未满足的需要,所述良好生物标志物适合作为诊断工具用于评估存在或不存在nsclc,并且更重要地,用于区分这种癌症的主要亚型ac和scc。发明概述本发明涉及在非小细胞肺癌(nsclc)中差异表达的新型生物标志物以及在nsclc亚型腺癌(ac)和鳞状细胞癌(scc)中差异表达,并且因此可以被用于区分这些nsclc亚型的生物标志物。本发明部分地基于未预期的发现,即某些蛋白显示出在ssc中与ac相比不同的表达模式和/或表达水平。根据某些方面,本发明公开了以下蛋白和/或编码以下蛋白的mrna的每一种的表达,在从被诊断为具有nsclc亚型scc的患者获得的肿瘤样品中与从被诊断为具有ac亚型的患者获得的样品中的表达相比更高:hat1(b型组蛋白乙酰转移酶);lrrfip2(富含亮氨酸重复flightless相互作用蛋白2(leucine-richrepeatflightless-interactingprotein2));akr1b10(醛酮还原酶家族1成员b10,一种分泌型蛋白);wdr82(包含wd重复的蛋白82(wdrepeat-containingprotein82));ttll12(微管蛋白酪氨酸连接酶样蛋白12);igf2bp3(胰岛素样生长因子2mrna结合蛋白);smc2(染色体结构维持蛋白2);和itga7(整联蛋白α-7)。根据某些方面,本发明还公开了以下蛋白和/或编码以下蛋白的mrna的每一种的表达,在从被诊断为具有ac的患者获得的肿瘤样品中与它们在从被诊断为scc的患者获得的样品中的表达相比更高:acad8(异丁酰基-coa脱氢酶);tsg101(肿瘤易感基因101蛋白);rab34(ras相关蛋白rab-34);rsu1(ras抑制蛋白);acot1(酰基-辅酶a硫酯酶1);gale(udp-葡萄糖4-差向异构酶);和hyou1(低氧上调蛋白1)。根据其他方面,已经发现蛋白smac/diablo(第二种来源于线粒体的胱天蛋白酶的活化物/具有低pi的凋亡结合蛋白的直接抑制物)主要位于从被诊断为具有ac的患者获得的样品中的线粒体和胞质溶胶中,而在诊断为scc的那些患者中,发现smac/diablo不仅位于线粒体和胞质溶胶中并且约50%位于核中。本发明还提供了nsclc的新鉴定的生物标志物(蛋白和/或mrna),其在从被诊断为nsclc的患者的癌性肺组织获得的样品中与从相同的受试者获得的健康组织相比高度表达。新型生物标志物包括但不限于apool(载脂蛋白o样);vps29(液泡蛋白分选相关蛋白29(vacuolarproteinsorting-associatedprotein29));和caf17(铁硫簇组装因子同系物(iron-sulfurclusterassemblyfactorhomolog)),迄今为止尚未知与癌症相关。因此,本发明提供了用于诊断nsclc和用于区分nsclc亚型scc和ac的方法和试剂盒。本发明还提供了辅助确定nsclc亚型ac的严重程度的标志物和标志物组合。本发明的标志物,单独或与另外的标志物组合,可以辅助疾病和/或其亚型的早期诊断,并且使得能够尽可能早地选择适当的疗法。本发明的若干种标志物和另外的标志物根据一个方面,本发明提供了一种用于在怀疑具有非小细胞肺癌(nsclc)的受试者中诊断选自腺癌(ac)和鳞状细胞癌(scc)的nsclc的亚型的方法,该方法包括:(a)确定从受试者获得的生物样品中选自蛋白和编码所述蛋白的mrna的至少一种生物标志物的表达水平,其中至少一种生物标志物选自由以下组成的组:hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3、smc2、acad8、rsu1、acot1、hyou1、gale、itga7、tsg101和rab34;(b)将所述至少一种生物标志物的表达水平与健康生物样品中所述至少一种生物标志物的表达水平和/或代表健康生物样品的参考值比较;任选地(c)计算从所述受试者获得的样品中所述至少一种生物标志物的表达水平与健康样品中的表达水平和/或参考值的倍数变化;和(d)诊断所述受试者,其中-与所述健康生物样品中的表达水平和/或参考值相比,从所述受试者获得的所述样品中选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和smc2组成的组的至少一种生物标志物的升高的表达水平,和/或选自由acad8、rsu1、acot1、hyou1和gale组成的组的至少一种生物标志物的降低的表达,指示所述受试者具有nsclc亚型scc;与所述健康生物样品中的表达水平和/或参考值相比,从所述受试者获得的所述样品中选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和smc2组成的组的至少一种生物标志物的降低的表达水平,和/或选自由acad8、rsu1、acot1、hyou1和gale组成的组的至少一种生物标志物的升高的表达,指示所述受试者具有nsclc亚型ac;生物标志物itga7与参考值相比相等或升高的倍数变化指示受试者具有nsclc亚型scc,其中参考值来源于从scc患者获得的多于一个样品中所述itga7生物标志物的表达与它在多于一个健康生物样品中的表达相比的倍数变化;生物标志物tsg101与参考值相比相等或升高的倍数变化指示受试者具有nsclc亚型ac,其中参考值来源于从ac患者获得的多于一个样品中所述tsg101生物标志物的表达与它在多于一个健康生物样品中的表达相比的倍数变化;生物标志物rab34与参考值相比相等或降低的倍数变化指示受试者具有nsclc亚型ac,其中参考值来源于从ac患者获得的多于一个样品中所述rab34生物标志物的表达与它在多于一个健康生物样品中的表达相比的倍数变化。根据某些实施方案,方法包括确定生物标志物的组合的表达水平,该组合选自由以下组成的组:至少2种、至少3种、至少4种、至少5种、至少6种、至少7种、至少8种、至少9种、至少10种、至少11种、至少12种、至少13种、至少14种和15种生物标志物。根据某些实施方案,方法包括确定选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和smc2组成的组的至少一种生物标志物以及选自由acad8、rsu1、acot1、hyou1和gale组成的组的至少一种生物标志物的表达水平。每种可能性代表本发明的单独实施方案。根据某些实施方案,方法包括确定选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3、smc2和itga7组成的组的至少一种生物标志物以及选自由acad8、rsu1、acot1、hyou1、gale、tsg101和rab34组成的组的至少一种生物标志物的表达水平。根据某些实施方案,方法包括确定标志物的组合的表达水平,该组合包括生物标志物hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和smc2。根据某些实施方案,方法包括确定标志物的组合的表达水平,该组合包括生物标志物acad8、rsu1、acot1、hyou1和gale。根据某些实施方案,方法包括确定标志物的组合的表达水平,该组合包括生物标志物hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3、smc2、itga7、acad8、rsu1、acot1、hyou1、gale、tsg101和rab34。根据某些实施方案,方法包括确定至少两种生物标志物的表达水平,所述方法还包括确定usp14(泛素羧基末端水解酶14)、vdac1(电压依赖的阴离子通道-1)和aif(凋亡诱导因子)的至少一种的表达水平,其中至少一种生物标志物与参考值相比相等或升高的倍数变化指示受试者具有nsclc亚型scc,其中参考值来源于从scc患者获得的多于一个样品中所述至少一种生物标志物的表达与在多于一个健康生物样品中的表达相比的倍数变化。根据某些实施方案,至少一种生物标志物的表达水平为与健康样品中所述生物标志物的表达或与参考值相比至少2倍、至少3倍、至少4倍、至少5倍、至少10倍、至少50倍、至少100倍、至少500倍、至少1,000倍和更高或更低。根据某些示例性实施方案,至少一种生物标志物的表达水平为与健康样品中所述生物标志物的表达或参考值相比高至少4倍。根据某些实施方案,生物标志物是蛋白。根据某些示例性实施方案,生物样品是肺组织样品。根据这些实施方案,健康生物样品从健康受试者或从怀疑具有nsclc的受试者的健康肺组织获得。根据某些实施方案,生物标志物是分泌型蛋白并且生物样品选自由血液样品、血浆样品和血清样品组成的组。根据一些实施方案,从受试者获得的生物样品为腹水。根据某些实施方案,方法还包括用适用于治疗ac的疗法治疗被诊断为具有nsclc亚型ac的受试者。根据本发明的教导,可以使用已知在治疗nsclc亚型ac中有效的任何疗法。根据一些实施方案,适用于治疗ac的疗法包括向受试者施用治疗有效量的至少一种剂,所述剂降低选自由tsg101、acad8和gale组成的组的至少一种蛋白的表达或活性。每种可能性代表本发明的单独实施方案。根据某些实施方案,方法还包括用适用于治疗scc的疗法治疗被诊断为具有nsclc亚型scc的受试者。根据本发明的教导,可以使用已知在治疗nsclc亚型scc中有效的任何疗法。根据一些实施方案,适用于治疗scc的疗法包括向受试者施用治疗有效量的至少一种剂,所述剂降低选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和itga7组成的组的至少一种蛋白的表达或活性。每种可能性代表本发明的单独实施方案。根据某些实施方案,降低至少一种蛋白的表达或活性的剂选自由化学剂或部分、蛋白、肽和多核苷酸分子组成的组。每种可能性代表本发明的单独实施方案。根据某些实施方案,剂是抗体。根据某些示例性实施方案,剂是选自由shrna、sirna和mirna组成的组的干扰rna(rnai)分子。根据又另外的方面,本发明提供了一种用于在怀疑具有非小细胞肺癌(nsclc)的受试者中诊断选自由鳞状细胞癌(scc)和腺癌(ac)组成的组的nsclc的亚型的方法,该方法包括(a)确定从受试者获得的包含细胞的样品中smac/diablo蛋白的存在,和(b)当显著量的smac/diablo蛋白存在于细胞核和细胞胞质溶胶中时,将所述受试者诊断为具有nsclc亚型scc,并且当无显著量的所述smac/diablo蛋白存在于细胞核中并且显著量的所述smac/diablo蛋白存在于胞质溶胶中时,将所述受试者诊断为具有nsclc亚型ac。根据某些实施方案,方法还包括用适用于治疗ac的疗法治疗被诊断为具有nsclc亚型ac的受试者。根据某些实施方案,方法还包括用适用于治疗scc的疗法治疗被诊断为具有nsclc亚型scc的受试者。用于治疗ac或scc的方法是如本领域已知的并且如上文描述的。根据又其他方面,本发明提供了一种用于在受试者中诊断nsclc的方法,该方法包括:(a)将受试者的生物样品中选自蛋白或编码该蛋白的mrna的至少一种生物标志物的表达水平与对照生物样品或参考值比较,其中至少一种生物标志物选自由apool、vps29、caf17及其任何组合组成的组;(b)在所述至少一种生物标志物或生物标志物的组合的表达水平与对照生物样品中的表达或与参考值相比增加的情况下,将受试者诊断为具有nsclc,。根据某些实施方案,用于诊断nsclc的方法包括比较至少两种生物标志物或三种生物标志物的表达水平。根据某些实施方案,方法还包括比较选自下文表2中列出的生物标志物的至少一种另外的生物标志物的表达水平。根据某些示例性实施方案,用于诊断nsclc的方法还包括比较选自由vdac1、aif、atp5b、hsp60、gadph、pgk1、eno1、ldha和rab11b组成的组的至少一种另外的生物标志物的表达水平。每种可能性代表本发明的单独实施方案。根据某些示例性实施方案,另外的标志物选自pgk1和rab11。根据某些实施方案,生物样品是肺组织。根据这些实施方案,对照样品从健康受试者获得。根据某些实施方案,参考值代表了代表从多于一个健康受试者获得的多于一个样品中每一种生物标志物的表达水平的统计度量。根据某些实施方案,至少一种生物标志物的表达水平为与健康样品中所述生物标志物的表达或参考值相比至少2倍、至少3倍、至少4倍、至少5倍、至少10倍、至少50倍、至少100倍、至少500倍、至少1,000倍和更高。根据某些示例性实施方案,至少一种生物标志物的表达水平为与健康样品中所述生物标志物的表达或与参考值相比高至少4倍。根据某些实施方案,至少一种生物标志物是蛋白。根据某些实施方案,将受试者诊断为具有nsclc的方法还包括用适用于治疗nsclc的疗法治疗所述受试者。用于治疗nsclc的疗法是本领域已知的。根据一些实施方案,治疗nsclc包括向受试者施用治疗有效量的至少一种剂,所述剂降低选自由apool、vps29和caf17组成的组的至少一种蛋白的表达或活性。降低至少一种生物标志物的表达的剂是如本领域已知的并且如上文描述的。根据另一个方面,本发明提供了一种用于预测nsclc亚型ac的严重程度的方法,该方法包括:(a)将从被诊断为具有nsclc亚型ac的受试者获得的生物样品中选自蛋白和编码所述蛋白的mrna的至少一种生物标志物的表达水平与参考值比较,其中至少一种生物标志物选自由以下组成的组:vdac1、smac、hyou1、ttll12、rab34、arl1、hat1、p40、napsa、lrrfip2、aif、titf、wdr82和tsg101;(b)预测疾病的严重程度的水平,其中选自由vdac1、smac、hyou1、ttll12和rab34组成的组的至少一种生物标志物的水平与参考值相比的增加将所述患者表征为具有严重形式的该疾病;并且其中选自由arl1、hat1、p40、napsa、lrrfip2、aif、titf、wdr82和tsg101组成的组的至少一种生物标志物的水平与参考值相比的增加将所述患者表征为具有较温和形式的该疾病。根据某些实施方案,较温和形式的该疾病指示与严重形式相比更长的生存率。根据某些实施方案,生物标志物为mrna标志物。根据本发明的某些实施方案,将受试者的生物样品中至少一种蛋白生物标志物或编码该蛋白生物标志物的mrna的表达水平与参考值比较包括确定样品中至少一种蛋白生物标志物或编码该蛋白生物标志物的mrna的表达水平,并且将所述表达水平与参考值比较。根据另外的实施方案,将受试者的生物样品中至少一种蛋白或mrna生物标志物的表达水平与对照样品比较包括确定从所述受试者获得的样品中和对照样品中至少一种蛋白或mrna生物标志物的表达水平,并且比较所述确定的水平。根据某些实施方案,样品为组织样品。根据某些实施方案,对照样品是从一个健康受试者或多于一个健康受试者(aheatlthysubjectorsubject(s))获取的组织。根据某些示例性实施方案,为了区分nsclc亚型,待分析的样品是从受试者获取的肿瘤组织,并且对照组织是从相同的受试者获取的健康组织。根据又另外的实施方案,对照组织从被诊断为nsclc亚型scc或亚型ac的一个或更多个受试者获取。根据又另一个方面,本发明提供了一种用于治疗nsclc亚型scc的方法,该方法包括向有相应需要的受试者施用治疗有效量的至少一种剂,所述剂降低选自由hat1、lrrfip2、akr1b10、wdr82、ttll12、itga7、igf2bp3和usp14组成的组的至少一种蛋白的表达或活性。根据又另外的方面,本发明提供了一种用于治疗nsclc亚型ac的方法,该方法包括向有相应需要的受试者施用治疗有效量的至少一种剂,所述剂降低选自由acad8、tsg101和gale组成的组的至少一种蛋白的表达或活性。根据又其他方面,本发明提供了一种用于治疗nsclc的方法,该方法包括向有相应需要的受试者施用治疗有效量的至少一种剂,所述剂降低选自由apool、vps29和caf17组成的组的至少一种蛋白的表达或活性。根据本发明的教导,可以使用本领域已知的并且如上文描述的可以降低生物标志物的表达或活性的任何剂。根据另外的方面,本发明提供了一种用于诊断从怀疑具有非小细胞肺癌(nsclc)的受试者获得的生物样品中选自腺癌(ac)和鳞状细胞癌(scc)的nsclc的亚型的试剂盒,该试剂盒包含:(a)至少一种剂,所述至少一种剂能够检测选自蛋白和编码所述蛋白的mrna的至少一种生物标志物的表达水平,该生物标志物选自由以下组成的组:hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3、smc2、acad8、rsu1、acot1、hyou1、gale、itga7、tsg101和rab34;(b)工具,所述工具用于将至少一种生物标志物的表达水平与第一参考值和/或与第二参考值和/或与第三参考值比较,所述第一参考值来源于健康生物样品中至少一种生物标志物的表达,所述第二参考值来源于从scc患者获得的多于一个样品中所述至少一种生物标志物的表达与多于一个健康生物样品中的表达相比的倍数变化,所述第三参考值来源于从ac患者获得的多于一个样品中至少一种生物标志物的表达与多于一个健康生物样品相比的倍数变化;(c)说明材料,所述说明材料提供对所述至少一种生物标志物的所述表达水平与nsclc亚型的相关性的指导,其中:与第一参考值相比,所述样品中选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和smc2组成的组的至少一种生物标志物的增加的表达水平,和/或选自由acad8、rsu1、acot1、hyou1和gale组成的组的至少一种生物标志物的降低的表达,指示所述受试者具有nsclc亚型scc;与第一参考值相比,样品中选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和smc2组成的组的至少一种生物标志物的降低的表达水平,和/或选自由acad8、rsu1、acot1、hyou1和gale组成的组的至少一种生物标志物的升高的表达,指示所述受试者具有nsclc亚型ac;生物标志物tga7与第二参考值相比相等或升高的倍数变化指示受试者具有nsclc亚型scc;生物标志物tsg101与第三参考值相比相等或升高的倍数变化指示受试者具有nsclc亚型ac;和/或生物标志物rab34与第三参考值相比相等或降低的倍数变化指示受试者具有nsclc亚型ac。根据某些实施方案,试剂盒还包含能够检测存在于生物样品内的细胞核内的smac/diablo蛋白的表达的至少一种剂和提供对细胞核和胞质溶胶内的smac/diablo的量与nsclc亚型的相关性的指导的说明材料,其中细胞核和胞质溶胶中显著量的smac/diablo蛋白将受试者诊断为具有nsclc亚型scc,并且细胞核中无显著量的所述smac/diablo蛋白而胞质溶胶中存在显著量的所述smac/diablo蛋白将受试者诊断为具有nsclc亚型ac。根据又另外的方面,本发明提供了一种用于诊断nsclc的试剂盒,该试剂盒包含:(a)至少一种剂,所述至少一种剂能够检测怀疑具有nsclc的受试者的生物样品中选自蛋白和编码所述蛋白的mrna的至少一种生物标志物的表达水平,该生物标志物选自由apool、vps29和caf17组成的组;(b)工具,所述工具用于将至少一种生物标志物的表达水平与从健康受试者获得的对照样品或与参考值比较;和(c)说明材料,所述说明材料提供对所述至少一种生物标志物的表达水平与对照样品或参考值相比的增加与nsclc的相关性的指导。将理解的是,本文公开的方面和实施方案的任何组合明确地包括在本发明的公开内容内。本发明的适用性的其他实施方案和全部范围将从下文给出的详细描述变得明显。然而,应当理解的是,详细描述和特定实施例,虽然指示本发明的优选的实施方案,但通过仅说明的方式给出,因为根据该详细描述在本发明的精神和范围内的多种变化和修改对本领域技术人员来说将变得明显。附图简述图1示出了从具有肺癌的患者的健康样品和肿瘤样品获得的样品中的蛋白表达的统计和功能分析。图1a示出了代表对于每种鉴定的蛋白的倍数变化(x轴)和倍数发现率(fdr,y轴)值的火山图。垂直线指示倍数变化>2或<-2,并且水平线指示p值<0.05。1,494种蛋白通过这些阈值。图1b:基于基因本体系统(genoontologysystem),显示出变化的表达的蛋白中的显著富集的功能组。图2示出了从肺癌患者获得的样品中vdac1和其他凋亡和能量相关的蛋白的过表达。图2a:用针对vdac1、smac、hk-i、mavs、aif和bcl-2的抗体探测的来源于肺癌患者的肿瘤(t)和健康(h)肺组织的组织裂解物的代表性免疫印迹。图2b:以平均值±sd展示了以下的定量分析:vdac1(37名患者,倍数变化(fc)=6.2,p值=5×10-5);smac(37名患者,fc=5,p值=3.4×10-5);hk-i(33名患者,fc=5.3,p值=5.3×10-3);mavs(22名患者,fc=2.6,p值=1.5×10-4);aif(35名患者,fc=3.5,p值=1.7×10-2)和bcl-2(22名患者,fc=1.5,p值=1.4×10-1)。图2c:vdac1、hk-i和smac的lc-hrms/ms数据。如由用于免疫印迹的mann-whitney检验和用于lc-hrms/ms数据的双向t-检验确定的,当p<0.001(***)、p<0.01(**)、p<0.05(*)时,健康组织和肿瘤组织之间的差异被认为是统计学上显著的。图2d:基于rnaseq对vdac1、hk-i、smac和aif的基因表达的定量分析。基因表达谱从对于肺癌患者的健康(n=110)和肿瘤肺样品(n=1,017)的公开可得数据(tcga肺癌数据集)获得。图2e:肺癌患者中vdac1、smac、aif、mavs和bcl-2的过表达。来自组织微阵列载玻片(biomax)的正常(n=5)和肺癌(n=20)组织样品的vdac1、smac、aif、mavs和bcl-2的代表性ihc染色。示出了在指示的强度染色的患者样品的百分比。图3示出了从肺癌患者获得的样品中已知和新鉴定的蛋白的过表达。图3a、3b:用针对hyou1(orp150)、ldha、hspd1(hsp60)、atp5b、gapdh和rab11b的抗体探测的来源于肺癌患者的肿瘤(t)和健康(h)肺组织的组织裂解物的代表性免疫印迹。图3c:lc-hrms/ms数据的定量分析。如由用于lc-hrms/ms数据的双向t-检验确定的,当p<0.001(***)、p<0.01(**)时,健康组织和肿瘤组织之间的差异被认为是统计学上显著的。图3d:基于rnaseq对gapdh、pgk1、eno1、ldha和hyou1的基因表达的定量分析。基因表达谱从肺癌患者的健康(n=110)和肿瘤肺样品(n=1,017)获得。图4示出了在ac和scc中差异表达的蛋白。图4a:组织阵列载玻片(biomax)中的人类正常肺组织(n=10)、肺scc组织(n=31)或肺ac组织(n=17)的vdac1、aif和smac的ihc染色,如材料和方法中描述的。示出了在指示的强度染色的切片的百分比。图4b:lc-hrms/ms数据被用于鉴定可以用于区分ac和scc的蛋白。如由mann-whitney检验确定的,当p<0.05(*)、p<0.01(**)或p<0.001(***)时,ac和scc组之间的差异被认为是统计学上显著的。图5示出了如由肺癌患者中的潜在蛋白标志物的rnaseq确定的基因表达。图5a:使从tcga导入的rnaseq数据经受使用t-检验的定量分析。展示了scc中与ac中相比蛋白表达的比率,并且当p<0.001(***)时被认为是统计学上显著的。根据功能,蛋白被分组为:apop,凋亡;metab,代谢;har,组蛋白活性调控;ubiq,泛素化;inflam,炎性响应;sp,表面活性物质产生;pt,蛋白转运。图5b:基于蛋白质组学数据,示出了ac和scc之间的差异表达的24种选择的基因的rnaseq数据的定量分析。功能组被指示为:ts,肿瘤抑制物;metab,半乳糖代谢;lm,脂质代谢;aam,氨基酸代谢;stp,结构蛋白;pi,蛋白酶抑制物;sip,信号传导通路;na,核活性;mt,线粒体易位酶,以及ir,免疫应答。图6示出了肺癌中的smac亚细胞定位。示出了组织阵列载玻片(biomax)中人类scc和ac肺癌中的smac(图6a)和aif(图6b)的ihc染色,以及smac的核和胞质溶胶定位。图6c:使用核/胞质溶胶分级(fractionation)试剂盒(biovision,milpitas,ca)遵循制造商的说明,从肺癌患者的ac和scc样品制备核提取物。在离心(16,000g,10min)之后,将上清液(胞质溶胶级分(fraction))和沉淀(核级分)重悬浮于初始体积中,并且经受针对smac、vdac1和aif的免疫印迹。图6d:定量分析,将结果展示为平均值±sem(n=3)。发明详述先前已经表明若干种标志物与肺癌包括非小细胞肺癌(nsclc)及其亚型腺癌(ac)和鳞状细胞癌(scc)相关。提出用于肺癌的诊断中的若干种标志物在表1中列出。本发明解决了对于用于诊断nsclc,特别是用于区分nsclc亚型scc和nsclc亚型ac的精确和有效的方法的持续需求,这使得能够基于诊断为每种疾病亚型选择适当的治疗。nsclc的诊断和nsclc亚型scc和ac的区分基于在癌性肺组织中与健康组织中相比和在scc癌性组织中与ac癌性组织中相比的蛋白和/或编码所述蛋白的rna的差异表达。诊断可以通过测量本文描述的一种或更多种生物标志物评估。正确的诊断,特别是nsclc亚型的精确诊断,使得能够选择和开始适合于疾病亚型的治疗干预或治疗方案,以延迟、降低或治疗受试者的疾病。本发明的诊断方法还可以提供癌性疾病和/或其亚型的早期诊断。早期诊断对增加患者的生命预期具有高度重要性。与从怀疑具有nsclc的受试者获得的样品中本发明的一种或更多种生物标志物的表达水平比较的对照样品是从健康受试者或从怀疑具有肺癌或受肺癌影响的受试者的健康组织获取的样品。对照参考值还基于从健康受试者或健康组织,或从已经被诊断为具有nsclc、nsclc亚型ac或nsclc亚型scc的受试者获取的样品。通常地,对照参考值是代表多于一个样品中每一种生物标志物的表达水平的平均值或另一种统计度量。对照和癌性水平和截止点可以基于生物标志物是单独使用还是在与其他生物标志物组合成一个指标或更多个指标的公式(formulae)中被使用而变化。可选地,正常或异常癌性水平可以是来自先前测试的发展或未发展nsclc、nsclc亚型ac或nsclc亚型scc的受试者的生物标志物模式或“特征(signature)”的数据库。一个或更多个临床参数可以与本发明的生物标志物组合使用,作为公式的输入或作为定义待使用特定生物标志物组(panel)和公式测量的相关群体的预先选择的标准。临床参数还可以是可用于生物标志物归一化和预处理,或生物标志物选择、公式类型选择和推导,和公式结果后处理的。表1:被提出用于诊断肺癌的生物标志物标志物2至6是用于指导靶向的疗法的预测性标志物,并且标志物11-14用于临床中诊断ac或scc。定义如本文使用的,术语“生物标志物”是指从具有nsclc的受试者获取的样品中与从健康受试者获取的样品中相比,或从具有nsclc亚型scc的受试者获取的样品中与具有nsclc亚型ac的受试者获取的样品中或与健康受试者获取的样品中相比,或从具有nsclc亚型ac的受试者获取的样品中与具有nsclc亚型scc的受试者获取的样品中或与健康受试者获取的样品中相比,差异表达的蛋白或基因(特别是rna,更特别是mrna)。如本文使用的,术语“诊断”意指评估受试者是否患有nsclc,和/或受试者是否患有nsclc亚型scc或nsclc亚型ac。如本领域技术人员将理解的,这样的评估通常不意图于对于所有(即100%)的待鉴定的受试者都是正确的。然而,该术语要求可以鉴定出统计学上显著部分的受试者。在一些实施方案中,术语诊断还指筛查(screening)。在一些实施方案中,用于癌症的筛查可以导致特定病例中的更早期诊断,并且诊断正确的疾病亚型可以导致适当的治疗。如本文使用的,术语“水平”是指生物样品中基因产物表达的程度。如本文提及的,术语“治疗”涉及改善与疾病相关的症状,和减轻严重程度或治愈疾病。术语“受试者”是指任何哺乳动物受试者。在一些实施方案中,受试者是人类受试者。如本文使用的,术语“患者”是指被诊断为具有nsclc、nsclc亚型ac和nsclc亚型ac的受试者。如本文使用的,术语“生物样品”是指从受试者获得的样品。根据某些典型的实施方案,样品是体内或体外获得的生物组织。生物样品可以是但不限于从受试者/患者分离的选自血液、血浆、血清的体液,器官,组织,级分和细胞。生物样品还可以包括生物样品(包括组织)的切片(例如,器官或组织的切片部分)。生物样品可以分散于溶液中,或可以固定于固体支持物上,诸如印迹、测定、阵列、载玻片、微量滴定或elisa板中。根据一个方面,本发明提供了一种用于在怀疑具有非小细胞肺癌(nsclc)的受试者中诊断选自腺癌(ac)和鳞状细胞癌(scc)的nsclc的亚型的方法,该方法包括:(a)确定从受试者获得的生物样品中选自蛋白和编码所述蛋白的mrna的至少一种生物标志物的表达水平,其中至少一种生物标志物选自由以下组成的组:hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3、smc2、acad8、rsu1、acot1、hyou1、gale、itga7、tsg101和rab34;(b)将至少一种生物标志物的表达水平与健康生物样品中所述至少一种生物标志物的表达水平和/或代表健康生物样品的参考值比较;任选地(c)计算从受试者获得的样品中所述至少一种生物标志物的表达水平与健康样品中的表达水平和/或参考值的倍数变化;和(d)诊断所述受试者,其中-与所述健康生物样品中的表达水平和/或参考值相比,从所述受试者获得的所述样品中选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和smc2组成的组的至少一种生物标志物的升高的表达水平,和/或选自由acad8、rsu1、acot1、hyou1和gale组成的组的至少一种生物标志物的降低的表达,指示所述受试者具有nsclc亚型scc;与所述健康生物样品中的表达水平和/或参考值相比,从所述受试者获得的所述样品中选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和smc2组成的组的至少一种生物标志物的降低的表达水平,和/或选自由acad8、rsu1、acot1、hyou1和gale组成的组的至少一种生物标志物的升高的表达,指示所述受试者具有nsclc亚型ac;生物标志物itga7与参考值相比相等或升高的倍数变化指示受试者具有nsclc亚型scc,其中参考值来源于从scc患者获得的多于一个样品中所述itga7生物标志物的表达与在多于一个健康生物样品中的表达相比的倍数变化;生物标志物tsg101与参考值相比相等或升高的倍数变化指示受试者具有nsclc亚型ac,其中参考值来源于从ac患者获得的多于一个癌性样品中所述tsg101生物标志物的表达与在多于一个健康生物样品中的表达相比的倍数变化;生物标志物rab34与参考值相比相等或降低的倍数变化指示受试者具有nsclc亚型ac,其中参考值来源于从ac患者获得的多于一个癌性样品中所述rab34生物标志物的表达与多于一个健康生物样品相比的倍数变化。根据某些实施方案,hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3、smc2、acad8、rsu1、acot1、hyou1、gale、itga7、tsg101和rab34生物标志物的每一个是蛋白生物标志物。根据某些实施方案,hat1、akr1b10、wdr82、ttl12、igf2bp3、smc2、acad8、rsu1、acot1、hyou1、gale、itga7、tsg101和rab34生物标志物的每一个是rna生物标志物。根据又另外的方面,本发明提供了一种用于诊断怀疑具有nsclc的受试者的nsclc的亚型的方法,所述选自nsclc的亚型选自由scc和ac组成的组的,该方法包括确定从受试者获得的包含细胞的样品中smac/diablo蛋白的存在,其中当显著量的smac/diablo蛋白存在于细胞核和细胞胞质溶胶中时,将所述受试者诊断为具有nsclc亚型scc,并且当无显著量的所述smac/diablo蛋白存在于细胞核中并且显著量的所述smac/diablo蛋白存在于胞质溶胶中时,将所述受试者诊断为具有nsclc亚型ac。根据又其他方面,本发明提供了一种用于在受试者中诊断nsclc的方法,该方法包括:(a)将受试者的生物样品中至少一种蛋白生物标志物或编码该蛋白的mrna的表达水平与参考值或对照样品比较,其中所述至少一种生物标志物选自由apool、vps29、caf17以及其任何组合组成的组;(b)在至少一种生物标志物或其组合的表达水平与参考值或对照样品相比增加的情况下,将受试者诊断为具有nsclc。根据某些实施方案,方法还包括比较选自表2中展示的组的至少一种另外的生物标志物或编码至少一种另外的生物标志物的mrna的表达水平。表2:nsclc生物标志物癌症生物标志物的鉴定是一个快速扩展的领域,而深度测序方法已经变得被广泛公认为检测和分析癌症生物标志物的手段。在同时,其他癌症相关的变化并不简单地反映为基因中的突变,而是反映为标志物蛋白的增加或减少的表达或翻译后修饰的变化,如一些癌症中报道的。本发明将nsclc中的代谢、凋亡和其他蛋白的表达水平的改变鉴定为用于可以允许更好地诊断nsclc并且甚至早期诊断nsclc的高灵敏平台的潜在手段。最重要地,本发明现在公开了允许区分ac和scc亚型的蛋白,其对于精确诊断和选择治疗是至关重要的,特别是在不清楚的病例中。nsclc中代谢相关的蛋白的过表达-潜在生物标志物本发明的发明人先前已经显示,线粒体门控蛋白(gatekeeperprotein)vdac1的水平与健康组织相比在不同的癌症类型中基本上更高(wo2013/035095)。因此,还检查了它在nsclc中的过表达(图2、图4a和图4b和图5a)。先前地,据报道在nsclc中vdac1基因表达水平增加,这伴随不良的结果。作为离子、ca2+、atp和其他代谢物跨越线粒体外膜的主要转运体,vdac1过表达可以向高能量需求的癌细胞提供许多优势。事实上,癌症发展对于vdac1的需求通过使用特异性sirna使癌细胞中的vdac1表达沉默导致在体外和体内二者中癌细胞增殖的明显抑制来证明。在本文也显示出在nsclc中过表达的其他代谢相关蛋白,包括糖酵解酶pgk1、ldha、gapdh、eno1和氧化磷酸化(oxphos)蛋白atp5b(图3c、表6)。这些之中,pgk1在本文中显示出与nsclc相关。线粒体易位的pgk1作为蛋白激酶起作用,在肿瘤发生中协调糖酵解和tc循环,并且作为二硫化物还原酶在肿瘤血管生成中起作用。pgk1由缺氧和egfr信号传导二者活化,并且先前被发现在脑肿瘤生成(lix等人molcell2016;61:705-19)和肿瘤血管生成(layaj等人nature.2000;408:869-73)中起作用。ldha在若干种癌症类型包括nsclc中过表达(miaop等人iubmblife.2013;65:904-10)。gapdh和eno1表达或多态性与nsclc中的不良预后相关(puzoner等人molcancer.2013;12:97;leesy等人scirep.2016;6:35603)。最后,f1f0atp合成酶的组成部分atp5b被鉴定为nsclc肿瘤细胞膜抗原(luzj等人bmccancer2009;9:16)。有趣地,网络分析证明,大多数这些蛋白是通过直接的物理相互作用或共表达关联的,并且一些是由受表观遗传修饰调控的基因簇编码的。最明显的是与细胞代谢过程相关的一组蛋白。更进一步地,该簇包括与oxphos相关的atp5b和vdac1(线粒体的门控),表明oxphos和糖酵解(癌细胞能量体内稳态(warburg效应)的重要因素)之间的偶联。这些结果指出nsclc中和其他癌症中重编程的代谢的重要性,并且列出的蛋白可以用作生物标志物。促凋亡蛋白smac/diablo和aif在nsclc中的表达smac/diablo(第二种线粒体来源的胱天蛋白酶的活化物,在本文中也被称为“smac”)和aif(凋亡诱导因子)通常位于线粒体膜间空间,并且在凋亡信号后释放到胞质溶胶(kroemerg等人physiolrev2007;87:99-163)。未预期地,尽管smac和aif具有促凋亡功能,但发现它们在nsclc中与健康肺组织相比过表达(图2、图4和图6)。smac,作为一种促凋亡蛋白,在凋亡期间从线粒体释放,并且对抗凋亡蛋白抑制物(iap)的抑制活性,因此释放它们结合的胱天蛋白酶。发现smac在一些癌症和肉瘤中过表达,但在其他癌症中显示出降低的表达水平。许多癌症中观察到的增加的smac表达水平与它的促凋亡活性之间的这种矛盾可能由smac的另一种未鉴定出的功能导致(paul,a等人mol.therapy2018;26(3):680-694)。aif在nsclc中也过表达(图2)。在细胞凋亡诱导后释放到胞质溶胶的aif易位到核,在核中它引发染色质浓缩和dna降解。作为一种促凋亡蛋白,尚不清楚为什么aif在癌细胞中过表达。然而,aif已经成为对于细胞生存而言至关重要的蛋白,因为小鼠中纯合aif敲除是胚胎致死的。提出了aif的促生存活性与氧化磷酸化、ros解毒(detoxification)、氧化还原传感(redox-sensing)、线粒体形态学和细胞周期调控相关。因此,在一些癌症中aif过表达可能通过这些另外的功能向癌细胞提供了优势。未预期地,本发明证明了smac/diablo的细胞定位,不仅在线粒体中被发现并且在核中被发现,特别是在scc样品的核中被发现(图6)。因此,核中smac/diablo的存在可能是关于scc的一个清楚的特征。在nsclc中表达改变的蛋白作为潜在生物标志物对来自相同的肺的健康组织和nsclc组织的蛋白质组学(lc-hrms/ms)分析揭示了癌症中高度表达的若干种蛋白,其中的一些蛋白先前被报道与其他癌症相关并且其他蛋白本身在本文第一次被报道(图1、图3、表6)。这些蛋白覆盖了一定范围的功能类别,诸如肿瘤抑制物、蛋白酶抑制物、结构蛋白、rna结合因子、免疫受体的信号传导、线粒体肽跨膜转运的协调物、脂质或半乳糖代谢或作为蛋白激酶起作用。rab11b蛋白在肿瘤组织中过表达(~8000倍),但在所有测试的样品中,几乎不存在于健康肺组织中(图3、表6)。rab11家族(rab11a、rab11b和rab25)与回收内体相关,并且rab25先前被报道与癌症相关(chengkw等人natmed,2004;10:1251-6)。已经表明癌症中的囊泡转运调控肿瘤侵袭(steffanjj等人plosone2014;9:e87882)。hyou1,也被称为hsp12a、grp170或orp150,在肺癌组织中过表达(~60倍)(图3、表6)。提出hyou1在er中的蛋白折叠和分泌中起重要作用,并且对缺氧诱导的细胞扰动(cellularperturbation)中的细胞保护有贡献(ozawak等人jbiolchem1999;274:6397-404)。hyou1显示出在乳腺癌和鼻咽癌中上调,并且与肿瘤侵袭性和不良预后相关。它还显示出在nsclc中过表达(bc,romw等人clinproteomics.2016;13:31)。发现egfr和mek1在肿瘤中与健康肺组织相比过表达(表6)。具有突变的蛋白形式的参与的egfr-ras-mapk途径的过度活化是肺癌中最通常的改变(campbell等人2016,同上;paezjg等人science2004;304:1497-500;mitsudomit等人cancersci2007;98:1817-24)。因此,许多这些蛋白可以用作nsclc生物标志物。用于scc和ac诊断的生物标志物nsclc的两种主要亚型ac和scc显示出在基因组、表观基因组、转录组和蛋白组内的突变的差异(campbell等人,2016,同上)。甲状腺转录因子-1(ttf-1)目前被用于临床中以区分ac和scc(fujitaj等人lungcancer2003;39:31-6)。尽管如此,区分这两种nsclc亚型仍然是挑战性的(zakowskimf等人archpathollabmed2016;140:1116-20)。精确的诊断对于选择适当的治疗并且因此增加患者的生命预期是基本的。本发明公开了新鉴定的允许区分ac和scc的蛋白,并且还确定了若干种先前报道的蛋白的差异表达(表7和10)。与来自健康组织的样品相比,hat1、lrrfip2、akr1b10、wdr82、ttll12、igf2bp3和smc2的表达在nsclc亚型scc中上调并且在nsclc亚型ac中下调。acad8、rsu1、acot1、hyou1和gale的表达水平在nsclc亚型ac中上调,而它在nsclc亚型scc中下调。itga7的表达水平在scc和ac亚型二者中上调,但在scc中具有显著地更明显的上调。对于已知在nsclc中过表达的usp14,显示出相同的模式。在另一方面,tsg10的表达虽然在两种亚型中也上调,但在ac中与scc相比显著更高。rab34的表达水平在ac和scc二者中与健康对照相比下调,但在ac中与scc相比降低显著地更低。akr1b10先前已经被报道为对吸烟者的nsclc特异性的潜在诊断标志物;tsg101显示出参与肺癌细胞增殖,并且igf2bp3被报道在多种类型的癌症包括nsclc中过表达。已经提出若干种蛋白与癌症相关但不与nsclc相关。ttl12和hat1先前被报道分别与前列腺癌或淋巴瘤和食管鳞状细胞癌进展相关(表7)。itga7已经显示出与膀胱癌的出现和发展相关。rab34已经被报道为胶质瘤和ras相关的肉瘤发生中与进展和预后相关的生物标志物。lrrfip2、wdr82、acot1、smc2、acad8、gale和rsu1先前未被鉴定为用于任何类型的癌症的可能生物标志物(图4b、表7)。最后,若干种这些蛋白的表达水平影响了ac患者生存,但对scc生存不具有影响(表9)。如本文证明的,基于如由lc-hrms/ms揭示的在ac和scc中它们的差异表达水平(图4b)选择的蛋白通常显示出在scc和ac中的差异rna水平(图5a)。进行进一步分析rnasequcscxena数据,选择编码显示出在ac和scc中的差异表达水平(lc-hrms/ms数据)的蛋白的基因。编码与多种功能相关的蛋白的mrna水平在ac和scc中变化(3-60倍)(图5b)。该分析确定了表明tp63和ck5、ck13、ck14、ck17、csta和ptn2作为用于scc的生物标志物的先前的报道。akr7a3和acad8在本文第一次被鉴定为在ac中相对于在scc中的它们的表达水平过表达(2-6倍)(图5b)。基因,诸如npc2(niemann-pick病,c2型)(一种分泌型蛋白)和arrb1先前被报道为用于肺ac的生物标志物并且在本文被确定(表8和10)。在ac中相对于scc高度表达的另一组有趣的基因是与脂肪酸/脂质代谢和转运相关的那些基因。先前报道与ac相关的是azgp1(锌-α2-糖蛋白)(albertusdl等人jthoraconcol2008;3:1236-44),一种刺激脂肪细胞中的脂质降解并且导致与一些晚期癌症相关的大量脂肪损失的分泌型蛋白(bingc等人procnatlacadsciusa2004;101:2500-5)。acot1(酰基-coa硫酯酶1),一种为过氧化物酶体脂质代谢的调控物的分泌型蛋白(huntmc等人jbiolchem2002;277:1128-38)和acad8(异丁酰基-coa脱氢酶),一种在脂肪酸或支链氨基酸诸如缬氨酸的代谢中催化酰基-coa衍生物的脱氢的线粒体蛋白(battailekp等人jbiolchem2004;279:16526-34),在本文中第一次被报道为用于nsclc亚型ac的标志物。在这个方面中,ac主要起源于2型肺泡(at2)细胞,而脂质代谢系统是与这些细胞相关的表面活性物质产生的一部分。总的来说,基于在本文第一次鉴定出的或在先前的报道中并且在本文确定的蛋白/mrna在ac或scc中的表达水平(倍数变化)、特异性表达,我们提出在scc和ac中差异表达的蛋白的列表,其中四种是可以被用于清楚地区分scc或ac的分泌型蛋白(表7、8和10)。这对于指导这两种nsclc亚型的适当的治疗具有高度重要性。总之,本发明鉴定出若干种蛋白,其表达水平在肺癌患者中高度增加。此外,这些生物标志物的一些可以被用作使得能够区分ac和scc的分析平台(profilingplatform)。这些分子的使用可以促进精确诊断和预后预测并且可以对个体化肺癌治疗有贡献。最后,搜索靶向nsclc亚型ac和nsclc亚型scc中差异表达的生物标志物的药物可能导致用于每一种肺癌亚型的新的特异性治疗。测量表达水平的方法将本发明的生物标志物的表达水平与它在对照样品中的表达或与参考值比较包括测量和确定生物标志物在生物样品中的表达水平。根据本发明的教导,可以使用本领域技术人员已知的用于检测标志物表达的任何方法。在一些实施方案中,表达水平可以通过本领域已知的蛋白质组学分析方法测量。蛋白质组学是鉴定和定量蛋白,或细胞和组织中表达的蛋白的量的比率的实践。本领域技术人员将熟悉许多特异性免疫测定形式及其变化形式,其可以是可用于实施本文公开的方法的,包括酶联免疫吸附测定(elisa)、酶联免疫斑点测定(elispot)、lc-hrms/ms分析、放射免疫测定(ria)、放射免疫沉淀测定(ripa)、免疫珠捕获测定、蛋白印迹、斑点印迹、凝胶迁移测定(gel-shiftassay)、流式细胞术、免疫组织化学(ihc)、荧光显微术、蛋白阵列、多重珠阵列、磁捕获和体内成像。通常参见e.maggio,enzyme-immunoassay,(1980)(crcpress,inc.,bocaraton,fla.)。“免疫测定”是一种使用与抗原特异性结合的抗体的测定。免疫测定的特征在于使用特定抗体的特异性结合特性以分离、靶向和/或定量抗原。当提及蛋白或肽(或其他表位)时,短语“与抗体特异性(或选择性)结合”或“与…特异性(或选择性)免疫反应”或“特异性相互作用或结合”,是指在一些实施方案中确定蛋白和其他生物制品的异质群体中的蛋白的存在的结合反应。因此,在指定的免疫测定条件下,特异性的抗体与特定蛋白结合比背景(非特异性信号)大至少两倍,并且基本上不以显著量与存在于样品中的其他蛋白结合。在这样的条件下与抗体的特异性结合可能需要选择其对特定蛋白特异性的抗体。例如,可以选择针对来自特定物种诸如大鼠、小鼠或人类的肺特异性蛋白产生(raise)的多克隆抗体,以仅获得与肺特异性蛋白特异性免疫反应并且不与除了肺特异性蛋白的多态变体(polymorphicvariant)和等位物(allele)之外的其他蛋白特异性免疫反应的那些多克隆抗体。这种选择可以通过减去与来自其他物种的肺特异性蛋白分子交叉反应的抗体来实现。多种免疫测定形式可以被用于选择与特定蛋白特异性免疫反应的抗体。例如,固相elisa免疫测定被常规用于选择与蛋白特异性免疫反应的抗体(关于可以被用于确定特异性免疫反应性的免疫测定形式和条件的描述,参见,例如,harlow&lane,antibodies,alaboratorymanual(1988))。通常地,特异性或选择性反应将是背景信号或噪声的至少两倍,并且更通常地是背景信号的多于10倍至100倍。在一些实施方案中,生物标志物的水平通过将生物样品与特异性抗体接触来测量。特异性抗体可以是例如多克隆抗体、单克隆抗体、嵌合抗体、人类抗体、亲和成熟抗体或抗体片段。虽然单克隆抗体对标志物/抗原高度特异性,但多克隆抗体可以优选地被用作捕获抗体以尽可能多地固定标志物/抗原。多克隆抗体通过将免疫原注射(例如,皮下或肌肉内注射)到合适的非人类哺乳动物(例如,小鼠或兔)中产生。通常地,免疫原应当诱导产生对靶抗原具有相对高亲和力的高滴度的抗体。如果期望,标志物可以通过本领域熟知的缀合技术缀合到载体蛋白。通常使用的载体包括匙孔虫戚血蓝蛋白(keyholelimpethemocyanin)(klh)、甲状腺球蛋白、牛血清白蛋白(bsa)和破伤风类毒素。然后将缀合物用于免疫动物。抗体然后从从动物获取的血液样品获得。文献中广泛描述了用于产生多克隆抗体的技术(参见,例如,methodsofenzymology,"productionofantiserawithsmalldosesofimmunogen:multipleintradermalinjections,"langone等人eds.(acad.press,1981))。由动物产生的多克隆抗体可以进一步被纯化,例如,通过与靶抗原结合的基质结合并且从与靶抗原结合的基质洗脱。本领域技术人员将知道通常在免疫学领域中用于多克隆抗体以及单克隆抗体的纯化和/或浓缩的多种技术。单克隆抗体(mab)可以通过使用熟知的技术容易地制备,诸如美国专利第4,196,265号中举例说明的那些。通常地,该技术包括用选择的免疫原组合物、多肽或肽免疫合适的动物。免疫组合物以有效刺激产生抗体的细胞的方式被施用。啮齿动物诸如小鼠和大鼠是优选的动物,然而,使用兔、绵羊或青蛙细胞也是可能的。使用大鼠可以提供某些优势,但小鼠是优选的,而balb/c小鼠是最优选的,因为这是最常规使用的并且通常给出更高百分比的稳定融合物。抗体可以根据已知技术,诸如被动结合,缀合到适用于诊断测定的固体支持物(例如,珠诸如蛋白a或蛋白g琼脂糖、微球、板、载玻片或由诸如乳胶或聚苯乙烯的材料形成的孔)。如本文描述的抗体同样可以根据已知技术与可检测的标记物(label)或基团诸如放射性标记物(例如,35s、125i、131i)、酶标记物(例如,辣根过氧化物酶、碱性磷酸酶)和荧光标记物(例如,荧光素、alexa、绿色荧光蛋白、罗丹明(rhodamine))缀合。免疫组织化学染色也可以被用于测量一种生物标志物或多于一种生物标志物的差异表达。该方法使得能够通过蛋白与特异性抗体的相互作用定位组织切片的细胞中的蛋白。为此,组织可以被固定在甲醛或其他合适的固定剂中,包埋在蜡或塑料中,并且使用切片机(microtome)切割成薄的切片(从约0.1mm至若干mm厚)。可选地,组织可以使用低温恒温器(cryostat)冷冻并且切割成薄的切片。组织的切片可以被排列到并且附着(affix)到固体表面上(即,组织微阵列)。将组织的切片与针对感兴趣的抗原的一级抗体孵育,随后洗涤以去除未结合的抗体。一级抗体可以与检测系统偶联,或一级抗体可以用与检测系统偶联的二级抗体检测。检测系统可以是荧光团或它可以是如上文描述的酶。染色的组织切片通常在显微镜下扫描。因为来自具有癌症的受试者的组织的样品可能是异质的,即一些细胞可能是正常的并且其他细胞可能是癌性的,所以可以确定组织中阳性染色细胞的百分比。这种测量,随染色的强度的定量一起,可以被用于产生关于生物标志物的表达值。根据某些实施方案,生物标志物表达通过ihc测量。在一些实施方案中,生物标志物的水平通过蛋白质组学分析测量。根据某些实施方案,生物标志物表达通过lc-ms/ms测量。核酸测试(nat)测定根据一些实施方案,本发明的方法包括比较和/或检测基因的表达水平。生物样品中感兴趣的核酸的检测可以通过基于nat的测定来实现,其包括核酸扩增技术,诸如pcr或其变化形式,例如实时pcr、定量pcr(qpcr)等。选择的或靶核酸序列的扩增可以通过多种合适的方法实施。许多扩增技术已经被描述并且可以容易地被改变以适合普通技术人员的特定需要。扩增技术的非限制性实例包括聚合酶链式反应(pcr)、连接酶链式反应(lcr)、链置换扩增(sda)、基于转录的扩增、q3复制酶系统以及基于核酸序列的扩增(nasba)。定量实时pcr(qrt-pcr)可以被用于测量一种标志物或多于一种生物标志物的差异表达。在qrt-pcr中,rna模板通常被逆转录成cdna,其然后通过pcr反应扩增。实时逐循环追踪pcr产物的量,这允许确定mrna的初始浓度。为了测量pcr产物的量,反应可以在与双链dna结合的荧光染料诸如sybrgreen的存在下进行。反应还可以用对正被扩增的dna特异性的荧光报告物探针进行。荧光报告物探针的非限制性实例是taqmantm探针(appliedbiosystems,fostercity,ca)。当在pcr延伸循环期间猝灭剂被去除时,荧光报告物探针发出荧光。多重qrt-pcr可以通过使用多种基因特异性报告物探针进行,其每一种包含不同的荧光团。荧光值在每一个循环期间被记录并且代表扩增反应中扩增到该点的产物的量。为了最小化误差并且降低样品之间的任何变化,qrt-pcr通常使用参考标准进行。理想的参考标准在不同的组织中以恒定水平表达,并且不受实验处理影响。合适的参考标准包括但不限于持家基因甘油醛-3-磷酸-脱氢酶(gapdh)和β-肌动蛋白的mrna。起始样品中的mrna的水平或每一种生物标志物的表达的倍数变化可以使用本领域熟知的计算来确定。核酸微阵列可以被用于定量多于一种生物标志物的差异表达。微阵列分析可以使用商购可得的设备、遵循制造商的方案进行。通常地,单链核酸(例如,cdna或寡核苷酸)被铺板或排列在微芯片基底上。然后排列的序列与来自感兴趣的细胞的特异性核酸探针杂交。荧光标记的cdna探针可以通过由从感兴趣的细胞提取的rna的逆转录掺入荧光标记的脱氧核苷酸来产生。可选地,rna可以通过体外转录扩增并且用标志物诸如生物素标记。然后标记的探针在高度严格的条件下与微芯片上固定的核酸杂交。在严格洗涤以去除非特异性结合的探针后,芯片通过共焦激光显微术或通过另一种检测方法诸如ccd照相机扫描。杂交文件中的原始荧光强度数据通常用稳健的多芯片平均(rma)算法预处理以产生表达值。原位杂交也可以被用于测量多于一种生物标志物的差异表达。该方法允许定位组织切片的细胞中感兴趣的mrna。对于该方法,组织可以被冷冻,或固定并且包埋,并且然后切割成薄的切片,其被排列并且附着在固体表面上。组织切片与将与感兴趣的mrna杂交的标记的反义探针孵育。杂交和洗涤步骤通常在高度严格的条件下进行。探针可以用荧光团或可以被另一种蛋白或抗体检测的小标签(tag)(诸如生物素或地高辛(digoxigenin))标记,使得标记的杂交体可以在显微镜下被检测和可视化。多种mrna可以同时被检测,条件是每一种反义探针具有可区分的标记物。杂交的组织阵列通常在显微镜下扫描。因为来自具有癌症的受试者的组织的样品可能是异质的,即一些细胞可能是正常的并且其他细胞可能是癌性的,所以可以确定组织中阳性染色的细胞的百分比。这种测量,随染色的强度的定量一起,可以被用于产生关于每一种生物标志物的表达值。试剂盒在一些实施方案中,本发明提供了成品(articleofmanufacture),例如,试剂盒,诸如fda批准的试剂盒,其包含诊断或预后试剂和使用说明。在一些实施方案中,试剂盒适于在容器上以监管机构关于药物的生产、使用或销售的规定的形式附上公告,该公告反映了组合物的形式或人类用途被该机构批准。根据某些方面,本发明提供了一种用于诊断从怀疑具有非小细胞肺癌(nsclc)的受试者获得的生物样品中选自腺癌(ac)和鳞状细胞癌(scc)的nsclc的亚型的试剂盒,该试剂盒包含:(a)至少一种剂,所述至少一种剂能够检测选自蛋白和编码该蛋白的mrna的至少一种生物标志物的表达水平,该生物标志物选自由以下组成的组:hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3、smc2、acad8、rsu1、acot1、hyou1、gale、itga7、tsg101和rab34;(b)工具,所述工具用于将至少一种生物标志物的表达水平与第一参考值和/或与第二参考值和/或与第三参考值比较,所述第一参考值来源于健康生物样品中至少一种生物标志物的表达,所述第二参考值来源于从scc患者获得的多于一个样品中所述至少一种生物标志物的表达与多于一个健康生物样品中的表达相比的倍数变化,所述第三参考值来源于从ac患者获得的多于一个样品中至少一种生物标志物的表达与多于一个健康生物样品相比的倍数变化;(c)说明材料,所述说明材料提供对所述至少一种生物标志物的所述表达水平与nsclc亚型的相关性的指导,其中:与第一参考值相比,所述样品中选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和smc2组成的组的至少一种生物标志物的增加的表达水平,和/或选自由acad8、rsu1、acot1、hyou1和gale组成的组的至少一种生物标志物的降低的表达,指示所述受试者具有nsclc亚型scc;与第一参考值相比,样品中选自由hat1、lrrfip2、akr1b10、wdr82、ttl12、igf2bp3和smc2组成的组的至少一种生物标志物的降低的表达水平,和/或选自由acad8、rsu1、acot1、hyou1和gale组成的组的至少一种生物标志物的升高的表达,指示所述受试者具有nsclc亚型ac;生物标志物tga7与第二参考值相比相等或升高的倍数变化指示受试者具有nsclc亚型scc;生物标志物tsg101与第三参考值相比相等或升高的倍数变化指示受试者具有nsclc亚型ac;和/或生物标志物rab34与第三参考值相比相等或降低的倍数变化指示受试者具有nsclc亚型ac。根据某些实施方案,试剂盒还包含能够检测存在于生物样品中的细胞核内smac/diablo蛋白的表达的至少一种剂和提供对细胞核和胞质溶胶内smac/diablo的量与nsclc亚型的相关性的指导的说明材料,其中细胞核和胞质溶胶中显著量的smac/diablo蛋白将受试者诊断为具有nsclc亚型scc,并且细胞核中无显著量的所述smac/diablo蛋白而胞质溶胶中存在显著量的所述smac/diablo蛋白将受试者诊断为具有nsclc亚型ac。根据某些另外的方面,本发明提供了一种用于诊断nsclc的试剂盒,该试剂盒包含:(a)至少一种剂,所述至少一种剂能够检测怀疑具有nsclc的受试者的生物样品中选自蛋白和编码所述蛋白的mrna的至少一种生物标志物的表达水平,该生物标志物选自由apool、vps29和caf17组成的组;(b)工具,所述工具用于将至少一种生物标志物的表达水平与从健康受试者获得的对照样品或与参考值比较;和(c)说明材料,所述说明材料提供对所述至少一种生物标志物的表达水平与对照样品或与参考值相比的增加与nsclc的相关性的指导。根据本发明的教导,试剂盒可以包括抗体、蛋白阵列、用于免疫测定中使用的试剂、蛋白对照、rna阵列、用于基于nat的测定中使用的试剂、除指导说明材料之外的说明页、基因表达数据库和/或用于确定和分析蛋白或rna生物标志物的表达水平的任何工具。治疗nsclc、nsclc亚型ac和nsclc亚型ac的方法本发明的诊断方法还可以包括根据诊断治疗受试者,并且本发明还提供了治疗具有nsclc、nsclc亚型ac或nsclc亚型scc的受试者的方法。这些方法牵涉的原理是向受试者施用降低在这些疾病的每一种中高度表达的蛋白的表达或活性的剂。根据某些方面,本发明提供了用于在治疗nsclc亚型scc中使用的降低至少一种蛋白的表达或活性的剂,所述蛋白选自由以下组成的组:hat1、lrrfip2、akr1b10、wdr82、ttll12、itga7、igf2bp3和usp14。根据某些另外的方面,本发明提供了用于在治疗nsclc亚型ac中使用的降低至少一种蛋白的表达或活性的剂,所述蛋白选自由acad8、tsg101和gale组成的组。根据又其他方面,本发明提供了用于在治疗nsclc中使用的降低至少一种蛋白的表达或活性的剂,所述蛋白选自由apool、vps29和caf17组成的组。根据一些实施方案,降低至少一种蛋白的表达或活性的剂选自由化学剂或部分、蛋白、肽和多核苷酸分子组成的组。根据一些实施方案,剂是抗体。用于制备与感兴趣的蛋白特异性结合的抗体的方法是本领域已知的并且在上文中描述。根据一些实施方案,剂是干扰rna(rnai)分子。在某些实施方案中,干扰rna分子选自由shrna、sirna和mirna组成的组。在某些方面中,本发明的干扰rna具有约19个至约49个核苷酸的长度。在其他方面中,干扰rna包括有义核苷酸链和反义核苷酸链。rna干扰(rnai)是双链rna(dsrna)被用于使基因表达沉默的过程。虽然不希望被任何理论或作用机制所束缚,rnai开始于由rna酶iii样酶dicer将较长的dsrna裂解成小干扰rna(sirna)。sirna是长度通常约19个至28个核苷酸,或20个至25个核苷酸,或21个至22个核苷酸的dsrna,并且通常包含2-核苷酸3’突出端和5’磷酸末端和3’羟基末端。sirna的一条链被掺入到被称为rna诱导的沉默复合物(risc)的核糖核蛋白复合物中。risc使用这一sirna链以鉴定与掺入的sirna链至少部分互补的mrna分子,并且然后裂解这些靶mrna或抑制它们的翻译。因此,掺入到risc中的sirna链被称为指导链(guidestrand)或反义链。另一条sirna链,被称为过客链(passengerstrand)或有义链,从sirna消除并且与靶mrna至少部分同源。本领域技术人员将认识到,原则上,sirna分子的任一条链可以被掺入到risc中并且作为指导链起作用。然而,sirna设计(例如,在期望的指导链的5’末端处减少的sirna双链体稳定性)可以有利于将期望的指导链掺入到risc中。sirna的反义链是sirna的主动指导物,因为反义链被掺入到risc中,因此允许risc鉴定与反义sirna链至少部分互补的靶mrna用于裂解或翻译抑制。risc介导裂解具有与指导链至少部分互补的序列的mrna导致该mrna和由该mrna编码的相应的蛋白的稳定状态水平的减少。可选地,risc还可以通过翻译抑制而不是裂解靶mrna来减少相应的蛋白的表达。本发明的干扰rna表现出以催化方式起作用,用于靶mrna的裂解,即干扰rna能够以亚化学计量的量实现靶mrna的抑制。如与反义疗法相比,要求显著更少的干扰rna以提供在这样的裂解条件下的治疗效果。适当的寡核苷酸的选择通过使用自动比对核酸序列并且指示同一性或同源性的区域的计算机程序来促进。这样的程序被用于比较例如通过搜索数据库诸如genbank或通过将pcr产物测序获得的核酸序列。来自一系列物种的核酸序列的比较允许选择显示出物种之间适当程度的同一性的核酸序列。这些程序允许选择与待控制的受试者中的靶核酸序列展现高度的互补性并且与其他物种中的相应核酸序列展现较低程度的互补性的寡核苷酸。本领域技术人员将认识到,在选择用于在本发明中使用的基因的适当的区域中存在相当大的自由度。药物组合物本发明的剂可以本身或以其中它们与合适的载体或赋形剂混合的药物组合物向受试者施用。合适的药学上可接受的载体的实例可以包括水、盐水、pbs(磷酸盐缓冲盐水)、糊精、甘油和乙醇。药学上可接受的载体可以被配制成用于向人类受试者或患者施用。组合物可以被配制成可以在施用后以快速或持续或延迟的方式释放活性成分的剂型。根据一些实施方案,组合物包含干扰rna分子作为活性剂。干扰rna分子可以以本领域已知的多种方法施用。全身施用的rna由于它在水中的高溶解度和负电荷而被肾脏或肝脏快速清除。因此,根据一些实施方案,rna被封装。封装可能增强rna在身体中的循环时间并且防止由细胞外核酸酶降解。根据一些实施方案,药物组合物包含sirna组分和脂质组分。根据某些实施方案,干扰rna分子在脂质体内被施用。例如,wo2006113679提供了用于通过中性(不带电荷的)脂质体将rna干扰分子递送到细胞的方法。wo201011317描述了两性脂质体组合物用于将用于在rna干扰中使用的小rna分子细胞递送的用途。根据其他实施方案,干扰rna分子直接地或通过核酸递送系统被施用。系统可以包含稳定rna的化合物,诸如脂质或蛋白。例如,wo1995022618公开了包含具有靶部分和核酸结合部分的融合蛋白的递送系统。根据其他实施方案,根据本发明的教导,组合物包含对一种生物标志物特异性的至少一种抗体作为活性剂。向患者或受试者施用的本发明的组合物的实际剂量可以通过物理和生理学因素诸如体重、状况的严重程度、先前或同时的治疗干预以及施用的途径确定。负责施用的从业人员将确定组合物中一种或更多种活性成分的浓度和用于个体受试者的适当的一种或更多种剂量。展示以下实施例以更充分地说明本发明的一些实施方案。然而,它们绝不应当被解释为限制本发明的宽范围。本领域技术人员可以容易地设想本文公开的原理的许多变化形式和修改,而不背离本发明的范围。实施例材料和方法材料苯甲基磺酰氟(pmsf)、碘化丙锭(pi)和台盼蓝购自sigma(st.louis,mo)。dulbecco改良的eagle培养基(dmem)和补充剂胎牛血清、l-谷氨酰胺和青霉素-链霉素购自biologicalindustries(beithaemek,israel)。辣根过氧化物酶(hrp)-缀合的抗小鼠、抗兔和抗山羊抗体来自kpl(gaithersburg,md)。3,3-二氨基联苯胺(dab)从immpact-dab(burlingame,ca)获得。在免疫印迹和免疫组织化学(ihc)中使用的一级抗体以及它们的稀释度在表3中列出。表3:使用的抗体展示了针对指示的蛋白的抗体、它们的目录号、来源以及在ihc和免疫印迹实验(蛋白印迹,wb)中使用的稀释度。患者本研究中展示的所有研究在获得知情同意后并且根据由索罗卡大学医学中心的伦理委员会(ethicscommitteeofsorokauniversitymedicalcenter)批准的机构审查委员会方案进行。所有人类组织在具有每个受试者的理解和书面同意的情况下收集,并且研究方法学符合由赫尔辛基宣言(declarationofhelsinki)设置的标准。nsclc样本从2010年至2016年从在手术时不具有任何治疗而经历肺切除的46名患者获得。患者的主要临床和病理学变量在表4中提供。新鲜的成对的健康组织样本和癌症组织样本从经历全肺切除术(pneumonectomy)或肺叶切除术(pulmonarylobectomy)以去除肿瘤组织的相同的肺癌患者获得。将样本立即冷冻在液氮中并且维持在-80℃直到通过免疫印迹或qpcr分析。如下文描述的,从组织样品提取蛋白。癌症和肿瘤周围的正常肺组织由医院病理学家验证。28名患者为男性并且27名为女性,平均年龄为68岁(范围为36-86岁)。疾病阶段根据国际肿瘤-节点-转移系统(internationaltumor-node-metastasissystem)(tmm)划分阶段,并且然后分类为从隐匿性癌症到0阶段、ia阶段、ib阶段、iia阶段、iib阶段、iiia阶段、iiib阶段至iv阶段(i级,n=30)、(ii级,n=10)、(iii级,n=5)、(iv级,n=1)的范围。表4:肺癌患者特征病人编号年龄(岁)性别癌症的类型疾病的阶段176fac2b277mscc1a354mac3a458mscc2b570mscc2b669fac2a736mac3a862mac1a982mac2a1048mac1a1165fac1a1278mscc1b1372mac1a1478mac1a1555mac1a1659fscc1a1774fscc2a1865mscc41976mscc3a2065fscc1a2161mac1a2254mscc1b2356fac1a2458mac1a2555fac1a2676fac1a2785mac1b2855fac1a2962mac2a3079mac3a3181mac1a3262fac1b3383fscc1b3477mscc1a3586mscc1b3674mscc1b3774mac1a3867fac2a3971mac1a4075fac3a4185mscc1a4277mscc2a4359fscc2a4459fscc1b4558mac1b4668fac1a从肺组织提取蛋白为了提取用于免疫印迹的蛋白,将健康肺组织和肿瘤肺组织溶解在裂解缓冲液(50mmtris-hcl,ph7.5、150mmnacl、1mmedta、1.5mmmgcl2、10%甘油、1%tritonx-100、蛋白酶抑制剂混合物(calbiochem))中,随后是声波处理和离心(10min,600g)。每种裂解物的蛋白浓度使用lowry测定确定。如下文描述的,将样品储存在-80℃直到通过凝胶电泳和免疫印迹分析。为了提取用于lc-hrms/ms的蛋白,将健康肺组织和肿瘤肺组织溶解在不同的裂解缓冲液(100mmtris-hcl,ph8.0、5mmdtt、4%sds和蛋白酶抑制剂混合物(calbiochem;100μl/10mg))中,随后匀浆,在95℃孵育持续3min并且离心(10min,15,000g)。每种裂解物的蛋白浓度使用lowry测定确定。如下文描述的,将样品储存在-80℃直到ms/ms分析。凝胶电泳和免疫印迹样品(10-40μg的蛋白)经受sds-page。凝胶用考马斯亮蓝染色或电转移到硝酸纤维素膜上用于免疫染色。包含转移的蛋白的膜用tris-缓冲盐水(tbs)中的5%脱脂奶粉和0.1%tween-20封闭,并且与不同的一级抗体(来源和稀释度如在表3中详细描述的)在4℃孵育过夜,随后用适当的hrp-缀合的二级抗体孵育持续1h。使用增强化学发光(biologicalindustries)检测hrp活性。使用fusion-fx(vilberlourmat,france)分析条带强度,并且将值对用作上样对照的适当的α-肌动蛋白信号的强度归一化。rna分离和qpcr总rna使用rneasy微试剂盒(qiagen)根据制造商的说明从健康肺样品和肿瘤肺样品分离。总rna质量使用agilentrna6000纳米试剂盒分析。qpcr使用特异性引物(kicqstart引物;sigmaaldrich)以一式三份,使用powersybergreen主混合物(appliedbiosystems,fostercity,ca)进行。靶基因的水平相对于β-肌动蛋白mrna水平归一化。样品通过7300实时pcr系统(appliedbiosystems)使用以下pcr参数扩增40个循环:95℃持续15秒,60℃持续1分钟,并且72℃持续1分钟。每种样品的拷贝数通过基于ct的校准的标准曲线方法计算。计算了三个重复的平均倍数变化(±sem)。检查的基因和使用的引物在表5中列出。表5:本研究中使用的qpcr引物lc-hrms/ms分析样品经受如下的溶液中胰蛋白酶消化:蛋白首先通过在60℃用5mmdtt孵育持续30min还原,随后在21℃在黑暗中用10mm碘乙酰胺烷基化持续30min。蛋白然后经受用胰蛋白酶(promega,madison,wi)以1:50的胰蛋白酶:蛋白比率在37℃消化持续16h。在消化之后,使用商业洗涤剂去除柱(pierce,rockford,il)从样品清除洗涤剂,并且使用固相提取柱(oasishlb,waters,milford,ma)脱盐。通过添加三氟乙酸(1%)停止消化。将样品储存在-80℃直到lc-hrms/ms分析。对于lc-hrms/ms,ulc/ms级溶剂被用于所有色谱步骤。每一种样品使用不分流(split-less)纳米超高效液相色谱柱(10kpsinanoacquity;waters)分离。流动相是(a)h2o和0.1%甲酸,和(b)乙腈和0.1%甲酸。样品的脱盐使用反相c18捕获柱(内径为180μm,长度为20mm,粒径为5μm;waters)在线进行。然后肽使用t3hss纳米柱(内径为75μm,长度为250mm,粒径为1.8μm;waters)以0.3μl/min分离。使用以下梯度将肽从柱洗脱到质谱仪中:4%至35%的(b)持续150min,35%至90%的(b)持续5min,维持在90%持续5min并且然后回到初始条件。纳米-uplc通过纳米-esi发射器(10μm的针(tip);newobjective,woburn,ma)在线偶联到使用flexion纳米喷雾装置(proxeon)的四极orbitrap质谱仪(qexecutive,thermoscientific)。以dda模式获得数据,使用top12方法(kelstrupcd等人jproteomeres.2012;11:3487-97)。将原始数据导入expressionist软件(genedata)(uedak等人plosone.2011;6:e18567;gurycav等人proteomics.2012;12:1207-1216)。该软件用于前体肽强度的保留时间比对和峰检测。主峰列表从所有ms/ms事件产生并且发出用于使用mascotv2.4(matrixsciences)搜索数据库。针对数据库搜索数据,该数据库包含来自uniprotkb/swissprot的正向和反向人类蛋白序列,以及125种通常的实验室污染物,总共20,304个条目。将固定的修饰设置为半胱氨酸的脲甲基化,而将可变修饰设置为甲硫氨酸的氧化。搜索结果然后被导回到expressionist用于注释检测到的峰。对鉴定进行过滤,使得全面错误发现率(globalfalsediscoveryrate)最高为1%。蛋白丰度基于三种最丰富的肽计算(d’arenag等人amjhematol.2006;81:598-602)。具有少于2种独特的肽的蛋白被排除在进一步分析外。分析了来自9名ac患者的样品,而健康和癌性肺组织从相同的患者肺获取。在另外的测定中,健康和癌性肺组织从5名ac和5名scc患者获取。对其鉴定出至少2种独特的肽的蛋白被用于进一步分析。组织微阵列(tma)载玻片上的免疫组织化学(ihc)对从biomaxus获得的福尔马林固定的和石蜡包埋的组织微阵列载玻片进行免疫组织化学染色。切片使用二甲苯和梯度乙醇系列脱石蜡。内源过氧化物酶活性通过将切片在3%h2o2中孵育10分钟来封闭。抗原恢复在0.01m柠檬酸盐缓冲液(ph6.0)中在95℃-98℃进行20min。在pbs(ph7.4)中洗涤切片后,非特异性抗体结合通过将切片在10%正常山羊血清中孵育2h来降低。在倾倒过量血清后,将切片在4℃与一级抗体(表3)孵育过夜。在用pbs洗涤后,将切片与适当的与辣根过氧化物酶缀合的二级抗体(表3)孵育持续2h。切片在pbs中洗涤三次并且随后,过氧化物酶催化的反应通过与0.02%dab孵育可视化。在水中冲洗后,将切片用苏木精复染,并且用vectashield封片介质(vectorlaboratories,burlingame,ca)封片。最后,在显微镜(dm2500,leica)下观察切片并且以指示的放大率用相同的光强度和曝光时间拍摄图像。对照用相同的方案实施但省略了一级抗体。biomax组织阵列癌症组织微阵列购自biomaxus(usbiomax)。这些包括用于肺癌的阵列(lc807),所述用于肺癌的阵列(lc807)包含肺正常组织(n=10)和处于不同阶段的多种肺癌类型,包括ac(n=21)、腺鳞状癌(n=1)、鳞状细胞癌(scc,n=31)、细支气管肺泡癌(bac;n=6)、小细胞癌(n=6)和大细胞癌(n=5)。第二种组织阵列(bc041115c)包含正常肺组织(n=10)、ac(n=51)和scc(n=41)癌性组织样品。rnaseq基因表达谱分析关于肺癌患者的健康和肿瘤样品的基因表达谱和热图的数据从xena,tcga[rnaseq使用多a+illuminahiseq](2016-08-16版,tcgahub,xena.ucsc.edu)获得,单位是泛癌(pan-cancer)归一化的(n=1,129)。使用t-检验进行线性倍数变化和统计分析。统计和生物信息学分析用于数据分析的所有描述性统计使用spss统计包17.0版计算。展示了从指示的独立实验获得的结果的平均值±sem。对照(健康)和实验(癌症)组之间的差异的显著性的水平由非参数mann-whitneyu检验确定。当p值被认为<0.05(*)、<0.01(**)或<0.001(***)时,差异被认为是统计学上显著的。lc-hr-ms/ms数据被导入partek基因组学套件软件(partek,st.louis,mo)中并且使用t-检验计算不同的组中蛋白的表达水平之间的差异。差异表达的蛋白的功能富集分析使用david和基因本体(go)生物信息学资源,v6.7进行(nawarakj等人biochimbiophysacta.2009;1794:159-67)。实施例1:来自nsclc患者的健康和肿瘤组织的蛋白谱的质谱分析为了鉴定在nsclc肿瘤组织中相对于健康组织显示出改变的表达水平的蛋白,癌性组织和健康组织的9个样品从nsclc患者的相同的肺收集并且经受lc-hrms/ms分析。基于所有检测到的蛋白的表达模式的分层聚类(hierarchicalclustering)清楚地允许区分健康组织和肿瘤组织(图1a),1,494种蛋白的表达水平被改变(倍数变化(fc)≥|2|并且错误发现率(fdr)<0.05,其中378种蛋白显示出fc≥|100|)(图1b)。上调和下调的蛋白基于fc和p值的组合被进一步分成两个簇,由于一些样品“不存在”一些蛋白。接下来,癌性肺组织和健康肺组织之间差异表达的蛋白的功能分析使用david和基因本体数据库进行(ashburnerm等人geneontology:toolfortheunificationofbiology.thegeneontologyconsortium.natgenet.2000;25:25-9;geneontologyconsortium.geneontologyconsortium:goingforward.nucleicacidsres.2015;43:d1049-56)。这样的分析揭示了与蛋白合成和降解相关的蛋白并且特别是被指定了在代谢中和到线粒体的作用的蛋白的富集(图1c)(表6)。表6:通过lc-hrms/ms鉴定健康供体和肺癌患者中差异表达的选择的蛋白上文表6基于如上文描述地进行的两个独立lc-hrms/ms实验。从每个实验,过滤了差异表达的蛋白(p值<0.01,fc≥|2|),并且选择了在两个实验中差异表达的蛋白。列出了与肺癌相关或具有作为生物标志物的潜力的蛋白。对于每种蛋白,指示了名称、倍数变化和p值以及其功能、亚细胞定位和与癌症的相关性。实施例2:代谢相关和凋亡相关的蛋白的改变的表达改变的代谢和抗凋亡机制的发展是癌症的特征。如先前描述的(wo2013/035095),与这些特征相关的若干种蛋白在某些类型的癌症中过表达。来自nsclc患者的相同的肺的肿瘤和健康组织的样品通过免疫印迹使用特异性抗体分析,以评估以下的水平:电压依赖的阴离子通道1(vdac1)、己糖激酶i(hk-i)、smac/diablo(smac)、凋亡诱导因子(aif)、线粒体抗病毒信号传导(mavs)和bcl-2(图2)。除bcl-2之外,所有这些蛋白在癌性组织中与从相同的nsclc患者获得的健康组织相比显著地过表达(3倍至6倍)(图2a、2b)。lc-hr-ms/ms进一步确定,vdac1、hk-i和smac的表达水平在癌组织中高度增加(图2c)。如从rnaseq基因表达谱分析数据揭示的,vdac1、hk-i、smac和aif的rna表达水平显示出相似的趋势,虽然在rna水平的表达较低(图2e)。vdac1、smac、aif、hk-i、mavs和bcl-2的表达水平还通过包含正常样品和nsclc来源的样品的组织微阵列中的ihc分析(图2f)。所有蛋白在肿瘤组织中高度表达。因此,虽然smac、aif是促凋亡蛋白,但它们在肿瘤组织中过表达。其他代谢相关的蛋白,诸如乳酸脱氢酶(ldha)、atp合成酶亚基5b(atp5b)、糖酵解酶甘油醛3磷酸脱氢酶(gapdh)、磷酸甘油酸激酶1(pgk1)和烯醇化酶-1(eno1),也在肿瘤组织中高度表达(更高达14倍),如通过lc-hr-ms/ms分析确定的(图3a、3d、3e)。这些结果指出肺癌中重编程的代谢和凋亡逃避(apoptosisavoidance)的重要性。实施例3:肺癌的生物标志物的鉴定lc-hr-ms/ms分析数据揭示了nsclc肿瘤中差异表达的许多其他蛋白(表6)。在肿瘤中表达变化最显著的蛋白,与它们被提出的功能和与癌症的关系一起,在表6中展示。这些包括ras相关蛋白rab11b(rab11b)、hyou1(orp150)和热休克蛋白hspd1(hsp60),ras相关蛋白rab11b(rab11b)是小gtp结合蛋白的ras超家族的成员,hyou1(orp150)在由氧剥夺引发的细胞保护的细胞机制中起关键作用。这些发现通过免疫印迹分析、rnasequcscxena数据和qrt-pcr确定(图3)。通过蛋白质组学在本文鉴定(并且通过免疫印迹分析、rnaseq基因表达谱分析数据和qrt-pcr确定)的蛋白的网络分析证明,大多数这些蛋白在若干个水平相互作用,而代谢过程相关的蛋白是中心。这些相互作用包括与细胞代谢相关的通常功能,并且包括彼此之间的直接物理相互作用。许多这些蛋白是共表达的,并且因此可以被定义为受表观遗传修饰调控的簇。实施例4:在ac和scc中差异表达的蛋白使用特异性抗体通过ihc染色对用于vdac1和aif(来自10个健康、31个scc和17个ac样品)和用于smac/diablo(来自20个健康、72个scc和72个ac样品)表达水平的肺组织微阵列进行的分析揭示了,这些蛋白在肺癌中与健康组织相比的高表达(图4a)。ihc结果(展示为显示出在指示的强度染色的患者样品的数目,并且表示为分析的切片的总数目的百分比)的数量分析显示出,vdac1、smac和aif表达水平在scc中高于在ac中(图4a)。接下来,来自ac和scc患者各五名的肺的癌性和健康组织样品经受lc-hr-ms/ms分析。2,959种蛋白的表达水平在癌性组织中相对于相应健康组织中的表达上调或下调,而1,513种蛋白的表达的变化是显著的。选择了显示出在两种nsclc亚型之间表达水平的变化最高(p值<0.01)的蛋白,并且在肿瘤中相对于健康组织的表达的倍数变化被计算并且展示为每种蛋白的scc/ac比率(图4b)。评估scc/ac比率揭示了hat1、itga7、lrrfip2、akr1b10(分泌型蛋白)、wdr82、ttll12和usp14在scc中高度过表达(高达500倍),vdac1和smac过表达程度较低,而hyou1、acot1、rab34和tsg101显示出在ac中较高的表达。表7展示了从具有nsclc亚型ac或scc的患者获得的肺样品中的这些蛋白和另外的蛋白的每一种的表达与健康受试者的肺样品或健康肺组织中的表达相比的倍数变化。还展示了scc与ac表达比率、被提出的蛋白的功能及其与癌症的关系。表7:用于区分nsclc亚型ac和scc的生物标志物使用rnaseq(ucscxena,n=1,129)对从健康和肺癌患者获得的组织分析显示出显著差异表达的若干种蛋白(ms/ms数据,图4b)和napsa(先前被提出用于区分ac和scc)的表达(图5a)。分析揭示了,acot1、rab34、tsg101和napsarna表达水平在scc中低于在ac中,而smac、akr1b10(分泌型蛋白)、hat1、usp14和ttll12以及在wdr82和vdac1的rna表达水平,在scc中相对于在ac中的表达更高(wdr82和vdac1的rna表达水平高的程度较低)。这些结果与蛋白质组学数据一致(图4b),并且因此提出使用这些蛋白和/或编码它们的rna作为标志物以区分ac和scc。在试图鉴定按照蛋白质组学数据中揭示的在nsclc中具有改变的表达的另外的蛋白(其可以区分ac和scc)时,使用rnasequcscxena数据确定若干种蛋白的rna水平(图5b)。编码tp63、ggh(分泌型蛋白)、ck5、ck13、ck14、ck17、csta、ranbp1、timm44、fen1、fen2、smc2和igf2bp3的rna水平在scc中相对于ac增加,而编码rsu1、akr7a3、gale、azgp1(分泌型蛋白)、acot1、abcd3、npc2(分泌型蛋白)、acad8、rps6ka3、arrb1和lrba的rna的水平显示出相反的趋势,即在ac中相对于scc表达更高。这些基因的产物的功能和先前报道的与ac或scc的关系在表8中列出。表8:由在scc和ac中差异表达的rna编码的蛋白实施例5:与ac和scc中的生存率相关的蛋白的表达为了进一步测试被提出以区分ac和scc的蛋白的预后价值,对肺癌患者的公开可得的基因表达数据集进行生存分析。进行了kaplan-meier分析,该kaplan-meier分析将患者生存评估为与ac和scc中的相对表示的mrna水平(高和低)的函数。结果显示出在ac患者中,高水平的vdac1、smac、hyou1、ttll12和rab34与低生存率相关,而高水平的akr1b10、aif(线粒体)、arl1、tsg101、hat1、p40、napsa、lrrfip2、titf1和wdr82与更高生存率相关(表9)。相反,这些蛋白的表达水平对scc生存率不具有影响(表9)。表9中展示的数据从kmplot.com获得。总样品数为2437,括号中展示了各组中的初始数目。kaplan-meier估计器使用了更早期(2015)版本的数据库(szaszam等人oncotarget.2016;7:49322-33)。表9:ac和scc肺癌亚型中的蛋白表达水平与生存之间的关系实施例5:smac/diablo在核中的存在有趣地,肺癌来源的样品的组织阵列中smac/diablo表达的分析揭示了,虽然smac是线粒体蛋白,但在scc的核和胞质溶胶中发现了高水平的该蛋白,但在ac组织样品中仅发现较低的程度(图6a)。先前的研究尚未报道smac在核中的存在。结果还显示出,已知在凋亡诱导后易位到核的aif不存在于核中(图6b)。为了进一步证明smac在核中的存在,在将核级分和胞质溶胶级分分离后,分析了从相同的肺的健康和肿瘤组织获得的ac和scc肺癌样品中smac的核分布(图6c、6d)。虽然在ac中约90%的smac在线粒体/胞质溶胶中,但在scc中约50%在线粒体/胞质溶胶中并且50%在核级分中发现(图6d)。在包含smac的核级分中,没有发现三种其他线粒体蛋白vdac1、mavs和aif(图6c),指示smac的特异性核定位。总之,如在本文确定的,来源于公开的数据和在本文第一次被鉴定的潜在地能够区分ac和scc的若干种生物标志物基于在scc或ac中差异表达而被选择(表10)。表10:用于区分ac和scc的选择的生物标志物展示了可以被用作生物标志物的蛋白,列出了它们在scc中相对于ac的表达水平,如通过蛋白质组学、qpcr(括号中)和rnaseq研究确定的。还指示了数据的来源。实施例6:apool、vps29和caf17的沉默用于治疗nsclc为了验证被鉴定为在nsclc中过表达的蛋白的重要性,检查了它们被特异性sirna沉默的效果。至少一种sirna,并且通常是两种sirna被设计用于使编码蛋白apool、vps29和caf17的每一种的rna沉默。此外,设计了非特异性加扰的sirna。体外测定nsclc细胞系的细胞用加扰的sirna或用对每种蛋白特异性的sirna转染,并且细胞生长使用磺基罗丹明b(srb)方法分析。在该方法中,用sirna转染后48h或96h,细胞用pbs洗涤两次,用10%三氯乙酸固定持续1-2h,并且随后用srb染色。使用100mmtris-碱从细胞提取srb,并且使用infinitem1000板读取仪(tecan,switzerland)确定在510nm处的吸光度。体内测定-使用裸鼠的异种移植物实验。将a549肺癌细胞(7×107)s.c.注射到无胸腺的8周龄雄性scid裸鼠的后腿侧面。在接种后11天,用数字卡尺以二维测量发展中的肿瘤,并且将肿瘤体积计算如下:体积=x2×y/2,其中x和y分别是肿瘤的宽和长尺寸。具有达到体积为65-100mm3的异种移植物的小鼠被随机分组用于不同的治疗(每组中8只或9只动物):pbs、非靶向(加扰的)sirna或针对选择的蛋白的sirna。使用jetpei递送试剂(10μgsirna/20μljetpei)将每种治疗物质注射到已建立的s.c.肿瘤中。每3天用pbs或适当的sirna注射(20μl/肿瘤)异种移植物。从接种当天开始,每周两次使用数字卡尺监测小鼠体重和肿瘤体积,持续33天的时间段。在实验的终点,即当肿瘤体积达到~250mm3时,用co2气体处死小鼠;切下肿瘤并且确定离体重量。每个肿瘤的一半固定在4%缓冲甲醛中,石蜡包埋并且处理用于组织学检查,而另一半冷冻在液氮中并且储存在-80℃用于免疫印迹分析。上文特定实施方案的描述将如此完全地揭示本发明的一般性质,使得其他人可以通过应用现有的知识,容易地为多种应用修改和/或改变这样的特定实施方案而不需要过度实验并且不背离一般概念,并且因此,这样的改变和修改应当并且预期被包含在所公开的实施方案的等同物的含义和范围内。将理解的是,本文使用的措辞或术语是出于描述并且非限制的目的。用于实施多种公开的功能的工具、材料和步骤可以采取多种可选的形式而不背离本发明。序列表<110>内盖夫生物技术国家研究所有限公司内盖夫本·古里安大学<120>用于肺癌的诊断的生物标志物<130>nibn/005pct<150>62/509214<151>2017-05-22<160>16<170>patentinversion3.5<210>1<211>20<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>1actcttccagccttccttcc20<210>2<211>20<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>2tgttggcgtacaggtctttg20<210>3<211>20<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>3gagcaggacgtgagacttct20<210>4<211>22<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>4tttgccaagaggagacttccaa22<210>5<211>22<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>5tgcccttaaaaggtatgcaggt22<210>6<211>20<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>6tctcggcaaactgtgggaaa20<210>7<211>20<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>7tggagcacgaggttttcgac20<210>8<211>20<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>8cgatgaccttgtagcacagc20<210>9<211>21<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>9gccagctcaagaaaatggtgt21<210>10<211>23<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>10aggtctctgtatttgtactgggt23<210>11<211>20<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>11cctcagcaacaacccctcta20<210>12<211>23<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>12ggtcatagatatcccgcaattca23<210>13<211>20<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>13gcttcgatttcagccccaac20<210>14<211>20<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>14tctctttggtttgccctcct20<210>15<211>20<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>15atggcgggatttggtgctat20<210>16<211>21<212>dna<213>人工序列(artificialsequence)<220><223>引物<400>16gttcaattgctgtgttggtgt21当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1