使用磷酸化的TBeta4和其他因子生成人诱导多能干细胞的制作方法
本申请要求于2017年8月25日提交的第62/550,337号美国临时专利申请以及于2018年7月24日提交的标题为“使用磷酸化的tbeta4和其他因子生成人诱导多能干细胞”的美国专利申请16/044,142的利益和优先权,其全部内容通过引用并入本申请。
本文讨论的这些和所有其他外部材料通过引用整体并入本文。当术语的定义或使用在并入的参考文献中与本文提供的术语的定义不一致或相反时,适用本文提供的该术语的定义,而参考文献中该术语的定义不适用。
本发明的技术领域是生成人诱导多能干细胞的组合物和方法。
背景技术:
以下背景讨论包括可用于理解本发明的信息。不承认本文提供的任何信息是现有技术或与当前要求保护的发明有关,或明确或隐含引用的任何出版物均为现有技术。
目前针对治疗退行性疾病存在需求,而胚胎干细胞植入已显示出一些希望。(ollelindvall&zaalkokaia,stemcellsforthetreatmentofneurologicaldisorders,441nature1094-96,2006)。但是,胚胎干细胞的使用存在争议。在2006年,yamanaka等人报道了使用四种转录因子oct3/4、sox2、c-myc和klft从小鼠胚胎成纤维细胞中诱导多能干细胞的产生。azutoshitakahashi&shinyayamanaka(inductionofpluripotentstemcellsfrommouseembryonicandadultfibroblastculturesbydefinedfactors,126cell663-76,2006)。在2007年,这些转录因子被用于诱导人类成纤维细胞的多能干细胞。(kazutoshitakahashietal.,inductionofpluripotentstemcellsfromadulthumanfibroblastsbydefinedfactors,131cell861-72,2007)。
诱导多能干细胞具有与胚胎干细胞相似的特性,并且还可以发展成退行性疾病疗法。另外,为了研究疾病进展,可以通过对健康和患病个体的体细胞进行程序重调来生成ipsc(诱导多能干细胞)。然后可以通过引入或纠正可能引起疾病的突变,而对ipsc进行基因修饰。然后将ipsc分化为目标细胞类型。(yufensamanthaseahetal.,inducedpluripotencyandgeneeditingindiseasemodelling:perspectivesandchallenges,16int.j.mol.sci.28614-34,2015)。
然而,几个问题阻止了ipsc在治疗中的广泛使用。其中一个问题是肿瘤的形成,因为yamanaka转录因子促进肿瘤发生,从而使植入的细胞不能正常运转。此外,由于使用病毒载体进行永久性基因组修饰,我们无法预测后果。
本文所标记的所有出版物都以相同的程度通过引用并入本文,如同每个单独的出版物或专利申请被具体地和单独地指示通过引用并入一样。当术语的定义或使用在并入的参考文献中与本文提供的术语的定义不一致或相反时,适用本文提供的该术语的定义,而参考文献中该术语的定义不适用。
在一些实施例中,用于描述和要求保护本发明的某些实施例的表示成分数量、性质(例如浓度、反应条件等)的数字应理解为在某些情况下被术语“约”修饰。因此,在一些实施例中,在说明书和所附权利要求书中阐述的数字参数是近似值,其可以根据特定实施例试图获得的期望特性而变化。在一些实施例中,应该根据报告的有效数字的数目并通过应用普通的舍入技术来解释数字参数。尽管列出本发明的一些实施例的广泛范围的数值范围和参数是近似值,但是在具体示例中列出的数值尽可能精确地报告。在本发明的一些实施例中呈现的数值可能包含某些误差,这些误差必然是由它们各自的测试测量中发现的标准偏差引起的。
如本文的说明书和随后的权利要求书中所使用的,除非上下文另外明确指出,否则“一个”,“一种”和“该”的含义包括复数形式。此外,如本文的描述中所使用的,“在...中”的含义包括“在...中”和“在...上”,除非上下文另外明确指出。
本文中数值范围的列举仅旨在用作分别指代落入该范围内的每个单独数值的速记方法。除非本文另外指出,否则将具有范围的每个单独的值并入说明书中,就如同其在本文中单独列举一样。除非本文另外指出或与上下文明显矛盾,否则本文描述的所有方法可以以任何合适的顺序执行。相对于本文的某些实施例提供的任何和所有示例或示例性语言(例如“例如”)的使用仅旨在更好地阐明本发明,并且不对以其他方式要求保护的本发明的范围构成限制。说明书中的任何语言都不应解释为表示对实施本发明必不可少的任何未要求保护的要素。
本文公开的本发明的替代元件或实施例的分组不应解释为限制。每个群组成员可以单独引用或要求保护,也可以与该群组的其他成员或本文中的其他元件组合使用。出于方便和/或可专利性的原因,一个群组中的一个或多个成员可以包含在一个群组中、或从一个群组中删除。当发生任何这样的包含或删除时,说明书在本文中被认为包含经修改的群组,从而满足所附权利要求中使用的所有马库什群组的书面描述。
因此,仍然需要诱导多能干细胞,其缺乏永久的基因组修饰,并且在植入患者体内时不形成肿瘤。
技术实现要素:
本发明的主题提供了使用外源tβ4、外源sox2和外源oct4在非胚性细胞和/或体细胞中诱导多能性的组合物和方法。诱导多能干细胞可衍生自非胚性细胞或体细胞。预期的诱导多能干细胞可以是类人猿(例如人诱导多能干细胞)或鼠类(例如小鼠诱导多能干细胞)。本发明人还设想可以在源自家畜的细胞中诱导多能性。本文的某些实施例提供的任何和所有实施例或示例性语言(例如,“例如”)的使用仅旨在更好地阐明本发明,并且不对所要求保护的本发明的范围构成限制。
优选地,外源τβ4为磷酸化的。磷酸化的τβ4通过激活p53途径并抑制ras致癌基因和jak-stat途径而促进多能性。
为了提高转染效率,可以将细胞膜穿透部分与外源tβ4、外源sox2和/或外源oct4偶联。如本文所用,术语“与...偶联”是指共价键合、静电的、抗生物素/抗生蛋白链菌素等。该偶联包括连接子和/或间隔子。如本文所用,除非上下文另有指示,否则术语“偶联至”旨在包括直接偶联(其中彼此偶联的两个元件彼此接触)和间接偶联(其中至少一个附加元件位于两个元件之间)。因此,术语“偶联至”和“与...偶联”同义地使用。
优选地,细胞膜穿透部分包括阳离子肽。阳离子肽包括精氨酸和赖氨酸,优选为基本上由r9-k9组成的序列(rrrrrrrrrkkkkkkkkk)。阳离子肽可包括一个或多个甘氨酸间隔子。任选地,柔性连接子可以将阳离子肽连接至tβ4、sox2和/或oc4。该讨论提供了本发明主题的许多示例性实施例。尽管每个实施例代表发明元素的单个组合,但是发明主题被认为包括所公开元素的所有可能的组合。因此,如果一个实施例包括元素a,b和c,而第二实施例包括元素b和d,则本发明主题也被认为包括a,b,c或d的其他剩余组合,即使未明确披露。
外源tβ4、外源sox2和/或外源oct4偶联至细胞核靶向部分很可能增加靶基因的表达。优选的细胞核靶向部分是谷胱甘肽-s-转移酶。
发明人考虑了根据本发明主题的诱导多能干细胞将在至少100次传代中保持多能性。
本发明的主题还包括一种组合物,该组合物包括外源tβ4、外源sox2和外源oct4,可以用于在非胚性细胞/体细胞中诱导多能性。在预期的组合物中,外源tβ4、外源sox2和外源oct4中的至少两种通过连接子偶联。换句话说,连接子偶联τβ4和sox2、τβ4和oct4或sox2和oct4。连接子也可以用于偶联τβ4、sox2和oct4。
细胞膜穿透部分(例如,阳离子肽)和/或细胞核靶向部分(例如,谷胱甘肽-s-转移酶)可以偶联至外源tβ4、外源sox2和/或外源oct4。细胞核靶向部分可以任选地偶联至外源tβ4、外源sox2和外源oct4中的至少一种。
本发明的主题还包括在体细胞中诱导多能性的方法,该方法包括以下步骤:(1)将τβ4、sox2和oct4蛋白引入体细胞中;和(2)在诱导体细胞去分化的条件下培养步骤(1)的所述体细胞,得到诱导多能干细胞。本发明的方法可以进一步包括在一定条件下培养所述诱导多能干细胞的步骤,使得所述诱导多能干细胞在100次传代后保持多能性。
通过以下对优选实施例的详细描述以及附图,本发明主题的各种目的、特征、方面和优点将变得更加显而易见,在附图中,相同的附图标记表示相同的部件。
附图说明
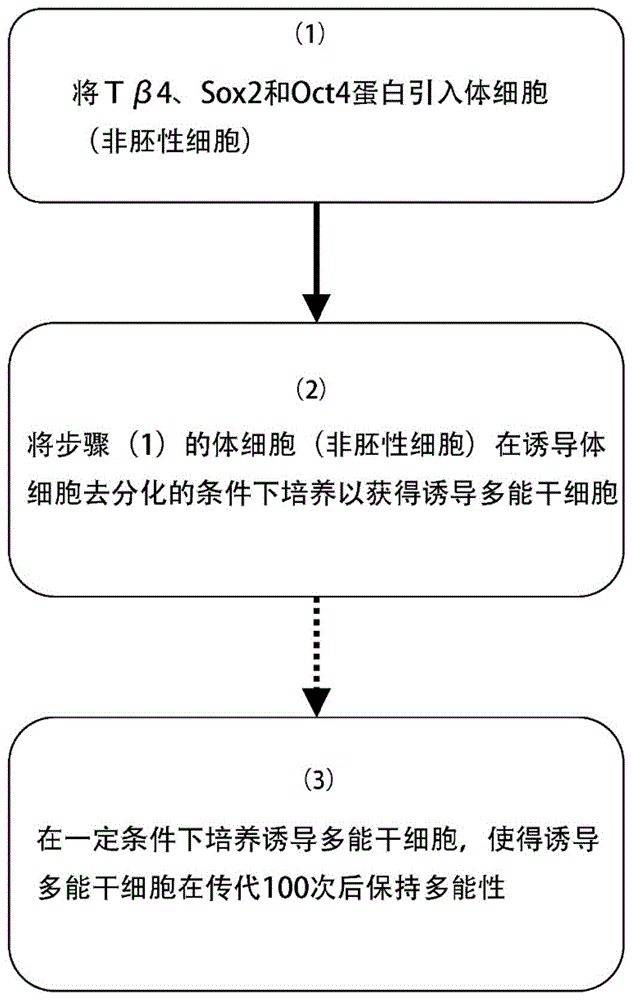
图1是根据本发明主题的方法的示意图。
具体实施方式
诱导多能干细胞(ipsc)具有治疗诸如糖尿病、阿尔茨海默氏病、帕金森氏病、心血管疾病和肌萎缩性侧索硬化症等疾病的潜力。因为ipsc是从成人体细胞中产生的,所以ipsc也可以用于自体细胞替代疗法和器官移植。发明人假设本发明的ipsc将表达细胞表面标志物,包括ssea1、ssea3、sox2、oct3/oct4、nanog、klf4、c-myc和lin28。发明人还期望根据本发明主题的ipsc表现出dna甲基化模式和源细胞的其他表观遗传特性。
本发明的主题提供了使用外源tβ4、外源sox2和外源oct4在非胚性细胞和/或体细胞中诱导多能性的组合物和方法。外源tβ4、外源sox2和外源oct4是用于程序重调包括成人体细胞在内的非胚性干细胞的重组蛋白。在获得诱导多能干细胞后,它们可以分化为例如心肌细胞、脂肪细胞、多巴胺能神经元、神经细胞、运动神经元、胰腺β细胞和造血祖细胞。这种诱导多能干细胞在疾病建模、药物筛选、再生医学和细胞治疗中具有潜在的应用。
诱导多能干细胞可以来源于哺乳动物的非胚性细胞或体细胞,其顺序为:偶蹄目、食肉目、鲸目、翼手目、皮翼目、贫齿目、蹄兔目、食虫目、兔目、有袋目、单孔目、奇蹄目、鳞甲目、鳍脚目、灵长目、长鼻目、啮齿目、海牛目和管齿目。预期的诱导多能干细胞可以是类人猿(例如人诱导多能干细胞)或鼠类(例如小鼠诱导多能干细胞)。发明人还设想可以在源自例如山羊、牛、马和绵羊等家畜的细胞中诱导多能性。
在本发明主题的优选实施方案中,体细胞/非胚性细胞包括成纤维细胞、脐带血细胞(优选cd34-阳性)、成纤维细胞样滑膜细胞、肝细胞、胃上皮细胞、b淋巴细胞、胰腺β细胞、角质形成细胞、牙齿干细胞、间充质基质细胞、外周单核血细胞(优选cd34-阳性)和/或任何其他合适的细胞。参见例如,junli,weisong&junzhou,advancesinunderstandingthecelltypesandapproachesusedforgeneratinginducedpluripotentstemcells,j.hematology&oncology(2014),at7:50(https://doi.org/10.1186/sl3045-014-0050-z).
不希望受限于特定假设,发明人期望外源胸腺素β4(“τβ4”)在非胚性和/或体细胞中,特别是与外源sox2和oct4组合,可诱导多能性同时还抑制肿瘤发生。τβ4是存在于所有细胞类型(红细胞除外)中包括43个氨基酸、4.9kda的蛋白质。τβ4发挥的许多生物学作用包括与g-肌动蛋白结合以及f-肌动蛋白解聚为g-肌动蛋白,这与细胞增殖、分化和迁移有关。在角膜中,τβ4具有抗炎特性,抑制细胞凋亡,并促进细胞迁移和伤口愈合。请参见gabrielsonse,pingqiu,michellekurpakus-wheater,thymosinbeta4:anovelcornealwoundhealingandanti-inflammatoryagent,1(3)clinicalophthalmology201-07(2007)。τβ4还被确定为神经系统损伤的潜在治疗方法,因为τβ4介导少突胶质生成并治疗脱髓鞘。请参见manoranjansantraetal,thymosinbeta4mediatesoligodendrocytedifferentiationbyupregulatingp38mapk,60(12)glia1826-38(2012)。
tβ4在诱导多能性中起作用有先例。τβ4已经显示出诱导成人心外膜来源的祖细胞回复到其胚胎表型。请参见paulr.riley&nicolasmart,thymosinβ4inducesepicardium-derivedneovascularizationintheadultheart.37(6)blochem.soc.trans.1218-20(2009)。riley和smart建议,合成的τβ4恢复多能性的能力可能有助于急性缺血性损伤后的心肌再生和新血管形成。在tβ4诱导心外膜来源的细胞中的多能性之后,所得的诱导多能性心外膜来源的细胞经历了上皮-间质转化、迁移离开心外膜、分化为可能有助于成人心脏新血管形成的血管前体。鉴于有报道称τβ4在t细胞和内皮细胞分化中起作用,tβ4诱导多能性的能力是不可预测的。
τβ4还显示出具有肿瘤抑制和致瘤性质。jocaers等报道了τβ4在多发性骨髓瘤中具有肿瘤抑制作用。请参见jocaersetal,thymosinβ4hastumorsuppressiveeffectsanditsdecreasedexpressionresultsinpoorprognosisanddecreasedsurvivalinmultiplemyeloma.95(1)haematologica163-67(2010)。具体而言,τβ4表达在多个骨髓瘤细胞中被下调,这与在小鼠中的存活时间较短有关。增强τβ4表达增加了存活时间。相反,τβ4的过表达与实体瘤(例如结肠癌)的体外生长、运动和侵袭增加以及体内肿瘤负荷增加有关。
优选地,外源tβ4被磷酸化以抑制致癌途径。示例性的tβ4氨基酸序列包括uniprot数据库登录号p62328(一级序列)及其保守修饰的变体。
meng等人先前证明了,当载体中包含土拨鼠转录后调控元件和强的脾病灶形成病毒以增加表达时,可以使用仅表达oct4和sox2的慢病毒载体对脐带血来源的cd34+细胞进行程序重调。请参见xianmeimengetal,efficientreprogrammingofhumancordbloodcd34+cellsintoinducedpluripotentstemcellswithoct4andsox2alone,20(2)moleculartherapy408-16(2012)。作者建议可以使用增加成纤维细胞中转基因表达的启动子(例如ef1)对成纤维细胞进行程序重调。程序重调也可以使用较弱的oct4和sox2表达启动子与编码klf4和myc的载体完成。但是,如前所述,myc具有致癌性。
通过用蛋白oct4和sox2直接对细胞进行程序重调,可以消除受到表达水平限制的程序重调效率的问题。预计程序重调将被τβ4,优选磷酸化的τβ4进一步增强。sox2的示例性氨基酸序列包括uniprot数据库登录号p48431(一级序列)及其保守修饰的变体。oct4的示例性氨基酸序列包括uniprot数据库登录号q01860(一级序列)及其保守修饰的变体。
使用根据本发明主题的组合物和方法,转染效率预计将大于1%、2%、5%和10%。为了进一步提高转染效率并因此提高程序重调效率,可以将细胞膜穿透部分与外源tβ4、外源sox2和/或外源oct4偶联。如本文所用,除非上下文另有指示,否则术语“偶联”旨在包括直接偶联(其中彼此偶联的两个元件彼此接触)和间接偶联(其中至少一个附加元件位于两个元件之间)。因此,术语“偶联至”和“与...偶联”同义地使用。例如,外源蛋白质和肽可以通过肽键共价键结合、通过静电相互作用偶联、通过亲和力偶联(例如生物素与抗生物素蛋白或抗生蛋白链菌素)等。偶联包括连接子和/或间隔子,例如g4s、聚乙二醇或其他合适的连接子。proteochemtm提供了几种合适的异型双功能交联剂,包括:anb-nos、bmps、emcs、gmbs、lc-spdp、mbs、pdph、sba、sia、sulfo-sia、smph、spdp、sulfo-lc-spdp、sulfo-mbs、sulfo-sanpah和/或sulfo-mscc(www.proteochem.coin/proteincrosslinkerssheterobifunctionalcrosslinkers-c-1_7.html?gclid=ciwr7ps42tucfutnfgodo_sb3a)。
优选地,细胞膜穿透部分包括阳离子肽。阳离子肽包括4至20个精氨酸和/或赖氨酸残基,优选9个精氨酸和9个赖氨酸残基。还预期其他递送方法,例如脂质体或水凝胶制剂。在这样的制剂中,细胞膜穿透部分可以与脂质体或水凝胶偶联,而不是与外源tβ4、sox2和/或oct4偶联(或除此之外)。该讨论提供了本发明主题的许多示例性实施方案。尽管每个实施方案代表发明元素的单个组合,但是发明主题被认为包括所公开元素的所有可能的组合。因此,如果一个实施例包括元素a,b和c,而第二实施例包括元素b和d,则本发明主题也被认为包括a,b,c或d的其他剩余组合,即使未明确披露。
将外源tβ4、外源sox2和/或外源oct4偶联至细胞核靶向部分可能增加靶基因的表达(例如,oct3/4,rexl,nanog,gata6,msx2,pax6,handl)负责程序重调体细胞/非胚性细胞以恢复为多能状态。优选的细胞核靶向部分是谷胱甘肽-s-转移酶(例如,uniprot数据库登录号p28161)。在此类脂质体和/或水凝胶制剂中,细胞核靶向部分可以是偶联至脂质体或水凝胶,而不是偶联至外源τβ4、sox2和/或oct4(或除此之外)。
外源蛋白质可以使用本领域已知的重组技术产生。发明人设想可以从单个表达序列翻译tβ4、sox2和oct4。或者,表达序列可包括τβ4和sox2、τβ4和oct4、sox2和oct4、τβ4、sox2、oct4及其任何组合。可以使用原核生物(例如大肠杆菌)、酵母菌(例如酵母、毕赤酵母、克鲁维酵母、汉逊酵母和耶氏酵母)或真核细胞(例如hek293和cho)来产生外源蛋白质。还考虑了昆虫细胞和无细胞方法。
发明人考虑了根据本发明主题的诱导多能干细胞将在至少5代、至少10代、至少20代、至少50代,优选至少100代中保持多能性。
本发明的主题还包括一种组合物,该组合物包括外源tβ4、外源sox2和外源oct4,可诱导非胚性细胞/体细胞中的多能性。在预期的组合物中,外源tβ4、外源sox2和外源oct4中的至少两种通过连接子偶联。换句话说,连接子偶联τβ4和sox2、τβ4和oct4或sox2和oct4。连接子也可以用于偶联τβ4、sox2和oct4。
细胞膜穿透部分(例如,阳离子肽)和/或细胞核靶向部分(例如,谷胱甘肽-s-转移酶)可以与外源tβ4、外源sox2和/或外源oct4偶联。细胞核靶向部分可以任选地与外源tβ4、外源sox2和外源oct4中的至少一种偶联。
图1示出了在体细胞(非胚性)细胞中诱导多能性的方法的流程图。在步骤(1)中,将τβ4、sox2和oct4蛋白引入体细胞。在步骤(2)中,将步骤(1)的体细胞在诱导体细胞去分化的条件下培养以获得诱导多能干细胞。在任选的步骤(3)中,在使得诱导多能干细胞在传代10、20、50或100次后保持多能性的条件下培养诱导多能干细胞。
实施例1
28天内每12小时用12mg/ml重组标记蛋白转染成纤维细胞或脂肪细胞,以对细胞进行程序重调。用em培养基(最好是条件em培养基)在饲养细胞上培养。选择ips菌落进行扩大。参见例如,kejinhu,allroadsleadtoinducedpluripotentstemcells:thetechnologiesofipscgeneration,23(12)stemcellsanddevelopment1285-1300(2014);xiao-yuedengetal,non-viralmethodsforgeneratingintegration-free,inducedpluripotentstemcells,10currentstemcellresearch&therapy153-58(2015)。
转化的ipsc将用碱性磷酸酶染色以检测多能干细胞标志物的表达,例如ssea-1、
ssea-3、ssea-4、tra-1-60、tra-1-81、tra-2-49/6e和/或nanog。
可以通过测试胚状体和/或畸胎瘤的形成来进一步测试程序重调。请参见kazutoshitakahashietal,inductionofpluripotentstemcellsfromadulthumanfibroblastsbydefinedfactors,131cell861-72(2007)。诱导多能性也可以通过产生嵌合小鼠来证实。请参见csillanemesetal,generationofmouseinducedpluripotentstemcellsbyproteintransduction,20(5)tissueengineering:partc383-392(2014)。
对于本领域的技术人员应当显而易见的是,在不背离本文的发明构思的前提下,除了已经描述的修改之外,还可以进行更多修改。因此,除了所附权利要求的范围之外,本发明主题不受限制。此外,在解释说明书和权利要求书时,应以与上下文一致的尽可能广泛的方式解释所有术语。特别地,术语“包括”和“包含”应被解释为以非排他性的方式指代元件、组件或步骤,指示所引用的元件、组件或步骤可以存在、利用或组合。以及其他未明确引用的元件、组件或步骤。说明书、权利要求所指的选自a、b、c...和n中的至少一种,该文本应解释为仅需要组中的一个元件,而不是a加n或b加n等。
- 还没有人留言评论。精彩留言会获得点赞!