一种金雀花碱N-异黄酮类化合物及其制备方法及应用与流程
本发明涉及药物合成技术领域,具体涉及一种金雀花碱n-异黄酮类化合物及其制备方法及应用。
背景技术:
金雀花碱(cytisine)是由husemann和marme在1865年从cytisuslaburnummed的种子中首次分离出来,多分布在金链花、野决明属、金雀花属、槐属植物中。该生物碱具有增强心肌收缩力、兴奋呼吸、增强运动能力、改善认知功能、抗抑郁、镇痛、抗肿瘤等药理作用,特别是该类化合物较强的抗癌活性。金雀花碱属于喹诺里嗪生物碱,其结构修饰集中在12位n的衍生化,主要有烷基化、酰基化、苄基化、苯甲酰基化、糖苷化等。
异黄酮类化合物(isoflavonoid)是一类基本母核是3-苯基色原酮的一类化合物,广泛存在于豆科植物中和牧草等中,是一类植物次生代谢产物。近几十年来,随着现代分离技术和结构研究方法发展,人们从植物或动物或海洋生物中分离得到各种异黄酮类化合物,许多研究发现这一类化合物具有多种的生物活性和良好的药理作用,如抗肿瘤、抗高血糖、抗真菌、抗病毒、抗炎、抗氧化剂和心血管疾病等,是一类有价值的药物是一类有价值的药物,在药物研发领域,利用拼接策略将多个活性分子通过特定化学键连接在一起,为人们寻找新型的活性分子开辟了崭新的视野。
技术实现要素:
本发明的目的就是为了克服上述现有技术存在的缺陷而提供一种金雀花碱n-异黄酮类化合物及其制备方法及应用。
本发明的目的可以通过以下技术方案来实现:一种金雀花碱n-异黄酮类化合物,该化合物的结构式如下:
其中,r1选自羟基、烷氧基、胺基或卤基中的一种,r2选自氢、烷基或芳基中的一种,r3选自羟基、烷氧基、胺基或卤基中的一种或几种组合。
采用discoverystudio4.5软件进行分子模拟,从中我们得到结论,本发明的化合物分子基本处于her2受体蛋白的活性空腔中心,被asp26、pro360、ala233、his229、leu275等多个氨残基包围,形成了较强的疏水作用。这些残基在底物分子周围组成了her2蛋白的活性口袋。其中底物分子5-oh、7-oh与asp26、ala233氨基酸残基形成双氢键,是主要的药效基团,故5-or2必须为能与asp26氨基酸残基形成氢键的官能团。
所述的化合物还包括上述结构式所对应的盐,所述盐通过上述结构式对应的物质与无机酸或有机酸反应制得,其中,所述无机酸包括盐酸、氢溴酸、硫酸、硝酸、胺基磺酸或磷酸中的一种,所述有机酸选自柠檬酸、酒石酸、乳酸、丙酮酸、乙酸、苯磺酸、对甲苯磺酸、甲磺酸、萘磺酸、乙磺酸、萘二磺酸、马来酸、苹果酸、丙二酸、富马酸、琥珀酸、丙酸、草酸、三氟乙酸、硬酯酸、扑酸、羟基马来酸、苯乙酸、苯甲酸、水杨酸、谷氨酸、抗坏血酸、对胺基苯磺酸、2-乙酰氧基苯甲酸或羟乙磺酸中的一种。
一种如上所述金雀花碱n-异黄酮类化合物的制备方法,包括以下步骤:
(1)在
(2)将步骤(1)制备得到
(3)将步骤(2)制备得到的
优选的,步骤(1)中,
优选的,步骤(2)中,
优选的,在步骤(3)中,
一种如上所述金雀花碱n-异黄酮类化合物的应用,该化合物用于制备治疗肿瘤的药物,如乳腺癌。
与现有技术相比,本发明的有益效果体现在以下几方面:
(1)制备方法高效、易于操作,且产物纯度高;
(2)可有效抑制癌细胞的迁移,具有良好的癌症治疗效果。
附图说明
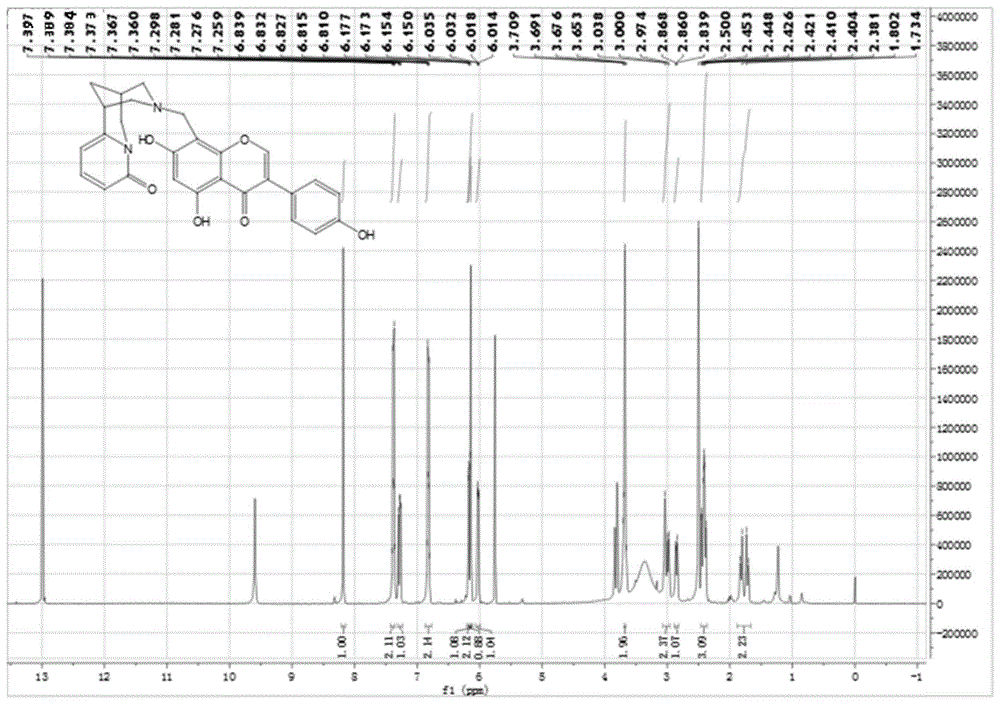
图1为实施例1制得的化合物的氢谱;
图2为实施例1制得的化合物的碳谱;
图3为实施例1制得的化合物的质谱;
图4为实施例1~3制备得到的化合物在不同浓度下对mda-mb-231乳腺癌细胞迁移能力的抑制结果测试图;
图5为实施例1~3制备得到的化合物在不同浓度下对4t1乳腺癌细胞迁移能力的抑制结果测试图;
图6为实施例1制得的化合物与her2受体蛋白作用图。
具体实施方式
下面对本发明的实施例作详细说明,本实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围不限于下述的实施例。
实施例1
化合物cnf1的合成,结构式如下:
制备步骤如下:
(1)7-甲氧基甲醚-5-羟基-3-碘色原酮的合成;(2)金雀异黄酮的合成;(3)金雀异黄酮和金雀花碱以曼尼希反应合成目标物。
具体工艺如下:
(1)以2,4,6-三羟基苯乙酮为原料,加入2.1倍当量的k2co3选择性使4、6位的羟基游离出来,然后加入2.12倍当量的氯甲基甲醚,得到2-羟基-4,6-二甲基甲醚苯乙酮,然后加入n,n-二甲基二甲缩醛在74℃的温度下以88%的产率合成氨烯酮,最后以一步简单的成环反应即在单质碘的作用下以75%的收率完成5,7-二甲基甲醚-3-碘色酮的合成。3-碘色原酮4溶于二氯中并置于搅拌器上以中速搅拌4h,脱去5位的甲基甲醚得3-碘色原酮5;结构式变化如下:
(2)化合物5和6在suzuki偶联反应下合成异黄酮7,在3mhcl下脱去7位的甲基甲醚,之后在三溴化硼下脱去甲氧基得金雀异黄酮9,结构式变化如下:
(3)金雀花碱和金雀异黄酮、福尔马林在dmap的催化下合成金雀花碱-n-亚甲基-(5,7,4’-三羟基)异黄酮cnf1,结构式变化如下:
向化合物9(0.5mmol)的异丙醇(5ml)溶液中加入金雀花碱(0.625mmol)和formalin(0.25ml,37%)、dmap(1.2mg),在氮气下,将其置于油浴中加热反应3h-overnight。tcl监测反应完全,快速柱层析纯化,得到化合物cnf1。
将制备得到的cnf1进行核磁及质谱分析,得到的氢谱、碳谱、质谱分别如图1、2、3所示。
1hnmr(400mhz,dmso)cytisineprotons:7.26(1h,dd,j=6.8;8.8,h-4),6.15(1h,dd,j=1.6;9.2,h-3),6.01(1h,dd,j=1.2;7.2,h-5),3.65,3.80(2h,2d,j=14.8,ch2-10),2.84-3.04(3h,m,h-11,13,7),2.38-2.50(3h,m,h-11,13,9),1.70-1.83(2h,m,ch2-8)。isoflavoneprotons:8.18(1h,s,h-2),7.37(2h,d,j=8.8,h-2',6'),6.81(2h,d,j=8.8,h-3’,5’),6.14(1h,s,h-6),3.68(2h,s,ch2-8)。13cnmr(100mhz,dmso)180.8,164.1,162.6,161.2,157.8,155.8,154.1,151.8,139.1,130.6,122.4,121.6,116,115.5,104.5,104.3,100.8,98.9,59.9,59.3,55.3,50.5,49.8,34.8,27.7,25.2。hrms(esi):m/z=471.16(calcd.471.16forc27h23n2o6[m-h]-)。m.p.=237-239℃。
从中我们可以分析出:从上述氢谱、碳谱及质谱可以确证其结构为金雀花碱-n-亚甲基-(5,7,4’-三羟基)异黄酮化合物,即化合物cnf1。
将制备得到的cnf1采用discoverystudio4.5软件进行分子模拟,其结果如图6所示,从图中可以看出,cnf1分子基本处于her2受体蛋白的活性空腔中心,被asp26、pro360、ala233、his229、leu275等多个氨残基包围,形成了较强的疏水作用。这些残基在底物分子周围组成了her2蛋白的活性口袋。其中底物分子5-oh、7-oh与asp26、ala233氨基酸残基形成双氢键,是主要的药效基团,故5-or2必须为能与asp26氨基酸残基形成氢键的官能团。
实施例2
化合物cnf2的合成,结构式如下:
其中r1=oh,r2=h,r3=r4=och3。具体制备步骤如下:
(1)制备异黄酮中间体,合成路线如下:
取化合物19化合物与3,4-二甲氧基苯硼酸进行suzuki偶联反应得到异黄酮化合物21,具体步骤:
将聚乙二醇10000(21g),和pd(oac)2(0.025g,0.11mmol)加入到含碳酸钠(0.548g,5.17mmol)的甲醇(25ml)溶液中,在但氮气下置于50℃的油浴下搅拌直至体系变成黑色后,马上将化合物19(0.820g,2.17mmol)和3,4-二甲氧基苯硼酸(1.395g,5.41mmol)的混合物加入到体系内。反应3h,tcl显示反应完全。加入水,使peg10000成固体析出,过滤,用乙酸乙酯洗涤析出的固体,将乙酸乙酯洗涤液和水相合并,并用乙酸乙酯萃取,有机层用无水硫酸钠干燥,减压除去溶剂,快速柱层析(pe:ea=8:1)得到白色固体化合物21(93%)
将化合物21(0.2g,0.43mmol)加入到甲醇溶液中,加入3mhcl并将其加热回流反应2h,tcl监测反应完全。加入水,并用二氯萃取,依次用水、浓盐水洗涤、无水硫酸钠干燥。减压旋去溶剂得到残留物,快速柱层析(pe:ea=4:1)得到白色固体异黄酮化合物21(0.11mg,91%)
(2)金雀花碱和异黄酮21、福尔马林在dmap的催化下合成金雀花碱-n-亚甲基-异黄酮cnf2。
向化合物21(0.5mmol)的异丙醇(5ml)溶液中加入金雀花碱(0.625mmol)和formalin(0.25ml,37%)、dmap(1.2mg),在氮气下,将其置于油浴中加热反应3h-overnight。tcl监测反应完全,快速柱层析纯化,得到化合物cnf2。
实施例3
化合物cnf3的合成,结构式如下:
其中r1=oh,r2=h,r3=h,r4=och3,具体制备步骤如下:
(1)制备异黄酮中间体,合成路线如下:
具体步骤基本同上实施方式二,关键中间体替换为对甲氧基苯硼酸,合成条件略调整,见技术路线中所示,
(2)金雀花碱和异黄酮20、福尔马林在dmap的催化下合成金雀花碱-n-亚甲基-异黄酮cnf3。
具体步骤同实施方式二,异黄酮替换为化合物20,其余不变。
药理活性检测:
以上cnf1-cnf3三个化合物抗肿瘤转移活性实验结果:
利用两种肿瘤细胞和细胞划痕实验模型研究三种样品对迁移能力的影响
分别取对数生长状态的乳腺癌mda-mb-231细胞和乳腺癌4t1细胞均匀种在costar6孔板中,每孔终体积为50%总体积,细胞密度控制在约1.5×105个/ml。每孔设3个复孔,实验重复5次。待细胞即将铺满后弃上清,用无菌接种环在每孔底部中央的纵向划一条模拟创伤的直线(创伤区),显微镜下测量创伤区宽度。用新培养基清洗3次,洗去漂浮的细胞,空白组中搅入不含药物的无血清培养基。样品分别溶于无血清培养基,实验组中加入三种化合物样品的溶液,至终浓度为10μm、30μm和90μm。分别于加样后和阴性对照组划线即将消失时显微镜下拍照各组创伤区并显微镜下测量创伤区的宽度,计算迁移距离、迁移比率(肿瘤细胞迁移距离/创伤区初始宽度)。三种化合物均样品可以抑制mda-mb-231细胞的迁移,创伤区肿瘤细胞迁移距离缩短,与空白组相比,各给药组迁移比率明显下降(*p<0.05,**p<0.01),且随着化合物剂量的增大,迁移比率下降更大,说明该抑制作用具有剂量依赖性(如图4所示)。三种化合物样品对乳腺癌4t1细胞的迁移能力抑制效果如图5所示,迁移比率明显下降。从图4和图5中可以看出,3种化合物抗肿瘤细胞迁移效果与阳性药物接近,具有较好的体外抗乳腺癌肿瘤细胞转移活性。
- 还没有人留言评论。精彩留言会获得点赞!