一种基于低共熔溶剂的脂氨基酸类化合物的制备方法与流程
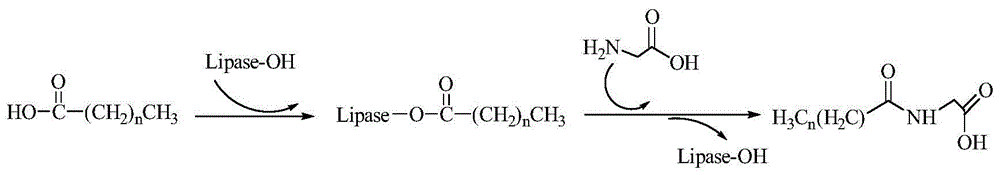
本发明涉及一种基于低共熔溶剂的脂氨基酸类化合物的制备方法,属于有机合成领域。
背景技术:
表面活性剂由于其独特的性质在食品领域内常被用于乳化剂、增稠剂、消泡剂等诸多方面,被称为“工业味精”,具有很大的需求量。近年来关于脂氨基酸类表面活性剂的研究成为热点。传统脂氨基酸类表面活性剂多为季铵盐类,虽具有良好的表面活性以及抑菌性,但也存在一定的细胞毒性强,限制了其在食品领域内的大量应用。相对于传统表面活性剂,脂氨基酸类表面活性剂具有更高的安全性,在食品领域内具有较好的应用前景。
目前,关于脂氨基酸类表面活性剂的合成研究多集中于化学法,对环境产生极大污染。酶法合成过程多采用有机溶剂作为反应体系,不仅不利于环境,且很容易导致酶的变性失活。2018年bernal等在foodchemistry期刊报道了利用脂肪酶以及蛋白酶为催化剂,以丙酮-水为体系,合成了月桂酰甘氨酸,产物得率为40%。wada,handa,imamura,sakiyama,adachi,matsuno,etal.(2002)在无溶剂体系中以脂肪酶novozyme435为催化剂合成了甘油酰精氨酸表面活性剂,其合成得率仅为15%。如何寻找一种合适的绿色溶剂已经成为了限制其合成以及应用的一大难题。
天然低共熔溶剂在酯化反应中已经得到了较多的应用,与酯化反应不同的是,脂肪酸与氨基酸的反应通常会生成季铵盐、而非脂氨基酸,为了提高脂氨基酸的得率,目前多采用两步法进行,即首先对脂肪酸或进行活化,而后进行氨基酸的亲核反应。因此,存在副产物多、产物合成效率低等问题。
技术实现要素:
为了克服上述现有技术的不足,本发明提供了一种基于低共熔溶剂的脂氨基酸类表面活性剂酶法制备方法。本发明所采用的技术方案包括:以脂肪酸、氨基酸为原料,脂肪酶calb作为催化剂,低共熔溶剂为介质,一步法直接合成脂氨基酸,并采用简单、高效的水洗-甲醇重结晶法直接得到纯度较高的产物本发明方法简便、绿色、安全、高效。
本发明的第一个发明目的是提供一种脂氨基酸类化合物的制备方法,所述方法包括:
以低共熔溶剂为介质,脂肪酸、氨基酸在催化剂作用下直接制备得到脂氨基酸类化合物。
在本发明的一种实施方式中,脂肪酸与氨基酸的摩尔比为1:1~2:1。
在本发明的一种实施方式中,所述氨基酸包括甘氨酸、赖氨酸、精氨酸、丙氨酸。
在本发明的一种实施方式中,所述脂肪酸为c2-c20脂肪酸。
在本发明的一种实施方式中,所述脂肪酸包括月桂酸、棕榈酸。
在本发明的一种实施方式中,所述催化剂包括脂肪酶calb。
在本发明的一种实施方式中,针对酰胺化反应的特点以及氨基酸、脂肪酸的溶解度对目前常用的低共熔溶剂进行了筛选,低共熔溶剂包括甜菜碱-甘油、甜菜碱-木糖醇、氯化胆碱-甘油、氯化胆碱-木糖醇中的任意一种。
在本发明的一种实施方式中,所述的低共熔溶剂是由氢键供体和氢键受体在60-100℃条件下按照一定化学计量比,经过旋转蒸发获得。
在本发明的一种实施方式中,氢键供体以及氢键受体的化学计量比为2:1~1:2。
在本发明的一种实施方式中,所述方法是在40-60℃,ph值7.0-8.0,搅拌速度200-300rpm下进行。
在本发明的一种实施例中,水的用量为反应体系的50%~100%(v/v)。
本发明的第二个目的是提供一种表面活性剂的制备方法,所述方法是预先制备脂氨基酸类化合物,然后在进行表面活性剂的制备,所述脂氨基酸类化合物的制备方法为上述方法。
本发明的第三个目的是提供一种乳化剂,所述方法是预先制备脂氨基酸类化合物,然后在进行乳化剂的制备,所述脂氨基酸类化合物的制备方法为上述方法。
本发明的第四个目的是提供一种增稠剂,所述方法是预先制备脂氨基酸类化合物,然后在进行增稠剂的制备,所述脂氨基酸类化合物的制备方法为上述方法。
本发明的第五个目的是提供一种消泡剂,所述方法是预先制备脂氨基酸类化合物,然后在进行消泡剂的制备,所述脂氨基酸类化合物的制备方法为上述方法。
与现有技术相比,本发明的有益效果是:
本发明利用绿色安全的天然低共熔溶剂替代传统的有机试剂为反应介质,无需水作为辅助混合溶剂,不仅极大程度的减小了对环境的污染,且由于天然低共熔溶剂良好的底物溶解性,以及能够较好的保持酶的稳定性以及活性,极大程度的改变了传统有机溶剂酶法合成脂氨基酸过程中底物溶剂性低,脂肪酶活性差的现状。反应产率显著高于目前已报道其他方法的脂氨基酸的酶法合成。
此外,目前天然低共熔用于酶法合成多采用底物转化率进行表征,并不能说明产物得率的高低,且基本没有涉及产物的纯化过程,本发明采用了简单高效的水洗-甲醇重结晶法得到纯度较高的产物,极大程度简化了酶法合成脂氨基酸的纯化过程。
附图说明
图1脂氨基酸的合成路线图;
图2不同天然低共熔溶剂中甘氨酸酸(a)、月桂酸(b)溶解度;每种温度下从左向右的溶剂分别为甜菜碱-甘油(b-gly)、甜菜碱-木糖醇(b-x)、氯化胆碱-甘油(c-gly)、氯化胆碱-木糖醇(c-x)、甜菜碱-甘油-水(b-gly-w)、氯化胆碱-甘油-水(c-gly-w);
图3不同天然低共熔溶剂中脂肪酶的活性,每种时间下从左向右的溶剂分别为tris缓冲液(50mm,ph8.0)(对照组)、甜菜碱-甘油(b-gly)、甜菜碱-木糖醇(b-x)、氯化胆碱-甘油(c-gly)、氯化胆碱-木糖醇(c-x)、甜菜碱-甘油-水(b-gly-w)、氯化胆碱-甘油-水(c-gly-w);
图4不同天然低共熔溶剂中脂肪酶的热稳定性;每种时间下从左向右的溶剂分别为甜菜碱-甘油(b-gly)、甜菜碱-木糖醇(b-x)、氯化胆碱-甘油(c-gly)、氯化胆碱-木糖醇(c-x)、甜菜碱-甘油-水(b-gly-w)、氯化胆碱-甘油-水(c-gly-w);
图5产物的鉴定图谱:a为红外光谱;b为质谱;c为核磁共振氢谱图及其相应图谱数据图表。
具体实施方式
本发明的主要思路在于:为脂氨基酸的酶法合成提供了新的思路,即采用了一系列具有良好的底物溶解性的酶友好型溶剂。本发明首先考察了天然低共熔溶剂对底物的溶解性,其次,又考察了溶剂对酶的活性以及稳定性的影响及其机制;最后,进行了脂氨基酸的合成实验,合成过程包括两个步骤:1)脂肪酶与脂肪酸结合,完成对脂肪酸的活化;2)氨基酸的氨基对活化后的脂肪酸中间体亲核进攻,形成酰胺。具体步骤如图1所示。
下面结合具体的实施例对本发明做进一步详细的说明。
实施例1
分别称取25mm的月桂酸以及25mm的甘氨酸,于25ml反应瓶中.向其中加入10ml天然低共熔溶剂(氯化胆碱-甘油),以及12.5mg脂肪酶calb。然后将反应瓶密封并置于恒温水浴摇床,60℃,2000rpm下持续反应48h。
反应结束后,取出反应瓶,加入大量的水,剧烈震荡,然后10000rpm离心10min,离心后,真空抽滤得到白色固体,加入甲醇,对粗产物重结晶两次,得到纯度为98%的纯产物。产物得率为50.49%。
通过图5中的质谱可以看出,产物中没有出现脂氨基酸合成过程中常见的副产物---二肽,具有较高的产物得率且同时副产物少。
采用电导率法测定了几种产物的cmc值,月桂酰甘氨酸0.0044mol/l,显著低于目前市面常用表面活性剂吐温十二烷基磺酸钠(0.009mol/l),是一种性能较好的表面活性剂。
实施例2
分别称取25mm的月桂酸以及25mm的甘氨酸,于25ml反应瓶中.向其中加入10ml天然低共熔溶剂(甜菜碱-甘油),以及12.5mg脂肪酶calb。然后将反应瓶密封并置于恒温水浴摇床,60℃,2000rpm下持续反应48h。
反应结束后,取出反应瓶,加入大量的水,剧烈震荡,然后10000rpm离心10min,离心后,真空抽滤得到白色固体,加入甲醇,对粗产物重结晶两次,得到纯度为98%的纯产物。产物最终得率为43.98%。
实施例3
分别称取25mm的月桂酸以及25mm的甘氨酸,于25ml反应瓶中.向其中加入10ml天然低共熔溶剂(甜菜碱-木糖醇),以及12.5mg脂肪酶calb。然后将反应瓶密封并置于恒温水浴摇床,60℃,2000rpm下持续反应48h。
反应结束后,取出反应瓶,加入大量的水,剧烈震荡,然后10000rpm离心10min,离心后,真空抽滤得到白色固体,加入甲醇,对粗产物重结晶两次,得到纯度为98%的纯产物。产物最终得率为38.97%。
实施例4
分别称取25mm的月桂酸以及25mm的甘氨酸,于25ml反应瓶中.向其中加入10ml天然低共熔溶剂(氯化胆碱-木糖醇),以及12.5mg脂肪酶calb。然后将反应瓶密封并置于恒温水浴摇床,60℃,2000rpm下持续反应48h。
反应结束后,取出反应瓶,加入大量的水,剧烈震荡,然后10000rpm离心10min,离心后,真空抽滤得到白色固体,加入甲醇,对粗产物重结晶两次,得到纯度为98%的纯产物。产物最终得率为41.40%。
实施例5:考察低共熔溶剂对反应底物的影响
准确称取10g天然低共熔溶剂(c-gly),于60℃恒温震荡水浴中,待温度恒定,称取10mg月桂酸加入其中,200rpm下震荡30min,然后用毛细管取出一滴在偏光显微镜下检测,如不出现偏振光,则说明溶解完全,则再次加入10mg月桂酸。直至不再继续溶解(出现偏振光)。最终底物溶解度按照如下公式计算:
s=mt×10/1000(1),
这里s为溶剂度,mt为总的底物添加量。最终月桂酸溶解度为24.98(g/100g)。
月桂酸在常用酶友好型溶剂丙酮中为微溶(0.01-0.1g/100g),在水中的溶解度为0。
甘氨酸在低共熔溶剂中的溶解度为22.78(g/100g),水中溶解度为25g/100g,丙酮中几乎不溶。
从图2可知,不同低共熔溶剂对两种底物的溶解度影响不一,其中在c-gly-w的溶解性最好,底物普适性也较好。
实施例6:考察不同低共熔溶剂对脂肪酶催化剂的影响
通过pnpp测定法测量脂肪酶活性以及热稳定性:将10μl酶溶液,加入到3990μlnades(pbs缓冲液,ph8.0,作为对照)中,在60℃(calb的最佳温度)下以200rpm的速度反应120min,240min和360min。立即从中取出10μl,并加入80μlpbs缓冲液(50mm,ph8.0)和10μlpnpp溶液中。将混合物在60℃,200rpm下反应5min,加入100μl乙醇(95%)立即终止反应。用spectramax190酶标仪(moleculardevices,german)在405nm处测量吸光度。根据pnp计算酶活性以及热稳定性。
结合图3可知,脂肪酶calb在nades中经过60℃,360min处理后依然能够保持较高的活性,可达6400u/ml。结构刚性和柔韧性之间的平衡是脂肪酶的高稳定性和活性的基础。nades可与酶相互作用以增加其结构刚性,从而提高其稳定性。此外,令人意想不到的是,如图3所示,在没有水的四种nades中,脂肪酶在360分钟后仍保持较高的活性;而在有参与的体系中,酶活逐渐收到抑制。发明人认为可能是因为酶表面可以与nades键合,如甘油,木糖醇等,这些有机小分子可以与酶形成复杂的氢键网络。
如图4所示,水分的存在削弱了nades与酶的相互作用,降低了酶的结构刚性和抵抗外部干扰的能力,导致脂肪酶的热稳定性降低,与酶活的效果趋势一致。
对照例1:
参照实施例1,将溶剂有低共熔溶剂替换为丙酮,其他条件不变,产物得率基本可以忽略不计。
上述实施例只为说明本发明的技术构思及特点。其目的在于让熟悉此项技术的人能够了解本发明的内容并据此加以实施。并不能以此限制本发明的保护范围,凡根据本发明精神实质所做的等效变化或修饰,都应该涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!