使用亲和色谱法的用于疫苗病毒的纯化方法与流程
本公开涉及使用亲和色谱法的用于疫苗病毒的分离和纯化方法,并且更具体地,涉及能够使用含有病毒亲和树脂的亲和色谱法来获得高纯度且高产率的疫苗病毒的用于病毒的分离和纯化方法。
背景技术:
在使用源自除人以外物种的细胞作为宿主细胞培养的疫苗病毒中,有必要去除宿主源性材料。为了去除宿主源性材料,在现有技术中,已使用了糖密度梯度离心法、尺寸排阻色谱法或离子交换色谱法。作为病毒纯化中常用的方法,这些方法比亲和色谱法更多地使用,因为这些方法不管病毒的类型如何都可以轻松应用。
糖密度梯度离心法是使用糖产生的密度差来纯化病毒的方法,并作为最传统且最古老的方法,它是研究初始阶段最常用的方法,因为它不需要单独的过程研究。为了将该方法应用于工业生产阶段,另外还需要昂贵的设备,且需要增加诸如用于去除糖的透析过程或尺寸排阻色谱法的过程,因此存在总加工时间长的缺点。研究中还报告了糖的粘度和高渗透压会影响病毒的感染性蛋白,降低过程的总体病毒产率(penghh等人,(2006)analbiochem,354(1):140-147)。
尺寸排阻色谱法是由于蛋白质修饰或渗透压而失效的方法,并且在现有技术(cn101695570b、cn101780278b)中,公开了使用尺寸排阻色谱法制备手足口病的灭活疫苗。然而,在尺寸排阻色谱法中,因为作为预处理过程而涉及过度浓缩过程,所以存在以下缺点,也就是说,因为病毒结构由于浓缩过程而破坏或产率由于增加了过程而降低。此外,在尺寸排阻色谱法中,因为规模扩大受到限制,所以其在研究阶段的应用相对容易,但是其在工业大量生产的规模上的应用受到限制。
已经使用离子交换色谱法进行了研究,其可以不考虑病毒样品的体积而使用(cn101695570b,ashokrajkatturvenkatachalam等人,(2014)virologyjournal,11:99)。大多数研究是通过以下方法进行的:将病毒吸附到带电荷的树脂(例如deae)上,然后用盐浓度高的缓冲液洗脱吸附的病毒。但是,为了使用离子交换色谱法,需要进行透析过程以降低样品的盐浓度,并且存在由于增加了过程而降低了收率的缺点。此外,因为病毒由各种类型的蛋白质而不是单一蛋白质组成,所以病毒具有各种电荷,因此需要进行用于维持病毒洗脱条件的过程研究。此外,存在电荷与病毒类似的杂质可能一起被洗脱的缺点。
技术实现要素:
技术问题
在这种背景下,本发明人努力寻找以高纯度和高产率纯化疫苗病毒的方法,并因此,他们发现了当使用亲和色谱法时能够以高纯度和高产率获得疫苗病毒的方法,从而完成了本公开。
技术方案
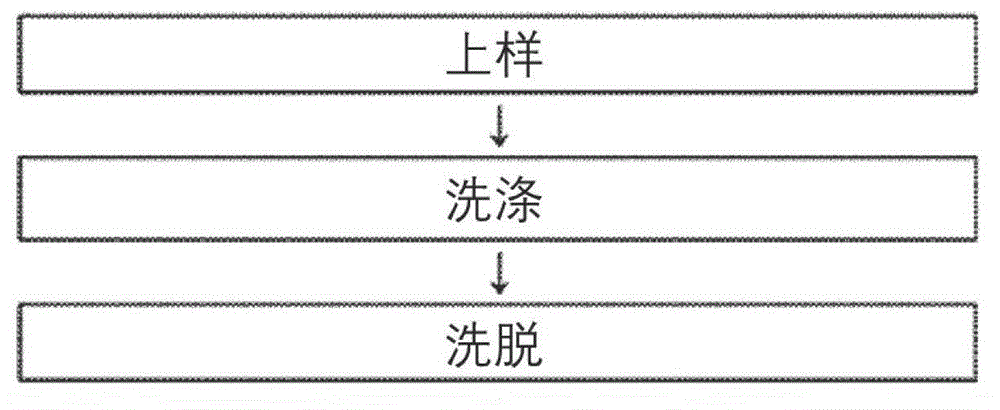
本公开的一方面提供了一种用于疫苗病毒的纯化方法,其包括:(a)将含有疫苗病毒的样品上样至含有病毒亲和树脂的亲和色谱柱上;(b)用洗涤溶液洗涤亲和色谱柱;以及(c)使用洗脱溶液从亲和色谱柱回收所需疫苗病毒。
本公开的另一方面提供了一种根据所述纯化方法纯化的疫苗病毒。
有益效果
根据本公开的纯化方法,尽管去除了除所需疫苗病毒以外的大多数杂质,但是可以以适合大量生产的高纯度和高产率纯化疫苗病毒。
附图说明
图1示出了进行本公开的纯化方法的程序。
图2和图3示出了使用含有硫酸葡聚糖的captotmdevirs树脂纯化疫苗病毒的结果。
图4和图5示出了使用含有肝素的hitrapheparin树脂纯化疫苗病毒的结果。
图6和图7示出了使用fractogeldeae树脂纯化疫苗病毒的结果。
图8和图9示出了使用fractogeltmae树脂纯化疫苗病毒的结果。
图10和图11示出了使用cimdeae树脂纯化疫苗病毒的结果。
具体实施方式
在下文中,将更详细地描述本公开。
同时,本公开中所公开的每个描述和实施方式也可以应用于其他描述和实施例中的每个。也就是说,本公开中所公开的各种组件的所有组合都属于本公开的范围。此外,本公开的范围可以不受以下具体描述的限制。
此外,本领域的技术人员可以通过仅使用一般实验来认识或确定本公开中所描述的本公开的具体实施方式的多个等效物。此外,此类等效物旨在被包括在本公开中。
图1示出了进行本公开的纯化方法的程序的实例。
参考图1,本公开的一方面提供了一种用于疫苗病毒的纯化方法,其包括:(a)将含有疫苗病毒的样品上样至含有病毒亲和树脂的亲和色谱柱上;(b)用洗涤溶液洗涤亲和色谱柱;以及(c)使用洗脱溶液从亲和色谱柱回收所需疫苗病毒。
用于疫苗病毒的纯化方法的每个步骤将如下详细描述。首先,步骤(a)是将含有疫苗病毒的样品上样至含有病毒亲和树脂的亲和色谱柱上的步骤。
对材料和制造方法没有限制,只要含有疫苗病毒的样品含有疫苗病毒即可。具体地,含有疫苗病毒的样品可以包括肠道病毒,但不限于此。样品可以由除人源性细胞以外的宿主细胞制备,但不限于此。
本公开中所使用的“亲和色谱法”是指使用以亲和力结合具体蛋白质的材料的色谱法。以亲和力结合具体蛋白质的材料是其中官能团与聚合物材料缀合的材料,并且结合与溶解于极性或非极性溶液中的具有亲和力的材料。
出于本公开的目的,亲和色谱法可以是含有疫苗病毒亲和树脂的亲和色谱法具体地,可以使用能够特异性结合疫苗病毒蛋白质的树脂进行色谱法。例如,疫苗病毒亲和树脂可以包括选自硫酸葡聚糖、肝素及其混合物的至少一种树脂。例如,疫苗病毒亲和树脂包括captotmdevirs(gehealthcare)和hitrapheparin(gehealthcare),但不限于此,并且任何能够特异性结合疫苗病毒蛋白质的树脂都是可能的。
例如,captotmdevirs树脂含有硫酸葡聚糖,hitrapheparin树脂含有肝素,并且树脂可以特异性结合疫苗病毒蛋白质。
在一个实施方式中,在步骤(a)中上样含有疫苗病毒的样品之前,可以用ph7.5至ph8.0的平衡溶液使柱平衡。具体地,平衡溶液可包含选自由磷酸钠、氯化钠、tris-hcl、2-(n-吗啉代)乙磺酸(mes)、3-吗啉代丙-1-磺酸(mops)、pipes、磷酸钾、氯化钾和2-[4-(2-羟乙基)哌嗪-1-基]乙磺酸(hepes)组成的组中的至少一种盐,但不限于此。
在一个实施方式中,所述方法可以进一步包括在步骤(a)之前进行离子交换色谱法、浓缩和/或透析。此步骤是通过去除含有疫苗病毒的样品中的主要杂质来增加样品的纯度。具体地,在步骤(a)之前,将含有疫苗病毒的样品浓缩并透析,并且在通过离子交换色谱法预先进行纯化之后,可以使用亲和树脂将含有疫苗病毒的样品上样至亲和色谱柱上。可以施加用于去除不结合亲和树脂的主要杂质并增强样品纯度的任何操作而没有限制。
在一个实施方式中,使用亲和色谱法的用于疫苗病毒的纯化方法的特征在于,在亲和色谱法之前不进行单独的浓缩或透析过程。在这种情况下,虽然过程简单,但是可以获得高产率且高纯度的结果。
在用于疫苗病毒的纯化方法中,步骤(b)是将洗涤溶液施加至上样了样品的色谱柱上的步骤,作为用洗涤溶液洗涤样品的步骤。
洗涤溶液可具有ph7.5至ph8.0的范围。具体地,洗涤溶液可包含选自由磷酸钠、氯化钠、tris、2-(n-吗啉代)乙磺酸(mes)、3-吗啉代丙-1-磺酸(mops)、pipes、磷酸钾、氯化钾和2-[4-(2-羟乙基)哌嗪-1-基]乙磺酸(hepes)组成的组中的至少一种盐,但不限于此。
出于本公开的目的,在步骤(b)中,可以通过洗涤溶液去除非特异性结合疫苗病毒亲和树脂的杂质。
在一个实施方式中,纯化方法可进一步包括在步骤(a)或(b)之后用平衡溶液排出与树脂不具有亲和力的杂质的步骤。此步骤可以特别地进行至少一次,但是通常可以不受限制地进行直到达到平衡。
在一个实施方式中,纯化方法可进一步包括在步骤(a)或(b)之后用再平衡溶液进行再平衡的步骤。再平衡溶液在洗涤步骤与洗脱步骤之间不与任何物质反应,在与未洗脱所需疫苗病毒的步骤(a)中的平衡溶液相同的条件下流动,然后在洗脱溶液流动之前流动以充当洗涤溶液与洗脱溶液之间的桥梁。
具体地,再平衡溶液可具有ph7.5至ph8.0的范围。具体地,再平衡溶液可包含选自由磷酸钠、氯化钠、tris-hcl、2-(n-吗啉代)乙磺酸(mes)、3-吗啉代丙-1-磺酸(mops)、pipes、磷酸钾、氯化钾和2-[4-(2-羟乙基)哌嗪-1-基]乙磺酸(hepes)组成的组中的至少一种盐,但不限于此。
在用于病毒的纯化方法中,步骤(c)是使用洗脱溶液从亲和色谱柱回收所需疫苗病毒的步骤。
洗脱溶液可具有ph7.5至ph8.0的范围。具体地,洗脱溶液可包含选自由磷酸钠、氯化钠、tris-hcl、2-(n-吗啉代)乙磺酸(mes)、3-吗啉代丙-1-磺酸(mops)、pipes、磷酸钾、氯化钾和2-[4-(2-羟乙基)哌嗪-1-基]乙磺酸(hepes)组成的组中的至少一种盐,但不限于此。
此外,洗脱溶液可含有0.1m至0.5m氯化钠,但可以使用可将所需疫苗病毒从亲和色谱柱中分离出来的盐,而无浓度限制。
使用本公开的纯化方法分离的所需疫苗病毒的纯度可为88%或更高,并且具体地,纯度为90%或更高、91%或更高、92%或更高、93%或更高、94%或更高、95%或更高、96%或更高、97%或更高或98%或更高。术语“纯度”意指去除了杂质的纯疫苗病毒,并且例如,如果纯度为92%,则剩余的8%意指杂质。此外,纯度可以简单地代表从洗脱溶液中分离出来的材料的纯度,但是最终纯度%可以根据所上样的样品的纯度%而变化。
术语“杂质”是除所需疫苗病毒以外的任何材料,并且例如可以包括宿主源性dna、宿主源性蛋白质、内毒素等,但不限于此。
此外,疫苗病毒的纯度可以通过专门提供以根据洗脱溶液的总蛋白质量测量宿主源性杂质的酶联免疫吸附测定(elisa)法来分析,但不限于此,并且当然,疫苗病毒的纯度可以使用cex-hplc、sec-hplc等进行分析。
在本公开中,病毒优选是肠道病毒,但不限于此。
此外,通过本公开的纯化方法纯化的疫苗病毒可以用作疫苗或免疫原性组合物,但不限于此。
本公开的另一方面提供了一种根据所述纯化方法纯化的疫苗病毒。疫苗病毒可以用作疫苗或免疫原性组合物,但不限于此。
在下文中,提出优选的实施例来帮助理解本公开。然而,以下实施例仅提供为使得可以更容易地理解本公开,并且本公开的内容不受实施例的限制。
实施例1.使用含有硫酸葡聚糖的captotmdevirs树脂的纯化
在实施例1中,使用含有硫酸葡聚糖配体的captotmdevirs树脂证实了疫苗病毒的纯化产率和杂质去除率。
使用20mm磷酸钠ph7.5缓冲液作为平衡溶液和洗涤溶液(0m氯化钠),并且制备了洗脱溶液并将其与ph7.5缓冲液一起使用,其中氯化钠在平衡溶液中将达到2m。
首先,将含有肠道病毒的疫苗病毒样品上样至柱上,然后通过与洗涤溶液一起流动进行洗涤。接下来,以线性浓度梯度使0m至2m氯化钠的洗脱液流动,收集洗脱溶液,然后以tcid50测量疫苗病毒含量,并测量杂质含量。
图2和图3示出了使用含有硫酸葡聚糖的captotmdevirs树脂纯化疫苗病毒的结果。
参考图2和图3,当将上样的样品的量与流过的量相比较(f/t)时,证实了大量杂质从上样的样品中去除。此外,当将上样的样品中所包括的病毒含量与流过的含量相比较(f/t)时,证实了大部分疫苗病毒被纯化,而没有损失疫苗病毒。
同时,洗脱溶液的氯化钠浓度从0m增加至2m以获取相应的级分。结果,当取得的级分的盐浓度在0.1m至0.9m、优选地0.1m至0.5m内时,证实了大量杂质被去除,并且同时,大部分疫苗病毒被纯化,而没有损失疫苗病毒。
例如,当取得的级分3和4的盐浓度在0.1m至0.5m内时,证实了回收了约81.1%的疫苗病毒,并且此时,杂质的去除率为约97.7%,并且因此,杂质的含量与其他级分相比非常低。
实施例2.使用含有肝素的hitrapheparin树脂的纯化
在实施例2中,使用含有肝素配体的hitrapheparin树脂证实了疫苗病毒的纯化产率和杂质去除率。
使用50mmtris-hclph8.0缓冲液作为平衡溶液和洗涤溶液,并且制备了洗脱溶液并使用,使得氯化钠在平衡溶液中将达到2m。
首先,将含有肠道病毒的疫苗病毒样品上样至柱上,然后通过与洗涤溶液一起流动进行洗涤。接下来,以线性浓度梯度使0m至2m氯化钠的洗脱液流动,收集洗脱溶液,然后以tcid50测量疫苗病毒含量,并测量杂质含量。
图4和图5示出了使用含有肝素的hitrapheparin树脂纯化疫苗病毒的结果。
参考图4和图5,当将上样的样品的量与流过的量相比较(f/t)时,证实了大量杂质从上样的样品中去除。此外,当将上样的样品中所包括的病毒含量与流过的含量相比较(f/t)时,证实了大部分疫苗病毒被纯化,而没有损失疫苗病毒。
同时,洗脱溶液的氯化钠浓度从0m增加至2m以获取相应的级分。结果,当取得的级分的盐浓度在0.1m至0.9m、优选地0.1m至0.5m并且最优选地0.1m至0.3m时,证实了大量杂质被去除,并且同时,大部分疫苗病毒被纯化,而没有损失疫苗病毒。
例如,当取得的级分4至7的盐浓度在0.1m至0.5m内时,证实了回收了约85.4%的疫苗病毒,并且此时,杂质的去除率为92.0%。
比较例1.使用fractogeldeae树脂的纯化
在比较例1中,使用含有二乙氨基乙基(deae)配体的fractogeldeae树脂证实了疫苗病毒的纯化产率和杂质去除率。
使用50mmtris-hclph8.0缓冲液作为平衡溶液和洗涤溶液,并且制备了洗脱溶液并使用,使得氯化钠在平衡溶液中将达到2m。
首先,将含有肠道病毒的疫苗病毒样品上样至柱上,然后通过与洗涤溶液一起流动进行洗涤。接下来,以线性浓度梯度使液流动,收集洗脱溶液,然后以tcid50测量疫苗病毒含量,并测量杂质含量。
图6和图7示出了使用fractogeldeae树脂纯化疫苗病毒的结果。
参考图6和图7,当增加盐浓度并取得相应级分时,在以具体盐浓度的级分11中,回收了约25.7%的疫苗病毒,并且此时,杂质去除率为51.3%。也就是说,证实了在疫苗病毒的回收率相对高的级分中,相较于其他级分,杂质含量非常高。
比较例2.使用fractogeltmae树脂的纯化
在比较例2中,使用含有三甲基铵甲基(tmae)配体的fractogeltmae树脂证实了疫苗病毒的纯化产率和杂质去除率。
使用50mmtris-hclph8.0缓冲液作为平衡溶液和洗涤溶液,并且制备了洗脱溶液并使用,使得氯化钠在平衡溶液中将达到2m。
首先,将含有肠道病毒的疫苗病毒样品上样至柱上,然后通过与洗涤溶液一起流动进行洗涤。以线性浓度梯度使液流动,收集洗脱溶液,然后以tcid50测量疫苗病毒含量,并测量杂质含量。
图8和图9示出了使用fractogeltmae树脂纯化疫苗病毒的结果。
参考图8和图9,当增加盐浓度并洗脱相应级分时,证实了在具体级分(级分5)中,回收了约20.5%的疫苗病毒,并且此时,杂质去除率为89.2%。
比较例3.使用cimdeae树脂的纯化
在比较例3中,使用由deae组成的盘形单一主体树脂证实了疫苗病毒的纯化产率和杂质去除率。
使用50mmtris-hclph8.0缓冲液作为平衡溶液和洗涤溶液,并且制备了洗脱溶液并使用,使得氯化钠在平衡溶液中将达到2m。
首先,将含有肠道病毒的疫苗病毒样品上样至柱上,然后通过与洗涤溶液一起流动进行洗涤。将平衡溶液和洗脱溶液以预定比率混合,以浓度梯度流动,使得氯化钠的浓度为100mm、140mm、200mm、400mm和600mm,收集洗脱溶液,然后以tcid50测量疫苗病毒含量。
图10和图11示出了使用cimdeae树脂纯化疫苗病毒的结果。
参考图10和图11,当增加盐浓度并洗脱相应级分时,证实了在140mm的盐浓度下,回收了约34.2%的疫苗病毒,并且证实了将其应用于实际过程是困难的,因为过程中压力过大。
实施例1和2以及比较例1至3的方法和结果总结在下表1中。
[表1]
这些结果表明,在本公开的使用亲和色谱法的疫苗病毒的纯化方法中,与使用离子交换色谱法的常规纯化方法相比,可以以高杂质去除率和高产率分离出所需疫苗病毒。
本领域的技术人员将理解,如上所述的本公开可以在不背离其技术精神或基本特征的情况下,以其他特定形式来实现。因此,应当理解,上述实施方式旨在以广泛意义说明,而非限制性的。例如,在上述实施例1和2中,使用含有硫酸葡聚糖的树脂和含有肝素的树脂证实了疫苗病毒的纯化产率和杂质去除率,但根据实施例,使用了硫酸葡聚糖和肝素以预定比率混合的树脂。
本公开的范围由以下描述的权利要求而不是具体实施方式来表示,并且应解释为,权利要求的含义和范围以及从其等效物得出的所有改变或修改形式均在本公开的范围内。
- 还没有人留言评论。精彩留言会获得点赞!