一种新型冠状病毒检测试剂盒、用途及其使用方法与流程
本发明属于基因检测领域,涉及一种利用多重实时荧光rt-pcr技术检测新型冠状病毒的试剂盒、用途及这种试剂盒的使用方法。
背景技术:
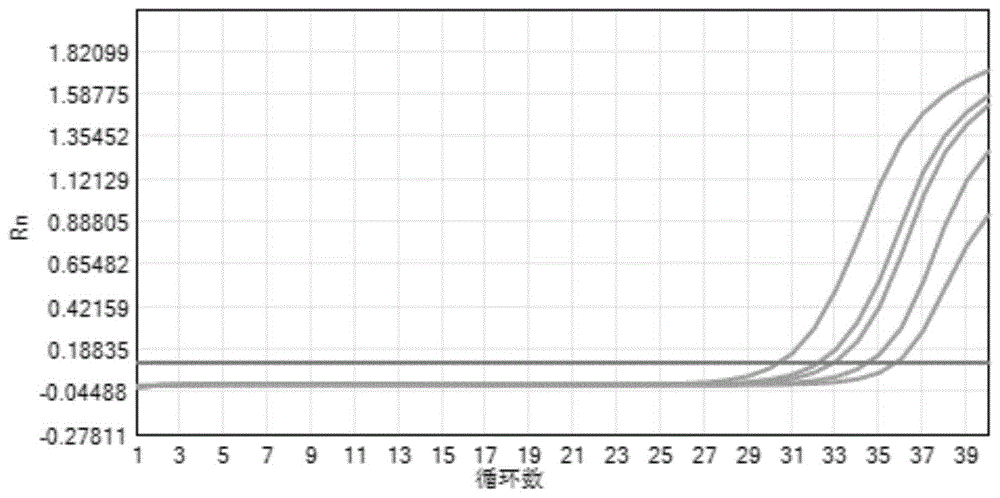
:冬季和早春为流行性感冒的爆发季节,每年这个时候成人中的普通感冒主要由冠状病毒所引起。冠状病毒是在动物和人体中发现的一个大型病毒家族,最早由鸡胚中分离出来,到目前为止,大约有15中不同的冠状病毒被发现。其中,能感染人的冠状病毒有六种,hcov-229e,hcov-0c43,hcov-nl63,hcov-hku1,sars-cov和mers-cov。在这6中病毒里,前四种只会引起普通的感冒,普通的病毒性感冒2-5天即会出现相应症状,经过治疗1-2周可以恢复。后两种是引起全球恐惧的严重急性呼吸综合征冠状病毒(sars-cov)和中东呼吸综合征冠状病毒(mers-cov)mers-cov,这两种病毒可引起全球范围内大范围的流行。2019新型冠状病毒的序列已先后被中国疾控中心以及世界卫生健康组织wto先后公布,新型冠状病毒和其他冠状病毒一样是一种ssrna病毒,测序结果显示,其全长约30kb,新型冠状病毒属于rna病毒,现在针对该病毒的研究刚刚开始,现目前,多数厂家都是采用两个区域进行检测,但是,在实际检测中,存在一定比例单个靶标区域阳性的结果,说明试剂对不同区域的敏感性存在差异,也可能是靶标之间的相互竞争所导致,此外,试剂盒的其他成分、反应体系以及样本的加入量都会影响检测分析敏感性、特异性以及检测重现性。目前,大多数检测试剂盒里面都有内质控品,这些质控品都是取样后直接向样本中添加,内质控品只能检测整个提取以及检测过程操作是否正确,但是却不能保证采样过程是否成功,而样本采集的是否成功关乎患者检测结果,采样量的多少又与样本能够成功检测息息相关。使用外源内标进行检测会导致大量的潜在的冠状病毒因取样失败漏检,患者得不到及时的隔离以及救治,最终导致病人的死亡以及健康者的传染。因此,开发一种检测快速、灵敏度高、特异性好、能够避免假阴性以及具有良好重现性的新型冠状病毒检测试剂盒。技术实现要素:为了解决上述问题,本发明提供了一种快速、灵敏度高、特异性好、能够避免假阴性以及具有良好重现性的检测新型冠状病毒的rt-pcr检测试剂盒。本发明提供了一种新型冠状病毒检测试剂盒,所述试剂盒主要包括引物探针混合物,所述引物探针混合物由orf1ab基因、n基因和s基因特异性的正、反向引物及特异性的探针组成。进一步的,本发明中orf1ab基因的正向引物的序列如seqidno:1所示;所述orf1ab基因的反向引物的序列如seqidno:2所示;本发明中n基因的的正向引物的序列如seqidno:3所示;所述n基因的反向引物的序列如seqidno:4所示;本发明中s基因的正向引物的序列如seqidno:5所示;所述s基因的反向引物的序列如seqidno:6所示。进一步的,本发明中orf1ab基因的探针的序列如seqidno:7所示;本发明中n基因的探针的序列如seqidno:8所示;本发明中s基因的探针的序列如seqidno:9所示。进一步的,本发明试剂盒中还包括内质控品,所述内质控品的正向引物的序列如seqidno:10所示,所述内质控品的反向引物的序列如seqidno:11所示。进一步的,本发明中内质控品的探针序列如seqidno:12所示。进一步的,本发明中探针的两端分别带有荧光基团和猝灭基团,所述荧光基团为fam、rox、vic、tet和cy5中的一种,所述猝灭基团为bhq1、bhq2、bhq3和mgbnfq中的一种。进一步的,本发明试剂盒还包括pcr反应液,所述反应液主要由如下组分组成:tris-hclph=8.51-10mm,kcl1-5mm,mgcl26-12mm,datp0.5-2mm,dctp0.5-2mm,dgtp0.5-2mm,dutp2-4mm,dtt1-5mm。进一步的,本发明中pcr反应液主要由如下成分组成:tris-hclph=8.55mm,kcl4mm,mgcl28mm,datp0.8mm,dctp0.8mm,dgtp0.8mm,dutp2mm,dtt2mm。进一步的,本发明试剂盒还包括pcr酶液,pcr酶液主要由如下成分组成:hotstarttaq10-50%,ung1-20%,hiscriptreversetranscriptase1%-10%,taqssb10-50%,甘油10-50%,anti-taq1-50%。进一步的,本发明试剂盒中pcr酶液主要由如下成分组成:hotstarttaq15%;anti-taq15%;ung7%;hiscriptreversetranscriptase8%;taqssb15%;甘油40%。本发明还提供采用如上任意一项所述的试剂盒来检测新冠状病毒的用途。本发明还提供使用如上任意一项所述的试剂盒的使用方法,所述方法包括如下步骤:1)核酸提取:采用核酸提取试剂对样本中的rna进行提取,得核酸提取产物;2)pcr扩增:pcr反应体系如下:pcr反应液10-50%;pcr酶液5-20%;单基因和内质控品的正向引物和反向引物分别0.1-4μm;探针0.05-0.8μm;核酸提取产物10-50%。进一步的,本发明中pcr反应体系如下:pcr反应液25%;pcr酶液10%;单项目和内质控品的正向引物和反向引物分别0.8μm;探针0.5μm;核酸提取产物30%。与现有技术相比,本发明具有如下优点:采用本发明中的试剂盒,通过试剂盒中的引物探针、pcr反应液、pcr酶液以及其他成分的结合、协同,最后得到一种快速、灵敏度高、特异性好以及具有良好重现性的检测新型冠状病毒的rt-pcr检测试剂盒;本发明中的内质控品为人基因组中的基因,不需要另外添加,样本中即含有,针对这个反应体系,我们设置了特异性的内质控品的引物和探针,能够增加判断采样是否成功的敏感性,能够避免检测结果假阴性,让潜在病患得到及时的隔离以及救治;研发人员在研发过程中偶然发现新型冠状病毒中的s基因具有很好的保守性,对于新型冠状病毒的检测具有很好的特异性。以下通过实施例形式的具体实施方式,对本发明的上述内容再做进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实施例。凡基于本发明上述内容所实现的技术属于本发明的内容。附图说明图1为本发明试剂盒对不同浓度样本中n基因的扩增图;图2为本发明试剂盒对不同浓度样本中orf1ab基因的扩增图;图3为本发明试剂盒对不同浓度样本中s基因的扩增图;图4为为本发明试剂盒特异性扩增图;图5为本发明试剂盒对除新冠病毒外的病原体中n基因的扩增图;图6为本发明试剂盒对除新冠病毒外的病原体中orf1ab基因的扩增图;图7为本发明试剂盒对除新冠病毒外的病原体中s基因的扩增图。具体实施方式说明:本发明中核酸提取试剂采用重庆中元汇吉生物技术有限公司生产的产品。实施例1一种新型冠状病毒检测试剂盒1、pcr反应液:tris-hclph=8.51mm,kcl1mm,mgcl26mm,datp0.5mm,dctp0.5mm,dgtp0.5mm,dutp2mm,dtt1mm。2、pcr酶液:hotstarttaq10%,ung1%,hiscriptreversetranscriptase1%,taqssb10%,anti-taq1%,甘油10%。3、基因引物对以及探针序列如下:orf1ab基因的正向引物的序列如seqidno:1所示;orf1ab基因的反向引物的序列如seqidno:2所示;n基因的的正向引物的序列如seqidno:3所示;n基因的反向引物的序列如seqidno:4所示;s基因的正向引物的序列如seqidno:5所示;s基因的反向引物的序列如seqidno:6所示;orf1ab基因的探针的序列如seqidno:7所示;n基因的探针的序列如seqidno:8所示;s基因的探针的序列如seqidno:9所示;orf1ab基因、n基因、s基因分别对应的荧光基团是tet、cy5、vic,对应的猝灭基团都为mgbnfq。4、内质控品的引物和探针序列如下所示:内质控品的正向引物的序列如seqidno:10所示;内质控品的反向引物的序列如seqidno:11所示;内质控品的探针序列如seqidno:12所示,内控品的荧光探针是rox。其中pcr反应体系如下:pcr反应液10%,pcr酶液5%,单基因和内质控品的正向引物和反向引物分别为0.1μm,探针都为0.05μm,核酸提取产物10%。实施例2一种新型冠状病毒检测试剂盒1、pcr反应液:tris-hclph=8.510mm,kcl5mm,mgcl212mm,datp2mm,dctp2mm,dgtp2mm,dutp4mm,dtt5mm。2、pcr酶液:hotstarttaq50%,ung20%,hiscriptreversetranscriptase10%,taqssb50%,甘油50%,anti-taq50%。3、基因引物对以及探针序列(与实施例1中相同)orf1ab基因、n基因、s基因分别对应的荧光基团是rox、tet、cy5,对应的猝灭基团都为bhq3。4、内质控品的引物和探针序列(与实施例1中相同)内质控品对应的荧光基团为vic。其中pcr反应体系如下:pcr反应液50%,pcr酶液20%,单基因和内质控品的正向引物和反向引物分别为4μm,探针都为为0.8μm,核酸提取产物30%。实施例3一种新型冠状病毒检测试剂盒1、pcr反应液:tris-hclph=8.55mm,kcl4mm,mgcl28mm,datp0.8mm,dctp0.8mm,dgtp0.8mm,dutp2mm,dtt2mm。2、pcr酶液:hotstarttaq15%,ung7%,hiscriptreversetranscriptase8%,taqssb15%,anti-taq15%,甘油40%。3、基因引物对以及探针序列(与实施例1中相同)orf1ab基因、n基因、s基因分别对应的荧光基团是rox,fam,cy5,对应的猝灭基团都为bhq1。4、内质控品的引物和探针序列(与实施例1中相同)荧光基团为vic。其中pcr反应体系如下:pcr反应液25%,pcr酶液10%,单基因和内质控品的正向引物和反向引物分别为0.8μm,探针都为0.5μm,核酸提取产物20%。实施例4新型冠状病毒检测试剂盒灵敏度、精密度以及特异性1、基本实验过程a、采样:我们提取的样本为企业阳性参考品,样本储存于-20℃或者-70℃冰箱中。b、核酸提取:采用重庆中元汇吉生物技术有限公司生产的核酸提取试剂,配套奥胜半自动核酸提取仪,主要步骤如下:1)将采取的样本加入第一列,每孔200μl;2)将核酸提取试剂中的各种成分按照比例加入第一列,每孔加入500μl;3)将核酸提取试剂中的洗涤液加入第三列,每孔600μl;4)将洗脱液加入第六列,每孔65ul;5)操作奥胜半自动核酸提取仪中,按照以下程序进行提取,最后获得核酸提提取产物;c、pcr扩增:使用上海宏石slan96ppcr仪,采用实施例3中所述的pcr反应体系,pcr反应程序如下:使用一个pcr管占用4个荧光通道,其中n基因占用fam,orf1ab占用rox通道,s基因占用cy5通道,内标占用vic通道。三个靶标基因出现两个或以上起即可判定为阳性。2、灵敏度1)实验过程:选择新型冠状病毒企业阳性参考品,使用阴性样本基质稀释成5个梯度(2000copies/ml、1000copies/ml、500copies/ml、250copies/ml、125copies/ml),其余实验步骤按照1中的基本实验过程进行操作。2)实验结果实验结果见图1、图2和图3以及表1表1灵敏度实验结果统计浓度(copies/ml)阳性检出数总测试数/次检出率200044/4100.00%100044/4100.00%50044/4100.00%25033/475%12533/475%分析:从图1、图2和图3可以看出,2000copies/ml、1000copies/ml、500copies/ml、250copies/ml这四个浓度的检测结果较好,曲线形态呈较好的s型,当浓度低于500copies/ml时,曲线形态已不正常;从表1中看出,浓度大于等于500copies/ml时,可以全部检出,而当浓度低于500copies/ml时,检出率只有75%,由此可知试剂盒的灵敏度线在500copies/ml附近。3、特异性1)实验过程:以企业阴性参考品作为基质,选择含有甲型流感病毒、乙型流感病毒、呼吸道合胞病毒、呼吸道合胞病毒、腺病毒、副流感病毒、肺炎克雷伯杆菌、肺炎链球菌、流感嗜血杆菌、铜绿假单胞菌、百日咳杆菌、嗜肺军团菌、金黄色葡萄球菌、肺炎支原体、肺炎衣原体的病原体作为交叉反应样本,其余的核酸提取以及pcr扩增按照1中的基本实验过程进行操作。2)实验结果:分析:实验结果见图4,由图4中可以看出对含有甲型流感病毒、乙型流感病毒、呼吸道合胞病毒、呼吸道合胞病毒、腺病毒、副流感病毒、肺炎克雷伯杆菌、肺炎链球菌、流感嗜血杆菌、铜绿假单胞菌、百日咳杆菌、嗜肺军团菌、金黄色葡萄球菌、肺炎支原体、肺炎衣原体的样本,本发明检测试剂盒并未发现特异性扩增,表明本发明检测试剂盒对新冠状病毒具有特异性。4、精密度1)实验过程:将新型冠状病毒企业精密度参考品稀释至1000copies/ml作为样本,平行测8次,其余实验步骤按照1中的基本实验过程进行操作。2)实验结果分析:实验结果见图5、图6和图7所示,从图中可以看出,曲线形态呈较好的s型,并且曲线的ctcv%见下表2,可知ctcv(%)均小于1%,说明本发明中的试剂盒的精密度较好,具有良好的稳定性。表2各个通道的ct和ctcv(%)值实施例5对比实施例(内质控品)1)实验过程:采用实施例3中的pcr反应体系;对比反应体系:采用质粒作为内质控品的引物以及探针(上游引物序列:ggttgtatcacatcgatcacct、下游引物序列:tgacagcaatttctcgacctat、探针序列:tccagcttctgagtcgctcggtcta);其余实验步骤按照实施例4中第1步中的基本实验过程进行操作2)实验结果如表3和表4所示。使用两个企业阳性参考品基质为样本进行检测发现自研试剂盒内标为阴性,此时可将样本判断为取样失败。而竞品试剂盒对企业阳性参考品基质为样本进行检测发现内标正常,判断样本为阴性样本。因此相比于对比的外源添加内标,本发明的内源性内标可以快速判断样本是否为假阴性。表3本发明试剂盒检测结果样本orf1abns内标企业阳性参考品阳性阳性阳性阳性企业阴性参考品阴性阴性阴性阳性阳性参考品基质阴性阴性阴性阴性表4对比试剂盒检测结果样本orf1abns内标企业阳性参考品阳性阳性/阳性企业阴性参考品阴性阴性/阳性阳性参考品基质阴性阴性/阳性实施例6对比实施例(与其他厂家的检测试剂盒进行对比)1)实验过程:对患者的同一部位三次采样,然后对三次样本(样本a、样本b、样本c进行核酸检测);采用实施例3中的pcr反应体系;对比厂家:某厂家生产的新型冠状病毒orf1ab/n基因rt-pcr检测试剂盒;其余实验步骤按照实施例4中第1步中的基本实验过程进行操作。2)实验结果:实验结果见下表5:表5本发明与竞品检测结果分析:从上表中看出,对同一个样本进行检测时本发明的ct值比竞品试剂盒普遍提前2-3个ct值,并且本发明试剂盒具有更高的检出率。序列表<110>重庆中元汇吉生物技术有限公司<120>一种新冠状病毒检测试剂盒、用途及其使用方法<130>2020.2.20<160>12<170>siposequencelisting1.0<210>1<211>19<212>dna<213>人工合成(artificiallysynthesized)<400>1cagaggacgcgcagggaat19<210>2<211>22<212>dna<213>人工合成(artificiallysynthesized)<400>2atctgtgtggccaacctcttct22<210>3<211>21<212>dna<213>人工合成(artificiallysynthesized)<400>3agcgaaatgcaccccgcatta21<210>4<211>21<212>dna<213>人工合成(artificiallysynthesized)<400>4tcttggttcaccgctctcact21<210>5<211>23<212>dna<213>人工合成(artificiallysynthesized)<400>5agatcgatcctgtcacctctgac23<210>6<211>20<212>dna<213>人工合成(artificiallysynthesized)<400>6atccgtctacgctgcagtct20<210>7<211>25<212>dna<213>人工合成(artificiallysynthesized)<400>7tgatgtttcaactggttttgtgctc25<210>8<211>24<212>dna<213>人工合成(artificiallysynthesized)<400>8ccgacgttgttttgatcgcgcccc24<210>9<211>23<212>dna<213>人工合成(artificiallysynthesized)<400>9acgctcagcctgcctagtgagcc23<210>10<211>24<212>dna<213>人工合成(artificiallysynthesized)<400>10cagatgtggatcagcaagcaggag24<210>11<211>27<212>dna<213>人工合成(artificiallysynthesized)<400>11tgtcaagaaagggtgtaacgcaactaa27<210>12<211>32<212>dna<213>人工合成(artificiallysynthesized)<400>12cgagtccggcccctccatcgtccaccgcaaat32当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1