三嗪酮类化合物及其片剂和在抗阿尔茨海默症中的用途的制作方法
本发明涉及医药领域,具体涉及三嗪酮类化合物及其片剂和在抗阿尔茨海默症中的用途。
背景技术:
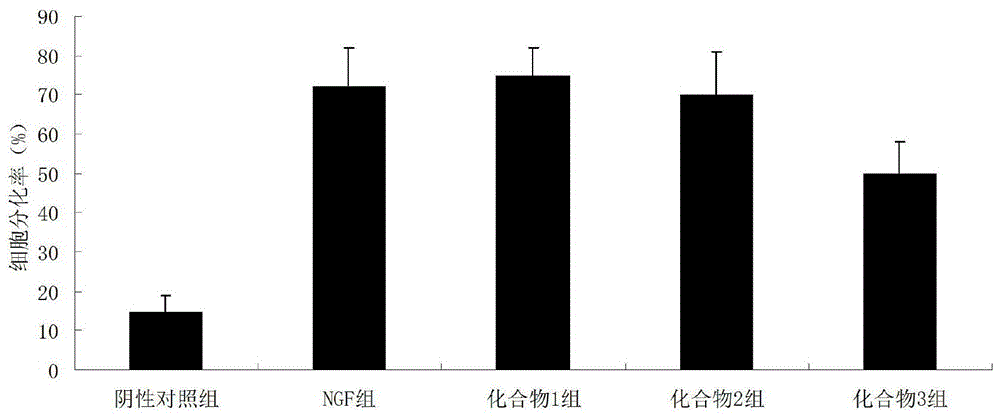
:抗阿尔茨海默症(ad)是一种起病隐匿的进行性发展的神经系统退行性疾病。临床上以记忆障碍、失语、失用、失认、视空间技能损害、执行功能障碍以及人格和行为改变等全面性痴呆表现为特征。根据认知能力和身体机能的恶化程度分为三个时期。第一阶段(1-3年)为轻度痴呆期,表现为记忆减退、判断能力下降、出现时间定向障碍、言语词汇少等;第二阶段(2-10年)为中度痴呆期,表现为远近记忆严重受损,简单结构的视空间能力下降,时间、地点定向障碍,不能独立进行室外活动等;第三阶段(8-12年)为重度痴呆期,患者已经完全依赖照护者,严重记忆力丧失,日常生活不能自理,呈现缄默、肢体僵直,最终昏迷,一般死于感染等并发症。ad病因迄今未明,目前该病的可能因素和假说多达30余种,如胆碱能神经元假说、aβ毒性假说、tau蛋白假说、胰岛素假说、自由基损伤假说等。目前,世界上较为接受的ad病理为“胆碱能缺失学说”。美国麻省理工学院的研究人员发现,阿尔茨海默症患者的脑中,胆碱水平比正常人少40%-50%。胆碱酯酶(che)是生物神经传导中的一种关键性的酶,能催化神经递质乙酰胆碱水解成胆碱和乙酸,使乙酰胆碱失去活性。临床医学治疗普遍采用乙酰胆碱酯酶抑制剂来阻止乙酰胆碱酯酶活性,从而达到降低或延缓乙酰胆碱的水解速度,恢复突触间隙乙酰胆碱的水平,达到对ad的控制与治疗。乙酰胆碱酯酶抑制剂(achei)是到目前为止临床上使用最为广泛的抗ad治疗药物。fda批准用于治疗ad的5种药物中除了美金刚属于nmda受体拮抗药外,其余4种他克林(tacrine)、多奈哌齐(donepezil)、加兰他敏(galanthamine)和卡巴拉汀(rivastigmine)均属于achei。抗ad药物不但品种稀少,且药物缺点也非常明显。如,他克林由于肝毒性较大,已逐渐被其他药物取代;加兰他敏的治疗效果不明显,且会导致严重的皮肤不良反应;多奈哌齐与卡巴拉汀胃肠道不良反应常见。因此寻找新的抗阿尔茨海默症药物,尤其是针对轻中度痴呆患者的脑功能水平的提高,患者生活质量的改善具有重要意义,而关于本发明提到的三嗪酮类化合物在抗阿尔茨海默症方面的研究至今还没有报道。技术实现要素:本发明提供了一种三嗪酮类化合物,其结构如式i所示:其中ar选自吡啶-2-基甲基、4-甲氧基苯基、2-吗啉乙基。进一步地,所述三嗪酮类化合物式i药学上可接受的盐。进一步地,所述三嗪酮类化合物式i选自化合物1、化合物2和化合物3,结构如下所示:所述化合物1、化合物2及化合物3的结构数据及其合成方法参见实施例部分。本发明还提供了所述化合物的体外对pc12细胞损伤的保护作用实验、小鼠morris水迷宫试验、跳台试验以及海马ach、ache、chat含量测定。本发明所述三嗪酮类化合物片剂处方的组成为:所述三嗪酮类化合物或其药学上可接受的盐0.1-5份,填充剂20-90份、崩解剂5-20份、粘合剂2-15份、润滑剂0.1-3份。其中起填充剂作用的辅料为淀粉、糊精、糖粉、乳糖、预胶化淀粉、微晶纤维素、甘露醇、药用碳酸钙中的一种或几种。其中起崩解剂作用的辅料为干淀粉、羧甲基淀粉钠、低取代羟丙基纤维素、交联聚乙烯吡咯烷酮、交联羧甲基纤维素钠、羧甲基纤维素钠中的一种或几种。其中起粘合剂作用的辅料为蒸馏水、乙醇、淀粉浆、糊精浆、羧甲基纤维素钠、羟丙基纤维素、甲基纤维素、乙基纤维素、羟丙甲纤维素、聚乙烯吡咯烷酮、聚乙二醇中的一种或几种。其中起润滑剂作用的辅料为硬脂酸镁、微粉硅胶、滑石粉、硬脂酰富马酸钠、聚乙二醇。还可选择其他具有填充作用的填充剂、其他具有崩解作用的崩解剂、其他具有粘合作用的粘合剂和其他具有润滑剂作用的润滑剂剂在本发明中应用。本发明的制备方法包括以下内容:(1)按处方称量辅料,过120目筛;(2)配制粘合剂,备用;(3)将填充剂、崩解剂依次加入湿法制粒机中干混,然后缓慢加入已配置好的粘合剂,湿混,制得软材;(4)将软材加入摇摆制粒机制粒,烘干;(5)整粒;(6)加入处方量的三嗪酮类化合物式i、润滑剂,混匀,压片。附图说明图1是本发明化合物对pc12细胞损伤的保护作用。具体实施方式实施例1:化合物1的合成反应管中加入(z)-苯基2(3-氧代丁烷-2-亚甲基)肼基甲酸酯(1当量)、硫酸镁(1当量)、吡啶-2-甲基甲胺(1.1当量)和三氟甲苯(3mol/l),密封后175℃加热入6h。反应管冷却至室温后,减压浓缩,并通过硅胶色谱纯化,得到化合物1。经结构确证,所合成化合物的1h-nmr和13c-nmr数据与文献(divergentreactivityofn-isocyanateswithprimaryandsecondaryamines:accesstopyridazinonesandtriazinones(org.lett.2016,18,658.661.))一致。实施例2:化合物2的合成反应管中加入(z)-苯基2(3-氧代丁烷-2-亚甲基)肼基甲酸酯(1当量)、硫酸镁(1当量)、4-甲氧基苯胺(1.1当量)和三氟甲苯(3mol/l),密封后175℃加热入6h。反应管冷却至室温后,减压浓缩,并通过硅胶色谱纯化,得到化合物2。经结构确证,所合成化合物的1h-nmr和13c-nmr数据与文献(divergentreactivityofn-isocyanateswithprimaryandsecondaryamines:accesstopyridazinonesandtriazinones(org.lett.2016,18,658.661.))一致。实施例3:化合物3的合成反应管中加入(z)-苯基2(3-氧代丁烷-2-亚甲基)肼基甲酸酯(1当量)、硫酸镁(1当量)、n-(2-氨基乙基)吗啉(1.1当量)和三氟甲苯(3mol/l),密封后175℃加热入6h。反应管冷却至室温后,减压浓缩,并通过硅胶色谱纯化,得到化合物3。经结构确证,所合成化合物的1h-nmr和13c-nmr数据与文献(divergentreactivityofn-isocyanateswithprimaryandsecondaryamines:accesstopyridazinonesandtriazinones(org.lett.2016,18,658.661.))一致。实施例4:制备1000片化合物1片剂(规格2mg/片)一、处方化合物12g、淀粉35g、糊精35g、糖粉15g、羧甲基淀粉钠(cms-na)7g、羧甲基纤维素钠(cmc-na)5g、硬脂酸镁1g。二、制备工艺(1)按处方称量辅料,过120目筛;(2)将处方量的cmc-na加入适量的95%乙醇中,搅拌至全部溶解,然后加入适量纯化水,搅拌均匀,配制成含羧甲基纤维素钠1%的50%乙醇溶液(w/w)作为粘合剂,备用;(3)将处方量的淀粉、糊精、糖粉、cms-na依次加入湿法制粒机中干混,搅拌混合5min。然后缓慢加入已配置好的粘合剂,湿混,搅拌混合3min,制得软材;(4)将软材加入摇摆制粒机制粒,烘干;(5)整粒;(6)加入处方量的化合物1、硬脂酸镁,混匀,压片。实施例5:制备1000片化合物2片剂(规格2mg/片)一、处方化合物22g、淀粉35g、糊精35g、糖粉15g、羧甲基淀粉钠(cms-na)7g、羧甲基纤维素钠(cmc-na)5g、硬脂酸镁1g。二、工艺步骤(1)按处方称量辅料,过120目筛;(2)将处方量的cmc-na加入适量的95%乙醇中,搅拌至全部溶解,然后加入适量纯化水,搅拌均匀,配制成含羧甲基纤维素钠1%的50%乙醇溶液(w/w)作为粘合剂,备用;(3)将处方量的淀粉、糊精、糖粉、cms-na依次加入湿法制粒机中干混,搅拌混合5min。然后缓慢加入已配置好的粘合剂,湿混,搅拌混合3min,制得软材;(4)将软材加入摇摆制粒机制粒,烘干;(5)整粒;(6)加入处方量的化合物2、硬脂酸镁,混匀,压片。实施例6:制备1000片化合物3片剂(规格2mg/片)一、处方化合物32g、淀粉35g、糊精35g、糖粉15g、羧甲基淀粉钠(cms-na)7g、羧甲基纤维素钠(cmc-na)5g、硬脂酸镁1g。二、工艺步骤(1)按处方称量辅料,过120目筛;(2)将处方量的cmc-na加入适量的95%乙醇中,搅拌至全部溶解,然后加入适量纯化水,搅拌均匀,配制成含羧甲基纤维素钠1%的50%乙醇溶液(w/w)作为粘合剂,备用;(3)将处方量的淀粉、糊精、糖粉、cms-na依次加入湿法制粒机中干混,搅拌混合5min。然后缓慢加入已配置好的粘合剂,湿混,搅拌混合3min,制得软材;(4)将软材加入摇摆制粒机制粒,烘干;(5)整粒;(6)加入处方量的化合物3、硬脂酸镁,混匀,压片。实施例7:制备1000片化合物1片剂(规格5mg/片)一、处方化合物15g、糊精29g、预胶化淀粉30g、微晶纤维素(mcc)20g、低取代羟丙纤维素(l-hpc)5g、交联聚乙烯吡咯烷酮(ppvp)3g、聚乙烯吡咯烷酮k30(pvp-k30)5g、滑石粉3g。二、工艺步骤(1)按处方称量辅料,过120目筛;(2)称取处方量的pvp-k30,加入到浓度为50%乙醇溶液中,配置成5%pvp-k30-乙醇溶液作为粘合剂;(3)将处方量的糊精29g、预胶化淀粉30g、mcc、l-hpc、ppvp依次加入湿法制粒机中干混,搅拌混合5min。然后缓慢加入已配置好的粘合剂,湿混,搅拌混合3min,制得软材;(4)将软材加入摇摆制粒机制粒,烘干;(5)整粒;(6)加入处方量的化合物1、滑石粉,混匀,压片。实施例8:制备1000片化合物2片剂(规格5mg/片)一、处方化合物25g、糊精29g、预胶化淀粉30g、微晶纤维素(mcc)20g、低取代羟丙纤维素(l-hpc)5g、交联聚乙烯吡咯烷酮(ppvp)3g、聚乙烯吡咯烷酮k30(pvp-k30)5g、滑石粉3g。二、工艺步骤(1)按处方称量辅料,过120目筛;(2)称取处方量的pvp-k30,加入到浓度为50%乙醇溶液中,配置成5%pvp-k30-乙醇溶液作为粘合剂;(3)将处方量的糊精29g、预胶化淀粉30g、mcc、l-hpc、ppvp依次加入湿法制粒机中干混,搅拌混合5min。然后缓慢加入已配置好的粘合剂,湿混,搅拌混合3min,制得软材;(4)将软材加入摇摆制粒机制粒,烘干;(5)整粒;(6)加入处方量的化合物2、滑石粉,混匀,压片。实施例9:制备1000片化合物3片剂(规格5mg/片)一、处方化合物35g、糊精29g、预胶化淀粉30g、微晶纤维素(mcc)20g、低取代羟丙纤维素(l-hpc)5g、交联聚乙烯吡咯烷酮(ppvp)3g、聚乙烯吡咯烷酮k30(pvp-k30)5g、滑石粉3g。二、工艺步骤(1)按处方称量辅料,过120目筛;(2)称取处方量的pvp-k30,加入到浓度为50%乙醇溶液中,配置成5%pvp-k30-乙醇溶液作为粘合剂;(3)将处方量的糊精29g、预胶化淀粉30g、mcc、l-hpc、ppvp依次加入湿法制粒机中干混,搅拌混合5min。然后缓慢加入已配置好的粘合剂,湿混,搅拌混合3min,制得软材;(4)将软材加入摇摆制粒机制粒,烘干;(5)整粒;(6)加入处方量的化合物3、滑石粉,混匀,压片。实施例10:制备1000片化合物1片剂(规格5mg/片)一、处方化合物15g、淀粉30g、微晶纤维素(mcc)30g、乳糖18g、羧甲基淀粉钠(cms-na)5g、交联羧甲基纤维素钠5g、羟丙甲纤维素(hpmc)5g、聚乙二醇6000(peg6000)2g。二、制备工艺(1)按处方称量辅料,过120目筛;(2)称取处方量的hpmc加入到总体积1/3的热水(80-90℃)中,充分分散与水化。冷却条件下不断搅拌,加冷水至总体积配制成2%的hpmc水溶液;(3)将处方量的淀粉、mcc、乳糖、cms-na、交联羧甲基纤维素钠依次加入湿法制粒机中干混,搅拌混合5min。然后缓慢加入已配置好的粘合剂,湿混,搅拌混合3min,制得软材;(4)将软材加入摇摆制粒机制粒,烘干;(5)整粒;(6)加入处方量的化合物1、peg6000,混匀,压片。实施例11:制备1000片化合物2片剂(规格5mg/片)一、处方化合物25g、淀粉30g、微晶纤维素(mcc)30g、乳糖18g、羧甲基淀粉钠(cms-na)5g、交联羧甲基纤维素钠5g、羟丙甲纤维素(hpmc)5g、聚乙二醇6000(peg6000)2g。二、制备工艺(1)按处方称量辅料,过120目筛;(2)称取处方量的hpmc加入到总体积1/3的热水(80-90℃)中,充分分散与水化。冷却条件下不断搅拌,加冷水至总体积配制成2%的hpmc水溶液;(3)将处方量的淀粉、mcc、乳糖、cms-na、交联羧甲基纤维素钠依次加入湿法制粒机中干混,搅拌混合5min。然后缓慢加入已配置好的粘合剂,湿混,搅拌混合3min,制得软材;(4)将软材加入摇摆制粒机制粒,烘干;(5)整粒;(6)加入处方量的化合物2、peg6000,混匀,压片。实施例12:制备1000片化合物3片剂(规格5mg/片)一、处方化合物35g、淀粉30g、微晶纤维素(mcc)30g、乳糖18g、羧甲基淀粉钠(cms-na)5g、交联羧甲基纤维素钠5g、羟丙甲纤维素(hpmc)5g、聚乙二醇6000(peg6000)2g。二、制备工艺(1)按处方称量辅料,过120目筛;(2)称取处方量的hpmc加入到总体积1/3的热水(80-90℃)中,充分分散与水化。冷却条件下不断搅拌,加冷水至总体积配制成2%的hpmc水溶液;(3)将处方量的淀粉、mcc、乳糖、cms-na、交联羧甲基纤维素钠依次加入湿法制粒机中干混,搅拌混合5min。然后缓慢加入已配置好的粘合剂,湿混,搅拌混合3min,制得软材;(4)将软材加入摇摆制粒机制粒,烘干;(5)整粒;(6)加入处方量的化合物3、peg6000,混匀,压片。试验例1:化合物1-3体外对pc12细胞损伤的保护作用pc12细胞具有神经细胞的一般特征,在神经生长因子(ngf)的作用下pc12细胞会停止分裂,长出突起,转化成神经元样细胞。因此,pc12细胞活性鉴定系统可以作为抗阿尔茨海默病药物的体外筛选方法。1、pc12细胞(大鼠肾上腺嗜铬瘤细胞株)的培养:接20×104个pc12细胞于100mm的培养皿中,含10mldmem培养基(其中含10%马血清、5%胎牛血清),两天后更换一次培养基,再过三天继代。先用pbs(磷酸盐缓冲液)将细胞洗两次,再加入10mlpbs于培养皿中,在37℃,5%co2的培养箱内培养10min,吹洗,转移到15ml的一次性离心管,离心后血球计数板上计数。24孔细胞培养板每孔先加入1ml含血清的dmem培养基,细胞计数后,每孔接2×104个细胞,co2培养箱培养24h后加样。2、活性测试:以二甲基亚砜(dmso)为阴性对照,ngf(40ng)为阳性对照,将化合物1-3配制成不同浓度的dmso溶液。用1ml含1%dmso和样品的dmem溶液(不含血清)将24孔细胞板的每孔原培养基取代后,放入37℃,5%co2的培养箱中培养。倒置显微镜下每隔24h、连续6天观察细胞形态变化,记录细胞的神经突起分化率(神经突起长于胞体直径一倍的细胞数目与视野下总细胞数目的比值),每个视野下约100个细胞,随机选取3处,并统计作图分析。试验结果见图1。试验结果表明,化合物1-3均具有促进pc12细胞突起伸长的作用,显示出拟神经生长因子活性。其中,化合物1和2生物活性明显,可作为抗阿尔茨海默病药物候选物进行后续研究。试验例2:实施例7、8小鼠药理实验1、动物:3月龄app转基因小鼠60只,雌雄各半,作为模型鼠。c57bl/6小鼠15只为正常对照。2、实验药物:盐酸多奈哌齐片(江苏豪森药业集团有限公司,5mg/片,阳性对照药)、实施例7片剂、实施例8片剂。使用时粉碎,用双蒸水溶解。3、分组及给药:将app转基因小鼠随机分为四组,分别为模型组、阳参盐酸多奈哌齐组(65mg/kg)、实施例7组(65mg/kg)、实施例8组(65mg/kg),每组15只。正常对照组和模型组给予等体积蒸馏水灌胃,每日1次。阳参组和实施例组灌胃相应药物,每日1次。各组小鼠灌胃24周,至9月龄时进行行为学实验。4、行为学测试:(1)morris水迷宫试验morris水迷宫水池直径120cm,水池深50cm。实验时将水池以四个等距离点均分为四个象限区,在第四象限位于池壁和圆心中间,放置有机玻璃站台。向水池中加水,水深约20cm,水面高出站台表面0.5cm,水温25±1℃,注入奶粉,混匀,使水成不透明的乳白色,达到动物视觉无法辨别池内有无平台的目的,并使计算机能成功跟踪小鼠的活动。试验在隔音的房间内进行,水池位置、光源位置及强度等各种试验条件在整个实验过程中保持不变,以供小鼠来定位平台位置。测试程序:定位航行实验,用于测量动物在水迷宫中的学习和记忆能力。每天进行1次,连续训练5天。第5天下午撤去平台,任选一个入水点,将小鼠面向池壁放入水池中,摄像系统自动记录小鼠3min内进出原平台区的次数及在原平台所在第四象限游泳时间和路程作为评价小鼠学习记忆成绩的指标。(2)跳台试验跳台仪实验箱与计算机自动记录系统相连。实验时将小鼠放入跳台仪实验箱内,适应环境5min,之后将小鼠轻放于跳台上,并将铜栅通电,当小鼠从跳台上跳下四肢接触铜栅时会受到电击,正常回避反应是跳上跳台返回安全区,逃避电击,如此学习5min,并记录此5min内的触电次数(错误次数),以此为学习成绩。24h后进行记忆能力测试,将小鼠置于跳台上,记录小鼠从停留在跳台上至第一次跳下受电击的时间即潜伏期和5min内的错误次数(小鼠四肢同时接触铜栅触电的次数),以此作为记忆功能的评价指标。(3)脑组织样品处理小鼠于末次行为学测试后,禁食12h,进行脑组织及血清取材。各组小鼠麻醉后眼球取血,离心(2500r/min,15min),分离血清保持温度在4℃以备后续指标检测;在低温下快速断头取全脑,以冰冷生理盐水清理血迹,用滤纸吸干,称重。每组随机选取6只投入4%多聚甲醛溶液中固定24h以上(4℃),之后换后固定液,待脑组织下沉后即可进行冰冻切片,或石蜡包埋,进行病理及免疫组化染色。其余小鼠分别迅速分离皮层和海马(冰砖上进行),各加入2ml生理盐水(蒸馏水)匀浆,低温高速离心机离心,分离上清液,用于组织含量测定。5、试验结果:(1)对app转基因小鼠空间学习记忆能力的影响试验结果显示,与正常组比较,模型组在morris水迷宫中穿越原平台位置次数、第四象限游泳时间和路程均显著减少。各给药组治疗后,在morris水迷宫中穿越原平台位置次数、第四象限游泳时间和路程均较模型组显著增多。实施例7组对app转基因小鼠空间学习记忆能力稍好于阳参组,实施例8组作用稍弱。结果见表1。表1对app转基因小鼠空间学习记忆能力的影响组别穿越次数(次)游泳时间(s)游泳路程(cm)正常对照组5.11±1.9349.30±11.09330.18±99.54模型组2.54±0.9731.05±10.24210.38±69.06阳参组4.98±1.2546.95±12.60320.01±89.95实施例7组5.21±2.0850.09±12.17333.54±89.18实施例8组4.33±1.2140.50±10.21310.22±90.50(2)对app转基因小鼠一次性回避反应记忆功能的影响试验结果显示,在跳台试验中,模型组错误次数较正常组明显增高,而实施例7、8及阳参组错误次数较模型组明显下降。结果见表2。表2对app转基因小鼠一次性回避反应记忆功能的影响组别错误次数(次)正常对照组1.45±0.33模型组2.68±0.45阳参组1.56±0.28实施例7组1.20±0.21实施例8组1.44±0.80(3)对app小鼠海马内乙酰胆碱、胆碱乙酰转移酶和乙酰胆碱酯酶含量的影响试验结果显示,与正常组相比,模型组海马内ach、胆碱乙酰转移酶(chat)的含量明显降低,而ache含量明显提高;实施例7、8及阳参组与模型组相比,海马内ach、chat的含量明显提高,而ache含量明显降低。说明实施例7、8能够有效提高海马内ach的含量,增强海马内chat的活性,抑制海马内ache的活性,从而改善app转基因痴呆模型病理学、胆碱能系统指标。其中实施例7作用优于阳参组,实施例8组作用稍弱。结果见表3。表3对app转基因小鼠海马ach、ache、chat含量的影响组别ach(iu/g.pro)ache(iu/g.pro)chat(iu/g.pro)正常对照组17.99±5.100.60±0.2118.24±5.51模型组10.89±3.011.01±0.339.98±2.35阳参组15.80±4.520.56±0.1516.00±4.51实施例7组17.51±4.850.59±0.1118.33±5.24实施例8组14.90±4.120.49±0.1515.62±4.25当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1