用于儿童过敏性紫癜评估的肠道菌群微生物的制作方法
本申请涉及生物医学技术领域,尤其涉及一种用于儿童过敏性紫癜评估的肠道菌群微生物。
背景技术:
近年来,过敏性紫癜(hsp)已成为儿童最常见的血管炎类型,过敏性紫癜全身性受累非常频繁,可能会出现肾受累等并发症,因此及时对儿童是否患有过敏性紫癜进行评估十分有必要。
大脑与胃肠道之间可以相互影响,相互作用,近些年研究发现,肠道通透性发生改变后,肠道微生物或代谢产物可进入血液,从而影响神经系统和宿主的健康,大脑和肠道双向的互动反应通过迷走神经相互联系,肠道菌群可以通过脑-肠轴影响神经系统的功能,脑-肠轴功能的变化也会改变肠道菌群结构,进而形成了细菌-脑-肠轴这一新的概念体系。
人体肠道中的微生物群落与宿主之间的关系记为密切,肠道菌群失调与多种临床疾病密切相关;肠道菌群在儿童过敏性紫癜过程中的作用并不明确,寻找可用来进行儿童过敏性紫癜评估的微生物标志物对探究肠道菌群在儿童过敏性紫癜过程中的作用机制具有重要的意义;且由于遗传因素在hsp的发病中占有一定比例,而hsp儿童与其母亲的肠道微生物群之间是否存在相关性尚不清楚。
技术实现要素:
本申请提供了用于儿童过敏性紫癜评估的肠道菌群微生物,以寻找可以用来评估儿童过敏性紫癜状况的微生物标志物。
为了解决上述技术问题,本申请实施例公开了如下技术方案:
本申请提供了一种用于儿童过敏性紫癜评估的肠道菌群微生物,所述微生物包括特征菌属,用于评估儿童过敏性紫癜,其中:
所述特征菌属包括:肠球菌属、梭杆菌属及链球菌属。
可选的,所述特征菌属还包括:roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属。
可选的,所述肠球菌属、梭杆菌属及链球菌属的相对丰度上升。
可选的,所述roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属的相对丰度下降。
可选的,采用试剂盒检测肠道菌群微生物。
可选的,所述采用试剂盒检测肠道菌群微生物,包括:
从对象粪便中提取dna样本;
针对dna样本构建测序文库;
对测序文库进行高通量测序,获得测序结果;
根据测序结果获得肠道菌群微生物的相对丰度。
与现有技术相比,本申请的有益效果为:
本申请提供了用于儿童过敏性紫癜评估的肠道菌群微生物中,通过将对象粪便排入一个清洁干燥的容器内,用采样勺从粪便内部挖取约500mg粪便,置于保存管中,用粪便菌群试剂盒提取微生物组总dna,设计含有barcode序列的特异引物,pcr扩增16srrna的v1-v2区,建立扩增子文库,illuminahiseq2500测序平台进行测序;降噪优化后的数据与健康儿童肠道菌群数据进行对比,重点分析肠球菌属、梭杆菌属及链球菌属、roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属的相对丰度,其中,所述roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属的相对丰度下降,所述肠球菌属、梭杆菌属及链球菌属的相对丰度上升。因此,肠球菌属、梭杆菌属及链球菌属、roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属具有较高的特异性和敏感性,在评估儿童过敏性紫癜过程中,将检测与研究结果相比较,来评估儿童肠道菌群微生物的水平变化,根据肠道菌群微生物的水平变化来判断是否存在过敏性紫癜的风险。
应当理解的是,以上的一般描述和后文的细节描述仅是示例性和解释性的,并不能限制本申请。
附图说明
为了更清楚地说明本申请的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,对于本领域普通技术人员而言,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
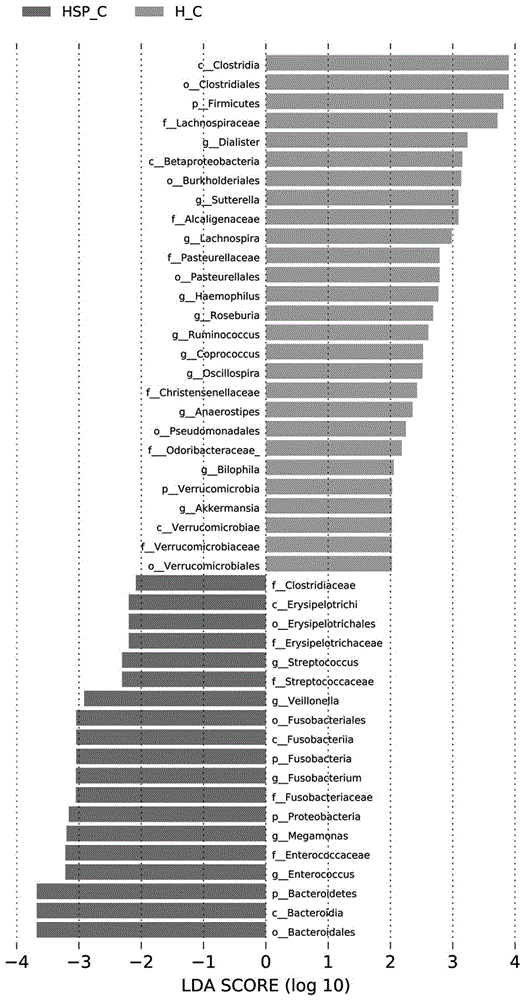
图1为本申请实施例中提供的用于儿童过敏性紫癜评估的肠道菌群微生物的相对丰度比照示意图;
图2为本申请实施例提供的用于儿童过敏性紫癜评估的肠道菌群微生物的又一相对丰度比照示意图;
图3为本申请实施例提供的用于儿童过敏性紫癜评估的肠道菌群微生物的又一相对丰度比照示意图。
具体实施方式
为了使本技术领域的人员更好地理解本申请中的技术方案,下面将结合本申请实施例中的附图,对本申请实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本申请一部分实施例,而不是全部实施例。基于本申请中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本申请保护的范围。
本申请提供了用于儿童过敏性紫癜评估的肠道菌群微生物中,通过将对象粪便排入一个清洁干燥的容器内,用采样勺从粪便内部挖取约500mg粪便,置于保存管中,用粪便菌群试剂盒提取微生物组总dna,设计含有barcode序列的特异引物,pcr扩增16srrna的v1-v2区,建立扩增子文库,illuminahiseq2500测序平台进行测序;降噪优化后的数据与健康儿童肠道菌群数据进行对比,重点分析肠球菌属、梭杆菌属及链球菌属、roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属的相对丰度,其中,所述roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属的相对丰度下降,所述肠球菌属、梭杆菌属及链球菌属的相对丰度上升,具体如下:
在一实施例中,本申请提供的用于儿童过敏性紫癜评估的肠道菌群微生物,所述微生物包括特征菌属,用于评估儿童过敏性紫癜,其中:
所述特征菌属包括:肠球菌属、梭杆菌属及链球菌属;所述特征菌属还包括:roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属。
进一步地,所述肠球菌属、梭杆菌属及链球菌属的相对丰度上升;所述roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属的相对丰度下降。
在本实施例中,采用试剂盒检测肠道菌群微生物。具体过程为:
从对象粪便中提取dna样本;
针对dna样本构建测序文库;
对测序文库进行高通量测序,获得测序结果;
根据测序结果获得肠道菌群微生物的相对丰度。
在本实施例中,采用试剂盒检测肠道菌群微生物,试剂盒为基于检测链球菌属、奈瑟菌属、嗜血杆菌属及卟啉单胞菌属、巨型球菌属、考拉杆菌属、梭菌属、粪球菌属及副普氏菌属丰度的诊断儿童过敏性紫癜的试剂盒,试剂盒组分如下:dna提取试剂、特异性检测肠球菌属、梭杆菌属及链球菌属、roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属16srrnade引物对、反应缓冲液、、三磷酸碱基脱氧核苷酸(dntps)、taq-聚合酶逆转录酶、dnase、rnase抑制剂、depc-水、无菌水。
具体包括:用粪便菌群试剂盒提取微生物组总dna,设计含有barcode序列的特异引物,pcr扩增16srrna的v1-v2区,建立扩增子文库,illuminahiseq2500测序平台进行测序,每个样本均产生相应的高质量测序结果。
根据测序结果获得肠道菌群微生物的相对丰度。
具体为:测序原始数据用flash软件进行拼接合成。利用qiime软件对序列进行过滤,过滤后的数据进行16srrna基因的分析。高质量的核苷酸序列根据greengenes数据库进行聚类,相似度>96%的核苷酸序列作为一个可操作性分类单元(otu),之后根据qiime软件中的rdp分类和greengenes软件中的参考数据集,将每一个otu进行细菌种属的分类鉴定,并计算其相对丰度。根据相对丰度,挑选两组存在显著差异的菌属。
在本实施例中,相对丰度下降或上升是指丰度差异,而丰度差异是指与正常或对照组体内水平相比,在过敏性紫癜儿童的患者体内得到更高或更低水平的微生物,从本申请的目的出发,本申请中选用正常儿童与过敏性紫癜儿童作对比,具体选取正常儿童与过敏性紫癜儿童中的粪便作为样本。
具体分析结果参考图1,图1为本申请实施例中提供的健康儿童和过敏性紫癜儿童的肠道菌群微生物的相对丰度比照示意图,其中示意图的左侧hsp-c代表患儿样本,右侧h-c代表健康儿童样本,图1示出所述肠球菌属、梭杆菌属及链球菌属的相对丰度上升;所述roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属的相对丰度下降。
由上述可见,肠球菌属、梭杆菌属及链球菌属、roseburia,ruminococcus、粪球菌属、嗜双球菌属及阿克曼菌属的特异性和敏感性较高,故在本申请实施例中选取这几个菌属为过敏性紫癜儿童肠道菌群评估的特征菌,因此为评估体系的关键。
因此,可以将检测与研究结果相比较,来评估儿童肠道菌群微生物中上述特征菌的水平变化,根据肠道菌群微生物的水平变化来判断是否存在过敏性紫癜的风险。
本申请发现了特征菌群在过敏性紫癜儿童中的水平变化,通过检测特征菌群的变化,可以实现过敏性紫癜儿童的评估,使用本发明的特征微生物作为标志物进行诊断,特异性高、敏感性强,应用于儿童过敏性紫癜评估具有较高的准确性。
在又一实施例中,如图2示出,图2左侧hsp-m代表患儿的母亲样,右侧h-m代表健康儿童的母亲样本,通过比较患有过敏性紫癜的儿童的母亲和健康儿童的母亲之间的肠道菌群,同样发现差异:与健康儿童的母亲相比,患有过敏性紫癜的儿童的母亲的肠道菌群中中普雷沃菌属和巨单胞菌属的相对丰度上升,而链球菌属、嗜血杆菌属、阿克曼菌属的相对丰度下降;这些潜在的生物标志物表明,患有过敏性紫癜的儿童的母亲和健康儿童的母亲的肠道菌群存在差异,且紫癜患儿肠道菌群与其母亲肠道菌群相似。
在又一实施例中,如图3示出,通过将患儿与其母亲的肠道菌群样本合并得到样本1,将健康儿童与其母亲的肠道菌群样本得到样本2,图3中左侧hsp-m+c代表样本1的相关数据,右侧h-m+c代表样本2的相关数据,通过对比若干个样本1和样本2发现样本1的丰富度和多样性低于样本2,且样本1和样本2的肠道微生物组分不同;且在样本1在中发现了酸性氨基球菌属和roseburia,而在样本2中并未发现酸性氨基球菌属和roseburia,因此酸性氨基球菌属和roseburia可作为区分样本1和样本2的潜在生物标志物。
由于以上实施方式均是在其他方式之上引用结合进行说明,不同实施例之间均具有相同的部分,本说明书中各个实施例之间相同、相似的部分互相参见即可。在此不再详细阐述。
本领域技术人员在考虑说明书及实践这里发明的公开后,将容易想到本申请的其他实施方案。本申请旨在涵盖本发明的任何变型、用途或者适应性变化,这些变型、用途或者适应性变化遵循本申请的一般性原理并包括本申请未公开的本技术领域中的公知常识或惯用技术手段。说明书和实施例仅被视为示例性的,本申请的真正范围和精神由权利要求的内容指出。
以上所述的本申请实施方式并不构成对本申请保护范围的限定。
- 还没有人留言评论。精彩留言会获得点赞!