一种吡唑并1,3,5-三嗪类化合物及其制备方法与流程
本发明涉及有机中间体技术领域,特别涉及一种吡唑并1,3,5-三嗪类化合物及其制备方法。
背景技术:
1,3,5-三嗪类化合物是一类重要的含氮杂环化合物,有良好的生物活性,在天然产物和药物化学中有着广泛的运用。具有1,3,5-三嗪结构单元的化合物具有多种生理活性,如抗肿瘤,抗结核,抗病毒,抗菌,抗疟以及作为酶抑制剂;此外,还可用于制备有机金属材料,液晶,分子探针和荧光增白剂。基于此,1,3,5-三嗪类化合物的应用引起了人们的广泛关注。
近些年来,国内外研究人员一直致力于1,3,5-三嗪类化合物的构建,如abhishekr.tiwari等用不同取代基的苄醇和苯甲脒盐酸盐,加入硫化镍作为催化剂,碳酸铯作碱,dmso作为溶剂,在100℃条件下反应16h,最终经过环合反应得到不同取代基的1,3,5-三嗪类化合物,整个反应过程需要较高的温度(100℃),碱以及nis催化剂等添加剂,条件苛刻,不易控制。(参见abhishekr.tiwari,nis-catalyzedoxidativecyclizationofalcoholswithamidines:asimpleandefficient,transition-metalfreemethodforthesynthesisof1,3,5-triazines.org.biomol.chem.2015,13(45),10973-10976),具体反应路线如下:
技术实现要素:
有鉴于此,本发明目的在于提供一种吡唑并1,3,5-三嗪类化合物及其制备方法。本发明构建了一种新型1,3,5-三嗪类化合物,并且,该1,2,4-三唑类化合物的制备过程无需催化剂,条件温和,易于控制。
为了实现上述发明目的,本发明提供以下技术方案:
本发明提供了一种吡唑并1,3,5-三嗪类化合物,具有式i所示结构:
式i中,r1为氢、烷基、卤素或苯基;r2为苯基、苄基、萘基、苯甲酰基、烷基取代的苯基、甲氧基取代的苯基、卤素取代的苯基、三氟甲基取代的苯基、对硝基取代的苯基、对腈基取代的苯基、烷基、环己基或甲酸乙酯基。
优选地,所述r1和r2中烷基独立为1~5个碳原子的烷基;
优选地,所述r2中,烷基取代的苯基为对乙基苯基或2,4,6-三甲基苯基,甲氧基取代的苯基为对甲氧基苯基、2,4-二甲氧基苯基或3,4,5-三甲氧基苯基,卤素取代的苯基为氟取代的苯基、氯取代的苯基或溴取代的苯基,三氟甲基取代的苯基为对三氟甲基苯基、邻三氟甲基苯基或3,5-双(三氟甲基)苯基。
本发明提供了以上方案所述吡唑并1,3,5-三嗪类化合物的制备方法,包括以下步骤:
将氨基吡唑类化合物、异硫氰酸酯类化合物、四甲基胍和极性有机溶剂混合,得到混合液;所述混合液在光照和20~80℃温度条件且无催化剂下进行光串联环化反应,得到所述吡唑并1,3,5-三嗪类化合物;
所述氨基吡唑类化合物具有式ii所示结构;所述异硫氰酸酯类化合物的结构式为r2n=c=s。
优选地,所述氨基吡唑类化合物、异硫氰酸酯类化合物与四甲基胍的摩尔比为(3~4):1:(2.9~3.1)。
优选地,所述极性有机溶剂为二甲基亚砜、n,n-二甲基甲酰胺、甲苯、乙醇、乙腈和二氯甲烷中的一种或几种。
优选地,所述极性有机溶剂的体积与所述氨基吡唑类化合物的物质的量的比为1l:0.1~0.3mol。
优选地,所述光照的光源波长为200~1000nm。
优选地,所述光串联环化反应的温度为40~60℃。
优选地,所述光串联环化反应的时间为1~48h。
本发明提供了一种吡唑并1,3,5-三嗪类化合物,具有式i所示结构,为新型结构的1,3,5-三嗪类化合物,拓展了1,3,5-三嗪类化合物的种类。本发明提供的吡唑并1,3,5-三嗪类化合物具有潜在抗菌、抗炎、抗癌、抗病毒、抗虫的特点,可在生物医药和农药中应用。
本发明提供了所述吡唑并1,3,5-三嗪类化合物的制备方法,将氨基吡唑类化合物、异硫氰酸酯类化合物、四甲基胍和极性有机溶剂混合,得到混合液;所述混合液在光照和20~80℃温度条件且无催化剂下进行光串联环化反应,得到所述吡唑并1,3,5-三嗪类化合物。在光照和20~80℃温度条件下,氨基吡唑类化合物、异硫氰酸酯类化合物和四甲基胍反应形成一种电子供体和受体复合物,原料并不能吸收可见光,但是这种复合物可以吸光,从而完成对原料的活化,进而促进原料的反应,无需催化剂即可制备得到所述吡唑并1,3,5三嗪类化合物,反应条件温和,步骤简单,易于控制。
附图说明
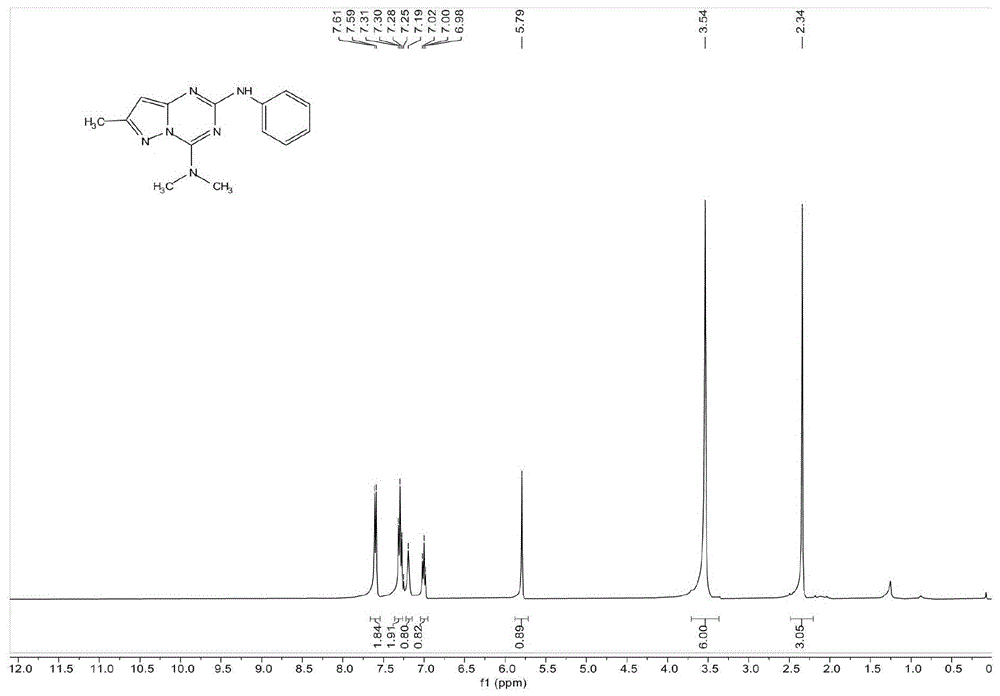
图1为本发明实施例1所得产品的核磁共振氢谱图;
图2为本发明实施例1所得产品的核磁共振碳谱图;
图3为本发明实施例2所得产品的核磁共振氢谱图;
图4为本发明实施例2所得产品的核磁共振碳谱图;
图5为本发明实施例3所得产品的核磁共振氢谱图;
图6为本发明实施例3所得产品的核磁共振碳谱图;
图7为本发明实施例4所得产品的核磁共振氢谱图;
图8为本发明实施例4所得产品的核磁共振碳谱图;
图9为本发明实施例5所得产品的核磁共振氢谱图;
图10为本发明实施例5所得产品的核磁共振碳谱图;
图11为本发明实施例6所得产品的核磁共振氢谱图;
图12为本发明实施例6所得产品的核磁共振碳谱图;
图13为本发明实施例7所得产品的核磁共振氢谱图;
图14为本发明实施例7所得产品的核磁共振碳谱图;
图15为本发明实施例8所得产品的核磁共振氢谱图;
图16为本发明实施例8所得产品的核磁共振碳谱图;
图17为本发明实施例9所得产品的核磁共振氢谱图;
图18为本发明实施例9所得产品的核磁共振碳谱图;
图19为本发明实施例10所得产品的核磁共振氢谱图;
图20为本发明实施例10所得产品的核磁共振碳谱图;
图21为本发明实施例11所得产品的核磁共振氢谱图;
图22为本发明实施例11所得产品的核磁共振碳谱图;
图23为本发明实施例12所得产品的核磁共振氢谱图;
图24为本发明实施例12所得产品的核磁共振碳谱图;
图25为本发明实施例13所得产品的核磁共振氢谱图;
图26为本发明实施例13所得产品的核磁共振碳谱图;
图27为本发明实施例14所得产品的核磁共振氢谱图;
图28为本发明实施例14所得产品的核磁共振碳谱图。
具体实施方式
本发明提供了一种吡唑并1,3,5-三嗪类化合物,具有式i所示结构:
式i中,r1为氢基、烷基、卤素或苯基;r2为苯基、苄基、萘基、苯甲酰基、烷基取代的苯基、甲氧基取代的苯基、卤素取代的苯基、三氟甲基取代的苯基、对硝基取代的苯基、对腈基取代的苯基、烷基、环己基或甲酸乙酯基。
在本发明中,所述r1为氢基、烷基、卤素或苯基。在本发明中,所述烷基优选为1~5个碳原子的烷基,进一步优选为甲基、乙基、叔丁基或二甲基;所述卤素优选为氟、氯或溴,进一步优选为溴。
在本发明中,所述r2为苯基、苄基、萘基、苯甲酰基、烷基取代的苯基、甲氧基取代的苯基、卤素取代的苯基、三氟甲基取代的苯基、对硝基取代的苯基、对腈基取代的苯基、烷基、环己基或甲酸乙酯基。在本发明中,所述烷基取代的苯基优选为对乙基苯基或2,4,6-三甲基苯基;所述甲氧基取代的苯基优选为对甲氧基苯基、2,4-二甲氧基苯基或3,4,5-三甲氧基苯基;所述卤素取代的苯基为氟取代的苯基、氯取代的苯基或溴取代的苯基,进一步优选为对氟苯基、对溴苯基、邻氯苯基、间氯苯基或2,4-二氟苯基;所述三氟甲基取代的苯基为对三氟甲基苯基、邻三氟甲基苯基或3,5-双(三氟甲基)苯基;所述烷基优选为1~5个碳原子的烷基,进一步优选为甲基或正丁基。
在本发明具体实施例中,所述吡唑并1,3,5-三嗪类化合物的具体结构为:
本发明提供的吡唑并1,3,5-三嗪类化合物,为新型结构的1,3,5-三嗪类化合物,拓展了1,3,5-三嗪类化合物的种类。本发明提供的吡唑并1,3,5-三嗪类化合物具有潜在抗菌、抗炎、抗癌、抗病毒、抗虫的特点,可在生物医药和农药中应用。
本发明提供了以上方案所述吡唑并1,3,5-三嗪类化合物的制备方法,包括以下步骤:
将氨基吡唑类化合物、异硫氰酸酯类化合物、四甲基胍和极性有机溶剂混合,得到混合液;所述混合液在光照和20~80℃温度条件且无催化剂下进行光串联环化反应,得到所述吡唑并1,3,5-三嗪类化合物;
所述氨基吡唑类化合物具有式ii所示结构;所述异硫氰酸酯类化合物的结构式为r2n=c=s。
本发明将氨基吡唑类化合物、异硫氰酸酯类化合物、四甲基胍和极性有机溶剂混合,得到混合液。在本发明中,所述氨基吡唑类化合物具有式ii所示结构,所述式ii所示结构中的的r1与所述式i所示结构中的r1保持一致,在此不再赘述。在本发明具体实施例中,所述氨基吡唑类化合物具体为3-氨基-5-甲基吡唑、3,4-二甲基-5-氨基吡唑、3-氨基-5-乙基吡唑、3-氨基-5-叔丁基吡唑、3-氨基-4-溴吡唑、3-氨基-5-苯基吡唑。
在本发明中,所述异硫氰酸酯类化合物的结构式为r2n=c=s,所述异硫氰酸酯类化合物结构式中的r2与所述式i所示结构中的r2保持一致,在此不再赘述。在本发明具体实施例中,所述异硫氰酸酯类化合物具体为异硫氰酸苯酯、对氟异硫氰酸苯酯、对甲氧基异硫氰酸苯酯、对乙基异硫氰酸苯酯、2,4-二甲氧基异硫氰酸苯酯、异硫氰酸苄酯、异硫氰酸甲酯、2,4,6-三甲基异硫氰酸苯酯。
在本发明中,所述氨基吡唑类化合物、异硫氰酸酯类化合物与四甲基胍的摩尔比优选为(3~4):1:(2.9~3.1),进一步优选为3:1:3。
在本发明中,所述所述极性有机溶剂优选为二甲基亚砜、n,n-二甲基甲酰胺、甲苯、乙醇、乙腈和二氯甲烷中的一种或几种;所述极性有机溶剂的体积与所述氨基吡唑类化合物的物质的量的比优选为1l:0.1~0.3mol。
本发明对所述氨基吡唑类化合物、异硫氰酸酯类化合物、四甲基胍和极性有机溶剂的来源没有特别的要求,采用本领域技术人员熟知的相应市售商品即可。本发明对所述混合的方法没有特别的要求,采用本领域技术人员熟知的方法将各原料组分混合均匀即可,本发明对各原料组分混合的先后顺序没有特别的要求,可以任意先后顺序混合。
得到混合液后,本发明将所述混合液在光照和20~80℃温度条件下进行光串联环化反应,得到所述吡唑并1,3,5-三嗪类化合物。在本发明中,所述光照的光源波长优选为200~1000nm,进一步优选为300~800nm,更优选为400~465nm。本发明对所述光源没有特别的要求,能够提供上述波长的光源均可。在本发明中,所述光串联环化反应的温度优选为40~60℃;所述光串联环化反应的时间优选为1~48h,进一步优选为6~24h。在本发明中,所述光串联环化反应优选在搅拌的条件下进行,本发明所述搅拌的速度没有特别的要求。
光串联环化反应后,本发明优选对所得光串联环化反应液进行提纯处理。在本发明中,所述提纯处理优选为柱层析。在本发明中,所述柱层析的洗脱液优选为石油醚和乙酸乙酯的混合溶剂,所述混合溶剂中石油醚和乙酸乙酯的体积比优选为1~30:1,进一步优选为5~20:1,更优选为5:1。本发明对柱层析的具体实施方法没有特别要求,采用本领域技术人员熟知的方式即可。本发明利用石油醚和乙酸乙酯为洗脱液,对环化反应后的混合液进行柱层析提纯处理,能够得到纯度较高的吡唑并1,3,5-三嗪类化合物。在本发明中,所述吡唑并1,3,5-三嗪类化合物的纯度优选为98.5~99.9%,进一步优选为99~99.9%。
本发明提供了所述吡唑并1,3,5-三嗪类化合物的制备方法,在光照和20~80℃温度条件下,氨基吡唑类化合物、异硫氰酸酯类化合物和四甲基胍反应形成一种电子供体和受体复合物,能够加快反应的进行,无需催化剂即可制备得到所述吡唑并1,3,5三嗪类化合物,反应条件温和,步骤简单,易于控制;另外,本发明提供的吡唑并1,3,5-三嗪类化合物的制备方法,对原料的适应性好,可用于不同取代基的吡唑并1,3,5-三嗪类化合物的制备。
下面结合实施例对本发明提供的吡唑并1,3,5-三嗪类化合物及其制备方法进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
实施例1
一种吡唑并1,3,5-三嗪类化合物,具有式i-(1)所示结构:
制备方法:在反应管中加入0.3mmol3-氨基-5-甲基吡唑、0.1mmol异硫氰酸苯酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,混合液在465nm光源照射下,60℃搅拌反应12h;反应结束后,通过析层析分离纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物20.4mg,产率76%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图1和图2所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm):δ7.61-7.59(d,j=8hz,2h),7.31-7.28(t,j=8hz,2h),7.19(s,1h),7.02-6.98(t,j=8hz,1h),5.79(s,1h),3.54(s,6h),2.34(s,3h).
13cnmr(100mhz,cdcl3,ppm):δ154.9,154.8,153.7,150.2,139.7,128.8,122.3,119.4,91.6,40.2,14.7.
ms(ei,70ev):m/z(%)=268,253,212,199,92.
根据以上数据和谱图分析可知,所得产物符合式i-(1)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例2
一种吡唑并1,3,5-三嗪类化合物,具有式i-(2)所示结构:
制备方法:在反应管中加入0.3mmol3,4-二甲基-5-氨基吡唑、0.1mmol的异硫氰酸苯酯、0.3mmol的四甲基胍、0.5ml乙腈和0.5mldmf混合,混合液在465nm光源照射下,20℃搅拌反应48h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物16.9mg,产率60%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图3和图4所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm):δ7.68-7.64(m,2h),7.33-7.29(m,2h),7.02-6.98(m,2h),3.54(s,6h),2.30(s,3h),2.09(s,3h).
13cnmr(100mhz,cdcl3,ppm):δ154.2,154.1,150.2,150.2,140.0,128.8,122.0,118.9,99.5,40.1,12.8,6.8.
ms(ei,70ev):m/z(%)=282,228,214,161,118.
根据以上数据和谱图分析可知,所得产物符合式i-(2)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例3
一种吡唑并1,3,5-三嗪类化合物,具有式i-(3)所示结构:
制备方法:在反应管中加入0.3mmol3-氨基-5-乙基吡唑、0.1mmol异硫氰酸苯酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,混合液在365nm光源照射下,70℃搅拌反应15h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物18.0mg,产率64%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图5和图6所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm):δ7.65-7.63(m,3h),7.35-7.31(m,2h),7.05-7.01(m,1h),5.86(s,1h),3.58(s,6h),2.77-2.71(q,j=8hz,2h),1.34-1.30(t,j=8h,3h).
13cnmr(100mhz,cdcl3,ppm):δ160.5,154.9,153.6,150.3,139.8,128.8,122.2,119.4,90.1,40.2,22.4,13.2.
ms(ei,70ev):m/z(%)=282,241,228,174,132.
根据以上数据和谱图分析可知,所得产物符合式i-(3)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例4
一种吡唑并1,3,5-三嗪类化合物,具有式i-(4)所示结构:
制备方法:在反应管中加入0.3mmol的3-氨基-5-叔丁基吡唑、0.1mmol的异硫氰酸苯酯、0.3mmol的四甲基胍、0.5ml乙腈和0.5mldmf混合,混合液在365nm光源照射下,80℃搅拌反应1h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物20.8mg,产率67%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图7和图8所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm):δ7.62-7.60(t,j=8hz,3h),7.31-7.27(q,j=8hz,2h),7.23(s,1h),5.88(s,1h),3.56(s,6h),1.34(s,9h).
13cnmr(100mhz,cdcl3,ppm):δ167.3,154.8,153.3,150.3,139.8,128.8,122.1,119.4,88.4,40.3,32.8,30.1.
ms(ei,70ev):m/z(%)=310,295,253,225,185.
根据以上数据和谱图分析可知,所得产物符合式i-(4)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例5
一种吡唑并1,3,5-三嗪类化合物,具有式i-(5)所示结构:
制备方法:在反应管中加入0.1mmol3-氨基-4-溴吡唑、0.1mmol异硫氰酸苯酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,混合液在415nm光源照射下,80℃搅拌反应6h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物24.2mg,产率73%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图9和图10所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm):δ7.76(s,1h),7.64-7.62(d,j=8hz,2h),7.34-7.31(t,j=8hz,2h),7.10(s,1h),7.06-7.00(t,j=8hz,1h),3.56(s,6h).
13cnmr(100mhz,cdcl3,ppm):δ155.4,150.2,149.9,144.5,139.3,128.9,122.7,119.4,40.6.
ms(ei,70ev):m/z(%)=332,294,196,132,118.
根据以上数据和谱图分析可知,所得产物符合式i-(5)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例6
一种吡唑并1,3,5-三嗪类化合物,具有式i-(6)所示结构:
制备方法:在反应管中加入0.3mmol3-氨基-5-苯基吡唑、0.1mmol异硫氰酸苯酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,混合液在465nm光源照射下,30℃搅拌反应12h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物21.1mg,产率64%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图11和图12所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm):δ7.90(s,2h),7.63-7.61(d,j=8hz,2h),7.44-7.29(m,5h),7.03-7.00(t,j=8hz,1h),6.30-6.29(d,j=4hz,1h),3.58(s,6h).
13cnmr(100mhz,cdcl3,ppm):δ155.6,155.0,154.0,150.2,139.6,133.0,128.9,128.8,128.6,126.4,122.4,119.5,88.7,40.5.
ms(ei,70ev):m/z(%)=330,278,253,200,132.
根据以上数据和谱图分析可知,所得产物符合式i-(6)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例7
一种吡唑并1,3,5-三嗪类化合物,具有式i-(7)所示结构:
制备方法:在反应管中加入0.3mmol3-氨基吡唑、0.1mmol异硫氰酸苯酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,在425nm光源照射下,60℃搅拌反应48h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物21.3mg,产率84%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图13和图14所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm):δ7.79(s,1h),7.62-7.60(d,j=8hz,2h),7.32-7.29(t,j=8hz,3h),7.03-7.00(t,j=8hz,1h),5.98(d,1h),3.56(s,6h).
13cnmr(100mhz,cdcl3,ppm):δ=154.9,153.3,150.6,144.9,139.6,128.9,122.5,119.5,91.6,40.4.
ms(ei,70ev):m/z(%)=254,212,156,132,104.
根据以上数据和谱图分析可知,所得产物符合式i-(7)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例8
一种吡唑并1,3,5-三嗪类化合物,具有式i-(8)所示结构:
制备方法:在反应管中加入0.1mmol3-氨基吡唑、0.1mmol对氟异硫氰酸苯酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,在465nm光源照射下,60℃搅拌反应12h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物19.6mg,产率72%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图15和图16所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm):7.79-7.78(d,j=4.0hz,1h),7.57-7.52(m,2h),7.17(s,1h),7.03-6.98(m,2h),5.96(d,1h),3.56(s,6h).
13cnmr(100mhz,cdcl3,ppm):δ158.5(d,j=24hz),155.0,153.2,150.5,144.9,135.6,121.4(d,j=7hz),115.3(d,j=2hz),100.0,91.5,40.4.
ms(ei,70ev):m/z(%)=272,228,203,190,136.
根据以上数据和谱图分析可知,所得产物符合式i-(8)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例9
一种吡唑并1,3,5-三嗪类化合物,具有式i-(9)所示结构:
制备方法:在反应管中加入0.3mmol3-氨基吡唑、0.1mmol对甲氧基异硫氰酸苯酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,混合液在1000nm光源照射下,60℃搅拌反应12h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物20.1mg,产率71%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图17和图18所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm):δ7.78-7.76(t,j=8hz,1h),7.50-7.46(m,2h),7.32(s,1h),6.87-6.84(q,j=4hz,2h),5.93-5.92(d,j=4hz,1h),3.78(s,3h),3.53(s,6h).
13cnmr(100mhz,cdcl3,ppm):δ155.4,155.3,153.4,150.4,144.8,132.7,121.9,114.0,91.2,55.5,40.3.
ms(ei,70ev):m/z(%)=284,269,199,188,148.
根据以上数据和谱图分析可知,所得产物符合式i-(9)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例10
一种吡唑并1,3,5-三嗪类化合物,具有式i-(10)所示结构:
制备方法:在反应管中加入0.3mmol3-氨基吡唑、0.1mmol对乙基异硫氰酸苯酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,在465nm光源照射下,60℃搅拌反应18h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物19.7mg,产率70%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图19和图20所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm)δ7.79-7.78(d,j=4.0hz,1h),7.52-7.50(d,j=8hz,2h),7.16-7.14(d,j=8hz,2h),6.99(s,1h),5.98-5.97(d,j=4hz,1h),3.56(s,6h),2.64-2.59(q,j=8hz,2h),1.25-1.21(q,j=8hz,3h).
13cnmr(100mhz,cdcl3,ppm)δ155.0,153.3,150.5,144.9,138.6,137.1,128.2,119.8,91.4,40.4,28.3,15.8.
ms(ei):m/z=282,267,238,213,197.
根据以上数据和谱图分析可知,所得产物符合式i-(10)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例11
一种吡唑并1,3,5-三嗪类化合物,具有式i-(11)所示结构:
制备方法:在反应管中加入0.3mmol3-氨基吡唑、0.1mmol2,4-二甲氧基异硫氰酸苯酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,混合液在200nm光源照射下,50℃搅拌反应6h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物22.0mg,产率70%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图20和图21所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm)δ8.33-8.31(d,j=8hz,1h),7.78-7.77(d,j=4hz,1h),7.21(s,1h),6.53-6.50(q,j=12hz,2h),5.98-5.97(d,j=4hz,1h),3.87(s,3h),3.80(s,3h),3.57(s,6h).
13cnmr(100mhz,cdcl3,ppm)δ155.3,154.9,153.3,150.4,149.4,144.8,122.7,120.1,103.7,98.7,91.3,55.7,55.6,40.4.
ms(ei):m/z=314,283,268,229,207.
根据以上数据和谱图分析可知,所得产物符合式i-(11)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例12
一种吡唑并1,3,5-三嗪类化合物,具有式i-(12)所示结构:
制备方法:在反应管中加入0.2mmol3-氨基吡唑、0.1mmol异硫氰酸甲酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,混合液在425nm光源照射下,60℃搅拌反应12h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物13.1mg,产率68%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图23和图24所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm)δ7.69(d,j=2hz,1h),5.86(s,1h),3.46(s,6h),2.94-2.93(d,j=4hz,3h).
13cnmr(100mhz,cdcl3,ppm)δ158.2,153.9,150.3,144.6,88.0,40.1,28.3.
ms(ei):m/z=192,163,123,82,57.
根据以上数据和谱图分析可知,所得产物符合式i-(12)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例13
一种吡唑并1,3,5-三嗪类化合物,具有式i-(13)所示结构:
制备方法:在反应管中加入0.3mmol3-氨基吡唑、0.1mmol异硫氰酸苄酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,在465nm光源照射下,60℃搅拌反应12h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物16.1mg,产率60%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图25和图26所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm)δ7.74(s,1h),7.36-7.31(q,j=12hz,4h),5.88(s,1h),5.33(s,1h),4.63-4.61(d,j=8hz,2h),3.49(s,6h).
13cnmr(100mhz,cdcl3,ppm)δ157.5,152.4,150.5,143.7,139.4,128.6,127.6,127.2,90.8,47.4,41.3.
ms(ei):m/z=268,224,197,163,134,106.
根据以上数据和谱图分析可知,所得产物符合式i-(13)所示吡唑并1,3,5-三嗪类化合物的结构。
实施例14
一种吡唑并1,3,5-三嗪类化合物,具有式i-(14)所示结构:
制备方法:在反应管中加入0.3mmol3-氨基吡唑、0.1mmol2,4,6-三甲基异硫氰酸苯酯、0.3mmol四甲基胍、0.5ml乙腈和0.5mldmf混合,在465nm光源照射下,60℃搅拌反应12h;反应结束后,通过析层析分纯化,柱层析洗脱液中石油醚和乙酸乙酯的体积比为5:1,得到纯化后的目标产物18.4mg,产率62%,纯度为99.9%。
对所得产物的结构进行表征,核磁共振氢谱图和核磁共振碳谱图分别如图23和图24所示,结构表征数据如下所示:
1hnmr(400mhz,cdcl3,ppm)δ7.70(d,j=2hz,1h),6.90(s,2h),5.78(s,1h),3.44(s,6h),2.28(s,3h),2.23(s,6h).
13cnmr(100mhz,cdcl3,ppm)δ156.8,154.0,150.6,144.7,136.0,133.2,128.7,93.2,40.1,21.0,10.0.
ms(ei):m/z=296,281,252,226,213.
根据以上数据和谱图分析可知,所得产物符合式i-(14)所示吡唑并1,3,5-三嗪类化合物的结构。
由实施例1~14的表征结果可知,本发明提供提供了一系列的吡唑并1,3,5-三嗪类化合物;本发明提供的制备方法利用光的照射和加热为原料提供所需能量,不添加催化剂即可得到目标产物,反应条件温和,易于控制;此外,本发明提供的制备方法原料易得,降低了原料成本;而且制备所得吡唑并1,3,5-三嗪类化合物具有较高的纯度,因此本发明提供的制备方法具有较大的市场推广价值。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!