一种阿伏苯宗的合成工艺方法与流程
1.本发明属于精细化工技术领域,一种制备有机中间体的方法,具体而言涉及一种制备阿伏苯宗的工艺方法。
背景技术:
2.传统意义上,将紫外光谱分为3个区,波长在320~400nm的长波紫外线称为uv-a,波长在280-320nm的中波紫外线称为uv-b,而波长在200-280nm的短波紫外线称为uv-c。uv-a穿透力最强,到达地表的量是uv-b的100倍,可造成晒红、晒伤,并可加强uv-b对皮肤的伤害力,可穿透至真皮层,是皮肤老化的主因;uv-b致癌性最强,晒红及晒伤作用为uv-a的1000倍;uv-c则可被臭氧层所阻隔,但近年来随着臭氧层的破坏,uv-c对人体的伤害也逐渐引起人们的重视。
3.人们为保护人体免受过量的紫外线辐射,把具有安全、高效吸收紫外线辐射的紫外线吸收剂广泛应用于化妆品、护发品、织物处理及洗涤剂中。其中由罗氏公司研发的丁基甲氧基二苯甲酰甲烷(parsol 1789,阿伏苯宗)是专门用于护肤化妆品的一类抗uv-a紫外光线吸收剂。阿伏苯宗是世界上仅有的少量几种uv-a型吸收剂中最为有效的一种,被美国fda列为非处方药(otc),准许在美国使用,欧盟和日本也已经批准其使用,为安全有效的防晒剂。因此,实现阿伏苯宗工业化生产,对提高经济效益,促进企业发展有重要的意义。
4.合成防晒剂阿伏苯宗文献报道的方法有以下几种。以对甲氧基苯乙酮和对叔丁基苯甲酸甲酯为原料的合成方法是以强碱做催化剂进行直接缩合(中国专利cn104876814和cn1958549,美国专利us4387089),用此法生产大体都用氨基钠、氢化钠或钠做催化剂,收率在48~78%。但是氨基钠在反应过程中易产生氨解等副反应;氢化钠和钠遇水剧烈反应,生产过程中安全隐患很大,对设备的要求也较高;且氨基钠和氢化钠价格昂贵,大规模生产需要的成本较高,在市场中无价格优势。以对叔丁基苯甲醛与对甲氧基苯乙酮在甲醇钠作用下缩合生成3-[4-叔丁基苯基]-1-(4-甲氧基苯基)-2-丙烯-1-酮,再经卤素加成,甲醇钠脱卤素合成(合成化学,2008,16(3):342-343;ep0994092a1),此法产率较高,但此法合成中需要用到溴素或者氯气。不仅对设备要求高,而且会对人和环境造成严重伤害。basf专利us6278025也以对叔丁基苯甲醛与对甲氧基苯乙酮为原料,先制得3-[4-叔丁基苯基]-1-(4-甲氧基苯基)-2-丙烯-1-酮,再以双氧水为氧化剂进行环氧化,最后以四(三苯基膦)化钯为催化剂进行开环制得阿伏苯宗,总收率71.91%。该法不使用卤素,但使用昂贵的催化剂进行开环,催化剂无法回收。以对叔丁基苯乙酮和对甲氧基苯甲酰氯为原料,进行酰基化反应生成阿伏苯宗(世界专利wo2006100225),用此法合成中,需用氯化亚铜做催化剂,反应时间达20h,后处理繁琐,还需用到氯仿等毒性较大的试剂。以对甲氧基苯甲酸甲酯和对叔丁基苯乙酮为原料,以氨基钠为催化剂,经缩合制得阿伏苯宗(中国专利cn109867597;chemistry-a european journal,2019,25(46):10797-10802),该法使用氨基钠做催化剂,仍存在前述的问题,原料对叔丁基苯乙酮价格较高,不易获得,且文献都未报道收率情况。
[0005]
阿伏苯宗的工业制备方法一般是以对甲氧基苯乙酮和对叔丁基苯甲酸甲酯为原
料,在惰性溶剂中,采用廉价的甲醇钠做催化剂,经claisen缩合制备,反应收率在65~92.8%(中国专利cn109305897;cn105085223;cn102786403)。中国专利cn102786403公开了采用这种方法制备阿伏苯宗,所用催化剂为甲醇钠或乙醇钠,所用惰性溶剂为二甲苯,在40-100℃,反应8h,专利给出的收率达到80%以上。但由于反应副产的甲醇未能及时移除反应体系,使得反应时间过长。类似的,dsm公司在其公布的世界专利wo2012/084770中,采用甲醇钾作为反应的催化剂,阿伏苯宗的定量计算收率高达95%。然而,该专利未对产品阿伏苯宗进行分离纯化,发明人多次重复该专利的合成方法,发现gc纯度为90-95%,分离纯化总收率仅87-90.5%。
[0006]
为此,仍需继续探索新的合成方法,以适应业界对高品质、低成本的防晒剂阿伏苯宗的需求。
技术实现要素:
[0007]
为解决上述问题,本发明人进行了锐意研究,结果发现:以对甲氧基苯乙酮与对叔丁基苯甲酸酯为原料,以醇钾溶液为催化剂,通过对合成工艺的分步控制,制备阿伏苯宗。通过本发明中的工艺合成方法,大幅提高合成工艺的收率,产品纯度高,色质浅,工艺过程得到明显简化,单釜产能大幅提高,有利于工业化生产,从而完成了本发明。
[0008]
本发明的目的之一在于提供一种阿伏苯宗工业化合成工艺方法,所述工艺方法采用对甲氧基苯乙酮和对叔丁基苯甲酸酯为原料。
[0009]
所述工艺方法包括以下步骤:
[0010]
步骤1、将对甲氧基苯乙酮滴加到催化剂溶液中,反应得到反应液ⅰ;
[0011]
步骤2、将对叔丁基苯甲酸酯加入到溶剂ⅰ中,再滴加反应液ⅰ,加热反应,得到反应液ⅱ;
[0012]
步骤3、对反应液ⅱ进行水解和中和,得到待处理液;
[0013]
步骤4、对待处理液进行后处理。
[0014]
本发明的第二目的在于提供一种对甲氧基苯乙烯醇钾盐,所述对甲氧基苯乙烯醇钾盐的结构为:
[0015]
本发明的第三目的在于提供一种以对甲氧基苯乙烯醇钾盐为原料合成阿伏苯宗的工艺方法,所述工艺方法包括以下步骤:
[0016]
步骤(1)、将对甲氧基苯乙烯醇钾盐溶液滴加到对叔丁基苯甲酸酯的溶液中,加热反应,得到反应液;
[0017]
步骤(2)、对反应液进行水解和中和,得到待处理液;
[0018]
步骤(3)、对待处理液进行后处理。
[0019]
本发明的第四目的在于提供了由上述两种方法制备得到的阿伏苯宗。所述阿伏苯宗色泽为微黄色或白色,收率不低于93%。
[0020]
根据本发明提供的一种阿伏苯宗的合成工艺,具有以下有益效果:
[0021]
(1)本发明分步控制反应过程,低温下反应,使阿伏苯宗粗产品含量由目前工业生
产的80-85wt%提高至97-98wt%,成品杂质含量控制在1%以内,小于生产指标的小于3%,降低了结晶难度;以对甲氧基苯乙酮为基础计算,本发明小试收率在93.40%,目前工业生产收率79%左右,收率相对提高14%。
[0022]
(2)本发明过程反应制备的阿伏苯宗碱金属盐溶于溶剂中,反应结束后,可将缩合物料转移至中和水洗釜中,从而避免了由于阿伏苯宗碱金属盐的析出,需要在缩合釜中进行水解和中和,简化了目前工业生产中缩合反应投料前缩合釜的预先水洗和干燥处理过程。
[0023]
(3)本发明后处理采用通二氧化碳气体代替目前工业生产中使用硫酸进行水解中和,条件更加温和,容易控制,简化水洗工艺,减少废水产生。
[0024]
(4)与目前工业生产相比较,本发明整个生产过程中物料都处于碱性,因此,仅需使用不锈钢釜即能完成整个生产,降低了设备要求,减少生产成本,所得产品阿伏苯宗色泽更淡,为微黄色至白色结晶粉末。
[0025]
(5)本发明采用二氧化碳中和反应物料,从而得到碳酸氢钾,再经高温煅烧,最终制得符合工业碳酸钾gb/t 1587-2016中i型一等品标准的碳酸钾,避免了固废的产生,碳酸钾作为副产外卖,从而降低了产品阿伏苯宗的生产成本,提高了盈利能力。
附图说明
[0026]
图1示出本发明实施例1中对甲氧基苯乙烯醇钾盐和对甲氧基苯乙酮的核磁共振谱图;
[0027]
图2示出本发明实施例1中阿伏苯宗粗产品气相色谱图;
[0028]
图3示出本发明实施例1中结晶后阿伏苯宗的气相色谱图;
[0029]
图4示出本发明对比例1中反应过程ⅰ中产物的气相色谱图。
具体实施方式
[0030]
下面通过具体实施方式对本发明进行详细说明,本发明的特点和优点将随着这些说明而变得更为清楚、明确。
[0031]
本发明中提供的阿伏苯宗工业化合成方法,不但产品收率高、纯度高,产能大幅提高,而且合成工艺在多个环节得到简化,产品合成条件更为温和,减少三废,并可得到高质量副产品。
[0032]
步骤1、将对甲氧基苯乙酮滴加到催化剂溶液中,反应得到反应液ⅰ。
[0033]
所述催化剂选自醇钾,优选为甲醇钾、乙醇钾或叔丁醇钾,更优选为甲醇钾。碱金属醇盐作为有机缩合反应的催化剂,可提供强碱性环境,选择性好、活性高。由于碱金属的碱性越强,其催化活性就越高,所以醇钾的催化活性较醇钠更为优越,并且甲醇钾的端基为甲基,位阻小,更有利于反应的进行。
[0034]
在本发明的一种优选方式中,将催化剂溶解在溶剂ⅱ中,所述溶剂ⅱ选自醇类,如甲醇、乙醇或叔丁醇,酮类,如丙酮,芳香烃类,如甲苯、二甲苯,优选为甲醇、乙醇或叔丁醇,更优选为甲醇。醇钾在溶剂中的质量分数为5%~35%,优选为10%~32%,更优选为12%~30%。若工业醇钾浓度过高,会有固体醇钾析出,不方便投料,催化剂分散不均匀,影响反应进行,若浓度过低,造成醇溶剂过多,增加运输成本,并且增加工艺过程中醇溶剂的处理
量。
[0035]
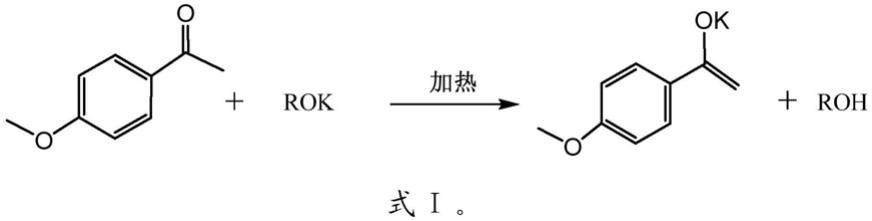
在本发明中,优选将对甲氧基苯乙酮滴加到醇钾溶液中,使对甲氧基苯乙酮在溶剂环境下与催化剂充分反应,得到醇和对甲氧基苯乙烯醇钾盐,具体反应如式ⅰ所示,其中r为烷基,优选为甲基、乙基或叔丁基,更优选为甲基。在该反应过程中,选择性高,副产物很少。在本发明的优选方案中,以甲醇钾为催化剂,甲醇为溶剂,生成的甲醇直接进入到溶剂中,不会引入新的杂质,有利于后处理工艺的简化。
[0036][0037]
所述加入的对甲氧基苯乙酮可以为固态对甲氧基苯乙酮或液态对甲氧基苯乙酮,也可以为对甲氧基苯乙酮溶解在溶剂ⅱ中形成的对甲氧基苯乙酮溶液,优选为液态对甲氧基苯乙酮或对甲氧基苯乙酮溶液,更优选为液态对甲氧基苯乙酮。优选地,所述液态对甲氧基苯乙酮在保温条件下加入,保温温度为37~90℃,优选为42~70℃,更优选为50-60℃。所述液态对甲氧基苯乙酮的加入方式为滴加。在本发明步骤1中,对甲氧基苯乙酮滴加的时长为0.3~5h,优选0.6~2h,更优选为0.8~1.2h。
[0038]
本发明人发现,将对甲氧基苯乙酮滴加到醇钾溶液中,使得醇钾溶液相对于对甲氧基苯乙酮大幅度过量,随着搅拌的进行,对甲氧基苯乙酮迅速分散在反应体系中,从而避免了局部浓度过大,使反应充分进行,副产物少,提高了反应的选择性。
[0039]
另外,如果对甲氧基苯乙酮滴加的时间过短,速度过快,则滴加进行反应的效果不明显,如果滴加时间过长,反应收率和选择性也不会进一步提高,延长生产周期。
[0040]
所述生成对甲氧基苯乙烯醇钾盐反应在温和加热条件下进行,反应温度为10~50℃,优选为15~40℃,更优选为20~30℃。醇钾化学性质活跃,反应温度过高,反应剧烈,不利于反应稳定进行;反应温度过低,反应进行缓慢,增长反应周期。
[0041]
所述生成对甲氧基苯乙烯醇钾盐反应在搅拌条件下进行。在该反应过程中,液态对甲氧基苯乙酮以滴加方式进入醇钾溶液中,对甲氧基苯乙酮进入到醇钾溶液中后需要迅速分散开,因此,优选反应在搅拌条件下进行。
[0042]
在本发明步骤1中,所述对甲氧基苯乙酮滴加结束后,继续保温反应,反应时间为10~50min,优选为20~40min,更优选为25~35min,继续保温反应过程是为了使对甲氧基苯乙酮充分反应。
[0043]
所述对甲氧基苯乙酮与醇钾的摩尔比为1:(0.4~2.5),优选为1:(0.8~1.5),更优选为1:(1~1.1)。从反应机理来看,对甲氧基苯乙酮与醇钾是等摩尔比进行反应的,为了使对甲氧基苯乙酮反应完全,无剩余,避免过量的对甲氧基苯乙酮转移到下一步反应中,影响下一步缩合反应的进行,使醇钾稍过量。
[0044]
优选地,所述反应在惰性气氛下进行,惰性气氛可以为氮气或氩气,优选为氮气。
[0045]
步骤2、将对叔丁基苯甲酸酯加入到溶剂ⅰ中,再滴加反应液ⅰ,加热反应,得到反应液ⅱ。
[0046]
所述叔丁基苯甲酸酯结构为:
[0047][0048]
r1为烷基,所述叔丁基苯甲酸酯选自叔丁基苯甲酸甲酯、叔丁基苯甲酸乙酯,叔丁基苯甲酸丙酯、叔丁基苯甲酸异丙酯、叔丁基苯甲酸丁酯、叔丁基苯甲酸异丁酯、叔丁基苯甲酸仲丁酯、叔丁基苯甲酸叔丁酯,优选为叔丁基苯甲酸甲酯和叔丁基苯甲酸乙酯,更优选为叔丁基苯甲酸甲酯。叔丁基苯甲酸甲酯的酯键中一端基团为甲基,位阻效应小,更容易进行缩合反应。另外,选择叔丁基苯甲酸甲酯进行缩合反应,反应过程中生产的甲醇可直接进入溶液,在优选方式中不会引入新的杂质。
[0049]
将步骤1中得到的反应液ⅰ滴加到反应体系中,其中的对甲氧基苯乙烯醇钾盐与对叔丁基苯甲酸酯进行缩合反应,得到阿伏苯宗的一种钾盐,反应如式ⅱ。
[0050][0051]
所述对叔丁基苯甲酸酯与对甲氧基苯乙酮的摩尔比为(0.4~2.5):1,优选为(0.8~1.5):1,更优选为(1~1.1):1。为使反应充分进行,选择使对叔丁基苯甲酸酯过量。
[0052]
所述溶剂ⅰ为有机溶剂,选自醇类,如乙二醇或丁二醇,芳香烃类,如甲苯或二甲苯,优选为芳香烃类,更优选为邻二甲苯。值得注意的是,在缩合反应中以邻二甲苯为反应溶剂,可以使反应生成阿伏苯宗钾盐溶于溶剂ⅰ中,防止阿伏苯宗钾盐析出,以便在后续后处理工艺中将缩合物料转移至中和水洗釜中进行水解和中和。
[0053]
目前工业生产中由于阿伏苯宗钠盐的析出,需要在缩合釜中进行水解、中和,因此,再次进行缩合反应前需要对缩合釜进行预先水洗和干燥处理,工艺繁琐,不能连续生产。本发明中采用整体转移缩合物料的方法简化了生产工艺,避免了对缩合反应釜反复预处理的过程。
[0054]
所述对叔丁基苯甲酸酯与溶剂ⅰ的质量比为1:(3~18),优选为1:(5~12),更优选为1:(6.5~8)。溶剂ⅰ的用量直接关系到反应速率和最终产物的产率,经过研究发现,对叔丁基苯甲酸酯与溶剂的质量比为1:(3~18)时,反应速率较快,最终产物的产率较高。
[0055]
在本发明的一种优选方式中,所述缩合反应进行的同时,在减压环境下分离溶剂ⅱ以促进反应的进行,邻二甲苯与甲醇沸点温差大,不会形成共沸,便于邻二甲苯与甲醇的分离。分离后的邻二甲苯可回收套用。
[0056]
目前,现有工艺中由于多使用的甲苯作为溶剂ⅰ,与反应生成的醇沸点接近,如甲醇,需要使用精馏柱不断分离出甲醇,促使反应生成阿伏苯宗;在本发明中的一种优选方式中,使用邻二甲苯作为溶剂ⅰ,不存在溶剂ⅰ和生成的醇在蒸馏过程中分离不开的问题,所以可以省去精馏柱的使用,大幅降低能耗。
[0057]
所述反应液ⅰ以滴加的方式加入到叔丁基苯甲酸酯溶液中。在搅拌条件下,反应体
系中对叔丁基苯甲酸酯相对于反应液ⅰ稍过量,随着搅拌的进行,对混合液迅速分散在反应体系中,从而避免了局部浓度过大,使缩合反应充分进行,副产物少,提高了缩合反应的收率。
[0058]
在一种优选的实施方式中,所述反应液ⅰ滴加时间为0.5~3h,优选为0.8~2h,更优选为1h。值得注意的是,反应液ⅰ的滴加时间需严格控制在上述范围内,若滴加时间<0.5h,对甲氧基苯乙烯醇钾盐的局部浓度高,在加热的缩合反应釜中会发生式ⅰ的逆反应,影响缩合的进一步的反应,发生对甲氧基苯乙酮的自缩合,降低阿伏苯宗的收率;若滴加时间>3h,加之后续的保温反应时间,产物在反应温度下易发生分解、聚合等副反应;上述两种情况,不论反应原料的自缩合或者反应最终产物的分解、聚合,均会造成产率下降,以及杂质去除难度加大的问题。
[0059]
所述反应液ⅰ滴加结束后,继续保温反应,反应时间为0.5~4h,优选为1~3h,更优选为1.5~2.5h。在反应液ⅰ滴加结束后,保持搅拌条件,继续保温,使反应体系充分反应,得到反应液ⅱ。
[0060]
所述加热反应的反应温度为40~150℃,优选为65~120℃,更优选为85~90℃。所述加热反应在减压条件下进行反应,反应真空度为5~80mmhg,优选为10~50mmhg,更优选为18~25mmhg。一方面,步骤2中,反应体系副产的甲醇及反应液1中带入的甲醇必须及时脱离反应体系,否则将引起副反应,降低反应的选择性和最终产品的收率;另一方面,反应温度过高,将使产品分解、聚合,所以只能真空条件下反应,目的是既能保证产品不分解、聚合,又能使甲醇及时采出。
[0061]
优选地,所述反应在惰性气氛下进行,惰性气氛可以为氮气或氩气,优选为氮气。
[0062]
相对于目前的生产工艺,本发明采用分步控制反应过程,先将对甲氧基苯乙酮滴加到过量的醇钾溶液中,使对甲氧基苯乙酮充分反应完全,使其生成对甲氧基苯乙烯醇钾盐,防止目前工艺中将对甲氧基苯乙酮滴加到对叔丁基苯甲酸酯和催化剂中引起的自缩合;另外,通过分步反应隔离了对叔丁基苯甲酸酯与催化剂,使二者不能直接接触,避免了对叔丁基苯甲酸酯自缩合,使原料对甲氧基苯乙酮完全转换为目标产物阿伏苯宗钾盐,提高产物的选择性和收率,减少杂质的生成,提高产能。
[0063]
步骤3、对反应液ⅱ进行水解和中和,得到待处理液。
[0064]
为得到阿伏苯宗,需要对反应液ⅱ进行水解和中和。
[0065]
所述水解为向反应液中加入水,步骤2中生成的阿伏苯宗碱金属盐在酸性环境下不能稳定存在,发生水解得到阿伏苯宗最终产物。
[0066]
为使水解反应顺利进行,需要中和反应液中的碱,可以加入无机酸,如稀盐酸或稀硫酸,在本发明中,优选向反应液中通入二氧化碳,中和反应液中的碱性溶液。
[0067]
相对于现有工艺中利用无机酸进行中和,本发明采用通入二氧化碳对反应液进行中和,中和过程更加温和,工艺实施过程容易控制,不用担心ph值调节过度。有机相中无酸残留,避免了现有工艺中由于酸的残留必须对有机相进行多次水洗,简化了工艺过程,减少了废水的产生。
[0068]
水解中和结束后,使反应液静置分层,分离得到水相和有机相。
[0069]
所述有机相主要为含有阿伏苯宗的有机溶剂,所述水相主要为含有碳酸氢盐或碳酸盐的水溶液。
[0070]
步骤4、对待处理液进行后处理。
[0071]
所述后处理过程包括有机相蒸馏、结晶、水相浓缩和煅烧。
[0072]
所述有机相蒸馏为采用减压蒸馏脱除有机相中的溶剂,得到粗产品。
[0073]
所述结晶为向粗产品中加入结晶溶剂,所述结晶溶剂为醇类溶剂,优选为甲醇、乙醇或异丙醇中任意一种或几种,更优选为甲醇。
[0074]
所述结晶溶剂与对叔丁基苯甲酸酯的质量比为(2~6):1,优选为(3~5):1,更优选为(3.5~4.5):1。与对叔丁基苯甲酸酯的质量比为(3.5~4.5):1的用量范围内,结晶溶剂可使产品在结晶过程中有效去除最终产物中的杂质,提高最终产物的纯度,且使得最终产物颜色合格,具有特征性的芳香气味;不会由于溶剂过少导致最终产物质量低,或者溶剂用量多,影响结晶量,增加溶剂消耗。
[0075]
对结晶得到的阿伏苯宗进行真空干燥,干燥温度为50~70℃,优选为65~70℃。
[0076]
所述水相浓缩为蒸发去除水相中的水分,得到馏底物,蒸发后的水分经收集可以循环使用。
[0077]
所述煅烧为对馏底物进行高温煅烧,得到碳酸钾,其质量符合工业碳酸钾gb/t 1587-2016中i型一等品标准。所述煅烧温度为600~1200℃,优选为700~1000℃,更优选为750~900℃。
[0078]
本发明中的目的之一还在于提供一种由对甲氧基苯乙烯醇钾盐合成阿伏苯宗的方法。该方法的步骤(1)~(3)过程与前述过程相同。
[0079]
本发明中提供的阿伏苯宗生产工艺,分步控制反应过程,大幅提高产物的选择和收率,通过控制工艺条件,简化生产工艺的后处理过程,溶剂易于分离,可回收套用,大幅减少废水的产生,得到高质量副产物碳酸钾,降低阿伏苯宗生产成本。
[0080]
实施例实施例1
[0081]
氮气保护下,于干燥洁净的四口烧瓶中加入98.0g的30%甲醇钾甲醇溶液,控制釜温在25~28℃,于1h内将60.0g液态对甲氧基苯乙酮滴入到甲醇钾溶液中,滴加结束后,继续保温反应30min,得158.0g对甲氧基苯乙烯醇钾盐溶液,转移至缩合工序待用。
[0082]
氮气保护下,于带搅拌器、温度计和减压回流分水装置的2000ml四口烧瓶中,加入600.0g邻二甲苯,和80.0g对叔丁基苯甲酸甲酯,水泵控制釜内真空度18~25mmhg,釜温控制在80~85℃,滴加158.0g对甲氧基苯乙烯醇钾盐溶液,同时采出甲醇,滴加时间为1h,滴加完毕后,保温保压搅拌2h后,停止加热,反应结束,共采出432.6g甲醇和少量邻二甲苯的混合液。
[0083]
反应结束后,加入150.0g水进行水解,并通入二氧化进行中和,待ph达到8~9时,停止通入二氧化碳,静置分层,得有机相361.7g,水相183.67g,取有机相样品进行气相色谱gc检测,扣除溶剂邻二甲苯后,阿伏苯宗粗产品的质量分数为98.7999%(以去除溶剂的总产物为100%)。
[0084]
蒸馏回收邻二甲苯,得到粗产品。向馏底粗产品中加入260g甲醇结晶,65~70℃真空干燥,得116.3g白色针状粉末晶体的阿伏苯宗,收率为93.40%(以对甲氧基苯乙酮计),气相色谱gc检测阿伏苯宗含量为99.59630%。
[0085]
于洁净的500ml四口烧瓶中加入183.67g水相,浓缩至干,得38.55g馏底(主要为碳酸氢钾)。将馏底转入500ml陶瓷坩埚中,置于氧氛炉中控制空气流量0.5~0.6l/min,于200
℃保温2h,500℃保温1h,800℃保温2h,得29.2g白色碳酸钾,含量为98.0%,收率为98.78%(按投入的钾离子计)。其质量符合工业碳酸钾gb/t 1587-2016中i型一等品标准。
[0086]
对比例
[0087]
对比例1
[0088]
反应过程ⅰ:氮气保护下,于干燥洁净的四口烧瓶中加入60.0g液态对甲氧基苯乙酮,控制釜温在25~28℃,于1h内将98.0g的30%甲醇钾甲醇溶液滴入到对甲氧基苯乙酮中,滴加结束后,继续保温反应30min,得到反应液。停止加热,加入水150g,通二氧化碳气体至体系ph达到8~9,静置分液得到水相和有机相。有机相在氮气气氛中,25~28℃下,静置反应液24小时。
[0089]
反应过程ⅱ:氮气保护下,于干燥洁净的四口烧瓶中加入98.0g的30%甲醇钾甲醇溶液,控制釜温在25~28℃,于1h内将60.0g对甲氧基苯乙酮滴入到甲醇钾溶液中,滴加结束后,继续保温反应30min。停止加热,氮气气氛中,在25~28℃下,静置反应液24小时。
[0090]
对比例2
[0091]
反应釜中加入800g甲苯、98.0g 30%的甲醇钾甲醇溶液和80g对叔丁基苯甲酸甲酯,升温至回流温度(98~103℃);
[0092]
开始滴加60g对甲氧基苯乙酮和80g甲苯组成的混合溶液,滴加过程中始终保持回流,釜温逐渐下降,滴加时间控制在1.5h。滴加完成后,保温(80~83℃)反应2h。
[0093]
反应过程中不采用精馏柱,但不断蒸出反应副产的甲醇。
[0094]
反应结束后,加入150.0g水进行水解,并通入二氧化进行中和,中和结束后静置分层,得到水相和有机相。有机相蒸馏脱去溶剂甲苯,馏底加入300g甲醇析晶,过滤,滤饼重结晶得到类白色针状晶体阿伏苯宗。
[0095]
上述方法制备得到的阿伏苯宗gc纯度(面积归一法)为98.67%。含量为98.7%,收率为79.5%。
[0096]
实验例
[0097]
实验例1
[0098]
取实施例1中得到的对甲氧基苯乙烯醇钾盐进行核磁共振波谱分析,使用inova 400mhz高分辨率核磁共振谱仪,tms为内标物,cdcl3为溶剂。对甲氧基苯乙酮和对甲氧基苯乙烯醇钾盐核磁谱图如图1所示。
[0099]
从图1中可以看出,反应结束后,代表对甲氧基苯乙酮中的与羰基相连的甲基上氢原子的共振峰δ(2.55,3h)几乎消失,而出现了代表对甲氧基苯乙烯醇钾盐中烯醇键上氢原子的共振峰δ(4.15,h)和δ(4.60,h)。δ(3.76,h)为甲氧基上的氢,δ(6.92,2h)和δ(7.65,2h)为苯环上的氢,说明反应得到了对甲氧基苯乙烯醇钾盐。
[0100]
实验例2
[0101]
取实施例1中水解、中和分离有机相后得到的阿伏苯宗粗产品进行气相色谱分析。色谱分析的色谱柱为hp-5,以氮气为载气,检测器为火焰离子化检测器(fid),检测器温度为300℃。柱温箱在60℃保持3min,再以30℃/min的升温速率升至280℃,保持10min。色谱图如图2所示。其中,26.087min处对应阿伏苯宗的保留时间,5min处为溶解样品的溶剂邻二甲苯,不将溶剂计算在内,粗产品中阿伏苯宗纯度为98.7999%,说明本发明中的工艺控制能够有效提高目标产物的选择性,大幅减少副产物的生成。
[0102]
实验例3
[0103]
取实施例1中结晶后得到的阿伏苯宗最终产品进行气相色谱分析。取适量样品用丙酮进行溶解,仪器使用db-1型色谱柱,fid检测器,以氦气为载气,柱温为280℃。色谱图如图3所示。其中,12.872min处对应阿伏苯宗的保留时间,0~2.5min间峰对应的物质为丙酮,不将丙酮计算在内,产品中阿伏苯宗纯度为99.59630%。
[0104]
实验例4
[0105]
分别取对比例1中反应过程ⅰ和反应过程ⅱ静置后的样品进行气相色谱分析,反应过程ⅰ得到的产物色谱图如图4所示。
[0106]
从图4中可以发现:1.628~4.382min之间的峰为取样中和后使用的萃取溶剂甲苯。图4中出现大量的对甲氧基苯乙酮自缩合产物,带有双甲氧基苯基的丁烯酮,结构式为:
[0107][0108]
反应过程ⅱ中的产物测得的色谱图中主要产物的保留时间与相同测试条件下的对甲氧基苯乙酮保留时间相同。另外,对静置24h后的样品进行核磁共振氢谱分析,发现与实验例1中对甲氧基苯乙酮的核磁共振氢谱类似,说明反应过程ⅱ中静置后产物又转化为对甲氧基苯乙酮。
[0109]
对比例1中的反应过程ⅰ和反应过程ⅱ可以从侧面说明,反应过程ⅰ中发生了对甲氧基苯乙酮的自缩合,静置后产物不会发生变化,而反应过程ⅱ中对甲氧基苯乙酮与甲醇钾先是反应得到对甲氧基苯乙烯醇钾盐,由于烯醇盐不能够长时间稳定存在,在静置后又发生逆反应转化为对甲氧基苯乙酮。
[0110]
以上结合具体实施方式和/或范例性实例以及附图对本发明进行了详细说明,不过这些说明并不能理解为对本发明的限制。本领域技术人员理解,在不偏离本发明精神和范围的情况下,可以对本发明技术方案及其实施方式进行多种等价替换、修饰或改进,这些均落入本发明的范围内。本发明的保护范围以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1